BACHELORARBEIT - Metzsch, Daniel
BACHELORARBEIT - Metzsch, Daniel
BACHELORARBEIT - Metzsch, Daniel
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
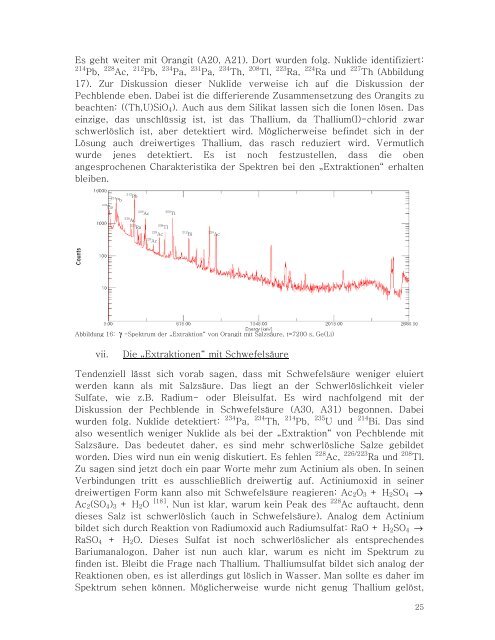
Es geht weiter mit Orangit (A20, A21). Dort wurden folg. Nuklide identifiziert:<br />
214 Pb, 228 Ac, 212 Pb, 234 Pa, 231 Pa, 234 Th, 208 Tl, 223 Ra, 224 Ra und 227 Th (Abbildung<br />
17). Zur Diskussion dieser Nuklide verweise ich auf die Diskussion der<br />
Pechblende eben. Dabei ist die differierende Zusammensetzung des Orangits zu<br />
beachten: ((Th,U)SiO 4 ). Auch aus dem Silikat lassen sich die Ionen lösen. Das<br />
einzige, das unschlüssig ist, ist das Thallium, da Thallium(I)-chlorid zwar<br />
schwerlöslich ist, aber detektiert wird. Möglicherweise befindet sich in der<br />
Lösung auch dreiwertiges Thallium, das rasch reduziert wird. Vermutlich<br />
wurde jenes detektiert. Es ist noch festzustellen, dass die oben<br />
angesprochenen Charakteristika der Spektren bei den „Extraktionen“ erhalten<br />
bleiben.<br />
214 Pb<br />
212 Pb<br />
234 Pa<br />
228 Ac<br />
208 Tl<br />
228 Ac<br />
223 Ra<br />
208 Tl<br />
228 Ac<br />
228 Ac<br />
212 Bi<br />
228 Ac<br />
Abbildung 16: γ -Spektrum der „Extraktion“ von Orangit mit Salzsäure, t=7200 s, Ge(Li)<br />
vii.<br />
Die „Extraktionen“ mit Schwefelsäure<br />
Tendenziell lässt sich vorab sagen, dass mit Schwefelsäure weniger eluiert<br />
werden kann als mit Salzsäure. Das liegt an der Schwerlöslichkeit vieler<br />
Sulfate, wie z.B. Radium- oder Bleisulfat. Es wird nachfolgend mit der<br />
Diskussion der Pechblende in Schwefelsäure (A30, A31) begonnen. Dabei<br />
wurden folg. Nuklide detektiert: 234 Pa, 234 Th, 214 Pb, 235 U und 214 Bi. Das sind<br />
also wesentlich weniger Nuklide als bei der „Extraktion“ von Pechblende mit<br />
Salzsäure. Das bedeutet daher, es sind mehr schwerlösliche Salze gebildet<br />
worden. Dies wird nun ein wenig diskutiert. Es fehlen 228 Ac, 226/223 Ra und 208 Tl.<br />
Zu sagen sind jetzt doch ein paar Worte mehr zum Actinium als oben. In seinen<br />
Verbindungen tritt es ausschließlich dreiwertig auf. Actiniumoxid in seiner<br />
dreiwertigen Form kann also mit Schwefelsäure reagieren: Ac 2 O 3 + H 2 SO 4 →<br />
Ac 2 (SO 4 ) 3 + H 2 O [18] . Nun ist klar, warum kein Peak des 228 Ac auftaucht, denn<br />
dieses Salz ist schwerlöslich (auch in Schwefelsäure). Analog dem Actinium<br />
bildet sich durch Reaktion von Radiumoxid auch Radiumsulfat: RaO + H 2 SO 4 →<br />
RaSO 4 + H 2 O. Dieses Sulfat ist noch schwerlöslicher als entsprechendes<br />
Bariumanalogon. Daher ist nun auch klar, warum es nicht im Spektrum zu<br />
finden ist. Bleibt die Frage nach Thallium. Thalliumsulfat bildet sich analog der<br />
Reaktionen oben, es ist allerdings gut löslich in Wasser. Man sollte es daher im<br />
Spektrum sehen können. Möglicherweise wurde nicht genug Thallium gelöst,<br />
25