- Seite 1 und 2: VorlesungsskriptumMolekül- und Fes
- Seite 3 und 4: Inhaltsverzeichnis1 Moleküle 71.1
- Seite 5 und 6: 6.2.4 Debye-Modell . . . . . . . .
- Seite 7 und 8: Kapitel 1Moleküle7
- Seite 9: Tabelle 1.1: Eigenfunktionen des Wa
- Seite 13 und 14: zu finden.Wenn man nun die Elektron
- Seite 15 und 16: im kleinen Kasten. Geht dieses Atom
- Seite 17 und 18: Abbildung 1.3: Pi-Bindung zweier p-
- Seite 19 und 20: Wobei der Index S Schwerpunktskoord
- Seite 22 und 23: Abbildung 1.7: sp 2 -OrbitalDreifac
- Seite 24 und 25: Abbildung 1.8: Strukturformel von E
- Seite 26 und 27: Teilchenketteso ergibt dies:Wendet
- Seite 28 und 29: Mit den Eigenlösungen:−2 ∂ 2
- Seite 30 und 31: 2.1 EinleitungDas Wort “Kristall
- Seite 32 und 33: Abbildung 2.2: Die fünf Bravaisgit
- Seite 34 und 35: 2.3 Elementarzellen2.3.1 Die primit
- Seite 36 und 37: Abbildung 2.8: Die Wigner-Seitz-Zel
- Seite 38 und 39: Die Koordinationszahlen (Anzahl der
- Seite 40 und 41: Abbildung 2.13: Die Millerindizes d
- Seite 42 und 43: 3×3-Matrix ausgedrückt werden.Bei
- Seite 44 und 45: 2.6 Beispiele für einfache Kristal
- Seite 46 und 47: Abbildung 2.20: Primitive Elementar
- Seite 48 und 49: 2.6.4 Natriumchlorid und PerowskitD
- Seite 50 und 51: 11.0079414,4Hex0.0843,756,1236,941H
- Seite 52 und 53: 3.1 EinleitungIn diesem Kapitel mö
- Seite 54 und 55: Abbildung 3.2: Ergebnisse eines Dop
- Seite 56 und 57: 3.5 FourieranalyseViele Eigenschaft
- Seite 58 und 59: heißt, wir sehen konstruktive Inte
- Seite 60 und 61:
anschreiben:n(r) = ∑ Gn G exp(iG
- Seite 62 und 63:
Abbildung 3.8: Streuung des einfall
- Seite 64 und 65:
Laue-BedingungDie Laue-Bedingung la
- Seite 66 und 67:
3.8 Brillouin-ZonenDer Begriff der
- Seite 68 und 69:
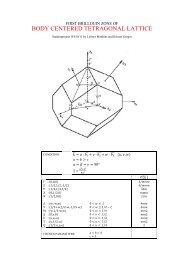
Erste Brillouin-Zone von sc, bcc un
- Seite 70 und 71:
3.10 XRD - Grundlagen der Röntgens
- Seite 72 und 73:
3.10.1 Pulverdiffraktometrie und R
- Seite 74 und 75:
Kapitel 4Kristallbindungen74
- Seite 76 und 77:
ein Valenzelektron ab und wird dadu
- Seite 78 und 79:
dem Absinken der Elektronegativitä
- Seite 80 und 81:
Abbildung 4.6: Kubisch raumzentrier
- Seite 82 und 83:
Kapitel 5Photonen82
- Seite 84 und 85:
man die Coulomb- Eichung (auch Stra
- Seite 86 und 87:
ω = c| ⃗ k|, (5.23)Dies ergibt s
- Seite 88 und 89:
sich für die Anzahl aller Zuständ
- Seite 90 und 91:
5.1.5 Die thermodynamischen Größe
- Seite 92 und 93:
Abbildung 5.7: Lösungen der Wellen
- Seite 94 und 95:
unbedingt notwendig ist, die Schrö
- Seite 96 und 97:
Bloch-Form, aber keine wohldefinier
- Seite 98 und 99:
Liegt dieses k außerhalb der erste
- Seite 100 und 101:
Zur Berechnung in drei Dimensionen
- Seite 102 und 103:
6.1 GitterschwingungenGitterschwing
- Seite 104 und 105:
Abbildung 6.3: Massenkette (Lecture
- Seite 106 und 107:
Abbildung 6.5: Hier sind die erlaub
- Seite 108 und 109:
Abbildung 6.7: Van Hove-Singularit
- Seite 110 und 111:
Abbildung 6.10: Schwarze Linie: gle
- Seite 112 und 113:
Abbildung 6.12: ZustandsdichteWerte
- Seite 114 und 115:
Abbildung 6.13: Vergleich zwischen
- Seite 116 und 117:
6.2.4 Debye-ModellGegenüber dem Ei
- Seite 118 und 119:
Beispiel Silizium:Abbildung 6.17: Z
- Seite 120 und 121:
Abbildung 6.19: Lennard-Jones Poten
- Seite 122 und 123:
Herleitung im 1-d.: An jedem Punkt
- Seite 124 und 125:
gel werden, um die Matrixelemente b
- Seite 126 und 127:
7.1 Fermi-Gas freier ElektronenÜbe
- Seite 128 und 129:
Abbildung 7.3: Zustandsdichte D(E)
- Seite 130 und 131:
Daraus lässt sich durch Einsetzen
- Seite 132 und 133:
Fermi-Energie 2-DFür T = 0n =∫E
- Seite 134 und 135:
Fermi-Energie 3-DFür T = 0n =∫E
- Seite 136 und 137:
E >= 3 5 E F (7.49)Betrachtet man d
- Seite 138 und 139:
wobei H eine Funktion der Energie u
- Seite 140 und 141:
Berechnung der inneren Energie u in
- Seite 142 und 143:
Abbildung 7.14: Experimentelle und
- Seite 144 und 145:
7.1.8 Kinetische GastheorieDie kine
- Seite 146 und 147:
Temperaturabhängigkeit der elektri
- Seite 148 und 149:
Abbildung 7.18: Thermische Leitfäh
- Seite 150 und 151:
Kapitel 8Energiebänder150
- Seite 152 und 153:
Abbildung 8.1: Energie in Abhängig
- Seite 154 und 155:
8.3 Empty Lattice ApproximationMan
- Seite 156 und 157:
Abbildung 8.5: 3D-Darstellung der B
- Seite 158 und 159:
Wenn man die bei der „plane wave
- Seite 160 und 161:
Die letzte Gleichung gilt für jede
- Seite 162 und 163:
Problem zu tun haben, muss es Lösu
- Seite 164 und 165:
struktur und der Ausbreitungsrichtu
- Seite 166 und 167:
9.1. DEHNUNG (STRAIN) UND SPANNUNG
- Seite 168 und 169:
9.2. STATISTISCHE PHYSIKNun bilden
- Seite 170 und 171:
9.3. KRISTALLGRUPPEN UND SYMMETRIEN
- Seite 172 und 173:
9.4. PYROELEKTRIZITÄTdafür ist de
- Seite 174 und 175:
9.7. PEROVSKITE STRUKTURENfolgende
- Seite 176 und 177:
10.1. EINLEITUNG KAPITEL 10. HALBLE
- Seite 178 und 179:
10.3. EFFEKTIVE MASSE KAPITEL 10. H
- Seite 180 und 181:
10.4. LADUNGSTRÄGERKONZENTRATION B
- Seite 182 und 183:
10.4. LADUNGSTRÄGERKONZENTRATION B
- Seite 184 und 185:
10.5. INTRINSISCHE UND EXTRINSISCHE
- Seite 186 und 187:
10.5. INTRINSISCHE UND EXTRINSISCHE
- Seite 188 und 189:
10.5. INTRINSISCHE UND EXTRINSISCHE
- Seite 190 und 191:
10.5. INTRINSISCHE UND EXTRINSISCHE
- Seite 192 und 193:
10.6. QUASIIMPULS ⃗ K KAPITEL 10
- Seite 194 und 195:
10.6. QUASIIMPULS ⃗ K KAPITEL 10
- Seite 196 und 197:
10.7. THERMOELEKTIZITÄT KAPITEL 10
- Seite 198 und 199:
10.8. ANWENDUNGEN KAPITEL 10. HALBL
- Seite 200 und 201:
10.8. ANWENDUNGEN KAPITEL 10. HALBL
- Seite 202 und 203:
10.8. ANWENDUNGEN KAPITEL 10. HALBL
- Seite 204 und 205:
Kapitel 11Kapitelname204
- Seite 206 und 207:
Kapitel 12Magnetismus206
- Seite 208 und 209:
12.1. DIA- UND PARAMAGNETISMUS KAPI
- Seite 210 und 211:
12.1. DIA- UND PARAMAGNETISMUS KAPI
- Seite 212 und 213:
12.1. DIA- UND PARAMAGNETISMUS KAPI
- Seite 214 und 215:
12.2. FERROMAGNETISMUS KAPITEL 12.
- Seite 216 und 217:
12.2. FERROMAGNETISMUS KAPITEL 12.
- Seite 218 und 219:
12.2. FERROMAGNETISMUS KAPITEL 12.
- Seite 220 und 221:
12.2. FERROMAGNETISMUS KAPITEL 12.
- Seite 222 und 223:
12.3. KRISTALLANISOTROPIE KAPITEL 1
- Seite 224 und 225:
12.3. KRISTALLANISOTROPIE KAPITEL 1
- Seite 226 und 227:
12.3. KRISTALLANISOTROPIE KAPITEL 1