Giáo án Hóa học - Lớp 10 Cơ bản - HỌC KỲ I - Bùi Xuân Đông - THPT Tân Lâm (2017)
LINK BOX: https://app.box.com/s/ioxcikpjs8zqh18v581oom9oqykkgmj1 LINK DOCS.GOOGLE: https://drive.google.com/file/d/1v48--LXeCECLlQPk-JBlhWRNywi5MD28/view?usp=sharing
LINK BOX:
https://app.box.com/s/ioxcikpjs8zqh18v581oom9oqykkgmj1
LINK DOCS.GOOGLE:
https://drive.google.com/file/d/1v48--LXeCECLlQPk-JBlhWRNywi5MD28/view?usp=sharing
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
https://twitter.com/daykemquynhon<br />
plus.google.com/+DạyKèmQuyNhơn<br />
www.facebook.com/daykem.quynhon<br />
http://daykemquynhon.blogspot.com<br />
http://daykemquynhon.ucoz.com<br />
Nơi bồi dưỡng kiến thức To<strong>án</strong> - Lý - <strong>Hóa</strong> cho <strong>học</strong> sinh cấp 2+3 /<br />
Diễn Đàn To<strong>án</strong> - Lý - <strong>Hóa</strong> <strong>10</strong>00B Trần Hưng Đạo Tp.Quy Nhơn Tỉnh Bình Định<br />
TRƯỜNG <strong>THPT</strong> TÂN LÂM<br />
TỔ LÝ – HÓA – SINH – C.NGHỆ<br />
ĐỀ SỐ 1<br />
HƯỚNG DẪN CHẤM<br />
KIỂM TRA 1 TIẾT – LẦN 1<br />
Môn: <strong>Hóa</strong> Học – <strong>Lớp</strong> <strong>10</strong>B1<br />
Thời gian: 45 phút<br />
Điểm<br />
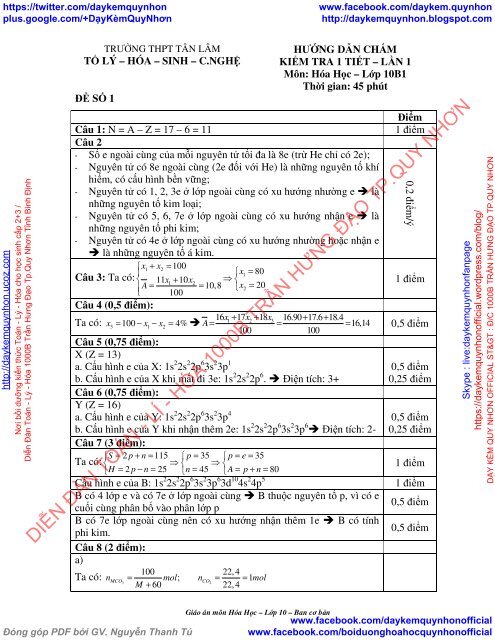
Câu 1: N = A – Z = 17 – 6 = 11<br />
1 điểm<br />
Câu 2<br />
- Số e ngoài cùng của mỗi nguyên tử tối đa là 8e (trừ He chỉ có 2e);<br />
- Nguyên tử có 8e ngoài cùng (2e đối với He) là những nguyên tố khí<br />
hiếm, có cấu hình bền vững;<br />
- Nguyên tử có 1, 2, 3e ở lớp ngoài cùng có xu hướng nhường e là<br />
những nguyên tố kim loại;<br />
- Nguyên tử có 5, 6, 7e ở lớp ngoài cùng có xu hướng nhận e là<br />
những nguyên tố phi kim;<br />
- Nguyên tử có 4e ở lớp ngoài cùng có xu hướng nhường hoặc nhận e<br />
là những nguyên tố á kim.<br />
⎧x1 + x2<br />
= <strong>10</strong>0<br />
⎪<br />
⎧x1<br />
= 80<br />
Câu 3: Ta có: ⎨ 11x1 + <strong>10</strong>x<br />
⇒<br />
2<br />
⎨<br />
1 điểm<br />
⎪A<br />
= = <strong>10</strong>,8 ⎩x2<br />
= 20<br />
⎩ <strong>10</strong>0<br />
Câu 4 (0,5 điểm):<br />
16x1 + 17x2 + 18x3<br />
16.90 + 17.6 + 18.4<br />
Ta có: x3 = <strong>10</strong>0 − x1 − x2<br />
= 4% A= = = 16,14 0,5 điểm<br />
<strong>10</strong>0 <strong>10</strong>0<br />
Câu 5 (0,75 điểm):<br />
X (Z = 13)<br />
a. Cấu hình e của X: 1s 2 2s 2 2p 6 3s 2 3p 1<br />
0,5 điểm<br />
b. Cấu hình e của X khi mất đi 3e: 1s 2 2s 2 2p 6 . Điện tích: 3+ 0,25 điểm<br />
Câu 6 (0,75 điểm):<br />
Y (Z = 16)<br />
a. Cấu hình e của Y: 1s 2 2s 2 2p 6 3s 2 3p 4<br />
0,5 điểm<br />
b. Cấu hình e của Y khi nhận thêm 2e: 1s 2 2s 2 2p 6 3s 2 3p 6 Điện tích: 2- 0,25 điểm<br />
Câu 7 (3 điểm):<br />
⎧S = 2 p + n = 115 ⎧ p = 35 ⎧ p = e = 35<br />
Ta có: ⎨ ⇒ ⎨ ⇒ ⎨<br />
1 điểm<br />
⎩H = 2 p − n = 25 ⎩n = 45 ⎩A = p + n = 80<br />
Cấu hình e của B: 1s 2 2s 2 2p 6 3s 2 3p 6 3d <strong>10</strong> 4s 2 4p 5<br />
1 điểm<br />
B có 4 lớp e và có 7e ở lớp ngoài cùng B thuộc nguyên tố p, vì có e<br />
0,5 điểm<br />
cuối cùng phân bố vào phân lớp p<br />
B có 7e lớp ngoài cùng nên có xu hướng nhận thêm 1e B có tính<br />
phi kim.<br />
0,5 điểm<br />
Câu 8 (2 điểm):<br />
a)<br />
<strong>10</strong>0 22, 4<br />
Ta có: nMCO<br />
= mol; n 1<br />
3 CO<br />
= = mol<br />
2<br />
M + 60 22, 4<br />
DIỄN ĐÀN TOÁN - LÍ - HÓA <strong>10</strong>00B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
0,2 điểm/ý<br />
Skype : live:daykemquynhonfanpage<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C <strong>10</strong>00B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
Đóng góp PDF bởi GV. Nguyễn Thanh Tú<br />
<strong>Giáo</strong> <strong>án</strong> môn <strong>Hóa</strong> Học – <strong>Lớp</strong> <strong>10</strong> – Ban cơ <strong>bản</strong><br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial