CHUYÊN ĐỀ CRACKING ANKAN - SDPP ĐỒ THỊ GIẢI NHANH BÀI TẬP HỢP CHẤT NHÔM - ESTE - LIPIT AMIN - AMINO AXIT - PROTEIN GV PHAN TRUNG NAM - THPT LÊ HỮU TRÁC
LINK BOX: https://app.box.com/s/jxpddq2hekhfhheejtry8lni2pvib2gk LINK DOCS.GOOGLE: https://drive.google.com/file/d/1_TNGKAIz3eJ1myx897C8OVIvVdAFeIYL/view?usp=sharing
LINK BOX:
https://app.box.com/s/jxpddq2hekhfhheejtry8lni2pvib2gk
LINK DOCS.GOOGLE:
https://drive.google.com/file/d/1_TNGKAIz3eJ1myx897C8OVIvVdAFeIYL/view?usp=sharing
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
https://twitter.com/daykemquynhon<br />
plus.google.com/+DạyKèmQuyNhơn<br />
www.facebook.com/daykem.quynhon<br />
http://daykemquynhon.blogspot.com<br />
http://daykemquynhon.ucoz.com<br />
Nơi bồi dưỡng kiến thức Toán - Lý - Hóa cho học sinh cấp 2+3 /<br />
Diễn Đàn Toán - Lý - Hóa 1000B Trần Hưng Đạo Tp.Quy Nhơn Tỉnh Bình Định<br />
<strong>GV</strong> <strong>PHAN</strong> <strong>TRUNG</strong> <strong>NAM</strong> TRƯỜNG <strong>THPT</strong> <strong>LÊ</strong> <strong>HỮU</strong> <strong>TRÁC</strong><br />
a<br />
y<br />
2.1.1 Dạng 1: OH - phản ứng với dung dịch Al 3+<br />
2.1.1. 1: Cho dung dịch kiềm tác dụng với dung dịch muối nhôm<br />
2.1.1.1.1. Thiết lập dáng của đồ thị và phương pháp giải<br />
Cho từ từ dung dịch chứa x molOH − 3<br />
vào dung dịch chứa a mol Al + thu được y mol<br />
Al(OH) 3 . Lập đồ thị biễu diễn lượng kết tủa thu được theo số mol NaOH cho vào<br />
theo a, x ?<br />
+ Pư xảy ra:<br />
Al 3+ + 3OH - → Al(OH) 3 ↓<br />
Al(OH) 3 + OH - → Al(OH) 4 - [AlO 2 - + + 2H 2 O]<br />
+ Đồ thị biểu diễn hai pư trên như sau:<br />
Số mol Al(OH) 3<br />
Dựa vào đồ thị và bản chất của phản ứng ta có:<br />
⎡x1<br />
= 3y<br />
⎢<br />
⎣x2<br />
= 4a − y<br />
2.1.1.1.2. Bài tập ví dụ<br />
nAl( OH )<br />
↓ max<br />
SKKN: SỬ DỤNG PHƯƠNG PHÁP <strong>ĐỒ</strong> <strong>THỊ</strong> <strong>GIẢI</strong> <strong>NHANH</strong> MỘT SỐ <strong>BÀI</strong> <strong>TẬP</strong> VỀ <strong>HỢP</strong> <strong>CHẤT</strong> CỦA <strong>NHÔM</strong> Page 3<br />
3<br />
x 1 3a x 2 4a số mol OH<br />
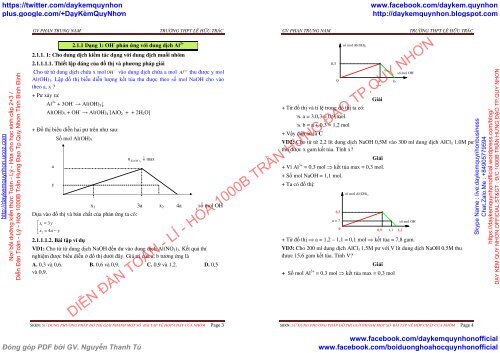
VD1: Cho từ từ dung dịch NaOH đến dư vào dung dịch Al(NO 3 ) 3 . Kết quả thí<br />
nghiệm được biểu diễn ở đồ thị dưới đây. Giá trị của a, b tương ứng là<br />
A. 0,3 và 0,6. B. 0,6 và 0,9. C. 0,9 và 1,2. D. 0,5<br />
và 0,9.<br />
<strong>GV</strong> <strong>PHAN</strong> <strong>TRUNG</strong> <strong>NAM</strong> TRƯỜNG <strong>THPT</strong> <strong>LÊ</strong> <strong>HỮU</strong> <strong>TRÁC</strong><br />
0,3<br />
+ Từ đồ thị và tỉ lệ trong đồ thị ta có:<br />
a = 3.0,3 = 0,9 mol.<br />
b = a + 0,3 = 1,2 mol<br />
+ Vậy đáp án là C<br />
sè mol Al(OH) 3<br />
sè mol OH -<br />
0 a b<br />
Giải<br />
VD2: Cho từ từ 2,2 lít dung dịch NaOH 0,5M vào 300 ml dung dịch AlCl 3 1,0M pư<br />
thu được x gam kết tủa. Tính x?<br />
Giải<br />
+ Vì Al 3+ = 0,3 mol ⇒ kết tủa max = 0,3 mol.<br />
+ Số mol NaOH = 1,1 mol.<br />
+ Ta có đồ thị:<br />
0,3<br />
a = ?<br />
sè mol Al(OH) 3<br />
sè mol OH -<br />
0 0,9<br />
+ Từ đồ thị ⇒ a = 1,2 – 1,1 = 0,1 mol ⇒ kết tủa = 7,8 gam.<br />
VD3: Cho 200 ml dung dịch AlCl 3 1,5M pư với V lít dung dịch NaOH 0,5M thu<br />
được 15,6 gam kết tủa. Tính V?<br />
Giải<br />
+ Số mol Al 3+ = 0,3 mol ⇒ kết tủa max = 0,3 mol<br />
DIỄN ĐÀN TOÁN - LÍ - HÓA 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
SKKN: SỬ DỤNG PHƯƠNG PHÁP <strong>ĐỒ</strong> <strong>THỊ</strong> <strong>GIẢI</strong> <strong>NHANH</strong> MỘT SỐ <strong>BÀI</strong> <strong>TẬP</strong> VỀ <strong>HỢP</strong> <strong>CHẤT</strong> CỦA <strong>NHÔM</strong> Page 4<br />
1,1<br />
1,2<br />
Skype Name : live:daykemquynhonbusiness<br />
Chat.Zalo.Me : +84905779594<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
Đóng góp PDF bởi <strong>GV</strong>. Nguyễn Thanh Tú<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial