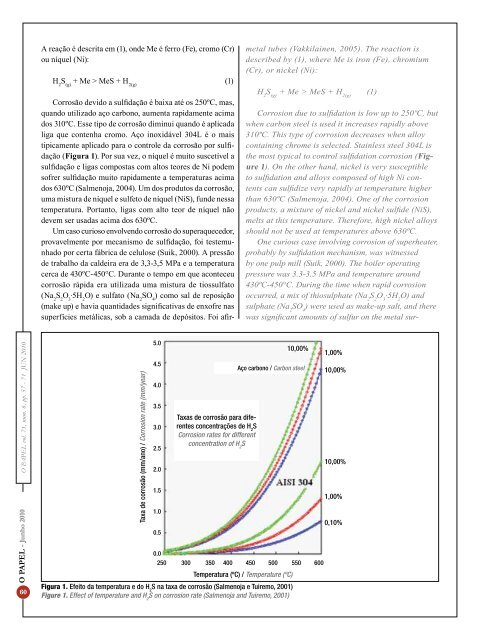
A reação é descrita em (1), onde Me é ferro (Fe), cromo (Cr)ou níquel (Ni):H 2S (g)+ Me > MeS + H 2(g)(1)Corrosão devido a sulfidação é baixa até os 250ºC, mas,quando utilizado aço carbono, aumenta rapidamente acimados 310ºC. Esse tipo de corrosão diminui quando é aplicadaliga que contenha cromo. Aço inoxidável 304L é o maistipicamente aplicado para o controle da corrosão por sulfidação(Figura 1). Por sua vez, o níquel é muito suscetível asulfidação e ligas compostas com altos teores de Ni podemsofrer sulfidação muito rapidamente a temperaturas acimados 630ºC (Salmenoja, 2004). Um dos produtos da corrosão,uma mistura de níquel e sulfeto de níquel (NiS), funde nessatemperatura. Portanto, ligas com alto teor de níquel nãodevem ser usadas acima dos 630ºC.Um caso curioso envolvendo corrosão do superaquecedor,provavelmente por mecanismo de sulfidação, foi testemunhadopor certa fábrica de celulose (Suik, 2000). A pressãode trabalho da caldeira era de 3,3-3,5 MPa e a temperaturacerca de 430ºC-450°C. Durante o tempo em que aconteceucorrosão rápida era utilizada uma mistura de tiossulfato(Na 2S 2O 3·5H 2O) e sulfato (Na 2SO 4) como sal de reposição(make up) e havia quantidades significativas de enxofre <strong>na</strong>ssuperfícies metálicas, sob a camada de depósitos. Foi afir-metal tubes (Vakkilainen, 2005). The reaction isdescribed by (1), where Me is iron (Fe), chromium(Cr), or nickel (Ni):H 2S (g)+ Me > MeS + H 2(g)(1)Corrosion due to sulfidation is low up to 250ºC, butwhen carbon steel is used it increases rapidly above310ºC. This type of corrosion decreases when alloycontaining chrome is selected. Stainless steel 304L isthe most typical to control sulfidation corrosion (Figure1). On the other hand, nickel is very susceptibleto sulfidation and alloys composed of high Ni contentscan sulfidize very rapidly at temperature higherthan 630ºC (Salmenoja, 2004). One of the corrosionproducts, a mixture of nickel and nickel sulfide (NiS),melts at this temperature. Therefore, high nickel alloysshould not be used at temperatures above 630ºC.One curious case involving corrosion of superheater,probably by sulfidation mechanism, was witnessedby one pulp mill (Suik, 2000). The boiler operatingpressure was 3.3-3.5 MPa and temperature around430ºC-450°C. During the time when rapid corrosionoccurred, a mix of thiosulphate (Na 2S 2O 3·5H 2O) andsulphate (Na 2SO 4) were used as make-up salt, and therewas significant amounts of sulfur on the metal sur-O PAPEL vol. 71, num. 6, pp. 57 - 71 JUN 2010O PAPEL - Junho 201060Taxa de corrosão (mm/ano) / Corrosion rate (mm/year)5.04.54.03.53.02.52.01.51.00.5Taxas de corrosão para diferentesconcentrações de H 2SCorrosion rates for differentconcentration of H 2SAço carbono / Carbon steel0.0250 300 350 400 450 500 550 600Temperatura (ºC) / Temperature (ºC)Figura 1. Efeito da temperatura e do H 2S <strong>na</strong> taxa de corrosão (Salmenoja e Tuiremo, 2001)Figure 1. Effect of temperature and H 2S on corrosion rate (Salmenoja and Tuiremo, 2001)10,00%1,00%10,00%10,00%1,00%0,10%
mado que o uso de Na 2S 2O 3·5H 2O poderia origi<strong>na</strong>r sulfetoextra e assim reduzir o ponto de fusão dos depósitos, comcrescimento da taxa de corrosão. Segundo Bruno (2004),em uma caldeira de recuperação a química do enxofre aindapredomi<strong>na</strong> sobre quaisquer influências do cloreto. Isso propõeque a química do enxofre poderia ser esquema de reação domais alto interesse para estudo.Yli-Olli et al. (2007) testaram, sob condições de redução,materiais como 304L, Sanicro 38, Sanicro 36Mo, Sanicro 65,4C54 e HR11N em diferentes misturas de gases de sulfetode hidrogênio (H 2S) e monóxido de carbono (CO), com esem adição de vapor d’água. Os resultados mostraram que aadição de 15% de vapor d’água protegia o material de testeda sulfidação. Sem o vapor d’água, a sulfidação começoua baixas concentrações de H 2S e foi se acelerando com oaumento da concentração. Nesses testes, o aço inoxidávelaustenítico 304L e o Sanicro 36Mo demonstraram a melhorresistência à sulfidação.face under the deposit layer. They state that the use ofNa 2S 2O 3·5H 2O might form extra sulfide and so reducemelting point of deposits and increase the corrosionrate. According to Bruno (2004), in a kraft recoveryboiler the sulfur chemistry is still domi<strong>na</strong>ting over anychloride influences. It means that the sulfur chemistrymay be most interesting reaction scheme to study.Yli-Olli et al. (2007) tested, under reducing conditions,materials such as 304L, Sanicro 38, Sanicro36Mo, Sanicro 65, 4C54 and HR11N in different hydrogensulphide (H 2S) and carbon monoxide (CO) gas mixtures,with and without addition of water vapour. Theresults showed that an addition of 15% of water vapourprotected the test materials from sulfidation. Withoutwater vapour, sulfidation started at low H 2S concentrationsand was accelerated by increasing the concentration.In these tests the austenitic stainless steel 304Land Sanicro 36Mo had the best sulfidation resistance.Oxidação ativaA oxidação ativa reporta-se a um processo onde a formaçãode cloreto metálico volátil incrementa a oxidação da liga.Nas ligas Fe-Cr, cloreto de ferro (FeCl 2) é principalmenteresponsável por oxidação ativa. Foram exami<strong>na</strong>dos algunsmecanismos de corrosão por cloro do superaquecedor (Grabkeet al.,1995), e podem ser sugeridas algumas reações.Cloretos alcalinos do fluxo de gás condensam nos tubos dosuperaquecedor e reagem com os óxidos de ferro ou cromo:2NaCl (s)+ Fe 2O 3(s)+ 0,5O 2> 2NaFeO 2+ Cl 2hematita (2)3NaCl (s)+ 2Fe 3O 4(s)+ 2O 2> 3NaFe 2O 4+ 1,5Cl 2magnetita(3)Os cloretos alcalinos no depósito podem também reagircom dióxido de enxofre da fase gás:2NaCl (s)+ SO 2 (g)+ O 2> Na 2SO 4+ Cl 2(4)O cloro formado propaga-se através de trincas ou poros nodepósito para a interface metálica e <strong>na</strong> ausência de oxigênio,condições redutoras, reage com ferro:Fe (s)+ Cl 2 (g)> FeCl 2 (s)(5)A altas temperaturas, o cloreto de ferro é volatilizado:FeCl 2 (s)> FeCl 2 (g)(6)Os cloretos de ferro gasosos formados reagem com oxigêniodando origem a um óxido de ferro poroso e regenerandocloro. A sequência das reações pode ser observada <strong>na</strong> Figura 2.2FeCl 2 (g)+ 1,5 O 2> Fe 2O 3+ 2Cl 2(7)3FeCl 2 (g)+ 2O 2> Fe 3O 4+ 3Cl 2(8)Active oxidationActive oxidation refers to a process where volatilemetal chloride formation enhances the oxidation of thealloy. In Fe-Cr alloys, iron chloride (FeCl 2) is mainlyresponsible for active oxidation. Some mechanisms for superheaterchlorine corrosion have been discussed (Grabkeet al., 1995), and some reactions can be suggested. Alkalichlorides from the flue gas condense on the superheatertubes and react with iron or chromium oxides:2NaCl (s)+ Fe 2O 3(s)+ 0.5O 2> 2NaFeO 2+ Cl 2hematite (2)3NaCl (s)+ 2Fe 3O 4(s)+ 2O 2> 3NaFe 2O 4+ 1.5Cl 2magnetite(3)The alkali chlorides in the deposit can also reactwith sulfur dioxide from the gas phase2NaCl (s)+ SO 2 (g)+ O 2> Na 2SO 4+ Cl 2(4)The chlorine formed diffuses through cracks orpores in the deposit to the metal interface and in absenceof oxygen, reducing conditions, reacts with iron:Fe (s)+ Cl 2 (g)> FeCl 2 (s)(5)At high temperatures, the iron chloride is volatilized:FeCl 2 (s)> FeCl 2 (g)(6)The formed gaseous iron chlorides react with oxygenforming a porous iron oxide and regenerating chlorine.The sequence of reactions can be observed in Figure 2.2FeCl 2 (g)+ 1.5 O 2> Fe 2O 3+ 2Cl 2(7)3FeCl 2 (g)+ 2O 2> Fe 3O 4+ 3Cl 2(8)O PAPEL - Junho 2010 O PAPEL vol. 71, num. 6, pp. 57 - 71 JUN 201061
- Page 2 and 3:
Quanto mais tecnologia,mais economi
- Page 4 and 5:
4O PAPEL - Junho 2010Artigo Gestão
- Page 6 and 7:
Sumário SummaryBANCO DE IMAGENS AB
- Page 8:
EditorialEditorialBanco de Imagens
- Page 11 and 12: cooperativos de ajuda mútua orien-
- Page 13: up in following one’s dream is a
- Page 16 and 17: Adora futebol,automóveis antigos e
- Page 18 and 19: CADERNO BRACELPAO PAPEL - Junho 201
- Page 20: CADERNO BRACELPAa logística revers
- Page 23 and 24: companies, Bracelpa promoted in Sã
- Page 25 and 26: Setor EconômicoEconomic sectorCres
- Page 27 and 28: Administração Eficaz&Competitivid
- Page 29 and 30: de vida em que a gestão da nossa v
- Page 31 and 32: Coluna ABPO ABPO ColumnSemestre fav
- Page 33 and 34: Artigo ABPOABPO ArticleRuptura nos
- Page 35: Adespeito de qualquer previsãoapoc
- Page 38 and 39: O PAPEL - Junho 201038Um bom exempl
- Page 40 and 41: Conhecimento essencialpara papel e
- Page 42 and 43: Voith Paper na PulPaper e Zellchemi
- Page 44 and 45: O PAPEL - Junho 2010O PAPEL vol. 71
- Page 46 and 47: O PAPEL vol. 71, num. 6, pp. 43 - 5
- Page 48 and 49: Tabela 3. Condições de branqueame
- Page 50 and 51: Tabela 6. Resultados teste de Tukey
- Page 52 and 53: Tabela 7. Médias do índice de tra
- Page 54 and 55: Referências / ReferencesO PAPEL vo
- Page 57 and 58: Artigo TécnicoPEER-REVIEWED ARTICL
- Page 59: pode induzir inesperadamente a alta
- Page 63 and 64: 2, 3, 4 e 9 podem também acontecer
- Page 65 and 66: alta do superaquecedor, no banco ge
- Page 67 and 68: Figura 4. Imagem por microscópio
- Page 69 and 70: Apêndice 1. Exemplo de composiçõ
- Page 71 and 72: 19. Malkow T. , Mäkipää M.I., Un
- Page 73: Este anúncio é para lembrar que o
- Page 76 and 77: ABTCP - Associação Brasileira Té
- Page 78 and 79: O PAPEL - Junho 201078lação a de
- Page 80 and 81: O PAPEL - Junho 201080Miolo(R$ por
- Page 82 and 83: DiretoriaBoard of DirectorsO PAPEL
- Page 84: Procurando as melhores oportunidade