pdf-Version
pdf-Version
pdf-Version
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
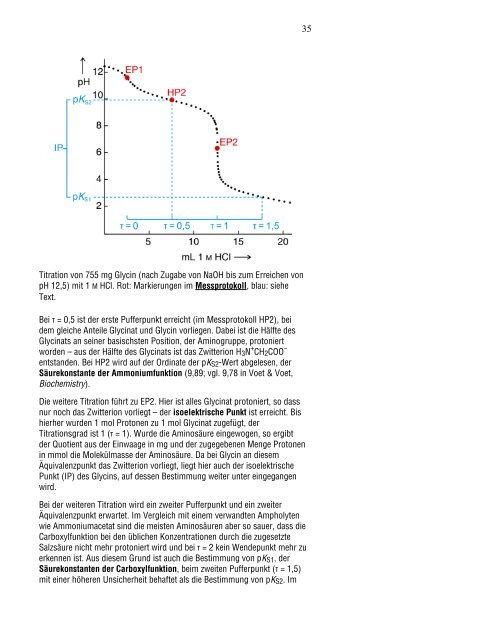
Titration von 755 mg Glycin (nach Zugabe von NaOH bis zum Erreichen von<br />
pH 12,5) mit 1 M HCl. Rot: Markierungen im Messprotokoll, blau: siehe<br />
Text.<br />
Bei τ = 0,5 ist der erste Pufferpunkt erreicht (im Messprotokoll HP2), bei<br />
dem gleiche Anteile Glycinat und Glycin vorliegen. Dabei ist die Hälfte des<br />
Glycinats an seiner basischsten Position, der Aminogruppe, protoniert<br />
worden – aus der Hälfte des Glycinats ist das Zwitterion H3N + CH2COO −<br />
entstanden. Bei HP2 wird auf der Ordinate der pKS2-Wert abgelesen, der<br />
Säurekonstante der Ammoniumfunktion (9,89; vgl. 9,78 in Voet & Voet,<br />
Biochemistry).<br />
Die weitere Titration führt zu EP2. Hier ist alles Glycinat protoniert, so dass<br />
nur noch das Zwitterion vorliegt – der isoelektrische Punkt ist erreicht. Bis<br />
hierher wurden 1 mol Protonen zu 1 mol Glycinat zugefügt, der<br />
Titrationsgrad ist 1 (τ = 1). Wurde die Aminosäure eingewogen, so ergibt<br />
der Quotient aus der Einwaage in mg und der zugegebenen Menge Protonen<br />
in mmol die Molekülmasse der Aminosäure. Da bei Glycin an diesem<br />
Äquivalenzpunkt das Zwitterion vorliegt, liegt hier auch der isoelektrische<br />
Punkt (IP) des Glycins, auf dessen Bestimmung weiter unter eingegangen<br />
wird.<br />
Bei der weiteren Titration wird ein zweiter Pufferpunkt und ein zweiter<br />
Äquivalenzpunkt erwartet. Im Vergleich mit einem verwandten Ampholyten<br />
wie Ammoniumacetat sind die meisten Aminosäuren aber so sauer, dass die<br />
Carboxylfunktion bei den üblichen Konzentrationen durch die zugesetzte<br />
Salzsäure nicht mehr protoniert wird und bei τ = 2 kein Wendepunkt mehr zu<br />
erkennen ist. Aus diesem Grund ist auch die Bestimmung von pKS1, der<br />
Säurekonstanten der Carboxylfunktion, beim zweiten Pufferpunkt (τ = 1,5)<br />
mit einer höheren Unsicherheit behaftet als die Bestimmung von pKS2. Im<br />
35