VSAO JOURNAL Nr. 5 - Oktober 2018
Energie - Onkologie Pharmazeutische Medizin Einheitliche Finanzierung - ja, aber
Energie -
Onkologie
Pharmazeutische Medizin
Einheitliche Finanzierung - ja, aber
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
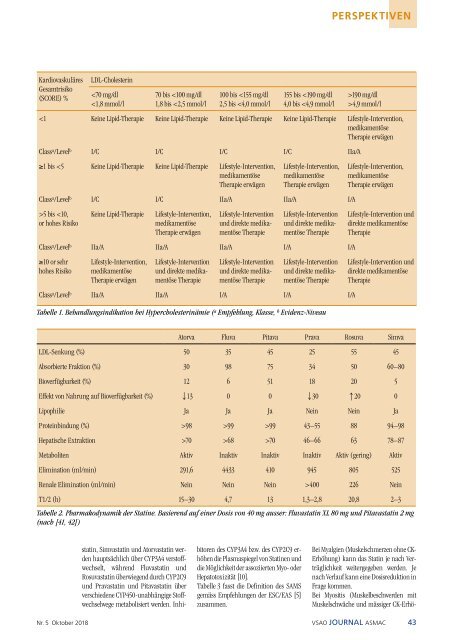
PERSPEKTIVEN<br />
Kardiovaskuläres<br />
Gesamtrisiko<br />
(SCORE) %<br />
LDL-Cholesterin<br />