- Seite 1: Helikal-chirale, stereoreguläre Po
- Seite 5: Die vorliegende Arbeit wurde unter
- Seite 9 und 10: Inhaltsverzeichnis Inhaltsverzeichn
- Seite 11 und 12: 6.5.3 Polymerisation von Monomer 55
- Seite 13 und 14: Abbildung 4-5: Drehwert von Copolym
- Seite 15 und 16: Verzeichnis der Schemata Schema 1-1
- Seite 17 und 18: Tabellenverzeichnis Tabelle 4-1: Ho
- Seite 19 und 20: 1 Einleitung Die Organokatalyse und
- Seite 21 und 22: Entwicklung angeführt werden. Orga
- Seite 23 und 24: natürlichen helikalen Polymers als
- Seite 25: esultieren. Da die Helixinversionsb
- Seite 28 und 29: die Kettenwachstumsreaktion startet
- Seite 30 und 31: Als „beliebteste“ Modell-Polyme
- Seite 32 und 33: Die Polymerüberstruktur kann als (
- Seite 34 und 35: 2.3 Chirale Polyisocyanate Bedingt
- Seite 36 und 37: D H NCO 30 25 [α] D = +0.65 (in Su
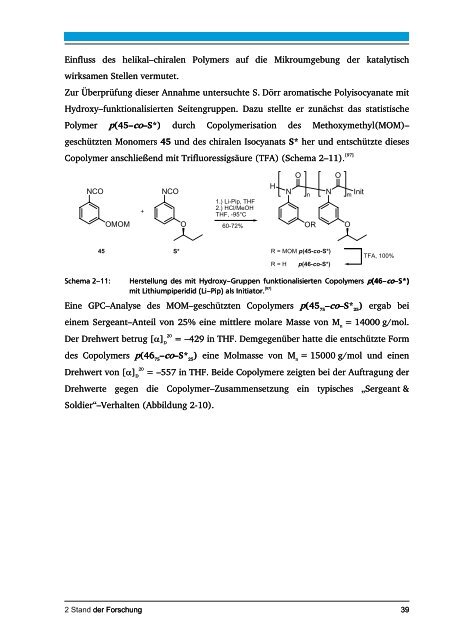
- Seite 38 und 39: gleichen optischen Aktivität wie e
- Seite 40 und 41: Es wurde erneut eine nicht-lineare
- Seite 42 und 43: [88, 89] Messung der Elliptizität
- Seite 44 und 45: 2.4 Helikale Polymere als Liganden
- Seite 48 und 49: [α] D 100 0 -100 -200 -300 -400 -5
- Seite 50 und 51: tropos atropos Abbildung 2-11: Trop
- Seite 53 und 54: 3 Zielsetzung Aufmerksam gemacht du
- Seite 55: Deren Konformation wiederum sollte
- Seite 58 und 59: R H O 2N 57 N O OH OH OPG OPG N O n
- Seite 60 und 61: 4.1.1 Suzuki-Kupplungen Der Schlüs
- Seite 62 und 63: Voraussetzungen erfüllen: So sollt
- Seite 64 und 65: dem bekannt war, dass es einhändig
- Seite 66 und 67: Bevor die Monomere 55a-55f zur Hers
- Seite 68 und 69: Das Homopolymer p(55a) entstand in
- Seite 70 und 71: Vorzugskonformation im helikalen R
- Seite 72 und 73: Temperatur gemessene Drehwert wiede
- Seite 74 und 75: [α] D 400 200 0 -200 -400 -600 -80
- Seite 76 und 77: In THF steigt die molare Elliptizit
- Seite 78 und 79: [α] D 200 0 -200 -400 -600 -800 n-
- Seite 80 und 81: Θ max (Polymer-Rückgrat) [mdeg m
- Seite 82 und 83: Die chiroptischen Eigenschaften der
- Seite 84 und 85: Θ max (Polymer-Rückgrat) [mdeg m
- Seite 86 und 87: Θ [mdeg m 2 mol -1 ] 5000 0 -5000
- Seite 88 und 89: geringem Ausmaß stattfand. Bei hö
- Seite 90 und 91: 4.2.10 Synthese des Copolymers p(53
- Seite 92 und 93: 4.3 Katalyseexperimente Während de
- Seite 94 und 95: O O O O H H R 2 O R 1 Abbildung 4-2
- Seite 96 und 97:
4.3.2 Morita-Baylis-Hillman-Reaktio
- Seite 98 und 99:
Insgesamt ist diese Reaktion wahrsc
- Seite 100 und 101:
Vorschrift von Rueping et al. [105]
- Seite 102 und 103:
4.4 Stereochemische Gesamtbetrachtu
- Seite 104 und 105:
(vgl. Kapitel 4.2), so scheint bei
- Seite 106 und 107:
A Helix B Helix C Achse Zentrochira
- Seite 108 und 109:
auf folgender Überlegung: Die Trim
- Seite 110 und 111:
Für das Phosphorsäurederivat p(54
- Seite 112 und 113:
Θ [mdeg m 2 mol -1 ] 10000 5000 0
- Seite 114 und 115:
die Gesamtflexibilität und damit a
- Seite 116 und 117:
und dem helikalen Rückgrat bewirke
- Seite 118 und 119:
OCN NCO O O O O OCN NCO OMOM OMOM O
- Seite 120 und 121:
88 N PMP n-C 5H 11 H N O O n N m In
- Seite 122 und 123:
einheitlichen Polymerrückgrat füh
- Seite 124 und 125:
Vorteilhaft aus präparativer Sicht
- Seite 126 und 127:
Reaktionsführung: Reaktionen bei T
- Seite 128 und 129:
Falls die Zuordnung der Signale nic
- Seite 130 und 131:
Das Spektrometer misst das CD-Signa
- Seite 132 und 133:
6.2.4 Allgemeine Arbeitsvorschrift
- Seite 134 und 135:
sowie des Initiators bezogen. Bei C
- Seite 136 und 137:
2 N NaOH und dann mit halbkonzentri
- Seite 138 und 139:
6.3.3.2 Herstellung von 2-Iod-4-nit
- Seite 140 und 141:
abgekühlt und 12.91 ml (56.15 mmol
- Seite 142 und 143:
Der AAV1 folgend werden 10.73 g (40
- Seite 144 und 145:
6.3.5.4 Herstellung von 5-Nitro-5'-
- Seite 146 und 147:
13 C-NMR C-NMR (CDCl3 , 125 MHz, 30
- Seite 148 und 149:
128.58 (1-C), 129.09 (9-C), 129.78
- Seite 150 und 151:
1 H-NMR H-NMR (CDCl3 , 500 MHz, 300
- Seite 152 und 153:
R F = 0.22 (PE/EE = 5:1). Schmp.: 7
- Seite 154 und 155:
6.4.3.3 Herstellung von 4-Isocyanat
- Seite 156 und 157:
C), 127.47 (6-C), 129.63 (1-C), 129
- Seite 158 und 159:
IR (Film): ν ~ = 2955.5, 2902.7 (C
- Seite 160 und 161:
13 C-NMR C-NMR (CDCl3, 125 MHz, 300
- Seite 162 und 163:
Schmp.: 52-53°C 1 H-NMR H-NMR (CDC
- Seite 164 und 165:
(99%) 5-Isocyanat-2,2'-bis-methoxym
- Seite 166 und 167:
6.5.2 Polymerisation von Monomer 55
- Seite 168 und 169:
0.02 Äq.) Lithium-Piperidid-Lösun
- Seite 170 und 171:
IR (KBr): ν ~ = 3069.0 (CH Aromat)
- Seite 172 und 173:
6.5.5.2 Copolymerisation von 5-Isoc
- Seite 174 und 175:
1 H-NMR H-NMR (CDCl3 , 300 MHz, 300
- Seite 176 und 177:
Drehwert: [ ] 20 D α [ ] 20 α [ ]
- Seite 178 und 179:
Drehwert: [ ] 20 D α [ ] 20 α [ ]
- Seite 180 und 181:
Drehwert: [ ] 20 D α [ ] 20 α [ ]
- Seite 182 und 183:
Drehwert: [ ] 20 D α [ ] 20 α [ ]
- Seite 184 und 185:
1 H-NMR H-NMR (CDCl3 , 300 MHz, 300
- Seite 186 und 187:
ESI-MS m/z (%): 1179 (13, [M(64)+Na
- Seite 188 und 189:
1 H-NMR (CDCl3 , 300 MHz, 300 K):
- Seite 190 und 191:
Drehwert: [ ] 20 D α [ ] 20 α [ ]
- Seite 192 und 193:
Drehwert: [ ] 20 D α [ ] 20 α [ ]
- Seite 194 und 195:
6.8 Synthese von polymeren Phosphor
- Seite 196 und 197:
Drehwert: [ ] 20 D α [ ] 20 α [ ]
- Seite 198 und 199:
= 3:1, 320 ml). Die Enantiomerenüb
- Seite 200 und 201:
[28] Y. Okamoto, T. Nakano, Chem. R
- Seite 202 und 203:
[91] K. Yoshiba, R. Hama, A. Teramo
- Seite 204 und 205:
[159] A. A. Maryott, M. E. Hobbs, P
- Seite 207:
Anna Karina Möller Rheinstr. 329 6
- Seite 211:
H N O p(S*) n O n-C 5H 11 n-C 5H 11