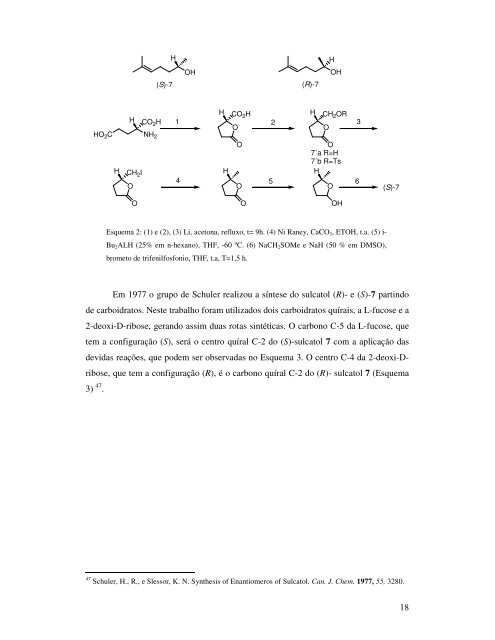
H CO 2H HO 2C NH 2 H CH 2I O O H OH (S)-7 (R)-7 H CO2H H CH2OR 1 2 3 O O O O 7´a R=H 7´b R=Ts H H 4 O 5 O 6 O Esquema 2: (1) e (2), (3) Li, acetona, refluxo, t= 9h. (4) Ni Raney, CaCO3, ETOH, t.a. (5) i- Bu2ALH (25% em n-hexano), THF, -60 ºC. (6) NaCH2SOMe e NaH (50 % em DMSO), brometo <strong>de</strong> trifenilfosfonio, THF, t.a, T=1,5 h. H OH OH (S)-7 Em 1977 o grupo <strong>de</strong> Schuler realizou a <strong>síntese</strong> do sulcatol (R)- e (S)-7 partindo <strong>de</strong> carboidratos. Neste trabalho foram utilizados dois carboidratos quírais, a L-fucose e a 2-<strong>de</strong>oxi-D-ribose, gerando assim duas rotas sintéticas. O carbono C-5 da L-fucose, que tem a configuração (S), será o centro quíral C-2 do (S)-sulcatol 7 com a aplicação das <strong>de</strong>vidas reações, que po<strong>de</strong>m ser observadas no Esquema 3. O centro C-4 da 2-<strong>de</strong>oxi-D- ribose, que tem a configuração (R), é o carbono quíral C-2 do (R)- sulcatol 7 (Esquema 3) 47 . 47 Schuler, H., R., e Slessor, K. N. Synthesis of Enantiomeros of Sulcatol. Can. J. Chem. 1977, 55, 3280. 18
CHO HO H H OH H OH HO H CH3 L-fucose H H H HO CHO H OH OH H CH3 2-<strong>de</strong>oxi-D-ribose O O 1 O 2 3 HO OCH3 O OCH 4 3 RO OCH 3 HO OH O OR R= H R=COC 6H 5 RO OBz R= H R=CH 3SO 2 5 O OCH3 6 O OR 7 H H CHO H H 8 OBz OH R=CH3 R= H OHCO H CH3 ROH2C O OCH H2CI O 3 OCH3 a b c H2CI O OCH 3 d RO R = H R =CH2SO3 R=p-CH3CH 6H4SO2 I Esquema3: (1) metanol, HCl 0,5M, refluxo, 1,5h. (2) cloreto <strong>de</strong> zinco, H3PO4 concentrado, acetona, t.a, 1,5h e cloreto <strong>de</strong> benzoila, piridina anidra, 2h. (3) ácido acético aquoso 50%, 70ºC, 1h e piridina anidra, cloreto <strong>de</strong> metanosulfonila, t.a, overnight. (4) io<strong>de</strong>to <strong>de</strong> sódio, zinco em pó, DMF, refluxo, 1h. (5) Pd em carbono 10%, H 2, metanol, t.a, 12h. (6) metanol, KOH 0,5M, refluxo, 1h. e Dowex 50[H + ] ,agua <strong>de</strong>stilada, 60 ºC, 3h (7) agua <strong>de</strong>stilada, periodato <strong>de</strong> sódio, 0ºC, 10 min. (8) io<strong>de</strong>to <strong>de</strong> isopropiltrifenilfosfonio, n-butillitio em hexano, THF, 0ºC, 1h. (a) HCL em metanol 0,01M, t.a, 30 min. e cloreto <strong>de</strong> metanosulfonila, piridina seca, t.a, 15h (b) io<strong>de</strong>to <strong>de</strong> sódio, DMF, 70ºC, 5h. (c) níquel Raney, KOH, metanol, H2, t.a, 14h e Dowex 50[H + ], água <strong>de</strong>stilada, 50 ºC, 1h. (d) io<strong>de</strong>to <strong>de</strong> isopropiltrifenilfosfonio, n-butillitio em hexano, THF anidro, 0ºC, 2h O OBz CH H H H H HO H CH3 (S)-sulcatol CH H H H H H OH CH3 (R)-sulcatol O grupo <strong>de</strong> Slessor realizou a <strong>síntese</strong> do (R)-sulcatol 7 em 1979, partindo do (S)- lactato <strong>de</strong> etila, via metiloxiranos quírais. Neste trabalho ele realizou uma abertura enantioseletiva do epóxido com um reagente <strong>de</strong> Grignard alilico tendo como produto da reação o (R)- sulcatol 7 em boa pureza óptica (Esquema 4). 48 H OTs CH 3 CO 2Et BH 3 THF H OTs KOH 50% H O MgCl OH CH 3 CH 2OH 2-o-p-toluenosulfonil (S)-lactato (R)-sulcatol Esquema 4: Síntese do sulcatol via metiloxiranos 48 Johnston, B. D., e Slessor, K. N. Facile Syntheses of Enantiomers of Sulcatol. Can. J. Chem. 1979, 57, 233. CuI 19 OCH 3
- Page 1 and 2: UNIVERSIDADE FEDERAL FLUMINENSE CEN
- Page 3 and 4: ALISSON FAGNER DOS SANTOS TRINDADE
- Page 5 and 6: ÍNDICE Resumo.....................
- Page 7 and 8: “Não há nada que seja maior evi
- Page 9 and 10: RESUMO Este trabalho amplia o estud
- Page 11 and 12: AG: Agitação Magnética AOP: Aspe
- Page 13 and 14: As hidrólises mediadas por enzimas
- Page 15 and 16: 2.2- Feromônios Fluxograma 1: Clas
- Page 17 and 18: nonanona 3 é o feromônio sexual f
- Page 19 and 20: 3 FEROMÔNIOS, HISTÓRICO E ALGUMAS
- Page 21: pragas. Foi observado que este inse
- Page 25 and 26: Em 2000 o (S)-sulcatol 7 foi sintet
- Page 27 and 28: Em 1991 Mori e colaboradores obtive
- Page 29 and 30: da água teve pouca influencia sobr
- Page 31 and 32: Em 1997 algumas bactérias anaerób
- Page 33 and 34: Posteriormente o álcool assim obti
- Page 35 and 36: Chem e colaboradores realizaram a s
- Page 37 and 38: Em 2004, Zarbin e colaboradores mai
- Page 39 and 40: 4. ENZIMAS As enzimas são proteín
- Page 41 and 42: A especificidade da enzima perante
- Page 43 and 44: 25 OH O + lipase O OAc OH + (R)-25a
- Page 45 and 46: necessita de elevadas temperaturas
- Page 47 and 48: O primeiro trabalho relatando o uso
- Page 49 and 50: 6. OBJETIVO Este trabalho tem como
- Page 51 and 52: OH Hidrólise enzimática OAc Aceti
- Page 53 and 54: 8- RESULTADOS E DISCUSSÃO Neste ca
- Page 55 and 56: Os álcoois foram preparados em bon
- Page 57 and 58: utilizá-la na hidrólise enzimáti
- Page 59 and 60: O uso do banho de ultra-som mostrou
- Page 61 and 62: Como é possível observar pelos re
- Page 63 and 64: Entrada Tempo Tabela 6: Hidrólises
- Page 65 and 66: C o n v e r s ã o % 60 50 40 30 20
- Page 67 and 68: hidrogênio dos álcoois e dos acet
- Page 69 and 70: Como foi descrito anteriormente, as
- Page 71 and 72: Desta maneira, como somente a regi
- Page 73 and 74:
eacional. O pico referente ao H-2 n
- Page 75 and 76:
Figura 12: espectros do 22 e 22a .
- Page 77 and 78:
PLE / Agitação Magnética /30´/1
- Page 79 and 80:
A conversão do acetato 26a no resp
- Page 81 and 82:
8.4.3 Analise das conversões dos a
- Page 83 and 84:
AOP/ Agitação Magnética/4 horas/
- Page 85 and 86:
PLE/ Agitação Magnética /3 horas
- Page 87 and 88:
10. EXPERIMENTAL O estudo da aplica
- Page 89 and 90:
CETONAS 10.2 PROCEDIMENTO GERAL PAR
- Page 91 and 92:
10.3 PROCEDIMENTO PARA REAÇÃO DE
- Page 93 and 94:
2) acetato de 2-metil-4-octanol 17a
- Page 95 and 96:
7) Acetato de 2-etil-hexanol 23a.
- Page 97 and 98:
1) Acetato de 1-metil-1-(5-metiltet
- Page 99 and 100:
4 20a 70 12 US 5 20a 90 10 AM 6 20a
- Page 101 and 102:
Tabela 12: Resultados da Hidrólise
- Page 103 and 104:
permaneceu sob agitação ou ultra-
- Page 105 and 106:
12. Byrne, K. J. Swigar, A. A., Sil
- Page 107 and 108:
33. Mori, K., Absolute-Configuratio
- Page 109 and 110:
55. Afonso, C. M., Barros, T. M., G
- Page 111 and 112:
75. Tuter, M., Secundo, F., Riva, S
- Page 113 and 114:
97. Okitsu, K.; Bandow, H.; Maeda,
- Page 115 and 116:
12. ANEXOS H2´, H3´, H4´, H5´ E
- Page 117 and 118:
137.04 138.72 128.92 128.59 127.47
- Page 119 and 120:
Espectro 9: Infravermelho do Cicloh
- Page 121 and 122:
H3C 1 O 2 O 8 3 CH3 9 4 5 10 CH3 6
- Page 123 and 124:
C 9 170.88 Chloroform-d C4 170 160
- Page 125 and 126:
Espectro 21: Infravermelho do aceta
- Page 127 and 128:
1481.6 1475.3 1469.0 1462.3 1456.2
- Page 129 and 130:
C 8 170.35 C 2 136.54 116.40 C3 Chl
- Page 131 and 132:
Espectro 33: Infravermelho do aceta
- Page 133 and 134:
H 1 ´, H 2 ´, H 3 ´ e H 4 ´ 7.3
- Page 135 and 136:
C 8 170.29 C 1 ´ 139.56 127.00 128
- Page 137 and 138:
Espectro 46 RMN 1 H (300 MHz, CDCl3