horizonte - der Koordinierungsstelle - Hochschule Mannheim
horizonte - der Koordinierungsstelle - Hochschule Mannheim
horizonte - der Koordinierungsstelle - Hochschule Mannheim
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
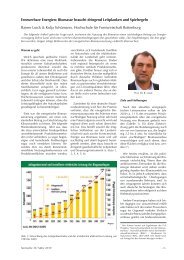
Messung <strong>der</strong> Wärmeproduktion von Bakterien im Bioreaktor: Kalorimetrische Regelung<br />
von Bioprozessen zur Herstellung von rekombinanten Proteinen<br />
Richard Biener, Anne Steinkämper, Thomas Horn, Johannes Hofmann, <strong>Hochschule</strong> Esslingen<br />
Rekombinante Proteine wie z.B. Insulin o<strong>der</strong> Interferone gehören zu den wichtigsten Produkten <strong>der</strong> mo<strong>der</strong>nen Biotechnologie.<br />
Hergestellt werden rekombinante Proteine mit gentechnisch verän<strong>der</strong>ten Organismen (GVO). Hier kommen<br />
neben den Mikroorganismen (E.coli o<strong>der</strong> Hefezellen) auch tierische Zellkulturen zum Einsatz. Zur Erhöhung <strong>der</strong> Produktivität<br />
und <strong>der</strong> Reproduzierbarkeit des Kultivierungsprozesses ist eine automatisierte Prozessführung erfor<strong>der</strong>lich. Im Beitrag<br />
wird gezeigt, wie mit Hilfe kalorimetrischer Methoden die spezifi sche Wachstumsrate von Mikroorganismen während <strong>der</strong><br />
Kultivierung in einem Standard-Bioreaktor geregelt werden kann. Diese Automatisierungsstrategie führt zu einer deutlichen<br />
Steigerung <strong>der</strong> Produktivität und Reproduzierbarkeit des Prozesses.<br />
Bedeutung <strong>der</strong> Hochzelldichtekultivierung<br />
in <strong>der</strong> pharmazeutischen Industrie<br />
Gentechnisch hergestellte Proteine,<br />
so genannte rekombinante Proteine,<br />
werden in <strong>der</strong> pharmazeutischen Industrie<br />
mit Hilfe gentechnisch verän<strong>der</strong>ter,<br />
leben<strong>der</strong> Mikroorganismen o<strong>der</strong> Zelllinien<br />
hergestellt. Allgemein werden<br />
diese als Biopharmazeutika bezeichnet.<br />
Beispiele für diese unverzichtbar<br />
gewordenen Arzneimittel sind Insuline,<br />
monoklonale Antikörper o<strong>der</strong> Erythropoetine.<br />
Beim Herstellungsprozess<br />
eines Biopharmazeutikums produzieren<br />
diese gentechnisch modifi zierten<br />
Bakterien, Hefen o<strong>der</strong> Säugetierzellen<br />
in einem Bioreaktor das entsprechende<br />
Protein. Zur Erhöhung <strong>der</strong> Proteinausbeute<br />
werden in <strong>der</strong> biopharmazeutischen<br />
Industrie Hochzelldichte-Fed-<br />
Batch-Prozesse eingesetzt [1, 2]. Um<br />
hohe Zelldichten zu erzielen, wird bei<br />
diesen Prozessen mit Hilfe einer Pumpe<br />
dem Bioreaktor ein konzentriertes<br />
Nährmedium kontinuierlich zugeführt.<br />
Über diese Zufütterung kann direkt<br />
das Zellwachstum und die Produktion<br />
stören<strong>der</strong> Nebenprodukte beeinfl usst<br />
werden. Nebenprodukte sind in diesen<br />
Prozessen unerwünscht, da sie das<br />
Wachstum <strong>der</strong> Zellen inhibieren, woraus<br />
auch eine geringe Proteinausbeute<br />
resultiert.<br />
Insulin, Interferon und weitere Arzneistoffe<br />
werden weit verbreitet von<br />
gentechnisch verän<strong>der</strong>ten Escherichia<br />
coli Bakterien hergestellt. Um die Produktivität<br />
von rekombinanten Proteinen<br />
in E. coli zu maximieren, muss<br />
die Zufütterung des Nährmediums mit<br />
<strong>der</strong> wachstumslimitierenden Kohlenstoff-Quelle<br />
(z.B. Glucose) so erfolgen,<br />
dass die Wachstumsrate <strong>der</strong> Bakterien<br />
unter einem kritischen Wert gehalten<br />
wird. Damit kann die Produktion von<br />
wachstumsinhibierenden Nebenprodukten<br />
(z.B. Acetat) minimiert werden<br />
und die Bakterien können ungehin<strong>der</strong>t<br />
wachsen. Durch diese Zufütterungs-<br />
strategie können Biotrockenmasse-<br />
Konzentrationen von mehr als 100 g/l<br />
erreicht werden [1]. Diese hohen Zelldichten<br />
führen wie<strong>der</strong>um zu hohen<br />
Proteinkonzentrationen. Die eingestellte<br />
Wachstumsrate sollte allerdings<br />
nicht zu klein sein, um die Prozessdauer<br />
möglichst kurz zu halten.<br />
Prozessführungsstrategien<br />
Für Hochzelldichte-Kultivierungsprozesse<br />
sind unterschiedliche Strategien<br />
in <strong>der</strong> Literatur beschrieben. Eine<br />
häufi g angewandte Methode ist die<br />
Zufütterung mit einem vorab festgelegten<br />
Profi l. Nachdem die Kohlenstoff-<br />
Quelle (z.B. Glucose) im Nährmedium<br />
verbraucht ist, wird dabei die Feeding-Rate<br />
exponentiell erhöht, um die<br />
spezifi sche Wachstumsrate näherungsweise<br />
konstant zu halten [3]. Ein fest<br />
vorgegebenes Zufütterungsprofi l hat<br />
im Wesentlichen den Nachteil, dass es<br />
bei einer falschen Abschätzung <strong>der</strong> Parameter<br />
o<strong>der</strong> bei einer Prozessstörung<br />
zu einer Überfütterung des limitierenden<br />
Substrats Glucose und damit auch<br />
zu einer erhöhten Acetatproduktion<br />
kommen kann. Daher ist es von Vorteil,<br />
eine geregelte Zufütterung vorzunehmen.<br />
In <strong>der</strong> Praxis werden oft indirekte<br />
Messgrößen für die Einstellung<br />
<strong>der</strong> Feedrate verwendet. Beispielsweise<br />
wird bei <strong>der</strong> DO-stat Methode die<br />
Feedrate über die Messung <strong>der</strong> Gelöstsauerstoffkonzentration<br />
(pO 2 ) geregelt.<br />
Wenn die wachstumslimitierende C-<br />
Quelle verbraucht ist, führt dies zu einem<br />
Anstieg des pO 2 und die Feedrate<br />
muss entsprechend angepasst werden,<br />
um den Substratmangel auszugleichen<br />
[4, 5]. Beim pH-stat wird die Feedrate<br />
aufgrund von Verän<strong>der</strong>ungen des pH-<br />
Werts bei einem Substratmangel eingestellt<br />
[6]. Bei beiden Strategien wird<br />
die spezifi sche Wachstumsrate indirekt<br />
durch den pH o<strong>der</strong> den pO 2 geregelt.<br />
Folglich ist eine konstante spezifi sche<br />
Wachstumsrate schwierig zu verwirklichen<br />
[7].<br />
Prof. Dr.-Ing. R. Biener<br />
Dipl. Biol. t. o. A. Steinkämper<br />
Dipl.-Ing. (FH) T. Horn<br />
Dipl.-Ing. (FH) J. Hofmann<br />
<strong>horizonte</strong> 40/ September 2012 - 3 -