Inserate Antidpressiva-neu
Inserate Antidpressiva-neu
Inserate Antidpressiva-neu
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
CEREBRALE AMYLOIDANGIOPATHIE<br />
einer post-mortem-Untersuchung des<br />
Gehirns, bei der wie oben beschriebene<br />
Veränderungen gewertet werden.<br />
Da die klinische Relevanz der CAA<br />
hauptsächlich in ihrer Ursache für nicht<br />
traumatische intrazerebrale Hämorrhagien<br />
(ICH) liegt, wurden die „Boston-<br />
Kriterien“ für die Diagnose von CAA-<br />
26<br />
4/2008<br />
bedingten ICH etabliert. Hier hilft vor<br />
allem die Lokalisation der ICH zur Diagnosefindung,<br />
da CAA vorwiegend lobäre<br />
cortikale Hämorrhagien verursacht,<br />
wohingegen in Regionen, die als<br />
typische Lokalisationen von hypertensiven<br />
Blutungen angesehen werden (z.B.<br />
Putamen, Thalamus und Brücke), keine<br />
CAA beobachtet wird.<br />
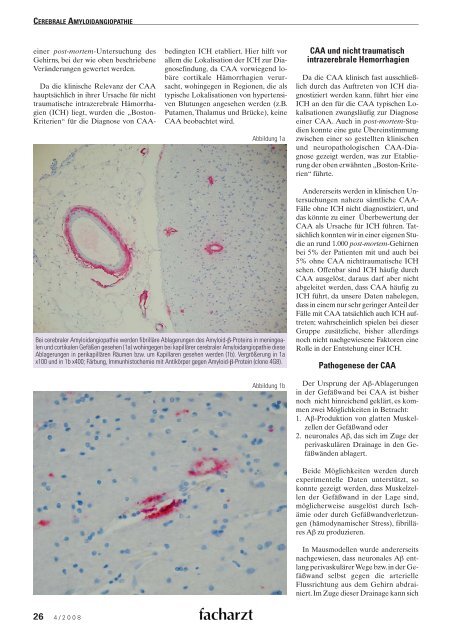
Abbildung 1a<br />
Bei cerebraler Amyloidangiopathie werden fibrilläre Ablagerungen des Amyloid-β-Proteins in meningealen<br />
und cortikalen Gefäßen gesehen (1a) wohingegen bei kapillärer cerebraler Amyloidangiopathie diese<br />
Ablagerungen in perikapillären Räumen bzw. um Kapillaren gesehen werden (1b). Vergrößerung in 1a<br />
x100 und in 1b x400; Färbung, Immunhistochemie mit Antikörper gegen Amyloid-β-Protein (clone 4G8).<br />
Abbildung 1b<br />
CAA und nicht traumatisch<br />
intrazerebrale Hemorrhagien<br />
Da die CAA klinisch fast ausschließlich<br />
durch das Auftreten von ICH diagnostiziert<br />
werden kann, führt hier eine<br />
ICH an den für die CAA typischen Lokalisationen<br />
zwangsläufig zur Diagnose<br />
einer CAA. Auch in post-mortem-Studien<br />
konnte eine gute Übereinstimmung<br />
zwischen einer so gestellten klinischen<br />
und <strong>neu</strong>ropathologischen CAA-Diagnose<br />
gezeigt werden, was zur Etablierung<br />
der oben erwähnten „Boston-Kriterien“<br />
führte.<br />
Andererseits werden in klinischen Untersuchungen<br />
nahezu sämtliche CAA-<br />
Fälle ohne ICH nicht diagnostiziert, und<br />
das könnte zu einer Überbewertung der<br />
CAA als Ursache für ICH führen. Tatsächlich<br />
konnten wir in einer eigenen Studie<br />
an rund 1.000 post-mortem-Gehirnen<br />
bei 5% der Patienten mit und auch bei<br />
5% ohne CAA nichttraumatische ICH<br />
sehen. Offenbar sind ICH häufig durch<br />
CAA ausgelöst, daraus darf aber nicht<br />
abgeleitet werden, dass CAA häufig zu<br />
ICH führt, da unsere Daten nahelegen,<br />
dass in einem nur sehr geringer Anteil der<br />
Fälle mit CAA tatsächlich auch ICH auftreten;<br />
wahrscheinlich spielen bei dieser<br />
Gruppe zusätzliche, bisher allerdings<br />
noch nicht nachgewiesene Faktoren eine<br />
Rolle in der Entstehung einer ICH.<br />
Pathogenese der CAA<br />
Der Ursprung der Aβ-Ablagerungen<br />
in der Gefäßwand bei CAA ist bisher<br />
noch nicht hinreichend geklärt, es kommen<br />
zwei Möglichkeiten in Betracht:<br />
1. Aβ-Produktion von glatten Muskelzellen<br />
der Gefäßwand oder<br />
2. <strong>neu</strong>ronales Aβ, das sich im Zuge der<br />
perivaskulären Drainage in den Gefäßwänden<br />
ablagert.<br />
Beide Möglichkeiten werden durch<br />
experimentelle Daten unterstützt, so<br />
konnte gezeigt werden, dass Muskelzellen<br />
der Gefäßwand in der Lage sind,<br />
möglicherweise ausgelöst durch Ischämie<br />
oder durch Gefäßwandverletzungen<br />
(hämodynamischer Stress), fibrilläres<br />
Aβ zu produzieren.<br />
In Mausmodellen wurde andererseits<br />
nachgewiesen, dass <strong>neu</strong>ronales Aβ entlang<br />
perivaskulärer Wege bzw.in der Gefäßwand<br />
selbst gegen die arterielle<br />
Flussrichtung aus dem Gehirn abdrainiert.Im<br />
Zuge dieser Drainage kann sich