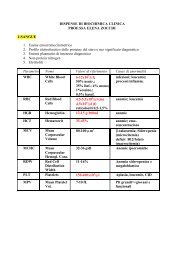
appunti di biochimica e biochimica nutrizionale - ClinicaVirtuale ...
appunti di biochimica e biochimica nutrizionale - ClinicaVirtuale ...
appunti di biochimica e biochimica nutrizionale - ClinicaVirtuale ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Giordano Perin; <strong>biochimica</strong>9: metabolismo degli amminoaci<strong>di</strong><br />
○ BIOSINTESI DI MOLECOLE IN GENERALE.<br />
○ COFATTORE DELL'ENZIMA COMT catecol O metil transferasi, enzima<br />
presente a livello epatico renale e intestinale, sostanzialmente questo enzima si<br />
occupa <strong>di</strong> trasferire un gruppo metilico su un composto <strong>di</strong> natura fenolica con la<br />
formazione <strong>di</strong> un legame etereo sul gruppo alcolico del fenolo stesso, SAM<br />
viene quin<strong>di</strong> convertito in SAO e rilascia il metile sull'ossidrile; il SAO non viene<br />
riconvertito in SAM ma subisce una serie <strong>di</strong> reazioni:<br />
■ IDROLISI DEL SAO vengono liberati OMOCISTEINA e ADENOSINA, questi:<br />
● OMOCISTEINA viene riconvertita generalmente in metionina e quin<strong>di</strong><br />
coinvolta <strong>di</strong> nuovo nella formazione <strong>di</strong> S adenosil metionina (con spesa <strong>di</strong><br />
tre molecole <strong>di</strong> fosfato); tuttavia la omocisteina può andare incontro ad un<br />
altro destino metabolico: può infatti essere trasformata in ALFA<br />
CHETOBUTIRRATO grazie all'operato <strong>di</strong> un enzima detto<br />
CISTATIONINA GAMMA LIASI.<br />
Queste reazioni sono particolarmente energetiche e quin<strong>di</strong> estremamente costose per la<br />
cellula.<br />
METABOLISMO DEL TRIPTOFANO:<br />
Il triptofano può andare incontro a due <strong>di</strong>fferenti vie cataboliche: la via<br />
più comune produce acetacetato e acido nicotinico, la seconda invece<br />
serotonina.<br />
TRASFORMAZIONE DEL TRIPTOFANO IN ACETACETATO E ACIDO<br />
NICOTINICO:<br />
● OSSIDAZIONE con ossigeno molecolare, si assiste alla rottura dell'anello<br />
aromatico con formazione <strong>di</strong> N FORMIL CHINURENINA:<br />
● IDROLISI DELLA FORMIL CHINURENINA, questa idrolizza la molecola in:<br />
○ FORMILE che si associa a tetraidrofolato formando l'N5 FORMIL<br />
TETRAIDROFOLATO utile, previa isomerizzazione a N10 formil tetraidrofolato<br />
per formare le purine.<br />
○ CHINURENINA che può essere trasformata con una serie <strong>di</strong> reazioni<br />
metaboliche in ACIDO NICOTINICO che può essere amminato a nicotinammide<br />
e quin<strong>di</strong> risultare utile per la formazione <strong>di</strong> coenzimi contenenti<br />
NICOTINAMMIDE. Il processo prevede l'incorporazione dell'atomo <strong>di</strong> azoto in<br />
una molecola aromatica, le altre parti carboniose vengono eliminate. In ogni<br />
caso il livello <strong>di</strong> sintesi non è sufficiente a sod<strong>di</strong>sfare il fabbisogno del nostro<br />
organismo, è necessaria la assunzione della nicotinammide come tale.<br />
18