patologia generale II.pdf - AppuntiMed
patologia generale II.pdf - AppuntiMed
patologia generale II.pdf - AppuntiMed
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>patologia</strong> <strong>generale</strong> <strong>II</strong> semestre<br />
La Pompa cardiaca e la Pressione<br />
<br />
Equilibrio idrico ed Edema<br />
L’aldosterone è un ormone fondamentalmente ininfluente sulla [Na], in quanto il suo aumento (⇒ ritenzione<br />
Na) va di pari passo con la [ADH] ⇒ il Sodio è legato all’acqua.<br />
Nell’iperaldosteronismo secondario ad un tumore benigno secernente si ha quindi comunque una sodiemia<br />
normale, in quanto viene ristabilita dall’ADH, il che genera un’ipervolemia compensativa.<br />
A livello di scambi capillari l’equilibrio tra filtrazione (lato arterioso) e riassorbimento (venula) è dovuto<br />
alle pressioni osmotica ed idrostatica che vengono a stabilirsi tra interstizio e vasi: nel passaggio tra il lato<br />
arterioso e venoso quello che cambia veramente è la pressione idrostatica… essendo questa però determinata<br />
in larga parte dallo stato di contrattura delle arteriole oltre che dal VCE, a livello di scambi capillari non si<br />
hanno particolari ripercussioni. (secondo soranzo)<br />
ART MEDIA VENOSA<br />
PHYDR capillare +25 (+32) +17 +10 (=)<br />
PHYDR interstiziale +6,3 +6,3 +6,3<br />
PONC plasmatica -28 (-25) -28 -28 (-25)<br />
PONC interstiziale +5 +5 +5<br />
tot. ⇒ +8,3 +0,3 -6,7<br />
Nell’edema si ha proprio la filtrazione oltre la parete, nell’interstizio di liquidi circolanti, che non potrà essere<br />
determinato dal settore arterioso (dalla PHYDR arteriosa) ma dalla PHYDR venosa, che peserà veramente sul<br />
capillare: per quello lo scompenso cardiaco colpisce di più, da un punto di vista edematoso…<br />
1) idrostatico ⇒ centrale (cardiaco), trombi / insufficienze - venose…<br />
Nb: l’edema cardiaco sarà sistemico: potrà riguardare virtualmente ogni parte del corpo, quello dato<br />
dall’ostruzione di una vena p.es invece sarà altamente localizzato (solo una gamba..). Da tener presente che<br />
può succedere che si sovrapponga ad uno scompenso locale (ostruzione venosa) quello cardiaco: per la<br />
legge di laplace si ha quindi che una gamba appare leggermente, impercettibilmente gonfia, l’altra, che ha<br />
due motivi per esserlo, lo sarà tanto da attrarre lei sola l’attenzione… attenzione !<br />
2) ipoproteico ⇒ scompenso epatico, albuminuria… (PONC↓)<br />
3) tossico/infiammatorio ⇒ il passaggio di proteine del SI nell’interstizio determina un aumento della<br />
PONC interstiziale.<br />
4) linfatico ⇒ questo tipo di edema non presenta “fovea”: cioè premendo il dito non ne rimane<br />
l’impronta: “l’acqua non si lascia spingere in parte”. Per definizione infatti uno stop al<br />
deflusso linfatico non implica solo una riduzione del flusso liquido, ma essendo i linfatici<br />
fenestrati lasciano passare tranquillamente le proteine, lavandole dall’interstizio.<br />
Agenti sul Cuore<br />
• β bloccanti ⇒ gittata ↓<br />
§<br />
Farmaci per l’ipertensione<br />
• Ca 2+ antagonisti ad effetto cardiaco diretto: il calcio ha infatti un molteplice ruolo nella<br />
regolazione della PHYDR:<br />
1) vasocostrittore di per se<br />
2) ET-1: il suo meccanismo è calcio mediato ⇒ si riduce il suo effetto<br />
3) AT<strong>II</strong>: anch’essa utilizza il calcio<br />
• α bloccanti sono di dominio della fisio<strong>patologia</strong> clinica<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 1
Farmaci con effetto a lungo termine<br />
• sartani: interferiscono con i recettori per l’AT<strong>II</strong><br />
• ACE inibitori<br />
• aldactane: inibitore dell’aldosterone<br />
§<br />
Ipertensione<br />
1) I tipo (95%): renina ↑ ⇒ farmaci AB: ACE inibitori e Beta bloccanti…<br />
Può derivare da stress prolungato ( ⇒ ipertono simpatico)<br />
2) <strong>II</strong> tipo: Na + ↑ renina ↓ : l’aumento del sodio è la causa primaria<br />
a. iperaldosteronismo: la [Na] sarà normale (effetto a rimbalzo dell’ADH). Può anche essere<br />
secondario ad una insufficienza cardiaca ⇒ ⊕ RAAS<br />
b. patologie renali: glomerulo nefriti, nefropatie, malattia policistica…<br />
c. altro: dall’assunzione di ormoni esogeni, malattie tiroidee, problemi cardiovascolari<br />
(coartazione, rigidità aortica, vasculiti, aumento di gittata…)<br />
⇒ farmaci CD: Ca 2+ antagonisti, Diuretici + dieta iposodica (quasi inutile nel tipo I)<br />
§<br />
Regolazione dell’attività Cardiaca<br />
La portata cardiaca è di circa 5,5l/min, la regolazione della gittata cardiaca è sotto il controllo di:<br />
1. Frank Starling (cuore sano) ⇒ espelle sempre il volume ematico intero che gli arriva:<br />
tensione parete (T)↑ ⇒ forza contrattile ↑<br />
la gittata cardiaca dipende dal ritorno venoso, sotto controllo dell’attività periferica e dalla<br />
compliance. Dinamica dell’incremento:<br />
• vasodilatazione periferica<br />
• incremento di volume in arrivo dalla periferia ⇒ ritorno venoso ↑ ⇒ T ↑<br />
2. SNA: la noradrenalina agisce stimolando l’attività di contrazione cardiaca (α1, β1).<br />
La stimolazione simpatica dipende anche dal ritorno venoso:<br />
• tensione sulla parete dell'atrio destro<br />
• recettori pressorii carotidei<br />
3. Regolazione Periferica: la dilatazione periferica è fondamentalmente metabolismo dipendente e<br />
legata soprattutto al calo del pH (metabolismo ↑ ⇒ ossigeno necessario ↑).<br />
Questo può avvenire in molte condizioni diverse, patologiche o meno:<br />
- sforzo fisico<br />
- ipertiroidismo: azione disaccoppiante ⇒ non viene prodotto ATP:<br />
medesimo effetto di un calo del flusso di ossigeno<br />
- anemia: flusso di ossigeno periferico↓<br />
- beriberi: avitaminosi B1 (tiamina) che migliora l'utilizzo di nutrienti<br />
- shunt: si tratta di una comunicazione patologica tra strutture venose e<br />
arteriose per cui si ha un netto incremento del ritorno di<br />
sangue al cuore. Pazienti soggetti a questo tipo di <strong>patologia</strong><br />
hanno un sovraccarico di ritorno di sangue al cuore.<br />
» pervietà del dotto di Botallo, che genera una<br />
comunicazione tra il sangue arterioso della<br />
aorta e quello della arteria polmonare<br />
• flusso al circolo polmonare ↑ (smaltito)<br />
• flusso di sangue nel cuore sinistro ↑ ⇒ gittata ↑<br />
» fistola arterovenosa<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 2
§<br />
Insufficienza Cardiaca (o ICC)<br />
1) scompenso cardiaco o insufficienza cardiaca congestizia (ICC): si definisce scompenso una<br />
situazione in cui il cuore non riesca a far fronte alle necessità dell'organismo:<br />
non riesce ad espellere tutto il sangue che gli arriva, cioè a trasformare il ritorno<br />
venoso in gittata: da Starling, passa a LaPlace.<br />
2) insufficienza cardiaca è il termine con cui si indicano tutte le deficienze e le patologie del cuore;<br />
a. compensata<br />
b. scompensata ⇒ scompenso cardiaco<br />
L'insufficienza cardiaca provoca un incremento della pressione venosa a monte della pompa cardiaca,<br />
tale incremento di pressione genera spesso degli edemi a livello soprattutto degli arti inferiori.<br />
Riserva Cardiaca<br />
La differenza fondamentale rispetto alla prestazione di un cuore, è legata a quella che viene definita riserva<br />
cardiaca, un individuo con una <strong>patologia</strong> cardiaca (come anche un infarto) potrà presentare quindi…<br />
riduzione della riserva = insufficienze cardiache<br />
incapacità di rispondere alle necessità dell'organismo = scompensi cardiaci<br />
Cause di insufficienza Cardiaca<br />
Possiamo dire fondamentalmente che le cause di una insufficienza cardiaca possono essere:<br />
1) Alterazioni del Muscolo<br />
Primitive<br />
Secondarie<br />
2) Difetti di Riempimento<br />
a. miocarditi: infiammazioni o infezioni del miocardio (tipica dei coxsaeckie B)<br />
b. miocardiopatie come quella tossica alcolica, relativamente frequente<br />
c. aritmie: lo scompenso cardiaco può provocare l'insorgenza di aritmie, le aritmie<br />
possono essere alla base dello scompenso… tachicardie parossistiche<br />
spesso instabili, possono generare questo tipo di problemi in quanto riduce la<br />
funzionalità del cuore.<br />
a. insufficienza coronarica: riduce la prestazione cardiaca<br />
b. infarto: riduce la funzionalità cardiaca<br />
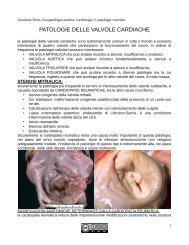
Patologie Valvolari<br />
a. stenosi mitralica: può essere causata da infiammazione della valvola per cause<br />
batteriche (streptococchi) o di altra natura, porta alla formazione<br />
di lesioni cicatriziali a livello della valvola stessa, tali lesioni<br />
provocano una stenosi valvolare che non fa passare il sangue.<br />
Calo del VCE, come nel caso di emorragie.<br />
Tamponamento Cardiaco: il cuore, costretto, non si dilata adeguatamente:<br />
a. foro di proiettile: (p.es) provoca comunicazione tra le cavità cardiache e il pericardio,<br />
causandone il riempimento di sangue: il pericardio, rigonfio, resiste<br />
alla attività cardiaca e provoca una mancata dilatazione<br />
b. pericardite: può incrementare la produzione di fluidi a livello pericardico, ed una<br />
successiva cicatrizzazione e calcificazione delle strutture pericardiche:<br />
porta alla formazione del “cuore a corazza”<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 3
3) Sovraccarico Cardiaco<br />
Pressorio (Sistolico): il cuore deve incrementare la attività di sistole e la pressione in uscita:<br />
a. PMEDIA arteriosa ↑ ⇒ livello pressorio generato dal ventricolo sinistro ↑↑<br />
b. PPOLMONARE ↑ : soprattutto in relazione a patologie di natura infiammatoria o infettiva<br />
del polmone che provoca ipertensione polmonare<br />
c. stenosi della valvola aortica: la stenosi della valvola aortica incrementa la attività<br />
pressoria del cuore per vincere la resistenza.<br />
Volumetrico o Diastolico: incremento patologico del sangue in arrivo al cuore<br />
a. insufficienze valvolari:<br />
- mitralica ⇒ reflusso nell’atrio durante la sistole. Il sangue atriale quindi, si<br />
assomma a quello in arrivo dai polmoni<br />
- aortica ⇒ reflusso dall’aorta, con l'effetto Windkessel , nel ventricolo<br />
b. shunt: fistoli, pervietà del dotto ed altre comunicazioni ateriovenose patologiche che<br />
portano ad un incremento del carico cardiaco: la fistolazione avviene<br />
soprattutto a livello femorale.<br />
Aumento della Richiesta: sovraccarico diastolico legato per esempio a:<br />
a. sforzo fisico<br />
La forza che distende il cuore è:<br />
b. febbre: il nostro metabolismo è temperatura dipendente, e sono +7 BPM / 1°C ↑<br />
tutto dipende dal centro termoregolatore ipotalamico influenzato dalla IL1.<br />
l'aumento della temperatura provoca:<br />
- orripilazione<br />
- vasocostrizione periferica: non permette la dispersione del calore: il SNA<br />
simpatico va ad agire quindi<br />
contemporaneamente a questo livello e sul cuore.<br />
- disaccoppiamento<br />
§<br />
Insufficienza Cardiaca e Laplace<br />
• proporzionale al raggio della struttura, “r”<br />
• inversamente proporzionale allo spessore della parete “h”<br />
Il sovraccarico sistolico o volumetrico è legato ad un incremento della tensione legata alla legge di Laplace:<br />
Sovraccarico Pressorio o Sistolico o Post Carico<br />
Caratteristico, come accennato, di un incremento della PAORTICA:<br />
- r ↓<br />
- h↑ in particolare l’aumento di spessore è a carico della parete interna: l’ipertrofia<br />
permette un aumento d’attività.<br />
T =<br />
Il sovraccarico sistolico è relativamente facile da gestire per il cuore…<br />
Sovraccarico Volumetrico o Diastolico o Pre-Carico<br />
Nel caso del sovraccarico volumetrico, il cuore reagisce in questo modo:<br />
- r ↑↑<br />
- distensione ↑<br />
- h ↑ non certo paragonabile alla ipertrofia concentrica: si parla di<br />
ipertrofia eccentrica, di piccolissima entità. Prelude ad uno<br />
scompenso.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 4<br />
P r<br />
2h
In questo caso la tensione gioca un ruolo fondamentale, da essa infatti dipendono:<br />
1) forza di contrazione<br />
2) ipertrofia: l'incremento di spessore della parete cardiaca è dovuta all’incremento di cAMP<br />
adrenalina dipendente, che porta ad una intensa sintesi proteica.<br />
3) consumo d’ossigeno: l'incremento della tensione porta ad un incremento del consumo, spesso in<br />
combinazione con l'incremento della frequenza.<br />
Nello sforzo fisico spesso è l'apporto di ossigeno che viene meno.<br />
§<br />
Conseguenze dello Scompenso Cardiaco<br />
a. Scompenso Anterogrado: calo della gittata ⇒ meno sangue alla periferia<br />
b. Scompenso Retrogrado: PVENOSA↑ ⇒ ristagno sanguigno a monte del cuore<br />
Si tratta di definizioni accademiche, in quanto entrambe le forme si presentano contemporaneamente.<br />
Differenze Nei 2 Tipi di Cuore<br />
I due tipi di cuore sono generalmente separati da questo punto di vista:<br />
scompenso sinistro<br />
• polmone: la pressione a livello venoso aumenta, fino a ritrasmettersi a tutto il circolo,<br />
causando appunto congestione ed edema sia a livello interstiziale che alveolare.<br />
In questa sede sono osservabili i siderofagi: macrofagi che fagocitano proteine leganti il ferro<br />
(Hb p.es), convertendola in emosiderina la cui presenza testimonia precedenti episodi<br />
edematosi<br />
» dispnea<br />
» ortopnea (va in affanno se posto in ortostatismo)<br />
» dispnea parossistica notturna (attacchi di ortopnea estrema che arrivano quasi al soffocamento,<br />
svegliando il paziente durante la notte)<br />
• reni: RAAS vs ANP<br />
• cervello: l’encefalopatia ipossica può generare di icc molto avanzate.<br />
scompenso destro (cuore polmonare):<br />
• sindrome congestizia venosa sistemica (del sistema portale: epatomegalia, splenomegalia)<br />
• edemi periferici (soprattutto delle parti inferiori del corpo: pretibiale, delle caviglie…)<br />
• sierose: versamenti pleurici, ascite<br />
Nb: mentre nell’ICC destra si ha edema polmonare, nella sinistra è tipico il versamento pleurico.<br />
In genere comunque l’ICC va ad essere bi ventricolare, dando entrambe le tipologie di sintomi.<br />
Insufficienza Cardiaca Compensata<br />
La <strong>patologia</strong> cardiaca può essere compensata in modo ottimale sia dalla terapia sia da fattori di tipo<br />
comportamentale. Un segno consente di identificare una insufficienza cardiaca compensata:<br />
1) PATRIALE↑ a riposo: anche se il ristagno non si riflette sulle strutture periferiche, l'atrio si dilata e<br />
incrementa la sua pressione interna.<br />
2) Riserva Cardiaca ↓ sotto sforzo:<br />
a. tachicardia<br />
b. pallore e sudorazione } di dipendenza simpatica<br />
c. dispnea: per insufficiente irrorazione cerebrale<br />
Ipervolemia e Scompenso Cardiaco<br />
Il calo della portata e della gittata cardiaca genera una razione a livello renale:<br />
PARTERIOSA ↓ ⇒ filtrazione ↓<br />
⊕ RAAAS: Renin Angiotensin ADH Aldosterone System<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 5
⇒ VCE ↑, si ha ipervolemia:<br />
Terapia dello Scompenso<br />
• moderata ⇒ ritorno venoso ↑ ⇒ gittata / attività cardiaca ↑ (Starling… fatto positivo)<br />
• grave: peggioramento della situazione:<br />
⇒ dilatazione cardiaca<br />
⇒ scompenso diastolico sinistro: provoca congestione polmonare:<br />
- deossigenazione del sangue<br />
- edema polmonare<br />
⇒ scompenso diastolico destro:<br />
- edemi periferici<br />
1) Diuretici:<br />
a. VCE ↓<br />
b. pre carico ↓<br />
c. consumo O2 ↓<br />
2) Anti Ipertensivi (ACE inibitori p.es)<br />
a. PARTERIOSA ↓<br />
b. Post carico ↓<br />
c. consumo O2 ↓<br />
3) Farmaci Digitalici (lanoxin p.es)<br />
a. contrattilità ↑<br />
parziale blocco Na + /K + ATPasi ⇒ Na + ↑ ⇒ inversione antiporto Na + /Ca 2+ ⇒ Na + ↓ Ca 2+ ↑<br />
b. post carico diastolico↓<br />
infatti: frazione di eiezione↑ ⇒ meno sangue nelle camere cardiache: il sangue in arrivo<br />
infatti trova la camera vuota<br />
c. tensione ↓<br />
d. consumo O2↓<br />
4) Nitroglicerina e derivati: tipicamente si dava a chi aveva problemi di angina.<br />
(p.es Carvasin sublinguareo, Trininina…)<br />
a. post carico↓ dato dalla vasodilatazione arteriosa<br />
b. pre carico↓ dato dalla contrazione delle vene cave: meno sangue al cuore<br />
⇒ cuore meno impegnato, cala la tensione, il consumo di O2.<br />
Dal punto di vista farmacologico si possono utilizzare dei cerotti che inviano nel sangue quantità<br />
continue di farmaco nel corso delle 24 ore.<br />
Nb: i βbloccanti non devono essere normalmente utilizzati nella gestione dello scompenso cardiaco: sono<br />
inibitori della attività simpatica, avrebbero l'effetto quindi di ridurre l’inotropismo<br />
⇒ Tensione↑ consumo O2↑ §<br />
Il Remodeling Cardiaco<br />
Anche se la giustificazione per una tendenza allo scompenso cardiaco, legata ad una ic compensata, come<br />
gravità resta sempre uguale, il paziente va incontro ad un deterioramento della popolazione cellulare<br />
cardiaca, di conseguenza anche una ipertrofia concentrica, con il tempo e con il deterioramento, diviene una<br />
cardiomiopatia dilatativa. La perdita delle cellule provoca:<br />
• calo dell’attività contrattile<br />
• calo dello spessore della parete (h)<br />
Diversi approcci terapeutici possono intervenire nel controllo di questa condizione…<br />
Una <strong>patologia</strong> cronica del cuore provoca generalmente quello che viene definito Hearth Remodeling:<br />
ipertrofia patologica delle cellule del miocardio<br />
⊕ attività apoptotica<br />
che alla lunga provocano l'insufficienza cardiaca;<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 6
ipertrofia patologica<br />
A seguito ovviamente di uno stimolo di tipo growth, una cellula del miocardio può:<br />
a. andare in contro ad apoptosi<br />
b. disorganizzare le strutture sarcomeriche<br />
c. andare incontro ad ipertrofia, che lungi dall’essere quella di tipo fisiologico ed<br />
equilibrata dell’atleta, è patologica:<br />
Ipertrofia Concentrica o da Sovraccarico Pressorio: le fibre..<br />
- si accorciano e sono tozze, in parallelo<br />
» lume ventricolare↓<br />
» δ capillare ↓<br />
» espressione di proteine fetali (meno efficaci)<br />
» tensione↑, consumo di O2 ↑<br />
Ipertrofia Eccentrica o da Sovraccarico di Volume:le fibre presentano..<br />
- morfologia molto allungata e poco spessa<br />
- disposizione in serie, con incremento del raggio<br />
Inoltre, da un punto di vista molecolare queste cellule esprimerebbero geni embrionali:<br />
• miosina embrionale, meno sensibile agli stimoli<br />
• PAN (Peptide Natriuretico Atriale): si sta pensando di utilizzarlo a livello diagnostico;<br />
sappiamo che la sua utilità a livello di decremento di VCE si perde nella<br />
cronicità (il rene diventa insensibile..)<br />
Dal punto di vista macroscopico inoltre il cuore perde la sua forma ovalare e le camere divengono circolari.<br />
Fattori Biochimici del Remodeling<br />
Il remodeling patologico del cuore è legato non solo al fattore fisico idrodinamico, ma anche ad un fattori<br />
biochimici significativi come l’IL-6<br />
stimola l’apoptosi<br />
riorganizza (negativamente) i sarcomeri<br />
⊕ espressione geni embrionali (⇒ proteine meno funzionali o alterate nell’ipertrofia p.es)<br />
Si è scoperto che il remodeling, più che allo stress pressorio sarebbe collegato a fattori biochimici indotti dallo<br />
stress patologico, quali:<br />
• E, NE<br />
• Endotelina<br />
• Istamina<br />
• GH<br />
• Mediatori dell’infiammazione<br />
- LPS<br />
- TNF<br />
- IL-1 }<br />
prodotti autocrinamente dalle cellule miocardiche in fase<br />
di trasformazione e promuoventi l’apoptosi.<br />
Queste ipotesi sono confermate dall’effetto di βbloccanti ed ACEinibitori, in grado si aumentare l’aspettativa<br />
di vita anche in pazienti non ipertesi (ragion per cui vengono comunque somministrati)…<br />
Alterazione dell’azione della NE<br />
recettori β2 ⇒ cAMP ↑ ⇒ ⊕ PKA ⇒ fosfolambano ↑ ⇒ apertura canali Ca 2+ (reticolo sarcoplasmatico)<br />
⇒ effetto inotropo positivo<br />
Nel cuore scompensato cronico si produce una “β adrenergic receptor kinase”, inattivante, che alla lunga<br />
desensibilizza dall’azione noradrenergica…<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 7
farmacologica<br />
si basa prevalentemente:<br />
chirurgica<br />
§<br />
Terapia Tradizionale<br />
nello scompenso cardiaco su diuretici<br />
nella prevenzione della alterazione biochimica della struttura cardiaca su:<br />
a. ACE inibitori<br />
b. βbloccanti: è un’eccezione attuabile o in soggetti giovani o se compensati dal<br />
resto della terapia. Si tratta comunque di β bloccanti particolari<br />
Spesso si rimuove parte della struttura cardiaca onde decrementare l'effetto della ipertrofia.<br />
terapia dell’ischemia cardiaca<br />
• derivati della nitroglicerina<br />
• βbloccanti: sono la prima scelta in caso di ischemia:<br />
- tachicardia<br />
- forza contrattile ↓<br />
- contrazione venosa ↓<br />
- PARTERIOSA ↓<br />
- aritmie<br />
⇒ si riduce il consumo di O2<br />
• trombo litici<br />
• angioplastica<br />
§<br />
Rigenerazione e Cellule Staminali<br />
Fino a qualche anno fa si era convinti che il cuore non fosse in grado di rigenerare: si distinguevano appunto<br />
tessuti labili (tessuti epiteliali, sangue), stabili (muscolo, fegato..) e perenni (miocardio, cervello…).<br />
Quelli labili sono tipicamente più soggetti all’azione di farmaci antiblastici. Questo principio è stato<br />
recentemente contraddetto da numerose osservazioni nel corso degli ultimi 10 anni:<br />
• presenza di attività mitotica, oltre alla proliferazione del tessuto cicatriziale (fibroso): in particolare<br />
queste cellule miocardiche con aspetto mitotico si noterebbero nei confini tra miocardio ancora vivo<br />
e tessuto cicatriziale di riparazione. Questo già si sapeva, ma si pensava riguardasse fenomeni legati<br />
ad ipertrofia con fusione di più cellule (da non confondere con l’iperplasia, la generazione di nuovi<br />
elementi cellulari, appunto).<br />
La cosa fondamentale che si nota è che un po’ come nel tessuto nervoso per opera della microglia,<br />
la deposizione del collagene (cicatrizzazione) porta al blocco dell’attività rigenerativa del<br />
tessuto. Già da un po’ di anni si è approfondita una ricerca in grado di bloccare questa<br />
cicatrizzazione con un incredibile miglioramento degli esiti dei traumi spinali.<br />
• attività apoptotica spontanea: si nota in campioni di tessuto: nel giro di una vita porterebbe alla<br />
scomparsa di tutto il tessuto, vista la frequenza… il fatto che ciò non avvenga è sintomo di<br />
un’attività mitotica rigenerativa<br />
• microscopia: si sono ottenute immagini con chiari fenomeni di cariocinesi e di mitosi, con nuclei e<br />
cellule in divisione.<br />
chr. metafasici cariocinesi citochinesi<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 8
La domanda che quindi ci si è posti e se queste cellule staminali legate alla rigenerazione fossero di origine<br />
miocardica o esogena: si sono stabiliti tre markers di cellule staminali (blu= nucleo, verde=makers)<br />
C-kit (foto a) ⇒ quello che si nota in particolare nella foto con questo marker<br />
è l’attiva mitosi in corso. Si noti tralaltro che le suddette cellule non<br />
contengono ancora fibre actomiosiniche: non sono ancora elementi<br />
contrattili attivi.<br />
MDR-1 (Multi Drug Resistance: foto b)<br />
SCA-1 (foto c)<br />
Nb: questi markers, presi singolarmente non sono gran che informativi, ma se presenti<br />
tutti assieme sono segno di “staminalità”.<br />
Staminali Circolanti<br />
Quindi in risposta a questo quesito, la teoria attuale è che ci siano cellule staminali di origine midollare in<br />
forma normalmente circolante (1-2%) che sarebbero richiamate dall’infiammazione.<br />
Sembrerebbero di una qualche efficacia interventi che prevedano l’iniezione nella zona infartuata di campioni<br />
cellulari di origine midollare. Si è provato anche a distinguere il materiale di matrice non leucocitaria dal resto<br />
della popolazione cellulare per poi effettuare l’iniezione, ma questo è sembrato avere minor efficacia,<br />
probabilmente per via delle citochine che verrebbero prodotte dalle cellule midollari, in grado di potenziare<br />
l’azione rigenerante.<br />
Staminali a livello cerebrale<br />
Ricordiamo la presenza accertata anche nel cervello, in particolare nella zona sub ventricolare (SVZ),<br />
nell’ippocampo nel bulbo olfattivo e nelle leptomeningi di cellule staminali in grado di differenziarsi in<br />
praticamente ogni direzione…<br />
Staminali Embrionali<br />
Sappiamo che a livello embrionale si trovano appunto cellule staminali, come anche a livello del cordone<br />
ombelicale (da cui l’ipotesi di criogenare queste cellule con l’ipotesi di possibilità curative per il futuro).<br />
Nel tentativo e nell’ideazione dell’utilizzo di queste cellule però sono emersi grossi problemi:<br />
a. morali: uccidere un embrione per salvare un altro individuo ?<br />
(non nel caso degli annessi placentari evidentemente)<br />
b. pratici di elaborazione delle cellule… questo coinvolge grandemente<br />
le multinazionali che spingerebbero verso mete lucrative<br />
c. antigenici / neoplastici: si è notato nell’ambito di alcuni trials come<br />
queste cellule possano sfuggire facilmente dal controllo generando<br />
tumori maligni anche piuttosto aggressivi.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 9
Patologia del Metabolismo Cellulare<br />
In quest’ambito va forte l’ipotesi di terapia genica, si tratta infatti spesso di difetti genici che portano a<br />
difetti ereditari legati alla mancanza di attività enzimatica.<br />
Questo può derivare da alterazioni o mal funzionamenti oltre che dall’assenza: antigenicamente quindi<br />
magari l’enzima si trova pure, ma c’è comunque il problema:<br />
1) accumulo di substrato a monte<br />
a. sostanze idrosolubili (il prodotto viene escreto p.es con le urine)<br />
galattosuria: malattia infantile (1:60'000) piuttosto rara caratterizzata dall’incapacità<br />
di elaborazione del galattosio tramite l’enzima GLAT (Gal-1-Puridiltrasferasi).<br />
Si ha quindi<br />
• accumulo di Gal1P, che ha proprietà tossiche (vomito, inappetenza, diarrea).<br />
• galattosemia dopo le poppate ↑<br />
• ↓ liberazione di glucosio da parte del fegato ⇒ ipoglicemia e convulsioni<br />
(cioè tremori tonico clonici).<br />
• ↑ attività aldoso reduttasica nel cristallino (via alternativa) ⇒ cataratta<br />
intolleranza al Lattosio nell’adulto: si ha un deficit di lattasi (disaccarasi) a livello<br />
dell’orletto a spazzola…Si ha ovviamente<br />
quindi accumulo dello zucchero:<br />
• mal assorbimento dello stesso<br />
• fermentazione ⇒ pH ↓ ⇒ irritazione / motilità intestinale<br />
b. sostanze insolubili (si ha precipitazione della sostanza)<br />
gotta: deposizione di sali di urati a livello articolare: si risolve in breve tempo<br />
c. accumulo in ambiente lipidico<br />
UDPG trasferasi deficienza: bilirubinemia indiretta nei nuclei della base. Infatti la<br />
bilirubina viene normalmente resa solubile nel fegato tramite<br />
glucuronazione. Soprattutto nei neonati, che non hanno ancora<br />
la BBB completamente sviluppata quindi la bilirubina può<br />
giungere a livello cerebrale depositandosi in questa sede.<br />
d. da accumulo, lisosomiali<br />
tesaurismosi lisosomiali ereditarie: sono malattie piuttosto gravi, ereditarie.<br />
In queste dinamiche si ha un rigonfiarsi dei lisosomi che non<br />
smaltiscono i substrati, che diventano materiale indigeribile;<br />
Questo può portare a patologie diverse, dipendentemente dalla<br />
sede di accumulo (come i gangliosidi nel SNC) o della<br />
specifiche cellule in cui avviene (macrofagi p.es).<br />
Patogenesi possibili:<br />
• modificazioni post trascrizionali: come l’aggiunta di M6P (mannosio 6P),<br />
utile a legare sulla membrana che formerà le<br />
vescicole di Golgi poi dirette ai lisosomi, gli<br />
enzimi idrolasici grazie al recettore<br />
specifico.<br />
• enzimi inattivi: p.es se si inserisce un codone di stop all’interno della sequenza<br />
dell’enzima, in un punto tale da inattivarlo<br />
• mancanza di attivatori enzimatici: sia dell’enzima che del substrato<br />
• proteine di trasporto: possono mancare quelle che trasportano i prodotti<br />
digeriti all’esterno del lisosoma.<br />
2) riduzione del prodotto<br />
3) attivazione di vie metaboliche alternative<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 10
esempi di tesaurismosi ereditarie<br />
a. glicogenosi 1 : accumulo di glicogeno, viene detto anche morbo di pompe: l’accumulo avviene a<br />
livello cardiaco, muscolare scheletrico, ed epatico.<br />
b. sfingolipidosi: accumulo di glicolipidi<br />
- m. di Gaucher: deficienza di glucocerebrosidasi: macrofaci nel sistema<br />
reticolo endoteliale, da cui l’epatosplenomegalia<br />
- m. Niemann Pick: macrofagi “schiumosi”. Carenza di sfingomielinasi.<br />
- m. di Tay Sachs: è una gangliosidasi; la più grave, in quanto determina<br />
ritardo mentale.<br />
c. tesaurismosi di trigliceridi<br />
- m. di Wolman: si ha steatosi epatica primitiva, in quanto manca l’enzima per<br />
scindere i trigliceridi (i legami tra glicerolo ed acidi grassi).<br />
Questa steatosi epatica primitiva è molto meno importante<br />
delle secondarie 2 , molto più comuni, e quindi non è<br />
importante da imparare.<br />
d. mucolipidosi: di complessi proteo-lipidici. Si avranno depositi sempre a livello di SNC e fegato<br />
e. mucopolisaccaridosi (GAG, ac.jaluronico, condroitin / dermatan / eparan - solfato)<br />
- m. di Hurler: manca la jaluronidasi;<br />
- m. di San Filippo: è una malattia ereditaria che provoca accumuli a livello di<br />
SNC a causa della mancanza di numerosi enzimi.<br />
f. accumulo di metalli:<br />
- malattia di Wilson: accumulo di rame (Cu 2+ , raro) a livello epatico e poi<br />
circolatorio: normalmente infatti il rame viene coniugato con una metallo proteina<br />
nel fegato ed espulso con la bile.<br />
- emocromatosi: accumulo di Fe 2+<br />
Omocistenuria ed Arterosclerosi<br />
L’omocistenuria si ha quando i livelli plasmatici di omocisteina impennano, il che è un risk factor accertato<br />
per sviluppo precoce di quadri di <strong>patologia</strong> vascolare (arterosclerosi) e tumori: l’effetto tumorale può<br />
derivare dalla metilazione del DNA: un gene metilato perde funzionalità. Difetti di metilazione possono<br />
essere correlati ad aumento rischio di <strong>patologia</strong> neoplastica maligna. Studi epidemiologici hanno<br />
dimostrato una relazione più <strong>generale</strong> tra livelli sierici totali di omocisteina ed arteropatia coronarica, le<br />
arteropatie periferiche, l’ictus e la trombosi venosa. Queste situazioni possono generarsi a partire deficit quali:<br />
cistationina β sintasi<br />
L’omocisteina è di fatto un perossidante, motivo per<br />
cui è associata puntualmente ad arterosclerosi.<br />
Normalmente viene smaltita (↑) generando o cisteina<br />
o Glutatione (GSH), in grado di smaltire l’acqua<br />
ossigenata andando in contro ad ossidazione (⇒<br />
GSHSG), per venir rigenerato poi nel ciclo dei<br />
pentosi. Il GSH è il principale elemento protettivo<br />
contro la perossidazione (la perossidasi infatti è<br />
molto più lenta).<br />
Nell’omocistenuria si ha la mancanza di cistationina β sintetasi: è una <strong>patologia</strong> pediatrica gravissima<br />
con formazione di trombi e ritardo mentale. L’iperomocisteinemia può rilevarsi in eterozigosi, sarà<br />
meno grave, ma comunque incrementerà il rischio di malattia aterosclerotica.<br />
MTHFR (MeTil Hydro Folate Reductase)<br />
Rappresenta un altro metodo di smaltimento dell’omocisteina che sfrutta l’acido folico, generando<br />
tetraidrofolato e metionina. Quest’azione è dipendente dalla vit.B12, cui carenze possono avere gli stessi<br />
effetti di aumento di rischio arterosclerotico e tumorale.<br />
1<br />
nella malattia di Van Gierke l’accumulo avviene a livello citoplasmatico, e non è quindi una tesaurismosi.<br />
L’accumulo non avviene a livello cardiaco, in questo caso.<br />
2<br />
si tratta di tesaurismosi lipidiche - steatosi <strong>II</strong>arie, sono dette iperlipidemie secondarie: piuttosto comuni<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 11
§<br />
Steatosi<br />
Si tratta di un accumulo di liposomi, più tipicamente a livello epatico. E’ una <strong>patologia</strong> completamente<br />
reversibile, anche se la possibilità di evoluzione cirrotica o cancerosa c’è sempre. Questo può avvenire oltre<br />
che a livello epatico anche in<br />
- rene (nei tubuli)<br />
- cuore: soprattutto in caso di anemizzazioni croniche (talassemie…) che<br />
portano a tipiche bande di steatosi. Anche la difterite inibisce il<br />
metabolismo della CAT.<br />
Un preparato steatoso presenta goccioline translucide (di origine lipidica) che occupano gran parte del volume<br />
cellulare: sono proprio i trigliceridi. In ematossilina-eosina si individuano infatti spazi otticamente vuoti, per<br />
essere sicuri si può eseguire una colorazione con colorante Sudan IV, specifico per i trigliceridi.<br />
I grassi derivano dalla dieta (chilomicroni per via linfatica) e dai tessuti periferici, dove gli a.grassi possono<br />
essere trasportati come tali (NEFA) dall’albumina (che rappresenta a livello <strong>generale</strong> un trasportatore per<br />
sostanze non idrosolubili). Una volta che i grassi giungono al fegato (ignora la proteina Z), vanno a costituire<br />
un pool citoplasmatico di NEFA, che può essere diversamente indirizzato:<br />
1) fosfolipidi di membrana: coniugandosi col colesterolo<br />
2) substrato energetico: grazie all’enzima CAT, a livello mitocondriale<br />
3) VLDL: coniugandosi col glicerolo formano i trigliceridi, che entrano nel sistema reticolo<br />
endoplasmico, divenendo una componente delle lipoproteine. Per formare questo tipo di<br />
sostanze servono le apolipoprotiene, che per essere prodotte necessitano di energia: per la<br />
sintesi proteica in particolare serve GTP, prodotto sempre a partire da ATP. Quindi tramite un<br />
passaggio nel golgi le vescicole porteranno all’esocitosi di VLDL, tipicamente di produzione<br />
epatica.<br />
Eziopatogenesi<br />
Cause extraepatiche:<br />
- Apporto di FFA (Free Fatty Acids) ↑<br />
a. diabete<br />
b. terapia cortisonica: provoca un rilascio di acidi grassi periferici<br />
- Carenze proteiche: impossibile sintetizzare lipoproteine. Questo è vero in ogni caso di<br />
denutrizione (anche nell’anoressia p.es)<br />
a. digiuno<br />
b. Kwashiorkor: causata principalmente nei bambini nei paesi del terzo mondo dalla<br />
denutrizione, la mancanza di proteine in particolare, anche in presenza di<br />
una dieta ricca di grassi e carboidrati. Si accompagna ad edema, addome<br />
disteso, epatomegalia…<br />
c. colite ulcerosa: malattia particolarmente debilitante, con transito intestinale molto<br />
accelerato (diarree…), che provocherà comunque denutrizione<br />
d. danno epatico: nell’alcoolismo o l’ipossia<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 12
Cause Epatiche<br />
- fosforilazione ossidativa ↓ ⇒ ATP↓<br />
motivo per cui mi aspetto una steatosi anche nell’ipertiroidismo, che essendo disaccoppiante riduce l’ATP<br />
- β ossidazione ↓<br />
Anche in caso di carenze di ossigeno, carenza di enzima CAT…<br />
- riduzione di sintesi proteica (LDL, VLDL…) o di fosfolipidi<br />
Possono derivare anche da alterazioni del RE, dell’App. di Golgi<br />
Tipi di Steatosi<br />
1) Da ipossia o da Stasi: p.es nell’insufficienza retrograda o destra, che provoca appunto congestione<br />
venosa a livello portale (epatosplenomegalia).<br />
Si può sommare, a questo quadro, anche l’anemia. Ovviamente il tutto si riduce<br />
alla mancanza di ATP e alla mancanza di βossidazione.<br />
fegato a noce moscata: istologicamente si notano processi di degenerazione a<br />
livello lobulare; Avendo ben presente la struttura del lobulo epatico, quello che<br />
succede è che il sangue arterioso arriva dalla periferia verso il centro:<br />
⇒ periferia conservata: il sangue il suo ossigeno ce l’ha, ed è appena uscito dall’arteria<br />
⇒ centro necrotico: lo scorrere lento del sangue a causa del mancato deflusso, fa si<br />
che al centro (lontano delle arteriole) il sangue sia completamente<br />
privo di ossigeno. Si notano quindi anche stravasi emorragici.<br />
⇒ mediamente (tra le cellule necrotiche e normali) si porranno le cellule steatosiche,<br />
abbastanza ipossiche da non essere normali, ma non abbastanza da<br />
morire (necrosi).<br />
2) Diabetica: se ne fa solo un cenno… (il diabete si farà in sede separata). Quello che c’è da ricordare è<br />
che la chetogenesi originata dal glucagone provoca l’attivazione della CAT<br />
⊕CAT ⇒ ⊕ βossidazione ⇒ accumulo acidi grassi ⇒ steatosi<br />
3) Da Iponutrizione:<br />
associazione all’alcolismo: si ha spesso associazione con la gastrite, che provoca<br />
insofferenza e nausea per i cibi carnei (il che può succedere anche alle incinte).<br />
Quindi l’alcolista non mangia normalmente carne; il problema energetico non si<br />
pone, ma quello dell’apporto proteico, si.<br />
4) Da Alcool: l’etanolo viene ossidato da un’alcool DH che forma acetaldeide, sua volta rielaborata ad<br />
acido acetico + CoA ⇒ ACoA.<br />
⇒ glicerolo ↑<br />
⇒ NADPH2 ↑<br />
⇒ ACoA ↑<br />
L’acetaldeide è epatotossica:<br />
⇒ sintesi Trigliceridi ↑<br />
sintesi proteica (LDL, VLDL↓)<br />
altera i mitocondri ⇒ ossidazione A.Grassi mitocondriale ↓<br />
⇒ steatosi<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 13
Ricordiamo la presenza del sistema MEOS (Microsomial Ethanol Oxidigin Systen), che è (punto<br />
fondamentale) inducibile ⇒ chi è abituato a bere ha un maggior potere di elaborazione dell’alcool.<br />
Questo sistema ha anche altre funzioni biochimiche, per esempio smaltisce i farmaci, che verranno<br />
metabolizzati ed eliminati molto più velocemente in chi è abituato a bere;<br />
⇒#1 farmaci assunti contemporaneamente all’alcool sono smaltiti molto più lentamente, in<br />
quanto vanno ad impegnare il MEOS doppiamente.<br />
⇒#2 cancerogeni chimici (il fumo di sigaretta per primo) siano tali solo se attivati (sono<br />
tecnicamente dei precancerogeni). Questa attivazione avviene spessissimo ad opera del<br />
MEOS epatico; In soggetti con MEOS indotto (bevitori p.es), si avrà una più efficace<br />
attivazione dei precancerogeni ed un maggior effetto mutagenico. Questo è<br />
particolarmente vero per il fumo di sigaretta, dove nel polmone è comprovata la presenza<br />
di un efficace sistema MEOS. Individui con sistema MEOS polmonare geneticamente<br />
poco sviluppato sono meno suscettibili all’azione cancerogena. Ricordiamo che le<br />
xantine (tipicamente contenute nel caffè) riducono l’attività del MEOS, con un effetto<br />
protettivo.<br />
Cirrosi Epatica (cenno)<br />
Si tratta della sostituzione del parenchima epatico con materiale cicatriziale, che può essere una naturale<br />
evoluzione di una steatosi epatica alcolica. Si nota il formarsi di pseudo lobuli: il fegato appare<br />
sepimentato in maniera irregolare (particolarmente evidente con colorazione Hazan Mallory).<br />
La Cirrosi si realizza in un processo di sclerosi, di cicatrizzazione: nella quasi totalità dei casi si tratta di<br />
• alcolismo<br />
• epatite virale<br />
• epatite biliare: evento molto raro (
Ricordiamo che nella sintesi del colesterolo è implicato anche questo elemento che viene a formarsi<br />
dall’OH metil Glutaril CoA (HMG-CoA), attraverso la sua reduttasi.<br />
Siccome questo è un intermezzo nella produzione di colesterolo, farmaci quali le statine sono quelli<br />
attualmente più utilizzati per l’ipercolesterolemia grazie al loro potere di bloccare la HMG-CoA reduttasi.<br />
Dato che altri metaboliti intermedi hanno un ruolo nell’infiammazione, le statine avrebbero come effetto<br />
collaterale, specialmente date con dosi piuttosto elevate, quello di ridurre anche l’infiammazione, attaccando<br />
doppiamente i processi arteriosclerotici (che sappiamo avere una base infiammatoria). Tutto questo a fronte di<br />
una estrema tollerabilità da parte del paziente medio.<br />
Si arriva quindi all’isopentenil pirofosfato, a questo punto ci sono due possibilità: si possono formare…<br />
- isopentenil adenina, utile nella replicazione del DNA.<br />
- geramil pirofosfato & farnesil pirofosfato: questi due sarebbero alla base<br />
dell’isoprenilazione delle proteine. Basti considerare che tutti i metaboliti intermedi del<br />
colesterolo sono isoprenoidi, che possono andare a coniugarsi con una proteina: questo ha la<br />
funzione di ancorare le proteine alla membrana.<br />
Un diverso rapporto tra questi due isoprenoidi che legano la proteina p21RAS sembrerebbe<br />
essere pro-cancerogeno (studio italiano). Questa proteina infatti ha le capacità catalitiche di<br />
una subunità α di G protein, ma senza l’attività intrinseca di tipo GTPasico (favorita dalle<br />
proteine GAP) che porta normalmente ad una auto inattivazione e sospensione del segnale.<br />
La p21ras è mutata in un gran numero di tumori di origine chimica, ed è un enzima molto<br />
simile ad una G-protein che rimanga sempre attiva, generando un segnale continuo<br />
collegato in qualche modo alla moltiplicazione cellulare in numerosi tessuti (colon, polmone).<br />
Sostanzialmente la modalità di isoprenilazione di queste proteine (più geramilata o più<br />
farnesilata) si traduce o meno nella <strong>patologia</strong> neoplastica. Piuttosto che un problema di<br />
struttura AAcidica quindi è un problema legato all’ancora.<br />
possibile meccanismo patogeno delle HIDS<br />
Nei linfociti, l’alterato rapporto di farnesilato e garmilato, potrebbe portare ad uno stimolo<br />
aspecifico, ⇒ prod. di IgD (linfociti immaturi); si presuppone una funzione antinfiammatoria 3 degli<br />
isoprenoidi:<br />
Stimolo: il<br />
bambino si è<br />
stancato troppo<br />
mevalonato<br />
chinasi↓↓<br />
⇓<br />
mevalonato ↓<br />
febbre<br />
⊕HMG-CoA<br />
reduttasi<br />
mevalonato↑<br />
funzione anti<br />
infiammatoria<br />
&<br />
defervescenza<br />
dal Farnesil Pirofosfato derivano inoltre elementi come il dolicolo (glicosilazione proteica), l’emeA (catena<br />
respiratoria), ubichinone (antiossidanti)…<br />
3 Prima è stato detto esattamente l’opposto: le statine bloccherebbero la produzione di isoprenoidi con azione anti<br />
infiammatoria. Evidentemente si tratta di interazioni fra metaboliti intermedi e vie metaboliche, il che produce effetti<br />
diversi… p.es basti considerare che il cortisolo deriva dal colesterolo, ed è l’anti infiammatorio più potente che esista…<br />
sostanzialmente non si sa, quindi…<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 15
TRAPS (TNF Receptor 1 - Associated Periodic Syndrome)<br />
Ovviamente si tratterà del gene del recettore al TNF, che determinerebbe un ridotto clivaggio del recettore.<br />
Si tratta del meccanismo di regolazione di tutte le citochine, dal TNF all’IL-1…<br />
Descriviamo quindi la regolazione dell’IL-1 (che è la più complessa: capita questa capite tutte). Le citochine<br />
hanno due e più recettori (di tipo I e <strong>II</strong>), nel caso dell’IL-1:<br />
• IL-1RI<br />
• IL-1AcP: a differenza delle altre citochine la IL-1 ha bisogno anche di un corecettore,<br />
una proteina ancillare (IL-1AcP appunto); Solo dall’unione di IL-1RI e<br />
IL-1AcP scaturirà la cascata a valle. L’IL-1R<strong>II</strong> è un recettore in grado di<br />
competere con il recettore di tipo I, modulando in questo modo la risposta.<br />
• IL-1R<strong>II</strong>: ha una corta coda citoplasmatica, e non è così in grado di trasdurre il segnale,<br />
riducendolo: sottraendo IL-1 all’IL-1RI, è detto “recettore trappola”.<br />
• IL1-Ra: Receptor antagonist; è un’azione a feedback. L’azione dell’IL-1 stessa porta alla<br />
produzione di questo elemento che le compete sull’IL-1RI.<br />
⇒ dalla carenza di IL-1Ra si hanno importanti sindromi auto infiammatorie con<br />
dermatiti, febbri, artriti… si risolve con una terapia cronica: somministrazione<br />
di IL-1Ra. Sono malattie pediatriche, che vanno attenuandosi con l’età, e sussistono<br />
unicamente in caso di deplezione omozigotica del gene all’IL-1a.<br />
Nb: un altro importante meccanismo di controllo consisterebbe nello shedding (eliminazione) della<br />
componente extracellulare del recettore nella matrice esterna: i frammenti, legando l’IL-1 agirebbero<br />
quindi di nuovo come competitori già nella matrice.<br />
è questo il meccanismo (riferito al TNF), che viene a mancare nella TRAPS, cioè una delle sindromi<br />
febbrili di origine non settica, dovuti alla mancata inibizione al segnale di tipo interleuchinico, che attiverà<br />
una “reazione infiammatoria a vuoto”.<br />
FMF (Febbre Mediterranea Familiare)<br />
Sembra essere mutato un gene implicato nella down-regolazione dei mediatori dell’infiammazione.<br />
OFaF (Orticaria Familiare a Frigore)<br />
Si tratta di bambini che esposti al freddo presentano un Rush Cutaneo<br />
SMW (Sindome di Michael - Wells)<br />
Sempre pediatrica, i bambini affetti presentano orticarie spontanee<br />
§<br />
Alterazioni del Metabolismo degli Amminoacidi<br />
Fenilchetonuria<br />
Viene a mancare l’enzima della reazione “fenilalanina tirosina”, e quindi prodotti quali…<br />
• tiroxina<br />
• DOPA, adrenalina<br />
• melanine<br />
Ci aspettiamo quindi<br />
1) deficit neurologici gravi<br />
a. ritardo mentale (DOPA…)<br />
b. crisi epilettiche<br />
2) ipopigmentazione (melanine..)<br />
3) difetti metabolici<br />
a. ipotiroidismo (tiroxina..)<br />
b. accumulo di fenilacetato 4 per l’attivazione di vie metaboliche alternative…<br />
Alcaptonuria<br />
tirosina ac.omogentisico ac.maleil acetacetico<br />
- conseguenze: polimerizzazione dell’ac.omogentistico ⇒ deposizione di pigmenti nel<br />
connettivo di articolazioni (artrite), tendini (oncronosi), cartilagini e sclere.<br />
- escrezione: urine nerastre 5 per ossidazione in ambiente alcalino<br />
4 Questo viene poi rilasciato con le urine, che assumono un caratteristico odore, tali da venir definite “urine di topo”.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 16
§<br />
Alterazioni del Ciclo dell’Urea<br />
Iperammoniemia (Hyperammonemia) Primaria<br />
Il ciclo dell’urea serve a smaltire lo ione ammonio (NH4):<br />
NH4 + ornitina citrullina + aspartato ornitina + urea<br />
Questo avviene tipicamente a livello epatico. Praticamente ognuno di questi passaggi richiede enzimi che<br />
possono essere carenti, nel qual caso si avrebbe iperammoniemia primaria.<br />
Questo stato è gravissimo, porta ad alterazioni neurologiche gravi, causando un’alta letalità neonatale.<br />
Iperammoniemia Secondaria<br />
In caso di Cirrosi, o comunque disfunzioni epatiche. In particolare è importante nella patogenesi lo<br />
shunt porta-cava, e la formazione dei pseudo lobuli epatici, dove si ha la deposizione di tessuto fibroso di<br />
riparazione nei lobuli danneggiati che arrivano a stravolgere il tessuto e la normale circolazione dell’organo:<br />
- grossi rami vasali interrotti dalle cicatrici<br />
- fenomeno infiammatorio sotteso alla cirrosi: presenza di mediatori infiammatori (citochine), che<br />
provocano una trans differenziazione delle cellule stellate che diventano fibroblasti.<br />
Le cellule stellate che rispondevano all’ossigenazione, alle richieste metaboliche ora non lo fanno più, questo<br />
porta ad una strozzatura dei vasi, il che porta alla conseguenza che non passa più sangue attraverso il<br />
fegato: trova un fortissimo impedimento, instaurando un’ipertensione portale, che scarica lungo le strade<br />
alternative costituite da collegamenti tra circolo portale e sistemico (vene cave):<br />
1) vene esofagee<br />
a. vena gastrica sinistra<br />
b. vene della sottomucosa esofagea<br />
⇒ azygos ⇒ cava superiore<br />
Normalmente le vene esofagee sarebbero filiformi, ma diventano<br />
sempre più evidenti man mano che il sangue portale vi si riversa,<br />
finendo per gonfiarsi nel lume esofageo (sono sottomucose, a livello<br />
del cardias), portando alla formazione di varici esofagee, all’interno<br />
delle quali il sangue ha una certa pressione. Questa localizzazione a<br />
livello di un punto delicato come il cardias porta alla formazione di<br />
reflussi esofagei, che possono provocare ulcerazione delle vene<br />
nell’esofago, con emorragia interna 6 . Questa emorragia è lenta<br />
(venosa), il paziente può non accorgersene:<br />
melena 7 , feci nere: presenza di sangue transitato<br />
nello stomaco e digerito.<br />
emesi con vomito caffeico: se il sangue che si accumula nello stomaco è tanto da<br />
irritarlo, è sempre presenza di sangue digerito.<br />
2) vene emorroidarie<br />
E’ un collegamento che appartiene forse solo accademicamente ai libri, sarebbe la stessa dinamica<br />
dello shunt esofageo.<br />
3) vene splenorenali<br />
tutta la capsula renale sarebbe ricca di vasi venosi a partire dalla vena splenica e si scaricano nella<br />
vena renale.<br />
4) micro-shunt interni<br />
con la liberazione di vari fattori di crescita (EGF…) si ha la crescita disordinata di vasi, che<br />
provocano uno scaricamento di sangue portale nelle vene, e quindi il sangue comincia anche a<br />
bypassare il fegato.<br />
5<br />
può avvenire anche in caso di melanomi in stato avanzato o di porfiria (scrubs rulez).<br />
6<br />
Ricordiamo anche altre cause comuni di emorragia interna: aneurisma aortico, gravidanza extrauterina (che dà i classici<br />
sintomi della peritonite e dell’emorragia interna, combinati)…<br />
7<br />
se la lesione è più a valle, si avrà invece feci con colorito rossastro, perché non transitando nello stomaco il snague non è<br />
digerito.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 17
⇒ tutti questi reflussi dal fegato sono comunque di sangue ricchissimo di ione ammonio.<br />
Il levulosio (levulose) o fruttosio è considerato un lassativo: è uno zucchero non assorbibile che<br />
arricchisce la fauna batterica zucchero-litica nei confronti di quella proteolitica. Questo provoca quasi<br />
una risoluzione della problematica in quanto l’acidificazione del colon provoca il rilascio nel lume di<br />
NH3. La dose del “farmaco” è importante, perché sovradosaggi possono portare a fermentazione<br />
intestinale.<br />
Conseguenze dell’iperammonemia<br />
Sono principalmente a carico del SNC. Non si sa perfettamente perché; nel SNC lo ione ammonio si complessa<br />
con l’acido α-chetaglutarico, che è un intermedio di Krebs, sottraendolo al ciclo, che è l’unica via<br />
attraverso cui il SNC è in grado di procurarsi energia (cioè attraverso la degradazione degli zuccheri).<br />
Questo inoltre porta ad un accumulo di glutammina, che non ha ripercussioni particolari.<br />
Il paziente epatopatico è inizialmente stuporoso (oh, è giorno, oh, sono in ospedale…), quindi sprofonda<br />
generalmente in un coma.<br />
Senescenza Tissutale<br />
1) Lesioni Cellulari, operate fondamentalmente da fattori di perossidazione.<br />
Tra questi ci sono gli AGE (Advaced Glicosilation of End products) le HSP<br />
(Heat Shock Protein). La lipofucsina è un pigmento che risulta fluorescente,<br />
giallastro, e deriva dalla perossidazione di lipidi<br />
2) CLK-1 (CLocK), gene le cui mutazioni provocano un rallentamento della moltiplicazione;<br />
trascriverebbe per un enzima coinvolto nella sintesi dell’ubichinone.<br />
3) Elicasi, un enzima che svolge il DNA e ne favorisce la riparazione. Questo è alterato a livello genico<br />
nella Sindrome di Werner, caratterizzata dall’invecchiamento precoce.<br />
4) Atassia Teleangectasia: dipende dalla compromissione della funzione coordinativa del cervelletto nei<br />
movimenti, e la comparsa di capillari ed angiomi cutanei. Si ha la<br />
malformazione della proteina ATM, un sensore del danno genomico.<br />
Quando c’è un’alterazione del DNA è in grado di attivarsi.<br />
5) Telomerasi: la presenza dei telomeri è fondamentale per la sopravvivenza delle cellule<br />
dell’organismo. La telomerasi è per lo più inattiva nei tessuti adulti (si ammette ora che in<br />
alcuni tessuti continui a funzionare), mentre è sicuramente attiva nei tessuti embrionali e<br />
nei tumori. La perdita dei telomeri, o meglio la loro riduzione, provoca la perdita di una<br />
funzione protettiva: in particolare impediscono..<br />
a. l’azione di nucleasi sul DNA<br />
b. la fusione aberrante tra cromosomi<br />
All’accorciamento eccessivo del telomero si ha l’attivazione della p53, che tramite fattori<br />
come il gene BAX, blocca la proliferazione cellulare. Applicato a livello sistemico, ciò<br />
provoca una diminuzione del numero di cellule con l’avanzare dell’età. In cultura è<br />
possibile bloccare la p53, e tutta una serie di virus (HBV, EBV, Papillomavirus) hanno il<br />
medesimo effetto. Quello che si osserva col mancato funzionamento della p53 è la<br />
formazione di cromosomi alterati, doppi, dicentrici: manca un meccanismo importante di<br />
controllo.<br />
p53<br />
E’ di fatto un tetramero legante il DNA, la cui produzione dipende come sempre da due alleli. Risulta<br />
alterata funzionalmente in praticamente tutti i tumori;<br />
Abbiamo già detto come gli oncogeni possono essere mono allelici dominanti, ma nel caso di anti-oncogeni<br />
per avere una loss of function c’è bisogno di un danno bi-allelico.<br />
Strategie di terapia genica con somministrazione del gene della p53 sono state provate, ma non hanno<br />
funzionato per la dinamica della dominanza negativa: si può avere che anche soltanto uno degli alleli risulti<br />
alterato, per cui il prodotto di una singola molecola aberrante provoca un montaggio aberrante anche di quelle<br />
sane. Quello che fa normalmente p53 è di attivarsi in caso di danno cellulare. A questo punto media il blocco<br />
del ciclo e la trascrizione di proteine di riparazione: la cellula ha un certo tempo per riparare il proprio DNA. Se questo<br />
non avviene la p53 rimane attiva e induce la trascrizione di geni come il BAX, che produrrà una inibizione della Bcl-2,<br />
un elemento bloccante l’apoptosi. Se invece il danno è riparato, p53 viene ubiquitinizzata e la cellula riprende il ciclo.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 18
§<br />
Apoptosi<br />
La morte cellulare è il termine invariabile della senescenza cellulare: può avvenire per apoptosi o per necrosi.<br />
necrosi: si ha un rigonfiamento dei mitocondri, avviene un’autolisi della cellula, una disgregazione, ad<br />
opera di enzimi presenti all’interno. La necrosi non riguarda singole cellule ma parti ampie di<br />
tessuti, ed induce una risposta infiammatoria.<br />
Per questo poi si ha la rimozione del materiale necrotico con richiamo di neutrofili e la<br />
stimolazione alla cicatrizzazione.<br />
Nell’apoptosi i mitocondri non vengono ad essere ingrossati, si ha una frammentazione della cellula, con<br />
formazione di valli che vanno sempimentando la cellula fino a formare corpi apoptotici che vengono<br />
fagocitati dagli elementi circostanti (non solo macrofagi, ma anche cellule del tessuto d’origine).<br />
Questo processo riguarda singole cellule e non si ha infiammazione. Questa dinamica è rimasta a lungo<br />
oscura, perché i corpi apoptotici, oltre a venir immediatamente fagocitati, nel vetrino appaiono come tagli di<br />
cellule integre. Per arrivarci, è stato risolutivo il C.Elegans, un nematode che pur avendo cellule in attiva<br />
divisione, è formato sempre da 945 cellule ⇒ doveva esistere un programma di controllo.<br />
L’apoptosi è anche un meccanismo di risposta a stimoli stressogeni: in una ischemia, anche prima<br />
dell’infarto si osserva apoptosi: questo è positivo, in quanto poi quel poco ossigeno si distribuisce a meno<br />
cellule. D’altra parte ci sono cellule che hanno bisogno di stimoli ormonali che ne impediscano l’apoptosi.<br />
E’ importante in questo contesto il FAS ligando, detto recettore di morte.<br />
esempi (domanda d’esame)<br />
1) Caernohabditis Elegans (nematode di 945 cellule): perde 131 cellule durante la maturazione<br />
(=programma ontogenetico)<br />
a. geni ced-3 / ced-4 ⇒ apoptosi<br />
b. gene ced-9 ⇒ sopravvivenza<br />
2) Cellule Interdigitali vanno incontro ad apoptosi durante lo sviluppo, provocando il distacco delle<br />
dita; questo tipo di evento sarà geneticamente determinato<br />
3) Timo: va mano a mano in regressione con l’età, tramite meccanismi apoptotici; inoltre provoca<br />
l’apoptosi delle cellule T autoreattive<br />
4) Cicli Fisiologici: p.es l’involuzione dell’epitelio ghiandolare mammario e della mucosa uterina in fase<br />
post-mestruale<br />
5) Risposta Immune: citotossicità di CTL e NK nei confronti di cellule<br />
a. infettate da virus<br />
b. allotipiche (trapianti, graft vs host disease)<br />
c. cellule tumorali<br />
6) spegnimento della risposta immunitaria: simile alla mancanza di un certo ormone:<br />
7) cellule neoplastiche<br />
8) Virus Citocidi<br />
carenza di fattori pro infiammatori e di Ag estraneo provoca l’apoptosi di tutto quel<br />
complesso cellulare che si era creato.<br />
cortisone: ad alte dosi provoca la morte dei linfociti in attiva proliferazione<br />
9) Tessuti Immunologicamente Privilegiati: la cornea, il testicolo… le cellule di questi tessuti<br />
presentano FAS ligant, che attivando il fattore di morte di<br />
eventuali cellule immunitarie che arrivino in loco.<br />
10) segnali embriogenici: programmati<br />
11) danni al DNA, mutazioni: che provocano l’attivazione della p53, che a livello mitocondriale, tramite<br />
diversi messaggi, provoca il rilascio del citocromo C (cytochrome-C)<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 19
12) Stress: come già citata, la carenza di ossigeno, lo stress ipossiemico provoca un aumentato tasso di<br />
morte cellulare.<br />
zone peri infartuali: sono irrorate con il contributo di diverse arterie: se una di queste<br />
si interrompe, il tessuto che riceve solo da quella andrà incontro<br />
ad infarto, le zone che erano supportate anche da quell’arteria<br />
avranno un aumento di apoptosi, che dall’1% fisiologico può<br />
raggiungere il 30%. Questo giustifica la riperfusione, la<br />
riabilitazione di un’arteria che era risultata occlusa anche a<br />
distanza dall’episodio infartuale.<br />
Nb: a chi ha avuto un infarto viene caldamente suggerito di fare jogging, per stimolare la<br />
neoangiogenesi, ma sforzi eccessivi probabilmente rischiano di far pendere troppo la<br />
bilancia dal lato dell’apoptosi piuttosto che l’angiogenesi…<br />
13) recettori di morte: FAS, TNF, TLR4 (Toll Like Receptor: il quarto è pro apoptotico e lega l’LPS).<br />
Il TNF è anche altro che un pro-apoptotico; è infatti una citochina infiammatoria,<br />
come ben sappiamo, molto simile alla IL-1: attiva fattori quali l’NF-κB, in grado<br />
di provocare attivazione infiammatoria. La sua diversa azione probabilmente<br />
dipende da diversi contesti biochimici.<br />
Quale che sia la strada, si arriva all’attivazione di specifiche endonucleasi ⇒ frammentazione del DNA in<br />
multipli di 200 BP (Base Pairs) 8 . Questo grazie alle caspasi esecutive (i numeri, caspasi-1,6,9.. non sono<br />
importanti).<br />
Nel corso della sepimentizzazione avviene la superficializzazione di molecole (come la fosfatidil serina) atte<br />
a segnalare alle cellule circostanti che un corpo è da fagocitare, per cui quello che può avvenire è che non<br />
sono solo cellule specializzate, ad eliminare i residui, ma anche quelle specializzate tissutali.<br />
Controllo del Ciclo<br />
1) Cicline: attivano le CDK (Ciclin Dependet Kinase) che entrano in sequenza lungo il ciclo cellulare,<br />
permettendone la progressione: sono prodotte solo in determinate fasi del ciclo e poi<br />
rapidamente eliminate nella via ubiquitina proteosomica.<br />
2) Inibitori delle CDK, che sono nominati come p16, 17…, 21,…53… è importante la sequenza<br />
⊕p53 ⊕p21 ciclo cellulare.<br />
3) Gene RB (Retino Blastoma): il suo prodotto rappresenta un meccanismo di controllo del passaggio<br />
dalla fase G1 alla fase S: normalmente è complessato in forma inattiva col fattore di<br />
trascrizione E2F, impedendo la progressione del ciclo. Poi il complesso ciclinaD-CDK4<br />
la fosforila il complesso RB-E2F liberando l’E2F e permettendo la progressione in S.<br />
4) Bcl-2: s’intende un gene appartenente a tutta una famiglia, in grado di regolare la permeabilità<br />
della membrana mitocondriale, e quindi il rilascio il citocromo C (componente della<br />
catena respiratoria), il quale si associa alla proteina figlia del gene APAF-1, formando un<br />
apoptosoma, in grado sua volta di clivare la procaspasi-9, attivandola. Il Bcl-2 a questo<br />
punto interagisce bloccando l’azione dell’APAF-1, e bloccando l’apoptosi: è quindi un<br />
oncogene, in quanto si oppone all’apoptosi delle cellule mutate<br />
§<br />
Necrosi<br />
Riguarda gruppi di cellule, più o meno ampie parti di tessuto in seguito ad insulti lesivi rilevanti in grado<br />
di danneggiare la cellula in modo irreversibile.<br />
- traumi<br />
- fattori fisici<br />
- fattori chimici<br />
- fattori biologici (virus litici)<br />
- fattori nutrizionali<br />
- risposte immuni<br />
- ipossia, ischemia<br />
- inquinamenti<br />
- carenze<br />
8 Anche nella necrosi si avrà la frammentazione del materiale genetico, ma senza criterio, e quindi ci sarà la generazione<br />
di frammenti di diverse dimensioni.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 20
Tipo di Danno<br />
• reversibile (cfr.pag.42 p.te I)<br />
- rigonfiamento del SRE<br />
- perdita di ribosomi dal RER<br />
- Addensamento dei mitocondri con distacco della membrana interna<br />
- comparsa di vescicolazioni sulla membrana cellulare (blebs)<br />
• irreversibile (limite sottile e non ben identificato)<br />
- rigonfiamento dei mitocondri<br />
- rottura delle blebs<br />
Alcuni Danni Cellulari<br />
1) Perossidativi / da radicali: si ha la perossidazione dei lipidi di membrana rilascio di<br />
malondialdeide, quindi crosslinking dei gruppi sulfidrilici di proteine<br />
e lipidi. Provoca inoltre alterazioni del DNA<br />
2) Da Virus: tutti i virus litici che portano alla morte della cellula, agiscono bloccando la sintesi<br />
proteica cellulare.<br />
Alterazioni Citologiche Classiche<br />
citoplasma<br />
eosinofilia: il citoplasma si fa più basico, quindi acidofilo, quindi eosinofilo;<br />
questo a causa delle proteine coagulate<br />
omogeneità del citoplasma<br />
globuli eosinofili (mitocondri rigonfi)<br />
permeabilizzazione ai coloranti vitali: si valuta se la membrana della cellula<br />
risulta permeabile p.es al tripano blu (500Da). Questo<br />
elemento normalmente non filtra la membrana, ma se la<br />
cellula è necrotica riuscirà a trovare un passaggio (membrana<br />
danneggiata) e colorerà elementi intra citoplasmatici.<br />
nucleo<br />
addensamento della cromatina<br />
picnosi: riduzione della dimensione e aumento di basofilia, segue in genere…<br />
carioressi: frammentazione nucleare<br />
cariolisi: scomparsa del nucleo<br />
Col tempo la cellula potrà quindi andare incontro a processi quali<br />
Tipi di Necrosi (importante!)<br />
1) coagulativa (infarto):<br />
autolisi: digestione da parte di enzimi lisosomiali propri dellla cellula<br />
eterolisi: digestione mediata da fagociti ed elementi richiamati dall’’infiammazione<br />
a. ischemia<br />
b. fenomeni fisici (bruciature, congelamenti…)<br />
La caratteristica di questa necrosi è che le cellule sono perfettamente riconoscibili (a livello di<br />
tipo di tessuto), salvo il fatto che alla microscopia ottica si notano alterazioni come la cariolisi, più<br />
quelle alterazioni sopra elencate.<br />
Una distinzione tipicamente anatomopatologica è quella di infarto rosso e bianco. Tipicamente si<br />
tratta di tessuti come il polmone e il fegato che hanno una doppia circolazione. Quello che si nota<br />
è che il tessuto non è bianco, carente di sangue, ma dopo essere andato in necrosi, si ha avuto il<br />
disfacimento del tessuto e un suo infarcimento di sangue.<br />
a. infarto rosso ⇒ tipicamente fegato e polmone<br />
b. infarto bianco ⇒ gli altri tessuti<br />
Nb: si nota nel cuore una tipica colorazione dorata al passaggio del coltello (anatomia patologica)<br />
dovuta alla perossidazione data dagli elementi mitocondriali.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 21
2) colliquativa: il materiale sarà liquefatto. Tipicamente in presenza di pus, che crea una omogeneità.<br />
E’ dovuta all’azione dei granulociti. Il tessuto non è più riconoscibile. Nella cisti<br />
cerebrale si ha inizialmente una necrosi coagulativa tipica della necrosi ischemica, ma<br />
poi le fasi sono così veloci che alla morte dell’individuo si è già arrivati alla forma<br />
colliquativa, tipica del materiale cerebrale.<br />
3) caseosa: richiama il formaggio fuso, biancastro. E’ quasi patognomonico per il granuloma<br />
turbecolare, dove al centro si ha una colliquazione che porta alla formazione di materiale<br />
con questa consistenza.<br />
4) gangrenosa: non aggiunge nulla alle necrosi di tipo coagulativo o colliquativa. E’ semplicemente la<br />
definizione clinica di necrosi coagulativa / colliquativa. P.es una gamba che abbia subito<br />
ischemia e quindi necrosi, si parlerà clinicamente di gangrena.<br />
a. gangrena secca ⇒ corrispettivi microscopici della necrosi coagulativa; Poniamo l’interruzione<br />
di una arteria di una gamba: diventerà immediatamente pallida, e successivamente<br />
si avrà morte cellulare tipicamente coagulativa. Man mano si avrà un<br />
rinsecchimento fino ad una mummificazione (color nero). La prognosi è buona:<br />
non si hanno particolari problemi, si perde la funzionalità dell’arto, ma se rimane lì<br />
non succede nulla. E’ benigna…<br />
b. gangrena umida ⇒ necrosi colliquativa; in genere si tratta di una necrosi coagulativa<br />
complicata da un’infezione: l’azione digestiva di batteri e leucociti<br />
trasforma il tutto in materiale purulento. Prognosticamente è molto<br />
peggio della gangrena secca: ci sarà una continua espansione. E’ tipica di<br />
chi ha carenze di difesa, come i diabetici, che hanno tutta una serie di<br />
caratteristiche che portano ad un minor flusso sanguigno anche a livello<br />
capillare, con una ridotta possibilità di cellule immunocompetenti di arrivare<br />
in sede. I batteri hanno un buon gioco in entrata, e l’infezione va avanti. Spesso<br />
l’unico modo di procedere è amputare.<br />
c. gangrena gassosa: tipica dei clostridi, che sono in grado di digerire praticamente qualsiasi<br />
cosa, e producono gas a livello interstiziale nei tessuti. La sensazione,<br />
alla pressione sul tessuto è quella della neve fresca. Come sempre, la<br />
soluzione alla presenza di pus è aprire, ed evacuare.<br />
5) steatonecrosi: è il caso della liponecrosi pancreatica. L’ostruzione dei canalicoli pancreatici porta<br />
all’accumulo ed alla digestione di pancreas e tessuti circostanti: si forma una sorta di<br />
raccolta di tessuto grasso emorragico. Talvolta è collegato all’alcolismo, ma<br />
normalmente si pensa che possa dipendere da infezioni delle vie biliari, che<br />
andrebbero individuate precocemente grazie a test come l’amilasi…<br />
6) fibrinoide: è un termine un po’ storico, se ne parla ancora in anatomia patologica. Riguarda<br />
fondamentalmente i preparati renali nel corso di malattie autoimmune: si associa ad<br />
ipertensione maligna (alti valori pressori fin dall’età giovane) ed alterazione quindi delle<br />
pareti arteriolari. Gli istologi avevano infatti stabilito regole di colorazione per<br />
identificare quel tipo di alterazione collegata con le collagenopatie (termine con cui si<br />
indicavano le malattie autoimmuni).<br />
fegatoI: lesione più recente, dove<br />
si nota la perdita di dettaglio a<br />
livello nucleare, la freccia in alto<br />
a destra indica una cellula con<br />
carioressi.<br />
fegato<strong>II</strong>: lesione avanzata (colliquativa):<br />
rimanenze di epatociti, assenza di margini<br />
riconoscibili, di elementi nucleari. I corpi<br />
vacuoli formi osservabili sono prodotti<br />
dell’apoptosi delle cellule infiammatorie,<br />
probabilmente.<br />
colliquazione cerebrale<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 22
immagine di necrosi caseosa: il linfonodo caseoso, che alla fine è riuscito, evidentemente ad isolare l’infezione, che<br />
risulta colliquata nella modalità di necrosi caseosa.. i lipidi del bacillo di Koch vengono infatti in qualche modo sciolti.<br />
(immagine) Si dice che sostanzialmente quella caseosa è una necrosi a metà tra colliquativa e colligativa, con materiali<br />
cellulari sparsi alteranti a soluzione fluida (seconda immagine di necrosi caseosa)<br />
Evoluzione della necrosi<br />
1) induzione di flogosi circostante<br />
la necrosi induce infiammazione (su base settica, ischemica, fisica… non importa, comunque si ha<br />
infiammazione)<br />
riassorbimento del materiale andato incontro a morte<br />
sostituzione di quel materiale<br />
con una rapidità ed una efficacia che dipende dal tessuto in cui ci si trova.<br />
cicatrice (organizzazione connettivale) ⇒ si può avere infine calcificazione della<br />
stessa, che risulta molto importante nella radiologia.<br />
tessuto rigenerato<br />
In ogni caso gli stimoli, i fattori di crescita, sia per quanto riguarda la formazione di una cicatrice (lo stimolo<br />
verso i fibroblasti a migrare e a produrre collagene..) più che delle cellule parenchimali circostanti, derivano<br />
da macrofagi e monociti, che sono le cellule “intelligenti”, centrali, che producono stimoli per le cellule<br />
circostanti, oltre ad aiutare nella ripulitura del materiale necrotico.<br />
Calcificazioni Patologiche<br />
1) distrofica ⇒ consegue alla necrosi; quella appena vista nella pagina prima, quindi. Gli esempi sono<br />
molto frequenti e si notano nelle radiografie dirette (senza mezzi di contrasto o altro).<br />
Avviene per formazione di cristalli di CaPO4 tipici anche del tessuto osseo, che si<br />
depositano a livello del materiale cicatriziale, con particolare affinità col collagene.<br />
Il processo ha inizio con l’accumulo di calcio e l’attivazione di fosfatasi Ca 2+ -dept.<br />
a. necrosi di ateromi: si parla ovviamente delle arterie, dove ai lati degli ateromi si hanno<br />
fenomeni di infiammazione a livello della capsula fibrosa che viene a<br />
crearsi. Questo può estendersi anche all’intera aorta, rendendola<br />
completamente rigida, il che, come si sa, aumenta la PD.<br />
b. invecchiamento: può non esserci per forza una base aterosclerotica, ma semplicemente un<br />
accumulo di materiale collagenico che sostituisce le cellule degenerate e<br />
che crea una base per la calcificazione.<br />
c. cancro: si tratta di calcificazioni a sabbia tipiche dell’adenocarcinoma duttale della<br />
mammella, soprattutto a livello linfonodale. E’ quasi patognomonico. Nell’ambito<br />
della crescita tumorale infatti si ha una vascolarizzazione discontinua, per cui si hanno<br />
continui fenomeni di necrosi all’interno.<br />
d. linfonodi tubercolari: quindi si parla di una infiammazione cronica. Prima si ha la necrosi<br />
caseosa, che in seguito va incontro a calcificazione. In queste malattie<br />
granulomatose si ha sempre un equilibrio tra batterio e organismo<br />
infettato. La calcificazione risulta l’atto finale di difesa, che però non<br />
esclude l’’eventualità di una reinfezione endogena. Questi possono<br />
essere più tipicamente polmonari, ma non solo.<br />
e. valvole cardiache: si rilevano nelle autopsie, si tratta dell’esito di fatti di fibrosi non<br />
collegati con fenomeni infettivi, che poi evolvono in calcificazione.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 23
2) metastatica “pura” ⇒ dipendentemente prettamente dall’alta calcemia, e coadiuvata da diversi<br />
fattori. Non è preoccupante particolarmente. Fondamentalmente parte<br />
dall’interstizio, non da tessuto necrotico come prima, ed in particolare a<br />
livello dei vasi sanguigni. Questo evento calcifico scollegato<br />
dall’aterosclerosi si può rilevare in qualsiasi distretto, non solo (come quella<br />
distrofica) nell’aorta e nelle prime diramazioni. Questo tipo di calcificazione<br />
non è preoccupante a livello arteriolare, riguarda infatti la parete, non<br />
il lume, quindi non ci saranno eventi di perforazioni, emorragie… è quasi<br />
normale trovare un circolo del Willis completamente solido. A livello delle<br />
arterie radiali si parla di strutture a trachea di pollo o a rosario.<br />
a. immobilizzazione: pazienti allettati per anni, o anche solo per mesi vanno incontro a<br />
demineralizzazioni ossee che portano ad una ipercalcemia<br />
b. tumori ossei che provochino demineralizzazioni (metastasi, leucemie, mieloma…)<br />
c. iperparatiroidismo<br />
d. forma idiopatica (infantile)<br />
e. ipertiroidismo (dato di fatto: meccanismo sconosciuto)<br />
f. ipersurrenalismo (Addison)<br />
Sunto sulla morte cellulare (markers)<br />
Attualmente il termine di “necrosi” è stato in parte rivisto, e si individuano infine situazioni di…<br />
1) Necrosi apoptotica o semplicemente “apoptosi”<br />
a. caspasi 3 attiva ⇒ è alla fine delle caspasi “iniziatrici”, il punto di collegamento con quelle<br />
“effettrici”.<br />
b. T.U.N.E.L. ⇒ è una reazione che dimostra la cariolisi. Va memorizzato. Individua i punti di<br />
taglio del DNA ad opera di nucleasi che intervengono verso le ultime fasi creando<br />
segmenti di c.a 800bp, in maniera piuttosto specifica: si lega al 3’OH terminale del<br />
nucleotide modificato dall’enzima. E’ considerata una delle reazioni più precise.<br />
c. Chromatin Ladder: si nota nell’elettroforesi la presenza di multipli di 200 paia di basi.<br />
In genere non si esegue.<br />
2) Necrosi oncotica o semplicemente “necrosi classica”<br />
a. C9: fattore 9 del complemento. Più che per accertare l’analisi microscopica, che si commenta<br />
da sola, serve per diagnosi precoci di attività necrotica. Si ricollega con la permeabilità al<br />
blu tripano.<br />
3) Necrosi autofagica: tipicamente a livello di SNC è una tipologia particolare di autofagia che si nota<br />
solo a livello centrale, e che presenta diversi meccanismi di innesco.<br />
a. ubiquitina: se ne ha sovrapproduzione.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 24
Infiammazione o Flogosi<br />
E’ la reazione di un tessuto vivente e vascolarizzato ad un danno locale, che può derivare da qualsivoglia<br />
stimolo. Gli stimoli infettivi vedono un profilo classico di aumento (inizialmente) stabilizzazione ed estinzione<br />
della popolazione batterica. Il ruolo del SI aspecifico è fondamentale: permette un controllo di base della<br />
popolazione batterica tale che l’attivazione del SI specifico possa poi essere efficace.<br />
Si distinguono tipicamente<br />
E’ diverso il momento in cui manca la risposta<br />
specifica: dopo la fase stabile si ha di nuovo un<br />
aumento indefinito della popolazione batterica.<br />
E’ quindi chiaro come siano necessarie entrambe<br />
le risposte.<br />
flogosi acuta (angioflogosi) ⇒ tende ad essere di breve durata, ma ci sono flogosi con queste caratteristiche,<br />
come quelle dell’osteomielite, che possono comunque durare anni.<br />
Si caratterizza per la presenza di fenomeni essudativi, cioè con passaggio delle<br />
proteine attraverso l’endotelio. Si ha inoltre la tipica infiltrazione di PMN<br />
neutrofili 9 .<br />
Qualunque sia la causa si presenta sempre con le stesse caratteristiche.<br />
flogosi cronica (istoflogosi) ⇒ tende a mantenersi nel tempo, presenta tempistiche anche di anni.<br />
L’essudazione è molto fugace, tipicamente iniziale; E’ di pertinenza<br />
macrofagica, possibilmente se c’è di mezzo una risposta immunitaria<br />
interverranno anche i linfociti. Si ha normalmente anche infiltrazione<br />
connettivale (fibroblasti).<br />
Normalmente diverse cause provocano differenze morfologiche che<br />
permettono una diagnosi; differentemente dall’angioflogosi, dove la<br />
manifestazione è identica a prescindere dalla causa.<br />
1) ⊕ elementi plasmatici / cellulari<br />
2) formazione di mediatori chimici<br />
§<br />
Flogosi Acuta (angioflogosi)<br />
3) alterazioni:<br />
a. emodinamiche<br />
b. della permeabilità vascolare (⇒ edema infiammatorio)<br />
c. migrazione di cellule<br />
rubor<br />
calor<br />
tumor<br />
dolor<br />
functio lesa<br />
9 ricordiamo che si hanno c.a 6-7mila leucociti, per un 70% c.a di PMN neutrofili.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 25
Elementi citoplasmatici coinvolti<br />
1) Complemento: importanti alcuni punti:<br />
- fattore C3b: in grado di fare da opsonina, favorendo l’azione dei granulociti.<br />
- cascata dal C5b al C9: assolutamente fondamentale nelle infezioni da Neisserie<br />
(meningococco e pneumococco). La cosa particolare è che in bambini<br />
deficienti di fattori del complemento si ha una maggiore frequenza di<br />
infezione, ma contestualmente una malattia meno aggressiva: si ha un<br />
ruolo forse “eccessivamente flogistico” da parte del complemento...<br />
come si sa la flogosi è un’arma a doppio taglio; sono così importanti i<br />
sistemi di controllo:<br />
2) coagulazione - fibrinolisi<br />
C1 inattivatore: il deficit causa una sindrome acuta (mediamente grave) che è<br />
l’angioedema ereditario o di Quinke, che risulta collegato<br />
con le chinine.<br />
DAF (Decay Accellerator Factor): il suo deficit giustifica la così detta anemia<br />
parossistica notturna: pazienti che la mattina hanno urine rossastre<br />
(a volte) e risultano anemizzati. In questo contesto avverrebbe una<br />
relativa ischemia a livello periferico, causata da mal distribuzione<br />
dell’ossigeno… l’acidità locale andrebbe ad attivare il complemento<br />
provocando emolisi.<br />
3) kinine: il frammento del X<strong>II</strong> fattore, detto X<strong>II</strong>f, attiva l’High Molecolar Weight Chinogen (HMWC),<br />
che si trasforma in bradichinina (che ha un peso minore). E’ interessate come sia la plasmina<br />
che la callicreina producano poi la bradichinina, che è un mediatore importante.<br />
Il C1 inattivatore controlla anche, in questo settore, l’attivazione della plasmina, entrando<br />
quindi anche in questo contesto (impedisce la prod. di bradichinina). Inoltre il fattore X<strong>II</strong>, in<br />
veste pro infiammatoria, può essere attivato da callicreina e plasmina.<br />
- callicreina:<br />
- bradichinina<br />
⊕ PMN<br />
fattore X<strong>II</strong> ⇒ X<strong>II</strong>a<br />
plasminogeno ⇒ plasmina<br />
vasodilatazione<br />
permeabilità<br />
contrazione muscoli lisci<br />
dolore<br />
Ci sono due tipi di recettori per queste chinine:<br />
1) B2 (costitutivo) ⇒ dopo un po’ si adatta, si<br />
de sensibilizza<br />
2) B1 (inducibile) ⇒ indotto dall’IL-1, il<br />
mediatore più importante della flogosi: in questo caso non c’è desensibilizzazione,<br />
permettendo alle kinine di agire in senso infiammatorio.<br />
Mastcellule e Basofili<br />
La mastcellula è attivabile praticamente da qualsiasi tipo di danno:<br />
1) traumi: il rosso di uno schiaffo p.es è dovuto da una stimolazione di questo tipo: è dovuto alla<br />
degranulazione<br />
2) stimoli termici: (variazioni di temperatura): basta poco, p.es gli allergici anche solo uscire a correre,<br />
specialmente nelle mezze stagioni, può provocare attacchi d’asma per attivazione<br />
fisica dei mastociti polmonari<br />
3) mediazioni nervose: p.es la sostanza P; teoricamente questo comporterebbe la possibile attivazione di<br />
questi meccanismi anche solo per vie nervose.<br />
4) IgE: nelle allergie si legano prematuramente alle mastcellule (recettori ad alta affinità), pronte a de<br />
granulare appena compare l’Ag<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 26
Quindi poi le mastcellule rilasciano praticamente quasi tutti i mediatori dell’infiammazione, provocando tra<br />
le altre cose anche la contrazione delle cellule muscolari lisce (che nei bronchioli terminali vuol dire: asma).<br />
Eosinofili<br />
Possono essere attivati da:<br />
1) immunocomplessi<br />
2) prodotti delle mastcellule<br />
3) prodotti dei linfociti (IL-5)<br />
La loro funzione è simile a quella di un neutrofilo, con una potenza decisamente maggiore (40-50 volte<br />
tanto), per agire contro agenti nocivi di dimensioni maggiori dei batteri:<br />
- elminti<br />
- vermi<br />
- protozoi<br />
Questa “potenza di fuoco” dipende da:<br />
• Eosinofiloperossidasi (molto più potente della mieloperossidasi)<br />
• Esoinophil Basic Protein<br />
• PAF<br />
c’è inoltre, da parte di queste cellule una funzione detossificante, dovuta a elementi quali<br />
• perossidasi (di nuovo)<br />
• Arilsulfatasi (⇒ degrada i leucotrieni)<br />
• Istaminasi (⇒ degrada l’istamina). Questo fa si che una ipereosinofilia negli allergici ha la funzione<br />
di spegnimento della reazione allergica e protezione dall’eccessiva flogosi.<br />
Cellule Endoteliali<br />
Presentano molteplici recettori, che le rendono sensibili a praticamente ogni stimolo di tipo infiammatorio:<br />
a. istamina<br />
b. serotonina<br />
c. PG<br />
d. LTC4, D4<br />
e. trombina<br />
f. fibropeptidi<br />
g. IL-1<br />
h. TNF<br />
Che mediano quindi numerose funzioni:<br />
1) produzione di NO, PGl2 ⇒ vasodilatazione<br />
2) permeabilità ↑<br />
3) espressione di molecole di adesione per i leucociti e di attivazione: PAF, IL-8 (PMN, Eos,<br />
Monociti, Linfociti)<br />
4) APC: espressione di MHC<strong>II</strong><br />
5) produzione di IL-1, IL-6 ⇒ effetti sistemici della flogosi<br />
6) espressione di TISSUE FACTOR ⇒ coagulazione e altre funzioni pro coagulanti (PAF, PAI-1, wWF)<br />
7) produzione di fattori di crescita per fibroblasti (ED-FGF)<br />
8) neoangiogenesi per stimolazione TGF-β, FGFβ, G-CSF, GM-CSF, VEGF<br />
A livello micro circolatorio si ha sempre la possibilità di una anastomosi tra l’arteriola e la venula che<br />
permette di escludere quello specifico microcircolo. Sostanzialmente l’arteriola in afferenza genera una meta<br />
arteriola, che rappresenta un canale preferenziale che descrive una “U”, come una racchetta: tra il ramo<br />
ascendente e quello discendente c’è tutta una serie di collegamenti formati dai capillari veri. Tutto questo<br />
sistema è controllato da sistemi di cellule muscolari lisce che hanno la proprietà appunto di poter escludere il<br />
circolo - cfr: sindorme di Raynaud, pag.1 di <strong>patologia</strong> <strong>generale</strong> I.<br />
Alterazioni Emodinamiche<br />
Sono eventi successivi…<br />
1) vasocostrizione arteriolare (incostante): dovuta all’azione diretta di elementi rilasciati dalle<br />
mastcellule (Ca, 5HT…)<br />
2) vasodilatazione: arteriole, capillari aumento del flusso ematico.. (NO, PGI2…)<br />
3) stasi: dilatazione ed aumento della permeabilità di capillari e venule ⇒ essudazione e emarginazione,<br />
migrazione leucocitaria.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 27
Extravasazione di Leucociti & Monociti<br />
Già le variazioni del flusso ematico aumentano le possibilità di contatto leucociti - endotelio (che normalmente<br />
non sono in contatto). Come si sa la diapedesi viene preceduta da diverse fasi: rolling, spreading, adesione,<br />
tutte mediate da diverse molecole di adesione. In questo modo il leucocita è in grado di oltrepassare<br />
l’endotelio senza minarne l’integrità. In particolare durante il rolling vengono rilasciati dall’endotelio fattori<br />
come l’IL-8 e il PAF che provocano un cambio di conformazione (l’attivazione) di una IgSF CAM 10 nota<br />
come ICAM (Intra Cellular Adhesion Molecule).<br />
LAD: Leukocyte Adhesion Deficency: malattia di tipo pediatrico, dove i soggetti presentavano<br />
- stomatiti<br />
- polmoniti<br />
- lesioni necrotico emorragiche<br />
- rallentamento nella guarigione delle ferite<br />
- leucocitosi neutrofila (20'000+)<br />
Questa sindrome si caratterizza per deficienze delle subunità delle integrine, che mediano la fase di<br />
spreading ed adesione: CD18 o catenaβ delle integrine 11 (LADI). C’è anche un LAD<strong>II</strong> dovuto alla<br />
mancanza di zuccheri Lewis X sialilati (sLe x ), dove però non si hanno problemi d’infezione, ma<br />
piuttosto di tipo neurologico, non dovuti a mancanza di migrazione leucocitaria.<br />
rolling spreading adesione diapedesi<br />
leucociti ⇒ CD15 (sLe x ) integrine<br />
PECAM-1<br />
endotelio ⇒ E/P-selectine<br />
ICAM-1 PECAM-1<br />
Sono proprio gli stimoli infiammatori che stimolano inizialmente l’espressione di elementi come le<br />
P selectine, che, accumulati a livello intracellulare vengono esposti per c.a 12 ore ed entro 10 minuti dallo<br />
stimolo. Altre, come le ICAM-1 / VCAM-2, che rimangono esposte fino a 2-3 giorni.<br />
Se inizialmente si ha il richiamo di neutrofili, cambiando col tempo il profilo d’espressione delle molecole<br />
di superficie si ha il richiamo di monociti, mediato sempre da CD11/18, ed anche dal VLA-4 (un’integrina),<br />
ligando per il VCAM-1 (Vascular Cell A.M.), coppia di molecole in grado di mediare sia il rolling sia<br />
l’adesione del monocita. Si è dimostrato come questi recettori, una volta stimolati, portino ad aumento di<br />
Ca 2+ intracellulare, utile per provocare la contrazione (⇒ parziale retrazione) delle cellule endoteliali, che<br />
permette di creare lo spazio utile al passaggio delle cellule monocitiche.<br />
I linfociti inoltre esprimono tutta una serie di altre molecole (come le L selectine) che gli permettono di<br />
accedere in diversi distretti, tra cui anche i linfonodi periferici per quanto riguarda quelli naive.<br />
Questo permette tutta una serie di fenomeni di ricircolazione linfocitaria a livello di organi linfoidi (dalle<br />
placche di Peyer ai linfonodi), che è di tipo altamente specifico (in una determinata ansa intestinale p.es si<br />
troverà una popolazione di linfociti ben diversi di quelli che possono risultare a livello cutaneo).<br />
10 Ig Super Family Cell Adhesion Molecule: ha domini Immunoglobulinici.<br />
11 le integrine legano le ICAM, e sono formate delle due catene α e β rispettivamente CD11 e CD18.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 28
Le chemochine sono, come suggerisce il nome citochine con funzione chemotattica data dal gradiente<br />
chimico con cui queste sono presenti nell’ambiente. Si trovano a livello dell’endotelio, e il capostipite (la<br />
prima ad essere individuata) è proprio l’IL-8. Le chemochine si distinguono in base alla posizione delle<br />
cisteine, in particolare si descrivono CC chemochine, che non presentano altri AA tra le cisteine, e le CXC<br />
che presentano l’interposizione di altri AA. Anche le cellule tumorali possono esprimere molecole di questo<br />
tipo, fattore che produrrà un’alta capacità di dare metastasi a causa del tropismo per i capillari linfatici che<br />
questi recettori conferiscono.<br />
Fagocitosi<br />
E’ un’azione mediata spesso da opsonine:<br />
1) IgG1, IgG3 ⇒ FcγR<br />
2) C3b del complemento ⇒ C3bR<br />
3) LPS-BP (permette all’LPS di venir eliminato di routine) ⇒ CD14 e TLR-4 (corecettore e recettore)<br />
Il leucocita ha quindi legato il batterio, e l’ingestione avviene grazie alla formazione di una vescicola di<br />
endocitosi. L’uccisione del microrganismo fagocitato avverrà grazie a meccanismi battericidi O2 dept o<br />
meno:<br />
O2 Indipendenti<br />
Nel fagosoma (vescicola di endocitosi) vengono riversati diversi enzimi idrolasici<br />
- catepsina<br />
- proteasi<br />
- elstasi<br />
- lisozima<br />
- lattoferrina<br />
- metallo proteasi<br />
O2 Dipendenti: dipendenti dalla NADPH ossidasi, che catalizza la formazione di<br />
superossido anione a partire dall’ossigeno: 2O2 ⇒ 2O2 - , quindi la superossido dismutasi<br />
catalizza la seguente reazione: 2O2 - ⇒ O2 + H2O2 (acqua ossigenata). L’H2O2 verrà utilizzata<br />
dalla mieloperossidasi, o verrà smaltita dalla perossidasi. Il NADPH verrà quindi rigenerato<br />
nel ciclo dei pentosi, utile contemporaneamente a rigenerare il glutatione, che è un anti<br />
ossidante.<br />
Nb: Il favismo è una malattia che si genera dalla mancanza della G6P-DH, che porta ovviamente ad una<br />
minor quantità di glutatione ridotto. Questo tipo di mutazione protegge dalla malaria (il globulo rosso è<br />
meno resistente, e il plasmode non riesce a prendere piede nell’organismo).<br />
L’acqua ossigenata quindi, in presenza di un alogeno (più frequentemente il cloro) forma ipoclorito<br />
(varechina) che viene quindi utilizzato contro i batteri. Il deficit di mieloperossidasi non è particolarmente<br />
debilitante, evidentemente la eosinofiloperossidasi va a supplire la mancanza con facilità.<br />
Un’altra via importante è la formazione di NO (ossido nitrico), sempre dipendente dal NADPH.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 29
3) Fibrinosa: se nell’essudato sieroso si trova anche la firbina. Questo crea ovviamente dei fenomeni<br />
adesivi (p.es a livello pleurico tra la pleura e le pareti, oppure sulle anse intestinali) 12 .<br />
Questo provoca un “inizio di cicatrici”, anche se non c’è ancora collagene. All’E.O. del<br />
polmone si possono riscontrare sfregamenti pleurici 13 . La terapia è costituita<br />
dall’attivatore del plasminogeno (TPA) a livello pleurico, con ottimi risultati.<br />
Un esito da flogosi fibrinosa era costituto dalle semimembrane della difterite.<br />
Nell’epatizzazione polmonare data da polmonite batterica si riscontra proprio la<br />
presenza (tra le altre cose) di fibrina a livello alveolare, che contribuisce al quadro<br />
anatomopatologico (se ne parlerà più avanti)..<br />
4) Catarrale: il catarro sarebbe formato da essudato (muco) arricchito di cellule epiteliali di<br />
sfaldamento, che si realizza in corso di<br />
reazione allergica<br />
agenti fisici<br />
agenti chimici<br />
infezioni virali<br />
Quando si comincia a vedere muco che varia il colore (tende al verdino, al grigio), è<br />
segno di una sovra infezione batterica, che darà luogo ad una manifestazione “muco<br />
purulenta”.<br />
5) Purulenta: è data da cocchi piogeni, e genera pus. L’infiammazione purulenta è definita<br />
dall’extravasazione di PMN neutrofili, non per forza dalla presenza batterica.<br />
Se l’essudato ha una consistenza tipica da dare evidenza clinica si ha pus, risultato di<br />
una colliquazione, che è sterile, ma può contenere microrganismi anaerobi, il pH<br />
inoltre è acido...<br />
PMN neutrofili<br />
detriti cellulari<br />
degradazione della sost. fondamentale<br />
La reazione di Rivalta è obsoleta ma valida: prendendo una gocciolina di pus,<br />
mettendola in aceto, si forma una nubecola, dovuta alla precipitazione di proteine<br />
mucopolisaccadiche. Questo può essere utile p.es in paesi del terzo mondo, dove non<br />
c’è la disponibilità di un laboratorio.<br />
Dipendentemente dalle modalità d’infezione, dalla sede, dal tipo di ferita (una ferita<br />
aperta drenerà automaticamente il pus senza incistarlo), ma soprattutto dalla<br />
responsività del’organismo, si avranno diverse dinamiche:<br />
Ascesso: è un qualcosa più legato alla cronicizzazione dell’evento flogistico / infettivo;<br />
tipica è l’infezione dovuta ad una puntura intramuscolare. Viene ad essere formato da<br />
una raccolta di PUS neo formata, circondata da una membrana detta “piogenica”:<br />
» PMN intatti<br />
» fibrina<br />
» fibroblasti<br />
Questi ultimi (i fibroblasti) vanno a formare una forma di riparazione connettivale: si<br />
dispongono a gruppi, si dice a “palizzata”, provocando una proliferazione micro<br />
vasale (abbondante emorragia andando a tagliare), in presenza anche di monociti.<br />
Un caso particolare è rappresentato dall’osso, come nelle fratture esposte: se, come<br />
succede, questo non può essere medicato e pulito accuratamente in tempi rapidi, tutto<br />
l’osso viene ad essere circondato da una membrana piogenica, diventando quasi un<br />
corpo esterno. Questi inclusi nella capsula, e la capsula piogenica stessa vengono detti<br />
nell’insieme sarcofagi (da distinguere dalle cellule necrotiche senza nucleo.<br />
Flemmone: raccolta di materiale purulento non circoscritta, che tende ad infiltrare i tessuti<br />
seguendo le vie di minore resistenza (p.es tra le fasce muscolari, nel sottocutaneo…).<br />
12 In chirurgia si parla di piastrone: aree dove il fibrinogeno può uscire tranquillamente e dare questo fenomeno. Può<br />
originare anche da una semplice appendicite, e va risolta, in quanto può generare anche fenomeni di aderenze, stenosi e<br />
deviazioni delle anse… quindi va risolta.<br />
13 che si distingue da quello bronchiale in quanto rimane costante anche dopo un colpo di tosse.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 31
2) sintesi di ormoni: ACTH, cortisone… ricordiamo la sindrome di Waterhouse Friederichsen<br />
3) neutrofilia: nell’ambito della leucocitosi infiammatoria, prevalgono nell’infiammazione acuta i<br />
neutrofili. Si arriva a 9-10mila leucociti, dove le proporzioni rimangono grossomodo<br />
costanti (quindi comunque i neutrofili prevalgono). E’ l’effetto dell’IL-1 a livello<br />
midollare.<br />
4) aumento della VES: anche considerando che in infiammazione cala l’albumina, giustifica il fatto che<br />
la VES aumenti.<br />
5) attivazione delle Lipasi: mediata della presenza dei macrofagi a livello del tessuto tumorale, il<br />
motivo per cui si dimagrisce in fase di malattia. I lipidi saranno<br />
metabolizzati dal fegato che in questa fase ha bisogno di substrati energetici<br />
(e che accederà anche al catabolismo proteico). Questo alla lunga può<br />
portare ad un dimagrimento estremo, definito cachessia.<br />
6) prod. epatica delle proteine della fase acuta: la produzione è stimolata principalmente da TNFα e<br />
IL1, ma anche da altri (IL6, IFNγ, IL-11…) .. l’entità della risposta è anche modulata.<br />
L’IFNγ testimonia come anche un’infezione virale sia in grado di scatenare una risposta<br />
sistemica; sappiamo inoltre come queste citochine sono in grado di stimolarsi a vicenda..<br />
a. PCR<br />
b. Amiloide A (poco importante nella clinica quotidiana)<br />
c. proteine del complemento<br />
d. proteine della coagulazione<br />
e. inibitori delle proteasi (lo avevamo visto nella fagocitosi, nella digestione della MEC da<br />
parte dei leucociti.. inibiscono gli effetti negativi dell’infiammazione)<br />
f. metallo proteine (sono anti ossidanti fondamentalmente)<br />
g. LPS-BP (che permette di ripulire l’LPS tramite il CD14)<br />
h. serumamyloid P component (cfr. amiloidosi)<br />
i. proteine della fase acuta negative: sono proteine che calano in questa situazione, l’albumina<br />
soprattutto<br />
7) ipotensione & Shock: è mediato sempre da questi mediatori, ma è tipico della sepsi, nello specifico,<br />
ed è un evento grave e non frequente.<br />
Sintomi tipici dell’influenza sono debolezza e mal di schiena: la giustificazione è un effetto diretto<br />
dell’IFNγ, che viene a localizzarsi anche a livello delle articolazioni, per cui stimoli anche normali e limitati<br />
scatenano molto facilmente reazioni infiammatorie locali. Si tratta di nevriti, sostanzialmente compressioni<br />
delle radici spinali su basi edematose.. ovviamente è un fenomeno contenuto, ma comunque l’origine è<br />
questa… il dolore nevritico (come la sciatica), può essere molto forte, e dipende dalla sofferenza nervosa<br />
determinata da una qualche compressione. Siccome la sintomatologia dipende da una molecola prodotta dai<br />
linfociti, evidentemente anche una leucemia linfatica può quindi dare questa sintomatologia, che è molto<br />
precoce. Inoltre, quello che si nota inizialmente nelle leucemie, è una anemizzazione. Quindi il paziente è<br />
doppiamente debole. L’astenia è altresì data da una ipocalcemia, soprattutto nei bambini.<br />
Diciamo che l’infiammazione è combattuta a livello locale da numerosi elementi, in primis l’IL-1Ra, che è<br />
particolarmente prodotta p.es da individui allenati, che risentono enormemente meno di stimoli fisici stressorii<br />
derivanti da una intensa attività.. Anche il meccanismo dello shedding ha una certa importanza, soprattutto nel<br />
caso di infezioni (p.es da HIV) per quanto riguarda l’IFNγ… diciamo che i meccanismi di contenimento in<br />
genere precedono e prevalgono sulle citochine infiammatorie, a testimoniare l’importanza di questi<br />
meccanismi, che valgono per tutte le citochine, per cui sono rilevabili recettori trappola e solubili qualche<br />
giorno prima dello scatenarsi della manifestazione clinica.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 33
Effetti Biologici dell’LPS (setticemia)<br />
1) CID: mediata principalmente dall’attivazione endoteliale / piastrinica:<br />
a. tissue factor ⇒ V<strong>II</strong>a: prodotto dalle cellule endoteliali, stimolate direttamente dall’LPS<br />
b. PAF<br />
c. fattore X<strong>II</strong><br />
2) attivazione delle piastrine, dovuta anche ai monociti / PMN circolanti<br />
a. coaguli della CID<br />
b. vasodilatazione: tramite la serotonina. Provoca congestione venosa…<br />
c. aumento della permeabilità<br />
3) monociti circolanti / PMN:<br />
a. PG, LT<br />
b. IL-1, TNF<br />
4) complemento<br />
a. ⊕ via alternativa<br />
b. C3a, C5a↑: effetto pro-flogistico<br />
5) IFNγ: è sempre coinvolto<br />
6) ⊕ipofisi: si ha la produzione di ACTH e βendorfine (che risultano essere vasodilatatorie)<br />
Nell’insieme, tutti questi eventi portano ad ipotensione e quindi ipoperfusione tissutale, che porta allo shock.<br />
La mortalità di questo stato è c.a del 50%, e sono state tentante numerose vie, anche grazie a inibitori di questa<br />
riposta sistemica, che però non sembrano migliorare la prognosi. In questo tipo di risposta, un ruolo davvero<br />
importante è svolto da PMN, monociti e complemento, che vanno ad amplificare il processo, che se fosse<br />
solo per la tossina batterica sarebbe molto meno marcato.<br />
Yarish Hirsch - Heimer reaction: è una reazione che è stata in particolar modo descritta nella leptospirosi.<br />
Sono leptospire sensibilissime agli antibiotici, che risultano comunque<br />
poco efficaci: nel disgregarsi si hanno tutta una serie di residui batterici a<br />
partire dai peptidoglicani. Tutti i frammenti scatenano una risposta<br />
sistemica dai PMN che attuano una esocitosi massiva, che può portare il<br />
paziente in shock.<br />
A seconda dell’aggressività della terapia antibiotica, comunque si espone il SI ad una stimolazione massiccia,<br />
per cui sarebbe opportuno spesso ridurre le dosi e prolungare il periodo di trattamento.<br />
Patologia da Citochine<br />
1) IFNγ, TNF, IL-1 ⇒ shock, cachessia neoplastica, CID (trombosi)<br />
2) PDGF ⇒ provoca la proliferazione della media nei traumi vasali<br />
3) IL-2 ⇒ aumenta la permeabilità vasale; era stata tentata come terapia allo shock per ottenere le LAK<br />
(cellule efficaci nei confronti di tumori solidi), ma gli effetti permeabilizzanti provocavano<br />
edemi cerebrali fulminanti e polmonari (Capillary Leakage Syndrome)<br />
4) TGFα / β ⇒ sarebbe responsabile degli eventi cirrotici, mediante effetti mitogeni e pro-collagenici<br />
nelle cellule epatiche<br />
5) TNF (cellule dendritiche cutanee) ⇒ provocherebbe psoriasi, mediata dall’IL-8 prodotta quindi nei<br />
cheratinociti<br />
Utilizzo terapeutico di citochine<br />
1) IL-2 ⇒ evoluzione, appunto delle NK in LAK, prestando attenzione all’effetto secondario.<br />
2) IFNα ⇒ sarebbe utilizzato nelle Hairy Cell Leukemia (porta a guarigione)<br />
3) α, β, γ IFN ⇒ malattie virali, l’IFN γ anche contro tumori solidi e parassiti endocellulari<br />
4) CSFs ⇒ in pazienti con leucemia, dopo aver attuato una terapia con antiblastici per ripulire il midollo,<br />
si può stimolarlo tramite CSF.<br />
5) IL-11 ⇒ attiva i megacariociti, e si somministra nella piastrinopenia<br />
6) EPO ⇒ nel caso di anemie<br />
7) Ab monoclonali / peptidi anti TNF / IL-1 ⇒ per combattere lo shock<br />
8) TGFβ 1 ⇒ artrite acuta / cronica: limita al formazione di materiale cicatriziale.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 34
Processo Riparativo<br />
Mediato normalmente dai macrofagi, consiste di alcune fasi:<br />
1) detersione dei residui cellulari<br />
2) rigenerazione degli elementi parenchimali: ci sono ovviamente tessuti con maggior o minor capacità<br />
ripartiva. Questo fatto è comunque indotto dai macrofagi.<br />
Si basa su fattori come l’EGF.<br />
a. necessità della LB: il tessuto epiteliale ha bisogno di una trama su cui appoggiarsi, che è<br />
una situazione sine qua non per la proliferazione cellulare<br />
b. inibizione da contatto: quando le cellule si trovano giustapposte, facilmente visualizzabile in<br />
vitro, avviene anche in vivo<br />
c. caloni: sono sostanze antimitotiche contenute nei tessuti; quello che si è visto è che<br />
eseguendo una resezione ottimale di una parte del fegato (senza residui), si dà per<br />
scontato che ci sarà una ricrescita prima eccessiva e poi un ridimensionamento, per<br />
riottenere un fegato delle giuste dimensioni. Si è provato a collegare a livello<br />
vascolare due animali di cui uno con la transezione epatica: quello che succedeva era<br />
che cresceva anche quello dell’animale sano. Quello che si è pensato è che il fegato,<br />
oltre a rilasciare (se resecato) fattori di crescita, rilasci anche elementi inibitori alla<br />
crescita, che vengono a mancare quindi se il fegato è transecato. Si pensava all’inizio<br />
che si trattasse di elementi noti come “caloni”, invece si sono rivelati essere regolatori<br />
di fattori proliferativi dei vasi (antiangiogenetici: vd.sotto).<br />
Si nota in chirurgia, che spesso all’atto di una tumorectomia, si ha un’esplosione<br />
della metastasizzazione. Anche questo tipo di fenomeno oggigiorno è spiegato con i<br />
fattori anti angiogenetici.<br />
3) ricostruzione connettivale: il processo fibrotico che in ultima analisi va a “riempire gli spazi”, o a<br />
ricostruire comunque gli elementi connettivali. Di nuovo il macrofago è<br />
la cellula che attira ed attiva i fibrociti. Laddove si formi materiale<br />
cicatriziale si ha un impedimento della rigenerazione degli elementi<br />
parenchimali. I cheloidi si hanno in corrispondenza di una ferita, anche<br />
chirurgica, e sono un’estrema ipertrofia della cicatrice. Evidentemente<br />
c’è una predisposizione, ma con le iniezioni di cortisone si ha una buona<br />
risposta del paziente.<br />
La cicatrizzazione dipende da:<br />
distretto (viso ≠ pianto del piede)<br />
contatto dei margini (una ferita in una sede di continuo movimento guarirà<br />
difficilmente)<br />
persistenza della noxa (dolore) / corpi estranei (ovviamente vanno rimossi)<br />
apporto ematico<br />
vit.C, cortisone (rispettivamente stimolano e inibiscono la cicatrizzazione)<br />
4) Angiogenesi: indotta da diversi elementi:<br />
a. VEGF agisce come fattore chemiotatitco per le cellule endoteliali (che formando<br />
inizialmente cordoni, poi si cavitano per dare luogo ai vasi).<br />
IFN / FGF vanno ad inibire questo elemento<br />
talidomide: farmaco anti-nausea con effetti teratogeni in grado di procurare<br />
focomelia, cioè l’assenza delle braccia e il collegamento diretto manospalla.<br />
La sua funzione, attraverso l’IL-6, sarebbe quella di inibire il<br />
VEGF, quindi è un anti angiogenetico.<br />
b. stimoli ipossici e/o ipoglicemici<br />
c. angiopoietina.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 35
d. HIF: Hypoxia Induced Factor (che poi indurrebbe il VEGF). In questo contesto sono importanti:<br />
p53 ⇒ ⊕ enzimi di degradazione dell’HIF<br />
pr39 (macrofagi) ⇒ enzimi di degradazione dell’HIF. Di nuovo i macrofagi<br />
sono in grado di guidare l’operazione “liberando” l’attività dell’HIF.<br />
Questo è importante in due situazioni:<br />
- nei trapianti: c’è tutta una grandissima attività medico-scientifico-clinica al<br />
riguardo del trapianto di isole pancreatiche nei diabetici.<br />
Tendenzialmente vengono impiantate nel rene… diciamo che una<br />
volta impiantate, queste hanno necessità di una neo<br />
vascolarizzazione; è così che entrano in gioco fattori come l’HIF.<br />
- nei tumori: normalmente i tumori non utilizzano tanto l’ossigeno, ma tendono a<br />
sfruttare la glicolisi. La situazione di questi tumori cambia<br />
radicalmente con la possibilità d’irrorazione. Questo aspetto è critico<br />
nel passaggio tra una situazione benigna e maligna di una neoplasia.<br />
Quello che si è visto nella pratica è che l’inibizione della<br />
neoangiogenesi sembra avere un buon effetto sulle metastasi.<br />
Inoltre, bloccare l’angiogenesi a livello di un tumore già sviluppato,<br />
terapeuticamente non porta a nulla, ma almeno impedendo l’ulteriore<br />
espansione si riduce la componente collegata al dolore da<br />
compressione dei nervi.<br />
5) Il tessuto di granulazione è il classico tessuto che si viene a formare sotto un’escara insorta da una<br />
ferita da sbucciamento. Sostanzialmente fibroblasti (FGF), macrofagi, qualche singolo PMN, presenza<br />
di capillari…<br />
Tra i fibroblasti si riconoscono:<br />
- fibrociti: sono inclusi nei tessuti (p.es i tendini), tipicamente quiescenti.<br />
- fibroblasti attivi: sono in attiva proliferazione, producono collagene<br />
- neofibroblasti: si confondono quasi fenotipicamente con una cellula muscolare<br />
liscia<br />
6) Rigenerazione Nervosa: NGF.. diciamo che a livello periferico non ci sono grosse difficoltà di<br />
rigenerazione; quest’attività è diretta dalle cellule di Schwann e dalla<br />
laminina, che provocano la generazione di un cono di crescita. Questi<br />
stimoli derivano direttamente dallo stroma.<br />
7) Guarigione delle ferite<br />
I intenzione: ferite nelle migliori condizioni, senza contaminazione, perdita di<br />
tessuti, margini ravvicinati e non mobili<br />
<strong>II</strong> intenzione: tutto l’opposto, ferite contaminate e con grosse alterazioni tissutali;<br />
guarirà comunque, ma molto lentamente e con molta cicatrice<br />
<strong>II</strong>I intenzione: quando la ferita viene presa in considerazione dal chirurgo, che attua<br />
una ripulitura e attua i punti di sutura, o gli steri strip.<br />
Il TGFβ sia favorisce la cirrosi sia viene data come terapia nelle artriti: diciamo che gioca un ruolo nelle<br />
fibrosi (soprattutto in quella renale), nell’ipertensione arteriosa, anche. Questi effetti opposti derivano<br />
probabilmente dal restante contesto di citochine/segnalatori cellulari..<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 36
§<br />
Istoflogosi o Flogosi Cronica<br />
Come la flogosi acuta può terminare con la cicatrizzazione e la guarigione;<br />
Classificazione delle istoflogosi<br />
a. Persistenza (cronicizzazione) di una flogosi purulenta<br />
b. Flogosi Croniche Aspecifiche: Coesistenza / evoluzione di angioflogosi (con PMN) e flogosi<br />
granulomatose (monociti infiltrati)<br />
c. Istoflogosi P.D.: si presentano granulomatose “ab inizio”<br />
Ci sono diversi modi di cronicizzare da parte di una reazione infiammatoria, e molto dipende dal modo di<br />
reagire dell’ospite..<br />
Deficit Leucocitari<br />
1) di numero<br />
terapie cortisoniche ad alte dosi<br />
chemoterapia (tumori, trapianti, malattie autoimmuni)<br />
HIV<br />
malattie virali (morbillo p.es): riducono la difesa mediata dai granulociti, quindi<br />
espone in particolare alle minacce batteriche.<br />
radiazioni<br />
malnutrizione / mal assorbimento: si dice che chi è mal nutrito è anergico; si<br />
avranno numerose patologie collegate ad infezioni tutte diverse<br />
tra di loro.<br />
2) di migrazione<br />
Diabete: il paziente va incontro a tipi d’infezione (ascessuale, pus..) molto più<br />
grave di un individuo normale.<br />
LAD-1<br />
Chemiotassi: associata ad altri difetti: Chediak Higashi (difetti citoscheletrici:<br />
sia di migrazione, fagocitosi, rilascio di granuli…)<br />
3) di fagocitosi<br />
anemie emolitiche: i globuli rossi vanno incontro a distruzione precoce, si parla di<br />
emolisi. Tutti i residui di globuli rossi vengono fagocitati dai<br />
macrofagi della milza, che sono “intasati” da materiale<br />
eritrocateretico, risultando poi insufficienti a svolgere la loro<br />
funzione antibatterica. Nei pazienti anemizzati inoltre<br />
l’organismo ha come primo obbiettivo di restaurare i globuli<br />
rossi, con minor produzione di leucociti.<br />
4) mancanza di sistemi microbicidi<br />
CGD (Chronic Granuloumatose Disease):<br />
deficit di C5-8: infezioni da Neisserie<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 37
Cronicizzazione di flogosi Purulenta<br />
1) osteomieliti, che si vedono p.es in seguito a fratture esposte. Il problema è che la struttura stessa<br />
dell’osso, soprattutto nella componente spugnosa, favorisce l’annidarsi e il nascondersi<br />
dei batteri. I leucociti avranno estrema difficoltà d’inoltrarsi in questi anfratti, e questa<br />
forma di istoflogosi può portare a malformazioni persistenti.<br />
2) ascesso: complesso, si ha un ispessimento della membrana piogenica, fino a formare anche una cisti.<br />
⇒ cisti: è l’evoluzione dell’ascesso, può anche essere quasi sterile, un modo di isolare il<br />
materiale di necrosi<br />
3) fistola: è una comunicazione patologica tra due domini (due cavità preformate, una cavità e<br />
l’esterno…) contente regolarmente materiale purulento. Tutto il tramite fistoloso avrà<br />
caratteristiche piogeniche, e rappresenterà un richiamo di granulociti, monociti, causerà<br />
proliferazione di fibroblasti.. donando al tutto una forma altamente persistente, anche in caso<br />
di svuotamento, che vede comunque la persistenza di batteri che nel tempo possono<br />
riaccendersi, dando di nuovo colliquazione, pus…La fistola va completamente assisa.<br />
4) favo: già visto, il raccogliersi di foruncoli in una lesione che raggiunge strati profondi della cute.<br />
Tipi di Istoflogosi<br />
1) Flogosi Cronica Aspecifica: è caratterizzata dalla presenza di<br />
fibrina<br />
edema<br />
PMN<br />
+<br />
tessuto<br />
di<br />
granulazione<br />
Ulcera Peptica Cronica: l'helicobacter pylori si annida in superficie dando vita:<br />
a. ad un processo di angioflogosi con necrosi<br />
b. ad un processo di istoflogosi caratterizzato dalla presenza di:<br />
- linfociti al di sotto del processo angioflogistico<br />
- fibroblasti indotti dai linfociti<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 38<br />
+<br />
macrofagi<br />
linfociti<br />
plasmacellule<br />
eosinofili<br />
Ulcera venosa cronica: si determina in genere per la distruzione di valvole e strutture venose, che<br />
determina uno scarico del sangue venoso, formando una stasi ematica,<br />
tipicamente a livello di aree declivi (caviglia). A questo punto una qualsiasi<br />
lesione, se non si favorisce la circolazione (⇒ l’arrivo in sede di cellule<br />
immunocompetenti) porta inevitabilmente ad una cronicizzazione.<br />
Ulcere gengivali da protesi dentaria<br />
Apiciti: sarebbero granulomi dentari, che interessano l’apice della radice. Molto frequentemente in<br />
seguito ad una carie si ha l’infezione del dente, per cui si ha una segregazione batterica<br />
mediamente silente, contro la quale l’organismo rivolge la sua difesa (vd.sopra), per cui<br />
asportando queste formazioni si nota proprio un quadro di flogosi cronica aspecifica.<br />
Pielonefrite Cronica: da una “normale” infezione delle vie urinarie, si ha una sintomatologia<br />
infettiva renale ricorrente, che sulla lunga distanza continua a tornare, fino a<br />
portare ad una definitiva fibrosi renale. Questi pazienti devono quindi sottoporsi<br />
a terapie antibiotiche di lunghissima durata (anni)<br />
Cirrosi Alcolica: non è settica, ma di fatto risulta cronica, per le modalità con cui avviene<br />
l’intossicazione<br />
Pancreatite Cronica: forma relativamente più benigna di quella acuta, di origine molto<br />
probabilmente settica, la terapia antibiotica dev’essere pesante ed immediata,<br />
senza la quale si assiste alla persistenza della forma cronica nel pancreas, che<br />
poco a poco viene danneggiato irreparabilmente.
2) Granulomi: si ricordi la presenza tissutale di monociti, che divenendo macrofagi si specializzano: cellule<br />
di Kuppfer, Langerhans, macrofagi alveolari, osteoclasti, microglia, istiociti (connettivo)…<br />
E’ fondamentale tenere presente che la flogosi granulomatosa si rivolge fondamentalmente<br />
ad agenti patogeni endocellulari, contro i quali l’organismo è relativamente inerme, perché i<br />
patogeni intracellulari sono assolutamente indifferenti a tutto il SI (Ab, linfociti T…), anche<br />
se la cellula ospite è un macrofago, p.es.<br />
priming: quello che fanno queste cellule (monociti e macrofagi) è di aumentare le loro capacità<br />
battericide: si tratta del fenomeno del priming, preparazione:<br />
la presenza di fattori infiammatori in presenza di leucociti determina in esso più che una degranulazione<br />
all’esterno, una forma di sintesi proteica rivolta a sistemi battericidi<br />
Può trattarsi di mediatori come il TNF, γ IFN, LPS, GM-CSF… che non in quantità esagerate,<br />
possono portare ad una attivazione del macrofago, che vede incrementate la produzione di<br />
reattivi, la funzione di APC, la produzione di NADPH ossigenasi, ecc ecc..<br />
trigger: in questa situazione, un secondo stimolo (trigger) porta alla distruzione del batterio:<br />
- fattori del complemento<br />
- materiali fagocitabili<br />
- prodotti batterici<br />
Nb: Il trigger, senza priming non sarebbe altrettanto efficace, proprio in virtù di quei meccanismi che<br />
tendono normalmente a contenere i meccanismi pro-infiammatori, con funzioni protettive<br />
dell’organismo. Nei granulomi, i linfociti servono solo ad armare i macrofagi (che poi faranno<br />
il lavoro) grazie alla produzione di IFNγ e TNF.<br />
Questo è il meccanismo che giustifica il perché nei granulomi si vengono a trovare<br />
• cellule epitelioidi (macrofagi super attivati), che sono estremamente più grandi di un<br />
macrofago (fino a 20x) e contengono un enorme complesso di<br />
Golgi, numerosissimi lisosomi..<br />
• cellule giganti: centinaia di volte più grande di un macrofago, determinate dalla fusione<br />
di più macrofagi, fenomeno che in condizioni normali non avverrebbe mai.<br />
Il granuloma può derivare anche dalla presenza di un corpo estraneo, che determina la classica<br />
attivazione, ma in assenza di linfociti, dal momento che viene a mancare la componente batterica.<br />
3) Istoflogosi Diffusa: oltre alla forma granulomatosa, si può avere una forma d’istoflogosi di tipo diffuso:<br />
Epatite cronica attiva: presenta un intervento dei linfociti, che vanno ad eliminare gli epatociti<br />
esponenti Ag virali (di virus di per se non citotossici), che vengono sostituiti<br />
con cicatrici<br />
Tiroidite di Hashimoto: è coinvolta tutta la tiroide, che viene man mano sostituita da tessuto fibroso<br />
Diabete Giovanile insulino dept: si ha l’eliminazione delle isole di Langerhans.<br />
Polmoniti interstiziali: possono evolversi verso una cronicizzazione, che porta ad una insufficienza<br />
ventilatoria spesso mortale.<br />
4) Istoflogosi Localizzata (focale): risposta infiammatoria focale ad andamento cronico, caratterizzata da<br />
infiltrati di cellule mononucleate<br />
non immunologici (da corpo estraneo p.es)<br />
a. tossici: dove c’è una forte componente di fibrosi;<br />
- asbesto: è l’amianto, che si presenta sotto forma di particelle aghiformi, che non<br />
possono essere fagocitate correttamente, e finisco per attivare cronicamente il<br />
macrofago. Si ha così il richiamo di fibroblasti, che tenderanno ad incistare i<br />
frammenti. Considerando che l’asbesto è un pulviscolo, si tratta di miliardi di<br />
particelle, dove ognuno formerà tutta una sua concentrazione di fibroblasti, per cui si<br />
avrà una fibrosi polmonare che porterà alla insufficienza ventilatoria e alla morte.<br />
- talco<br />
- silice<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 39
. non tossici: infiltrati caratterizzati esclusivamente dai macrofagi; non si ha intervento<br />
fibroblastico, se non in modo molto ridotto (niente cicatrice). Diciamo che nel<br />
mondo occidentale i polmoni appaiono in genere neri, come i linfonodi<br />
polmonari. Si tratta di antracosi, che non è una malattia, ma un quadro<br />
anatomopatologico. Si tratta di macrofagi che, fagocitato materiale carbonoso,<br />
non si sono attivati, e rimangono lì.<br />
- carbone<br />
- plastica<br />
- ferro<br />
immunologici (ad alto turnover): dipende moltissimo dall’organismo, che può essere ad…<br />
a. alta resistenza: l’organismo si difende bene;<br />
esempi<br />
- TBC micro nodulare (o tubercoloma): si tratta della forma più frequente<br />
di infezione tubercolare, costituita da 2-3 tubercoli<br />
in corrispondenza dell’ilo polmonare<br />
- sifilide tubercoloide (gommosa), si formano ulcere con materiale<br />
viscido, tremendamente infettante, che sono proprio<br />
delle gomme luetiche.<br />
- lebbra tubercolare (forma meno “cattiva”)<br />
- sarcoidosi 14 : in questa <strong>patologia</strong> a carattere tipicamente fibrosante, non ci<br />
sono elementi batterici, nonostante la presenza dei granulomi.<br />
caratteristiche<br />
- pochi microrganismi<br />
- molti linfociti<br />
- molte cellule epitelioidi<br />
- notevole fibrosi circostante, che permetterà all’organismo di isolare<br />
l’infezione.<br />
b. bassa resistenza: si ha poca risposta immunologica, che permette una grossa diffusione dei<br />
bacilli<br />
esempi<br />
- TBC miliare: che vede la formazione in tutto l’organismo di granuli della<br />
dimensione dei chicchi di miglio. Si parla di diffusione<br />
miliarica.<br />
- lebbra fibromatosa: data dal Mycobacterium Leprae, è la forma più<br />
aggressiva.<br />
caratteristiche<br />
- molti microrganismi<br />
- pochi linfociti<br />
- poche cellule epitelioidi<br />
- scarsa fibrosi<br />
c. forme intermedie (post virali: morbillo, HIV, etc…)<br />
- TBC nodulare (non “micro”): darà più o meno linfoadenopatia (infetta,<br />
tubercolare), sierosite (infiammazione, non infezione),<br />
escavazione (svuotamento bronchiale del tubercolo, con<br />
formazione della caverna), fistole (tipicamente cutanee). In<br />
genere il tubercoloso ha anche emottisi o comunque muco<br />
striato di sangue, a causa dell’erosione delle pareti delle<br />
caverne che possono ledere piccole arterie.<br />
- sifilide cerebrale cardiovascolare: dà luogo ad aneurismi aortici, con<br />
dilatazioni a “sacco”.<br />
14<br />
E’ una malattia che si caratterizza per la formazione di grosse formazioni fibrose a livello mediastinico che danno<br />
grossi problemi di compressione; Contemporaneamente a livello tissutale - istologico si hanno granulomi che portano<br />
alla fibrosi dei tessuti, a livello interstiziale. Al momento è incurabile, non si ha presenza di batteri, e l’unica terapia<br />
rimane ancora il cortisone.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 40
TBC primaria<br />
prime ore: insediamento bacilli, fugace arrivo PMN: anche in questo caso si ha l’arrivo di questi<br />
elementi, in forma però aspecifica<br />
24h dopo: già in questo tempo già si rilevano solo macrofagi, che vanno a fagocitare gli elementi, e si<br />
ha linfangite + linfadenite. Se l’infezione è a livello cutaneo si ha un’ulcera dura che non<br />
guarisce (sempre con linfangite e linfadenite).<br />
diversi giorni dopo:<br />
a. complesso primario: tubercolo I + linfangite + linfadenite. Tubercoloma<br />
(TBC nodulare = buona difesa e/o scarsa virulenza)<br />
b. polmonite acuta (lobite) tubercolare con pleurite tubercolare siero fibrinosa<br />
c. meningite TBC: il materiale infetto può contaminare il sangue tanto da poter dare luogo<br />
ad una meningite tubercolare.<br />
evoluzione del tubercolo:<br />
a. tutti i territori infiammatori confluiscono e calcificano<br />
b. Se l’organismo risponde bene si ha colliquazione sierosa, che poi può evolvere alla<br />
calcificazione.<br />
c. diffusione: se si ha la formazione della caverna, con una diffusione per via bronchiale<br />
(endopolmonare) o linfo-sanguigna (diffusione nell’ambiente interno). La TBC aperta si<br />
rivolge verso l’esterno.<br />
TBC post- primaria<br />
Reinfezione endogena: chi abbia avuto un complesso primario completamente guarito, ad una certa età è in<br />
grado di andare incontro ad una tubercolosi post primaria, identica a quella primaria, sostanzialmente, solo che<br />
nasce all’interno dell’organismo per problemi di difesa.<br />
Sifilide<br />
All’ingresso segue una moltiplicazione in situ con una diffusione non solo linfatica, ma fin da subito anche<br />
ematica.<br />
3 settimane: sifiloma primario (duro, localizzato nel punto d’infezione): si forma un’ulcera (o<br />
nodulo cutaneo) che deriva dal fatto che il batterio torna dopo essersi<br />
diffuso sistematicamente anche nel punto d’inoculo, dove troverà un<br />
contesto di cellule del SI tale da fare da trigger per l’ulcerazione e il<br />
danno tissutale.<br />
6 settimane si ha la sifilide <strong>II</strong> (roseole, papule con secrezione settica)<br />
Anni: si ha la sifilide <strong>II</strong>I, si formano granulomi perivascolari con necrosi (gomme).<br />
Malattie che danno Granulomi<br />
• aortite luetica ⇒ sacciforme (già citata)<br />
• granulomi encefalici (fibrosi)<br />
- TBC<br />
- sarcoidosi<br />
- lebbra<br />
- granuloma reumatico (streptococco a livello articolare)<br />
- nodulo reumatoide<br />
- linfogranuloma venereo<br />
- granuloma melitense<br />
- Morva (Bacillus Mallei)<br />
- protozoi (diversi)<br />
- actinomicosi<br />
- rinoscleroma<br />
- varie malattie tropicali (ifomiceti, blastino<br />
miceti, sporotricum)<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 41
Jalinosi<br />
Si può inserire nell’ambito della guarigione, cicatrizzazione… è un termine altamente aspecifico, che indica<br />
la presenza di materiale omogeneo rosa (ematossilina & eosina) , che può essere intra / extra - cellulare;<br />
fondamentalmente sono proteine.<br />
P.es:<br />
1) intracellulare<br />
2) extracellulare<br />
- nel rene in corso di proteinuria<br />
- alterazioni cellulari nel corso di infezioni virali (sono proteine virali nel nucleo)<br />
- alcolisti, hanno inclusioni di materiale jalino negli epatociti: è definita pre<br />
cheratina.<br />
- collagene di vecchie cicatrici (se fossero nuove, più che solo collagene, sarebbe<br />
pieno di fibroblasti)<br />
- arteriole renali: nel diabete e nell’ipertensione; si tratta di proteine filtrate<br />
attraverso l’endotelio alterato<br />
- glomeruli renali: ci sono diverse patologie, in particolare la maggior parte delle<br />
glomerulo nefriti sono autoimmuni, e ce ne sono molte;<br />
fondamentalmente è la stessa cosa: si ha alterazione della membrana<br />
basale e filtrazione di proteine.<br />
- amiloide: nell’amiloidosi ovviamente<br />
Amiloidosi<br />
Si definisce con amiloide un gruppo di sostanze extracellulari di natura proteica, che si correlano con un<br />
numero di patologie diverse, ma hanno una manifestazione di questo tipo.<br />
1) macroscopicamente: l’organo di un paziente colpito da amiloidosi risulta ingrossato<br />
2) microscopia: i patologi per cercare di indagare il tessuto cercavano diverse colorazioni, in particolare<br />
risultò utile il procedimento che prima utilizzava tintura di iodio e quindi acido<br />
solforico (H2SO4), che è una tecnica che mette in evidenza l’amido vegetale, ragion per<br />
cui questo materiale venne definito “amiloide”<br />
a. tintura di iodio + H2SO4 ⇒ blu<br />
b. E-E ⇒ materiale jalino, amorfo, rosa…<br />
c. rosso congo + luce polarizzata ⇒ si utilizza ancora oggi, senza la luce polarizzata, con la<br />
quale si otterrebbe una birifrangenza verde, che dimostra la fibrillarità del materiale.<br />
d. coloranti basici (cristal violetto, …) ⇒ ci si rese conto che con questi coloranti si otteneva<br />
una colorazione rosa porpora: mucopolisaccaridi (acidi)<br />
e. PAS + ⇒ testimonia la presenza di glicoproteine<br />
3) microscopia elettronica<br />
a. componente P ⇒ componente pentagonale, formata da 5 unità globulari unite a ciambella,<br />
questa componente non è presente nei depositi cerebrali, unica eccezione<br />
b. struttura fibrillare a β foglietto ⇒ coincide con l’osservazione della birifrangenza col<br />
rosso congo<br />
4) immunoistochimica<br />
a. fibrille (80% dei casi)<br />
b. componente P (no nel SNC)<br />
c. glucosaminoglicani (sempre presenti)<br />
L’idea, vista l’affinità col rosso Congo (da un punto di vista terapeutico) è di associare un qualcosa in grado di<br />
sciogliere il materiale jalinoso legato a molecole molto piccole di rosso Congo.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 42
§<br />
Vecchia classificazione<br />
Quando c’è una flogosi, una infezione, le varie citochine rilasciate, finendo nel fegato inducono la produzione<br />
delle fasi acute. Al di là di quelle utilizzate per fare diagnosi, bisogna considerare elementi come l’amiloide A.<br />
1) secondaria (a malattie / infiammazioni croniche), che si nota a livello di<br />
a. fegato: nella fase acuta va a produrre i due elementi dell’amiloide: la amiloide A e la<br />
componente P (pentamerica).<br />
b. milza<br />
c. rene: a forza di essere sostituito con depositi di amiloide, va incontro a proteinuria, nefrosi e<br />
necrosi<br />
malattie reumatiche: in tutte le malattie autoimmuni si presuppone uno stato<br />
flogistico piuttosto costante, che porterà ad amiloidosi<br />
TBC: soprattutto nelle forme intermedie, dove si ha costante infiammazione<br />
Osteomielite: è la classica malattia che se non curata porta ad amiloidosi,<br />
tipicamente renale: il paziente che si porta questa infiammazione<br />
per anni, finisce per morire di insufficienza renale..<br />
Colite ulcerosa<br />
NON si osserva né nel LES, né in Crohn.<br />
2) primitiva: depositi presenti senza particolari ragioni<br />
a. cuore: IC, aritmie: in questo caso l’amiloidosi colpisce le componenti elettriche del cuore<br />
b. lingua e gastro intestinale: interessa tutto il tratto digerente, fin anche alla mucosa rettale<br />
(90% delle forme sistemiche). Questa classificazione è (appunto) vecchia: oggi si sa che<br />
l’interessamento GI è presente anche nelle forme secondarie, e si può (e si fa) fare diagnosi<br />
con una biopsia di mucosa rettale.<br />
3) ereditaria famigliare: in certe famiglie<br />
4) organo limitata: forme che vanno ad interessare esclusivamente un organo<br />
a. cervello<br />
b. cuore<br />
c. articolazioni<br />
d. organi endocrini<br />
e. cute<br />
f. polmone<br />
g. nervi<br />
§<br />
immunoistochimica delle fibrille<br />
1) SAA: Il fegato nell’amiloidosi sintetizza la SAA (Serum Amiloid A, una HDL).<br />
2) AL (Amyloid L): sta per subunità λ delle Ig, tipiche di pazienti con mieloma ⇒ proteinuria di Bence<br />
Jones 15 . In questo caso ci sarà deposito di AL, che danno amiloidosi; in questo caso<br />
la gravità del tumore mette in ombra la componente amiloidotica.<br />
3) pre Albumina: amiloide sistemica senile, presente nel 100% degli anziani (magari modesti, moderati,<br />
ma presenti).<br />
4) β o A4 - proteina: è una sorta di recettore di membrana presente sulla superficie dei neuroni del SNC.<br />
Sappiamo che questa proteina è codificata nel Chr 21: questi depositi di amiloide a<br />
livello cerebrale sono caratteristici dell’Alzheimer e della Sindrome di Down<br />
(trisomia 21). Anche in questo caso, nel cervello senile si ritrovano tracce di questo<br />
elemento.<br />
15 Semplicemente ponendo l’urina in acido (anche acetico), se ci sono proteine si forma la nubecola: prova di Rivalta.<br />
Per sapere se è proprio Bence Jones basta scaldare le urine e si nota il dissolvimento della nubecola (cosa che non<br />
avverrebbe con l’albumina)<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 43
5) β2 microglobulina: negli emodializzati cronici ci sono depositi di amiloide dovuti a questa sostanza,<br />
in quanto non è filtrata dai filtri dell’emodialisi.<br />
6) Cistatina C: proteina presente sia nel plasma che nel liquido cerebrospinale; Il deposito si ha nel caso<br />
di emorragia cerebrale ereditaria (con amiloidosi)<br />
7) AE (Amiloide Endocrina): p.es formata da<br />
a. calcitonina nel carcinoma midollare della tiroide.<br />
b. catene β dell’insulina (nel diabete <strong>II</strong>)<br />
c. STH (o GH): tumori dell’adenoipofisi<br />
8) AP (componente P) ⇒ quella pentamerica<br />
9) Glicosaminoglicani: presenti in tutte le forme, giustificano la PAS positività<br />
§<br />
Teoria di Cohen<br />
Dato che alcune molecole che provocano amiloidosi sono fisiologiche e normalmente presenti, ci si è<br />
cominciati a chiedere se ci dovessero essere modificazioni, delle alterazioni cellulari che portino alla<br />
<strong>patologia</strong>. Non è un semplice trasudato, ma si evidenziano delle alterazioni cellulari che precedono la<br />
deposizione extracellulare di amiloide, specie in milza e linfonodi.<br />
I. [sostanza amiloidogena]↑: in plasma o anche in sede locale.<br />
<strong>II</strong>. aumento dei macrofagi, che tentano di digerirla<br />
<strong>II</strong>I. insufficiente smaltimento della sostanza da parte dei macrofagi ⇒ deposizione di sostanza<br />
insolubile.<br />
§<br />
Alzheimer<br />
Si ammette quasi generalmente che la demenza dell’Alzheimer è molto simile alla demenza senile ed alla<br />
demenza tipica del Down.<br />
• angiopatia amiloide: sono cioè colpiti molto i vasi sanguigni<br />
• placche neuritiche<br />
• amassi neuro fibrillari di amiloide dentro i pirenofori (ma senza la componente P)<br />
Nb: l’A4 proteina induce produzione di NO2 dalla neuroglia, creando ulteriori lesioni.<br />
In questa <strong>patologia</strong> si rilevano microscopicamente delle placche senili, che rappresentano degenerazioni del<br />
tessuto<br />
APP<br />
La proteina responsabile dell’Alzheimer è normalmente presente sulle membrane, e si definisce APP<br />
(Amiloyd β Precussor Protein). Su questa vanno ad agire delle proteine dette secreatsi, che nei pazienti colpiti<br />
presentano delle modificazioni genetiche:<br />
α secretasi: cliva la proteina sulla membrana<br />
β secretasi: agisce nel moncone che rimane a livello endocellulare<br />
γ secreatsi: finisce l’opera, e genera gli elementi (αβ peptide) che andranno a<br />
formare delle fibre<br />
Inoltre l’Apo-E 4 è un’altra proteina che risulta mutata in questa situazione, e che è correlata con l’aumento<br />
dei depositi.<br />
Da un punto di vista terapeutico si è tentato.. (Bava dixit)<br />
immunoterapia: dotare il sistema di Ab in grado di indurre la microglia ad attaccare i<br />
filamenti. Disassemblati questi complessi (sempre in vitro) i neuroni<br />
sopravvivono<br />
inibitori della β o γ secretasi<br />
Agenti anti-aggreganti<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 44
§<br />
Angiopatia Diabetica<br />
Il diabetico ha regolarmente l’ateriosclerosi jalina (il diabete è il quarto fattore di rischio, oltre a fumo,<br />
ipertensione e ipercolesterolemia). Diciamo<br />
1) Localizzazioni (6)<br />
- retina<br />
- glomeruli e midollare renale: il diabetico va regolarmente incontro a insufficienza<br />
renale. La causa finale del diabetico (curato bene o<br />
male, prima o dopo) è di andare in insufficienza<br />
renale, ed ha regolarmente fenomeni di proteinuria,<br />
dovuta a varie modificazioni (tube della polarità<br />
della membrana basale…)<br />
- pelle: a causa della scarsa vascolarizzazione tipicamente presenterà ulcere che non<br />
tendono alla guarigione soprattutto a livello dei piedi<br />
- muscoli scheletrici: a volte si hanno atrofie di interi fasci<br />
- vasa nervorum: parestesie, sensazioni di caldo/freddo, iperestesia, anestesia,<br />
formicolii… sono tutte situazioni causate dallo stress dei nervi<br />
- vasi placentari: se i disturbi si fanno molto giovanili<br />
2) Anatomia (2)<br />
3) Retina (5)<br />
- arteriole: si nota sclerosi di tipo jalino.<br />
- capillari: si ha inspessimento PAS + della membrana basale (depositi di<br />
collagene IV), con permeabilità↑ (peptidoglicani↓)<br />
⇒ trasudazione proteine ↑ ⇒ depositi ↑<br />
- degenerazione dei periciti: AGEs (Advanced Glycosylation Endproducts). Alla fine i<br />
periciti controllano tutto: dalla pervietà alla<br />
permeabilità. Questo punto è molto importante<br />
- micro aneurismi: si notano nella retinoscopia come piccole macchiette bianche<br />
- Cotton Wool Spots: corrispondono a stravasi di liquidi, trasudazioni a livello<br />
retinico, che appaiono come batuffoli di cotone, osservando il<br />
fondo dell’occhio.<br />
- shunts artero venosi<br />
- retinopatia proliferativa: il proliferare dei vasi (angiogenesi) che si approfondano<br />
nel corpo vitreo, dove danno quindi fibrosi, a causa del<br />
fatto che finiscono per chiudersi (obliterarsi) e<br />
cicatrizzare.<br />
Se da una parte c’è la presenza di agenti quali gli AGE (di cui fa parte anche l’Hb glicosilata), con un forte<br />
potere glicosilante ed ossidativo, l’AT<strong>II</strong>, cosa questa da ricordare, porta a produzione di numerose<br />
citochine ed in particolare TGFβ, che porta a sua volta a..<br />
- MEC ↑: sostanzialmente fattori ossidanti, AGEs, AT<strong>II</strong> provocano un’attivazione<br />
dei macrofagi locali ⇒ del mesangio ⇒ dei fibroblasti.<br />
- ⊕ glomerulo sclerosi<br />
- ACE ↑ ⇒AT<strong>II</strong> ↑<br />
- albuminuria<br />
Infatti sembra che avvenga nel diabetico, l’anormale produzione di ACE a livello glomerulare. Il trattamento<br />
del diabetico quindi verterà contemporaneamente del mantenere l’Hb glicosilata bassa con un buon controllo<br />
sulla glicemia e sull’utilizzo di ACE inibitori.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 45
Dalla Microbiologia del Prof. Tonin:<br />
Prioni: Encefalopatie Spongiformi Trasmissibili<br />
Si è a conoscenza delle malattie da loro causate da molto tempo, ma sono state a loro associate solo di recente.<br />
- Kuru ⇒ malattia che si trovava (ora non ce n’è quasi più, grazie alla proibizione del<br />
cannibalismo) in Nuova Guinea:<br />
» atassia (perdita della coordinazione motoria)<br />
» difficoltà deambulatoria<br />
» demenza<br />
» morte (4-24 mesi)<br />
- Creutzfeldt Jakob Disease ⇒ 1 caso / milione; simile al Kuru: si sapeva essere legata ad<br />
un agente infettante in quanto si era notato che poteva essere<br />
legata a certe pratiche mediche (come elettrodi<br />
intracerebrali), si era individuata anche una associazione<br />
genica in alcune popolazioni.<br />
- Insonnia familiare letale ⇒ si muore per assenza di sonno<br />
Nb: nel mondo animale, di questi esempi se ne hanno molti (visoni, cervi.. mucca pazza 16 )<br />
Si tratta di agenti infettanti costituiti da una proteina aberrante che ha una controparte normale codificata<br />
dall’ospite: noi normalmente possediamo una PRP (Protease Resistant Protein), senza la quale, topi knockout<br />
vedono diminuite capacità di apprendimento, ritmo sonno/veglia alterato… è una proteina che non si sa bene a<br />
cosa serva. La PRP** (anomala) genererebbe cambiamenti conformazionali su proteine normali<br />
⇒ degenerazione: è un loop che si auto mantiene (ogni proteina modificata è in grado di modificarne a sua<br />
volta…), ed è alla base della trasmissibilità della <strong>patologia</strong>.<br />
Causano quindi malattie neurodegenerative, fatali in uomo e animali nel giro di 1-2 anni; è irreversibile, e<br />
per ora non c’è terapia.<br />
La diagnosi (più spesso effettuata in veterinaria) sfrutta la biologia molecolare.<br />
Lo scrapie è tipicamente della pecora che si procura lesioni a causa di grattamento<br />
La mutazione “spongiforme” si concretizza in un processo multifocale che porta all’incostante formazione di<br />
vacuoli, apparentemente vuoti e di diversa grandezza all’interno del neuropilo.<br />
La diagnosi di cui si parla si esegue attuando una digestione con proteinasi K del campione: la caratteristica<br />
della PRP**, differentemente dalla PRP wild type è di essere proteasi resistente: un western Blot del tessuto<br />
estratto dopo parziale digestione permette di diagnosticare la presenza di PRP**.<br />
16 Nasce dalla gestione degli scarti delle mucche macellate: qualche genio ha ben pensato di fabbricare con questi scarti<br />
delle farine da somministrate al bestiame, facendone un cannibale. Questo è totalmente non naturale, ed ha portato<br />
alle ben note conseguenze.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 46
1) Arteriosclerosi<br />
a. aterosclerosi<br />
b. arteriolosclerosi<br />
c. sclerosi calcifica della media<br />
2) Arteriti<br />
3) Tumori vascolari<br />
Malattie delle arterie<br />
§<br />
Aterosclerosi<br />
Riguarda fondamentalmente le arterie di tipo elastico. Non viene interessata la tonaca media, ma solo quella<br />
intima. Le caratteristiche dell’ateroma l’abbiamo già visto (dispensa I).<br />
normale progressione delle placche<br />
1) confluenza: siamo abituati ad osservare reperti anatomopatologici per cui tutta l’aorta può diventare<br />
una placca aterosclerotica.<br />
2) protrusione (non infiltrazione) con stenosi<br />
3) ingrossamento verso la media<br />
complicazioni<br />
1) calcificazione (rigidità della parete)<br />
- perdita di dicrotismo sfigmico<br />
- PD↑ (sistolica↑ diastolica↓). Difatti la regola una volta diceva che l’anziano doveva<br />
avere una PMAX = 100+età. Oggi invece sappiamo che non è fisiologico e bisogna<br />
cercare di contenere la pressione, ovviamente<br />
2) ulcerazione<br />
- trombosi / embolia. Il fatto embolico si ha per lo più a livello carotideo/polmonare<br />
- emorragia<br />
- infiltrazione sanguigna, che può andare a scollare la placca, contribuendo al fatto<br />
stenotico. Questo può avvenire anche a partire dai vasa vasorum<br />
3) aneurismi: dovuti all’assottigliamento della tonaca media del vaso (muscolo-elastica). Si tratta della<br />
legge di Laplace, dove la dilatazione si auto alimenta, e ovviamente si tratta dei grandi vasi;<br />
più frequentemente dell’aorta, dove i gradienti pressori vanno maggiormente a provocare<br />
insulti alla media in modo più diretto. L’aneurisma assumerà una conformazione<br />
fusiforme, differentemente da quelli sifilici, tipicamente sacciformi. Esistono anche degli aneurismi<br />
ereditari che riguardano tipicamente l’arteria comunicante anteriore dell’esagono del Willis;<br />
Danni da malattia Aterosclerotica<br />
1) cuore<br />
- micardio sclerosi (una sorta di remodeling), dovuta alla perdita di elementi<br />
cellulari, e che implica anche una ..<br />
- ..IC ed…<br />
- infarti<br />
2) Cervello<br />
3) arti inferiori<br />
- TIA (Transitory Ischemic Attak): quando un’arteria già stenotica viene p.es<br />
complicata da un calo pressorio sistemico. Il paziente cade a terra. Il tutto è<br />
reversibile, in quanto dura sufficientemente poco<br />
- ischemia acuta: ostruzione di una arteria (embolia, complicazioni di un ateroma..)<br />
- ischemia acuta: tipicamente dolori crampiformi che insorgono nell’attività<br />
muscolare, quando la richiesta di sangue è maggiore e la stenosi dovuta<br />
all’aterosclerosi si somma all’aumentato metabolismo del muscolo. Tipicamente il<br />
soggetto potrà compiere un certo tragitto, per poi dover arrestare la marcia il tempo<br />
necessario per perfondere l’arto, e poi potrà riprendere per la lo stesso tempo.<br />
- claudicatio<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 47
Arteriolosclerosi<br />
jalina<br />
Si ha un ispessimento jalino, omogeneo della parete arteriolare, con assottigliamento del vaso. L’endotelio, di<br />
nuovo, è intatto e la lesione si configura come benigna.<br />
Si ha particolarmente in anziani e diabetici, dovuta all’aumento di permeabilità che permette l’infiltrazione<br />
proteica della parete.<br />
iperplastica<br />
Genera arterie a bulbo di cipolla, con giustapposizione di cellule muscolari lisce e riduzione del lume.<br />
La conseguenza più importante è renale: nefrosclerosi maligna. Talvolta, porta a necrosi acuta della parete<br />
arteriolare con depositi di fibrinoide (cfr. necrosi fibrinoide)<br />
La patogenesi deriva dall’iperplasia di cellule muscolari lisce e deposito di sostanza extracellulare.<br />
Si caratterizza da pressioni diastoliche > 110 mmHg<br />
Saranno fatte meglio a fisio<strong>patologia</strong>.<br />
Quelle forse più interessanti sono le ..<br />
§<br />
§<br />
Vasculiti<br />
- malattia di Kawasaky: auto ab contro l’endotelio: si ha flogosi<br />
- malattia di Horton: ricordiamo l’arterite temporale<br />
Neoplasie<br />
Una neoplasia è una proliferazione tissutale che si caratterizza per (4)<br />
Malignità e Benignità<br />
progressività<br />
atipia: si diversifica dei tessuti circostanti<br />
autonomia: non risente di stimoli esterni<br />
afinalismo<br />
differenziazione: i tessuti sono normalmente ben differenziati, mentre i tumori più sono maligni<br />
più sono indifferenziati, cioè si distinguono dal tessuto da cui hanno avuto<br />
origine: sono più o meno anaplastici, dove per “anaplasia” si intende il<br />
contrario di differenziazione, una regressione.<br />
modalità di crescita:<br />
a. espansiva: c’è un asse vascolare centrale che permette la crescita di un tumore benigno.<br />
⇒ la crescita ad un certo punto dovrà fermarsi<br />
⇒ si ha la formazione, quasi regolare della capsula, un velo di tessuto<br />
cicatriziale, collagene… questo permetterà una facile asportazione<br />
b. infiltrante: il tumore maligno si procura approvvigionamento ematico dalle zone<br />
circostanti tramite neo angiogenesi. E’ un’invasione dei tessuti circostanti.<br />
I margini saranno quindi sfrangiati. Questo permetterà quasi sempre di<br />
distinguere clinicamente tra malignità e benignità: già in un RX si vede se la<br />
neo-massa è infiltrante o meno (cfr. lastre mammella di Turoldo).<br />
metastasi: sono tipiche delle lesioni maligne.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 49
§<br />
Tratti Clinici dei Tumori<br />
(sia benigni che maligni)<br />
compressione: un tumore anche se benigno biologicamente, può crescere p.es nella scatola<br />
cranica. Ovviamente non c’è espandibilità, e ci saranno lesioni anche mortali.<br />
ostruzioni: il mixoma è un tumore benigno che cresce nel cuore, ma è raro. Ci possono anche<br />
essere tumori benigni abbastanza grandi da ostruire il colon.<br />
ulcerazione: regolare per i tumori maligni, non avviene invece nei benigni.<br />
emorragie: possibili nei benigni, regolari nei maligni. Il sangue occulto nelle feci è diventato un<br />
test classico.<br />
endocrinopatie: molti tumori rilasciano sostanze simil ormonali o ormonali vere e proprie, sia<br />
che siano maligni che benigni.<br />
trombosi: è una caratteristica dei maligni, che danno regolarmente trombosi profonde.<br />
Al contrario non è una caratteristica dei benigni. Diciamo che in fasi avanzate di<br />
tumori coinvolgenti il fegato sarà in ultima analisi il contrario, mancherà capacità<br />
coagulativa in virtù della cessata produzione proteica del fegato.<br />
metastatizzazione. ovviamente dei maligni; le sedi sono tipicamente (a memoria) (6):<br />
a. linfonodi locali (via linfatica)<br />
b. fegato<br />
c. polmoni<br />
d. ossa<br />
e. cervello<br />
f. surrene<br />
cachessia: indebolimento fisico (magrezza, atrofia..) tipico dei tumori maligni<br />
§<br />
Classificazione<br />
Ce ne sono diverse: comportamentale, istogenetica, anatomo topografica (del cervello, del polmone..),<br />
clinica (grading, staging…)...<br />
Classificazione istologica<br />
cellula o tessuto di origine tumore benigno tumore maligno<br />
epiteli di rivestimento<br />
- stratificate squamose<br />
- cellule basali<br />
- mesoteli (sierose)<br />
- ep. di transizione<br />
- polipo, papilloma<br />
- cheratosi seborroica<br />
- mesotelioma fibroso<br />
- papilloma a cellule di transizione<br />
(può sanguinare)<br />
carcinoma… può essere<br />
- carcinoma squamo cellulare 18<br />
(delle cellule squamose)<br />
⇒ metastatizza, a meno che non sia<br />
cutaneo, dove non dà metastasi<br />
- carc. baso cellulare o baselioma<br />
(delle cellule basali)<br />
⇒ non metastatizza, ma recidiva<br />
- mesotelioma (dei mesoteli):<br />
terribilmente metastatizzante.<br />
- carcinoma a cellule di transizione<br />
18 può derivare da una metaplasia, un cambiamento fenotipico dell’epitelio bronchiale. Tipicamente nei fumatori, dove<br />
da cilindrico semplice ciliato diventa cubico pluristratificato piatto stratificato. Questa è una modalità di<br />
reazione dell’epitelio. Nel caso di trasformazione neoplastica ci sarà un carcinoma squamo cellulare del polmone, che<br />
ha la caratteristica di essere terribilmente metastatico.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 50
epitelio ghiandolare<br />
- fegato<br />
- tubuli seminiferi<br />
adenoma adenocarcinoma<br />
- epatoma<br />
- seminoma (più benigno)<br />
- carcinoma embrionale<br />
epitelio placentare mola idatidea mola vescicolare / corion carcinoma<br />
fibroblasti<br />
fibroma<br />
fibrosarcoma<br />
immaturi fetali<br />
mixoma<br />
mixosarcoma<br />
adipociti lipoma liposarcoma (p.es nel retro peritoneo,<br />
diagnosi difficile)<br />
condrociti condroma condro sarcoma<br />
osteociti osteoma: classico tumore benigno con<br />
una malignità clinica (livello craniale,<br />
articolare..)<br />
osteosarcoma<br />
meningi mengioma meningioma maligno<br />
epitelio ematico emangioma: spider, angiomi cutanei emangiosarcoma (molto maligno)<br />
endotelio linfatico linfangioma linfangiosarcoma<br />
tessuto emopoietico<br />
- eritroblasti<br />
- mieloblasti<br />
- monoblasti<br />
- linfociti<br />
- plasmacellule<br />
tessuto muscolare<br />
- striato<br />
- liscio<br />
tessuto nervoso<br />
- astrociti<br />
- oligodendrociti<br />
- cell di Schwan<br />
- neuroblasti<br />
- melanociti<br />
- tessuto<br />
enterocromaffine<br />
misti (2+ tessuti < unico<br />
foglietto embrionale)<br />
non sono conosciute forme benigne<br />
- rabdomioma (raro)<br />
- leiomioma (frequenti)<br />
- astrocitoma<br />
- oligodendroglioma<br />
- schwannoma<br />
- glioneuroma (deriva dalla<br />
differenziazione della forma maligna<br />
che diventa beigna: strano)<br />
- nevo<br />
- feocromocitoma<br />
- eritro leucemia 19<br />
- leucemia mieloide<br />
- leucemia monoblastica<br />
- linfomi (circoscritti, solidi)<br />
leucemia linfoide (diffusa, ematica)<br />
- mieloma multiplo o plasmocitoma<br />
- rabdomiosarcoma<br />
- leiomiosarcoma<br />
- glioma o glioblastoma: terribile.<br />
dà recidive metastatiche<br />
diffusamente nel SNC<br />
- oligodendroglioma maligno<br />
- Schwannoma maligno<br />
- neuroblastoma<br />
- melanoma<br />
- carcinoide: produce serotonina, è<br />
maligno, ma dà subito segno di se: dà<br />
vampate di calore, ipertensione..<br />
inoltre sono dosabili cataboliti della<br />
serotonina nelle urine. Si può trovare<br />
tipicamente nel polmone, dell’ileo e<br />
nell’appendice. frequente, ben<br />
conosciuto.<br />
- gh. salivari<br />
- adenoma pleiomorfo (parotide 20 ) - tumore misto delle ghh.salivari<br />
embrionali (cell. totipotenti) teratoma maturo, cisti dermoide teratocarcinoma<br />
19 “leucemia” = leucociti in circolo: ci possono essere forme “aleucemiche”, se non ci sono elementi in circolo, ma la<br />
situazione è ancora circoscritta al midollo. Mettiamo<br />
20 il rischio, nell’escissione, è la resezione del nervo faciale, che crea notevolissime deformità.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 51
Grading<br />
Misura il grado in cui il tumore è anaplastico, la sua malignità. In genere si fa riferimento ad:<br />
atipie cellulari<br />
atipie nucleari (nuclei sovra numerati p.es)<br />
rapporto nucleo/citoplasma.<br />
I tumori maligni crescono appunto per infiltrazione dei tessuti circostanti, con un meccanismo che sfrutta il<br />
VEGF, che determina neoangiogenesi in corrispondenza del tumore, garantendogli una forma di irrorazione.<br />
<br />
Giustificazione della Metastasi<br />
La metastatizzazione dipende dai meccanismi di crescita, che permettono alle cellule di migrare e spostarsi<br />
facilmente. E’ un evento che può essere altamente precoce (come nei melanomi, dove a volte metastatizza<br />
ancora prima che ci si renda conto della malignità della lesione).<br />
Meccanismi<br />
Migrazione<br />
• perdita di ancoraggio al tessuto di origine. Si estrinseca nella scomparsa delle proteine<br />
di adesione. Quindi ci saranno diverse vie di diffusione<br />
(cfr. più avanti).<br />
• adesione alla matrice (crowling)<br />
• degradazione della matrice (collagenasi, Matrix MetalloProteinases collagene IV)<br />
chemochine: le cellule neoplastiche presentano recettori per le chemochine, in modo che<br />
queste siano in grado di dirigere la migrazione delle cellule. In particolare le<br />
cellule dei vasi linfatici producono chemochine, che spiegano il trofismo<br />
verso queste strutture e l’iniziale approdo a livello linfonodale<br />
organi filtro: polmoni, fegato, ossa, cervello, surrenali… al di là dell’irrorazione diciamo<br />
che si tratta di stasi che possa facilitare l’approdo di cellule metastatiche. La<br />
stasi è favorita nelle ossa a livello delle lacune, nel cervello nelle lacune<br />
meningee, etc.. A livello osseo le metastasi possono frequentemente<br />
provocare compressione delle radici nervose.<br />
recettori endoteliali: le cellule endoteliali hanno recettori per i leucociti, che possono essere<br />
sfruttati. Nel surrene in particolare questo meccanismo sembra importante.<br />
seed & soil (seme & suolo): dev’esserci una sintonia tra cellula cancerosa e tessuto<br />
“candidato” alla metastasi. I fibroblasti tumore associati sono gli elementi che<br />
circondano il tumore proliferante. L’evoluzione del tumore dipenderà in parte dalla<br />
produzione da parte di questo tessuto di ormoni e fattori di crescita. Questo<br />
travalica la definizione di “proliferazione autonoma”, ma è una forma vecchia di<br />
definizione, limitante. Attualmente sono stati visti questi aspetti ambientali.<br />
Vie di metastatizzazione<br />
Solo una misera % delle cellule che si distaccano sono in grado poi di dare effettivamente metastasi<br />
• linfatica: arriverà ai linfonodi. Particolarmente vero per i carcinomi. Inizialmente<br />
saranno i linfonodi satelliti, cioè quelli di riferimento per la zona in cui nasce e<br />
comincia a diffondersi il tumore. Il linfatico efferente provocherà la diffusione a<br />
linfonodi collegati, ma anche saltando possibilmente delle stazioni: è<br />
possibile p.es in un carcinoma della mammella una linfoadenopatia<br />
sottoclaveare (Vichrow) che risparmia l’ascella.<br />
• via ematica: tendenzialmente dei sarcomi (connettivali). Diciamo che rappresenta la<br />
forma di diffusione successiva ai linfonodi ed al sistema linfatico. A questo<br />
livello la metastasi non è data dalla singola cellula, ma da un gruppo di<br />
cellule, che quando arrivano in una sede (polmone ad.es) andranno a porsi a<br />
livello terminale di un vaso, un po’ come un embolo. Sarà a livello del<br />
microvaso sanguigno che poi partirà l’invasione. Sono quindi forse in parte<br />
inutili gli studi sui recettori che dovrebbero mediare una diapedesi della<br />
cellula nel tessuto da infiltrare.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 52
• via trans celomatica: nelle sierose. Tipicamente il tumore di Kruckenberg, che dallo<br />
stomaco attraverso la cavità peritoneale si porta all’ovaio. Può<br />
trattarsi anche della pleura, e tramite questa la parete della cavità<br />
toracica. Avendo le pleure recettori dolorifici, il risultato di questo<br />
processo è un riscontro dolorifico.<br />
<br />
Neoangiogenesi<br />
(opzionale da sapere)<br />
L’Hypoxia Induced Factor (HIF) induce la neoangiogenesi, principalmente tramite il VEGF, ed è un elemento<br />
in grado di definire un tumore come più aggressivo. La p53 anche in questa sede avrebbe un ruolo nel<br />
controllo della neoangiogenesi (favorisce gli enzimi degradanti l’HIF, al contrario della pr39).<br />
La VHF, o sindrome di Von Hippel Lindau compare spesso in bambini, dove viene identificato grazie alla<br />
comparsa di angiomi cutanei, che possono corrispondere ad analoghe strutture cerebrali. Questi blastomi<br />
sarebbero indotti dal fattore HIF: il gene VHF produrrebbe infatti una proteina in grado di complessarsi con<br />
altre proteine a formare un complesso in grado di ubiquitinizzare l’HIF.<br />
Ci sono elementi in grado di ridurre normalmente l’attività angiogenetica:<br />
In terapia si possono usare anche<br />
• plasminogeno ⇒ ⊕ angiostatina<br />
• collagene ⇒ ⊕ endostatina tumstatina<br />
• talidomide (farmaco inizialmente antinausea, teratogeno proprio a cause delle sue<br />
proprietà anti angiogenetiche)<br />
• analoghi del VEGF o VEGF-R<br />
• MoAb (Mono clonal Ab)<br />
è una sindrome biologico clinica caratterizzata da (5):<br />
<br />
Cachessia<br />
- anemia<br />
- anoressia<br />
- astenia<br />
- dimagrimento<br />
- modificazione della composizione dei liquidi corporei<br />
Nb: la cachessia non è specifica della malattia tumorale. Si possono fare degli esempi<br />
• malattia neoplastica<br />
• suppurazioni croniche<br />
• ICC<br />
• nefrite cronica<br />
• denutrizione<br />
• malattie endocrine<br />
• senilità<br />
• AIDS<br />
• tubercolosi<br />
• lebbra<br />
• Crohn<br />
• BPCO<br />
• fibrosi cistica<br />
• ustioni estese<br />
• …<br />
I meccanismi sono diversi, ma non è dovuto al consumo energetico del tumore.<br />
1) TNF, IFNγ ⇒ sintesi miosina (i pazienti non hanno più grasso, ma anche la massa muscolare si<br />
ritrova drammaticamente ridotta)<br />
2) IL-6 ⇒ ⊕ ubiquitina ⇒ miosina ↓<br />
3) PIF (Proteolysis Induced Facotor)<br />
4) TNF ⇒ leptina, insulina ⇒ CRH (neuropeptidi anoressigenici) ⇒ erc.melanocortina ⇒ NE, Dopa,<br />
5HT ⇒ anoressia, lipolisi.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 53
C.a nel 10% dei casi si accompagnano a tumori.<br />
1) produzione ormonale ectopica<br />
<br />
Sindromi para neoplastiche<br />
- sindrome di Cushing: da cancro a piccole cellule del polmone. Quindi si hanno i<br />
rilievi clinici di un cushing, dovuti ad un tumore<br />
- ipercalcemia (astenia): la prima cosa da pensare in un paziente debole è un<br />
tumore da qualche parte, ed equivale alla stanchezza in<br />
seguito a sforzi debolissimi, diverso dall’essere stanco a<br />
letto. L’astenia è collegata quindi anche a questo aspetto.<br />
Ci sono una serie di neoplasie in cui c’è infatti un’iper<br />
produzione di PTH e PTH related protein:<br />
• carcinoma della mammella<br />
• rene<br />
• ovaio<br />
• polmone<br />
2) neuriti, neuromialgie: possono anche essere sintomi lievi: iper, ipo-estesia, formicolii, o l’isioestesia<br />
(alterazioni della sensiibilità<br />
3) tromboflebiti vaganti: una flebite che da una gamba si estende all’altra, e vanno anche oltre<br />
4) acanthosis nigrans: compaiono delle marezzature nerastre con ipercheratosi…<br />
• polmoni<br />
• utero<br />
• stomaco<br />
5) osteoartropatia ipertrofica: si basa sulla neoproliferazione di tessuti a livello periferico, da cui anche<br />
l’ippocratismo digitale, soprattutto in pneumopatie ed in <strong>generale</strong><br />
patologie da mancata perfusione tissutale.<br />
6) CID: ormai è tardi, ma in <strong>generale</strong> è dovuto a..<br />
• cancro della prostata<br />
Ag oncofetali<br />
<br />
Markers Tumorali<br />
(cfr. anche il meeting “markers tumorali”, con la lezione del prof. G.Grassi)<br />
a. CEA (Carcino Embrionic Ag): lo si può trovare altissimo, ma può essere assolutamente nn<br />
informativo.. Non è specifico, ed aumenta in numerose forme di neoplasie anche.<br />
b. AFP (alfa-feto proteina): già àpiù specifico, per cancro del fegato e testicolo<br />
Ag tumori specifici<br />
a. PSA: per la prostata, che è un tumore molto e a s y se preso in tempo.<br />
b. calcitonina: nel cancro della tiroide (che viene anche ad essere una forma di EA, Amiloide<br />
Endocrina).<br />
c. serotonina (ac.vanilmandelico nelle urine): è da carcinoide, se viene individuato in tempo si<br />
può togliere senza problemi e può essere bronchiale, appendicolare, pancreatico,<br />
gastrico… è aumentata anche nel feocromocitorma (cancro della midollare del<br />
surrene, è la forma benigna) ⇒ NE↑<br />
d. HCG (Human Chorionic Gonadotropin): cancro del testicolo<br />
mucine<br />
nuovi<br />
a. APC<br />
b. p53<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 54
Ormai non si hanno più dubbi sul fatto che le cellule dei tumori maligni siano di derivazione midollare.<br />
E’ chiaro quindi che lo schema precedentemente visto salta completamente, perché una cellula staminale<br />
midollare ha già caratteristiche quali<br />
- fenotipo indifferenziato<br />
- mancanza di elementi di adesione<br />
- moltiplicazione illimitata<br />
- telomerasi ON<br />
Non ha cioè bisogno della progressione. Il tumore si può sviluppare a partire da una staminale che si trovi<br />
in diversi stadi:<br />
1) cellula totipotente ⇒ carcinomi embrionali: cattivissimi<br />
2) cellula parzialmente differenziata ⇒ cancro poco differenziato: comunque cattivo<br />
3) cellula che ha potuto differenziarsi ⇒ cancro ben differenziato: che assume le caratteristiche<br />
istologiche di quel tessuto<br />
4) cellula terminalmente differenziata ⇒ tumore benigno<br />
Le staminali sono a doppio taglio dunque: se da una parte i fatti infiammatori locali sono un richiamo per<br />
cellule totipotenti midollari con funzione riparatoria, dall’altra possono sviluppare un tumore, sia perché sono<br />
mutate già nel midollo, sia perché subiscono mutazioni in fasi successive, come visto sopra.<br />
Quella che alla fin fine farà la maggior parte della trasformazione sarà comunque l’instabilità genomica, che<br />
farà sì che la cellula non si ripari ma diventi maligna, al di là delle mutazioni spicciole, per cui uno stimolo<br />
(come p.es il danno da elicobacter pylori nello stomaco) che normalmente non dovrebbe essere scatenante,<br />
diventa il trigger per cui queste cellule predisposte perdono il controllo e danno un tumore.<br />
§<br />
Ereditarietà & Neoplasie<br />
Si conoscono diverse sindromi ereditarie: quasi certezza della comparsa di neoplasia. Sono situazioni<br />
emblematiche, scontate quasi..<br />
- APC (Adenomatous Polyposis Coli) ⇒ T.colon, intestino, endometrio<br />
- MEN-1/2 (Multiple Endocrine Neoplasia): dovuto all’oncogene RET, il paziente va incontro a diverse<br />
neoplasie a carico di ghiandole endocrine (tiroide, paratiroide, surrene, neurofibromatosi…)<br />
- Sindrome di Li Fraumeni: caratterizzata dalla perdita di un allele di p53. Autosomica dominante.<br />
- Retinoblastoma: spesso bilaterale, che si può sommare all’osteosarcoma. Questi due sono tra i<br />
peggiori cancri che ci siano.<br />
- Xeroderma Pigmentoso: è alterato un gene care taker, il Nucleotide Excision Repair (NER). Questi<br />
soggetti hanno tremende dermatiti in seguito ad esposizione agli UV (sole,<br />
neon…), che col tempo diventano tumori cutanei. Questi soggetti sono più<br />
esposti inoltre in linea <strong>generale</strong> allo sviluppo di altri tumori (instabilità<br />
genomica)<br />
- Atassia Teleangectasia: l’ATM è un sensore di danno. Quindi i soggetti hanno disturbi della motilità<br />
(mancanza di coordinazione) che si associa ad angiomi. Diciamo che l’ATM<br />
attiva la p53, quindi è lo stesso tipo di danno.<br />
- Anemia di Fanconi: si tratta di forme di anemizzazione dovute ad aplasie midollare e/o ipoplasia del<br />
tessuto che crea i leucociti. Predispone alla <strong>patologia</strong> tumorale, grazie a<br />
mutazioni a carico di elementi come il RAD-51, BRCA-1…<br />
- Tumori Familiari: patogenesi multifattoriale, con un rischio aumentato 2-3x.<br />
Si tratta p.es del cancro della mammella o del colon, ovaio, cervello, melanomi…<br />
non è tragicamente alta come probabilità quindi, ma c’è, ed è legato a deficienze del<br />
BRCA-1/2.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 56
Retinoblastoma<br />
In questo caso è fondamentale il gene “RB”, che controlla il passaggio da G1 a S: normalmente il fattore RB<br />
inibisce infatti il fattore E2F, quindi le cicline fosforilano l’RB che perde l’affinità e l’E2F è libero di<br />
stimolare la moltiplicazione<br />
Esistono sia casi ereditari che sporadici. Si pensa che nei casi di ereditarietà ci sia già un allele mutato; una<br />
seconda mutazione determinerà lo sviluppo del cancro. Al contrario i casi sporadici hanno bisogno di due<br />
mutazioni, per cui l’età di insorgenza sarà in genere più tardiva.<br />
E’ un classico caso di loss of eterozigosity, perdita di eterozigosità.<br />
Alterazioni Epigenetiche (acquisite) associate alla progressione Tumorale<br />
1) PAX 1-9: Sono stati individuati dei geni detti PAX, che sono embrionali e codificano per fattori di<br />
trascrizione per la regolazione di accrescimento, sopravvivenza, differenziazione di<br />
tessuti embrionali, ma che possono riattivarsi nell’adulto con funzioni riparative; alcuni<br />
risultano addirittura oncosoppressori, ma molti sono oncogeni.<br />
2) oncomirs (miroRNAs): sono piccoli spezzoni che vanno a interferire con la trascrizione dell’RNA.<br />
Essendo brevi sono poco specifici, possono cioè interagire con una moltitudine<br />
di geni che abbiano un segmento in comune. E’ un sistema di controllo innato<br />
della cellula, che va a controllare gruppi di geni, e che possono avere una<br />
valenza terapeutica (terapia genica: p.es ce ne sono in grado di inibire il<br />
Bcl-2). Si tratta più tipicamente di regioni fragili correlate all’instabilità<br />
genomica.<br />
3) DNA methylation Pattern: si sa che la metilazione del DNA avviene a livello delle “CPG islands”<br />
sparse nel genoma, ed equivale ad una inattivazione di quei tratti. Durante<br />
la fecondazione 22 si ha un fatto epigenetico, un evento nuovo, che vede<br />
metilazioni e de metilazioni, per cui certi geni possono risultare attivi,<br />
anche in modo dannoso, procurando una maggiore propensione alla<br />
moltiplicazione cellulare.<br />
<br />
Predisposizione Non Ereditaria alle Neoplasie<br />
1) iperplasia, quella endometriale p.es può dare origine a displasia della cervice, oppure quella da<br />
cheratosi solare<br />
2) metaplasia: cambiamento del fenotipo. Pur mantenendosi nell’ambito di quello stesso tessuto di<br />
derivazione embrionale (l’epitelio resta epitelio, come dire..). Nei fumatori p.es si ha la<br />
metaplasia bronchiale, che diventa dopo una serie di mutazioni pavimentoso, e che può<br />
portare ad un carcinoma squamocellulare del polmone…<br />
⇒ leucoplachie: tipicamente per la presenza di protesi, si assume a meta e iper - plasia.. si vede<br />
come la formazione di un placca bianca protettiva p.es in casi di protesi dentarie, come<br />
risposta allo sfregamento..<br />
3) cirrosi: questa, di per se, nell’ambito rigenerativo, qualche cellula può risultare mutata…<br />
4) infiammazione: si tratta dei ROI (Reactive Oxygen Intermediates), che possono portare ad<br />
instabilità genomica (COX2): colite ulcerosa, m. di Crohn, gastrite, epatiti,<br />
pancreatite cronica… si notano effetti benefici dell’aspirina. Sostanzialmente quindi<br />
là dove c’è una infiammazione è più facile che ci sia reclutamento di staminali<br />
midollari, che possono quindi sviluppare il tumore.<br />
22 La fecondazione in vitro si associa spesso a malattie da alterato “imprinting”, cioè con alterazioni di questo tipo di<br />
meccanismi di metilazione.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 57
Pron. “fogelstain”.<br />
<br />
Cancerogenesi<br />
(modello di Volgestein)<br />
E’ il modello prima dell’ipotesi midollare, che può ancora essere considerato valido, sempre che venga riferito<br />
alla cellula staminale di per sé.<br />
1) iniziazione: p.es una irritazione = I mutazione (congenita - acquisita)<br />
2) promozione = moltiplicazione cellulare<br />
a. alcool / fumo<br />
b. grassi alimentari (incidenza di tumore al colon dei giapponesi)<br />
c. estrogeni<br />
3) progressione = accumulo di mutazioni<br />
es: distruzione APC ⊕ COX (aspirina) RAS p53↓ TGFβ cancro del colon<br />
Quello che è importante che rimanga è il concetto di gerarchia delle alterazioni: cioè, queste mutazioni non<br />
hanno tutte le stesso peso! questo è importante per applicare terapie geniche mirate.<br />
Cancerogenesi Chimica<br />
Parlando di sostanze chimiche, la caratteristica principe è la capacità di indurre una :<br />
1) essere elettrofile, in modo di legare direttamente il DNA<br />
2) formare addotti, cioè complessi covalenti col DNA<br />
3) replicazione: la cellula deve essere poi una cellula che si replichi. Questa “aggiunta”, l’addotto, genererà<br />
un errore di lettura, che nel contesto della replicazione genererà una mutazione nella<br />
cellula figlia.<br />
Questo modello della cancerogenesi chimica è stato studiato con un esperimento:<br />
Si pennella la cute di un topo col catrame per indurre un tumore cutaneo. Servono più pennellate per indurre il tumore.<br />
Pennellando solo una volta non si induce il tumore, a meno di non applicare poi olio di croton, che applicato da solo non<br />
induce nessun tumore. Questo ha definito la differenza tra iniziatore (prima pennellata di catrame) e promozione (altro<br />
catrame o olio di croton).<br />
In molti cancri si nota la presenza di un’impronta digitale: sono specifici per alcune sequenze di basi: p.es<br />
- aflatossina ⇒ p53<br />
- cancerogeni chimici in <strong>generale</strong> ⇒ p21<br />
1) cancerogeni diretti<br />
Così come sono risultano cancerogeni (sono elettrofili, formano addotti). Questa categoria<br />
fortunatamente è minimale, rispetto alla gran maggioranza.<br />
Sono tipicamente utilizzati come antiblastici: ciclofosfamide - endoxan, clorambucil, melata,<br />
nitrosourea.<br />
2) cancerogeni indiretti: tipicamente richiedono un’attivazione. da sapere<br />
a. idrocarburi aromatici policiclici: p.es da parte del P450 (citocromo), come per il fumo di<br />
sigaretta, alimenti bruciati, derivati del benzolo…<br />
» benzo-pirene<br />
» benzo-antracene<br />
b. amine aromatiche<br />
» β naftil amina: è un colorante. Quello che succede è che l’anilina viene trasformata<br />
in β naftil amina, glucuronata a livello epatico viene filtrata ed accumulata nella<br />
vescica con l’urina, dove una glucuronidasi urinaria provocava il cancro della<br />
vescica.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 58
c. nitrosamine: i nitrati vengono usati come fertilizzanti. Esistono però dei batteri nitrificanti,<br />
che li trasformano in nitriti, che sono senz’altro alla base di alcune forme di<br />
cancro dello stomaco. Il problema non si pone per la verdura fresca, ma per<br />
quella conservata (scatolame…)<br />
d. coloranti azoici<br />
» A127: un tempo era utilizzato nella fanta<br />
e. cancerogeni “naturali”<br />
» aflatossina-B1: è la contaminazione da parte dell’Aspergillus flavus del granoturco<br />
che determina la formazione della tossina, la quale in soggetti con HBV può<br />
provocare il cancro del fegato<br />
» griseofulvina<br />
f. altri<br />
» Asbesto (amianto): si associa con<br />
mesotelioma pleurico<br />
cancro del polmone<br />
» cromo, nikel<br />
cancro del polmone<br />
» arsenico<br />
carcinoma cutaneo<br />
» diossina ⇒ sregolazione geni PAX<br />
<br />
Alterazioni citogenetiche & Neoplasie<br />
(ereditarie / acquisite)<br />
a. alterazioni cromosomiche (traslocazioni, inversioni)<br />
b. amplificazioni<br />
- linfoma di Burkitt: si ha la translocazione 8 -14 del gene myc, che si inserisce<br />
al posto del gene delle Ig, che sono un gene estremamente up regolato (devono<br />
essere continuamente prodotte). Ovviamente stiamo parlando di linfociti B<br />
- Chr Filadelfia: CML (Chronic Myelogenous Leukemia): si trovano giustapposti<br />
per una translocazione 9-22 i geni..<br />
• abl (oncogeno)<br />
• Bcr<br />
⇒ produzione di una TK molto attiva, che induce la proliferazione.<br />
L’imatinib è un farmaco creato apposta per combattere questo meccanismo, ed è<br />
molto efficace, tanto da aver trasformato queste leucemie mieloidi da acute a<br />
croniche. Non si ha guarigione, solo cronicizzazione, anche se attualmente si<br />
stanno facendo tentativi con la contemporanea somministrazione di antiblastici<br />
classici.<br />
- HSR (Homogeneously Staining Region): p.es del gene N-myc, che viene<br />
amplificato enormemente, e al posto della classica colorazione a bande del<br />
cromosoma si nota una colorazione omogenea.<br />
c. double minutes: frammenti di cromosoma<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 59
Cancerogenesi Virale<br />
esistono come noto virus dotati di materiale genetico a RNA e DNA, di fatto le possibilità sono diverse<br />
Virus a RNA<br />
Si tratta di virus generalmente dotati di trascrittasi inversa, sicuramente:<br />
Virus a DNA<br />
HCV: chiaramente e predispone al carcinoma epatico, anche se non è chiara la patogenesi.<br />
Potrebbero esserci collegamenti tra cirrosi e moltiplicazione cellulare.<br />
HTLV-1 (Human Tcell Leukemia Virus -1): colpisce invece i linfociti di tipo CD4 +<br />
- latenza estremamente lunga<br />
- endemico in Giappone e presente ai caraibi<br />
di fatto inibisce elementi quali: ATM (sensore di danno), e p16 (proteina di controllo<br />
delle cicline). Inoltre ha la capacità di stimolare fattori di moltiplicazione come la IL-2.<br />
Hepadna Virus: tra cui sicuramente ricordiamo L'HBV: si associa al carcinoma del fegato;<br />
endemico in Africa ed in estremo oriente<br />
Una proteina sintetizzata dal virus ha la capacità di legare la p53…<br />
⇒ flogosi, aflatossina, che può partecipare alla genesi di carcinomi epatici<br />
(che si sviluppa dopo anni di cirrosi).<br />
EBV (γ herpes virus): si lega alle cellule B, nello specifico ai recettori CD21. Il virus ha la<br />
capacità di produrre EBNA-2 che di fatto interferisce con l’attività di<br />
a. cicline<br />
b. LMP-1 (Latent Membrane Protein-1)<br />
possiamo dire che le conseguenze possono essere:<br />
- mononucleosi: faringo tonsillite, febbre, astenia, linfoadenopatia e fugace epatite associata a<br />
splenomegalia.<br />
- linfoma di Burkitt che però si verifica solo nelle regioni dove è presente la malaria, che<br />
sembrerebbe stimolare la translocazione 8-14 del myc, appunto.<br />
- linfoma a cellule B: negli immunodepressi, pazienti affetti da AIDS o sotto trattamento<br />
- carcinoma nasofaringeo; si verifica unicamente in Cina meridionale, non è dato sapere<br />
perché. Si tratta di un tumore solido del faringe.<br />
- linfoma di Hodgkin: si tratta di un linfoma che esiste anche da noi. Ricordiamo che è un<br />
tumore solido. Il marker caratteristico sono le cellule di Sternberg:<br />
sono linfociti B molto grandi, si pensa che la loro presenza determini:<br />
a) sintesi di fattori di crescita<br />
b) proliferazione delle cellule B e T.<br />
l’effetto definitivo è legato alla presenza di fattori di stimolazione e costimolazione…<br />
• associazione al CD21 & infezione della cellula<br />
• mononucleosi infettiva: proteine virali ⇒ ⊕proliferazione cellulare<br />
• esposizione di mAg virali<br />
CTL: morte cellulare<br />
mutazione delle cellule: translocazione 8-14 ⇒ ⊕c-myc ⇒ linfoma<br />
Nb: altre mutazioni possono poi contribuire al processo tumorale.<br />
HPV (Human Papilloma Virus), esistono diverse sottofamiglie di papilloma virus:<br />
- 1, 2, 4, 6, 7, 11 ⇒ benigni: verruche e papillomi…<br />
- 16, 18, 31 ⇒ maligni: carcinoma della cervice uterina<br />
tutte queste forme virali producono proteine quali…<br />
- E6 ⇒ p53<br />
- E7 ⇒ p53<br />
⇒ p21<br />
⇒ RB /e2F<br />
agiscono cioè sulla capacità della cellule di andare in fase di blocco della crescita e di apoptosi.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 60
La benignità o malignità dell’infezione sembra sia dovuta a..<br />
a) diversa forza di legame proteina / substrato<br />
b) polimorfismi della p53: le forme polimorfiche sono funzionanti in modo<br />
fondamentalmente uguale potremmo ipotizzate, ma presentano<br />
una affinità differente per E6 ed E7. Ci saranno quindi delle<br />
persone più o meno predisposte alla evoluzione in carcinoma.<br />
c) risk factors: il genoma integrandosi tende perde parte dei meccanismi di autocontrollo<br />
alla produzione dei fattori, inoltre possono considerando<br />
» fumo<br />
» estrogeni<br />
si giustifica in modo ancor più significativo la trasformazione neoplastica.<br />
Da una lesione in itinere e in fase di avanzamento, si precisano le tappe dal<br />
punto di vista istologico essenziale per il PAP test, si hanno in ordine:<br />
1) metaplasia cioè cambiamenti fenotipici della struttura cellulare.<br />
2) displasia: dove non è riconoscibile un tessuto epiteliale normale.<br />
3) carcinoma in situ: la cellula è chiaramente e francamente neoplastica, in<br />
corrispondenza di un tessuto epiteliale, ma che non ha ancora<br />
attraversato la membrana basale.<br />
4) carcinoma.<br />
l'evoluzione poi è legata prevalentemente alla presenza di fattori di crescita e mutageni. In ogni<br />
caso la metaplasia permane presente, non torna indietro.<br />
SKV (Sarcoma Kaposi Virus): sappiamo che blocca la proteina p53 ed è spesso una conseguenza<br />
dell'AIDS. Questi virus a DNA tendono a<br />
integrarsi nel genoma: abbastanza di frequente.. una volta integrati, non si<br />
replicano in quanto vengono persi i meccanismi di<br />
amplificazione.<br />
formare episomi: si tratta di frammenti di DNA posti al di fuori dei cromosomi<br />
sintetizzare proteine, che rendono le cellule antigenicamente riconoscibili<br />
<br />
Immunologia dei Tumori<br />
Esistono degli Ag tumorali ben conosciuti, purtroppo spesso le cellule tumorali però subiscono dei<br />
cambiamenti che risultano protettivi:<br />
1) assenza di Ag (improbabile)<br />
2) sotto espressione dell’MHC-I ⇒ soppressione della risposta specifica (T citotossica), che è<br />
MHC ristretta. Si sono fatti studi su tentativi di restaurare<br />
questo tipo di risposta, ma non hanno portato a nulla<br />
3) produzione di citochine soppressorie: TGFβ in primis.<br />
4) proprietà coagulanti: in questo modo quando la cellula entra in circolo viene ricoperta da<br />
piastrine, in modo da non venir riconosciuta e sfuggire al SI.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 61
Patologia Genetica<br />
Mutazioni puntiformi<br />
1) di sequenze codificanti<br />
- sense: un AA al posto di un altro<br />
• benigna<br />
• non conservativa (es. β-globina in an. falciforme)<br />
- non sense: se p.es diventa una tripletta di stop (es. β-globina in β 0 talassamia)<br />
2) di sequenze non codificanti<br />
- seq. promoter, enhancer (talassemie α, β)<br />
Mutazioni di sequenze<br />
Si parla di pozioni codificanti (delezioni, inserzioni)<br />
a. frame shift mutation<br />
• perdita di una base per gluc. Transfer. gr. sanguigno 0<br />
• inserzione di quadripletta in Tay Sachs<br />
b. non frame shift (multipli di 3)<br />
• delezione di fenil alanina in fibrosi cistica<br />
c. da amplificazione di triplette (contenenti G,C)<br />
• malattie da triplette<br />
» sindrome dell’X fragile<br />
» Familiar Mental Retardation (FMR): si ha comunque ritardo<br />
mentale, e riguarda i maschi<br />
(fenomeno dell’anticipazione 23 ).<br />
Mutazioni con alterazioni Cromosomiche<br />
1) di struttura<br />
2) di numero<br />
- delezioni<br />
- trans locazioni<br />
- inversioni<br />
- formazione di isocromosomi (perdita di un braccio)<br />
- formazione di cromosomi ad anello<br />
- trisomia 21 o Sindrome di Down.<br />
E’ quella maggiormente compatibile con la vita. Contiene geni per le cellule<br />
nervose, per il metabolismo del folato, e per altri meccanismi ancora. Può essere<br />
dovuto ad una disfunzione meiotica dell’ovulo materno, oppure per translocazione<br />
Robertsoniana, mosaicismo…<br />
• facies, ritardo mentale<br />
• cardiopatie congenite<br />
• malattia di Alzheimer<br />
• disturbi immunitari<br />
- non compatibili con la vita: 8,9,13,18,22… morte entro 1 anno<br />
- sessuali<br />
• Turner: 45, X0 (invero mosaici, o solo delezioni): permette la vita, ma con<br />
numerose alterazioni. Tipico è l’igroma del collo, una plica<br />
cutanea a livello della nuca. Solo femmine, sterili.<br />
• S. di Klinefelter: 47, XXY, fino a 49,XXXXXY. Ci possono essere anche<br />
qui dei mosaici (46, XY), ci sarà ipogonadismo e lupus.<br />
Solo maschi.<br />
23<br />
la spiegazione risiede nel fatto che l’espansione delle triplette avviene solo a livello di gametogenesi, ragion per cui i<br />
figli di un individuo che ha già questa <strong>patologia</strong>.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 62
Bisogna considerare alcuni punti (7) :<br />
<br />
Malattie ereditarie<br />
pleiotropismo: molti effetti clinici derivanti da un’unica mutazione<br />
eterogeneità genetica: tante possibile mutazioni per avere lo stesso segno clinico<br />
mutazioni protettive: come la talassemia per la malaria<br />
geni ad ampio effetto: sono le malattie a trasmissione mendeliana<br />
alterazioni dei cromosomi: danno le malattie cromosomiche o genomiche (come app. visto)<br />
malattie ad eredità poligenica: le più complesse, sono le multifattoriali. Predisposizione + trigger<br />
alterazioni epigenetiche: anche dopo la fecondazione ci possono essere mutazioni. E’ ovviamente<br />
fuori da ogni prevedibilità di tipo mendeliano<br />
Malattie mendeliane<br />
Spesso si ha espressione parziale nell’eterozigote, mentre completa nell’omozigote, oppure una<br />
codominanza, dove tutti gli alleli sono espressi (come p.es i gruppi sanguigni AB)<br />
1) penetranza: anche quando si ha una mutazione, bisogna vedere come questa mutazione venga<br />
riequilibrata da altri geni, che suppliscono o contrastano quella determinata<br />
alterazione, così come anche l’ambiente potrà influire pro o contro.<br />
2) espressività: una volta appurato che c’è la malattia, ne stabilisce la gravità.<br />
3) gain of function: p.es l’espansione delle triplette CAG 24 avviene tipicamente nella<br />
gametogenesi, ovviamente se da un punto di vista ereditario si avrà una<br />
amplificazione del numero di triplette man mano, e questo darà luogo al<br />
fenomeno dell’anticipazione.<br />
4) loss of function: p.es nella dominanza negativa, che abbiamo visto per la p53: basta che una<br />
delle 4 subunità sia alterata e non funziona tutta la proteina, o come nella<br />
sindrome di Marphan, dove solo una subunità collagenica mutata porta alla<br />
compromissione di tutta la struttura.<br />
5) evasione da regolazione a feedback complessa: p.es nell’ipercolesterolemia la riduzione del<br />
50% del recettore LDL.<br />
6) malattie recessive: sono abbastanza uniformi, tipicamente si tratta di tutte quelle<br />
metaboliche. Anche se metà enzima funziona, funziona. Quando<br />
capitano in omozigosi o sono incompatibili con la vita o si manifestano<br />
con grande precocità (pediatriche).<br />
7) malattie collegate ai Chr sessuali: ci sono diverse possibilità<br />
- Chr Y: mutazione nella spermatogenesi sterilità<br />
- Chr X: se un solo X sarà patologico avrà nella donna carattere recessivo. Ci può<br />
essere in questo caso un 50% di espressione (nella specializzazione uno dei due X<br />
viene silenziato a caso). Nella G6PDH deficienza (favismo), pur essendo la<br />
<strong>patologia</strong> recessiva, si nota un lieve grado di emolisi.<br />
- nel maschio: XY è sicuro espresso (emofilie, Chronic Granulomatouse Disease…)<br />
24 nell’Huntigton questo porta alla formazione di una proteina nota come Huntingtina.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 63
Glucocorticoide endogeno ⇒ cortisolo<br />
Glucocorticoidi<br />
Sappiamo bene quali siano i caratteri dell’infiammazione. Come ben si sa l’infiammazione è alla base sia di<br />
meccanismi positivi, in risposta ad insulti di microrganismi esterni, ma d’altra parte moltissime patologie<br />
derivano da un suo eccesso.<br />
La zona fascicolata è alla base della produzione del cortisolo a partire dal colesterolo, così come aldosterone<br />
e testosterone.<br />
1) nell’ipotalamo si ha rilascio di CRH in seguito alle citochine immesse in circolo dal SI<br />
2) le afferenze dolorose convergono altrettanto a stimolare il rilascio di CRH<br />
3) nell’ipofisi anteriore si produce sotto stimolo del CRH l’ACTH<br />
4) il cortisolo come gran parte degli ormoni ha azione di feedback negativo<br />
5) altri effetti, evidenti soprattutto in terapie con cortisone di tipo cronico si ripercuotono su<br />
a. fegato (iperglicemizzante: ⊕gluconeogenesi)<br />
b. muscoli (atrofia dovuta ad insulino resistenza)<br />
c. tessuto adiposo (consunzione delle scorte)<br />
Il cortisolo ha un recettore citoplasmatico α, che è ubiquitario (in tutte le cellule), ma iper espresso nelle<br />
cellule dell’infiammazione. Il recettore è legato all’HSP90, utile a mantenerlo in una conformazione adeguata<br />
per favorire il legame col cortisolo. Il recettore β non porta a nulla ed è regolatorio.<br />
Dall’unione con l’ormone si forma un etero dimero, che ha una azione a livello nucleare, di regolazione<br />
genica.<br />
prod. metalloproteasi, firbine, citochine<br />
Tra le proteine indotte si ha la annessina I che va ad inibire la produzione dell’acido arachidonico legandosi<br />
alla PLA-2. Ricordiamo in questo contesto l’importanza dell’NF-κB, un fattore che viene appunto inibito dal<br />
cortisolo.<br />
Riassumendo gli effetti del cortisolo<br />
⊕ produzione di enzimi ⇒ coinvolti nel metabolismo del glucosio (iperglicemizzanti)<br />
⊕ prod. annessina-1<br />
COX-2, IFNγ, TNFα, IL-2,6,8 collagenasi, E-selectina. Ricordiamo che l’IL-2 è il nodo fondamentale per<br />
la moltiplicazione linfocitaria. Questo si aggiunge all’effetto apoptotico sui linfociti, determinando<br />
l’immunosoppressione.<br />
In definitiva l’azione cardine nell’impedire l’infiammazione, a più breve termine, è la diminuzione del flusso<br />
del microcircolo, che impedisce l’arrivo dei vari fattori infiammatori, l’effetto mediato dagli effetti sulla<br />
trascrizione è più tardivo.<br />
Effetti collaterali<br />
ipertensione endocranica: dovuto all’aumento della responsività alle catecolammine<br />
effetti centrali: attraversa la BBB, e si possono avere sintomi psicotici depressivi<br />
gobba di bufalo: dovuta alla redistribuzione del tessuto adiposo, che oltrettutto tende ad accumularsi<br />
in addome. Questo forse perché questi adipociti rispondono all’insulina ma non ai<br />
glucocorticoidi (quindi non subisocno l’effetto lipolitico)<br />
VCE↑: agendo sui recettori dell’aldosterone tende ad aumentare la volemia<br />
assottigliamento della pelle: agisce sulle fibre elastiche della cute<br />
ecchimosi facili: sempre dovuto al catabolismo delle fibre elastiche<br />
osteoporosi: scaturisce dall’induzione degli osteoclasti, che avviene tramite la sintesi di una specifica<br />
proteina con quest’effetto.<br />
tendenza all’iperglicemia: porta a slatentizzazione del diabete<br />
immunodepressione<br />
atrofia muscolare<br />
Diciamo che gli effetti collaterali derivano dalla proprietà del cortisolo di indurre la produzione di proteine.<br />
L’effetto anti infiammatorio deriva invece dalla sua proprietà di bloccare la sintesi di citochine e la PLA-2.<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 65
Nota<br />
Questa è una raccolta di appunti, sintesi di materiale preso da diversissime fonti e rielaborato; come tale non<br />
è impassibile di errori, ANZI. Quindi inviterei a :<br />
1. non prendere tutto quello che c’è scritto per oro colato<br />
2. contattarmi se c’è qualcosa di sbagliato all’indirizzo<br />
theshire88@gmail.com<br />
Grazie a tutti e buono studio !!<br />
Giuseppe Marini: Patologia Generale <strong>II</strong> (aa.2009/2010) 66