(19) 대한민국특허청(KR) (12) 공개특허공보(A) - Questel
(19) 대한민국특허청(KR) (12) 공개특허공보(A) - Questel
(19) 대한민국특허청(KR) (12) 공개특허공보(A) - Questel
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
(51) Int. Cl.<br />
(<strong>19</strong>) <strong>대한민국특허청</strong>(<strong>KR</strong>)<br />
(<strong>12</strong>) <strong>공개특허공보</strong>(A)<br />
A61K 39/395 (2006.01) C07K 16/24 (2006.01)<br />
C07H 21/04 (2006.01) A61P 29/00 (2006.01)<br />
(21) 출원번호 10-2011-7014632<br />
(22) 출원일자(국제출원일자) 2009년11월24일<br />
심사청구일자 없음<br />
(85) 번역문제출일자 2011년06월24일<br />
(86) 국제출원번호 PCT/US2009/006274<br />
(87) 국제공개번호 WO 2010/065079<br />
국제공개일자 2010년06월10일<br />
(30) 우선권주장<br />
<strong>12</strong>/366,567 2009년02월05일 미국(US)<br />
(뒷면에 계속)<br />
전체 청구항 수 : 총 200 항<br />
(54) IL6에 대한 항체 및 이의 용도<br />
(57) 요 약<br />
(11) 공개번호 10-2011-01<strong>12</strong>308<br />
(43) 공개일자 2011년10월<strong>12</strong>일<br />
(71) 출원인<br />
앨더 바이오파마슈티컬즈, 인코포레이티드<br />
미국 워싱턴 바슬 노쓰 크릭 파크웨이 싸우스<br />
11804 (우: 98011)<br />
(72) 발명자<br />
가르시아 - 마르틴즈, 레온<br />
미국 98072 워싱턴 우딘빌 에스.이. 214 스트리트<br />
4926<br />
젠센, 앤 엘리자베쓰 카발호<br />
미국 98725 워싱턴 머킬테오 하버 포인테 블러바<br />
드 <strong>12</strong>303<br />
(뒷면에 계속)<br />
(74) 대리인<br />
남상선<br />
본 발명은 질병을 예방하거나 치료하고, 또는 병든 환자의 생존력 또는 삶의 질을 개선하기 위하여, IL-6에 대한<br />
결합 특이성을 갖는 IL-6 길항제, 예를 들면, Ab1 항체 또는 항체 단편을 이용한 치료 방법에 관계한다. 바람직<br />
한 구체예에서, 이들 환자는 치료 이전에 상승된 혈청 C-반응성 단백질 수준, 감소된 혈청 알부민 수준, 상승된<br />
D-이합체 또는 다른 혈액응고 연쇄고리(coagulation cascade) 관련된 단백질(들), 악액질, 발열, 쇠약 및/또는<br />
피로를 나타내는(또는 이들이 발생할 위험이 있는) 환자를 포함할 것이다. 본 발명의 요법은 또한, 다른 활성제,<br />
예를 들면, 화학요법제, 항-응고제, 스타틴 등의 투여를 포함할 수 있다.<br />
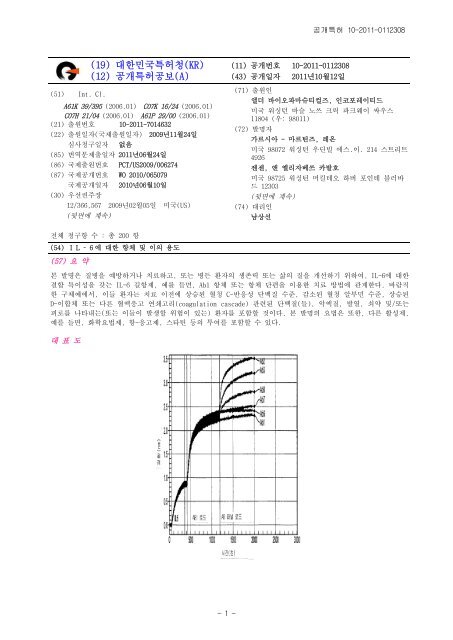
대 표 도<br />
- 1 -<br />
공개특허 10-2011-01<strong>12</strong>308
(72) 발명자<br />
올슨, 카티에<br />
미국 98028 워싱턴 켄모어 엔이 182 스트리트 #<br />
디207 6700<br />
더찰, 벤<br />
미국 98109 워싱턴 시애틀 #204 덱스터 애브뉴 노<br />
오쓰 2422<br />
레이덤, 존<br />
미국 981<strong>19</strong> 워싱턴 시애틀 10 애브뉴 2409<br />
코바스비치, 브라이언<br />
미국 98296 워싱턴 스노호미시 에스이 233 스트리<br />
트 13916<br />
스미쓰, 제프리 티. 엘.<br />
미국 98004 워싱턴 벨뷰 엔. 이. <strong>12</strong> 스트리트<br />
10270 아파트먼트 에프307<br />
리톤, 마크<br />
미국 981<strong>19</strong> 워싱턴 시애틀 웨스트 라이 스트리트<br />
913<br />
슈엣츠만, 란달<br />
미국 98053 워싱턴 레드몬드 엔이 238 플레이스<br />
5733<br />
- 2 -<br />
(30) 우선권주장<br />
공개특허 10-2011-01<strong>12</strong>308<br />
<strong>12</strong>/391,615 2009년02월24일 미국(US)<br />
<strong>12</strong>/391,717 2009년02월24일 미국(US)<br />
<strong>12</strong>/399,156 2009년03월06일 미국(US)<br />
<strong>12</strong>/502,581 2009년07월14일 미국(US)<br />
61/117,811 2008년11월25일 미국(US)<br />
61/117,839 2008년11월25일 미국(US)<br />
61/117,861 2008년11월25일 미국(US)
특허청구의 범위<br />
청구항 1<br />
IL-6과 연관된 질환 또는 이상을 예방, 치료, 또는 진단하는 방법으로서, 상기 방법은 Ab1 항체 또는 항체 단편<br />
을 병든 개체에 투여하는 단계를 포함하고, 여기서 Ab1 항체 및 항체 단편은<br />
서열 번호: 709에 적어도 75% 동일성을 갖는 폴리펩티드, 서열 번호: 723의 폴리뉴클레오티드에 적어도 75% 동<br />
일성을 갖는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드, 중간 엄밀도(stringency) 조건 하에 서열 번호:<br />
723의 역상보 서열을 갖는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티<br />
드, 또는 높은 엄밀도 조건 하에 서열 번호: 723의 역상보 서열을 갖는 폴리뉴클레오티드에 하이브리드화되는<br />
폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드를 포함하는 경쇄 폴리펩티드; 그리고<br />
서열 번호: 657에 적어도 75% 동일성을 갖는 폴리펩티드, 서열 번호: 700의 폴리뉴클레오티드에 적어도 75% 동<br />
일성을 갖는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드, 중간 엄밀도 조건 하에 서열 번호: 700의 역상보<br />
서열을 갖는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드, 또는 높은<br />
엄밀도 조건 하에 서열 번호: 700의 역상보 서열을 갖는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티<br />
드에 의해 인코딩되는 폴리펩티드를 포함하는 중쇄 폴리펩티드를 포함하고;<br />
여기서 Ab1 항체 또는 항체 단편은 IL-6에 특이적으로 결합하고 IL-6과 연관된 한 가지 이상의 활성을<br />
길항하는, 방법.<br />
청구항 2<br />
청구항 1에 있어서, 경쇄 폴리펩티드는 서열 번호: 709의 경쇄 골격 영역 서열과 비교하여, 경쇄 골격 영역(들)<br />
내에서 하나 이상의 치환을 포함하는 것을 특징으로 하는 방법.<br />
청구항 3<br />
청구항 2에 있어서, 경쇄 골격 영역 내에서 하나 이상의 치환은 공여자 서열의 상응하는 위치의 서열에 의한 치<br />
환이고, 여기서 공여자 서열은 서열 번호: 2; 인간, 토끼, 또는 비-인간 영장류 경쇄 서열; 그리고 Ab2, Ab3,<br />
Ab4, Ab5, Ab6, Ab7, Ab8, Ab9, Ab10, Ab11, Ab<strong>12</strong>, Ab13, Ab14, Ab15, Ab16, Ab17, Ab18, Ab<strong>19</strong>, Ab20, Ab21,<br />
Ab22, Ab23, Ab24, Ab25, Ab26, Ab27, Ab28, Ab29, Ab30, Ab31, Ab32, Ab33, Ab34, Ab35, 또는 Ab36 중에서<br />
한 가지의 경쇄를 포함하고,<br />
여기서 치환은 하나 이상의 아미노산의 대체, 삽입 및/또는 결실을 유발하고, 그리고<br />
여기서 상응하는 위치는 서열 번호: 709의 골격 영역과 공여자 서열 사이에 서열 정렬에 의해 결정되는 것을 특<br />
징으로 하는 방법.<br />
청구항 4<br />
청구항 1에 있어서, 중쇄 폴리펩티드는 서열 번호: 657의 중쇄 골격 영역 서열과 비교하여 중쇄 골격 영역 내에<br />
서 하나 이상의 치환을 포함하는 것을 특징으로 하는 방법.<br />
청구항 5<br />
청구항 4에 있어서, 중쇄 골격 영역 내에서 하나 이상의 치환은 공여자 서열의 상응하는 위치의 서열에 의한 치<br />
환이고, 여기서 공여자 서열은 서열 번호: 3; 인간, 토끼, 또는 비-인간 영장류 중쇄 서열; 그리고 Ab2, Ab3,<br />
Ab4, Ab5, Ab6, Ab7, Ab8, Ab9, Ab10, Ab11, Ab<strong>12</strong>, Ab13, Ab14, Ab15, Ab16, Ab17, Ab18, Ab<strong>19</strong>, Ab20, Ab21,<br />
Ab22, Ab23, Ab24, Ab25, Ab26, Ab27, Ab28, Ab29, Ab30, Ab31, Ab32, Ab33, Ab34, Ab35, 또는 Ab36 중에서<br />
한 가지의 중쇄를 포함하고,<br />
여기서 치환은 하나 이상의 아미노산의 대체, 삽입 및/또는 결실을 유발하고, 그리고<br />
여기서 상응하는 위치는 서열 번호: 657의 골격 영역과 공여자 서열 사이에 서열 정렬에 의해 결정되는 것을 특<br />
징으로 하는 방법.<br />
- 3 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 6<br />
청구항 1 내지 5중 어느 한 항에 있어서,<br />
경쇄 폴리펩티드는<br />
서열 번호: 4에 적어도 72.7% 동일성(11개 잔기 중에서 적어도 8개에 동일)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 85.7% 동일성(7개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR2;<br />
서열 번호: 6에 적어도 50% 동일성(<strong>12</strong>개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR3;<br />
서열 번호: 4에 적어도 90.9% 유사성(11개 잔기 중에서 적어도 10개에 유사)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 100% 유사성(7개 잔기 중에서 적어도 7개에 유사)을 갖는 경쇄 CDR2; 또는<br />
서열 번호: 6에 적어도 66.6% 유사성(<strong>12</strong>개 잔기 중에서 적어도 8개에 유사)을 갖는 경쇄 CDR3을 포함하는 하나<br />
이상의 Ab1 경쇄 CDR 폴리펩티드를 포함하고; 그리고<br />
중쇄 폴리펩티드는<br />
서열 번호: 7에 적어도 80% 동일성(5개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 50% 동일성(16개 잔기 중에서 적어도 8개에 동일)을 갖는 중쇄 CDR2;<br />
서열 번호: 9에 적어도 33.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR3;<br />
서열 번호: 7에 적어도 100% 유사성(5개 잔기 중에서 적어도 5개에 유사)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 56.2% 유사성(16개 잔기 중에서 적어도 9개에 유사)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 50% 유사성(<strong>12</strong>개 잔기 중에서 적어도 6개에 유사)을 갖는 중쇄 CDR3을 포함하는 하나 이<br />
상의 Ab1 중쇄 CDR 폴리펩티드를 포함하는 것을 특징으로 하는 방법.<br />
청구항 7<br />
청구항 1 내지 5중 어느 한 항에 있어서,<br />
경쇄 폴리펩티드는<br />
서열 번호: 4에 적어도 81.8% 동일성(11개 잔기 중에서 적어도 9개에 동일)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 71.4% 동일성(7개 잔기 중에서 적어도 5개에 동일)을 갖는 경쇄 CDR2; 또는<br />
서열 번호: 6에 적어도 83.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 10개에 동일)을 갖는 경쇄 CDR3을 포함하는 하나<br />
이상의 Ab1 경쇄 CDR 폴리펩티드를 포함하고; 그리고<br />
중쇄 폴리펩티드는<br />
서열 번호: 7에 적어도 60% 동일성(5개 잔기 중에서 적어도 3개에 동일)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 87.5% 동일성(16개 잔기 중에서 적어도 14개에 동일)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 83.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 10개에 동일)을 갖는 중쇄 CDR3을 포함하는 하나<br />
이상의 Ab1 중쇄 CDR 폴리펩티드를 포함하는 것을 특징으로 하는 방법.<br />
청구항 8<br />
청구항 6 내지 7중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 상기 경쇄 CDR 폴리펩티드 중에서 적어도<br />
2개 및 상기 중쇄 CDR 폴리펩티드 중에서 적어도 2개를 포함하는 것을 특징으로 하는 방법.<br />
청구항 9<br />
IL-6과 연관된 질환 또는 이상을 예방 또는 치료하는 방법으로서, 상기 방법은 Ab1 항체 또는 항체 단편을 병든<br />
개체에 투여하는 단계를 포함하고, 여기서 Ab1 항체 또는 항체 단편은<br />
서열 번호: 4에 적어도 72.7% 동일성(11개 잔기 중에서 적어도 8개에 동일)을 갖는 경쇄 CDR1;<br />
- 4 -<br />
공개특허 10-2011-01<strong>12</strong>308
서열 번호: 5에 적어도 85.7% 동일성(7개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR2; 또는<br />
서열 번호: 6에 적어도 50% 동일성(<strong>12</strong>개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR3을 포함하는 2개 이<br />
상의 Ab1 경쇄 CDR 폴리펩티드; 그리고<br />
서열 번호: 7에 적어도 80% 동일성(5개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 50% 동일성(16개 잔기 중에서 적어도 8개에 동일)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 33.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR3을 포함하는 2개<br />
이상의 Ab1 중쇄 CDR 폴리펩티드를 포함하고;<br />
여기서 Ab1 항체 또는 항체 단편은 IL-6에 특이적으로 결합하고 IL-6과 연관된 한 가지 이상의 활성을<br />
길항하는, 방법.<br />
청구항 10<br />
IL-6과 연관된 질환 또는 이상을 예방 또는 치료하는 방법으로서, 상기 방법은 Ab1 항체 또는 항체 단편을 병든<br />
개체에 투여하는 단계를 포함하고, 여기서 Ab1 항체 또는 항체 단편은<br />
서열 번호: 4에 적어도 90.9% 유사성(11개 잔기 중에서 적어도 10개에 유사)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 100% 유사성(7개 잔기 중에서 적어도 7개에 유사)을 갖는 경쇄 CDR2; 또는<br />
서열 번호: 6에 적어도 66.6% 유사성(<strong>12</strong>개 잔기 중에서 적어도 8개에 유사)을 갖는 경쇄 CDR3을 포함하는 2개<br />
이상의 Ab1 경쇄 CDR 폴리펩티드; 그리고<br />
서열 번호: 7에 적어도 100% 유사성(5개 잔기 중에서 적어도 5개에 유사)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 56.2% 유사성(16개 잔기 중에서 적어도 9개에 유사)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 50% 유사성(<strong>12</strong>개 잔기 중에서 적어도 6개에 유사)을 갖는 중쇄 CDR3을 포함하는 2개 이<br />
상의 Ab1 중쇄 CDR 폴리펩티드를 포함하고;<br />
여기서 Ab1 항체 또는 항체 단편은 IL-6에 특이적으로 결합하고 IL-6과 연관된 한 가지 이상의 활성을<br />
길항하는, 방법.<br />
청구항 11<br />
청구항 9 내지 10중 어느 한 항에 있어서, 상기 Ab1 항체 또는 항체 단편은 상기 경쇄 CDR1, 상기 경쇄 CDR3,<br />
상기 중쇄 CDR2, 그리고 상기 중쇄 CDR3을 포함하는 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong><br />
청구항 9 내지 10중 어느 한 항에 있어서, 상기 Ab1 항체 또는 항체 단편은 상기 경쇄 CDR1, 상기 경쇄 CDR2,<br />
상기 경쇄 CDR3, 상기 중쇄 CDR1, 상기 중쇄 CDR2, 그리고 상기 중쇄 CDR3을 포함하는 것을 특징으로 하는<br />
방법.<br />
청구항 13<br />
청구항 9 내지 <strong>12</strong>중 어느 한 항에 있어서, 상기 경쇄와 중쇄 CDR 폴리펩티드는 Fab, Fab', F(ab')2, Fv, scFv,<br />
IgNAR, SMIP, 카멜바디(camelbody), 또는 나노바디(nanobody)를 포함하는 항체 또는 항체 단편 내에 포함되는<br />
것을 특징으로 하는 방법.<br />
청구항 14<br />
청구항 9 내지 <strong>12</strong>중 어느 한 항에 있어서, 상기 Ab1 항체 또는 항체 단편의 가변 경쇄와 중쇄 영역 각각에서 골<br />
격 영역(FR) 1, 2, 3과 4는 변형되지 않거나, 또는 각각, 서열 번호: 2와 서열 번호: 3의 모(parent) 토끼 항체<br />
경쇄 또는 중쇄의 상응하는 FR 잔기에 의한 2개 또는 3개 정도의 인간 FR 잔기의 치환에 의해 변형된, 인간 FR<br />
이고,<br />
공개특허 10-2011-01<strong>12</strong>308<br />
여기서 상기 인간 경쇄 FR 1, 2와 3은 FR1의 시작에서부터 FR3의 끝까지 연장되는 서열 번호: 2의 모 토끼 항체<br />
- 5 -
경쇄의 하위서열(subsequence)에 대한 높은 상동성 수준(인간 생식선 항체 서열의 라이브러리 또는 데이터베이<br />
스 내에 포함된 다른 인간 생식선 항체 서열에 비하여)에 기초하여 인간 생식선 항체 서열의 라이브러리 또는<br />
데이터베이스로부터 선택된 인간 가변 경쇄 항체 서열로부터 유래되고; 그리고<br />
여기서 상기 인간 경쇄 FR4는 서열 번호: 2 내에 포함된 모 토끼 항체 경쇄 FR4에 대한 높은 상동성 수준(인간<br />
생식선 항체 서열의 라이브러리 또는 데이터베이스 내에 포함된 다른 인간 생식선 항체 서열에 비하여)에 기초<br />
하여 인간 생식선 항체 서열의 라이브러리 또는 데이터베이스로부터 선택된 인간 가변 경쇄 항체 서열로부터 유<br />
래되고; 그리고<br />
여기서 상기 인간 중쇄 FR 1, 2와 3은 FR1의 시작에서부터 FR3의 끝까지 연장되는 서열 번호: 3의 모 토끼 항체<br />
중쇄의 하위서열에 대한 높은 상동성 수준(인간 생식선 항체 서열의 라이브러리 또는 데이터베이스 내에 포함된<br />
다른 인간 생식선 항체 서열에 비하여)에 기초하여 인간 생식선 항체 서열의 라이브러리 또는 데이터베이스로부<br />
터 선택된 인간 가변 중쇄 항체 서열로부터 유래되고; 그리고<br />
여기서 상기 인간 중쇄 FR4는 서열 번호: 3 내에 포함된 모 토끼 항체 중쇄 FR4에 대한 높은 상동성 수준(인간<br />
생식선 항체 서열의 라이브러리 또는 데이터베이스 내에 포함된 다른 인간 생식선 항체 서열에 비하여)에 기초<br />
하여 인간 생식선 항체 서열의 라이브러리 또는 데이터베이스로부터 선택된 인간 가변 중쇄 항체 서열로부터 유<br />
래되는 것을 특징으로 하는 방법.<br />
청구항 15<br />
청구항 1 내지 14중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 건강한 인간 개체에서 적어도 대략 22일<br />
의 생체내 반감기를 갖는 것을 특징으로 하는 방법.<br />
청구항 16<br />
청구항 1 내지 14중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 건강한 인간 개체에서 적어도 대략 25일<br />
의 생체내 반감기를 갖는 것을 특징으로 하는 방법.<br />
청구항 17<br />
청구항 1 내지 14중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 건강한 인간 개체에서 적어도 대략 30일<br />
의 생체내 반감기를 갖는 것을 특징으로 하는 방법.<br />
청구항 18<br />
청구항 1 내지 17중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 대략 50 피코몰 미만의 IL-6에 대한 결합<br />
친화성(Kd), 또는 10 -4<br />
청구항 <strong>19</strong><br />
S -1<br />
이하의 IL-6으로부터의 해리 속도(Koff)를 갖는 것을 특징으로 하는 방법.<br />
청구항 1 내지 18중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 완전한(intact) 인간 IL-6 폴리펩티드 또<br />
는 이의 단편 상에 존재하는, 서열 번호: 702와 서열 번호: 704의 폴리펩티드 또는 서열 번호: 2와 서열 번호:<br />
3의 폴리펩티드로 본질적으로 구성되는 항-IL-6 항체와 동일한 선형(linear) 또는 입체형태적(conformational)<br />
에피토프(들)에 특이적으로 결합하고 및/또는 상기 선형 또는 입체형태적 에피토프(들)에 결합하는 것에 대해<br />
경쟁하는 것을 특징으로 하는 방법.<br />
청구항 20<br />
청구항 <strong>19</strong>에 있어서, 완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는 동일한 선형 또는 입체형태적<br />
에피토프에 결합하는 것 및/또는 상기 선형 또는 입체형태적 에피토프에 결합하는 것에 대해 경쟁하는 것은 본<br />
래의 인간 IL-6 폴리펩티드의 전장에 걸쳐있는 겹쳐지는 선형 펩티드 단편들을 이용한 에피토프 매핑에 의해 확<br />
인되고, 그리고 서열 번호: 1의 아미노산 잔기 37-51, 아미노산 잔기 70-84, 아미노산 잔기 169-183, 아미노산<br />
잔기 31-45 및/또는 아미노산 잔기 58-72를 각각 포함하는 것들에서 선택되는 IL-6 단편 내에 포함된 하나 이상<br />
의 잔기를 포함하는 것을 특징으로 하는 방법.<br />
청구항 21<br />
- 6 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 1 내지 20중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 비당화되는(aglycosylated) 것을 특징으<br />
로 하는 방법.<br />
청구항 22<br />
청구항 1 내지 21중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 이펙터 기능, 반감기, 단백질가수분해,<br />
및/또는 당화(glycosylation)를 변화시키기 위하여 변형된 Fc 영역을 포함하는 것을 특징으로 하는 방법.<br />
청구항 23<br />
청구항 1 내지 22중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 인간, 인간화, 단일 사슬, 또는 키메라<br />
항체인 것을 특징으로 하는 방법.<br />
청구항 24<br />
청구항 1 내지 23중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 Fab, Fab', F(ab')2, Fv, 또는 scFv를 포<br />
함하는 것을 특징으로 하는 방법.<br />
청구항 25<br />
청구항 1 내지 24중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 인간 Fc를 추가로 포함하는 것을 특징으<br />
로 하는 방법.<br />
청구항 26<br />
청구항 25에 있어서, 인간 Fc는 IgG1, IgG2, IgG3, IgG4, IgG5, IgG6, IgG7, IgG8, IgG9, IgG10, IgG11,<br />
IgG<strong>12</strong>, IgG13, IgG14, IgG15, IgG16, IgG17, IgG18 또는 IgG<strong>19</strong>로부터 유래되는 것을 특징으로 하는 방법.<br />
청구항 27<br />
청구항 1 내지 26중 어느 한 항에 있어서, IL-6과 연관된 한 가지 이상의 활성은 감소된 혈청 알부민; 상승된<br />
C-반응성 단백질("CRP"); 피로; 발열; 식욕부진(식욕의 상실); 체중 감소; 악액질; 쇠약; 감소된 Glasgow 예후<br />
점수("GPS"); 상승된 혈청 D-이합체; 비정상적인 혈액응고 프로필; 또는 이들의 임의의 조합을 포함하는 생체내<br />
활성인 것을 특징으로 하는 방법.<br />
청구항 28<br />
청구항 1 내지 26중 어느 한 항에 있어서, IL-6과 연관된 한 가지 이상의 활성 중에서 한 가지 이상은 T1165 세<br />
포의 증식 자극; IL-6R에 대한 IL-6의 결합; gp130 신호-전달 당단백질의 활성화(이합체화); IL-6/IL-6R/gp130<br />
멀티머의 형성; 인간 IL-6 수용체를 발현하도록 변형된 HepG2 세포에 의한 합토글로빈 생산의 자극, 또는 이들<br />
의 임의의 조합을 포함하는 시험관내 활성인 것을 특징으로 하는 방법.<br />
청구항 29<br />
청구항 1 내지 28중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 재조합 세포로부터 발현되는 것을 특징으<br />
로 하는 방법.<br />
청구항 30<br />
청구항 29에 있어서, 세포는 포유동물, 효모, 세균, 그리고 곤충 세포에서 선택되는 것을 특징으로 하는 방법.<br />
청구항 31<br />
청구항 30에 있어서, 세포는 효모 세포인 것을 특징으로 하는 방법.<br />
청구항 32<br />
청구항 31에 있어서, 세포는 2배체 효모 세포인 것을 특징으로 하는 방법.<br />
- 7 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 33<br />
청구항 31에 있어서, 효모 세포는 피치아(Pichia) 효모인 것을 특징으로 하는 방법.<br />
청구항 34<br />
청구항 1 내지 33중 어느 한 항에 있어서, IL-6과 연관된 질환 또는 이상은 암; 과혈액응고와 연관된 질환 또는<br />
이상; 상승된 혈청 CRP와 연관된 질환 또는 이상; 저알부민혈증과 연관된 질환 또는 이상; 염증 질환; 바이러스<br />
질환; 소모성 증후군; 자가면역 질환; 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 35<br />
청구항 1 내지 33중 어느 한 항에 있어서, IL-6과 연관된 질환 또는 이상은 일반적인 피로, 운동-유발된 피로,<br />
암-관련된 피로, 염증 질환-관련된 피로, 만성 피로 증후군, 암-관련된 악액질, 심장-관련된 악액질, 호흡기-관<br />
련된 악액질, 신장-관련된 악액질, 연령-관련된 악액질, 류머티스성 관절염, 전신성 홍반성 루푸스(SLE), 전신<br />
성 유년형 특발성 관절염, 건선, 건선성 관절병증, 강직성 척추염, 염증성 장 질환(IBD), 류머티스성 다발성 근<br />
육통, 거대 세포 동맥염, 자가면역 혈관염, 이식편 대(對) 숙주 질환(GVHD), 쇼그렌 증후군, 성인 발병성 스틸<br />
병, 류머티스성 관절염, 전신성 유년형 특발성 관절염, 골관절염, 골다공증, 뼈의 파제트병, 골관절염, 다발성<br />
골수종, 호지킨 림프종, 비-호지킨 림프종, 전립선암, 백혈병, 신장 세포 암, 다발성 캐슬만씨병, 난소암, 암<br />
화학요법에서 약물 내성, 암 화학요법 독성, 허혈성 심장 질환, 죽상동맥경화증(atherosclerosis), 비만, 당뇨<br />
병, 천식, 다발성 경화증, 알츠하이머병, 뇌혈관 질환, 발열, 급성기 반응, 알레르기, 빈혈, 염증의 빈혈(만성<br />
질환의 빈혈), 고혈압, 우울증, 만성 질환과 연관된 우울증, 혈전증, 혈소판증가증(thrombocytosis), 급성 심장<br />
마비, 대사 증후군, 유산, 비만, 만성 전립선염, 사구체신염, 골반 염증 질환, 재관류 손상, 이식 거부반응, 이<br />
식편 대(對) 숙주 질환(GVHD), 사이토킨 폭풍(cytokine storm), 조류 인플루엔자, H1N1 인플루엔자, 돼지 인플<br />
루엔자, H5N1 인플루엔자, 천연두, 대유행 인플루엔자, 성인 호흡 곤란 증후군(ARDS), 중증 급성 호흡기 증후군<br />
(SARS), 패혈증, 또는 전신성 염증 반응 증후군(SIRS)을 포함하는 것을 특징으로 하는 방법.<br />
청구항 36<br />
청구항 34에 있어서, 과혈액응고와 연관된 질환 또는 이상은 암, 급성 정맥 혈전증, 폐 색전증, 임신 동안 혈전<br />
증, 출혈성 피부 괴사, 급성 또는 만성 범발성 혈관내 혈액응고(DIC), 수술로부터 응괴 형성, 장기 요양, 장기<br />
간의 부동, 정맥 혈전증, 전격성 수막염균 혈증, 급성 혈전성 뇌졸중, 급성 관상동맥 폐쇄증, 급성 말초 동맥<br />
폐쇄증, 광범위 폐 색전증, 액와 정맥 혈전증, 광범위 골대퇴정맥 혈전증, 폐쇄된 동맥 도관(occluded arterial<br />
cannulae), 폐쇄된 정맥 도관(occluded venous cannulae), 심근증, 간의 정맥폐쇄성 질환, 저혈압, 감소된 심<br />
박출량, 감소된 혈관 저항, 폐 고혈압, 감소된 폐 유순도, 백혈구감소증, 혈소판감소증(thrombocytopenia), 헤<br />
파린-유도된 혈소판감소증(HIT), 헤파린-유도된 혈소판감소증과 혈전증(HITT), 심방 세동, 인공 심장 판막의 이<br />
식, 혈전증에 대한 유전적 민감도, 인자 V 라이덴병, 프로트롬빈 유전자 돌연변이, 메틸렌테트라하이드로폴레이<br />
트 환원효소(MTHFR) 다형성, 혈소판-수용체 다형성, 외상, 골절, 화상, 또는 이들의 임의의 조합을 포함하는 것<br />
을 특징으로 하는 방법.<br />
청구항 37<br />
청구항 34에 있어서, 상승된 혈청 CRP와 연관된 질환 또는 이상은 만성 염증 질환, 류머티스성 관절염, 유년형<br />
류머티스성 관절염, 건선, 건선성 관절병증, 강직성 척추염, 전신성 홍반성 루푸스, 크론병, 궤양성 대장염, 천<br />
포창, 피부근염, 다발근육염, 류머티스성 다발성 근육통, 거대 세포 동맥염, 혈관염, 결절성 다발동맥염, 베게<br />
너 육아종증, 가와사키병, 고립형 CNS 혈관염, Churg-Strauss 관절염, 현미경적 다발동맥염, 현미경적 다발혈관<br />
염, 헤노호-쉐라인 자반증(Henoch-Schonlein), 본태성 한랭글로불린혈증성 혈관염, 류머티스성 혈관염, 한랭글<br />
로불린혈증, 재발성 다발연골염, 베체트병, 다까야수 동맥염, 허혈성 심장 질환, 뇌졸중(stroke), 다발성 경화<br />
증, 패혈증, 바이러스 감염에 속발성인 혈관염, 버거스씨병, 암, 진행된 암, 골관절염, 전신 경화증, CREST 증<br />
후군, 라이터병, 뼈의 파제트병, 쇼그렌 증후군, 1형 당뇨병, 2형 당뇨병, 가족성 지중해열, 자가면역 혈소판감<br />
소증, 자가면역 용혈성 빈혈, 자가면역 갑상선 질환, 악성 빈혈, 백반, 원형탈모증, 원발성 담도 경화증, 자가<br />
면역 만성 활성 간염, 알코올성 간경화증, 바이러스 간염, B형 간염, C형 간염, 다른 장기 특이적 자가면역 질<br />
환, 화상, 특발성 폐 섬유증, 만성 폐쇄성 폐 질환, 알레르기 천식, 다른 알레르기 질환, 또는 이들의 임의의<br />
조합을 포함하는 것을 특징으로 하는 방법.<br />
- 8 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 38<br />
청구항 34에 있어서, 저알부민혈증과 연관된 질환 또는 장애는 암, 진행된 암, 류머티스성 관절염, AIDS, 심장<br />
질환, 간 질환, 탈수, 영양실조, 납 노출, 말라리아, 호흡 질환, 노령, 갑상선 기능저하증, 결핵, 뇌하수체 저<br />
하증, 신경쇠약, 고나트륨혈증, 저나트륨혈증, 신장 질환, 지라동맥(splenica), 강직성 척추염, 성장 실패(부진<br />
한 성장), 염증성 장 질환, 셀리악병, 외상, 환상, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방<br />
법.<br />
청구항 39<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 34 내지 38중 어느 한 항에 있어서, 암은 가시세포종(Acanthoma), 선방 세포 암종(Acinic cell<br />
carcinoma), 청신견종(Acoustic neuroma), 선단 흑자성 흑색종(Acral lentiginous melanoma), 선단한선종<br />
(Acrospiroma), 급성 호산성 백혈병(Acute eosinophilic leukemia), 급성 림프모구성 백혈병(Acute<br />
lymphoblastic leukemia), 급성 거핵모구성 백혈병(Acute megakaryoblastic leukemia), 급성 단구성 백혈병<br />
(Acute monocytic leukemia), 성숙을 동반한 급성 골수모구성 백혈병(Acute myeloblastic leukemia with<br />
maturation), 급성 골수성 수상돌기 세포 백혈병(Acute myeloid dendritic cell leukemia), 급성 골수성 백혈<br />
병(Acute myeloid leukemia), 급성 전골수성 백혈병(Acute promyelocytic leukemia), 사기질종(Adamantinoma),<br />
선암종(Adenocarcinoma), 선양 낭성 암종(Adenoid cystic carcinoma), 선종(Adenoma), 선양 치성 종양<br />
(Adenomatoid odontogenic tumor), 부신피질 암종(Adrenocortical carcinoma), 성체 T-세포 백혈병(Adult T-<br />
cell leukemia), 공격성 NK-세포 백혈병(Aggressive NK-cell leukemia), AIDS-관련된 암(AIDS-Related<br />
Cancers), AIDS-관련된 림프종(AIDS-related lymphoma), 포상 연부 육종(Alveolar soft part sarcoma), 법랑아<br />
세포 섬유치아종(Ameloblastic fibroma), 항문 암(Anal cancer), 퇴행성 대세포 림프종(Anaplastic large cell<br />
lymphoma), 역형성 갑상선 암(Anaplastic thyroid cancer), 혈관면역모세포형 T-세포 림프종<br />
(Angioimmunoblastic T-cell lymphoma), 혈관근육지방종(Angiomyolipoma), 맥관육종(Angiosarcoma), 충수 암<br />
(Appendix cancer), 별아교세포종(Astrocytoma), 비정형 기형 횡문근양 종양(Atypical teratoid rhabdoid<br />
tumor), 기저 세포 암종(Basal cell carcinoma), 기저-유사 암종(Basal-like carcinoma), B-세포 백혈병(B-<br />
cell leukemia), B-세포 림프종(B-cell lymphoma), 집합관 암종(Bellini duct carcinoma), 담도 암(Biliary<br />
tract cancer), 방광 암(Bladder cancer), 모세포종(Blastoma), 골 암(Bone Cancer), 골 종양(Bone tumor), 뇌<br />
간 교종(Brain Stem Glioma), 뇌 종양(Brain Tumor), 유방암(Breast Cancer), 브렌너 종양(Brenner tumor), 기<br />
관지 종양(Bronchial Tumor), 세기관지폐포 암종(Bronchioloalveolar carcinoma), 갈색 종양(Brown tumor), 버<br />
킷 림프종(Burkitt's lymphoma), 원발부위 불명암(Cancer of Unknown Primary Site), 유암종(Carcinoid<br />
Tumor), 암종(Carcinoma), 인 시튜 암종(Carcinoma in situ), 음경 암종(Carcinoma of the penis), 원발부위<br />
불명 암종(Carcinoma of Unknown Primary Site), 암육종(Carcinosarcoma), 캐슬만씨병(Castleman's Disease),<br />
중추신경계 배아성 종양(Central Nervous System Embryonal Tumor), 소뇌 별아교세포종(Cerebellar<br />
Astrocytoma), 대뇌 별아교세포종(Cerebral Astrocytoma), 자궁경부 암(Cervical Cancer), 담관암종<br />
(Cholangiocarcinoma), 연골종(Chondroma), 연골육종(Chondrosarcoma), 척삭종(Chordoma), 융모막암종<br />
(Choriocarcinoma), 맥락막총 유두종(Choroid plexus papilloma), 만성 림프성 백혈병(Chronic Lymphocytic<br />
Leukemia), 만성 단구성 백혈병(Chronic monocytic leukemia), 만성 골수성 백혈병(Chronic myelogenous<br />
leukemia), 만성 골수증식성 질환(Chronic Myeloproliferative Disorder), 만성 호중구성 백혈병(Chronic<br />
neutrophilic leukemia), 투명-세포 종양(Clear-cell tumor), 대장 암(Colon Cancer), 결장직장 암(Colorectal<br />
cancer), 머리인두종(Craniopharyngioma), 피부 T-세포 림프종(Cutaneous T-cell lymphoma), 데고스 질환<br />
(Degos disease), 융기성 피부섬유육종(Dermatofibrosarcoma protuberans), 유피낭종(Dermoid cyst), 복부 결<br />
합조직형성 소원형세포 종양(Desmoplastic small round cell tumor), 미만성 거대 B 세포 림프종(Diffuse<br />
large B cell lymphoma), 배아형성장애 신경상피 종양(Dysembryoplastic neuroepithelial tumor), 배아 암종<br />
(Embryonal carcinoma), 내배엽동 종양(Endodermal sinus tumor), 자궁내막 암(Endometrial cancer), 자궁내막<br />
자궁 암(Endometrial Uterine Cancer), 자궁내막양 종양(Endometrioid tumor), 장병증 연관 T-세포 림프종<br />
(Enteropathy-associated T-cell lymphoma), 상의모세포종(Ependymoblastoma), 상의세포종(Ependymoma), 상피<br />
양 육종(Epithelioid sarcoma), 적백혈병(Erythroleukemia), 식도 암(Esophageal cancer), 감각신경모세포종<br />
(Esthesioneuroblastoma), 유잉 계통 종양(Ewing Family of Tumor), 유잉 계통 육종(Ewing Family Sarcoma),<br />
유잉 육종(Ewing's sarcoma), 두개외 생식세포 종양(Extracranial Germ Cell Tumor), 생식샘외 생식세포 종양<br />
(Extragonadal Germ Cell Tumor), 간외 담도 암(Extrahepatic Bile Duct Cancer), 유방외성 파제트병<br />
(Extramammary Paget's disease), 난관 암(Fallopian tube cancer), 태아속 태아(Fetus in fetu), 섬유종<br />
- 9 -
공개특허 10-2011-01<strong>12</strong>308<br />
(Fibroma), 섬유육종(Fibrosarcoma), 소포성 림프종(Follicular lymphoma), 소포성 갑상선 암(Follicular<br />
thyroid cancer), 담낭 암(Gallbladder Cancer), 담낭 암(Gallbladder cancer), 신경절교종(Ganglioglioma),<br />
신경절신경종(Ganglioneuroma), 위 암(Gastric Cancer), 위 림프종(Gastric lymphoma), 위장 암<br />
(Gastrointestinal cancer), 위장 유암종(Gastrointestinal Carcinoid Tumor), 위장 기질 종양<br />
(Gastrointestinal Stromal Tumor), 위장 기질 종양(Gastrointestinal stromal tumor), 생식세포 종양(Germ<br />
cell tumor), 배세포종(Germinoma), 임신성 융모막암종(Gestational choriocarcinoma), 임신성 융모성 종양<br />
(Gestational Trophoblastic Tumor), 뼈의 거대 세포 종양(Giant cell tumor of bone), 다형성교모세포종<br />
(Glioblastoma multiforme), 신경교종(Glioma), 대뇌신경교종증(Gliomatosis cerebri), 사구 종양(Glomus<br />
tumor), 글루카곤종(Glucagonoma), 생식아세포종(Gonadoblastoma), 과립층 세포 종양(Granulosa cell tumor),<br />
모상 세포 백혈병(Hairy Cell Leukemia), 모상 세포 백혈병(Hairy cell leukemia), 두경부 암(Head and Neck<br />
Cancer), 두경부 암(Head and neck cancer), 심장 암(Heart cancer), 혈관모세포종(Hemangioblastoma), 혈관주<br />
위세포종(Hemangiopericytoma), 혈관육종(Hemangiosarcoma), 혈액학적 악성종양(Hematological malignancy),<br />
간세포 암종(Hepatocellular carcinoma), 간비 T-세포 림프종(Hepatosplenic T-cell lymphoma), 유전성 유방-<br />
난소암 증후군(Hereditary breast-ovarian cancer syndrome), 호지킨 림프종(Hodgkin Lymphoma), 호지킨 림프<br />
종(Hodgkin's lymphoma), 하인두 암(Hypopharyngeal Cancer), 시상하부 신경교종(Hypothalamic Glioma), 염증<br />
유방암(Inflammatory breast cancer), 안구내 흑색종(Intraocular Melanoma), 섬 세포 암종(Islet cell<br />
carcinoma), 섬 세포 종양(Islet Cell Tumor), 연소형 골수단구성 백혈병(Juvenile myelomonocytic leukemia),<br />
카포시 육종(Kaposi Sarcoma), 카포시 육종(Kaposi's sarcoma), 신장 암(Kidney Cancer), 클라츠킨씨 종양<br />
(Klatskin tumor), 크루켄버그 종양(Krukenberg tumor), 후두 암(Laryngeal cancer), 후두 암(Laryngeal<br />
cancer), 악성 흑자 흑색종(Lentigo maligna melanoma), 백혈병(Leukemia), 백혈병(Leukemia), 입술과 구강 암<br />
(Lip and Oral Cavity Cancer), 지방육종(Liposarcoma), 폐암(Lung cancer), 황체종(Luteoma), 림프관종<br />
(Lymphangioma), 림프관육종(Lymphangiosarcoma), 림프상피종(Lymphoepithelioma), 림프성 백혈병(Lymphoid<br />
leukemia), 림프종(Lymphoma), 마크로글로불린혈증(Macroglobulinemia), 악성 섬유성 조직구종(Malignant<br />
Fibrous Histiocytoma), 악성 섬유성 조직구종(Malignant fibrous histiocytoma), 뼈의 악성 섬유성 조직구종<br />
(Malignant Fibrous Histiocytoma of Bone), 악성 신경교종(Malignant Glioma), 악성 중피종(Malignant<br />
Mesothelioma), 악성 말초신경초 종양(Malignant peripheral nerve sheath tumor), 악성 횡문근양 종양<br />
(Malignant rhabdoid tumor), 악성 트리톤 종양(Malignant triton tumor), MALT 림프종(MALT lymphoma), 덮개<br />
세포 림프종(Mantle cell lymphoma), 비만 세포 백혈병(Mast cell leukemia), 종격동 생식세포 종양<br />
(Mediastinal germ cell tumor), 종격동 종양(Mediastinal tumor), 갑상선 수질암(Medullary thyroid cancer),<br />
속질모세포종(Medulloblastoma), 속질모세포종(Medulloblastoma), 속질상피종(Medulloepithelioma), 흑색종<br />
(Melanoma), 흑색종(Melanoma), 수막종(Meningioma), 메르켈 세포 암종(Merkel Cell Carcinoma), 중피종<br />
(Mesothelioma), 중피종(Mesothelioma), 잠복원발성 전이성 편평 목 암(Metastatic Squamous Neck Cancer with<br />
Occult Primary), 전이성 요로상피 암종(Metastatic urothelial carcinoma), 혼합 뮬러 종양(Mixed Mullerian<br />
tumor), 단구성 백혈병(Monocytic leukemia), 구강 암(Mouth Cancer), 점액 종양(Mucinous tumor), 다발성 내<br />
분비 종양 증후군(Multiple Endocrine Neoplasia Syndrome), 다발성 골수종(Multiple Myeloma), 다발성 골수종<br />
(Multiple myeloma), 균상식육종(Mycosis Fungoides), 균상식육종(Mycosis fungoides), 골수형성이상 질환<br />
(Myelodysplastic Disease), 골수형성이상 증후군(Myelodysplastic Syndromes), 골수성 백혈병(Myeloid<br />
leukemia), 골수성 육종(Myeloid sarcoma), 골수증식 질환(Myeloproliferative Disease), 점액종(Myxoma), 비<br />
강 암(Nasal Cavity Cancer), 코인두 암(Nasopharyngeal Cancer), 코인두 암종(Nasopharyngeal carcinoma), 신<br />
생물(Neoplasm), 신경집종(Neurinoma), 신경모세포종(Neuroblastoma), 신경모세포종(Neuroblastoma), 신경섬유<br />
종(Neurofibroma), 신경종(Neuroma), 결절성 흑색종(Nodular melanoma), 비-호지킨 림프종(Non-Hodgkin<br />
Lymphoma), 비-호지킨 림프종(Non-Hodgkin lymphoma), 비-흑색종 피부 암(Nonmelanoma Skin Cancer), 비-소세<br />
포 폐암(Non-Small Cell Lung Cancer), 안종양(Ocular oncology), 희소별아교세포종(Oligoastrocytoma), 핍지<br />
교종(Oligodendroglioma), 호산성세포종(Oncocytoma), 시신경초 수막종(Optic nerve sheath meningioma), 구강<br />
암(Oral Cancer), 구강 암(Oral cancer), 입인두 암(Oropharyngeal Cancer), 골육종(Osteosarcoma), 골육종<br />
(Osteosarcoma), 난소암(Ovarian Cancer), 난소암(Ovarian cancer), 난소 상피 암(Ovarian Epithelial<br />
Cancer), 난소 생식세포 종양(Ovarian Germ Cell Tumor), 난소 저급성 악성 종양(Ovarian Low Malignant<br />
Potential Tumor), 유방의 파제트병(Paget's disease of the breast), 판코스트 종양(Pancoast tumor), 췌장암<br />
(Pancreatic Cancer), 췌장암(Pancreatic cancer), 갑상샘 유두 암(Papillary thyroid cancer), 유두종증<br />
(Papillomatosis), 곁신경절종(Paraganglioma), 부비동 암(Paranasal Sinus Cancer), 부갑상선 암(Parathyroid<br />
Cancer), 음경 암(Penile Cancer), 혈관주위 상피모양 세포 종양(Perivascular epithelioid cell tumor), 인두<br />
- 10 -
암(Pharyngeal Cancer), 갈색세포종(Pheochromocytoma), 중간 분화의 송과체 실질 종양(Pineal Parenchymal<br />
Tumor of Intermediate Differentiation), 송과체모세포종(Pineoblastoma), 하수체세포종(Pituicytoma), 뇌하<br />
수체 선종(Pituitary adenoma), 뇌하수체 종양(Pituitary tumor), 혈장 세포 신생물(Plasma Cell Neoplasm),<br />
흉막폐아세포종(Pleuropulmonary blastoma), 다배아종(Polyembryoma), 전구 T-림프모구성 림프종(Precursor T-<br />
lymphoblastic lymphoma), 원발성 중추신경계 림프종(Primary central nervous system lymphoma), 원발성 삼출<br />
성 림프종(Primary effusion lymphoma), 원발성 간세포 암(Primary Hepatocellular Cancer), 원발성 간 암<br />
(Primary Liver Cancer), 원발성 복막 암(Primary peritoneal cancer), 원시 신경외배엽 종양(Primitive<br />
neuroectodermal tumor), 전립선암(Prostate cancer), 복막가성점액종(Pseudomyxoma peritonei), 직장 암<br />
(Rectal Cancer), 신장 세포 암종(Renal cell carcinoma), 염색체 15에서 NUT 유전자가 관련된 호흡기 암종<br />
(Respiratory Tract Carcinoma Involving the NUT Gene on Chromosome 15), 망막모세포종(Retinoblastoma),<br />
횡문근종(Rhabdomyoma), 횡문근육종(Rhabdomyosarcoma), 리히터 변형(Richter's transformation), 천미골 기형<br />
종(Sacrococcygeal teratoma), 타액선 암(Salivary Gland Cancer), 육종(Sarcoma), 다발성신경초종<br />
(Schwannomatosis), 피지선 암종(Sebaceous gland carcinoma), 속발성 신생물(Secondary neoplasm), 정상피종<br />
(Seminoma), 장액 종양(Serous tumor), 세르톨리 라이디히 세포 종양(Sertoli-Leydig cell tumor), 성삭-기질<br />
종양(Sex cord-stromal tumor), 세자리 증후군(Sezary Syndrome), 인환 세포 암종(Signet ring cell<br />
carcinoma), 피부 암(Skin Cancer), 청색 소원형세포 종양(Small blue round cell tumor), 소세포 암종(Small<br />
cell carcinoma), 소세포 폐암(Small Cell Lung Cancer), 소세포 림프종(Small cell lymphoma), 소장 암(Small<br />
intestine cancer), 연부 조직 육종(Soft tissue sarcoma), 소마토스타틴종(Somatostatinoma), 매연 사마귀<br />
(Soot wart), 척추 종양(Spinal Cord Tumor), 척추 종양(Spinal tumor), 비장 번연 림프종(Splenic marginal<br />
zone lymphoma), 편평 세포 암종(Squamous cell carcinoma), 위 암(Stomach cancer), 표재 확장성 흑색종<br />
(Superficial spreading melanoma), 천막위 원시 신경외배엽 종양(Supratentorial Primitive Neuroectodermal<br />
Tumor), 표면 상피-기질 종양(Surface epithelial-stromal tumor), 활액 육종(Synovial sarcoma), T-세포 급성<br />
림프모구성 백혈병(T-cell acute lymphoblastic leukemia), T-세포 큰 과립성 림프구 백혈병(T-cell large<br />
granular lymphocyte leukemia), T-세포 백혈병(T-cell leukemia), T-세포 림프종(T-cell lymphoma), T-세포<br />
전림프성 백혈병(T-cell prolymphocytic leukemia), 기형종(Teratoma), 말기 림프성 암(Terminal lymphatic<br />
cancer), 고환 암(Testicular cancer), 난포막종(Thecoma), 인후 암(Throat Cancer), 흉선 암종(Thymic<br />
Carcinoma), 가슴샘종(Thymoma), 갑상선 암(Thyroid cancer), 신우와 요관의 이행 세포 암(Transitional Cell<br />
Cancer of Renal Pelvis and Ureter), 이행 세포 암종(Transitional cell carcinoma), 요막관 암(Urachal<br />
cancer), 요도 암(Urethral cancer), 비뇨생식기 신생물(Urogenital neoplasm), 자궁 육종(Uterine sarcoma),<br />
포도막 흑색종(Uveal melanoma), 질 암(Vaginal Cancer), 버너-모리슨 증후군(Verner Morrison syndrome), 사<br />
마귀모양 암종(Verrucous carcinoma), 시각경로 신경교종(Visual Pathway Glioma), 외음부 암(Vulvar Cancer),<br />
왈덴스트룀 마크로글로불린혈증(Waldenstrom's macroglobulinemia), 바르틴 종양(Warthin's tumor), 윌름 종양<br />
(Wilms' tumor), 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 40<br />
청구항 39에 있어서, 암은 결장직장 암, 비-소세포 폐암, 담관암, 중피종, 캐슬만씨병, 신장 세포 암종, 또는<br />
이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 41<br />
청구항 1 내지 40중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편의 투여 이전에, 개체는 아래의 증상 중에서<br />
한 가지 이상을 나타내거나, 또는 이들 증상이 발생할 위험이 있는 것을 특징으로 하는 방법:<br />
감소된 혈청 알부민; 상승된 C-반응성 단백질("CRP"); 피로; 발열; 식욕부진(식욕의 상실); 체중 감소; 악액질;<br />
쇠약; 감소된 Glasgow 예후 점수("GPS"); 상승된 혈청 D-이합체; 비정상적인 혈액응고 프로필; 그리고 이들의<br />
임의의 조합.<br />
청구항 42<br />
청구항 41에 있어서, 상기 증상은 Ab1 항체 또는 항체 단편의 투여 이전에, 동시에, 또는 이후에 개체에 투여된<br />
다른 치료제의 부작용인 것을 특징으로 하는 방법.<br />
청구항 43<br />
- 11 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 1 내지 40중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 상승된 IL-6과 연관된 한 가지 이상의 증<br />
상의 예방 또는 치료를 위한 치료 효과량으로 투여되는 것을 특징으로 하는 방법.<br />
청구항 44<br />
청구항 43에 있어서, 치료 효과량은 수용자 개체의 체중의 대략 0.1 내지 20 ㎎/kg인 것을 특징으로 하는 방법.<br />
청구항 45<br />
청구항 41에 있어서, Ab1 항체의 투여 이후에 상기 증상을 평가하기 위하여 개체를 모니터하는 단계를 추가로<br />
포함하는 것을 특징으로 하는 방법.<br />
청구항 46<br />
청구항 41에 있어서, 상기 증상은 Ab1 항체 또는 항체 단편 투여 이전에 나타나는 것을 특징으로 하는 방법.<br />
청구항 47<br />
청구항 46에 있어서, 상기 증상은 Ab1 항체 투여후 대략 1-5주 이내에 개선되거나, 또는 정상 상태로 복원되는<br />
것을 특징으로 하는 방법.<br />
청구항 48<br />
청구항 47에 있어서, 상기 증상은 이후, 2번의 연속 Ab1 항체 투여 사이에 존재하는 전체 기간 동안 개선된 상<br />
태로 유지되는 것을 특징으로 하는 방법.<br />
청구항 49<br />
청구항 41에 있어서, 개체의 혈액응고 프로필은 D-이합체, 인자 II, 인자 V, 인자 VIII, 인자 IX, 인자 XI, 인<br />
자 XII, F/피브린 분해 산물, 트롬빈-항트롬빈 III 복합체, 피브리노겐, 플라스미노겐, 프로트롬빈, 그리고 폰<br />
빌레브란드 인자 중에서 한 가지 이상의 개체의 혈청 수준의 측정치에 의해 평가되는 것을 특징으로 하는 방법.<br />
청구항 50<br />
청구항 41에 있어서, 개체의 혈액응고 프로필은 응고 능력의 기능적 측정치에 의해 평가되는 것을 특징으로 하<br />
는 방법.<br />
청구항 51<br />
청구항 50에 있어서, 응고 능력의 기능 측정치(functional measurement)는 프로트롬빈 시간(PT), 프로트롬빈 비<br />
율(PR), 국제 표준화 비율(INR), 또는 이들의 임의의 조합에서 선택되는 것을 특징으로 하는 방법.<br />
청구항 52<br />
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여에 앞서 개체의 국제 표준화 비율(INR)을 측정하는 단계,<br />
그리고 개체의 INR이 대략 0.9 이하인 경우 Ab1 항체 또는 항체 단편을 개체에게 투여하는 단계를 추가로 포함<br />
하는 것을 특징으로 하는 방법.<br />
청구항 53<br />
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여에 앞서 개체의 국제 표준화 비율(INR)을 측정하는 단계,<br />
그리고 개체의 INR이 대략 0.5 이하인 경우 Ab1 항체 또는 항체 단편을 개체에게 투여하는 단계를 추가로 포함<br />
하는 것을 특징으로 하는 방법.<br />
청구항 54<br />
청구항 52 내지 53중 어느 한 항에 있어서, 개체의 INR은 개체에 Ab1 항체 또는 항체 단편의 투여후 4주 이내에<br />
대략 0.9가 넘게 증가되는 것을 특징으로 하는 방법.<br />
청구항 55<br />
- <strong>12</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여에 앞서 개체의 혈청 D-이합체 수준을 측정하는 단계, 그<br />
리고 개체의 혈청 D-이합체 수준이 정상적인 참고 범위를 초과하면 Ab1 항체 또는 항체 단편을 투여하는 단계를<br />
추가로 포함하는 것을 특징으로 하는 방법.<br />
청구항 56<br />
청구항 55에 있어서, 개체의 혈청 D-이합체 수준은 개체에 Ab1 항체 또는 항체 단편의 투여후 4주 이내에 정상<br />
적인 참고 범위의 상한 미만으로 떨어지는 것을 특징으로 하는 방법 .<br />
청구항 57<br />
청구항 41에 있어서, 개체의 혈액응고 프로필에서 연장된 개선을 유발하는 것을 특징으로 하는 방법.<br />
청구항 58<br />
청구항 41에 있어서, 개체의 혈액응고 프로필은 Ab1 항체 또는 항체 단편의 투여후 대략 2주 이내에 측정가능하<br />
게 개선되는 것을 특징으로 하는 방법.<br />
청구항 59<br />
청구항 58에 있어서, 개체의 혈액응고 프로필은 개체에 Ab1 항체 또는 항체 단편의 투여후 대략 <strong>12</strong>주에 측정가<br />
능하게 개선된 상태로 유지되는 것을 특징으로 하는 방법.<br />
청구항 60<br />
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여에 앞서 개체의 체온을 측정하는 단계, 그리고 개체의 체<br />
온이 대략 38℃보다 높으면 Ab1 항체 또는 항체 단편을 투여하는 단계를 추가로 포함하는 것을 특징으로 하는<br />
방법.<br />
청구항 61<br />
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여에 앞서 개체의 체중을 측정하는 단계, 그리고 개체의 체<br />
중이 대략 30일 이내에 대략 5% 이상 감소하거나, 또는 개체의 제지방량 지수(lean body mass index)가 대략 17<br />
㎏/m 2<br />
(남성 개체) 또는 대략 14 ㎏/m 2<br />
(여성 개체)보다 낮으면 Ab1 항체 또는 항체 단편을 투여하는 단계를 추가<br />
로 포함하는 것을 특징으로 하는 방법.<br />
청구항 62<br />
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여에 앞서 개체의 근력을 측정하는 단계, 그리고 개체의 근<br />
력이 대략 30일 이내에 대략 20%가 넘게 감소하면 Ab1 항체 또는 항체 단편을 투여하는 단계를 추가로 포함하는<br />
것을 특징으로 하는 방법.<br />
청구항 63<br />
청구항 41에 있어서, 개체에서 악액질, 쇠약, 피로, 및/또는 발열의 연장된 개선을 유발하는 것을 특징으로 하<br />
는 방법.<br />
청구항 64<br />
청구항 41에 있어서, 개체의 체질량은 Ab1 항체 또는 항체 단편의 투여후 대략 4주 이내에 대략 1㎏ 상승되는<br />
것을 특징으로 하는 방법.<br />
청구항 65<br />
청구항 41에 있어서, 개체의 악액질은 Ab1 항체 또는 항체 단편의 투여후 대략 4주 이내에 측정가능하게 개선되<br />
는 것을 특징으로 하는 방법.<br />
청구항 66<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 65에 있어서, 개체의 악액질은 개체의 총 체질량, 제지방량(lean body mass), 제지방량 지수, 및/또는<br />
- 13 -
부속지(appendicular) 제지방량의 측정치에 의해 평가되는 것을 특징으로 하는 방법.<br />
청구항 67<br />
청구항 66에 있어서, 개체의 체질량의 측정치는 개체의 종양(들) 및/또는 혈관외액 수집물(들)의 추정된 중량을<br />
제외(뺄셈)하는 것을 특징으로 하는 방법.<br />
청구항 68<br />
청구항 66에 있어서, 개체의 악액질은 Ab1 항체 또는 항체 단편의 투여후 대략 8주 시점에 측정가능하게 개선된<br />
상태로 유지되는 것을 특징으로 하는 방법.<br />
청구항 69<br />
청구항 41에 있어서, 개체의 쇠약은 Ab1 항체 또는 항체 단편의 투여후 대략 2주 이내에 측정가능하게 개선되는<br />
것을 특징으로 하는 방법.<br />
청구항 70<br />
청구항 69에 있어서, 개체의 쇠약은 Ab1 항체 또는 항체 단편의 투여후 대략 <strong>12</strong>주 시점에 측정가능하게 개선된<br />
상태로 유지되는 것을 특징으로 하는 방법.<br />
청구항 71<br />
청구항 41에 있어서, 개체의 피로는 Ab1 항체 또는 항체 단편의 투여후 대략 1주 이내에 측정가능하게 개선되는<br />
것을 특징으로 하는 방법.<br />
청구항 72<br />
청구항 71에 있어서, 개체의 피로는 FACIT-F FS 검사법에 의해 측정되는 것을 특징으로 하는 방법.<br />
청구항 73<br />
청구항 72에 있어서, 개체의 FACIT-F FS 점수는 적어도 대략 10 점 개선되는 것을 특징으로 하는 방법.<br />
청구항 74<br />
청구항 71에 있어서, 개체의 피로는 항-IL-6 항체 투여후 대략 <strong>12</strong>주 시점에 측정가능하게 개선된 상태로 유지되<br />
는 것을 특징으로 하는 방법.<br />
청구항 75<br />
청구항 41에 있어서, 개체의 발열은 Ab1 항체 또는 항체 단편의 투여후 대략 1주 이내에 측정가능하게 개선되는<br />
것을 특징으로 하는 방법.<br />
청구항 76<br />
청구항 75에 있어서, 개체의 발열은 Ab1 항체 또는 항체 단편의 투여후 대략 <strong>12</strong>주 시점에 측정가능하게 개선된<br />
상태로 유지되는 것을 특징으로 하는 방법.<br />
청구항 77<br />
청구항 41에 있어서, 개체는 Ab1 항체 또는 항체 단편의 투여 이전에, 상승된 혈청 CRP 수준을 나타내는 것을<br />
특징으로 하는 방법.<br />
청구항 78<br />
청구항 41에 있어서, 개체는 Ab1 항체 또는 항체 단편의 투여 이전에, 감소된 혈청 알부민 수준을 나타내는 것<br />
을 특징으로 하는 방법.<br />
청구항 79<br />
- 14 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 41에 있어서, 개체의 Glasgow 예측 점수(GPS)가 개선되는 것을 특징으로 하는 방법.<br />
청구항 80<br />
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여 이전에 개체의 혈청 CRP 수준을 측정하는 단계, 그리고<br />
개체의 혈청 CRP 수준이 적어도 대략 5 ㎎/ℓ이면 Ab1 항체 또는 항체 단편을 투여하는 단계를 추가로 포함하는<br />
것을 특징으로 하는 방법.<br />
청구항 81<br />
청구항 41에 있어서, 개체의 혈청 CRP 수준은 Ab1 항체 또는 항체 단편의 투여후 1주 이내에 대략 10 ㎎/ℓ 미<br />
만으로 감소되는 것을 특징으로 하는 방법.<br />
청구항 82<br />
청구항 41에 있어서, 개체의 혈청 CRP 수준은 Ab1 항체 또는 항체 단편의 투여후 1주 이내에 대략 5 ㎎/ℓ 미만<br />
으로 감소되는 것을 특징으로 하는 방법.<br />
청구항 83<br />
청구항 41에 있어서, 개체의 혈청 CRP 수준은 Ab1 항체 또는 항체 단편의 투여후 1주 이내에 대략 1 ㎎/ℓ 미만<br />
으로 감소되는 것을 특징으로 하는 방법.<br />
청구항 84<br />
청구항 41에 있어서, 개체의 혈청 CRP 수준에서 연장된 감소를 유발하는 것을 특징으로 하는 방법.<br />
청구항 85<br />
청구항 81에 있어서, Ab1 항체 또는 항체 단편의 투여후 14일 시점에, 개체의 혈청 CRP 수준은 대략 10 ㎎/ℓ<br />
미만으로 유지되는 것을 특징으로 하는 방법.<br />
청구항 86<br />
청구항 81에 있어서, Ab1 항체 또는 항체 단편의 투여후 21일 시점에, 개체의 혈청 CRP 수준은 대략 10 ㎎/ℓ<br />
미만으로 유지되는 것을 특징으로 하는 방법.<br />
청구항 87<br />
청구항 81에 있어서, Ab1 항체 또는 항체 단편의 투여후 28일 시점에, 개체의 혈청 CRP 수준은 대략 10 ㎎/ℓ<br />
미만으로 유지되는 것을 특징으로 하는 방법.<br />
청구항 88<br />
청구항 81에 있어서, Ab1 항체 또는 항체 단편의 투여후 35일 시점에, 개체의 혈청 CRP 수준은 대략 10 ㎎/ℓ<br />
미만으로 유지되는 것을 특징으로 하는 방법.<br />
청구항 89<br />
청구항 81에 있어서, Ab1 항체 또는 항체 단편의 투여후 42일 시점에, 개체의 혈청 CRP 수준은 대략 10 ㎎/ℓ<br />
미만으로 유지되는 것을 특징으로 하는 방법.<br />
청구항 90<br />
청구항 81에 있어서, Ab1 항체 또는 항체 단편의 투여후 49일 시점에, 개체의 혈청 CRP 수준은 대략 10 ㎎/ℓ<br />
미만으로 유지되는 것을 특징으로 하는 방법.<br />
청구항 91<br />
청구항 81에 있어서, Ab1 항체 또는 항체 단편의 투여후 56일 시점에, 개체의 혈청 CRP 수준은 대략 10 ㎎/ℓ<br />
미만으로 유지되는 것을 특징으로 하는 방법.<br />
- 15 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 92<br />
청구항 41에 있어서, Ab1 항체 또는 항체 단편의 투여 이전에 개체의 혈청 알부민 수준을 측정하는 단계, 그리<br />
고 개체의 혈청 알부민 수준이 대략 35 g/ℓ 이하이면 Ab1 항체 또는 항체 단편을 투여하는 단계를 추가로 포함<br />
하는 것을 특징으로 하는 방법.<br />
청구항 93<br />
청구항 92에 있어서, 개체의 혈청 알부민 수준은 Ab1 항체 또는 항체 단편의 투여후 대략 5주 이내에 대략 35<br />
g/ℓ가 넘게 증가되는 것을 특징으로 하는 방법.<br />
청구항 94<br />
청구항 41에 있어서, 개체의 혈청 알부민 수준에서 연장된 증가를 유발하는 것을 특징으로 하는 방법.<br />
청구항 95<br />
청구항 94에 있어서, Ab1 항체 또는 항체 단편의 투여후 42일 시점에, 개체의 혈청 알부민 수준은 35 g/ℓ 초과<br />
로 유지되는 것을 특징으로 하는 방법.<br />
청구항 96<br />
청구항 94에 있어서, Ab1 항체 또는 항체 단편의 투여후 49일 시점에, 개체의 혈청 알부민 수준은 35 g/ℓ 초과<br />
로 유지되는 것을 특징으로 하는 방법.<br />
청구항 97<br />
청구항 94에 있어서, Ab1 항체 또는 항체 단편의 투여후 56일 시점에, 개체의 혈청 알부민 수준은 35 g/ℓ 초과<br />
로 유지되는 것을 특징으로 하는 방법.<br />
청구항 98<br />
청구항 41에 있어서, 개체의 혈청 알부민 수준은 Ab1 항체 또는 항체 단편의 투여후 대략 5주 이내에 대략 5 g/<br />
ℓ 증가되는 것을 특징으로 하는 방법.<br />
청구항 99<br />
청구항 41에 있어서, 혈액응고 프로필을 평가하기 위하여 개체를 모니터하는 단계를 추가로 포함하는 것을 특징<br />
으로 하는 방법.<br />
청구항 100<br />
청구항 41에 있어서, 개체는 치료 이전에, 상승된 혈청 D-이합체 수준을 나타내는 것을 특징으로 하는 방법.<br />
청구항 101<br />
청구항 41에 있어서, 개체는 치료 이전에, 상승된 혈청 C-반응성 단백질(CRP) 수준을 나타내는 것을 특징으로<br />
하는 방법.<br />
청구항 102<br />
청구항 1 내지 101중 어느 한 항에 있어서, 항-IL-6 항체 또는 항체 단편은 대략 4주의 기간 마다 1회 정도의<br />
빈도로 개체에 투여되는 것을 특징으로 하는 방법.<br />
청구항 103<br />
청구항 102에 있어서, 항-IL-6 항체 또는 항체 단편은 대략 8주의 기간 마다 1회 정도의 빈도로 개체에 투여되<br />
는 것을 특징으로 하는 방법.<br />
청구항 104<br />
- 16 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 103에 있어서, 항-IL-6 항체 또는 항체 단편은 대략 <strong>12</strong>주의 기간 마다 1회 정도의 빈도로 개체에 투여되<br />
는 것을 특징으로 하는 방법.<br />
청구항 105<br />
청구항 104에 있어서, 항-IL-6 항체 또는 항체 단편은 대략 16주의 기간 마다 1회 정도의 빈도로 개체에 투여되<br />
는 것을 특징으로 하는 방법<br />
청구항 106<br />
청구항 1 내지 40중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 IL-6 발현 질병 부위의 검출을 위한 진단<br />
효과량으로 투여되는 것을 특징으로 하는 방법.<br />
청구항 107<br />
청구항 106에 있어서, Ab1 항체 또는 항체 단편은 IL-6 발현 질병 부위에서 항체의 검출을 용이하게 하는 방사<br />
성핵종, 형광단, 또는 다른 검출가능 라벨에 직접적으로 또는 간접적으로 결합되는 것을 특징으로 하는 방법.<br />
청구항 108<br />
청구항 106에 있어서, IL-6 발현 종양 또는 전이를 검출하는데 이용되는 것을 특징으로 하는 방법.<br />
청구항 109<br />
청구항 106에 있어서, IL-6 발현 세포와 연관된 염증의 부위의 존재를 검출하는데 이용되는 것을 특징으로 하는<br />
방법.<br />
청구항 110<br />
청구항 106에 있어서, 결과는 적절한 치료 계획의 설계를 용이하게 하는데 이용되는 것을 특징으로 하는 방법.<br />
청구항 111<br />
청구항 106에 있어서, 상기 치료 계획은 방사선요법, 화학요법 또는 이들의 조합을 포함하는 것을 특징으로 하<br />
는 방법.<br />
청구항 1<strong>12</strong><br />
청구항 1 내지 101중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 화학요법제, 스타틴, 사이토킨, 면역억<br />
제제, 유전자 치료제, 항-응고제, 항-악액질제, 항-쇠약제, 항-피로제, 항-발열제, 항-메스꺼움제, 항-구토제,<br />
IL-6 길항제, 세포독성제, 진통제, 해열제, 소염제, 항생제, 항바이러스제, 항-사이토킨제, 다른 치료제, 또는<br />
이들의 임의의 조합을 포함하는 다른 치료제와 공동-투여되는 것을 특징으로 하는 방법.<br />
청구항 113<br />
청구항 1<strong>12</strong>에 있어서, 화학요법제는 VEGF 길항제, EGFR 길항제, 플라틴, 탁솔, 이리노테칸, 5-플루오로우라실,<br />
젬시타빈, 류코보린, 스테로이드, 시클로포스파미드, 멜팔란, 빈카 알칼로이드, 빈블라스틴, 빈크리스틴, 빈데<br />
신, 비노렐빈, 무스틴, 티로신 키나아제 저해제, 방사선요법, 성 호르몬 길항제, 선택성 안드로겐 수용체 조절<br />
제, 선택성 에스트로겐 수용체 조절제, PDGF 길항제, TNF 길항제, IL-1 길항제, 인터루킨, IL-<strong>12</strong>, IL-2, IL-<br />
<strong>12</strong>R 길항제, 독소 접합된 단일클론 항체, 종양 항원 특이적 단일클론 항체, Erbitux, Avastin,<br />
Pertuzumab, 항-CD20 항체, Rituxan<br />
, 오크렐리주맙, 오파투무맙, DXL625, Herceptin<br />
, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 114<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 1<strong>12</strong>에 있어서, 항-응고제는 아브식시맙(ReoPro), 아세노쿠마롤, 항트롬빈 III, 아르가트로반, 아스피<br />
린, 비발리루딘(Angiomax), 클로피도그렐, 다비가트란, 다비가트란 이텍실레이트(Pradaxa/Pradax), 데시<br />
- 17 -
루딘(Revasc/Iprivask), 디피리다몰, 엡티피바티드(Integrilin), 폰다파리눅스, 헤파린, 히루딘, 이드라<br />
파리눅스, 레피루딘(Refludan), 저분자량 헤파린, 멜라가트란, 페닌디온, 펜프로코우몬, 티클로피딘, 티로피<br />
반(Aggrastat), 와파린, 지멜라가트란, 지멜라가트란(Exanta/ Exarta), 또는 이들의 임의의 조합을 포함<br />
하는 것을 특징으로 하는 방법.<br />
청구항 115<br />
청구항 1<strong>12</strong>에 있어서, 스타틴은 아토르바스타틴, 체리바스타틴, 플루바스타틴, 로바스타틴, 메바스타틴, 피타바<br />
스타틴, 프라바스타틴, 로수바스타틴, 심바스타틴, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방<br />
법.<br />
청구항 116<br />
청구항 1<strong>12</strong>에 있어서, 다른 치료제는 종양 괴사 인자-알파, 인터페론 감마, 인터루킨 1 알파, 인터루킨 1 베타,<br />
인터루킨 6, 단백분해 유도 인자, 백혈병-저해 인자, 또는 이들의 임의의 조합을 포함하는 인자의 길항제인 것<br />
을 특징으로 하는 방법.<br />
청구항 117<br />
청구항 1<strong>12</strong>에 있어서, 항-악액질제는 칸나비스, 드로나비놀(Marinol), 나빌론(Cesamet), 칸나비디올, 칸나비<br />
크로멘, 테트라히드로칸나비놀, 사티벡스, 메게스트롤 아세테이트, 또는 이들의 임의의 조합을 포함하는 것을<br />
특징으로 하는 방법.<br />
청구항 118<br />
청구항 1<strong>12</strong>에 있어서, 항-메스꺼움제 또는 항-구토제는 5-HT3 수용체 길항제, 아쥬와인, 알리자프리드, 항콜린<br />
약, 항히스타민제, 아프레피탄트, 벤조디아제핀, 칸나비크로멘, 칸나비디올, 칸나비노이드, 칸나비스, 카소피탄<br />
트, 클로르프로마진, 시클리진, 덱사메타손, 덱사메타손, 디멘하이드리네이트(Gravol), 디펜히드라민, 돌라세<br />
트론, 돔페리돈, 도파민 길항제, 독실라민, 드로나비놀(Marinol), 드로페리돌, 에메트롤, 생강(ginger), 그라<br />
니세트론, 할로페리돌, 히드록사진, 히오신, 로라제팜, 메클리진, 메토클로프라미드, 미다졸람, 무시몰, 나빌론<br />
(Cesamet), nk1 수용체 길항제, 온단세트론, 팔로노세트론, 페퍼민트, 페너간, 프로클로르페라진, Promacot, 프<br />
로메타진, 펜타진, 프로포폴, 사티벡스, 테트라히드로칸나비놀, 트리메토벤자미드, 트로피세트론, 난드롤론, 스<br />
틸베스트롤, 탈리도미드, 레날리도미드, 그렐린 효능제, 미오스타틴 길항제, 항-미오스타틴 항체, 선택성 안드<br />
로겐 수용체 조절제, 선택성 에스트로겐 수용체 조절제, 앤지오텐신 AII 길항제, 베타 2 아드레날린성 수용체<br />
효능제, 베타 3 아드레날린성 수용체 효능제, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 1<strong>19</strong><br />
청구항 1<strong>12</strong>에 있어서, 다른 치료제는 타목시펜, BCL-2 길항제, 에스트로겐, 비스포스포네이트, 테리파라티드,<br />
스트론튬 라넬레이트, 나트륨 알렌드로네이트(Fosamax), 리세드로네이트(Actonel), 랄록시펜, 이반드로네이트<br />
(Boniva), 오바토클락스, ABT-263, 고시폴, 제피티닙, 상기 성장 인자 수용체 티로신 키나아제 저해제, 에를로<br />
티닙, 상피 성장 인자 수용체 저해제, 프소랄렌, 트리옥시살렌, 메톡살렌, 베르갑텐, 레티노이드, 에트레티네이<br />
트, 아시트레틴, 인플릭시맙(Remicade<br />
공개특허 10-2011-01<strong>12</strong>308<br />
), 아달리무맙, 인플릭시맙, 에타네르셉트, Zenapax, 시클로스포린, 메토트렉세이트, 과립구-집락 자극 인자,<br />
필그라스팀, 레노그라스팀, 뉴포젠, 뉴라스타, 2-아릴프로피온산, 아세클로페낙, 아세메타신, 아세틸살리실산<br />
(아스피린), 알클로페낙, 알미노프로펜, 아목시프린, 암피론, 아릴알카노산, 아자프로파존, 베노릴레이트, 베녹<br />
사프로펜, 브롬페낙, 카르프로펜, 셀레콕시브, 콜린 마그네슘 살리실레이트, 클로페존, COX-2 저해제, 덱시부프<br />
로펜, 덱스케토프로펜, 디클로페낙, 디플루니살, 드록시캄, 에텐자미드, 에토돌락, 에토리콕시브, 파이슬라민,<br />
페남산, 펜부펜, 페노프로펜, 플루페남산, 플루녹사프로펜, 플루비프로펜, 이부프로펜, 이부프록삼,<br />
인도메타신, 인도프로펜, 케부존, 케토프로펜, 케토롤락, 로르녹시캄, 록소프로펜, 루미라콕시브, 마그네슘 살<br />
리실레이트, 메클로페남산, 메페남산, 멜록시캄, 메타미졸, 메틸 살리실레이트, 모페부타존, 나부메톤, 나프록<br />
센, N-아릴안트라닐산, 옥사메타신, 옥사프로진, 옥시캄, 옥시펜부타존, 파레콕시브, 페나존, 페닐부타존, 페닐<br />
부타존, 피록시캄, 피르프로펜, 프로펜, 프로글루메타신, 피라졸리딘 유도체, 로페콕시브, 살리실<br />
살리실레이트, 살리실아미드, 살리실레이트, 설핀피라존, 설린닥, 수프로펜, 테녹시캄, 티아프로펜산,<br />
- 18 -
톨페남산, 톨메틴, 발데콕시브, 아미카신, 아미노글리코시드, 아목실린, 암피실린, 안사마이신, 아르스페나민,<br />
아지트로마이신, 아즐로실린, 아즈트레오남, 바시트라신, 카르바세펨, 카르바페넴, 카르베니실린, 세파클로르,<br />
세파드록실, 세팔렉신, 세팔로틴, 세팔로틴, 세파만돌, 세파졸린, 세프디니르, 세프디토렌, 세페핌, 세픽심, 세<br />
포페라존, 세포탁심, 세폭시틴, 세프포독심, 세프프로질, 세프타지딤, 세프티부텐, 세프티족심, 세프토비프롤,<br />
세프트리악손, 세푸록심, 세팔로스포린, 클로람페니콜, 실라스타틴, 시프로플록사신, 클라리트로마이신, 클린다<br />
마이신, 클록사실린, 콜리스틴, 코-트리목사졸, 달포프리스틴, 데메클로사이클린, 디클록사실린, 디리트로마이<br />
신, 도리페넴, 독시사이클린, 에녹사신, 에르타페넴, 에리트로마이신, 에탐부톨, 플루클록사실린,<br />
포스포마이신, 푸라졸리돈, 퓨시드산, 가티플록사신, 겔다나마이신, 젠타마이신, 글리코펩티드, 헤르비마이신,<br />
이미페넴, 이소니아지드, 카나마이신, 레보플록사신, 린코마이신, 리네졸리드, 로메플록사신, 로라카르베프, 마<br />
크롤리드, 마페니드, 메로페넴, 메티실린, 메트로니다졸, 메즐로실린, 미노사이클린, 모노박탐, 목시플록사신,<br />
무피로신, 나프실린, 네오마이신, 네틸마이신, 니트로푸란토인, 노르플록사신, 오플록사신, 옥사실린, 옥시테트<br />
라사이클린, 파로모마이신, 페니실린, 페니실린, 피페라실린, 플라텐시마이신, 폴리믹신 B, 폴리펩티드, 프론토<br />
실, 피라진아미드, 퀴놀론, 퀴누프리스틴, 리팜피신, 리팜핀, 록시트로마이신, 스펙티노마이신,<br />
스트렙토마이신, 설파세타미드, 설파메티졸, 설파닐아미드, 설파살라진, 설피속사졸, 설폰아미드,<br />
테이코플라닌, 텔리트로마이신, 테트라사이클린, 테트라사이클린, 티카르실린, 티니다졸, 토브라마이신, 트리메<br />
토프림, 트리메토프림-설파메톡사졸, 트롤레안도마이신, 트로바플록사신, 반코마이신, 알도스테론, 베클로메타<br />
손, 베타메타손, 코르티코스테로이드, 코르티솔, 코르티손 아세테이트, 데옥시코르티코스테론 아세테이트, 덱사<br />
메타손, 플루드로코르티손 아세테이트, 글루코코르티코이드, 하이드로코르티손, 메틸프레드니솔론, 프레드니솔<br />
론, 프레드니손, 스테로이드, 트리암시놀론, 아바카비르, 아시클로비르, 아시클로비르, 아데포비르, 아만타딘,<br />
암프레나비르, 항레트로바이러스 고정 용량 복합제, 항레트로바이러스 상승작용 강화제, 아르비돌, 아타자나비<br />
르, 아트리플라, 브리부딘, 시도포비르, 콤비비르, 다루나비르, 델라비르딘, 디다노신, 도코사놀, 에독수딘, 에<br />
파비렌즈, 엠트리시타빈, 엔푸비르티드, 엔테카비르, 침입 저해제, 팜시클로비르, 포미비르센, 포삼프레나비르,<br />
포스카르네트, 포스포네트, 융합 저해제, 간시클로비르, 가르다실, 이바시타빈, 이독수리딘, 이미퀴모드, 이무<br />
노비르, 인디나비르, 이노신, 인테그라아제 저해제, 인터페론, I형 인터페론, II형 인터페론, III형 인터페론,<br />
라미부딘, 로피나비르, 로비리드, 마라비록, MK-0518, 모록시딘, 넬피나비르, 네비라핀, 넥사비르, 뉴클레오시<br />
드 유사체, 오셀타미비르, 펜시클로비르, 페라미비르, 플레코나릴, 포도필로독소, 프로테아제 저해제, 역전사효<br />
소 저해제, 리바비린, 리만타딘, 리토나비르, 사퀴나비르, 스타부딘, 테노포비르, 테노포비르, 디소프록실, 티<br />
프라나비르, 트리플루리딘, 트리지비르, 트로만타딘, 트루바다, 발라시클로비르, 발간시클로비르, 비크리비록,<br />
비다라빈, 비라미딘, 잘시타빈, 자나미비르, 지도부딘, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하<br />
는 방법.<br />
청구항 <strong>12</strong>0<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 1<strong>12</strong>에 있어서, 세포독성제, 화학요법제, 또는 면역억제제는 1-데히드로테스토스테론, 1-메틸니트로소우<br />
레아, 5-플루오로우라실, 6-메르캅토퓨린, 6-메르캅토퓨린, 6-티오구아닌, 아바타셉트, 아브락산, 아시트레틴,<br />
아클라루비신, 악티늄-225( 225<br />
Ac), 악티노마이신, 아달리무맙, 아데노신 데아미나아제 저해제, 아펠리모맙, 아플<br />
리베르셉트, 아푸투주맙, 알레파셉트, 알리트레티노인, 알킬 설포네이트, 알킬화제, 알트레타민, 알보시딥, 아<br />
미노레불린산/메틸 아미노레불리네이트, 아미노프테린, 아미노프테린, 암루비신, 암사크린, 암사크린, 아나그렐<br />
리드, 아나킨라, 안트라센디온, 안트라사이클린, 안트라사이클린, 안트라사이클린, 안트라마이신(AMC); 항유사<br />
분열제, 항생제, 항-CD20 항체, 항엽산염(antifolate), 항-림프구 글로불린, 대사길항물질, 항-흉선세포 글로불<br />
린, 삼산화비소, 아셀리주맙, 아스파라기나아제, 아스파라긴 고갈제, 아스타틴-211( 211<br />
At), 아틀리주맙, 아토롤<br />
리무맙, 아트라센탄, Avastin, 아자시티딘, 아자티오프린, 아젤라스틴, 아지리딘, 바실릭시맙, BAYX 항체, 벨<br />
라타셉트, 벨리무맙, 벨로테칸, 벤다무스틴, 베르틸리무맙, 벡사로텐, 비산트렌, 비스무스-213( 213<br />
Bi), 비스무스<br />
-2<strong>12</strong>( 2<strong>12</strong><br />
Bi), 블레오마이신, 블레오마이신, 블레오마이신, BLyS 항체, 보르테조밉, 부설판, 부설판, 칼시뉴린 저<br />
해제, 칼리키아마이신, 캄토테신, 캄토테신, 카페시타빈, 카르보플라틴(파라플라틴), 카르보쿠온, 카르미노마이<br />
신, 카르모푸르, 카르무스틴, 카르무스틴(BSNU), CAT 항체, CD11a 항체, CD147/Basigin 항체, CD154 항체,<br />
CD18 항체, CD20 항체, CD23 항체, CD3 항체, CD4 항체, CD40 항체, CD62L/L-셀렉틴 항체, CD80 항체, CDK 저<br />
해제, 세델리주맙, 셀레콕시브, 세톨리주맙 페골, 클로람부실, 클로람부실, 시클로스포린, 시스-디클로로디아민<br />
백금(II)(DDP) 시스플라틴, 클라드리빈, 클레놀릭시맙, 클로파라빈, 콜히친, 보체 성분 5 항체, 구리-67( 67<br />
Cu),<br />
코르티코스테로이드, CTLA-4 항체, CTLA-4 융합 단백질, 시클로필린 저해제, 시클로포스파미드, 시클로토스파미<br />
- <strong>19</strong> -
드, 시타라빈, 시타라빈, 시토칼라신 B, 세포독성 리보뉴클레아제, 다카르바진, 다클리주맙, 닥티노마이신, 닥<br />
티노마이신(악티노마이신 D), 다우노루비신, 다우노루비신, 다우노루비신(구명칭: 다우노마이신), 데시타빈, 데<br />
포롤리무스, 디메콜신, 데토루비신, 디브로모만니톨, 디에틸카르바마진, 디히드로폴레이트 환원효소 저해제, 디<br />
히드록시 안트라신 디온, 디프테리아 독소, DNA 중합효소 저해제, 도세탁셀, 도를리모맙 아리톡스, 도를릭시주<br />
맙, 독소루비신(아드리아마이신), DXL625, 에쿨리주맙, 에팔리주맙, 에파프록시랄, EGFR 길항제, 엘레스클로몰,<br />
엘사미트루신, 엘실리모맙, 에메틴, 엔도텔린 수용체 길항제, 에피포도필로톡신, 에피루비신, 에포틸론,<br />
Erbitux, 에를리주맙, 에스트라무스틴, 에타네르셉트, 에티듐 브롬화물, 에토글루시드, 에토포시드, 에토포시<br />
드 인산염, 에베롤리무스, 파랄리모맙, 파르네실트랜스퍼라아제 저해제, FKBP 저해제, 플록수리딘, 플루다라빈,<br />
플루오로우라실, 폰톨리주맙, 포테무스틴, 갈릭시맙, 갈륨-67( 67<br />
Ga), 간테네루맙, 가빌리모맙, 젬시타빈, 글루코<br />
코르티코이드, 골리무맙, 고밀릭시맙, 그라미시딘 D, 구스페리무스, Herceptin<br />
, 히드라진, 히드록시우레아, 메틸화억제제(hypomethylating agent), 이다루비신, 이다루비신, 이포스파미드,<br />
IL-1 길항제, IL-1 수용체 길항제, IL-<strong>12</strong>, IL-<strong>12</strong> 항체, IL-<strong>12</strong>R 길항제, IL-13 항체, IL-2, IL-2 저해제, IL-2<br />
수용체/CD25 항체, IL-6 항체, 이마티닙 메실레이트, 면역글로불린 E 항체, IMP 탈수소효소 저해제,<br />
인플릭시맙, 이놀리모맙, 인테그린 항체, 인터페론 항체, 인터페론, 인터루킨 5 항체, 인터루킨-6 수용체 항체,<br />
인터루킨, 요오드-<strong>12</strong>5( <strong>12</strong>5<br />
I), 요오드-131( 131<br />
I), 이필리무맙, 이리노테칸, 익사베필론, 켈릭시맙, 라로탁셀, 납-<br />
2<strong>12</strong>( 2<strong>12</strong><br />
Pb), 레브릴리주맙, 레플루노미드, 레날리도미드, 레르델리무맙, 류코보린, LFA-1 항체, 리도카인, 리폭<br />
시게나아제 저해제, 로무스틴(CCNU), 로니다민, 루칸톤, 루밀릭시맙, 루테튬-177( 177<br />
Lu), 마크롤리드, 만노설판,<br />
마실리모맙, 마소프로콜, 메클로레타민, 멜팔란, 메폴리주맙, 메르캅토퓨린, 메텔리무맙, 메토트렉세이트, 미세<br />
소관 조립 저해제, 미세소관 안정성 강화제, 미트라마이신, 미토브로니톨, 미토구아존, 미토마이신, 미토마이신<br />
C, 미토탄, 미톡산트론, 모롤리무맙, mTOR 저해제, 무로모납-CD3, 무스틴, 미코페놀산, 미토탄(O,P'-(DDD)), 나<br />
탈리주맙, 네다플라틴, 네렐리모맙, 니무스틴, 질소 머스타드, 니트로소우레아, 노르디히드로구아이아레틱산<br />
(nordihydroguaiaretic acid), 오블리메르센, 오크렐리주맙, 오크렐리주맙, 오둘리모맙, 오파투무맙, 올라파립,<br />
오말리주맙, 오르타탁셀, 오텔릭시주맙, 옥살리플라틴, 옥살리플라틴, 파클리탁셀(탁솔), 파스콜리주맙, PDGF<br />
길항제, 페가스파가제, 페메트렉세드, 펜토스타틴, 페르투주맙, 펙셀리주맙, 포스포디에스테라아제 저해제, 인-<br />
32( 32<br />
P), 피메크롤리무스 아베티무스, 피라루비신, 픽산트론, 플라틴, 플리카마이신, 폴리 ADP 리보오스 중합효<br />
소 저해제, 포르피머 나트륨, 포르피린 유도체, 프레드니무스틴, 프로카인, 프로카르바진, 프로카르바진, 프로<br />
프라놀롤, 프로테아좀 저해제, 슈도모나스(Pseudomonas) 외독소, 슈도모나스(Pseudomonas) 독소, 퓨린 합성 저<br />
해제, 퓨로마이신, 피리미딘 합성 저해제, 방사성핵종, 방사선요법, 랄티트렉세드, 라니무스틴, 레슬리주맙, 레<br />
티노이드 X 수용체 효능제, 레티노이드, 레늄-186( 186<br />
Re), 레늄-188( 188<br />
Re), 리보뉴클레오티드 환원효소 저해제,<br />
리신, 릴로나셉트, Rituxan<br />
, 로벨리주맙, 루비테칸, 루플리주맙, 사마륨-153( 153<br />
Sm), 사트라플라틴, 스칸듐-47( 47<br />
Sc), 선택성 안드로겐 수용<br />
체 조절제, 선택성 에스트로겐 수용체 조절제, 셀리시클립, 세무스틴, 성 호르몬 길항제, 시플리주맙, 시롤리무<br />
스, 스테로이드 아로마타아제 저해제, 스테로이드, 스트렙토조신, 스트렙토조토신, 타크롤리무스, 탈라포르핀,<br />
탈리주맙, 탁산, 탁솔, 테가푸르, 텔리모맙 아리톡스, 테모포르핀, 테모졸로미드, 템시롤리무스, 템시롤리무스,<br />
테넬릭시맙, 테니포시드, 테플리주맙, 테리플루노미드, 테세탁셀, 테스톨락톤, 테트라카인, 탈리도미드, 티오에<br />
파 클로람부실, 티오퓨린 티오구아닌, 티오TEPA(ThioTEPA), 티미딜레이트 신타아제 저해제, 티아조푸린, 티피파<br />
르닙, T-림프구 항체, TNF 길항제, TNF 항체, TNF 융합 단백질, TNF 수용체 융합 단백질, TNF-알파 저해제, 토<br />
클리주맙, 토포이소머라제 저해제, 토포테칸, 토랄리주맙, 트라벡테딘, 트레멜리무맙, 트레오설판, 트레티노인,<br />
트리아젠, 트리아지쿠온, 트리에틸렌멜라민, 트리플라틴 테트라니트레이트, 트로포스파미드, 종양 항원 특이적<br />
단일클론 항체, 티로신 키나아제 저해제, 우라무스틴, 우스테키누맙, 발루비신, 발루비신, 바팔릭시맙, VEGF 길<br />
항제, 베팔리모맙, 베르테포르핀, 빈블라스틴, 빈카 알칼로이드, 빈크리스틴, 빈데신, 빈플루닌, 비노렐빈, 비<br />
실리주맙, 보리노스타트, 이트튬-88( 88<br />
Y), 이트튬-90( 90<br />
Y), 자놀리무맙, 질류톤, 지랄리무맙, 졸리모맙<br />
아리톡스, 조루비신, 조타롤리무스, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>1<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 1<strong>12</strong>에 있어서, 다른 활성제는 TNF-알파, IL-2, IL-4, IL-6, IL-10, IL-<strong>12</strong>, IL-13, IL-18, IFN-알파,<br />
- 20 -
IFN-감마, BAFF, CXCL13, IP-10, VEGF, EPO, EGF, HRG, 간세포 성장 인자(HGF), 헵시딘, 또는 이들의 임의의<br />
조합을 포함하는 인자의 하나 이상의 효능제, 길항제, 또는 조절제인 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>2<br />
청구항 1<strong>12</strong>에 있어서, IL-6 길항제는 항-IL-6 항체 또는 이의 단편, 안티센스 핵산, 폴리펩티드, 소분자, 또는<br />
이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>3<br />
청구항 <strong>12</strong>2에 있어서, 안티센스 핵산은 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1, JAK2, JAK3,<br />
또는 SYK를 인코딩하는 서열의 적어도 대략 10개의 뉴클레오티드를 포함하는 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>4<br />
청구항 <strong>12</strong>2에 있어서, 안티센스 핵산은 DNA, RNA, 펩티드 핵산, 잠금(locked) 핵산, 모르폴리노(포스포로디아미<br />
데이트 모르폴리노 올리고), 글리세롤 핵산, 트레오즈(threose) 핵산, 또는 이들의 임의의 조합을 포함하는 것<br />
을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>5<br />
청구항 <strong>12</strong>2에 있어서, 항-IL-6 항체 또는 이의 단편은 Ab1, Ab2, Ab3, Ab4, Ab5, Ab6, Ab7, Ab8, Ab9, Ab10,<br />
Ab11, Ab<strong>12</strong>, Ab13, Ab14, Ab15, Ab16, Ab17, Ab18, Ab<strong>19</strong>, Ab20, Ab21, Ab22, Ab23, Ab24, Ab25, Ab26, Ab27,<br />
Ab28, Ab29, Ab30, Ab31, Ab32, Ab33, Ab34, Ab35, Ab36, 이들 중에서 한 가지의 IL-6 결합 단편, 이들 중에서<br />
한 가지의 변이체, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>6<br />
청구항 <strong>12</strong>2에 있어서, IL-6 길항제 폴리펩티드는 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1,<br />
JAK2, JAK3, 그리고 SYK로 구성된 군에서 선택되는 서열을 갖는 폴리펩티드의 단편을 포함하는 것을 특징으로<br />
하는 방법.<br />
청구항 <strong>12</strong>7<br />
청구항 <strong>12</strong>6에 있어서, 단편은 적어도 40개 아미노산 길이를 갖는 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>8<br />
청구항 <strong>12</strong>2에 있어서, IL-6 길항제는 가용성 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1, JAK2,<br />
JAK3, SYK, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 방법.<br />
청구항 <strong>12</strong>9<br />
청구항 1<strong>12</strong>에 있어서, IL-6 길항제는 반감기 증가 모이어티에 결합되는 것을 특징으로 하는 방법.<br />
청구항 130<br />
청구항 1<strong>12</strong> 내지 <strong>12</strong>9중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 하나 이상의 다른 치료제에 직접적으<br />
로 또는 간접적으로 결합되는 것을 특징으로 하는 방법.<br />
청구항 131<br />
청구항 1 내지 101중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 검출가능 라벨에 직접적으로 또는 간접<br />
적으로 결합되는 것을 특징으로 하는 방법.<br />
청구항 132<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 131에 있어서, 검출가능 라벨은 형광 염료, 생물발광 물질, 방사성 물질, 화학발광 모이어티, 스트렙타<br />
비딘, 아비딘, 비오틴, 방사성 물질, 효소, 기질, 양고추냉이 과산화효소, 아세틸콜린에스테라아제, 알칼리성<br />
포스파타아제, 베타-갈락토시다아제, 루시페라아제, 로다민, 플루오레세인, 플루오레세인 이소티오시아네이트,<br />
- 21 -
움벨리페론, 디클로로트리아지닐아민, 피코에리트린, 염화단실, 루미놀, 루시페린, 에쿼린(aequorin), 요오드<br />
<strong>12</strong>5( <strong>12</strong>5<br />
I), 탄소 14( 14<br />
C), 황 35( 35<br />
S), 트리튬( 3<br />
H), 32( 32<br />
P), 또는 이들의 임의의 조합을 포함하는 것을 특징으로<br />
하는 방법.<br />
청구항 133<br />
청구항 1 내지 30 또는 청구항 34 내지 <strong>12</strong>8중 어느 한 항에 있어서, Ab1 항체는 Ab1 항체를 인코딩하는 하나 이<br />
상의 핵산 형태로 개체에 투여되는 것을 특징으로 하는 방법.<br />
청구항 134<br />
청구항 133에 있어서, 하나 이상의 핵산은 바이러스, 리포좀, 양이온성 지질 복합체, 양이온성 중합체 복합체,<br />
또는 나노입자 복합체로서 수용자 내로 도입되는 것을 특징으로 하는 방법.<br />
청구항 135<br />
청구항 133에 있어서, 하나 이상의 핵산은 효모 또는 인간 선호 코돈(preferred codon)으로 구성되는 것을 특징<br />
으로 하는 방법.<br />
청구항 136<br />
청구항 133에 있어서, 하나 이상의 핵산은 벡터 내에 포함되는 것을 특징으로 하는 방법.<br />
청구항 137<br />
청구항 136에 있어서, 벡터는 플라스미드 또는 재조합 바이러스 벡터인 것을 특징으로 하는 방법.<br />
청구항 138<br />
청구항 133에 있어서, 하나 이상의 핵산은 서열 번호: 723과 서열 번호: 700; 서열 번호: 701과 서열 번호:<br />
703; 서열 번호: 705와 서열 번호: 707; 서열 번호: 720과 서열 번호: 724; 그리고 서열 번호: 10과 서열 번호:<br />
11의 중쇄와 경쇄 폴리뉴클레오티드 서열을 포함하는 것을 특징으로 하는 방법.<br />
청구항 139<br />
전술한 항중 어느 한 항에 있어서, Ab1 항체는<br />
(a) 서열 번호: 709와 서열 번호: 657; 서열 번호: 702와 서열 번호: 704; 서열 번호: 706과 서열 번호: 708;<br />
서열 번호: 20과 서열 번호: <strong>19</strong>; 또는 서열 번호: 2와 서열 번호: 3을 포함하는 경쇄와 중쇄 폴리펩티드;<br />
(b) (a)의 임의의 폴리펩티드에 적어도 80%, 85%, 90%, 95%, 96%, 97%, 98%, 또는 99% 동일성을 갖는 폴리펩티<br />
드;<br />
(c) 중간으로 또는 고도로 엄밀한 하이브리드화 조건 하에, 서열 번호: 723과 서열 번호: 700; 서열 번호: 701<br />
과 서열 번호: 703; 서열 번호: 705와 서열 번호: 707; 서열 번호: 720과 서열 번호: 724; 그리고 서열 번호:<br />
10과 서열 번호: 11의 임의의 중쇄와 경쇄 폴리뉴클레오티드 서열에 하이브리드화되는 폴리뉴클레오티드;<br />
(d) 서열 번호: 723과 서열 번호: 700; 서열 번호: 701과 서열 번호: 703; 서열 번호: 705와 서열 번호: 707;<br />
서열 번호: 720과 서열 번호: 724; 그리고 서열 번호: 10과 서열 번호: 11의 임의의 중쇄와 경쇄 폴리뉴클레오<br />
티드 서열에 적어도 80%, 85%, 90%, 95%, 96%, 97%, 98%, 또는 99% 동일성을 갖는 폴리뉴클레오티드;<br />
(e) (c) 또는 (d)의 임의의 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드를 포함하는 것을 특징으로 하는 방<br />
법.<br />
청구항 140<br />
Ab1 항체 및 다른 치료 화합물을 포함하는 치료 조성물로서,<br />
공개특허 10-2011-01<strong>12</strong>308<br />
Ab1 항체는 서열 번호: 709에 적어도 75% 동일성을 갖는 폴리펩티드, 서열 번호: 723의 폴리뉴클레오티드에 적<br />
어도 75% 동일성을 갖는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드, 중간 엄밀도 조건 하에 서열 번호:<br />
723의 역상보 서열을 갖는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티<br />
- 22 -
드, 또는 높은 엄밀도 조건 하에 서열 번호: 723의 역상보 서열을 갖는 폴리뉴클레오티드에 하이브리드화되는<br />
폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드를 포함하는 경쇄 폴리펩티드; 그리고<br />
서열 번호: 657에 적어도 75% 동일성을 갖는 폴리펩티드, 서열 번호: 700의 폴리뉴클레오티드에 적어도 75% 동<br />
일성을 갖는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드, 중간 엄밀도 조건 하에 서열 번호: 700의 역상보<br />
서열을 갖는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드, 또는 높은<br />
엄밀도 조건 하에 서열 번호: 700의 역상보 서열을 갖는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티<br />
드에 의해 인코딩되는 폴리펩티드를 포함하는 중쇄 폴리펩티드를 포함하고;<br />
여기서 Ab1 항체 또는 항체 단편은 IL-6에 특이적으로 결합하고 IL-6과 연관된 한 가지 이상의 활성을<br />
길항하고; 그리고<br />
여기서 다른 치료 화합물은 화학요법제, 스타틴, 사이토킨, 유전자 치료제, 항-응고제, 항-악액질제,<br />
항-쇠약제, 항-피로제, 항-발열제, 항-메스꺼움제, 항-구토제, IL-6 길항제, 세포독성제, 다른 치료 화합물, 또<br />
는 이들의 임의의 조합을 포함하는, 치료 조성물.<br />
청구항 141<br />
청구항 140에 있어서, 경쇄 폴리펩티드는 서열 번호: 709의 경쇄 골격 영역 서열과 비교하여, 경쇄 골격 영역<br />
(들) 내에서 하나 이상의 치환을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 142<br />
청구항 141에 있어서, 경쇄 골격 영역(들) 내에서 하나 이상의 치환은 공여자 서열의 상응하는 위치의 서열에<br />
의한 치환이고, 여기서 공여자 서열은 서열 번호: 2; 인간, 토끼, 또는 비-인간 영장류 경쇄 서열; 그리고 Ab2,<br />
Ab3, Ab4, Ab5, Ab6, Ab7, Ab8, Ab9, Ab10, Ab11, Ab<strong>12</strong>, Ab13, Ab14, Ab15, Ab16, Ab17, Ab18, Ab<strong>19</strong>, Ab20,<br />
Ab21, Ab22, Ab23, Ab24, Ab25, Ab26, Ab27, Ab28, Ab29, Ab30, Ab31, Ab32, Ab33, Ab34, Ab35, 또는 Ab36 중<br />
에서 한 가지의 경쇄를 포함하고,<br />
여기서 치환은 하나 이상의 아미노산의 대체, 삽입 및/또는 결실을 유발하고, 그리고<br />
여기서 상응하는 위치는 서열 번호: 709의 골격 영역과 공여자 서열 사이의 서열 정렬에 의해 결정되는 것을 특<br />
징으로 하는 치료 조성물.<br />
청구항 143<br />
청구항 142에 있어서, 중쇄 폴리펩티드는 서열 번호: 657의 중쇄 골격 영역 서열과 비교하여 중쇄 골격<br />
영역(들) 내에서 하나 이상의 치환을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 144<br />
청구항 143에 있어서, 중쇄 골격 영역(들) 내에서 하나 이상의 치환은 공여자 서열의 상응하는 위치의 서열에<br />
의한 치환이고, 여기서 공여자 서열은<br />
서열 번호: 3; 인간, 토끼, 또는 비-인간 영장류 중쇄 서열; 그리고 Ab2, Ab3, Ab4, Ab5, Ab6, Ab7, Ab8, Ab9,<br />
Ab10, Ab11, Ab<strong>12</strong>, Ab13, Ab14, Ab15, Ab16, Ab17, Ab18, Ab<strong>19</strong>, Ab20, Ab21, Ab22, Ab23, Ab24, Ab25, Ab26,<br />
Ab27, Ab28, Ab29, Ab30, Ab31, Ab32, Ab33, Ab34, Ab35, 또는 Ab36 중에서 한 가지의 중쇄를 포함하고,<br />
여기서 치환은 하나 이상의 아미노산의 대체, 삽입 및/또는 결실을 유발하고, 그리고<br />
여기서 상응하는 위치는 서열 번호: 657의 골격 영역과 공여자 서열 사이의 서열 정렬에 의해 결정되는 것을 특<br />
징으로 하는 치료 조성물.<br />
청구항 145<br />
청구항 140 내지 144중 어느 한 항에 있어서,<br />
경쇄 폴리펩티드는<br />
서열 번호: 4에 적어도 72.7% 동일성(11개 잔기 중에서 적어도 8개에 동일)을 갖는 경쇄 CDR1;<br />
- 23 -<br />
공개특허 10-2011-01<strong>12</strong>308
서열 번호: 5에 적어도 85.7% 동일성(7개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR2;<br />
서열 번호: 6에 적어도 50% 동일성(<strong>12</strong>개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR3;<br />
서열 번호: 4에 적어도 90.9% 유사성(11개 잔기 중에서 적어도 10개에 유사)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 100% 유사성(7개 잔기 중에서 적어도 7개에 유사)을 갖는 경쇄 CDR2; 또는<br />
서열 번호: 6에 적어도 66.6% 유사성(<strong>12</strong>개 잔기 중에서 적어도 8개에 유사)을 갖는 경쇄 CDR3을 포함하는 하나<br />
이상의 Ab1 경쇄 CDR 폴리펩티드를 포함하고; 그리고<br />
중쇄 폴리펩티드는<br />
서열 번호: 7에 적어도 80% 동일성(5개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 50% 동일성(16개 잔기 중에서 적어도 8개에 동일)을 갖는 중쇄 CDR2;<br />
서열 번호: 9에 적어도 33.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR3;<br />
서열 번호: 7에 적어도 100% 유사성(5개 잔기 중에서 적어도 5개에 유사)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 56.2% 유사성(16개 잔기 중에서 적어도 9개에 유사)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 50% 유사성(<strong>12</strong>개 잔기 중에서 적어도 6개에 유사)을 갖는 중쇄 CDR3을 포함하는 하나 이<br />
상의 Ab1 중쇄 CDR 폴리펩티드를 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 146<br />
청구항 140 내지 144중 어느 한 항에 있어서,<br />
경쇄 폴리펩티드는<br />
서열 번호: 4에 적어도 81.8% 동일성(11개 잔기 중에서 적어도 9개에 동일)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 71.4% 동일성(7개 잔기 중에서 적어도 5개에 동일)을 갖는 경쇄 CDR2; 또는<br />
서열 번호: 6에 적어도 83.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 10개에 동일)을 갖는 경쇄 CDR3을 포함하는 하나<br />
이상의 Ab1 경쇄 CDR 폴리펩티드를 포함하고; 그리고<br />
중쇄 폴리펩티드는<br />
서열 번호: 7에 적어도 60% 동일성(5개 잔기 중에서 적어도 3개에 동일)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 87.5% 동일성(16개 잔기 중에서 적어도 14개에 동일)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 83.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 10개에 동일)을 갖는 중쇄 CDR3을 포함하는 하나<br />
이상의 Ab1 중쇄 CDR 폴리펩티드를 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 147<br />
청구항 145 내지 146중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 상기 경쇄 CDR 폴리펩티드 중에서 적<br />
어도 2개 및 상기 중쇄 CDR 폴리펩티드 중에서 적어도 2개를 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 148<br />
Ab1 항체 및 다른 치료 화합물을 포함하는 치료 조성물로서,<br />
Ab1 항체는<br />
서열 번호: 4에 적어도 72.7% 동일성(11개 잔기 중에서 적어도 8개에 동일)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 85.7% 동일성(7개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR2; 또는<br />
서열 번호: 6에 적어도 50% 동일성(<strong>12</strong>개 잔기 중에서 적어도 6개에 동일)을 갖는 경쇄 CDR3을 포함하는 2개 이<br />
상의 Ab1 경쇄 CDR 폴리펩티드; 그리고<br />
서열 번호: 7에 적어도 80% 동일성(5개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR1;<br />
- 24 -<br />
공개특허 10-2011-01<strong>12</strong>308
서열 번호: <strong>12</strong>0에 적어도 50% 동일성(16개 잔기 중에서 적어도 8개에 동일)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 33.3% 동일성(<strong>12</strong>개 잔기 중에서 적어도 4개에 동일)을 갖는 중쇄 CDR3을 포함하는 2개<br />
이상의 Ab1 중쇄 CDR 폴리펩티드를 포함하고;<br />
여기서 Ab1 항체 또는 항체 단편은 IL-6에 특이적으로 결합하고 IL-6과 연관된 한 가지 이상의 활성을<br />
길항하고, 그리고<br />
여기서 다른 치료 화합물은 화학요법제, 스타틴, 사이토킨, 유전자 치료제, 항-응고제, 항-악액질제,<br />
항-쇠약제, 항-피로제, 항-발열제, 항-메스꺼움제, 항-구토제, IL-6 길항제, 세포독성제, 다른 치료 화합물, 또<br />
는 이들의 임의의 조합을 포함하는, 치료 조성물.<br />
청구항 149<br />
Ab1 항체 및 다른 치료 화합물을 포함하는 치료 조성물로서,<br />
Ab1 항체는<br />
서열 번호: 4에 적어도 90.9% 유사성(11개 잔기 중에서 적어도 10개에 유사)을 갖는 경쇄 CDR1;<br />
서열 번호: 5에 적어도 100% 유사성(7개 잔기 중에서 적어도 7개에 유사)을 갖는 경쇄 CDR2; 그리고<br />
서열 번호: 6에 적어도 66.6% 유사성(<strong>12</strong>개 잔기 중에서 적어도 8개에 유사)을 갖는 경쇄 CDR3; 그리고<br />
서열 번호: 7에 적어도 100% 유사성(5개 잔기 중에서 적어도 5개에 유사)을 갖는 중쇄 CDR1;<br />
서열 번호: <strong>12</strong>0에 적어도 56.2% 유사성(16개 잔기 중에서 적어도 9개에 유사)을 갖는 중쇄 CDR2; 또는<br />
서열 번호: 9에 적어도 50% 유사성(<strong>12</strong>개 잔기 중에서 적어도 6개에 유사)을 갖는 중쇄 CDR3을 포함하는 2개 이<br />
상의 Ab1 중쇄 CDR 폴리펩티드를 포함하고;<br />
여기서 Ab1 항체 또는 항체 단편은 IL-6에 특이적으로 결합하고 IL-6과 연관된 한 가지 이상의 활성을<br />
길항하고, 그리고<br />
여기서 다른 치료 화합물은 화학요법제, 스타틴, 사이토킨, 유전자 치료제, 항-응고제, 항-악액질제,<br />
항-쇠약제, 항-피로제, 항-발열제, 항-메스꺼움제, 항-구토제, IL-6 길항제, 세포독성제, 다른 치료 화합물, 또<br />
는 이들의 임의의 조합을 포함하는, 치료 조성물.<br />
청구항 150<br />
청구항 148 내지 149중 어느 한 항에 있어서, 상기 Ab1 항체 또는 항체 단편은 상기 경쇄 CDR1, 상기 경쇄<br />
CDR3, 상기 중쇄 CDR2, 그리고 상기 중쇄 CDR3을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 151<br />
청구항 148 내지 149중 어느 한 항에 있어서, 상기 Ab1 항체 또는 항체 단편은 상기 경쇄 CDR1, 상기 경쇄<br />
CDR2, 상기 경쇄 CDR3, 상기 중쇄 CDR1, 상기 중쇄 CDR2, 그리고 상기 중쇄 CDR3을 포함하는 것을 특징으로 하<br />
는 치료 조성물.<br />
청구항 152<br />
청구항 144 내지 147중 어느 한 항에 있어서, 상기 경쇄와 중쇄 CDR 폴리펩티드는 Fab, Fab', F(ab')2, Fv,<br />
scFv, IgNAR, SMIP, 카멜바디, 또는 나노바디를 포함하는 항체 또는 항체 단편 내에 포함되는 것을 특징으로 하<br />
는 치료 조성물.<br />
청구항 153<br />
청구항 148 내지 151중 어느 한 항에 있어서,<br />
Ab1 항체 또는 항체 단편의 가변 경쇄와 중쇄 영역 각각에서 골격 영역(FR) 1, 2, 3과 4는 변형되지 않거나, 또<br />
는 각각, 서열 번호: 2와 서열 번호: 3의 모 토끼 항체 경쇄 또는 중쇄의 상응하는 FR 잔기에 의한 2개 또는 3<br />
개 정도의 인간 FR 잔기의 치환에 의해 변형된, 인간 FR이고,<br />
- 25 -<br />
공개특허 10-2011-01<strong>12</strong>308
여기서 상기 인간 경쇄 FR 1, 2와 3은 FR1의 시작에서부터 FR3의 끝까지 연장되는 서열 번호: 2의 모 토끼 항체<br />
경쇄의 하위서열에 대한 높은 상동성 수준(인간 생식선 항체 서열의 라이브러리 또는 데이터베이스 내에 포함된<br />
다른 인간 생식선 항체 서열에 비하여)에 기초하여 인간 생식선 항체 서열의 라이브러리 또는 데이터베이스로부<br />
터 선택된 인간 가변 경쇄 항체 서열로부터 유래되고; 그리고<br />
여기서 상기 인간 경쇄 FR4는 서열 번호: 2 내에 포함된 모 토끼 항체 경쇄 FR4에 대한 높은 상동성 수준(인간<br />
생식선 항체 서열의 라이브러리 또는 데이터베이스 내에 포함된 다른 인간 생식선 항체 서열에 비하여)에 기초<br />
하여 인간 생식선 항체 서열의 라이브러리 또는 데이터베이스로부터 선택된 인간 가변 경쇄 항체 서열로부터 유<br />
래되고; 그리고<br />
여기서 상기 인간 중쇄 FR 1, 2와 3은 FR1의 시작에서부터 FR3의 끝까지 연장되는 서열 번호: 3의 모 토끼 항체<br />
중쇄의 하위서열에 대한 높은 상동성 수준(인간 생식선 항체 서열의 라이브러리 또는 데이터베이스 내에 포함된<br />
다른 인간 생식선 항체 서열에 비하여)에 기초하여 인간 생식선 항체 서열의 라이브러리 또는 데이터베이스로부<br />
터 선택된 인간 가변 중쇄 항체 서열로부터 유래되고; 그리고<br />
여기서 상기 인간 중쇄 FR4는 서열 번호: 3 내에 포함된 모 토끼 항체 중쇄 FR4에 대한 높은 상동성 수준(인간<br />
생식선 항체 서열의 라이브러리 또는 데이터베이스 내에 포함된 다른 인간 생식선 항체 서열에 비하여)에 기초<br />
하여 인간 생식선 항체 서열의 라이브러리 또는 데이터베이스로부터 선택된 인간 가변 중쇄 항체 서열로부터 유<br />
래되는 것을 특징으로 하는 치료 조성물.<br />
청구항 154<br />
청구항 140 내지 153중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 건강한 인간 개체에서 적어도 대략 22<br />
일의 생체내 반감기를 갖는 것을 특징으로 하는 치료 조성물.<br />
청구항 155<br />
청구항 140 내지 153중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 건강한 인간 개체에서 적어도 대략 25<br />
일의 생체내 반감기를 갖는 것을 특징으로 하는 치료 조성물.<br />
청구항 156<br />
청구항 140 내지 153중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 건강한 인간 개체에서 적어도 대략 30<br />
일의 생체내 반감기를 갖는 것을 특징으로 하는 치료 조성물.<br />
청구항 157<br />
청구항 140 내지 156중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 대략 50 피코몰 미만의 IL-6에 대한<br />
결합 친화성(Kd), 또는 10 -4<br />
조성물.<br />
청구항 158<br />
S -1<br />
이하의 IL-6으로부터의 해리 속도(Koff)를 갖는 것을 특징으로 하는 치료<br />
청구항 140 내지 157중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 완전한 인간 IL-6 폴리펩티드 또는 이<br />
의 단편 상에 존재하는, 서열 번호: 702와 서열 번호: 704의 폴리펩티드 또는 서열 번호: 2와 서열 번호: 3의<br />
폴리펩티드로 본질적으로 구성되는 항-IL-6 항체와 동일한 선형 또는 입체형태적 에피토프(들)에 특이적으로 결<br />
합하고 및/또는 상기 선형 또는 입체형태적 에피토프(들)에 결합하는 것에 대해 경쟁하는 것을 특징으로 하는<br />
치료 조성물.<br />
청구항 159<br />
청구항 158에 있어서, 완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는 동일한 선형 또는 입체형태<br />
적 에피토프에 결합 및/또는 이러한 선형 또는 입체형태적 에피토프에 결합하는 것에 대한 경쟁은 본래의 인간<br />
IL-6 폴리펩티드의 전장에 걸쳐있는 겹쳐지는 선형 펩티드 단편들을 이용한 에피토프 매핑에 의해 확인되고, 그<br />
리고 서열 번호: 1의 아미노산 잔기 37-51, 아미노산 잔기 70-84, 아미노산 잔기 169-183, 아미노산 잔기 31-45<br />
및/또는 아미노산 잔기 58-72를 각각 포함하는 것들에서 선택되는 IL-6 단편 내에 포함된 하나 이상의 잔기를<br />
포함하는 것을 특징으로 하는 치료 조성물.<br />
- 26 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 160<br />
청구항 140 내지 159중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 비당화되는 것을 특징으로 하는 치료<br />
조성물.<br />
청구항 161<br />
청구항 140 내지 160중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 이펙터 기능, 반감기,<br />
단백질가수분해, 및/또는 당화(glycosylation)를 변화시키기 위하여 변형된 Fc 영역을 함유하는 것을 특징으로<br />
하는 치료 조성물.<br />
청구항 162<br />
청구항 140 내지 161중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 인간, 인간화, 단일 사슬, 또는 키메<br />
라 항체인 것을 특징으로 하는 치료 조성물.<br />
청구항 163<br />
청구항 140 내지 162중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 Fab, Fab', F(ab')2, Fv, 또는 scFv를<br />
포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 164<br />
청구항 140 내지 163중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 인간 Fc를 추가로 포함하는 것을 특징<br />
으로 하는 치료 조성물.<br />
청구항 165<br />
청구항 164에 있어서, 인간 Fc는 IgG1, IgG2, IgG3, IgG4, IgG5, IgG6, IgG7, IgG8, IgG9, IgG10, IgG11,<br />
IgG<strong>12</strong>, IgG13, IgG14, IgG15, IgG16, IgG17, IgG18 또는 IgG<strong>19</strong>로부터 유래되는 것을 특징으로 하는 치료 조성<br />
물.<br />
청구항 166<br />
청구항 140 내지 165중 어느 한 항에 있어서, IL-6과 연관된 한 가지 이상의 활성은 감소된 혈청 알부민; 상승<br />
된 C-반응성 단백질("CRP"); 피로; 발열; 식욕부진(식욕의 상실); 체중 감소; 악액질; 쇠약; 감소된 Glasgow 예<br />
후 점수("GPS"); 상승된 혈청 D-이합체; 비정상적인 혈액응고 프로필; 또는 이들의 임의의 조합을 포함하는 생<br />
체내 활성인 것을 특징으로 하는 치료 조성물.<br />
청구항 167<br />
청구항 140 내지 165중 어느 한 항에 있어서, IL-6과 연관된 한 가지 이상의 활성 중에서 한 가지 이상은 T1165<br />
세포의 증식 자극; IL-6R에 대한 IL-6의 결합; gp130 신호-전달 당단백질의 활성화(이합체화); IL-6/IL-<br />
6R/gp130 멀티머의 형성; 인간 IL-6 수용체를 발현하도록 변형된 HepG2 세포에 의한 합토글로빈 생산의 자극,<br />
또는 이들의 임의의 조합을 포함하는 시험관내 활성인 것을 특징으로 하는 치료 조성물.<br />
청구항 168<br />
청구항 140 내지 167중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 재조합 세포로부터 발현되는 것을 특<br />
징으로 하는 치료 조성물.<br />
청구항 169<br />
청구항 168에 있어서, 세포는 포유동물, 효모, 세균, 그리고 곤충 세포에서 선택되는 것을 특징으로 하는 치료<br />
조성물.<br />
청구항 170<br />
청구항 169에 있어서, 세포는 효모 세포인 것을 특징으로 하는 치료 조성물.<br />
- 27 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 171<br />
청구항 170에 있어서, 세포는 2배체 효모 세포인 것을 특징으로 하는 치료 조성물.<br />
청구항 172<br />
청구항 171에 있어서, 효모 세포는 피치아(Pichia) 효모인 것을 특징으로 하는 치료 조성물.<br />
청구항 173<br />
청구항 140 내지 172중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 화학요법제, 스타틴, 사이토킨, 면역<br />
억제제, 유전자 치료제, 항-응고제, 항-악액질제, 항-쇠약제, 항-피로제, 항-발열제, 항-메스꺼움제,<br />
항-구토제, IL-6 길항제, 세포독성제, 진통제, 해열제, 소염제, 항생제, 항바이러스제, 항-사이토킨제, 다른 치<br />
료제, 또는 이들의 임의의 조합을 포함하는 다른 치료제와 공동-투여되는 것을 특징으로 하는 치료 조성물.<br />
청구항 174<br />
청구항 173에 있어서, 화학요법제는 VEGF 길항제, EGFR 길항제, 플라틴, 탁솔, 이리노테칸, 5-플루오로우라실,<br />
젬시타빈, 류코보린, 스테로이드, 시클로포스파미드, 멜팔란, 빈카 알칼로이드, 빈블라스틴, 빈크리스틴, 빈데<br />
신, 비노렐빈, 무스틴, 티로신 키나아제 저해제, 방사선요법, 성 호르몬 길항제, 선택성 안드로겐 수용체 조절<br />
제, 선택성 에스트로겐 수용체 조절제, PDGF 길항제, TNF 길항제, IL-1 길항제, 인터루킨, IL-<strong>12</strong>, IL-2, IL-<br />
<strong>12</strong>R 길항제, 독소 접합된 단일클론 항체, 종양 항원 특이적 단일클론 항체, Erbitux, Avastin,<br />
Pertuzumab, 항-CD20 항체, Rituxan<br />
, 오크렐리주맙, 오파투무맙, DXL625, Herceptin<br />
, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 175<br />
청구항 173에 있어서, 항-응고제는 아브식시맙(ReoPro), 아세노쿠마롤, 항트롬빈 III, 아르가트로반, 아스피<br />
린, 비발리루딘(Angiomax), 클로피도그렐, 다비가트란, 다비가트란 이텍실레이트(Pradaxa/Pradax), 데시<br />
루딘(Revasc/Iprivask), 디피리다몰, 엡티피바티드(Integrilin), 폰다파리눅스, 헤파린, 히루딘, 이드라<br />
파리눅스, 레피루딘(Refludan), 저분자량 헤파린, 멜라가트란, 페닌디온, 펜프로코우몬, 티클로피딘, 티로피<br />
반(Aggrastat), 와파린, 지멜라가트란, 지멜라가트란(Exanta/ Exarta), 또는 이들의 임의의 조합을 포함<br />
하는 것을 특징으로 하는 치료 조성물.<br />
청구항 176<br />
청구항 173에 있어서, 스타틴은 아토르바스타틴, 체리바스타틴, 플루바스타틴, 로바스타틴, 메바스타틴, 피타바<br />
스타틴, 프라바스타틴, 로수바스타틴, 심바스타틴, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 치<br />
료 조성물.<br />
청구항 177<br />
청구항 173에 있어서, 다른 치료제는 종양 괴사 인자-알파, 인터페론 감마, 인터루킨 1 알파, 인터루킨 1 베타,<br />
인터루킨 6, 단백분해 유도 인자, 백혈병-저해 인자, 또는 이들의 임의의 조합을 포함하는 인자의 길항제인 것<br />
을 특징으로 하는 치료 조성물.<br />
청구항 178<br />
청구항 173에 있어서, 항-악액질제는 칸나비스, 드로나비놀(Marinol), 나빌론(Cesamet), 칸나비디올, 칸나비<br />
크로멘, 테트라히드로칸나비놀, 사티벡스, 메게스트롤 아세테이트, 또는 이들의 임의의 조합을 포함하는 것을<br />
특징으로 하는 치료 조성물.<br />
청구항 179<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 173에 있어서, 항-메스꺼움제 또는 항-구토제는 5-HT3 수용체 길항제, 아쥬와인, 알리자프리드, 항콜린<br />
- 28 -
약, 항히스타민제, 아프레피탄트, 벤조디아제핀, 칸나비크로멘, 칸나비디올, 칸나비노이드, 칸나비스, 카소피탄<br />
트, 클로르프로마진, 시클리진, 덱사메타손, 덱사메타손, 디멘하이드리네이트(Gravol), 디펜히드라민, 돌라세<br />
트론, 돔페리돈, 도파민 길항제, 독실라민, 드로나비놀(Marinol), 드로페리돌, 에메트롤, 생강(ginger), 그라<br />
니세트론, 할로페리돌, 히드록사진, 히오신, 로라제팜, 메클리진, 메토클로프라미드, 미다졸람, 무시몰, 나빌론<br />
(Cesamet), nk1 수용체 길항제, 온단세트론, 팔로노세트론, 페퍼민트, 페너간, 프로클로르페라진, Promacot, 프<br />
로메타진, 펜타진, 프로포폴, 사티벡스, 테트라히드로칸나비놀, 트리메토벤자미드, 트로피세트론, 난드롤론, 스<br />
틸베스트롤, 탈리도미드, 레날리도미드, 그렐린 효능제, 미오스타틴 길항제, 항-미오스타틴 항체, 선택성 안드<br />
로겐 수용체 조절제, 선택성 에스트로겐 수용체 조절제, 앤지오텐신 AII 길항제, 베타 2 아드레날린성 수용체<br />
효능제, 베타 3 아드레날린성 수용체 효능제, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 치료 조<br />
성물.<br />
청구항 180<br />
청구항 173에 있어서, 다른 치료제는 타목시펜, BCL-2 길항제, 에스트로겐, 비스포스포네이트, 테리파라티드,<br />
스트론튬 라넬레이트, 나트륨 알렌드로네이트(Fosamax), 리세드로네이트(Actonel), 랄록시펜, 이반드로네이트<br />
(Boniva), 오바토클락스, ABT-263, 고시폴, 제피티닙, 상기 성장 인자 수용체 티로신 키나아제 저해제, 에를로<br />
티닙, 상피 성장 인자 수용체 저해제, 프소랄렌, 트리옥시살렌, 메톡살렌, 베르갑텐, 레티노이드, 에트레티네이<br />
트, 아시트레틴, 인플릭시맙(Remicade<br />
공개특허 10-2011-01<strong>12</strong>308<br />
), 아달리무맙, 인플릭시맙, 에타네르셉트, Zenapax, 시클로스포린, 메토트렉세이트, 과립구-집락 자극 인자,<br />
필그라스팀, 레노그라스팀, 뉴포젠, 뉴라스타, 2-아릴프로피온산, 아세클로페낙, 아세메타신, 아세틸살리실산<br />
(아스피린), 알클로페낙, 알미노프로펜, 아목시프린, 암피론, 아릴알카노산, 아자프로파존, 베노릴레이트, 베녹<br />
사프로펜, 브롬페낙, 카르프로펜, 셀레콕시브, 콜린 마그네슘 살리실레이트, 클로페존, COX-2 저해제, 덱시부프<br />
로펜, 덱스케토프로펜, 디클로페낙, 디플루니살, 드록시캄, 에텐자미드, 에토돌락, 에토리콕시브, 파이슬라민,<br />
페남산, 펜부펜, 페노프로펜, 플루페남산, 플루녹사프로펜, 플루비프로펜, 이부프로펜, 이부프록삼,<br />
인도메타신, 인도프로펜, 케부존, 케토프로펜, 케토롤락, 로르녹시캄, 록소프로펜, 루미라콕시브, 마그네슘 살<br />
리실레이트, 메클로페남산, 메페남산, 멜록시캄, 메타미졸, 메틸 살리실레이트, 모페부타존, 나부메톤, 나프록<br />
센, N-아릴안트라닐산, 옥사메타신, 옥사프로진, 옥시캄, 옥시펜부타존, 파레콕시브, 페나존, 페닐부타존, 페닐<br />
부타존, 피록시캄, 피르프로펜, 프로펜, 프로글루메타신, 피라졸리딘 유도체, 로페콕시브, 살리실<br />
살리실레이트, 살리실아미드, 살리실레이트, 설핀피라존, 설린닥, 수프로펜, 테녹시캄, 티아프로펜산,<br />
톨페남산, 톨메틴, 발데콕시브, 아미카신, 아미노글리코시드, 아목실린, 암피실린, 안사마이신, 아르스페나민,<br />
아지트로마이신, 아즐로실린, 아즈트레오남, 바시트라신, 카르바세펨, 카르바페넴, 카르베니실린, 세파클로르,<br />
세파드록실, 세팔렉신, 세팔로틴, 세팔로틴, 세파만돌, 세파졸린, 세프디니르, 세프디토렌, 세페핌, 세픽심, 세<br />
포페라존, 세포탁심, 세폭시틴, 세프포독심, 세프프로질, 세프타지딤, 세프티부텐, 세프티족심, 세프토비프롤,<br />
세프트리악손, 세푸록심, 세팔로스포린, 클로람페니콜, 실라스타틴, 시프로플록사신, 클라리트로마이신, 클린다<br />
마이신, 클록사실린, 콜리스틴, 코-트리목사졸, 달포프리스틴, 데메클로사이클린, 디클록사실린, 디리트로마이<br />
신, 도리페넴, 독시사이클린, 에녹사신, 에르타페넴, 에리트로마이신, 에탐부톨, 플루클록사실린,<br />
포스포마이신, 푸라졸리돈, 퓨시드산, 가티플록사신, 겔다나마이신, 젠타마이신, 글리코펩티드, 헤르비마이신,<br />
이미페넴, 이소니아지드, 카나마이신, 레보플록사신, 린코마이신, 리네졸리드, 로메플록사신, 로라카르베프, 마<br />
크롤리드, 마페니드, 메로페넴, 메티실린, 메트로니다졸, 메즐로실린, 미노사이클린, 모노박탐, 목시플록사신,<br />
무피로신, 나프실린, 네오마이신, 네틸마이신, 니트로푸란토인, 노르플록사신, 오플록사신, 옥사실린, 옥시테트<br />
라사이클린, 파로모마이신, 페니실린, 페니실린, 피페라실린, 플라텐시마이신, 폴리믹신 B, 폴리펩티드, 프론토<br />
실, 피라진아미드, 퀴놀론, 퀴누프리스틴, 리팜피신, 리팜핀, 록시트로마이신, 스펙티노마이신,<br />
스트렙토마이신, 설파세타미드, 설파메티졸, 설파닐아미드, 설파살라진, 설피속사졸, 설폰아미드,<br />
테이코플라닌, 텔리트로마이신, 테트라사이클린, 테트라사이클린, 티카르실린, 티니다졸, 토브라마이신, 트리메<br />
토프림, 트리메토프림-설파메톡사졸, 트롤레안도마이신, 트로바플록사신, 반코마이신, 알도스테론, 베클로메타<br />
손, 베타메타손, 코르티코스테로이드, 코르티솔, 코르티손 아세테이트, 데옥시코르티코스테론 아세테이트, 덱사<br />
메타손, 플루드로코르티손 아세테이트, 글루코코르티코이드, 하이드로코르티손, 메틸프레드니솔론, 프레드니솔<br />
론, 프레드니손, 스테로이드, 트리암시놀론, 아바카비르, 아시클로비르, 아시클로비르, 아데포비르, 아만타딘,<br />
암프레나비르, 항레트로바이러스 고정 용량 복합제, 항레트로바이러스 상승작용 강화제, 아르비돌, 아타자나비<br />
르, 아트리플라, 브리부딘, 시도포비르, 콤비비르, 다루나비르, 델라비르딘, 디다노신, 도코사놀, 에독수딘, 에<br />
파비렌즈, 엠트리시타빈, 엔푸비르티드, 엔테카비르, 침입 저해제, 팜시클로비르, 포미비르센, 포삼프레나비르,<br />
- 29 -
포스카르네트, 포스포네트, 융합 저해제, 간시클로비르, 가르다실, 이바시타빈, 이독수리딘, 이미퀴모드, 이무<br />
노비르, 인디나비르, 이노신, 인테그라아제 저해제, 인터페론, I형 인터페론, II형 인터페론, III형 인터페론,<br />
라미부딘, 로피나비르, 로비리드, 마라비록, MK-0518, 모록시딘, 넬피나비르, 네비라핀, 넥사비르, 뉴클레오시<br />
드 유사체, 오셀타미비르, 펜시클로비르, 페라미비르, 플레코나릴, 포도필로독소, 프로테아제 저해제, 역전사효<br />
소 저해제, 리바비린, 리만타딘, 리토나비르, 사퀴나비르, 스타부딘, 테노포비르, 테노포비르, 디소프록실, 티<br />
프라나비르, 트리플루리딘, 트리지비르, 트로만타딘, 트루바다, 발라시클로비르, 발간시클로비르, 비크리비록,<br />
비다라빈, 비라미딘, 잘시타빈, 자나미비르, 지도부딘, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하<br />
는 치료 조성물.<br />
청구항 181<br />
청구항 173에 있어서, 세포독성제, 화학요법제, 또는 면역억제제는 1-데히드로테스토스테론, 1-메틸니트로소우<br />
레아, 5-플루오로우라실, 6-메르캅토퓨린, 6-메르캅토퓨린, 6-티오구아닌, 아바타셉트, 아브락산, 아시트레틴,<br />
아클라루비신, 악티늄-225( 225<br />
Ac), 악티노마이신, 아달리무맙, 아데노신 디아미나아제 저해제, 아펠리모맙, 아플<br />
리베르셉트, 아푸투주맙, 알레파셉트, 알리트레티노인, 알킬 설포네이트, 알킬화제, 알트레타민, 알보시딥, 아<br />
미노레불린산/메틸 아미노레불리네이트, 아미노프테린, 아미노프테린, 암루비신, 암사크린, 암사크린, 아나그렐<br />
리드, 아나킨라, 안트라센디온, 안트라사이클린, 안트라사이클린, 안트라사이클린, 안트라마이신(AMC); 항유사<br />
분열제, 항생제, 항-CD20 항체, 항엽산염, 항-림프구 글로불린, 대사길항물질, 항-흉선세포 글로불린, 삼산화비<br />
소, 아셀리주맙, 아스파라기나아제, 아스파라긴 고갈제, 아스타틴-211( 211<br />
At), 아틀리주맙, 아토롤리무맙, 아트<br />
라센탄, Avastin, 아자시티딘, 아자티오프린, 아젤라스틴, 아지리딘, 바실릭시맙, BAYX 항체, 벨라타셉트, 벨<br />
리무맙, 벨로테칸, 벤다무스틴, 베르틸리무맙, 벡사로텐, 비산트렌, 비스무스-213( 213<br />
Bi), 비스무스-2<strong>12</strong>( 2<strong>12</strong><br />
Bi),<br />
블레오마이신, 블레오마이신, 블레오마이신, BLyS 항체, 보르테조밉, 부설판, 부설판, 칼시뉴린 저해제, 칼리키<br />
아마이신, 캄토테신, 캄토테신, 카페시타빈, 카르보플라틴(파라플라틴), 카르보쿠온, 카르미노마이신, 카르모푸<br />
르, 카르무스틴, 카르무스틴(BSNU), CAT 항체, CD11a 항체, CD147/Basigin 항체, CD154 항체, CD18 항체, CD20<br />
항체, CD23 항체, CD3 항체, CD4 항체, CD40 항체, CD62L/L-셀렉틴 항체, CD80 항체, CDK 저해제, 세델리주맙,<br />
셀레콕시브, 세톨리주맙 페골, 클로람부실, 클로람부실, 시클로스포린, 시스-디클로로디아민 백금(II)(DDP) 시<br />
스플라틴, 클라드리빈, 클레놀릭시맙, 클로파라빈, 콜히친, 보체 성분 5 항체, 구리-67( 67<br />
Cu), 코르티코스테로이<br />
드, CTLA-4 항체, CTLA-4 융합 단백질, 시클로필린 저해제, 시클로포스파미드, 시클로토스파미드, 시타라빈, 시<br />
타라빈, 시토칼라신 B, 세포독성 리보뉴클레아제, 다카르바진, 다클리주맙, 닥티노마이신, 닥티노마이신(악티노<br />
마이신 D), 다우노루비신, 다우노루비신, 다우노루비신(구명칭: 다우노마이신), 데시타빈, 데포롤리무스, 디메<br />
콜린, 데토루비신, 디브로모만니톨, 디에틸카르바마진, 디히드로폴레이트 환원효소 저해제, 디히드록시 안트라<br />
신 디온, 디프테리아 독소, DNA 중합효소 저해제, 도세탁셀, 도를리모맙 아리톡스, 도를릭시주맙, 독소루비신<br />
(아드리아마이신), DXL625, 에쿨리주맙, 에팔리주맙, 에파프록시랄, EGFR 길항제, 엘레스클로몰, 엘사미트루신,<br />
엘실리모맙, 에메틴, 엔도텔린 수용체 길항제, 에피포도필로톡신, 에피루비신, 에포틸론, Erbitux, 에를리주<br />
맙, 에스트라무스틴, 에타네르셉트, 에티듐 브롬화물, 에토글루시드, 에토포시드, 에토포시드 인산염, 에베롤리<br />
무스, 파랄리모맙, 파르네실트랜스퍼라아제 저해제, FKBP 저해제, 플록수리딘, 플루다라빈, 플루오로우라실, 폰<br />
톨리주맙, 포테무스틴, 갈릭시맙, 갈륨-67( 67<br />
Ga), 간테네루맙, 가빌리모맙, 젬시타빈, 글루코코르티코이드, 골리<br />
무맙, 고밀릭시맙, 그라미시딘 D, 구스페리무스, Herceptin<br />
공개특허 10-2011-01<strong>12</strong>308<br />
, 히드라진, 히드록시우레아, 메틸화억제제(hypomethylating agent), 이다루비신, 이다루비신, 이포스파미드,<br />
IL-1 길항제, IL-1 수용체 길항제, IL-<strong>12</strong>, IL-<strong>12</strong> 항체, IL-<strong>12</strong>R 길항제, IL-13 항체, IL-2, IL-2 저해제, IL-2<br />
수용체/CD25 항체, IL-6 항체, 이마티닙 메실레이트, 면역글로불린 E 항체, IMP 탈수소효소 저해제,<br />
인플릭시맙, 이놀리모맙, 인테그린 항체, 인터페론 항체, 인터페론, 인터루킨 5 항체, 인터루킨-6 수용체 항체,<br />
인터루킨, 요오드-<strong>12</strong>5( <strong>12</strong>5<br />
I), 요오드-131( 131<br />
I), 이필리무맙, 이리노테칸, 익사베필론, 켈릭시맙, 라로탁셀, 납-<br />
2<strong>12</strong>( 2<strong>12</strong><br />
Pb), 레브릴리주맙, 레플루노미드, 레날리도미드, 레르델리무맙, 류코보린, LFA-1 항체, 리도카인, 리폭<br />
시게나아제 저해제, 로무스틴(CCNU), 로니다민, 루칸톤, 루밀릭시맙, 루테튬-177( 177<br />
Lu), 마크롤리드, 만노설판,<br />
마실리모맙, 마소프로콜, 메클로레타민, 멜팔란, 메폴리주맙, 메르캅토퓨린, 메텔리무맙, 메토트렉세이트, 미세<br />
소관 조립 저해제, 미세소관 안정성 강화제, 미트라마이신, 미토브로니톨, 미토구아존, 미토마이신, 미토마이신<br />
C, 미토탄, 미톡산트론, 모롤리무맙, mTOR 저해제, 무로모납-CD3, 무스틴, 미코페놀산, 미토탄(O,P'-(DDD)), 나<br />
- 30 -
탈리주맙, 네다플라틴, 네렐리모맙, 니무스틴, 질소 머스타드, 니트로소우레아, 노르디히드로구아이아레틱산<br />
(nordihydroguaiaretic acid), 오블리메르센, 오크렐리주맙, 오크렐리주맙, 오둘리모맙, 오파투무맙, 올라파립,<br />
오말리주맙, 오르타탁셀, 오텔릭시주맙, 옥살리플라틴, 옥살리플라틴, 파클리탁셀(탁솔), 파스콜리주맙, PDGF<br />
길항제, 페가스파가제, 페메트렉세드, 펜토스타틴, 페르투주맙, 펙셀리주맙, 포스포디에스테라아제 저해제, 인-<br />
32( 32<br />
P), 피메크롤리무스 아베티무스, 피라루비신, 픽산트론, 플라틴, 플리카마이신, 폴리 ADP 리보오스 중합효<br />
소 저해제, 포르피머 나트륨, 포르피린 유도체, 프레드니무스틴, 프로카인, 프로카르바진, 프로카르바진, 프로<br />
프라놀롤, 프로테아좀 저해제, 슈도모나스(Pseudomonas) 외독소, 슈도모나스(Pseudomonas) 독소, 퓨린 합성 저<br />
해제, 퓨로마이신, 피리미딘 합성 저해제, 방사성핵종, 방사선요법, 랄티트렉세드, 라니무스틴, 레슬리주맙, 레<br />
티노이드 X 수용체 효능제, 레티노이드, 레늄-186( 186<br />
Re), 레늄-188( 188<br />
Re), 리보뉴클레오티드 환원효소 저해제,<br />
리신, 릴로나셉트, Rituxan<br />
, 로벨리주맙, 루비테칸, 루플리주맙, 사마륨-153( 153<br />
Sm), 사트라플라틴, 스칸듐-47( 47<br />
Sc), 선택성 안드로겐 수용<br />
체 조절제, 선택성 에스트로겐 수용체 조절제, 셀리시클립, 세무스틴, 성 호르몬 길항제, 시플리주맙, 시롤리무<br />
스, 스테로이드 아로마타아제 저해제, 스테로이드, 스트렙토조신, 스트렙토조토신, 타크롤리무스, 탈라포르핀,<br />
탈리주맙, 탁산, 탁솔, 테가푸르, 텔리모맙 아리톡스, 테모포르핀, 테모졸로미드, 템시롤리무스, 템시롤리무스,<br />
테넬릭시맙, 테니포시드, 테플리주맙, 테리플루노미드, 테세탁셀, 테스톨락톤, 테트라카인, 탈리도미드, 티오에<br />
파 클로람부실, 티오퓨린 티오구아닌, 티오TEPA, 티미딜레이트 신타아제 저해제, 티아조푸린, 티피파르닙, T-림<br />
프구 항체, TNF 길항제, TNF 항체, TNF 융합 단백질, TNF 수용체 융합 단백질, TNF-알파 저해제, 토클리주맙,<br />
토포이소머라제 저해제, 토포테칸, 토랄리주맙, 트라벡테딘, 트레멜리무맙, 트레오설판, 트레티노인, 트리아젠,<br />
트리아지쿠온, 트리에틸렌멜라민, 트리플라틴 테트라니트레이트, 트로포스파미드, 종양 항원 특이적 단일클론<br />
항체, 티로신 키나아제 저해제, 우라무스틴, 우스테키누맙, 발루비신, 발루비신, 바팔릭시맙, VEGF 길항제, 베<br />
팔리모맙, 베르테포르핀, 빈블라스틴, 빈카 알칼로이드, 빈크리스틴, 빈데신, 빈플루닌, 비노렐빈, 비실리주맙,<br />
보리노스타트, 이트튬-88( 88<br />
Y), 이트튬-90( 90<br />
Y), 자놀리무맙, 질류톤, 지랄리무맙, 졸리모맙 아리톡스,<br />
조루비신, 조타롤리무스, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 182<br />
청구항 173에 있어서, 다른 활성제는 TNF-알파, IL-2, IL-4, IL-6, IL-10, IL-<strong>12</strong>, IL-13, IL-18, IFN-알파,<br />
IFN-감마, BAFF, CXCL13, IP-10, VEGF, EPO, EGF, HRG, 간세포 성장 인자(HGF), 헵시딘, 또는 이들의 임의의<br />
조합을 포함하는 인자의 하나 이상의 효능제, 길항제, 또는 조절제인 것을 특징으로 하는 치료 조성물.<br />
청구항 183<br />
청구항 173에 있어서, IL-6 길항제는 항-IL-6 항체 또는 이의 단편, 안티센스 핵산, 폴리펩티드, 소분자, 또는<br />
이들의 임의의 조합을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 184<br />
청구항 183에 있어서, 안티센스 핵산은 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1, JAK2, JAK3,<br />
또는 SYK를 인코딩하는 서열의 적어도 대략 10개의 뉴클레오티드를 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 185<br />
청구항 183에 있어서, 안티센스 핵산은 DNA, RNA, 펩티드 핵산, 잠금 핵산, 모르폴리노(포스포로디아미데이트<br />
모르폴리노 올리고), 글리세롤 핵산, 트레오제 핵산, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는<br />
치료 조성물.<br />
청구항 186<br />
청구항 183에 있어서, 항-IL-6 항체 또는 이의 단편은 Ab1, Ab2, Ab3, Ab4, Ab5, Ab6, Ab7, Ab8, Ab9, Ab10,<br />
Ab11, Ab<strong>12</strong>, Ab13, Ab14, Ab15, Ab16, Ab17, Ab18, Ab<strong>19</strong>, Ab20, Ab21, Ab22, Ab23, Ab24, Ab25, Ab26, Ab27,<br />
Ab28, Ab29, Ab30, Ab31, Ab32, Ab33, Ab34, Ab35, Ab36, 이들 중에서 한 가지의 IL-6 결합 단편, 이들 중에서<br />
한 가지의 변이체, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 치료 조성물.<br />
- 31 -<br />
공개특허 10-2011-01<strong>12</strong>308
청구항 187<br />
청구항 183에 있어서, IL-6 길항제 폴리펩티드는 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1,<br />
JAK2, JAK3, 그리고 SYK로 구성된 군에서 선택되는 서열을 갖는 폴리펩티드의 단편을 포함하는 것을 특징으로<br />
하는 치료 조성물.<br />
청구항 188<br />
청구항 187에 있어서, 단편은 적어도 40개 아미노산 길이를 갖는 것을 특징으로 하는 치료 조성물.<br />
청구항 189<br />
청구항 183에 있어서, IL-6 길항제는 가용성 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1, JAK2,<br />
JAK3, SYK, 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 <strong>19</strong>0<br />
청구항 173에 있어서, IL-6 길항제는 반감기 증가 모이어티에 결합되는 것을 특징으로 하는 치료 조성물.<br />
청구항 <strong>19</strong>1<br />
청구항 170 내지 <strong>19</strong>0중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 하나 이상의 다른 치료제에 직접적으<br />
로 또는 간접적으로 결합되는 것을 특징으로 하는 치료 조성물.<br />
청구항 <strong>19</strong>2<br />
청구항 140 내지 167중 어느 한 항에 있어서, Ab1 항체 또는 항체 단편은 검출가능 라벨에 직접적으로 또는 간<br />
접적으로 결합되는 것을 특징으로 하는 치료 조성물.<br />
청구항 <strong>19</strong>3<br />
청구항 <strong>19</strong>2에 있어서, 검출가능 라벨은 형광 염료, 생물발광 물질, 방사성 물질, 화학발광 모이어티, 스트렙타<br />
비딘, 아비딘, 비오틴, 방사성 물질, 효소, 기질, 양고추냉이 과산화효소, 아세틸콜린에스테라아제, 알칼리성<br />
포스파타아제, 베타-갈락토시다아제, 루시페라아제, 로다민, 플루오레세인, 플루오레세인 이소티오시아네이트,<br />
움벨리페론, 디클로로트리아지닐아민, 피코에리트린, 염화단실, 루미놀, 루시페린, 에쿼린, 요오드 <strong>12</strong>5( <strong>12</strong>5<br />
I),<br />
탄소 14( 14<br />
C), 황 35( 35<br />
S), 트리튬( 3<br />
H), 32( 32<br />
P), 또는 이들의 임의의 조합을 포함하는 것을 특징으로 하는 치료<br />
조성물.<br />
청구항 <strong>19</strong>4<br />
청구항 140 내지 <strong>19</strong>3중 어느 한 항에 있어서, Ab1 항체는 Ab1 항체를 인코딩하는 하나 이상의 핵산 형태로 개체<br />
에 투여되는 것을 특징으로 하는 치료 조성물.<br />
청구항 <strong>19</strong>5<br />
청구항 <strong>19</strong>4에 있어서, 하나 이상의 핵산은 바이러스, 리포좀, 양이온성 지질 복합체, 양이온성 중합체 복합체,<br />
또는 나노입자 복합체로서 수용자 내로 도입되는 것을 특징으로 하는 치료 조성물.<br />
청구항 <strong>19</strong>6<br />
청구항 <strong>19</strong>4에 있어서, 하나 이상의 핵산은 효모 또는 인간 선호 코돈으로 구성되는 것을 특징으로 하는 치료 조<br />
성물.<br />
청구항 <strong>19</strong>7<br />
청구항 <strong>19</strong>4에 있어서, 하나 이상의 핵산은 벡터 내에 포함되는 것을 특징으로 하는 치료 조성물.<br />
청구항 <strong>19</strong>8<br />
공개특허 10-2011-01<strong>12</strong>308<br />
청구항 <strong>19</strong>4에 있어서, 벡터는 플라스미드 또는 재조합 바이러스 벡터인 것을 특징으로 하는 치료 조성물.<br />
- 32 -
[0001]<br />
[0002]<br />
[0003]<br />
[0004]<br />
[0005]<br />
[0006]<br />
청구항 <strong>19</strong>9<br />
청구항 <strong>19</strong>4에 있어서, 하나 이상의 핵산은 서열 번호: 723과 서열 번호: 700; 서열 번호: 701과 서열 번호:<br />
703; 서열 번호: 705와 서열 번호: 707; 서열 번호: 720과 서열 번호: 724; 그리고 서열 번호: 10과 서열 번호:<br />
11의 중쇄와 경쇄 폴리뉴클레오티드 서열을 포함하는 것을 특징으로 하는 치료 조성물.<br />
청구항 200<br />
청구항 140 내지 <strong>19</strong>3중 어느 한 항에 있어서, Ab1 항체는<br />
(a) 서열 번호: 709와 서열 번호: 657; 서열 번호: 702와 서열 번호: 704; 서열 번호: 706과 서열 번호: 708;<br />
서열 번호: 20과 서열 번호: <strong>19</strong>; 또는 서열 번호: 2와 서열 번호: 3을 포함하는 경쇄와 중쇄 폴리펩티드;<br />
(b) (a)의 임의의 폴리펩티드에 적어도 80%, 85%, 90%, 95%, 96%, 97%, 98%, 또는 99% 동일성을 갖는 폴리펩티<br />
드;<br />
(c) 중간으로 또는 고도로 엄밀한 하이브리드화 조건 하에, 서열 번호: 723과 서열 번호: 700; 서열 번호: 701<br />
과 서열 번호: 703; 서열 번호: 705와 서열 번호: 707; 서열 번호: 720과 서열 번호: 724; 그리고 서열 번호:<br />
10과 서열 번호: 11의 임의의 중쇄와 경쇄 폴리뉴클레오티드 서열에 하이브리드화되는 폴리뉴클레오티드;<br />
(d) 서열 번호: 723과 서열 번호: 700; 서열 번호: 701과 서열 번호: 703; 서열 번호: 705와 서열 번호: 707;<br />
서열 번호: 720과 서열 번호: 724; 그리고 서열 번호: 10과 서열 번호: 11의 임의의 중쇄와 경쇄 폴리뉴클레오<br />
티드 서열에 적어도 80%, 85%, 90%, 95%, 96%, 97%, 98%, 또는 99% 동일성을 갖는 폴리뉴클레오티드;<br />
(e) (c) 또는 (d)의 임의의 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드를 포함하는 것을 특징으로 하는 치<br />
료 조성물.<br />
명 세 서<br />
기 술 분 야<br />
관련 출원에 대한 교차 참조<br />
본 출원은 2008년 11월 25일자로 제출된 미국 가출원 No. 61/117,839, 61/117,861, 그리고 61/117,811에 우선<br />
권을 주장하며; 그리고 본 출원은 2009년 7월 14일자로 제출된 미국 출원 <strong>12</strong>/502,581, 2009년 3월 6일자로 제출<br />
된 US Serial No. <strong>12</strong>/399,156, 2009년 2월 24일자로 제출된 US Serial No. <strong>12</strong>/391,717, 그리고 2009년 2월 5일<br />
자로 제출된 US Serial No. <strong>12</strong>/366,567의 일부 연속 출원이며, 이들 각각의 내용은 본 발명에 그 전체가 참조로<br />
서 편입된다.<br />
2009년 11월 24일자에 만들어진 332,081 바이트 크기의 "67858o706002.txt"파일의 서열 목록은 본 발명에 그<br />
전체가 참조로서 편입된다.<br />
발명의 분야<br />
본 발명은 신규한 항-IL-6 항체, 신규한 치료법, 항-IL-6 항체를 이용한 치료 프로토콜, 그리고 항-IL-6 항체를<br />
포함하는 제약학적 제제에 관련하여, 상기 언급된 특허 출원에서 개시된 출원인의 기존 발명의 연장이다. 바람<br />
직한 구체예에서, 항-IL-6 항체는 Ab1이고, 이는 토끼 또는 이의 인간화된 형태, 그리고 이의 중쇄, 경쇄,<br />
단편, 변이체, 그리고 CDR, 또는 완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는, Ab1과 동일한 선<br />
형 또는 입체형태적 에피토프에 특이적으로 결합하는 항체 또는 항체 단편을 포함한다. 본 출원은 특히, 본 명<br />
세서에서 Ab1 및 이의 변이체로 지칭되는 예시적인 인간화된 항체의 바람직한 제제와 치료 용도에 관계한다. 바<br />
람직한 구체예에서, 이러한 항-IL-6 항체는 적어도 대략 25일의 생체내 반감기, 알부민을 증가시키는 생체내 효<br />
과, C-반응성 단백질을 낮추는 생체내 효과, 정상적인 혈액응고 프로필을 복원하는 생체내 효과, 대략 50 피코<br />
몰(picomolar) 미만의 IL-6에 대한 결합 친화성(Kd), 및/또는 10 -4<br />
갖는다.<br />
S -1<br />
공개특허 10-2011-01<strong>12</strong>308<br />
이하의 IL-6으로부터 해리 속도(Koff)를<br />
본 발명은 또한, IL-6과 연관된 질환 또는 이상을 스크리닝하는 방법, 그리고 상기 항체, 또는 이의 단편 또는<br />
- 33 -
[0007]<br />
[0008]<br />
[0009]<br />
[0010]<br />
[0011]<br />
[00<strong>12</strong>]<br />
[0013]<br />
[0014]<br />
변이체를 투여함으로써 IL-6과 연관된 질환 또는 이상을 예방하거나 치료하는 방법에 관계한다.<br />
한 측면에서, 본 발명은 병든 환자의 생존력 또는 삶의 질을 개선하는 방법에 관계하고, 상기 방법은 환자에게<br />
항-IL-6 항체, 예를 들면, Ab1 또는 이의 항체 단편 또는 변이체를 투여하는 단계, 여기서 환자의 C-반응성 단<br />
백질("CRP") 수준이 낮아지고 및/또는 환자의 알부민 수준이 상승되며, 그리고 선택적으로, 환자의 CRP 및/또는<br />
알부민 수준을 결정하기 위하여 환자를 모니터하는 단계를 포함한다.<br />
다른 측면에서, 본 발명은 병든 환자에서 C-반응성 단백질 수준을 낮추는 방법에 관계하고, 상기 방법은 환자에<br />
게 IL-6 길항제, 예를 들면, Ab1을 투여하는 단계, 여기서 환자의 CRP 수준이 낮아지고, 그리고 환자를 모니터<br />
하여 CRP 수준을 평가하는 단계를 포함한다. 다른 측면에서, 본 발명은 병든 환자에서 알부민 수준을 상승시키<br />
는 방법에 관계하고, 상기 방법은 환자에게 IL-6 길항제, 예를 들면, Ab1을 투여하는 단계, 여기서 환자의 혈청<br />
알부민 수준이 높아지고, 그리고 환자를 모니터하여 알부민 수준을 평가하는 단계를 포함한다.<br />
다른 측면에서, 본 발명은 병든 환자, 예를 들면 상승된 CRP 수준을 보이는 환자에서 악액질, 쇠약, 피로 및/또<br />
는 발열을 예방하거나 치료하는 방법에 관계하고, 상기 방법은 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체<br />
를 환자에게 투여하는 단계, 여기서 환자의 악액질, 쇠약, 피로 및/또는 발열이 개선되거나, 또는 정상 상태로<br />
복원되고, 그리고 선택적으로, 환자를 모니터하여 악액질, 쇠약, 피로, 및/또는 발열을 평가하는 단계를 포함한<br />
다.<br />
다른 구체예에서, 본 발명은 과혈액응고 상태인 환자에서 혈전증을 예방하거나 치료하는 방법에 관계하고, 상기<br />
방법은 항-IL-6 항체, 예를 들면, Ab1 또는 이의 항체 단편 또는 변이체를 환자에 투여하는 단계, 여기서 환자<br />
의 혈액응고 프로필이 개선되거나, 또는 정상 상태로 복원되고, 그리고 선택적으로, 환자를 모니터하여 혈액응<br />
고 프로필을 평가하는 단계를 포함한다.<br />
다른 측면에서, 본 발명에서는 신규한 제약학적 조성물, 그리고 신규한 복합 요법에서 이들의 용도를 제시하고,<br />
이는 항-IL-6 항체, 예를 들면, Ab1 또는 이의 단편 또는 변이체, 그리고 적어도 한 가지 다른 치료 화합물, 예<br />
를 들면, 스타틴, 항-응고제, 항-구토제, 항-메스꺼움제, 항-악액질제, 화학요법제, 항-사이토킨제 등의 투여를<br />
포함한다.<br />
배 경 기 술<br />
체중 감소, 피로, 그리고 근육 쇠약은 진행된 형태의 암을 앓는 환자의 매우 공통적인 증상이고, 그리고 이들<br />
증상은 암이 계속 진행됨에 따라 악화될 수 있다. 피로, 체중 감소 및 근육 쇠약은 예로써 생활방식과 인간관계<br />
를 파괴함으로써, 그리고 암 치료를 지속하는 환자의 의지 또는 능력에 영향을 줌으로써 진행된 형태의 암을 앓<br />
는 환자의 회복에 현저한 부정적인 영향을 줄 수 있다. 피로, 체중 감소와 근육 쇠약을 해결하는 공지된 방법에<br />
는 체력과 운동의 규칙적인 일과, 환자의 활동력을 보존하는 방법, 그리고 빈혈-유도된 피로와 근육 쇠약을 해<br />
결하는 치료가 포함된다. 그럼에도 불구하고, 암 환자에서 피로, 체중 감소와 근육 쇠약을 개선하는 방법 및/또<br />
는 치료제가 당분야에서 여전히 요구된다.<br />
혈전증은 암 환자에서 사망의 주요 원인이다(Bick, N Engl J Med 349:109-111 (2003)). 가령, 심각하고 치명적<br />
인 혈전증 사건이 폐암 환자의 대략 6%에서 발생한다(Alguire et al., J Clin Oncol 2004 Vol 22 (July 15th<br />
Supplement) No. 14S: 8082). 암 환자는 종종, 과혈액응고를 나타내는데, 여기서 혈액응고 체계가 증가된 응고<br />
성향(clotting tendency)을 갖는다(Rickles and Edwards, Blood 62:14-31 (<strong>19</strong>83)). 과혈액응고의 마커는 적어<br />
도 일부 암의 경우에 불량한 환자 결과와 상관된다(Bick, Semin Thromb Hemostat 18:353-372 (<strong>19</strong>92); Buccheri<br />
et al., Cancer 97:3044-3052 (2003); Wojtukiewicz, Blood Coagul Fibrinolysis 3:429-437 (<strong>19</strong>92)). 과혈액<br />
응고의 원인에는 암 자체 및 암 치료(가령, 화학요법)가 포함된다. 과혈액응고는 혈전증 사건의 증가된 위험을<br />
유발하고, 이는 환자가 몸져누울 때 더욱 악화될 수 있다. 금기가 아닐 때, 항응고제 요법은 일부 암에서 생존<br />
이점을 제공하였다(Lebeau et al., Cancer 74:38-45 (<strong>19</strong>94); Chahinian et al., J Clin Oncol 7:993-1002<br />
(<strong>19</strong>89)). 하지만, 치료 옵션이 종종 제한되는데, 그 이유는 많은 암 환자가 대량 출혈의 상승된 위험에 처해 있<br />
고, 따라서 그렇지 않으면 혈전증의 위험을 감소시키기 위하여 예방적으로 제공될 수 있는 항응고제의 투여가<br />
배제되기 때문이다. 요약하면, 암 환자에서 혈전증의 예방에 가용한 방법이 불충분하고, 따라서 새로운 요법이<br />
요구된다. 이런 요법은 암 환자 생존을 강화시키고 더욱 나은 삶의 질을 증진할 것이다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
혈전증은 또한, 만성 질환 또는 만성 염증을 앓는 환자, 수술 환자, 몸져누운 개체, 그리고 정형외과 환자를 비<br />
롯한 다른 환자 군에서 부작용과 사망의 주요 원인일 수 있다. 달리 금기가 아닐 때, 예방적 방법은 종아리 압<br />
박(calf compression)과 항응고제(가령, 저분자량 헤파린)를 포함한다. 이들 예방적 방법은 혈전증의 위험을 감<br />
- 34 -
[0015]<br />
[0016]<br />
[0017]<br />
[0018]<br />
[00<strong>19</strong>]<br />
[0020]<br />
[0021]<br />
[0022]<br />
소시킬 수는 있지만 제거하지는 못한다. 이들 예방적 방법이 항상 효과적이지는 않고 일부 환자의 경우에 금기<br />
이며, 그리고 항응고제가 잠재적으로 치명적인 부작용, 예를 들면, 대량 출혈을 유발할 수 있기 때문에, 이들<br />
환자에서 혈전증을 예방하는 대안적 방법이 요구된다. 이들 방법은 환자 결과를 개선할 것이다.<br />
인터루킨-6(이하"IL-6")(일명 인터페론-β2; B-세포 분화 인자; B-세포 자극 인자-2; 간세포 자극 인자; 하이브<br />
리도마 성장 인자; 및 형질세포종 성장 인자)은 급성 염증 반응의 조절, B-세포 및 T-세포 분화를 비롯한 특이<br />
적 면역 반응의 조절, 골 대사, 혈소판형성, 상피 증식, 월경, 신경 세포 분화, 신경 보호, 노화, 암, 그리고<br />
알츠하이머병에서 발생되는 염증 반응과 같은 다수의 생물학적 과정에 관여하는 다기능성 사이토킨이다(참조:<br />
A. Papassotiropoulos et al, Neurobiology of Aging, 22:863-871 (2001)).<br />
IL-6은 신호-전달 당단백질 gp130 및 IL-6 수용체("IL-6R")(일명 gp80)의 적어도 하나의 소단위로 구성된 수용<br />
체 복합체를 통하여 세포 반응을 촉진시키는 사이토킨 집단의 구성원이다. IL-6R은 또한 가용성 형태("sIL-<br />
6R")로 존재할 수 있다. IL-6은 IL-6R에 결합하여, 신호-전달 수용체 gp130을 이합체화시킨다(참조: Jones, SA,<br />
J. Immunology, 175:3463-3468 (2005)).<br />
인간에서, IL-6을 인코딩하는 유전자는 5개 엑손 및 4개 인트론으로 조직되며, 7p21에서 염색체 7의 짧은 팔에<br />
맵핑(mapping)된다. IL-6 RNA의 번역 및 번역후 프로세싱은 성숙 형태에서 184개 아미노산을 포함하는 21 내지<br />
28 kDa의 단백질을 발생시킨다(참조: A. Papassotiropoulos, et al, Neurobiology of Aging, 22:863-871<br />
(2001)).<br />
본 명세서에서 더욱 상세하게 기술된 바와 같이, IL-6은 피로, 악액질, 자가면역 질환, 골격계 질환, 암, 심장<br />
질환, 비만, 당뇨병, 천식, 알츠하이머병 및 다발성 경화증이 포함되지만 이들에 국한되지 않는 다수의 질환과<br />
이상의 발생에서 중요한 역할을 하는 것으로 생각된다. 광범위한 질환과 이상에서 IL-6의 확인된 관련성으로 인<br />
하여, IL-6과 연관된 질환의 예방 또는 치료에 유용한 조성물 및 방법뿐만 아니라, IL-6과 연관된 질환 또는 이<br />
상을 갖는 환자를 확인하기 위한 스크리닝 방법이 당분야에서 여전히 요구된다. 특히 바람직한 항-IL-6 조성물<br />
은 환자에게 투여될 때 최소한의 부작용을 나타내거나, 또는 부작용을 최소화시키는 것들이다. IL-6과 연관된<br />
질환 또는 이상을 감소 또는 저해하는 조성물 또는 방법은 병든 환자에게 유익하다.<br />
IL-6의 기능은 면역 반응에 국한되지 않는데, 그 이유는 IL-6이 조혈, 혈소판형성, 파골세포 형성, C-반응성 단<br />
백질(CRP) 및 혈청 아밀로이드 A(SAA) 단백질의 상승을 유발하는 간 급성기 반응의 유도에서 작용하기<br />
때문이다. 상피 각질형성세포, 신장 혈관사이 세포, 골수종 및 형질세포종 세포에 대한 성장 인자인 것으로 알<br />
려져 있다(Grossman et al., <strong>19</strong>89 Prot Natl Acad Sci., 86, (16) 6367-6371; Horii et al., <strong>19</strong>89, J<br />
Immunol, 143, <strong>12</strong>, 3949-3955; Kawano et al., <strong>19</strong>88, Nature 332, 6159, 83-85). IL-6은 단핵세포/대식세포,<br />
섬유아세포, 상피 각질형성세포, 혈관 내피 세포, 신장 혈관사이 세포, 신경교 세포, 연골세포, T 및 B-세포 및<br />
일부 종양 세포를 비롯한 광범위한 세포 유형에 의해 생산된다(Akira et al, <strong>19</strong>90, FASEB J., 4, 11, 2860-<br />
2867). IL-6을 구성적으로 생산하는 종양 세포를 제외하고, 정상 세포들은 적절하게 자극되지 않으면, IL-6을<br />
발현하지 않는다.<br />
유방암, 백혈병, 난소암, 전립선암, 췌장암, 림프종, 폐암, 신장 세포 암종, 결장직장 암, 그리고 다발성 골수<br />
종(가령, Chopra et al., 2004, MJAFI 60:45-49; Songur et al., 2004, Tumori 90:<strong>19</strong>6-200; Blay et al.,<br />
<strong>19</strong>92, Cancer Research 52:3317-3322; Nikiteas et al., 2005, World J. Gasterenterol. 11:1639-1643;<br />
reviewed in Heikkila et al., 2008, Eur J Cancer, 44:937-945)을 비롯한 다양한 유형의 암에서 상승된 IL-6<br />
수준이 관찰되었다. 앞서 언급된 바와 같이, IL-6은 적어도 일부 유형의 암의 증식 또는 생존을 촉진시키는데<br />
역할을 하거나, 또는 하는 것으로 의심된다. 게다가, 이들 연구 중에서 일부는 IL-6 수준과 환자 결과 사이에<br />
상관관계를 증명하였다. 종합하면, 이들 결과는 IL-6의 저해가 치료요법적으로 유익할 수 있다는 가능성을 암시<br />
한다. 실제로, 임상 연구(Trikha et al., 2003, Clinical Cancer Research 9:4653-4665에서 재검토됨)에서, 특<br />
히 IL-6이 암 세포 증식 또는 생존을 촉진하는데 직접적인 역할을 하는 암에서 다양한 항-IL-6 항체의 투여에<br />
기인한 환자 결과에서 상당한 개선이 밝혀졌다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
앞서 언급된 바와 같이, IL-6은 간 급성기 반응을 촉진하여, CRP의 증가된 생산 및 상승된 혈청 CRP 수준을 초<br />
래한다. 이런 이유로, C-반응성 단백질(CRP)은 IL-6 활성의 대리 마커(surrogate marker)를 포함하는 것으로 보<br />
고되었다. 따라서 상승된 IL-6 활성은 혈청 CRP의 측정을 통하여 검출될 수 있다. 역으로, 예로써, 중화 항-IL-<br />
6 항체의 투여를 통한 IL-6 활성의 효과적인 저해는 혈청 CRP 수준의 결과적인 감소에 의해 검출될 수 있다.<br />
최근의 임상 시험에서, 상승된 CRP(2.0 ㎎/ℓ 이상)을 갖는 명백하게 건강한 개체에 로수바스타틴을 투여하면,<br />
- 35 -
[0023]<br />
[0024]<br />
[0025]<br />
[0026]<br />
[0027]<br />
[0028]<br />
이들의 CRP 수준이 37% 감소하고, 그리고 심근 경색, 발작, 동맥 재혈관화, 불안정한 협심증으로 위한 입원, 또<br />
는 심혈관 원인으로 인한 사망의 발생률이 상당히 감소하는 것으로 밝혀졌다. Ridker et al., N Engl J Med.<br />
2008 Nov 9 [Epub ahead of print].<br />
일부 암 및 다른 질환의 병인에서 IL-6의 직접적인 역할에 추가하여, 만성적으로 상승된 IL-6 수준은 환자의 행<br />
복 및 삶의 질에 부정적인 영향을 주는 것으로 보인다. 가령, 상승된 IL-6 수준은 악액질과 발열, 그리고 감소<br />
된 혈청 알부민과 연관되는 것으로 보고되었다. Gauldie et al., <strong>19</strong>87, PNAS 84:7251-7253; Heinric et al.,<br />
<strong>19</strong>90, 265:621-636; Zamir et al., <strong>19</strong>93, Metabolism 42:204-208; Zamir et al., <strong>19</strong>92, Arch Surg, <strong>12</strong>7:170-<br />
174. 중화 항체에 의한 IL-6 저해는 암 환자에서 발열 및 악액질을 개선하는 것으로 보고되었지만, 이들 환자의<br />
혈청 알부민 수준에서 개선은 보고되지 않았다(Emille et al., <strong>19</strong>94, Blood, 84:2472-2479; Blay et al.,<br />
<strong>19</strong>92, Cancer Research 52:3317-3322; Bataille et al., <strong>19</strong>95, Blood, 86: 685-691).<br />
다양한 연구에서, 암 환자에서 CRP는 가치있는 예후 인자이고, 상승된 CRP 수준이 불량한 결과를 예언하는 것으<br />
로 제시되었다(참조: Hefler et al, Clin Cancer Res, 2008 Feb 1;14(3):710-4; Nagaoka et al, Liver Int,<br />
2007 Oct;27(8):1091-7; Heikkila et al, J Epidemiol Community Health, 2007 Sep;61(9):824-33, Review;<br />
Hara et al, Anticancer Res, 2007 Jul-Aug;27(4C):3001-4; Polterauer et al, Gynecol Oncol, 2007<br />
Oct;107(1):114-7, Epub 2007 Jul 6; Tingstedt et al, Scand J Gastroenterol, 2007 Jun;42(6):754-9; Suh<br />
et al, Support Care Cancer, 2007 Jun;15(6):613-20, Epub 2007 Jan 18; Gerhardt et al, World J<br />
Gastroenterol, 2006 Sep 14;<strong>12</strong>(34):5495-500; McArdle et al, Urol Int, 2006;77(2):<strong>12</strong>7-9; Guillem et al,<br />
Dis Esophagus, 2005;18(3):146-50; Brown et al, Cancer, 2005 Jan 15;103(2):377-82). 감소된 혈청 알부민<br />
(저알부민혈증) 역시 암을 비롯한 많은 심각한 질병에서 발병률 및 치사율의 증가와 연관된다(가령, Vigano et<br />
al., Arch Intern Med, 2000 Mar 27;160(6):861-8; Hauser et al., Support Care Cancer, 2006<br />
Oct;14(10):999-1011; Seve et al., Cancer, 2006 Dec 1;107(11):2698-705). 저알부민혈증과 불량한 환자 결과<br />
사이에 명백한 연결고리는 직접적인 알부민 주입을 통하여 알부민 수준을 복원시키면 환자 생존이 촉진될 수 있<br />
음을 암시하지만, 알부민 주입 단독은 진행된 암 환자(Demirkazik et al., Proc Am Soc Clin Oncol 21: 2002<br />
(abstr 2892)) 또는 다른 치명적인 질환 환자 군(Wilkes et al., Ann Intern Med, 2001 Aug 7;135(3):149-64에<br />
서 재검토됨)의 생존을 개선시키지 못하였다.<br />
Glasgow 예후 점수(GPS)는 알부민(< 35 ㎎/ℓ = 1 점) 및 CRP(> 10 ㎎/ℓ = 1 점)의 수준을 통합하는 염증-기<br />
초된 예후 점수이다(Forrest et al., Br J Cancer, 2004 May 4;90(9):1704-6). 2004년 도입된 이후, Glasgow<br />
예후 점수는 위-식도암, 비-소세포폐암, 결장직장 암, 유방암, 난소암, 기관지 암, 그리고 전이성 신장 암을 비<br />
롯한 다수의 암에서 사망 예측인자로서 예후 가치를 갖는 것으로 이미 확인되었다(Forrest et al., Br J<br />
Cancer, 2004 May 4;90(9):1704-6; Sharma et al., Clin Colorectal Cancer, 2008 Sep;7(5):331-7; Sharma et<br />
al., Eur J Cancer, 2008 Jan;44(2):251-6; McMillan et al., Nutr Cancer, 2001;41(1-2):64-9; McMillan,<br />
Proc Nutr Soc, 2008 Aug;67(3):257-62; Ramsey et al., Cancer, 2007 Jan 15;109(2):205-<strong>12</strong>).<br />
U.S. 특허 출원 공개 번호 20080081041(항-IL-6 항체를 이용한 암 치료 관련)에서는 IL-6이 질병 활성과 연관되<br />
고, 그리고 CRP가 IL-6 활성의 대리 마커이기 때문에, 항-IL-6 항체로 IL-6을 중화시킴으로써 CRP의 지속적인<br />
억제가 생물학적 활성을 획득하는데 필수적인 것으로 간주될 수 있다고 개시한다(CNTO 328, Zaki et al., Int J<br />
Cancer, 2004 Sep 10;111(4):592-5). 동일한 특허 출원에서 양성 및 악성 전립선 질환 환자에서 IL-6과 CRP의<br />
상관관계가 McArdle(McArdle et al. 2004 Br J Cancer 91(10):1755-1757)에 의해 이미 조사되었다고 지시한다.<br />
McArdle는 전립선암 환자와 비교하여 양성 질환 환자에서 IL-6과 CRP의 농도 간에 유의적인 차이가 없다는 것을<br />
발견하였고, 암 환자에서는 종양 등급이 증가할수록 IL-6과 CRP 농도 둘 모두에 유의적인 증가가 있다고 보고하<br />
였다. 86명의 전립선암 환자에 대한 평균 혈청 CRP 값은 1.8 ㎎/ℓ이었다. 이에 근거하여, 상기 특허 출원에서<br />
발명자들은 6 ㎎/㎏의 항-IL-6 항체(CNTO 328)가 격주로 투여되는 제안된 약량 및 일정을 가정하고, 그리고 이<br />
것이 전이성 HRPC를 가진 개체에서 CRP의 지속적인 억제를 달성할 것이라고 주장한다.<br />
IL-6 신호전달은 JAK1, JAK2, 그리고 JAK3을 비롯한 세포질 티로신 키나아제의 Jak-Tyk 집단에 의해 매개된다<br />
(Murray J Immunol. 2007 Mar 1;178(5):2623-9). Sivash 등은 구강 편평 암종 세포에서 사이클로펜테논 프로스<br />
타글란딘 15d-PGJ2에 의한 IL-6-매개된 JAK 신호전달의 폐기를 보고한다(British Journal of Cancer (2004)<br />
91, 1074-1080.). 이들 결과는 JAK1, JAK2, 또는 JAK3의 저해제가 IL-6의 길항제로 이용될 수 있음을<br />
암시한다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
Ulanova 등은 비-수용체 단백질 티로신 키나아제 Syk의 저해(siRNA을 이용)가 표피 세포에 의한 IL-6 생산을 감<br />
- 36 -
[0029]<br />
[0030]<br />
[0031]<br />
[0032]<br />
[0033]<br />
[0034]<br />
[0035]<br />
소시킨다고 보고한다. Am J Physiol Lung Cell Mol Physiol. 2005 Mar;288(3):L497-507. 이들 결과는 Syk의 저<br />
해제가 IL-6의 길항제로 이용될 수 있음을 암시한다.<br />
Kedar 등은 탈리도미드(thalidomide)를 이용한 치료가 신장 세포 암종 환자의 실질적인 분획물에서 정상 또는<br />
거의 정상적인 수준으로 CRP 및 IL-6의 혈청 수준을 유의하게 감소시킨다고 보고한다. Int J Cancer. 2004 Jun<br />
10;110(2):260-5. 이들 결과는 탈리도미드, 그리고 아마도 이의 유도체, 예를 들면, 레날리도미드가 IL-6의 유<br />
용한 길항제라는 것을 암시한다.<br />
이에 더하여, 다른 공개된 특허 출원, US 20070292420은 진행된 단계 다발성 골수종을 가진 난치성 환자(N=<strong>12</strong>)<br />
를 치료하기 위하여 항-IL-6(cCLB-8) 항체를 이용한 상(phase) I 약량 상승 연구를 교시하고, 그리고 상기 연구<br />
에 의해 일부 환자가 질환 안정화를 갖는다는 것이 증명된다고 지시한다. 상기 출원은 또한, 치료 중단후, M 단<br />
백질 수준의 증가가 가속화되고, 이것이 치료 중지후 질환이 재발한다는 것을 암시한다고 보고한다. 항-IL-6<br />
cCLB-8 항체는 유리 순환 IL-6을 저해하였다.<br />
상기 출원은 또한, 이러한 항체 시험에서 독성(2명의 심하게 전처리된 환자에서 일시적인 혈소판감소증 제외)<br />
또는 알레르기 반응이 관찰되지 않고, 그리고 모든 환자에서 C-반응성 단백질(CRP)이 검출 수준 미만으로 감소<br />
한다는 것을 지시한다. 이들 항체(cCLB-8 항체)는 보고된 바에 의하면, 17.8일의 순환 반감기를 보유하고, 인간<br />
항-키메라 항체(HACA) 면역 반응이 관찰되지 않았다(van Zaanen et al. <strong>19</strong>98). 이들은 CNTO 328의 투여가<br />
혈압, 맥박, 체온, 헤모글로빈, 간 기능 및 신장 기능에 변화를 일으키지 않았다고 주장한다. 2명의 심하게 전<br />
처리된 환자에서 일시적인 혈소판감소증을 제외하고, 독성이나 알레르기 반응이 관찰되지 않았으며, 그리고 인<br />
간 항-키메라 항체(HACA) 면역 반응이 관찰되지 않았다. 이러한 연구에서 3명의 환자는 치료 동안 경색-관련 합<br />
병증이 발생하는 것으로 보고되었지만, 이들 발명자들은 항-IL-6 cCLB-8 항체와 관련 가능성이 없는 것으로 결<br />
론내렸는데, 그 이유는 감염성 합병증이 말기 단계 다발성 골수종에서 흔히 보고되고 주요 사망원인이기 때문이<br />
다. 이들은 상기 결과에 근거하여, 항-IL-6 cCLB-8 항체가 다발성 골수종 환자에서 안전하다고 결론내린다.<br />
본 명세서에 기술된 일정한 항-IL-6 항체는 또한, 아래의 공개된 특허 출원 및 공개되지 않은 특허 출원에서 개<br />
시되고, 이들은 본 출원의 양수인에 의해 공동-소유된다: 2009년 2월 24일자 제출된 U.S. 2009/0028784, WO<br />
2008/144763, U.S. Ser. No. <strong>12</strong>/391,717(Atty. Docket No. 67858.702201), 그리고 2009년 2월 5일자 제출된<br />
U.S. Ser. No. <strong>12</strong>/366,567(Atty. Docket No. 67858.702101).<br />
다른 항-IL-6 항체는 아래의 U.S. 특허 및 공개된 특허 출원에서 개시되었다: 7,482,436; 7,291,721;<br />
6,<strong>12</strong>1,423; 2008/0075726; 2007/0178098; 2007/0154481; 2006/0257407; 그리고 2006/0188502.<br />
앞서 언급된 바와 같이, 상승된 IL-6은 악액질, 쇠약, 피로, 그리고 발열의 발병에 관여한다. 피로와 연관된 질<br />
환과 이상에는 일반적인 피로, 스트레스-관련된 피로, 운동-유발된 피로, 암-관련된 피로, 염증 질환-관련된 피<br />
로와 만성 피로 증후군이 포함되지만 이들에 국한되지 않는다(참조: Esper DH, et al, The cancer cachexia<br />
syndrome: a review of metabolic and clinical manifestations, Nutr Clin Pract., 2005 Aug;20 (4):369-76;<br />
Vgontzas AN, et al, IL-6 and its circadian secretion in humans, Neuroimmunomodulation, 2005;<strong>12</strong>(3):131-<br />
40; Robson-Ansley, PJ, et al, Acute interleukin-6 administration impairs athletic performance in<br />
healthy, trained male runners, Can J Appl Physiol., 2004 Aug;29(4):411-8; Shephard RJ., Cytokine<br />
responses to physical activity, with particular reference to IL-6: sources, actions, and clinical<br />
implications, Crit Rev Immunol., 2002;22(3):165-82; Arnold, MC, et al, Using an interleukin-6<br />
challenge to evaluate neuropsychological performance in chronic fatigue syndrome, Psychol Med., 2002<br />
Aug;32(6):1075-89; Kurzrock R., The role of cytokines in cancer-related fatigue, Cancer, 2001 Sep<br />
15;92(6 Suppl):1684-8; Nishimoto N, et al, Improvement in Castleman's disease by humanized anti-<br />
interleukin-6 receptor antibody therapy, Blood, 2000 Jan 1; 95 (1):56-61; Vgontzas AN, et al,<br />
Circadian interleukin-6 secretion and quantity and depth of sleep, J Clin Endocrinol Metab., <strong>19</strong>99<br />
Aug;84(8):2603-7; 그리고 Spath-Schwalbe E, et al, Acute effects of recombinant human interleukin 6 on<br />
endocrine and central nervous sleep functions in healthy men, J Clin Endocrinol Metab., <strong>19</strong>98<br />
May;83(5):1573-9; 이들 각각의 내용은 본 발명에서 그 전체가 참조로서 편입된다).<br />
공개특허 10-2011-01<strong>12</strong>308<br />
악액질과 연관된 질환과 이상에는 암-관련된 악액질, 심장-관련된 악액질, 호흡기-관련된 악액질, 신장-관련된<br />
악액질과 연령-관련된 악액질이 포함되지만 이들에 국한되지 않는다(참조: Barton, BE., Interleukin-6 and new<br />
strategies for the treatment of cancer, hyperproliferative diseases and paraneoplastic syndromes,<br />
Expert Opin Ther Targets, 2005 Aug;9(4):737-52; Zaki MH, et al, CNTO 328, a monoclonal antibody to IL-<br />
- 37 -
[0036]<br />
[0037]<br />
[0038]<br />
[0039]<br />
6, inhibits human tumor-induced cachexia in nude mice, Int J Cancer, 2004 Sep 10;111(4):592-5; Trikha<br />
M, et al, Targeted anti-interleukin-6 monoclonal antibody therapy for cancer: a review of the<br />
rationale and clinical evidence, Clin Cancer Res., 2003 Oct 15;9(13):4653-65; Lelli G, et al,<br />
Treatment of the cancer anorexia-cachexia syndrome: a critical reappraisal, J Chemother., 2003<br />
Jun;15(3):220-5; Argiles JM, et al, Cytokines in the pathogenesis of cancer cachexia, Curr Opin Clin<br />
Nutr Metab Care, 2003 Jul;6(4):401-6; Barton BE., IL-6-like cytokines and cancer cachexia:<br />
consequences of chronic inflammation, Immunol Res., 2001;23(1):41-58; Yamashita JI, et al,<br />
Medroxyprogesterone acetate and cancer cachexia: interleukin-6 involvement, Breast Cancer,<br />
2000;7(2):130-5; Yeh SS, et al, Geriatric cachexia: the role of cytokines, Am J Clin Nutr., <strong>19</strong>99<br />
Aug;70(2):183-97; Strassmann G, et al, Inhibition of experimental cancer cachexia by anti-cytokine and<br />
anti-cytokine-receptor therapy, Cytokines Mol Ther., <strong>19</strong>95 Jun;1(2):107-13; Fujita J, et al, Anti-<br />
interleukin-6 receptor antibody prevents muscle atrophy in colon-26 adenocarcinoma-bearing mice with<br />
modulation of lysosomal and ATP-ubiquitin-dependent proteolytic pathways, Int J Cancer, <strong>19</strong>96 Nov<br />
2768(5):637-43; Tsujinaka T, et al, Interleukin 6 receptor antibody inhibits muscle atrophy and<br />
modulates proteolytic systems in interleukin 6 transgenic mice, J Clin Invest., <strong>19</strong>96 Jan l;97(l):244-<br />
9; Emilie D, et al, Administration of an anti-interleukin-6 monoclonal antibody to patients with<br />
acquired immunodeficiency syndrome and lymphoma: effect on lymphoma growth and on B clinical Symptoms,<br />
Blood, <strong>19</strong>94 Oct 1584 (8):2472-9; 그리고 Strassmann G, et al, Evidence for the involvement of<br />
interleukin 6 in experimental cancer cachexia, J Clin Invest., <strong>19</strong>92 May;89(5):1681-4; 이들 각각의 내용<br />
은 본 발명에 그 전체가 참조로서 편입된다)<br />
다른 악액질-관련된 질환은 성장 부진(faltering growth)으로 알려져 있는 성장 실패인데, 여기서 아동은 예상<br />
보다 낮은 체중 증가 속도를 보인다. 성장 실패는 전형적으로, 제3 백분위수(percentile) 미만의 체중, 또는 짧<br />
은 기간 내에 2가지 주요 성장 파라미터의 백분위 점수(percentile rank)에서 감소로서 정의된다. 성장 실패는<br />
이질적인 의학적 및 사회심리학적 원인에 기인하고, 그리고 이러한 원인은 종종, 진단되지 않는다. 최근의 한<br />
연구(총 34명의 환자)에서, 성장 실패로 진단된 환자에서 IL-6 수준에서 통계학적으로 유의한 상승이 보고되었<br />
다(Shaoul et al. J Pediatr Gastroenterol Nutr., 2003 Oct;37(4):487-91).<br />
발명의 내용<br />
해결하려는 과제<br />
발명의 요약<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명은 IL-6에 결합 특이성을 갖는 특이적 항체, 인간화 또는 키메라 또는 단일 쇄 항체, 그리고 이들의 단<br />
편과 변이체, 특히 특이적 에피토프 특이성 및/또는 기능적 특성을 갖는 항체, 그리고 이들 항체 및 다른 항-<br />
IL-6 항체를 이용한 신규한 치료법에 대한 출원인의 기존 발명의 연장이다. 본 발명의 한 구체예는 IL-6 및/또<br />
는 IL-6/IL-6R 복합체에 결합할 수 있는 특이적 인간화된 항체, 그리고 이들의 단편과 변이체를 포함한다. 이들<br />
항체는 가용성 IL-6 또는 세포 표면 발현된 IL-6에 결합할 수 있다. 또한, 이들 항체는 IL-6, IL-6/IL-6R 복합<br />
체, IL-6/IL-6R/gp130 복합체 및/또는 IL-6/IL-6R/gp130의 멀티머 중에서 한 가지 이상의 형성 또는 생물학적<br />
효과를 저해할 수 있다. 본 발명은 항-IL-6 항체, 바람직하게는 본 명세서에서 기술된 항체를 이용한 신규한 치<br />
료법 및 치료 프로토콜에 관계한다. 특히, 본 발명은 병든 환자, 예를 들면, 치료 이전에 상승된 D-이합체 및/<br />
또는 CRP 수준을 보이는 환자에서 혈전증을 예방하거나 치료하는 방법에 관계하고, 상기 방법은 IL-6 길항제,<br />
예를 들면, 항-IL-6 항체(가령, Ab1) 또는 이의 항체 단편 또는 변이체와 같은 하기에서 확인된 것들을 환자에<br />
게 투여하는 단계를 포함하고, 여기서 환자의 혈액응고 프로필이 개선되거나 정상 상태로 복원된다. 일부 구체<br />
예에서, 이들 방법은 IL-6 길항제, 예를 들면, Ab1을 돕고(상승작용하고), 따라서 혈전증을 더욱 효과적으로 치<br />
료하거나 예방할 수 있는 스타틴과 같은 다른 활성물질을 투여하는 단계를 추가로 포함할 수 있다.<br />
본 발명은 또한, 병든 환자, 예를 들면, 상승된 CRP 수준 및/또는 낮아진 알부민 수준을 보이는 환자의 생존력<br />
또는 삶의 질을 개선하는 방법에 관계하고, 상기 방법은 환자에게 아래에서 확인된 것들과 같은 IL-6 길항제,<br />
예를 들면, 항-IL-6 항체(가령, Ab1), 또는 이의 항체 단편 또는 변이체를 투여하는 단계를 포함하고, 여기서<br />
환자의 C-반응성 단백질("CRP") 수준이 낮아지고 및/또는 환자의 알부민 수준이 상승된다. 일부 구체예에서, 이<br />
들 방법은 IL-6 길항제, 예를 들면, Ab1을 돕고(상승작용하고), 따라서 환자를 더욱 효과적으로 치료할 수 있는<br />
- 38 -
[0040]<br />
[0041]<br />
[0042]<br />
[0043]<br />
[0044]<br />
[0045]<br />
[0046]<br />
[0047]<br />
[0048]<br />
스타틴과 같은 다른 활성물질을 투여하는 단계를 추가로 포함할 수 있다.<br />
본 발명의 또 다른 구체예는 토끼 및 이의 인간화된 형태를 비롯한 Ab1, 그리고 이의 중쇄, 경쇄, 단편,<br />
변이체, 그리고 CDR에 관계한다. 제시된 인간의 임상 시험 데이터에서, Ab1의 인간화된 형태가 투여되었다.<br />
바람직한 구체예에서, 이는 본 명세서에서 기술된 항체를 투여하여 달성되고, 이들 항체는 본 명세서에서 기술<br />
된 VH, VL 및 CDR 폴리펩티드의 서열, 또는 예시된 항-IL-6 항체 서열의 하나 이상의 CDR을 포함하는 인간화 또<br />
는 키메라 또는 단일 쇄 이형 및 이들을 인코딩하는 폴리뉴클레오티드를 포함한다. 바람직하게는, 이들 항체는<br />
비당화될 것이다. 본 발명의 더욱 특정한 구체예에서, 이들 항체는 gp130 활성화를 차단하고 및/또는 50 피코몰<br />
미만의 결합 친화력(Kd) 및/또는 10 -4<br />
S -1<br />
이하의 Koff 값을 보유할 것이다.<br />
본 발명의 또 다른 구체예에서, 이들 항체 및 인간화된 이형은 토끼 면역 세포(B 림프구)로부터 유래되며, 인간<br />
생식선 서열에 대한 이들의 상동성(서열 동일성)에 기초하여 선택될 수 있다. 이들 항체는 최소한의 서열 변화<br />
를 요구하거나 서열 변화를 요구하지 않고, 따라서 인간화 이후에 기능적 성질의 유지가 용이하다. 예시적인 구<br />
체예에서, 이들 인간화된 항체는 하기에 기술된 바와 같은 모(가령, 토끼) 항체에 상당히 유사한(높은 수준의<br />
서열 동일성을 갖는) 인간 골격을 포함할 것이다.<br />
본 발명의 또 다른 구체예에서, 목적 항체는 IL-6 주동된 T1165 증식 분석, IL-6 모의된 HepG2 합토글로빈 생산<br />
분석 등과 같은 기능 분석에서 이들의 활성에 기초하여 선택될 수 있다. 본 발명의 추가 구체예는 예로써, 토끼<br />
면역 세포로부터 유래된 VH, VL 및 CDR 폴리펩티드 또는 이들의 변이체 또는 단편을 포함하는 항-IL-6 항체로부<br />
터 단편 및 이들을 인코딩하는 폴리뉴클레오티드, 그리고 IL-6 및/또는 IL-6/IL-6R 복합체 또는 IL-6/IL-<br />
6R/gp130 복합체 및/또는 이들의 멀티머를 인식할 수 있는 신규한 항체 및 폴리펩티드 조성물의 생산에서 이들<br />
항체 단편 및 이들을 인코딩하는 폴리뉴클레오티드의 용도에 관계한다.<br />
본 발명은 또한, 하나 이상의 기능적 또는 검출가능 모이어티에 접합된 항-IL-6 항체 및 이들의 인간화, 키메라<br />
또는 단일 쇄 이형, 그리고 이들의 다른 결합 단편과 변이체의 접합체의 투여를 고려한다. 본 발명은 또한, 상<br />
기 인간화된 항-IL-6 또는 항-IL-6/IL-6R 복합체 항체, 그리고 이들의 결합 단편과 변이체를 만드는 방법을 고<br />
려한다. 한 구체예에서, 결합 단편에는 Fab, Fab', F(ab')2, Fv와 scFv 단편이 포함되지만 이들에 국한되지 않<br />
는다.<br />
본 발명의 구체예는 IL-6 또는 이의 이상 발현과 연관된 질환과 이상의 진단, 평가 및 치료를 위한 항-IL-6 항<br />
체의 용도에 관계한다. 본 발명은 또한, IL-6 또는 이의 이상 발현과 연관된 질환과 이상의 진단, 평가 및 치료<br />
를 위한 항-IL-6 항체의 단편 또는 변이체의 용도에 관계한다. 목적 항체, 특히 인간화, 키메라와 단일 쇄 항체<br />
의 바람직한 용도는 암 관련된 피로, 악액질 및/또는 류머티스성 관절염의 치료 및 예방이다.<br />
본 발명의 다른 구체예는 재조합 숙주 세포, 바람직하게는 2배체 효모, 예를 들면, 2배체 피치아(Pichia) 및 다<br />
른 효모 균주에서 항-IL-6 항체의 생산에 관계한다.<br />
본 발명의 또 다른 구체예는 암으로 진단된 환자의 생존력 또는 삶의 질을 개선하는 방법에 관계하고, 상기 방<br />
법은 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체를 환자에게 투여하는 단계, 여기서 환자의 혈청 C-반응성<br />
단백질("CRP") 수준이 안정화되고, 바람직하게는 감소되고, 그리고 환자의 혈청 CRP 수준의 감소를 평가하기 위<br />
하여 환자를 모니터하는 단계를 포함하고, 이때 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 완전한 인간<br />
IL-6 폴리펩티드, 또는 이의 항체 단편 또는 변이체 상에 존재하는, Ab1을 포함하는 항-IL-6 항체, 그리고 IL-6<br />
에 특이적으로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된 항<br />
체의 하나 이상의 CDR을 포함)과 동일한 선형 또는 입체형태적 에피토프에 특이적으로 결합하고 및/또는 이러한<br />
선형 또는 입체형태적 에피토프에 결합하는 것에 대해 경쟁할 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 또 다른 구체예는 암으로 진단된 환자에서 근력을 개선하는 방법에 관계하고, 상기 방법은 항-IL-6<br />
항체, 또는 이의 항체 단편 또는 변이체를 환자에게 투여하는 단계, 여기서 환자의 근력이 개선되고, 그리고 환<br />
자의 근력을 평가하기 위하여 환자를 모니터하는 단계를 포함하고, 이때 항-IL-6 항체, 또는 이의 항체 단편 또<br />
는 변이체는 완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는, Ab1을 포함하는 항-IL-6 항체, 그리<br />
고 IL-6에 특이적으로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확<br />
인된 항체의 하나 이상의 CDR을 포함)과 동일한 선형 또는 입체형태적 에피토프에 특이적으로 결합하고 및/또는<br />
이러한 선형 또는 입체형태적 에피토프에 결합하는 것에 대해 경쟁할 수 있다. 이들 방법에서, 바람직하게는 환<br />
자의 근력은 악력 측정 시험(손 악력 검사)에 의해 측정되었을 때, 항-IL-6 항체, 또는 이의 항체 단편 또는 변<br />
- 39 -
[0049]<br />
[0050]<br />
[0051]<br />
[0052]<br />
[0053]<br />
[0054]<br />
[0055]<br />
이체의 투여후 대략 4주 이내에 적어도 대략 15% 개선되며, 그리고 더욱 바람직하게는, 환자의 근력은 악력 측<br />
정 시험에 의해 측정되었을 때, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체의 투여후 대략 4주 이내에 적<br />
어도 대략 20% 개선된다.<br />
본 발명의 또 다른 구체예는 혈청 알부민 증가가 요구되는 환자에서 혈청 알부민을 증가시키는 방법에<br />
관계하고, 상기 방법은 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체를 환자에게 투여하는 단계, 여기서 환<br />
자의 혈청 알부민 수준이 개선되고, 그리고 환자의 혈청 알부민 수준을 평가하기 위하여 환자를 모니터하는 단<br />
계를 포함하고, 이때 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 완전한 인간 IL-6 폴리펩티드, 또는 이<br />
의 항체 단편 또는 변이체 상에 존재하는, Ab1을 포함하는 항-IL-6 항체, 그리고 IL-6에 특이적으로 결합하고,<br />
바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포<br />
함)과 동일한 선형 또는 입체형태적 에피토프에 특이적으로 결합하고 및/또는 이러한 선형 또는 입체형태적 에<br />
피토프에 결합하는 것에 대해 경쟁할 수 있다. 바람직하게는, 이들 방법은 항-IL-6 항체, 또는 이의 항체 단편<br />
또는 변이체의 투여후 대략 6주 이내에 환자의 생존력이 개선되는 조건 및/또는 혈청 알부민 수준이 대략 5-10<br />
g/ℓ, 바람직하게는 7-8 g/ℓ 증가되는 조건하에 달성된다. 이들 환자에는 류머티스성 관절염, 암, 진행된 암,<br />
간 질환, 신장 질환, 염증성 장 질환, 셀리악병, 외상, 화상, 감소된 혈청 알부민과 연관된 기타 질환, 또는 이<br />
들의 임의의 조합으로 진단된 환자가 포함되지만 이들에 국한되지 않는다.<br />
본 발명의 한 구체예에서, 환자는 류머티스성 관절염, 유년형 류머티스성 관절염, 건선, 건선성 관절병증, 강직<br />
성 척추염, 전신성 홍반성 루푸스, 크론병, 궤양성 대장염, 천포창, 피부근염, 다발근육염, 류머티스성 다발성<br />
근육통, 거대 세포 동맥염, 혈관염, 결절성 다발동맥염, 베게너 육아종증, 가와사키병, 고립형 CNS 혈관염,<br />
Churg-Strauss 관절염, 현미경적 다발동맥염, 현미경적 다발혈관염, 헤노호-쉐라인 자반증, 본태성 한랭글로불<br />
린혈증성 혈관염, 류머티스성 혈관염, 한랭글로불린혈증, 재발성 다발연골염, 베체트병, 다까야수 동맥염, 허혈<br />
성 심장 질환, 발작, 다발성 경화증, 패혈증, 바이러스 감염(가령, B형 간염, C형 간염, HIV,<br />
거대세포바이러스, 엡스타인-바 바이러스, 파보바이러스 B<strong>19</strong> 등)에 속발성인 혈관염, 버거스씨병, 암, 진행된<br />
암, 골관절염, 전신 경화증, CREST 증후군, 라이터병, 뼈의 파제트병, 쇼그렌 증후군, 1형 당뇨병, 2형 당뇨병,<br />
가족성 지중해열, 자가면역 혈소판감소증, 자가면역 용혈성 빈혈, 자가면역 갑상선 질환, 악성 빈혈, 백반, 원<br />
형탈모증, 원발성 담도 경화증, 자가면역 만성 활성 간염, 알코올성 간경화증, B형과 C형 간염을 비롯한 바이러<br />
스 간염, 다른 장기 특이적 자가면역 질환, 화상, 특발성 폐 섬유증, 만성 폐쇄성 폐 질환, 알레르기 천식, 다<br />
른 알레르기 질환 또는 이들의 임의의 조합으로 진단될 수 있다.<br />
본 발명의 한 구체예에서, 환자는 치료 이전에 상승된 C-반응성 단백질(CRP) 수준을 가질 수 있다.<br />
본 발명의 다른 구체예는 병든 환자의 생존력 또는 삶의 질을 개선하는 방법에 관계하고, 상기 방법은 환자에게<br />
IL-6 길항제, 예를 들면, Ab1을 투여하는 단계, 여기서 환자의 혈청 C-반응성 단백질("CRP") 수준이 감소되고,<br />
그리고 환자의 혈청 CRP 수준의 감소를 평가하기 위하여 환자를 모니터하는 단계를 포함한다.<br />
본 발명의 또 다른 구체예는 병든 환자의 생존력 또는 삶의 질을 개선하는 방법에 관계하고, 상기 방법은 환자<br />
에게 IL-6 길항제, 예를 들면, Ab1을 투여하는 단계, 여기서 환자의 혈청 알부민 수준이 증가되고, 그리고 환자<br />
의 혈청 알부민 수준의 증가를 평가하기 위하여 환자를 모니터하는 단계를 포함한다.<br />
본 발명의 또 다른 구체예는 병든 환자의 생존력 또는 삶의 질을 개선하는 방법에 관계하고, 상기 방법은 환자<br />
에게 IL-6 길항제, 예를 들면, Ab1을 투여하는 단계, 여기서 환자의 혈청 C-반응성 단백질("CRP") 수준이 감소<br />
되고, 그리고 환자의 혈청 알부민 수준이 증가되며, 그리고 환자의 혈청 CRP 수준의 감소 및 환자의 혈청 알부<br />
민 수준의 증가를 평가하기 위하여 환자를 모니터하는 단계를 포함한다.<br />
본 발명의 다른 구체예는 과혈액응고 상태인 환자에서 혈전증을 예방하거나 치료하는 방법에 관계하고, 상기 방<br />
법은 환자에게 IL-6 길항제, 예를 들면, 항-IL-6 항체(가령, Ab1), 그리고 IL-6에 특이적으로 결합하고, 바람직<br />
하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포함)을<br />
투여하는 단계, 여기서 환자의 혈액응고 프로필이 개선되거나 정상 상태로 복원되고, 그리고 환자를 모니터하여<br />
혈액응고 프로필을 평가하는 단계를 포함한다. 바람직하고 예시적인 하기 구체예에서 논의된 바와 같이, 항-IL-<br />
6 항체는 Ab1의 CDR을 포함하는 인간화 항체를 포함하고, 그리고 더욱 바람직하게는, 각각 서열 번호: 657과 서<br />
열 번호: 709의 가변 중쇄와 경쇄, 그리고 각각 서열 번호: 588과 서열 번호: 586의 불변 영역을 포함하거나,<br />
또는 하나 이상의 아미노산이 IL-6 결합 친화성의 실질적인 파괴없이, 치환 또는 결실에 의해 변형되는 이들의<br />
변이체를 포함할 것이다.<br />
- 40 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0056]<br />
[0057]<br />
[0058]<br />
[0059]<br />
[0060]<br />
[0061]<br />
[0062]<br />
[0063]<br />
[0064]<br />
[0065]<br />
[0066]<br />
[0067]<br />
[0068]<br />
[0069]<br />
[0070]<br />
[0071]<br />
[0072]<br />
이런 방법에서, IL-6 길항제가 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체라면, 바람직하게는 상기 항체는<br />
완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는, Ab1 및 이의 단편과 변이체를 포함하는 항-IL-6<br />
항체와 동일한 선형 또는 입체형태적 에피토프에 특이적으로 결합하고 및/또는 이러한 선형 또는 입체형태적 에<br />
피토프에 결합하는 것에 대하여 경쟁할 수 있다. 혈전증을 예방하거나 치료하는 본 발명의 방법에서, 환자의 혈<br />
액응고 프로필은 D-이합체, 인자 II, 인자 V, 인자 VIII, 인자 IX, 인자 XI, 인자 XII, F/피브린 분해 산물, 트<br />
롬빈-항트롬빈 III 복합체, 피브리노겐, 플라스미노겐, 프로트롬빈, 그리고 폰 빌레브란드 인자 중에서 한 가지<br />
이상의 환자의 혈청 수준의 측정치에 의해, 그리고 바람직하게는 항-IL-6 항체의 투여에 앞서 환자의 혈청 D-이<br />
합체 수준을 측정하는 단계, 그리고 환자의 혈청 D-이합체 수준이 상승되면 항-IL-6 항체, 또는 이의 항체 단편<br />
또는 변이체를 투여하는 단계를 포함하는 방법에 의해 평가된다. 이에 더하여, C 반응성 단백질의 수준 역시,<br />
치료에 앞서 환자에서 평가되고, 그리고 상승되면, 이는 환자에서 혈전증의 증가된 위험에 대한 추가의 지시자<br />
로서 이용될 수 있다.<br />
본 발명의 한 구체예는 과혈액응고와 연관된 질환 또는 이상을 앓는 환자를 치료하는 방법에 관계하고, 상기 방<br />
법은 IL-6 길항제, 예를 들면, Ab1을 환자에게 투여하는 단계, 여기서 환자의 혈액응고 프로필이 개선되거나 정<br />
상으로 복원되고, 그리고 환자를 모니터하여 혈액응고 프로필을 평가하는 단계를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 환자는 치료 이전에 상승된 혈청 D-이합체 수준을 가질 수 있다.<br />
본 발명의 한 구체예에서, 환자는 치료 이전에 감소된 혈청 알부민 수준을 가질 수 있다.<br />
본 발명의 한 구체예에서, 치료 이후에 환자의 Glasgow 예후 점수(GPS)가 개선될 수 있다.<br />
본 발명의 한 구체예에서, 환자는 치료 이전에 상승된 혈청 CRP 수준을 가질 수 있다.<br />
본 발명의 한 구체예에서, 본 발명의 방법은 적어도 한 가지 스타틴의 투여를 추가로 포함할 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1, JAK2,<br />
JAK3, SYK, 또는 이들의 임의의 조합을 표적으로 할 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 항체, 항체 단편, 펩티드, 글리코알코이드, 안티센스(antisense)<br />
핵산, 리보자임, 레티노이드, 아베미르(avemir), 소분자, 또는 이들의 임의의 조합을 포함할 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 항-IL-6R, 항-gp130, 항-p38 MAP 키나아제, 항-JAK1, 항-JAK2, 항-<br />
JAK3, 또는 항-SYK 항체 또는 항체 단편을 포함할 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 탈리도미드, 레날리도미드, 또는 이들의 임의의 조합을 포함하는 소분<br />
자를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 길항제는 항-IL-6 항체(가령, Ab1), 또는 이의 항체 단편 또는 변이체를 포함할 수<br />
있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 완전한 인간 IL-6 폴리펩티드 또<br />
는 이의 단편 상에 존재하는, Ab1을 포함하는 항-IL-6 항체, 그리고 IL-6에 특이적으로 결합하고, 바람직하게는<br />
비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포함)과 동일한<br />
선형 또는 입체형태적 에피토프에 특이적으로 결합하고 및/또는 이러한 선형 또는 입체형태적 에피토프에 결합<br />
하는 것에 대해 경쟁할 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체는 완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는, Ab1과<br />
동일한 선형 또는 입체형태적 에피토프에 결합하고 및/또는 이러한 선형 또는 입체형태적 에피토프에 결합하는<br />
것에 대해 경쟁할 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 완전한 인간 IL-6 폴리펩티드 또<br />
는 이의 단편 상에 존재하는, Ab1을 포함하는 항-IL-6 항체, 그리고 IL-6에 특이적으로 결합하고, 바람직하게는<br />
비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포함)과 동일한<br />
선형 또는 입체형태적 에피토프에 특이적으로 결합할 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 완전한 인간 IL-6 폴리펩티드 또<br />
는 이의 단편 상에 존재하는, Ab1과 동일한 선형 또는 입체형태적 에피토프에 특이적으로 결합할 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 Ab1에 의해 특이적으로 결합되는<br />
- 41 -
[0073]<br />
[0074]<br />
[0075]<br />
[0076]<br />
[0077]<br />
[0078]<br />
[0079]<br />
[0080]<br />
[0081]<br />
[0082]<br />
[0083]<br />
완전한 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는 동일한 선형 또는 입체형태적 에피토프에 특이적으로 결<br />
합할 수 있고, 이때 본래의 인간 IL-6 폴리펩티드의 전장에 걸쳐있는 겹쳐지는 선형 펩티드 단편들을 이용한 에<br />
피토프 매핑에 의해 확인될 때, 상기 에피토프는 아미노산 잔기 37-51, 아미노산 잔기 70-84, 아미노산 잔기<br />
169-183, 아미노산 잔기 31-45 및/또는 아미노산 잔기 58-72를 각각 포함하는 것들에서 선택되는 IL-6 단편 내<br />
에 포함된 하나 이상의 잔기를 포함한다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 Ab1을 포함하는 항-IL-6 항체, 그<br />
리고 IL-6에 특이적으로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서<br />
확인된 항체의 하나 이상의 CDR을 포함) 내에 포함된 것들과 동일한 가변 경쇄 및 가변 중쇄 영역 각각에서 적<br />
어도 2개의 상보성 결정 영역(CDR)을 포함할 수 있다. 일정한 구체예에서, 이들 CDR을 포함하는 항체는 본 명세<br />
서에 기술된 인간화 방법에 기초하여, 적절한 인간 골격을 이용하여 작제될 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 Ab1 내에 포함된 것들과 동일한<br />
가변 경쇄 및 가변 중쇄 영역 각각에서 적어도 2개의 상보성 결정 영역(CDR)을 포함할 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체 내에 모든 CDR은 Ab1을 포함하는 항<br />
-IL-6 항체, 그리고 IL-6에 특이적으로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체<br />
와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포함) 내에 포함된 CDR과 동일할 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체 내에 모든 CDR은 Ab1 내에 포함된<br />
하나 이상의 CDR과 동일할 수 있다.<br />
바람직한 예시적인 구체예에서, 항-IL-6 항체는 Ab1 내에 모든 CDR을 포함할 수 있다. 더욱 바람직한 구체예에<br />
서, 항-IL-6 항체는 서열 번호: 657 및 서열 번호: 709의 가변 중쇄 및 경쇄 서열, 또는 이들의 변이체를 포함<br />
할 것이다.<br />
바람직한 구체예에서, 인간화된 항-IL-6 항체는 서열 번호:657 및 서열 번호:709에 각각 포함된 가변 중쇄 및<br />
가변 경쇄 서열을 포함하고, 그리고 바람직하게는, 서열 번호:588 및 서열 번호:586에 각각 포함된 중쇄와 경쇄<br />
불변 영역, 그리고 IL-6 결합 및/또는 원하는 이펙터 기능에 실질적으로 영향을 주지 않는 하나 이상의 아미노<br />
산 치환 또는 결실을 포함하는 이들의 변이체를 추가로 포함할 수 있다. 이러한 구체예는 또한, 가변 중쇄(서열<br />
번호: 700) 및 가변 경쇄(서열 번호:723) 서열, 그리고 불변 영역 중쇄(서열 번호: 589) 및 불변 영역 경쇄(서<br />
열 번호:587) 서열을 인코딩하는 하나 이상의 핵산을 포함하거나, 또는 대안으로 이러한 핵산으로 구성되는 폴<br />
리뉴클레오티드를 고려한다. 이러한 구체예는 서열 번호:657 및 서열 번호:709에 각각 포함된 가변 중쇄 및 가<br />
변 경쇄 서열, 그리고 서열 번호:588 및 서열 번호:586에 각각 포함된 중쇄와 경쇄 불변 영역에, IL-6 결합 및/<br />
또는 원하는 이펙터 기능에 실질적으로 영향을 주지 않는 하나 이상의 아미노산 치환 또는 결실을 포함하는 변<br />
이체를 인코딩하는 핵산 역시 고려한다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 비당화될 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 이펙터 기능, 반감기, 단백질가수<br />
분해, 및/또는 당화(glycosylation)를 변화시키기 위하여 변형된 Fc 영역을 포함할 수 있다. 바람직하게는, Fc<br />
영역은 당화가 제거되도록 변형된다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 인간 항체, 인간화 항체, 단일 쇄<br />
항체 또는 키메라 항체일 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 토끼(모) 항-IL-6 항체로부터 유<br />
래된 인간화 항체일 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체의 가변 경쇄 영역 및 가변 중쇄 영<br />
역 내에 골격 영역(FR)은 변형되지 않거나, 또는 가변 경쇄 또는 중쇄 영역 내의 2개 또는 3개 정도의 인간 FR<br />
잔기를 모 토끼 항체의 상응하는 FR 잔기에 의해 치환함으로써 변형된, 인간 FR일 수 있고, 그리고 이들 인간<br />
FR은 인간 생식선 항체 서열의 라이브러리 내에 포함된 다른 인간 생식선 항체 서열에 비하여, 상응하는 토끼<br />
가변 중쇄 또는 경쇄 영역에 대한 높은 상동성 수준에 기초하여 인간 생식선 항체 서열의 라이브러리로부터 선<br />
택된 인간 가변 중쇄와 경쇄 항체 서열로부터 유래될 수 있다. 하기 바람직한 구체예에서 상세하게 개시된 바와<br />
같이, 항체는 인간화된 모 항체의 FR에 대한 높은 상동성(서열 동일성 수준)에 기초하여 선택된 인간 FR를 포함<br />
할 것이다.<br />
- 42 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0084]<br />
[0085]<br />
[0086]<br />
[0087]<br />
[0088]<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 대략 4주, 대략 8주, 대략 <strong>12</strong>주,<br />
대략 16주, 대략 20주, 또는 대략 24주의 기간 마다 1회 정도의 빈도로 환자에 투여될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈액응고 프로필은 2번의 연속 항-IL-6 항체 투여 사이에 존재하는 전체 기간<br />
동안 개선된 상태로 유지될 수 있다.<br />
본 발명의 한 구체예에서, 2번의 연속 항-IL-6 항체 투여 사이에 존재하는 전체 기간 동안 환자의 혈청 CRP 수<br />
준은 감소된 상태로 유지되고 및/또는 혈청 알부민 수준은 상승된 상태로 유지될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 악액질, 쇠약, 피로, 및/또는 발열은 2번의 연속 항-IL-6 항체 투여 사이에<br />
존재하는 전체 기간 동안 개선된 상태로 유지될 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 환자는 가시세포종, 선방 세포 암종, 청신견종, 선단 흑자성 흑색종, 선단한선종, 급<br />
성 호산성 백혈병, 급성 림프모구성 백혈병, 급성 거핵모구성 백혈병, 급성 단구성 백혈병, 성숙을 동반한 급성<br />
골수모구성 백혈병, 급성 골수성 수상돌기 세포 백혈병, 급성 골수성 백혈병, 급성 전골수성 백혈병, 사기질종,<br />
선암종, 선양 낭성 암종, 선종, 선양 치성 종양, 부신피질 암종, 성체 T-세포 백혈병, 공격성 NK-세포 백혈병,<br />
AIDS-관련된 암, AIDS-관련된 림프종, 포상 연부 육종, 법랑아세포 섬유치아종, 항문 암, 퇴행성 대세포<br />
림프종, 역형성 갑상선 암, 혈관면역모세포형 T-세포 림프종, 혈관근육지방종, 맥관육종, 충수 암, 별아교세포<br />
종, 비정형 기형 횡문근양 종양, 기저 세포 암종, 기저-유사 암종, B-세포 백혈병, B-세포 림프종, 집합관<br />
암종, 담도 암, 방광 암, 모세포종, 골 암, 골 종양, 뇌간 교종, 뇌 종양, 유방암, 브렌너 종양, 기관지 종양,<br />
세기관지폐포 암종, 갈색 종양, 버킷 림프종, 원발부위 불명암, 유암종, 암종, in situ 암종, 음경 암종, 원발<br />
부위 불명 암종, 암육종, 캐슬만씨병, 중추신경계 배양 종양, 소뇌 별아교세포종, 대뇌 별아교세포종, 자궁경부<br />
암, 담관암, 연골종, 연골육종, 척삭종, 융모막암종, 맥락막총 유두종, 만성 림프성 백혈병, 만성 단구성 백혈<br />
병, 만성 골수성 백혈병, 만성 골수증식성 질환, 만성 호중구성 백혈병, 투명-세포 종양, 대장 암, 결장직장<br />
암, 머리인두종, 피부 T-세포 림프종, Degos 질환, 융기성 피부섬유육종, 유피낭종, 복부 결합조직형성 소원형<br />
세포 종양, 미만성 거대 B 세포 림프종, 배아형성장애 신경상피 종양, 배아 암종, 내배엽동 종양, 자궁내막 암,<br />
자궁내막 자궁 암, 자궁내막양 종양, 장병증 연관 T-세포 림프종, 상의모세포종, 상의세포종, 상피양 육종, 적<br />
백혈병, 식도 암, 감각신경모세포종, 유잉 계통 종양, 유잉 계통 육종, 유잉 육종, 두개외 생식세포 종양, 생식<br />
샘외 생식세포 종양, 간외 담도 암, 유방외성 파제트병, 난관 암, 태아속 태아, 섬유종, 섬유육종, 소포성 림프<br />
종, 소포성 갑상선 암, 담낭 암, 담낭 암, 신경절교종, 신경절신경종, 위 암, 위 림프종, 위장 암, 위장<br />
유암종, 위장 기질 종양, 위장 기질 종양, 생식세포 종양, 배세포종, 임신성 융모막암종, 임신성 융모성 종양,<br />
뼈의 거대 세포 종양, 다형성교모세포종, 신경교종, 대뇌신경교종증, 사구 종양, 글루카곤종, 생식아세포종, 과<br />
립층 세포 종양, 모상 세포 백혈병, 모상 세포 백혈병, 두경부 암, 두경부 암, 심장 암, 혈관모세포종, 혈관주<br />
위세포종, 혈관육종, 혈액학적 악성, 간세포 암종, 간비 T-세포 림프종, 유전성 유방-난소암 증후군, 호지킨 림<br />
프종, 호지킨 림프종, 하인두 암, 시상하부 신경교종, 염증 유방암, 안구내 흑색종, 섬 세포 암종, 섬 세포 종<br />
양, 연소형 골수단구성 백혈병, 카포시 육종, 카포시 육종, 신장 암, 클라츠킨씨 종양, 크루켄버그 종양, 후두<br />
암, 후두 암, 악성 흑자 흑색종, 백혈병, 백혈병, 입술과 구강 암, 지방육종, 폐암, 황체종, 림프관종, 림프관<br />
육종, 림프상피종, 림프성 백혈병, 림프종, 마크로글로불린혈증, 악성 섬유성 조직구종, 악성 섬유성 조직구종,<br />
뼈의 악성 섬유성 조직구종, 악성 신경교종, 악성 중피종, 악성 말초신경초 종양, 악성 횡문근양 종양, 악성 트<br />
리톤 종양, MALT 림프종, 덮개 세포 림프종, 비만 세포 백혈병, 종격동 생식세포 종양, 종격동 종양, 갑상선 수<br />
질암, 속질모세포종, 속질모세포종, 속질상피종, 흑색종, 흑색종, 수막종, 메르켈 세포 암종, 중피종, 중피종,<br />
잠복원발성 전이성 편평 목 암, 전이성 요로상피 암종, 혼합 뮬러 종양, 단구성 백혈병, 구강 암, 점액 종양,<br />
다발성 내분비 종양 증후군, 다발성 골수종, 다발성 골수종, 균상식육종, 균상식육종, 골수형성이상 질환, 골수<br />
형성이상 증후군, 골수성 백혈병, 골수성 육종, 골수증식 질환, 점액종, 비강 암, 코인두 암, 코인두 암종, 신<br />
생물, 신경집종, 신경모세포종, 신경모세포종, 신경섬유종, 신경종, 결절성 흑색종, 비-호지킨 림프종, 비-호지<br />
킨 림프종, 비-흑색종 피부 암, 비-소세포 폐암, 안종양, 희소별아교세포종, 핍지교종, 호산성세포종, 시신경초<br />
수막종, 구강 암, 구강 암, 입인두 암, 골육종, 골육종, 난소암, 난소암, 난소 상피 암, 난소 생식세포 종양,<br />
난소 저급성 악성 종양, 유방의 파제트병, 판코스트 종양, 췌장암, 췌장암, 갑상샘 유두 암, 유두종증, 곁신경<br />
절종, 부비동 암, 부갑상선 암, 음경 암, 혈관주위 상피모양 세포 종양, 인두 암, 갈색세포종, 중간 분화의 송<br />
과체 실질 종양, 송과체모세포종, 하수체세포종, 뇌하수체 선종, 뇌하수체 종양, 플라스마 세포 신생물, 흉막폐<br />
아세포종, 다배아종, 전구 T-림프모구성 림프종, 원발성 중추신경계 림프종, 원발성 삼출성 림프종, 원발성 간<br />
세포 암, 원발성 간 암, 원발성 복막 암, 원시 신경외배엽 종양, 전립선암, 복막가성점액종, 직장 암, 신장 세<br />
포 암종, 염색체 15에서 NUT 유전자가 관련된 호흡기 암종, 망막모세포종, 횡문근종, 횡문근육종, 리히터 변형<br />
- 43 -
[0089]<br />
[0090]<br />
[0091]<br />
[0092]<br />
[0093]<br />
[0094]<br />
[0095]<br />
[0096]<br />
[0097]<br />
[0098]<br />
[0099]<br />
(Richter's transformation), 천미골 기형종, 타액선 암, 육종, 다발성신경초종, 피지선 암종, 속발성 신생물,<br />
정상피종, 장액 종양, 세르톨리 라이디히 세포 종양, 성삭-기질 종양, 세자리 증후군, 인환 세포 암종, 피부<br />
암, 청색 소원형세포 종양, 소세포 암종, 소세포 폐암, 소세포 림프종, 소장 암, 연부 조직 육종, 소마토스타틴<br />
종, 매연 사마귀, 척추 종양, 척추 종양, 비장 번연 림프종, 편평 세포 암종, 위 암, 표재 확장성 흑색종, 천막<br />
위 원시 신경외배엽 종양, 표면 상피-기질 종양, 활액 육종, T-세포 급성 림프모구성 백혈병, T-세포 큰 과립성<br />
림프구 백혈병, T-세포 백혈병, T-세포 림프종, T-세포 전림프성 백혈병, 기형종, 말기 림프성 암, 고환 암, 난<br />
포막종, 인후 암, 흉선 암종, 가슴샘종, 갑상선 암, 신우와 요관의 이행 세포 암, 이행 세포 암종, 요막관 암,<br />
요도 암, 비뇨생식기 신생물, 자궁 육종, 포도막 흑색종, 질 암, 버너-모리슨 증후군, 사마귀모양 암종, 시각경<br />
로 신경교종, 외음부 암, 왈덴스트룀 마크로글로불린혈증, 바르틴 종양, 윌름 종양, 또는 이들의 임의의 조합에<br />
서 선택되는 암으로 진단될 수 있다.<br />
본 발명의 한 구체예에서, 환자는 결장직장 암, 비-소세포 폐암, 담관암, 중피종, 캐슬만씨병, 신장 세포 암종,<br />
또는 이들의 임의의 조합에서 선택되는 암으로 진단될 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 서열 번호: 3, 18, <strong>19</strong>, 652, 656,<br />
657, 658, 661, 664, 665, 704, 또는 708을 포함하는 중쇄 폴리펩티드 서열을 포함하고; 그리고 서열 번호: 2,<br />
20, 647, 651, 660, 666, 699, 702, 706, 또는 709를 포함하는 VL 폴리펩티드 서열을 추가로 포함하거나, 또는<br />
이들의 변이체를 포함할 수 있고, 이때 상기 VH 또는 VL 폴리펩티드 내에서 하나 이상의 골격 잔기(FR 잔기)가<br />
다른 아미노산 잔기로 치환되어 인간 IL-6에 특이적으로 결합하는 항-IL-6 항체, 또는 이의 항체 단편 또는 변<br />
이체가 산출되거나, 또는 CDR이 상기 서열에 상동한 인간 골격 내로 통합되는 폴리펩티드를 포함할 수 있다. 바<br />
람직하게는, 가변 중쇄와 경쇄는 서열 번호: 657 및 709에서 것들을 포함한다.<br />
본 발명의 한 구체예에서, 하나 이상의 상기 FR 잔기는 상기 VH 또는 VL 폴리펩티드 내에 포함된 상보성 결정 영<br />
역(CDR)이 유래되는 모 토끼 항-IL-6 항체 내에서 상응하는 부위에 존재하는 아미노산으로, 또는 보존적 아미노<br />
산 치환에 의해 치환될 수 있다.<br />
본 발명의 한 구체예에서, 상기 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 인간화될 수 있다.<br />
본 발명의 한 구체예에서, 상기 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 키메라일 수 있다.<br />
본 발명의 한 구체예에서, 상기 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 인간 Fc, 예를 들면, 서열<br />
번호:704 및 702에 포함된 가변 중쇄와 경쇄 불변 영역으로 구성되는 Fc 영역을 추가로 포함할 수 있다.<br />
본 발명의 한 구체예에서, 상기 인간 Fc는 IgG1, IgG2, IgG3, IgG4, IgG5, IgG6, IgG7, IgG8, IgG9, IgG10,<br />
IgG11, IgG<strong>12</strong>, IgG13, IgG14, IgG15, IgG16, IgG17, IgG18 또는 IgG<strong>19</strong>로부터 유래될 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 서열 번호: 3, 18, <strong>19</strong>, 652, 656,<br />
657, 658, 661, 664, 665, 704, 708, 2, 20, 647, 651, 660, 666, 699, 702, 706, 또는 709의 폴리펩티드 서<br />
열 중에서 하나 이상에 적어도 90% 서열 상동성을 갖는 폴리펩티드를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 적어도 대략 22일, 적어도 대략<br />
25일, 또는 적어도 대략 30일의 소실 반감기를 가질 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제, 예를 들면, Ab1은 화학요법제와 공동-투여될 수 있다. 본 발명의 한 구<br />
체예에서, 화학요법제에는 VEGF 길항제, EGFR 길항제, 플라틴, 탁솔, 이리노테칸, 5-플루오르우라실, 젬시타빈,<br />
류코보린, 스테로이드, 시클로포스파미드, 멜팔란, 빈카 알칼로이드(가령, 빈블라스틴, 빈크리스틴, 빈데신과<br />
비노렐빈), 무스틴, 티로신 키나아제 저해제, 방사선요법, 성 호르몬 길항제, 선택성 안드로겐 수용체 조절제,<br />
선택성 에스트로겐 수용체 조절제, PDGF 길항제, TNF 길항제, IL-1 길항제, 인터루킨(가령 IL-<strong>12</strong> 또는 IL-2),<br />
IL-<strong>12</strong>R 길항제, 독소 접합된 단일클론 항체, 종양 항원 특이적 단일클론 항체, Erbitux, Avastin,<br />
Pertuzumab, 항-CD20 항체, Rituxan<br />
, 오크렐리주맙, 오파투무맙, DXL625, Herceptin<br />
, 또는 이들의 임의의 조합이 포함되지만 이들에 국한되지 않는다.<br />
본 발명의 한 구체예에서, 다른 치료 화합물은 스타틴일 수 있다.<br />
- 44 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0100]<br />
[0101]<br />
[0102]<br />
[0103]<br />
[0104]<br />
[0105]<br />
[0106]<br />
[0107]<br />
[0108]<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체는 검출가능 라벨 또는 치료제에 직<br />
접적으로 또는 간접적으로 부착될 수 있다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체 또는 항체 단편은 Ab1, 또는 Ab1의 CDR 중에서 모두 또는 대부분을 포<br />
함하는 이의 인간화, 키메라, 단일 쇄 또는 단편일 수 있다.<br />
본 발명의 한 구체예에서, 질환 또는 이상은 급성 정맥 혈전증, 폐 색전증, 임신 동안 혈전증, 출혈성 피부 괴<br />
사, 급성 또는 만성 범발성 혈관내 혈액응고(DIC), 수술로부터 응괴 형성, 장기 요양, 장기간의 부동, 정맥 혈<br />
전증, 전격성 수막염균 혈증, 급성 혈전성 뇌졸중, 급성 관상동맥 폐쇄증, 급성 말초 동맥 폐쇄증, 광범위 폐<br />
색전증, 액와 정맥 혈전증, 광범위 골대퇴정맥 혈전증, 폐쇄된 동맥 도관, 폐쇄된 정맥 도관, 심근증, 간의 정<br />
맥폐쇄성 질환, 저혈압, 감소된 심박출량, 감소된 혈관 저항, 폐 고혈압, 감소된 폐 유순도, 백혈구감소증, 혈<br />
소판감소증, 헤파린-유도된 혈소판감소증(HIT), 헤파린-유도된 혈소판감소증과 혈전증(HITT), 심방 세동, 인공<br />
심장 판막의 이식, 혈전증에 대한 유전적 민감도, 인자 V 라이덴병, 프로트롬빈 유전자 돌연변이, 메틸렌테트라<br />
하이드로폴레이트 환원효소(MTHFR) 다형성, 혈소판-수용체 다형성, 외상, 골절, 화상, 또는 이들의 임의의 조합<br />
에서 선택될 수 있다.<br />
본 발명의 한 구체예에서, 질환 또는 이상은 암, 류머티스성 관절염, AIDS, 심장 질환, 탈수, 영양실조, 납 노<br />
출, 말라리아, 호흡 질환, 노령, 갑상선 기능저하증, 결핵, 뇌하수체 저하증, 신경쇠약, 고나트륨혈증, 저나트<br />
륨혈증, 신장 질환, 지라동맥, 강직성 척추염, 성장 실패(부진한 성장), 또는 이들의 임의의 조합에서 선택될<br />
수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 악액질-연관된 인자, 쇠약-연관된 인자, 피로-연관된 인자, 및/또는 발<br />
열-연관된 인자의 길항제의 투여를 포함할 수 있다. 악액질-연관된 인자, 쇠약-연관된 인자, 피로-연관된 인자,<br />
및/또는 발열-연관된 인자는 종양 괴사 인자-알파, 인터페론 감마, 인터루킨 1 알파, 인터루킨 1 베타, 인터루<br />
킨 6, 단백분해 유도 인자, 백혈병-저해 인자, 또는 이들의 임의의 조합에서 선택될 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 칸나비스, 드로나비놀(Marinol), 나빌론(Cesamet), 칸나비디올, 칸나<br />
비크로멘, 테트라히드로칸나비놀, 사티벡스, 메게스트롤 아세테이트, 또는 이들의 임의의 조합에서 선택되는 항<br />
-악액질 약제의 투여를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 5-HT3 수용체 길항제, 아쥬와인, 알리자프리드, 항콜린약,<br />
항히스타민제, 아프레피탄트, 벤조디아제핀, 칸나비크로멘, 칸나비디올, 칸나비노이드, 칸나비스, 카소피탄트,<br />
클로르프로마진, 시클리진, 덱사메타손, 덱사메타손, 디멘하이드리네이트(Gravol), 디펜히드라민,<br />
돌라세트론, 돔페리돈, 도파민 길항제, 독실라민, 드로나비놀(Marinol), 드로페리돌, 에메트롤, 생강, 그라니<br />
세트론, 할로페리돌, 히드록사진, 히오신, 로라제팜, 메클리진, 메토클로프라미드, 미다졸람, 무시몰, 나빌론<br />
(Cesamet), nk1 수용체 길항제, 온단세트론, 팔로노세트론, 페퍼민트, 페너간, 프로클로르페라진, Promacot, 프<br />
로메타진, 펜타진, 프로포폴, 사티벡스, 테트라히드로칸나비놀, 트리메토벤자미드, 트로피세트론, 난드롤론, 스<br />
틸베스트롤, 탈리도미드, 레날리도미드, 그렐린 효능제, 미오스타틴 길항제, 항-미오스타틴 항체, 선택성 안드<br />
로겐 수용체 조절제, 선택성 에스트로겐 수용체 조절제, 앤지오텐신 AII 길항제, 베타 2 아드레날린성 수용체<br />
효능제, 베타 3 아드레날린성 수용체 효능제, 또는 이들의 임의의 조합에서 선택되는 항-메스꺼움제 또는 항구<br />
토제의 투여를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 5-HT3 수용체 길항제, 아쥬와인, 알리자프리드, 항콜린약,<br />
항히스타민제, 아프레피탄트, 벤조디아제핀, 칸나비크로멘, 칸나비디올, 칸나비노이드, 칸나비스, 카소피탄트,<br />
클로르프로마진, 시클리진, 덱사메타손, 덱사메타손, 디멘하이드리네이트(Gravol), 디펜히드라민,<br />
돌라세트론, 돔페리돈, 도파민 길항제, 독실라민, 드로나비놀(Marinol), 드로페리돌, 에메트롤, 생강, 그라니<br />
세트론, 할로페리돌, 히드록사진, 히오신, 로라제팜, 메클리진, 메토클로프라미드, 미다졸람, 무시몰, 나빌론<br />
(Cesamet), nk1 수용체 길항제, 온단세트론, 팔로노세트론, 페퍼민트, 페너간, 프로클로르페라진, Promacot, 프<br />
로메타진, 펜타진, 프로포폴, 사티벡스, 테트라히드로칸나비놀, 트리메토벤자미드, 트로피세트론, 난드롤론, 스<br />
틸베스트롤, 탈리도미드, 레날리도미드, 그렐린 효능제, 미오스타틴 길항제, 항-미오스타틴 항체, 선택성 안드<br />
로겐 수용체 조절제, 선택성 에스트로겐 수용체 조절제, 앤지오텐신 AII 길항제, 베타 2 아드레날린성 수용체<br />
효능제, 베타 3 아드레날린성 수용체 효능제, 또는 이들의 임의의 조합에서 선택되는 항-메스꺼움제 또는 항구<br />
토제의 투여를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 발열은 환자의 체온의 치수에 의해 평가될 수 있다.<br />
- 45 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0109]<br />
[0110]<br />
[0111]<br />
[01<strong>12</strong>]<br />
[0113]<br />
[0114]<br />
[0115]<br />
[0116]<br />
[0117]<br />
[0118]<br />
[01<strong>19</strong>]<br />
[0<strong>12</strong>0]<br />
[0<strong>12</strong>1]<br />
[0<strong>12</strong>2]<br />
[0<strong>12</strong>3]<br />
[0<strong>12</strong>4]<br />
[0<strong>12</strong>5]<br />
[0<strong>12</strong>6]<br />
[0<strong>12</strong>7]<br />
[0<strong>12</strong>8]<br />
[0<strong>12</strong>9]<br />
[0130]<br />
[0131]<br />
본 발명의 한 구체예에서, 상기 방법은 항-IL-6 항체의 투여에 앞서 환자의 체온을 측정하는 단계, 그리고 환자<br />
의 체온이 대략 38℃보다 높으면 항-IL-6 항체 또는 이의 항체 단편 또는 변이체를 투여하는 단계를 포함할 수<br />
있다.<br />
본 발명의 한 구체예에서, 상기 방법은 항-IL-6 항체의 투여전 24시간 이내에 환자의 체온을 측정하는 단계, 그<br />
리고 환자의 체온 치수가 발열이 존재함을 지시하면 항-IL-6 항체 또는 이의 항체 단편 또는 변이체를 투여하는<br />
단계를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 항-IL-6 항체의 투여에 앞서 환자의 체중을 측정하는 단계, 그리고 환자<br />
의 체중이 대략 30일 이내에 대략 5%보다 많이 감소하거나, 또는 환자의 제지방량 지수가 대략 17 ㎏/m 2<br />
(남성<br />
환자) 또는 대략 14 ㎏/m 2<br />
(여성 환자)보다 낮으면 항-IL-6 항체 또는 이의 항체 단편 또는 변이체를 투여하는<br />
단계를 추가로 포함할 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 항-IL-6 항체의 투여에 앞서 환자의 근력을 측정하는 단계, 그리고 환자<br />
의 근력이 대략 30일 이내에 대략 20%보다 많이 감소하면 항-IL-6 항체 또는 이의 항체 단편 또는 변이체를 투<br />
여하는 단계를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 환자에서 악액질, 쇠약, 피로, 및/또는 발열의 연장된 개선을 유발할 수<br />
있다.<br />
본 발명의 한 구체예에서, 환자의 체질량은 항-IL-6 항체 또는 이의 항체 단편 또는 변이체의 투여후 대략 4주<br />
이내에 대략 1㎏ 상승될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 악액질은 항-IL-6 항체 투여후 대략 4주 이내에 측정가능하게 개선될 수<br />
있다.<br />
본 발명의 한 구체예에서, 환자의 악액질은 환자의 총 체질량, 제지방량, 제지방량 지수, 및/또는 부속지 제지<br />
방량의 치수에 의해 평가될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 체질량의 치수는 환자의 종양(들) 및/또는 혈관외액 수집물(들)의 추정된 중<br />
량을 제외(뺄셈)할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 악액질은 항-IL-6 항체 투여후 대략 8주 시점에 측정가능하게 개선된 상태로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 쇠약은 항-IL-6 항체 투여후 대략 4주 이내에 측정가능하게 개선될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 쇠약은 손 악력 검사법에 의해 측정될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 손 악력은 적어도 대략 15%, 또는 적어도 대략 20% 개선될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 쇠약은 항-IL-6 항체 투여후 대략 8주 시점에 측정가능하게 개선된 상태로 유<br />
지될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 피로는 항-IL-6 항체 투여후 대략 1주 이내에 측정가능하게 개선될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 피로는 FACIT-F FS 검사법에 의해 측정될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 FACIT-F FS 점수는 적어도 대략 10 점 개선될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 피로는 항-IL-6 항체 투여후 대략 8주 시점에 측정가능하게 개선된 상태로 유<br />
지될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 발열은 항-IL-6 항체 투여후 대략 1주 이내에 측정가능하게 개선될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 발열은 항-IL-6 항체 투여후 대략 8주 시점에 측정가능하게 개선된 상태로 유<br />
지될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 삶의 질이 개선될 수 있다.<br />
본 발명의 한 구체예에서, 한 가지 이상의 항-응고제 또는 스타틴의 투여를 포함할 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 한 가지 이상의 항응고제는 아브식시맙(ReoPro), 아세노쿠마롤, 항트롬빈 III, 아<br />
- 46 -
[0132]<br />
[0133]<br />
[0134]<br />
[0135]<br />
[0136]<br />
[0137]<br />
[0138]<br />
[0139]<br />
[0140]<br />
[0141]<br />
[0142]<br />
[0143]<br />
[0144]<br />
[0145]<br />
[0146]<br />
[0147]<br />
[0148]<br />
르가트로반, 아스피린, 비발리루딘(Angiomax), 클로피도그렐, 다비가트란, 다비가트란 이텍실레이트(Pradaxa<br />
/Pradax), 데시루딘(Revasc/Iprivask), 디피리다몰, 엡티피바티드(Integrilin), 폰다파리눅스, 헤파<br />
린, 히루딘, 이드라파리눅스, 레피루딘(Refludan), 저분자량 헤파린, 멜라가트란, 페닌디온, 펜프로코우몬,<br />
티클로피딘, 티로피반(Aggrastat), 와파린, 지멜라가트란, 지멜라가트란(Exanta/ Exarta), 또는 이들의<br />
임의의 조합에서 선택될 수 있다.<br />
본 발명의 한 구체예에서, 한 가지 이상의 스타틴은 아토르바스타틴, 체리바스타틴, 플루바스타틴, 로바스타틴,<br />
메바스타틴, 피타바스타틴, 프라바스타틴, 로수바스타틴, 심바스타틴, 또는 이들의 임의의 조합에서 선택될 수<br />
있다.<br />
본 발명의 한 구체예에서, 환자의 혈액응고 프로필은 D-이합체, 인자 II, 인자 V, 인자 VIII, 인자 IX, 인자<br />
XI, 인자 XII, F/피브린 분해 산물, 트롬빈-항트롬빈 III 복합체, 피브리노겐, 플라스미노겐, 프로트롬빈, 그리<br />
고 폰 빌레브란드 인자 중에서 한 가지 이상의 환자의 혈청 수준의 측정치에 의해 평가될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈액응고 프로필은 응고 능력의 기능 측정치에 의해 평가될 수 있다.<br />
본 발명의 한 구체예에서, 응고 능력의 기능 측정치는 프로트롬빈 시간(PT), 프로트롬빈 비율(PR), 국제 표준화<br />
비율(INR), 또는 이들의 임의의 조합에서 선택될 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 IL-6 길항제의 투여에 앞서 환자의 국제 표준화 비율(INR)을 측정하는<br />
단계, 그리고 환자의 INR이 대략 0.9보다 낮으면 IL-6 길항제, 예를 들면, Ab1을 환자에게 투여하는 단계를 포<br />
함할 수 있다.<br />
본 발명의 한 구체예에서, 본 발명은 IL-6 길항제의 투여에 앞서 환자의 국제 표준화 비율(INR)을 측정하는 단<br />
계, 그리고 환자의 INR이 대략 0.5보다 낮으면 IL-6 길항제, 예를 들면, Ab1을 환자에게 투여하는 단계를 포함<br />
할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 INR은 환자에 IL-6 길항제의 투여후 4주 이내에 대략 0.9 이상으로 증가될 수<br />
있다.<br />
본 발명의 한 구체예에서, 상기 방법은 IL-6 길항제의 투여에 앞서 환자의 혈청 D-이합체 수준을 측정하는<br />
단계, 그리고 환자의 혈청 D-이합체 수준이 정상적인 참고 범위를 초과하면 IL-6 길항제, 예를 들면, Ab1을 투<br />
여하는 단계를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈청 D-이합체 수준은 환자에 IL-6 길항제의 투여후 4주 이내에 정상적인 참<br />
고 범위의 상한 미만으로 떨어질 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 환자의 혈액응고 프로필에서 연장된 개선을 유발할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈액응고 프로필은 IL-6 길항제의 투여후 대략 2주 이내에 측정가능하게 개선<br />
될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈액응고 프로필은 환자에 IL-6 길항제의 투여후 대략 <strong>12</strong>주에 측정가능하게<br />
개선된 상태로 유지될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 생존력이 개선될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 안티센스 핵산일 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 예로써, IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1,<br />
JAK2, JAK3, 또는 SYK를 인코딩하는 서열의 적어도 대략 10개의 뉴클레오티드를 포함하는 안티센스 핵산일 수<br />
있다.<br />
본 발명의 한 구체예에서, 안티센스 핵산은 DNA, RNA, 펩티드 핵산, 잠금(locked) 핵산, 모르폴리노(포스포로디<br />
아미데이트 모르폴리노 올리고), 글리세롤 핵산, 트레오즈(threose) 핵산, 또는 이들의 임의의 조합을 포함할<br />
수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 Actemra(토클리주맙), Remicade<br />
, Zenapax(다클리주맙), 또는 이들의 임의의 조합을 포함할 수 있다.<br />
- 47 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0149]<br />
[0150]<br />
[0151]<br />
[0152]<br />
[0153]<br />
[0154]<br />
[0155]<br />
[0156]<br />
[0157]<br />
[0158]<br />
[0159]<br />
[0160]<br />
[0161]<br />
[0162]<br />
[0163]<br />
[0164]<br />
[0165]<br />
[0166]<br />
[0167]<br />
[0168]<br />
[0169]<br />
[0170]<br />
본 발명의 한 구체예에서, IL-6 길항제는 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1, JAK2,<br />
JAK3, SYK, 또는 이들의 임의의 조합의 단편을 포함하는 서열을 갖는 폴리펩티드, 예를 들면, 적어도 40개의 아<br />
미노산 길이를 갖는 단편 또는 전장 폴리펩티드를 포함할 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 가용성 IL-6, IL-6 수용체 알파, gp130, p38 MAP 키나아제, JAK1,<br />
JAK2, JAK3, SYK, 또는 이들의 임의의 조합을 포함할 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제는 반감기 증가 모이어티(moiety)에 결합될 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 항-IL-6 항체의 투여 이전에 환자의 혈청 CRP 수준을 측정하는 단계, 그<br />
리고 환자의 혈청 CRP 수준이 적어도 대략 5 ㎎/ℓ이면 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체를 투여<br />
하는 단계를 포함할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈청 CRP 수준은 IL-6 길항제 투여후 1주 이내에 대략 5 ㎎/ℓ 미만으로 감소<br />
될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈청 CRP 수준은 IL-6 길항제 투여후 1주 이내에 대략 1 ㎎/ℓ 미만으로 감소<br />
될 수 있다.<br />
본 발명의 한 구체예에서, 치료는 환자의 혈청 CRP 수준에서 연장된 감소를 유발할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈청 CRP 수준은 IL-6 길항제 투여후 대략 1주 이내에 대략 10 ㎎/ℓ 미만으<br />
로 감소될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 14일 시점에, 환자의 혈청 CRP 수준은 대략 10 ㎎/ℓ 미만으로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 21일 시점에, 환자의 혈청 CRP 수준은 대략 10 ㎎/ℓ 미만으로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 28일 시점에, 환자의 혈청 CRP 수준은 대략 10 ㎎/ℓ 미만으로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 35일 시점에, 환자의 혈청 CRP 수준은 대략 10 ㎎/ℓ 미만으로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 42일 시점에, 환자의 혈청 CRP 수준은 대략 10 ㎎/ℓ 미만으로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 49일 시점에, 환자의 혈청 CRP 수준은 대략 10 ㎎/ℓ 미만으로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 56일 시점에, 환자의 혈청 CRP 수준은 대략 10 ㎎/ℓ 미만으로<br />
유지될 수 있다.<br />
본 발명의 한 구체예에서, 환자의 생존력이 개선된다.<br />
본 발명의 한 구체예에서, 상기 방법은 IL-6 길항제의 투여 이전에 환자의 혈청 알부민 수준을 측정하는 단계,<br />
그리고 환자의 혈청 알부민 수준이 대략 35 g/ℓ 이하이면 IL-6 길항제, 예를 들면, Ab1를 투여하는 단계를 포<br />
함할 수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈청 알부민 수준은 IL-6 길항제 투여후 대략 5주 이내에 대략 35 g/ℓ 이상<br />
으로 증가될 수 있다.<br />
본 발명의 한 구체예에서, 치료는 환자의 혈청 알부민 수준에서 연장된 증가를 유발할 수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 42일 시점에, 환자의 혈청 알부민 수준은 35 g/ℓ 초과로 유지될<br />
수 있다.<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 49일 시점에, 환자의 혈청 알부민 수준은 35 g/ℓ 초과로 유지될<br />
수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, IL-6 길항제 투여후 56일 시점에, 환자의 혈청 알부민 수준은 35 g/ℓ 초과로 유지될<br />
- 48 -
[0171]<br />
[0172]<br />
[0173]<br />
[0174]<br />
[0175]<br />
[0176]<br />
[0177]<br />
[0178]<br />
[0179]<br />
[0180]<br />
[0181]<br />
수 있다.<br />
본 발명의 한 구체예에서, 환자의 혈청 알부민 수준은 IL-6 길항제 투여후 대략 5주 이내에 대략 5 g/ℓ 증가될<br />
수 있다.<br />
본 발명의 한 구체예에서, 환자는 류머티스성 관절염, 암, 진행된 암, 간 질환, 신장 질환, 염증성 장 질환, 셀<br />
리악병, 외상, 화상, 감소된 혈청 알부민과 연관된 기타 질환, 또는 이들의 임의의 조합으로 진단될 수 있다.<br />
본 발명의 한 구체예에서, 상기 방법은 아토르바스타틴, 체리바스타틴, 플루바스타틴, 로바스타틴, 메바스타틴,<br />
피타바스타틴, 프라바스타틴, 로수바스타틴, 심바스타틴, 또는 이들의 임의의 조합이 포함되지만 이들에 국한되<br />
지 않는 한 가지 이상의 스타틴을 환자에게 투여하는 단계를 추가로 포함할 수 있다.<br />
본 발명의 또 다른 구체예는 Ab1과 같은 IL-6 길항제, 그리고 항응고제를 포함하는 조성물에 관계한다. 본 발명<br />
의 한 구체예에서, 한 가지 이상의 항응고제는 아브식시맙(ReoPro), 아세노쿠마롤, 항트롬빈 III, 아르가트로<br />
반, 아스피린, 비발리루딘(Angiomax), 클로피도그렐, 다비가트란, 다비가트란 이텍실레이트(Pradaxa/Pradax<br />
), 데시루딘(Revasc/Iprivask), 디피리다몰, 엡티피바티드(Integrilin), 폰다파리눅스, 헤파린,<br />
히루딘, 이드라파리눅스, 레피루딘(Refludan), 저분자량 헤파린, 멜라가트란, 페닌디온, 펜프로코우몬, 티클<br />
로피딘, 티로피반(Aggrastat), 와파린, 지멜라가트란, 지멜라가트란(Exanta/ Exarta), 또는 이들의 임의<br />
의 조합에서 선택될 수 있다.<br />
본 발명의 또 다른 구체예는 Ab1과 같은 IL-6 길항제, 그리고 화학요법제를 포함하는 조성물에 관계한다. 본 발<br />
명의 한 구체예에서, 화학요법제는 VEGF 길항제, EGFR 길항제, 플라틴, 탁솔, 이리노테칸, 5-플루오르우라실,<br />
젬시타빈, 류코보린, 스테로이드, 시클로포스파미드, 멜팔란, 빈카 알칼로이드(가령, 빈블라스틴, 빈크리스틴,<br />
빈데신과 비노렐빈), 무스틴, 티로신 키나아제 저해제, 방사선요법, 성 호르몬 길항제, 선택성 안드로겐 수용체<br />
조절제, 선택성 에스트로겐 수용체 조절제, PDGF 길항제, TNF 길항제, IL-1 길항제, 인터루킨(가령 IL-<strong>12</strong> 또는<br />
IL-2), IL-<strong>12</strong>R 길항제, 독소 접합된 단일클론 항체, 종양 항원 특이적 단일클론 항체, Erbitux, Avastin,<br />
Pertuzumab, 항-CD20 항체, Rituxan<br />
, 오크렐리주맙, 오파투무맙, DXL625, Herceptin<br />
, 또는 이들의 임의의 조합에서 선택될 수 있다.<br />
과제의 해결 수단<br />
상세한 설명<br />
정의<br />
본 발명은 다양한 개변이 가능하기 때문에, 특정 방법, 프로토콜, 세포주, 동물 종 또는 속, 그리고 기술된 반<br />
응물에 한정되지 않는 것으로 이해된다. 또한, 본 명세서에서 이용된 용어는 특정 구체예를 설명하는 것을 목적<br />
으로 하고, 그리고 첨부된 특허청구범위에 의해서만 한정되는 본 발명의 범위를 한정하는 것으로 의도되지 않는<br />
다.<br />
"변이체"(Ab1을 비롯한 항체에 적용됨)에는 단일-쇄 항체, 이합체, 멀티머, 서열 변이체, 도메인 치환 변이체<br />
등이 포함된다. 단일-쇄 항체, 예를 들면, SMIP, 상어 항체, 나노바디(가령, 낙타 항체). 서열 변이체는 동일성<br />
(또는 유사성) 비율, 예를 들면, 99%, 95%, 90%, 85%, 80%, 70%, 60% 등에 의해, 또는 허용되는 보존성 또는<br />
비-보존성 치환의 숫자에 의해 특정될 수 있다. 도메인 치환 변이체에는 관련된 단백질의 유사한 도메인으로 단<br />
백질의 도메인의 치환이 포함된다. 유사한 도메인은 서열, 구조(실제 또는 예측), 또는 기능의 유사성에 의해<br />
확인될 수 있다. 가령, 도메인 치환 변이체에는 하나 이상의 CDR 및/또는 골격 영역의 치환이 포함된다.<br />
본 명세서에서, 단수 형태는 달리 명시되지 않으면, 복수 지시물을 포함한다. 따라서 예로써, "세포"에 대한 지<br />
시는 복수의 세포를 포함하고, 그리고 "단백질"에 대한 지시는 하나 이상의 단백질 및 당업자에게 공지된 이들<br />
의 등가물에 대한 지시를 포함한다. 본 명세서에 이용된 모든 기술 용어와 과학 용어는 달리 명시되지 않으면,<br />
본 발명이 속하는 분야에 평균적인 지식을 가진 자에 의해 통상적으로 이해되는 바와 동일한 의미를 갖는다.<br />
인터루킨-6(IL-6): 본 명세서에서, 인터루킨-6(IL-6)은 GenBank 단백질 수탁 No. NP_000591로서 가용한 아래<br />
의 2<strong>12</strong>개 아미노산 서열:<br />
- 49 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0182]<br />
[0183]<br />
[0184]<br />
[0185]<br />
MNSFSTSAFGPVAFSLGLLLVLPAAFPAPVPPGEDSKDVAAPHRQPLTSSERIDKQIRYILDGISALRKETCNKSNMCESSKEALAENNLNLPKMAEKDGCF<br />
QSGFNEETCLVKIITGLLEFEVYLEYLQNRFESSEEQARAVQMSTKVLIQFLQKKAKNLDAITTPDPTTNASLLTKLQAQNQWLQDMTTHLILRSFKEFLQS<br />
SLRALRQM (서열 번호: 1)뿐만 아니라, 이러한 IL-6 아미노산 서열의 임의의 프리-프로(pre-pro), 프로(pro)-와<br />
성숙 형태, 그리고 이러한 서열의 대립유전자 변이체를 비롯한 돌연변이체와 변이체를 포함한다.<br />
IL-6 길항제: 본 명세서에서, 용어 "IL-6 길항제", 그리고 이의 문법적 변형은 IL-6 신호전달의 효과를 예방하<br />
거나, 저해하거나, 또는 감소시키는 임의의 조성물을 포함한다. 일반적으로, 이런 길항제는 IL-6, IL-6 수용체<br />
알파, gp130, 또는 IL-6 신호 전달에 관여하는 임의의 분자의 수준 또는 활성을 감소시키거나, 또는 이들 사이<br />
에 복합체의 수준 또는 활성(가령, IL-6 / IL-6 수용체 복합체의 활성)을 감소시킬 수 있다. 길항제에는 DNA,<br />
RNA, 또는 핵산 유사체, 예를 들면, 펩티드 핵산, 잠금 핵산, 모르폴리노(포스포로디아미데이트 모르폴리노 올<br />
리고), 글리세롤 핵산, 또는 트레오즈 핵산을 비롯한 안티센스 핵산이 포함된다(참조: Heasman, Dev Biol. 2002<br />
Mar 15;243(2):209-14; Hannon and Rossi, Nature. 2004 Sep 16;431(7006):371-8; Paul et al., Nat<br />
Biotechnol. 2002 May;20(5):505-8; Zhang et al., J Am Chem Soc. 2005 Mar 30;<strong>12</strong>7(<strong>12</strong>):4174-5; Wahlestedt<br />
et al., Proc Natl Acad Sci U S A. 2000 May 9;97(10):5633-8; Hanvey et al., <strong>19</strong>92 Nov 27;258(5087):1481-<br />
5; Braasch et al., Biochemistry. 2002 Apr 9;41(14):4503-10; Schoning et al., Science. 2000 Nov<br />
17;290(5495):1347-51). 이에 더하여, IL-6 길항제에는 특히, IL-6 신호전달을 차단하는 펩티드, 예를 들면,<br />
US 특허 No. 6,599,875; 6,172,042; 6,838,433; 6,841,533; 5,210,075 등 중에서 한 가지에서 기술된 것들이<br />
포함된다. 또한, 본 발명에 따른 IL-6 길항제에는 사이토킨 생산, 더욱 구체적으로 IL-6 생산에서 p38 MAP 키나<br />
아제의 역할을 고려할 때, p38 MAP 키나아제 저해제, 예를 들면, US20070010529 등에서 보고된 것들이 포함될<br />
수 있다. 게다가, 본 발명에 따른 IL-6 길항제에는 US20050090453에서 보고된 글리코알칼로이드 화합물, 그리고<br />
상기 문헌에서 보고된 IL-6 길항제 스크리닝 분석을 이용하여 분리가능한 다른 IL-6 길항제 화합물이 포함된다.<br />
다른 IL-6 길항제에는 본 명세서에 기술된 항-IL-6 항체를 비롯한(하지만 이들에 한정되지 않는) 항체, 예를 들<br />
면, 항-IL-6 항체, 항-IL-6 수용체 알파 항체, 항-gp130 항체, 그리고 항-p38 MAP 키나아제 항체, Actemra<br />
(토클리주맙), Remicade<br />
, Zenapax(다클리주맙), 또는 이들의 임의의 조합이 포함된다. 다른 IL-6 길항제에는 IL-6 신호전달에 관여하<br />
는 분자, 예를 들면, IL-6, IL-6 수용체 알파, 그리고 gp130의 일부분 또는 단편이 포함되고, 이들은 본래의,<br />
돌연변이, 또는 변이 서열일 수 있고, 그리고 선택적으로, 다른 모이어티(가령, 반감기-증가 모이어티, 예를 들<br />
면, Fc 도메인)에 결합될 수 있다. 가령, IL-6 길항제는 가용성 IL-6 수용체 또는 단편, 가용성 IL-6 수용체:Fc<br />
융합 단백질, IL-6의 소분자 저해제, 항-IL-6 수용체 항체 또는 이의 항체 단편 또는 변이체, 안티센스 핵산 등<br />
일 수 있다. 다른 IL-6 길항제에는 아베미르, 예를 들면, C326(Silverman et al., Nat Biotechnol. 2005<br />
Dec;23(<strong>12</strong>):1556-61), 그리고 소분자, 예를 들면, 합성 레티노이드 AM80(타미바로텐)(Takeda et al.,<br />
Arterioscler Thromb Vasc Biol. 2006 May;26(5):1177-83)이 포함된다. 이런 IL-6 길항제는 전술한 폴리펩티드<br />
또는 안티센스 서열을 인코딩하거나, 또는 이들 서열이 발현되도록 하는 핵산과 개체를 접촉시키는 것을 비롯한<br />
당분야에 공지된 임의의 수단에 의해 투여될 수 있다.<br />
혈전증: 본 명세서에서, 혈전증은 혈관 내에 혈전(blood clot)을 지칭한다. 상기 용어는 제한 없이, 심부 정맥<br />
혈전증, 문맥 혈전증, 목 정맥 혈전증, 신장 정맥 혈전증, 뇌졸중, 심근 경색, 버드-키아리 증후군, 파제트-스<br />
크로에터(Paget-Schroetter) 병, 그리고 대뇌 정맥동 혈전증을 비롯한 동맥과 정맥 혈전증을 포함한다. 혈전증<br />
과 연관된 질환과 이상에는 제한 없이, 급성 정맥 혈전증, 폐 색전증, 임신 동안 혈전증, 출혈성 피부 괴사, 급<br />
성 또는 만성 범발성 혈관내 혈액응고(DIC), 수술로부터 응괴 형성, 장기 요양, 장기간의 부동, 정맥 혈전증,<br />
전격성 수막염균 혈증, 급성 혈전성 뇌졸중, 급성 관상동맥 폐쇄증, 급성 말초 동맥 폐쇄증, 광범위 폐 색전증,<br />
액와 정맥 혈전증, 광범위 골대퇴정맥 혈전증, 폐쇄된 동맥 도관, 폐쇄된 정맥 도관, 심근증, 간의 정맥폐쇄성<br />
질환, 저혈압, 감소된 심박출량, 감소된 혈관 저항, 폐 고혈압, 감소된 폐 유순도, 백혈구감소증, 그리고 혈소<br />
판감소증이 포함된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
D-이합체: 본 명세서에서, D-이합체는 플라스민 효소에 의한 혈전의 파괴 동안 생산되는 피브린 분해 산물을 지<br />
칭한다. D-이합체에 대하여 특이적으로 반응하는 단일클론 항체, 예를 들면, DD-3B6/22(Elms et al., <strong>19</strong>86, Am<br />
J Clin Pathol. 85:360-4)는 용이하게 가용하다. D-이합체 수준의 임상적 측정은 예로써, 적혈구 응집 검사,<br />
ELISA 등을 이용하여 일과적으로 수행된다(Dempfle, Semin Vasc Med, 2005 Nov;5(4):315-20에서 검토됨). D-이<br />
합체의 치수는 측정 방법과 검사 실험실에 따라 달라질 수 있다; 그럼에도 불구하고, 정상적인 "참고 범위<br />
(reference range)"는 예로써, 건강한 개체로부터 치수를 획득함으로써, 임의의 특정 방법과 검사 실험실에 대<br />
하여 용이하게 확립될 수 있다. 따라서 상승된 D-이합체 수준은 당업자에 의해, 특정 방법과 검사 실험실에 대<br />
- 50 -
[0186]<br />
[0187]<br />
[0188]<br />
[0189]<br />
한 참고 범위를 초과하는 D-이합체 수준을 지칭하는 것으로 이해된다.<br />
혈액응고 프로필: 본 명세서에서, 혈액응고 프로필은 일반적으로, 혈액응고 체계의 기능을 지칭한다. 응고의 조<br />
직 인자(외적)와 접촉 활성화(내적) 경로는 혈액응고 프로필의 구성요소이다. 정상적인 혈액응고 프로필은 정상<br />
적인 건강한 개체에서처럼 기능하는 혈액응고, 다시 말하면, 출혈을 제어하는 능력 및 과도한 응고 성향<br />
(thrombotic tendency) 사이에 균형 유지를 지칭한다. 비정상적인 혈액응고 프로필은 혈액응고 성향에서 감소<br />
또는 증가일 수 있다. 한 가지 특히 비정상적인 혈액응고 프로필은 과혈액응고인데, 이는 과도한 응괴 형성의<br />
매우 증가된 위험을 지칭하고 혈전증의 높은 위험을 유발한다. 혈액응고 프로필은 당분야에 공지된 다양한 검사<br />
법과 분석법, 예를 들면: 활성화된 부분 트롬보플라스틴 시간(aPTT) 검사법; 프로트롬빈 시간(PT) 검사법(<strong>12</strong> 내<br />
지 15초의 전형적인 참고 범위); PT 검사법으로부터 도출된 치수, 예를 들면, 프로트롬빈 비율(PR)과 국제 표준<br />
화 비율(INR)(0.8 내지 1.2의 전형적인 참고 범위); 피브리노겐 검사법(가령, Clauss 방법(Clauss A, "Rapid<br />
Physiological Coagulation Method for the Determination of Fibrinogen [German],"Acta Haematol, <strong>19</strong>57,<br />
17:237-46) 또는 Ellis 방법(Ellis BC and Stransky A, "A Quick and Accurate Method for the Determination<br />
of Fibrinogen in Plasma,"J Lab Clin Med, <strong>19</strong>61, 58:477-88); 활성화된 단백질 C 저항, 단백질 C, 단백질 S,<br />
그리고 항트롬빈에 대한 분석법; 항인지질 항체(루푸스 항응고제와 항카르디오리핀 항체)에 대한 분석법; 상승<br />
된 호모시스틴; 플라스미노겐, 이상피브리노겐혈증, 헤파린 보조인자 II, 또는 혈소판 과응집능에 대한 분석법<br />
에 의해 평가될 수 있다. 혈액응고 프로필을 평가하는데 유용한 다른 분석법에는 응고 인자 및/또는 응고의 지<br />
시자, 예를 들면, D-이합체, 인자 II, 인자 V, 인자 VIII, 인자 IX, 인자 XI, 인자 XII, F/피브린 분해 산물,<br />
트롬빈-항트롬빈 III 복합체, 혈소판증가증, 피브리노겐, 플라스미노겐, 프로트롬빈, 그리고 폰 빌레브란드 인<br />
자의 혈청 수준의 측정이 포함된다. 혈액응고 프로필에서 악화는 정상적인 혈액응고 성향의 악화, 다시 말하면,<br />
측정된 값이 비정상적으로 되거나, 또는 이전보다 정상적인 범위로부터 더욱 벗어나는 것을 반영하는 혈액응고<br />
의 지시자, 예를 들면, 전술한 임의의 분석법에서 측정가능한 변화를 지칭한다. 혈액응고 프로필에서 개선은 정<br />
상적인 혈액응고 성향의 부분적인 또는 완전한 회복, 다시 말하면, 치료적 개입(therapeutic intervention), 예<br />
를 들면, 항-IL-6 항체의 투여후, 측정된 값이 정상적인 범위에 있거나, 또는 치료적 개입 이전보다 정상적인<br />
범위에 더욱 근접하는 것을 반영하는 혈액응고의 지시자, 예를 들면, 전술한 임의의 분석법에서 측정가능한 변<br />
화를 지칭한다.<br />
질환 또는 이상: 본 명세서에서, "질환 또는 이상"은 환자가 진단되었거나, 또는 앓고 있는 것으로 의심되는<br />
질환 또는 이상, 특히 상승된 IL-6과 연관된 질환 또는 이상을 지칭한다. 질환 또는 이상은 제한 없이, 약제 또<br />
는 치료(가령, 방사선요법)의 부작용, 그리고 상승된 IL-6을 수반하는 증상으로 특징되는 특발성 이상을 포함한<br />
다.<br />
악액질: 본 명세서에서, 악액질(일명, 소모성 질환)은 특히, 진행성 여윔, 쇠약, 전반적으로 나쁜 건강, 영양<br />
실조, 체질량(body mass)의 감소, 근육량(muscle mass)의 감소, 또는 만성 염증 반응의 배경에서 골격근의 가속<br />
화된 상실로 특징되는 임의의 질환을 지칭한다(Kotler, Ann Intern Med. 2000 Oct 17;133(8):622-34에서 재검<br />
토됨). 악액질이 빈번하게 관찰되는 질환과 이상에는 암, 류머티스성 관절염, AIDS, 심장 질환, 탈수,<br />
영양실조, 납 노출, 말라리아, 호흡 질환, 노령, 갑상선 기능저하증, 결핵, 뇌하수체 저하증, 신경쇠약, 고나트<br />
륨혈증, 저나트륨혈증, 신장 질환, 지라동맥, 강직성 척추염, 성장 실패(부진한 성장) 및 기타 질환, 특히 만성<br />
질환이 포함된다. 악액질은 또한, 특발성(불명의 원인으로부터 발생함)일 수 있다. 환자에서 체중 평가는 종양<br />
또는 수액 축적, 예를 들면, 종양 중량, 혈관외액 축적 등을 제외하는 것으로 이해된다. 악액질은 환자의 총 체<br />
질량(종양 또는 수액 축적 제외), 총 제지방량(지방-없음), 팔과 다리의 마른 질량(부속지 마른 질량, 예로써<br />
이중-에너지 x-선 흡수계측 또는 생체전기 저항 분광법(bioelectric impedance spectroscopy)을 이용하여 측정<br />
됨), 및/또는 제지방량 지수(환자 키의 제곱으로 나눗셈된 제지방량)의 측정에 의해 평가될 수 있다(참조:<br />
Kotler, Ann Intern Med. 2000 Oct 17;133(8):622-34; Marcora et al., Rheumatology (Oxford). 2006<br />
Nov;45(11):1385-8).<br />
쇠약: 본 명세서에서, 쇠약은 전형적으로, 근력 및/또는 근지구력의 상실로서 나타나는 신체 피로를 지칭한다.<br />
쇠약은 중심적(체내에서 대부분 또는 모든 근육에 영향을 준다) 또는 주변적(근육의 부분집합에 영향을 준다)일<br />
수 있다. 쇠약에는 환자의 근육이 피크 및/또는 지속된 힘 출력의 일부 치수에서 감소하는 "진정 쇠약", 그리고<br />
환자가 객관적으로 측정된 체력이 거의 동일하게 유지되지만 과제의 수행을 위하여 더욱 많은 노력이 요구된다<br />
는 것을 감지하는 "감지 쇠약"이 포함되고, 그리고 객관적으로 측정되거나, 또는 환자에 의해 자가-보고될 수<br />
있다. 가령, 쇠약은 전형적으로 악력계를 이용하는 손 악력 검사(근력을 평가하기 위한 의학적으로 인정된 검사<br />
법)에 의해, 객관적으로 측정될 수 있다.<br />
- 51 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0<strong>19</strong>0]<br />
[0<strong>19</strong>1]<br />
[0<strong>19</strong>2]<br />
[0<strong>19</strong>3]<br />
[0<strong>19</strong>4]<br />
[0<strong>19</strong>5]<br />
[0<strong>19</strong>6]<br />
피로: 본 명세서에서, 피로는 정신적 피로를 지칭한다(신체 피로는 "쇠약"을 참조). 피로에는 졸음<br />
(somnolence) 및/또는 감소된 집중력이 포함된다. 피로는 당분야에 공지된 다양한 검사법, 예를 들면, FACIT-<br />
F(만성 질환 치료의 기능적 평가-피로) 검사법을 이용하여 측정될 수 있다(참조: Cella, D., Lai, J.S., Chang,<br />
C.H., Peterman, A., & Slavin, M. (2002). Fatigue in cancer patients compared with fatigue in the<br />
general population. Cancer, 94(2), 528-538; Cella, D., Eton, D.T., Lai,F J-S., Peterman, A.H & Merkel,<br />
D.E. (2002). Combining anchor and distribution based methods to derive minimal clinically important<br />
differences on the Functional Assessment of Cancer Therapy anemia and fatigue scales. Journal of Pain<br />
& Symptom Management, 24 (6) 547-561).<br />
발열: 본 명세서에서, "발열"은 적어도 섭씨 1 내지 2도 상승된 체온 설정점(body temperature set-point)을<br />
지칭한다. 발열은 종종, 한기, 떨림, 증가된 심장박동, 그리고 개체의 신체가 증가된 설정점에 도달하는 호흡<br />
속도로 나타나는 저체온의 주관적 감정과 연관된다. 의학 분야에서 널리 인지되는 바와 같이, 정상적인 체온은<br />
전형적으로, 활동 수준 및 하루중 시간에 따라 변하는데, 최고 온도가 오후와 초저녁 시간에 관찰되고, 그리고<br />
최저 온도가 수면 주기(sleep cycle)의 후반 동안 관찰되고, 그리고 온도 측정은 외부 인자, 예를 들면, 구강<br />
호흡(mouth breathing), 식품 또는 음료의 소비, 흡연, 또는 실온(측정의 유형에 따라)에 의해 영향을 받을 수<br />
있다. 더욱이, 개체에 대한 정상적인 온도 설정점은 대략 섭씨 0.5도까지 변할 수 있고, 따라서 의료 전문가는<br />
발열이 존재하는 지를 진단하기 위하여 이들 인자에 비추어 개체의 온도를 해석할 수 있다. 일반적으로 말하면,<br />
발열은 전형적으로, 섭씨 38.0도 초과의 중심 체온(core body temperature), 섭씨 37.5도 초과의 구강 체온<br />
(oral temperature), 또는 섭씨 37.2도 초과의 겨드랑이 체온(axillary temperature)으로 진단된다.<br />
개선된: 본 명세서에서, "개선된", "개선" 및 다른 문법적 변형은 치료에 기인하는 임의의 유익한 변화를 포함<br />
한다. 유익한 변화는 치료가 부재할 때보다 환자의 상태가 나아지는 임의의 변화이다. "개선된"은 원치 않는 이<br />
상의 예방, 이상이 악화되는 속도의 늦춤, 원치 않는 이상의 발달 지연, 그리고 본질적으로 정상적인 상태로의<br />
회복이 포함한다. 가령, 악액질에서 개선은 환자의 질량, 예를 들면, 총 체질량(악액질의 평가 동안 정상적으로<br />
제외되는 중량, 가령 종양 중량, 혈관외액 축적 등 제외), 제지방량, 및/또는 부속지 마른 질량에서 증가, 그리<br />
고 질량 상실의 속도의 지연 또는 늦춤, 또는 환자가 진단된 질환 또는 이상과 연관된 질량 상실의 예방 또는<br />
늦춤을 포함한다. 다른 실례에서, 쇠약에서 개선은 환자의 체력 증가, 그리고 체력 상실의 속도에서 지연 또는<br />
늦춤, 또는 환자가 진단된 질환 또는 이상과 연관된 체력 상실의 예방 또는 늦춤을 포함한다. 또 다른<br />
실례에서, 피로에서 개선은 환자의 피로에서 감소, 그리고 피로 증가의 속도에서 지연 또는 늦춤, 또는 환자가<br />
진단된 질환 또는 이상과 연관된 피로 증가의 예방 또는 늦춤을 포함한다. 또 다른 실례에서, 발열에서 개선은<br />
환자의 발열에서 감소, 그리고 발열 증가의 속도에서 지연 또는 늦춤, 또는 환자가 진단된 질환 또는 이상과 연<br />
관된 발열 증가의 예방 또는 늦춤을 포함한다.<br />
C-반응성 단백질(CRP): 본 명세서에서, C-반응성 단백질(CRP)은 GenBank 단백질 수탁 No. NP_000558로서 가용<br />
한 아래의 224개 아미노산 서열:<br />
MEKLLCFLVLTSLSHAFGQTDMSRKAFVFPKESDTSYVSLKAPLTKPLKAFTVCLHFYTELSSTRGYSIFSYAT<strong>KR</strong>QDNEILIFWSKDIGYSFTVGGSEILF<br />
EVPEVTVAPVHICTSWESASGIVEFWVDGKPRVRKSLKKGYTVGAEASIILGQEQDSFGGNFEGSQSLVGDIGNVNMWDFVLSPDEINTIYLGGPFSPNVLN<br />
WRALKYEVQGEVFTKPQLWP (서열 번호: 726)뿐만 아니라, 이러한 CRP 아미노산 서열의 임의의 프리-프로(pre-pro),<br />
프로(pro)-와 성숙 형태, 그리고 이러한 서열의 대립유전자 변이체를 비롯한 돌연변이체와 변이체를 포함한다.<br />
예로써, 혈청, 간, 종양, 또는 신체의 다른 부위에서 CRP 수준은 일과적인 방법 및 상업적으로 가용한 시약, 예<br />
를 들면, ELISA, 항체 스트립 검사법, 면역혼탁법, 급속 면역확산법, 시각적 응집, 웨스턴 블롯, 노던 블롯 등<br />
을 이용하여 용이하게 측정될 수 있다. 앞서 언급된 바와 같이, CRP 수준은 본 발명에 따라서 혈전증이 발병했<br />
거나 발병할 위험이 있는 환자에서도 측정될 수 있다.<br />
인터루킨-6 수용체(IL-6R); 일명 IL-6 수용체 알파(IL-6RA): 본 명세서에서, "인터루킨-6 수용체"("IL-6R";<br />
또한 "IL-6 수용체 알파" 또는 "IL-6RA")는 Swiss-Prot 단백질 수탁 No. P08887로서 가용한 아래의 468개 아미<br />
노산 서열:<br />
공개특허 10-2011-01<strong>12</strong>308<br />
MLAVGCALLAALLAAPGAALAPRRCPAQEVARGVLTSLPGDSVTLTCPGVEPEDNATVHWVLRKPAAGSHPSRWAGMGRRLLLRSVQLHDSGNYSCYRAGRP<br />
AGTVHLLVDVPPEEPQLSCFRKSPLSNVVCEWGPRSTPSLTTKAVLLVRKFQNSPAEDFQEPCQYSQESQKFSCQLAVPEGDSSFYIVSMCVASSVGSKFSK<br />
TQTFQGCGILQPDPPANITVTAVARNPRWLSVTWQDPHSWNSSFYRLRFELRYRAERSKTFTTWMVKDLQHHCVIHDAWSGLRHVVQLRAQEEFGQGEWSEW<br />
SPEAMGTPWTESRSPPAENEVSTPMQALTTNKDDDNILFRDSANATSLPVQDSSSVPLPTFLVAGGSLAFGTLLCIAIVLRFKKTWKLRALKEGKTSMHPPY<br />
SLGQLVPERPRPTPVLVPLISPPVSPSSLGSDNTSSHNRPDARDPRSPYDISNTDYFFPR (서열 번호: 727)뿐만 아니라, 이러한 아미노<br />
- 52 -
[0<strong>19</strong>7]<br />
[0<strong>19</strong>8]<br />
[0<strong>19</strong>9]<br />
[0200]<br />
[0201]<br />
산 서열의 임의의 프리-프로(pre-pro), 프로(pro)-와 성숙 형태, 그리고 이러한 서열의 대립유전자 변이체를 비<br />
롯한 돌연변이체와 변이체를 포함한다.<br />
gp130: 본 명세서에서, gp130(일명 인터루킨-6 수용체 아단위 베타)은 Swiss-Prot 단백질 수탁 No. P40189로<br />
서 가용한 아래의 918개 전구 아미노산 서열:<br />
MLTLQTWVVQALFIFLTTESTGELLDPCGYISPESPVVQLHSNFTAVCVLKEKCMDYFHVNANYIVWKTNHFTIPKEQYTIINRTASSVTFTDIASLNIQLT<br />
CNILTFGQLEQNVYGITIISGLPPEKPKNLSCIVNEGKKMRCEWDGGRETHLETNFTLKSEWATHKFADCKA<strong>KR</strong>DTPTSCTVDYSTVYFVNIEVWVEAENAL<br />
GKVTSDHINFDPVYKVKPNPPHNLSVINSEELSSILKLTWTNPSIKSVIILKYNIQYRTKDASTWSQIPPEDTASTRSSFTVQDLKPFTEYVFRIRCMKEDG<br />
KGYWSDWSEEASGITYEDRPSKAPSFWYKIDPSHTQGYRTVQLVWKTLPPFEANGKILDYEVTLTRWKSHLQNYTVNATKLTVNLTNDRYLATLTVRNLVGK<br />
SDAAVLTIPACDFQATHPVMDLKAFPKDNMLWVEWTTPRESVKKYILEWCVLSDKAPCITDWQQEDGTVHRTYLRGNLAESKCYLITVTPVYADGPGSPESI<br />
KAYLKQAPPSKGPTVRTKKVGKNEAVLEWDQLPVDVQNGFIRNYTIFYRTIIGNETAVNVDSSHTEYTLSSLTSDTLYMVRMAAYTDEGGKDGPEFTFTTPK<br />
FAQGEIEAIVVPVCLAFLLTTLLGVLFCFN<strong>KR</strong>DLIKKHIWPNVPDPSKSHIAQWSPHTPPRHNFNSKDQMYSDGNFTDVSVVEIEANDKKPFPEDLKSLDLF<br />
KKEKINTEGHSSGIGGSSCMSSSRPSISSSDENESSQNTSSTVQYSTVVHSGYRHQVPSVQVFSRSESTQPLLDSEERPEDLQLVDHVDGGDGILPRQQYFK<br />
QNCSQHESSPDISHFERSKQVSSVNEEDFVRLKQQISDHISQSCGSGQMKMFQEVSAADAFGPGTEGQVERFETVGMEAATDEGMPKSYLPQTVRQGGYMPQ<br />
(서열 번호: 728)뿐만 아니라, 이러한 아미노산 서열의 임의의 프리-프로(pre-pro), 프로(pro)-와 성숙 형태,<br />
예를 들면, 도시된 서열의 23번 내지 918번 아미노산에 의해 인코딩된 성숙 형태, 그리고 이러한 서열의 대립유<br />
전자 변이체를 비롯한 돌연변이체와 변이체를 포함한다.<br />
Glasgow 예후 점수(GPS): 본 명세서에서, Glasgow 예후 점수(GPS)는 < 35 ㎎/ℓ 미만의 혈청 알부민 수준에<br />
대하여 1 점, 그리고 10 ㎎/ℓ 초과의 CRP 수준에 대하여 1 점을 부과하는 염증-기초된 예후 점수를 지칭한다.<br />
따라서 0의 GPS는 정상적인 알부민과 CRP를 지시하고, 1의 GPS는 감소된 알부민 또는 상승된 CRP를 지시하고,<br />
그리고 2의 GPS는 감소된 알부민 및 상승된 CRP 둘 모두를 지시한다.<br />
효과량: 본 명세서에서, "효과량", "효과적인 양", "효과적인 X의 양" 등은 투여되면 치료가 필요한 질환의 한<br />
가지 이상의 증상을 다소간 경감하거나 감소시키고, 또는 예방이 필요한 질환의 임상적 마커 또는 증상의 개시<br />
를 지연시키는데 효과적인 활성 성분의 양을 지칭한다. 따라서 효과량은 예로써, (i) 질환의 진행 속도를 역진<br />
시키고; (ii) 질환의 진행을 다소간 저해하고; 및/또는, (iii) 질환과 연관된 한 가지 이상의 증상을 다소간 경<br />
감하는(또는, 바람직하게는 제거하는) 효과를 나타내는 활성 성분의 양을 지칭한다. 효과량은 치료가 필요한 질<br />
환에 대한 공지된 생체내와 시험관내 모형 시스템에서 관련된 화합물로 실험함으로써 경험적으로 결정될 수 있<br />
다. 구(句) "효과량"이 이용되는 문맥은 특정한 소요 효과를 지시할 수 있다. 가령, "과혈액응고 상태를 예방하<br />
거나 치료하는데 효과적인 항-IL-6 항체의 양" 및 유사한 구(句)는 개체에 투여될 때, 개체의 혈액응고 프로필<br />
에서 측정가능한 개선을 유발하거나, 또는 개체가 위험에 처해있는 혈액응고 프로필의 악화를 예방하거나, 늦추<br />
거나, 지연시키거나, 또는 중지시키는 항-IL-6 항체의 양을 지칭한다. 유사하게, "혈청 CRP 수준을 감소시키는<br />
데 효과적인 항-IL-6 항체의 양" 및 유사한 구(句)는 개체에 투여될 때, 혈청 CRP 수준에서 측정가능한 감소를<br />
유발하거나, 또는 개체에서 위험한 혈청 CRP 수준 증가를 예방하거나, 늦추거나, 지연시키거나, 또는 억제하는<br />
항-IL-6 항체의 양을 지칭한다. 유사하게, "혈청 알부민 수준을 증가시키는데 효과적인 항-IL-6 항체의 양" 및<br />
유사한 구(句)는 개체에 투여될 때, 혈청 알부민 수준에서 측정가능한 증가를 유발하거나, 또는 개체에서 위험<br />
한 혈청 알부민 수준 감소를 예방하거나, 늦추거나, 지연시키거나, 또는 억제하는 항-IL-6 항체의 양을 지칭한<br />
다. 유사하게, "쇠약을 감소시키는데 효과적인 항-IL-6 항체의 양" 및 유사한 구(句)는 개체에 투여될 때, 손<br />
악력 검사에 의한 측정에서 쇠약에서 측정가능한 감소를 유발하는 항-IL-6 항체의 양을 지칭한다. 유사하게, "<br />
체중을 증가시키는데 효과적인 항-IL-6 항체의 양" 및 유사한 구(句)는 개체에 투여될 때, 환자의 체중에서 측<br />
정가능한 증가를 유발하는 항-IL-6 항체의 양을 지칭한다. 효과량은 개체의 체중, 연령, 성별과 병력, 그리고<br />
환자 상태의 심각도, 질환의 유형, 투여 방식 등에 따라 달라질 것이다. 효과량은 가령, 적정(효과량이 확인될<br />
때까지 증가하는 용량의 투여)에 의해 및/또는 이전 환자에 효과적이었던 양을 참고함으로써, 일과적인 실험을<br />
이용하여 용이하게 결정될 수 있다. 일반적으로, 본 발명의 항-IL-6 항체는 환자의 체중의 대략 0.1 ㎎/㎏ 내지<br />
대략 20 ㎎/㎏ 범위의 용량으로 투여될 것이다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
혈액응고 프로필에서 연장된 개선: 본 명세서에서, "혈액응고 프로필에서 연장된 개선" 및 유사한 구(句)는 치<br />
료(가령, IL-6 길항제, 예를 들면, Ab1의 투여)가 시작된 때부터 대략 1주 이내에 검출가능하고, 그리고 치료가<br />
시작된 때부터 연장된 기간, 예를 들면, 적어도 대략 14일, 적어도 대략 21일, 적어도 대략 28일, 적어도 대략<br />
35일, 적어도 대략 40일, 적어도 대략 50일, 적어도 대략 60일, 적어도 대략 70일, 적어도 대략 11주, 또는 적<br />
어도 대략 <strong>12</strong>주 동안 개선된 상태로 유지되는, 최초 혈액응고 프로필(즉, 치료가 시작되기 이전의 시점에서 혈<br />
- 53 -
[0202]<br />
[0203]<br />
[0204]<br />
[0205]<br />
[0206]<br />
[0207]<br />
[0208]<br />
[0209]<br />
액응고 프로필)에 비하여 개체의 혈액응고 프로필에서 측정가능한 개선을 지칭한다.<br />
혈청 CRP에서 연장된 감소: 본 명세서에서, "혈청 CRP에서 연장된 감소" 및 유사한 구(句)는 치료(가령, 항-<br />
IL-6 항체의 투여)가 시작된 때로부터 대략 1주 이내에 검출가능하고 연장된 지속 기간, 예를 들면, 치료가 시<br />
작된 때로부터 적어도 대략 14일, 적어도 대략 21일, 적어도 대략 28일, 적어도 대략 35일, 적어도 대략 40일,<br />
적어도 대략 50일, 적어도 대략 60일, 적어도 대략 70일, 적어도 대략 11주, 또는 적어도 대략 <strong>12</strong>주 동안 초기<br />
혈청 CRP 수준 미만으로 유지되는, 초기 혈청 CRP 수준(즉, 치료가 시작되기 이전의 시점에서 혈청 CRP 수준)에<br />
비하여 혈청 CRP 수준에서 측정가능한 감소를 지칭한다.<br />
혈청 알부민에서 연장된 증가: 본 명세서에서, "혈청 알부민에서 연장된 증가" 및 유사한 구(句)는 치료(가령,<br />
항-IL-6 항체의 투여)가 시작된 때로부터 대략 1주 이내에 검출가능하고 연장된 지속 기간, 예를 들면, 치료가<br />
시작된 때로부터 적어도 대략 14일, 적어도 대략 21일, 적어도 대략 28일, 적어도 대략 35일, 적어도 대략<br />
40일, 적어도 대략 50일, 적어도 대략 60일, 적어도 대략 70일, 적어도 대략 11주, 또는 적어도 대략 <strong>12</strong>주 동안<br />
초기 혈청 알부민 수준 초과로 유지되는, 초기 혈청 알부민 수준(즉, 치료가 시작되기 이전의 시점에서 혈청 알<br />
부민 수준)에 비하여 혈청 알부민 수준에서 측정가능한 증가를 지칭한다.<br />
악액질에서 연장된 개선: 본 명세서에서, "악액질에서 연장된 개선"은 치료가 시작된 때로부터 대략 4주 이내에<br />
검출가능하고 연장된 지속 기간, 예를 들면, 적어도 대략 35일, 적어도 대략 40일, 적어도 대략 50일, 적어도<br />
대략 60일, 적어도 대략 70일, 적어도 대략 11주, 또는 적어도 대략 <strong>12</strong>주 동안 개선된 상태로 유지되는, 초기<br />
수준(즉, 치료가 시작되기 이전의 시점에서 수준)에 비하여 환자의 체질량, 제지방량, 부속지 제지방량, 및/또<br />
는 제지방량 지수에서 측정가능한 개선을 지칭한다.<br />
쇠약에서 연장된 개선: 본 명세서에서, "쇠약에서 연장된 개선"은 치료가 시작된 때로부터 대략 2주 이내에 검<br />
출가능하고 연장된 지속 기간, 예를 들면, 적어도 대략 21일, 적어도 대략 28일, 적어도 대략 35일, 적어도 대<br />
략 40일, 적어도 대략 50일, 적어도 대략 60일, 적어도 대략 70일, 적어도 대략 11주, 또는 적어도 대략 <strong>12</strong>주<br />
동안 개선된 상태로 유지되는, 초기 수준(즉, 치료가 시작되기 이전의 시점에서 수준)에 비하여 근력에서 측정<br />
가능한 개선을 지칭한다.<br />
피로에서 연장된 개선: 본 명세서에서, "피로에서 연장된 개선"은 치료가 시작된 때로부터 대략 1주 이내에 검<br />
출가능하고 연장된 지속 기간, 예를 들면, 적어도 대략 14일, 적어도 대략 21일, 적어도 대략 28일, 적어도 대<br />
략 35일, 적어도 대략 40일, 적어도 대략 50일, 적어도 대략 60일, 적어도 대략 70일, 적어도 대략 11주, 또는<br />
적어도 대략 <strong>12</strong>주 동안 개선된 상태로 유지되는, 초기 수준(즉, 치료가 시작되기 이전의 시점에서 수준)에 비하<br />
여 피로에서 측정가능한 개선을 지칭한다.<br />
발열에서 연장된 개선: 본 명세서에서, "발열에서 연장된 개선"은 치료가 시작된 때로부터 대략 1주 이내에 검<br />
출가능하고 연장된 지속 기간, 예를 들면, 적어도 대략 14일, 적어도 대략 21일, 적어도 대략 28일, 적어도 대<br />
략 35일, 적어도 대략 40일, 적어도 대략 50일, 적어도 대략 60일, 적어도 대략 70일, 적어도 대략 11주, 또는<br />
적어도 대략 <strong>12</strong>주 동안 개선된 상태로 유지되는, 초기 수준(즉, 치료가 시작되기 이전의 시점에서 수준)에 비하<br />
여 발열(가령, 피크 온도 또는 온도가 상승되는 시간의 양)에서 측정가능한 감소를 지칭한다.<br />
교배 적격성 효모 종: 본 발명에서, 이는 배양에서 성장될 수 있는 임의의 2배체 또는 4배체 효모를 폭넓게 포<br />
함하는 것으로 의도된다. 효모의 이런 종은 반수체, 2배체, 또는 4배체 형태로 존재할 수 있다. 소정의 배수성<br />
의 세포는 적절한 조건 하에, 상기 형태로 무제한의 세대 동안 증식할 수 있다. 2배체 세포는 또한, 포자를 형<br />
성하여 반수체 세포를 형성할 수 있다. 순차적 교배는 2배체 균주의 추가 교배 또는 융합을 통하여 4배체 균주<br />
를 산출할 수 있다. 본 발명에서, 2배체 또는 배수체 효모 세포는 바람직하게는, 교배 또는 스페로플라스트 융<br />
합에 의해 생산된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 교배 적격성 효모는 아릭시오지마(Arxiozyma) 속; 아스코보트리오지마<br />
(Ascobotryozyma) 속; 시테로마이세스(Citeromyces) 속; 데바리오마이세스(Debaryomyces) 속; 덱케라(Dekkera)<br />
속; 에레모세시움(Eremothecium) 속; 이사첸키아(Issatchenkia) 속; 카자크스타니아(Kazachstania) 속; 클루이<br />
베로마이세스(Kluyveromyces) 속; 코다메아(Kodamaea) 속; 로드데로마이세스(Lodderomyces) 속; 파치솔렌<br />
(Pachysolen) 속; 피치아(Pichia) 속; 사카로마이세스(Saccharomyces) 속; 사투르니스포라(Saturnispora) 속;<br />
테트라피시스포라(Tetrapisispora) 속; 토룰라스포라(Torulaspora) 속; 윌리오프시스(Williopsis) 속; 그리고<br />
지고사카로마이세스(Zygosaccharomyces) 속을 비롯한 효모균(Saccharomycetaceae) 과(科)의 구성원이다. 본 발<br />
명에 잠재적으로 유용한 다른 유형의 효모에는 야로위아(Yarrowia), 로도스포리듐(Rhodosporidium), 칸디다<br />
- 54 -
[0210]<br />
[0211]<br />
[02<strong>12</strong>]<br />
[0213]<br />
[0214]<br />
[0215]<br />
[0216]<br />
[0217]<br />
[0218]<br />
[02<strong>19</strong>]<br />
(Candida), 한세눌라(Hansenula), 필로바슘(Filobasium), 필로바시델라(Filobasidellla), 스포리디오볼루스<br />
(Sporidiobolus), 불레라(Bullera), 류코스포리듐(Leucosporidium)과 필로바시델라(Filobasidella)가<br />
포함된다.<br />
본 발명의 바람직한 구체예에서, 교배 적격성 효모는 피치아(Pichia) 속의 구성원이다. 본 발명의 더욱 바람직<br />
한 구체예에서, 피치아(Pichia) 속의 교배 적격성 효모는 아래의 종: 피치아 파스토리스(Pichia pastoris), 피<br />
치아 메타놀리카(Pichia methanolica), 그리고 한세눌라 폴리모르파(Hansenula polymorpha)(Pichia angusta)<br />
중에서 한 가지이다. 본 발명의 특히 바람직한 구체예에서, 피치아(Pichia) 속의 교배 적격성 효모는 피치아 파<br />
스토리스(Pichia pastoris) 종이다.<br />
반수체 효모 세포: 정상적인 게놈(염색체) 보체의 각 유전자의 단일 사본을 보유하는 세포.<br />
배수체 효모 세포: 정상적인 게놈(염색체) 보체의 하나 이상의 사본을 보유하는 세포.<br />
2배체 효모 세포: 전형적으로, 2개의 반수체 세포의 융합(교배) 과정에 의해 형성되는, 정상적인 게놈 보체의<br />
본질적으로 모든 유전자의 2개 사본(대립유전자)을 보유하는 세포.<br />
4배체 효모 세포: 전형적으로, 2개의 반수체 세포의 융합(교배) 과정에 의해 형성되는, 정상적인 게놈 보체의<br />
본질적으로 모든 유전자의 4개 사본(대립유전자)을 보유하는 세포. 4배체는 2개, 3개, 4개, 또는 그 이상의 상<br />
이한 발현 카세트를 보유할 수 있다. 이런 4배체는 선택성 교배 동형접합성 자웅이주 a/a와 알파/알파 2배체에<br />
의해 사카로마이세스 세레비지애(S. cerevisiae)에서, 그리고 영양요구성 2배체를 획득하는 반수체의 순차적 교<br />
배에 의해 피치아(Pichia)에서 획득될 수도 있다. 가령, [met his] 반수체는 2배체 [his]를 획득하기 위하여<br />
[ade his] 반수체와 교배될 수 있다; 그리고 [met arg] 반수체는 2배체 [arg]를 획득하기 위하여 [ade arg] 반<br />
수체와 교배될 수 있다; 이후, 이들 2배체 [his] x 2배체 [arg]로 4배체 독립영양체가 획득된다. 당업자가 인지<br />
하는 바와 같이, 2배체 세포의 이익과 효용에 대한 지시는 4배체 세포에도 적용될 수 있다.<br />
효모 교배: 2개의 반수체 효모 세포가 자연적으로 융합하여 1개의 2배체 효모 세포를 형성하는 과정.<br />
감수분열: 2배체 효모 세포가 감소성 분열을 겪고 4개의 반수체 포자 산물을 형성하는 과정. 각 포자는 이후,<br />
발아하고 반수체 무성적 성장 세포주를 형성한다.<br />
선별가능 마커: 선별가능 마커는 예로써, 형질전환 현상을 통하여, 상기 유전자를 수용하는 세포 상에 성장 표<br />
현형(물리적 성장 특징)을 공여하는 유전자 또는 유전자 단편이다. 선별가능 마커는 이러한 선별가능 마커 유전<br />
자를 수용하지 못한 세포가 성장할 수 없는 조건 하에, 상기 세포가 선택성 성장 배지 내에서 생존하고 성장할<br />
수 있도록 한다. 선별가능 마커 유전자는 일반적으로, 양성 선별가능 마커 유전자, 예를 들면, 2개의 ts 돌연변<br />
이체가 교배되거나, 또는 하나의 ts 돌연변이체가 형질전환될 때 항생제 또는 다른 약물, 온도에 대한 내성을<br />
세포에 공여하는 유전자; 음성 선별가능 마커 유전자, 예를 들면, 생합성 유전자를 보유하지 못한 모든 세포에<br />
의해 요구되는 특정 영양소 없이 배지 내에서 성장하는 능력을 세포에 공여하는 생합성 유전자, 또는 야생형 유<br />
전자를 보유하지 못한 세포에 의한 성장 무능력을 세포에 공여하는 돌연변이된 생합성 유전자; 등을 비롯한 여<br />
러 유형으로 나눠진다. 적절한 마커에는 ZEO; G418; LYS3; MET1; MET3a; ADE1; ADE3; URA3; 등이 포함되지만<br />
이들에 국한되지 않는다.<br />
발현 벡터: 이들 DNA 벡터는 표적 숙주 세포 내에서 외래 단백질의 발현을 위한 조작을 용이하게 하는 요소를<br />
포함한다. 편의하게, 서열의 조작 및 형질전환을 위한 DNA의 생산은 먼저, 세균 숙주, 예를 들면, 대장균(E.<br />
coli)에서 수행되고, 그리고 통상적으로, 벡터는 세균 복제 기점 및 적절한 세균 선별 마커를 비롯하여, 이런<br />
조작을 용이하게 하는 서열을 포함할 것이다. 선별 마커는 선택성 배양 배지에서 성장된 형질전환된 숙주 세포<br />
의 생존 또는 성장에 필요한 단백질을 인코딩한다. 선별 유전자를 포함하는 벡터로 형질전환되지 않은 숙주 세<br />
포는 배양 배지에서 생존하지 못할 것이다. 전형적인 선별 유전자는 (a) 항생제 또는 다른 독소에 내성을 공여<br />
하고, (b) 영양요구성 결핍을 보완하고, 또는 (c) 복합 배지로부터 가용하지 않은 핵심 영양소를 공급하는 단백<br />
질을 인코딩한다. 효모의 형질전환을 위한 전형적인 벡터와 방법은 예로써, Burke, D., Dawson, D., & Stearns,<br />
T. (2000). Methods in yeast genetics: a Cold Spring Harbor Laboratory course manual. Plainview, N.Y.:<br />
Cold Spring Harbor Laboratory Press에서 기술된다.<br />
본 발명의 방법에 이용되는 발현 벡터는 형질전환된 효모 균주를 확인하기 위한 선별가능 영양요구성 또는 약물<br />
마커를 비롯한 효모 특이적 서열을 추가로 포함할 것이다. 약물 마커는 효모 숙주 세포 내에서 벡터의 사본수를<br />
증폭하는 데에도 이용될 수 있다.<br />
- 55 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0220]<br />
[0221]<br />
[0222]<br />
[0223]<br />
[0224]<br />
[0225]<br />
[0226]<br />
[0227]<br />
목적되는 폴리펩티드 코딩 서열은 효모 세포 내에서 상기 폴리펩티드의 발현을 제공하는 전사와 번역 조절 서열<br />
에 작동가능하게 연결된다. 이들 벡터 성분에는 인핸서 요소, 프로모터, 그리고 전사 종결 서열 중에서 한 가지<br />
이상이 포함되지만 이들에 국한되지 않는다. 또한, 폴리펩티드의 분비를 위한 서열, 예를 들면, 신호 서열 등이<br />
포함될 수 있다. 효모 복제 기점은 발현 벡터가 종종 효모 게놈 내로 통합되기 때문에, 선택적이다.<br />
본 발명의 한 구체예에서, 목적 폴리펩티드는 효모 2배체 세포로부터 폴리펩티드의 최적화된 분비를 제공하는<br />
서열에 작동가능하게 연결되거나, 또는 융합된다.<br />
핵산은 다른 핵산 서열과 기능적 상관관계로 배치될 때 "작동가능하게 연결된다." 가령, 신호 서열에 대한 DNA<br />
는 폴리펩티드의 분비에 참여하는 단백원으로서 발현되면, 상기 폴리펩티드에 대한 DNA에 작동가능하게 연결된<br />
다; 프로모터 또는 인핸서는 코딩 서열의 전사에 영향을 주면, 상기 코딩 서열에 작동가능하게 연결된다. 일반<br />
적으로, "작동가능하게 연결되고"는 연결되는 DNA 서열들이 연속되고, 그리고 분비 리더의 경우에, 연속되고 해<br />
독틀 내에 있음을 의미한다. 하지만, 인핸서는 연속될 필요가 없다. 연결은 편의한 제한 부위에서 결찰에 의해,<br />
또는 대안으로, 당업자에게 익숙한 PCR/재조합 방법(GatewayR Technology; Invitrogen, Carlsbad California)<br />
에 의해 달성된다. 이런 부위가 존재하지 않으면, 합성 올리고뉴클레오티드 어댑터 또는 링커가 편의한 관례에<br />
따라서 이용된다.<br />
프로모터는 그들이 작동가능하게 연결된 특정 핵산 서열의 전사와 번역을 제어하는, 구조 유전자의 개시 코돈에<br />
대해 상류(5')에 위치하는 비번역 서열(일반적으로, 대략 100 내지 1000 bp 이내)이다. 이들 프로모터는 여러<br />
부류: 유도성, 구조성, 그리고 억제성 프로모터(리프레서의 부재에 응하여 전사의 수준을 증가시킴)로<br />
나눠진다. 유도성 프로모터는 배양 조건에서 일부 변화, 예를 들면, 영양소 또는 온도 변화의 존재 또는 부재에<br />
응하여 그들의 제어 하에 DNA로부터 증가된 수준의 전사를 개시할 수 있다.<br />
효모 프로모터 단편은 또한, 발현 벡터의 효모 게놈 내에서 동일한 부위 내로의 상동성 재조합과 통합을 위한<br />
부위로서 기능할 수 있다 ; 대안으로 선별가능 마커가 상동성 재조합을 위한 부위로서 이용된다. 피치아<br />
(Pichia) 형질전환은 Cregg et al. (<strong>19</strong>85) Mol. Cell. Biol. 5:3376-3385에서 기술된다.<br />
피치아(Pichia)로부터 적절한 프로모터의 실례에는 AOX1 프로모터(Cregg et al. (<strong>19</strong>89) Mol. Cell. Biol.<br />
9:1316-1323); ICL1 프로모터(Menendez et al. (2003) Yeast 20(13):1097-108); 글리세르알데히드-3-포스페이<br />
트 탈수소효소 프로모터(GAP)(Waterham et al. (<strong>19</strong>97) Gene 186(1):37-44); 그리고 FLD1 프로모터(Shen et al.<br />
(<strong>19</strong>98) Gene 216(1):93-102)가 포함된다. GAP 프로모터는 강한 구조성 프로모터이고, 그리고 AOX와 FLD1 프로<br />
모터는 유도성이다.<br />
다른 효모 프로모터에는 ADH1, 알코올 탈수소효소 II, GAL4, PHO3, PHO5, Pyk, 그리고 이들로부터 유래된 키메<br />
라 프로모터가 포함된다. 부가적으로, 비-효모 프로모터, 예를 들면, 포유동물, 곤충, 식물, 파충류, 양서류,<br />
바이러스, 그리고 조류 프로모터가 본 발명에 이용될 수 있다. 가장 전형적으로, 프로모터는 포유동물 프로모터<br />
(발현된 유전자에 잠재적으로 내인성)를 포함하거나, 또는 효모 시스템에서 효과적인 전사를 제공하는 효모 또<br />
는 바이러스 프로모터를 포함할 것이다.<br />
목적 폴리펩티드는 직접적으로 뿐만 아니라 이종성 폴리펩티드, 예를 들면, 성숙 단백질 또는 폴리펩티드의 N-<br />
말단에서 특정한 절단 부위를 보유하는 신호 서열 또는 다른 폴리펩티드와의 융합 폴리펩티드로서 재조합 방식<br />
으로 생산될 수 있다. 일반적으로, 신호 서열은 벡터의 한 성분이거나, 또는 벡터 내로 삽입되는 폴리펩티드 코<br />
딩 서열의 일부일 수 있다. 선택되는 이종성 신호 서열은 바람직하게는, 숙주 세포 내에서 가용한 표준 경로 중<br />
에서 한 가지를 통해 인식되고 처리되는 것이다. 사카로마이세스 세레비지애(S. cerevisiae) 알파 인자 프리-프<br />
로(pre-pro) 신호는 피치아 파스토리스(P. pastoris)로부터 다양한 재조합 단백질의 분비에 효과적인 것으로 증<br />
명되었다. 다른 효모 신호 서열에는 알파 교배 인자 신호 서열, 전화효소 신호 서열, 그리고 다른 분비된 효모<br />
폴리펩티드로부터 유래된 신호 서열을 포함된다. 부가적으로, 이들 신호 펩티드 서열은 2배수 효모 발현 시스템<br />
에서 강화된 분비를 제공하도록 조작될 수 있다. 목적되는 다른 분비 신호에는 포유동물 신호 서열 역시 포함되<br />
는데, 이들은 분비되는 단백질에 이종성이거나, 또는 분비되는 단백질에 대한 본래의 서열일 수 있다. 신호 서<br />
열에는 프리-펩티드 서열이 포함되고, 그리고 일부 경우에 프로-펩티드 서열이 포함될 수 있다. 면역글로불린<br />
사슬에서 관찰되는 신호 서열, 예를 들면, K28 프리프로톡신(preprotoxin) 서열, PHA-E, FACE, 인간 MCP-1, 인<br />
간 혈청 알부민 신호 서열, 인간 Ig 중쇄, 인간 Ig 경쇄 등을 비롯한 이와 같은 많은 신호 서열이 당분야에 공<br />
지되어 있다(참조: Hashimoto et. al. Protein Eng 11(2) 75(<strong>19</strong>98); 그리고 Kobayashi et. al. Therapeutic<br />
Apheresis 2(4) 257 (<strong>19</strong>98)).<br />
- 56 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0228]<br />
[0229]<br />
[0230]<br />
[0231]<br />
[0232]<br />
[0233]<br />
[0234]<br />
[0235]<br />
[0236]<br />
[0237]<br />
전사는 전사 활성자 서열을 벡터 내로 삽입함으로써 증가될 수 있다. 이들 활성자는 DNA의 cis-작용 요소이고,<br />
통상적으로 대략 10 내지 300개 bp를 보유하며, 프로모터에 작용하여 이의 전사를 증가시킨다. 전사 인핸서는<br />
상대적으로 방향과 위치 독립적이고, 전사 단위에 대해 5'와 3'에서, 인트론 내에서, 그리고 코딩 서열 그 자체<br />
내에서 관찰된다. 인핸서는 코딩 서열에 대해 5' 또는 3' 위치에서 발현 벡터 내로 절단접합될 수 있지만, 바람<br />
직하게는 프로모터로부터 5' 위치에 존재한다.<br />
진핵 숙주 세포에 이용되는 발현 벡터는 또한, 전사의 종결 및 mRNA의 안정화를 위하여 필요한 서열을 포함할<br />
수 있다. 이런 서열은 진핵 또는 바이러스 DNA 또는 cDNA의 비번역 부위 내에서, 번역 종결 코돈에 대해 3'로부<br />
터 통상적으로 가용하다. 이들 부위는 mRNA의 비번역 부분 내에서, 폴리아데닐화된 단편으로서 전사되는 뉴클레<br />
오티드 조각을 포함한다.<br />
하나 이상의 전술한 성분을 포함하는 적절한 벡터의 작제는 표준 결찰 기술 또는 PCR/재조합 방법을 이용한다.<br />
분리된 플라스미드 또는 DNA 단편은 절단되고, 재단되고, 그리고 재조합 방법을 통해 필요한 플라스미드를 생성<br />
시키기 위한 원하는 형태로 재-결찰된다. 작제된 플라스미드 내에서 정확한 서열을 확인하는 분석을 위하여, 숙<br />
주 세포를 형질전환시키기 위한 결찰 혼합물이 이용되고, 그리고 성공적인 형질전환체가 적절한 경우에, 항생제<br />
내성(가령, 암피실린 또는 Zeocin(플레오마이신))에 의해 선별된다. 형질전환체로부터 플라스미드가<br />
제조되고, 제한 엔도뉴클레아제 절단에 의해 분석되고 및/또는 서열화된다.<br />
단편의 제한과 결찰에 대한 대안으로서, att 부위와 재조합 효소에 기초된 재조합 방법이 DNA 서열을 벡터 내로<br />
삽입하는데 이용될 수 있다. 이런 방법은 예로써, Landy (<strong>19</strong>89) Ann.Rev.Biochem. 58:913-949에서 기술되고;<br />
그리고 당업자에게 공지되어 있다. 이런 방법은 람다 및 대장균(E.coli)-인코딩된 재조합 단백질의 혼합물에 의<br />
해 매개되는 분자간 DNA 재조합을 이용한다. 재조합은 상호작용 DNA 분자 상에서 특이적 부착(att) 부위 사이에<br />
발생한다. att 부위의 설명을 위하여, Weisberg and Landy (<strong>19</strong>83) Site-Specific Recombination in Phage<br />
Lambda, in Lambda II, Weisberg, ed.(Cold Spring Harbor, NY:Cold Spring Harbor Press), pp.211-250를 참<br />
조한다. 이들 재조합 부위에 접하는 DNA 조각은 재조합후, att 부위가 각 모 벡터에 의해 제공된 서열로 구성되<br />
는 하이브리드 서열이 되도록 치환된다. 재조합은 임의의 위상의 DNA 사이에 발생할 수 있다.<br />
att 부위는 목적 서열을 적절한 벡터 내로 결찰하고; 특이적 프라이머의 이용을 통해 att B 부위를 포함하는<br />
PCR 산물을 생성시키고; att 부위를 포함하는 적절한 벡터 내로 클로닝된 cDNA 라이브러리를 생성시키는 등으로<br />
써 목적 서열 내로 도입될 수 있다.<br />
본 명세서에서, 접힘은 폴리펩티드와 단백질의 3-차원 구조를 지칭하고, 여기서 아미노산 잔기 사이에 상호작용<br />
은 상기 구조를 안정화시키는 기능을 한다. 비-공유 상호작용이 구조를 결정하는데 중요하긴 하지만, 통상적으<br />
로 목적 단백질은 2개의 시스테인 잔기에 의해 형성된 분자내 및/또는 분자간 공유 이황화 결합을 보유할 것이<br />
다. 자연 발생 단백질과 폴리펩티드 또는 이들의 유도체와 변이체의 경우에, 적절한 접힘은 전형적으로, 최적<br />
생물학적 활성을 생성시키는 배열이고, 그리고 활성, 예를 들면, 리간드 결합, 효소 활성 등에 대한 분석으로<br />
편의하게 모니터될 수 있다.<br />
일부 경우에, 예를 들면, 원하는 산물이 합성 기원인 경우에, 생물학적 활성에 기초된 분석은 의미가 덜할 것이<br />
다. 이런 분자의 적절한 접힘은 물리적 특성, 에너지 고려, 모델링 연구 등에 기초하여 결정될 수 있다.<br />
발현 숙주는 접힘 및 이황화 결합 형성을 강화시키는 한 가지 이상의 효소, 다시 말하면, 폴다아제(foldase),<br />
샤프로닌(chaperonin) 등을 인코딩하는 서열의 도입에 의해 더욱 변형될 수 있다. 이런 서열은 당분야에 공지된<br />
벡터, 마커 등을 이용하여 효모 숙주 세포 내에서 구조성으로 또는 유도성으로 발현될 수 있다. 바람직하게는,<br />
원하는 발현 패턴을 위하여 충분한 전사 조절 요소를 포함하는 이들 서열은 표적화된 방법을 통하여 효모 게놈<br />
내로 안정적으로 통합된다.<br />
가령, 진핵 PDI는 단백질 시스테인 산화와 이황화 결합 이성화의 효과적인 촉매일 뿐만 아니라, 샤프롱 활성을<br />
보인다. PDI의 Co-발현은 다발성 이황화 결합을 보유하는 활성 단백질의 생산을 용이하게 할 수 있다. 또한,<br />
BIP(면역글로불린 중쇄 결합 단백질); 시클로필린; 등의 발현이 목적된다. 본 발명의 한 구체예에서, 각각의 반<br />
수체 모 균주는 별개의 접힘 효소를 발현한다, 가령 한 균주는 BIP를 발현하고, 그리고 다른 균주는 PDI 또는<br />
이들의 조합을 발현한다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
용어 "원하는 단백질" 또는 "표적 단백질"은 동의어로서 이용되고, 일반적으로 본 명세서에서 기술된 인간화된<br />
항체 또는 이의 결합 부분을 지칭한다. 용어 "항체"는 에피토프에 적합하고 이를 인식하는 특이적 형상을 갖는<br />
임의의 폴리펩티드 사슬-포함 분자 구조를 포함하는 것으로 의도되고, 여기서 하나 이상의 비-공유 결합 상화작<br />
- 57 -
[0238]<br />
[0239]<br />
[0240]<br />
[0241]<br />
용이 상기 분자 구조와 에피토프 사이에 복합체를 안정화시킨다. 전형적인 항체 분자는 면역글로불린이고, 그리<br />
고 모든 공급원, 예를 들면, 인간, 설치류, 토끼, 소, 양, 돼지, 개, 기타 포유동물, 닭, 기타 조류 등으로부터<br />
모든 유형의 면역글로불린, IgG, IgM, IgA, IgE, IgD 등은 "항체"인 것으로 간주된다. 본 발명에 따른 출발 물<br />
질로서 유용한 항체를 생산하기 위한 바람직한 공급원은 토끼이다. 다수의 항체 코딩 서열이 보고되었고, 그리<br />
고 다른 것들은 당분야에 널리 공지된 방법에 의해 생산될 수 있다. 이들의 실례에는 키메라 항체, 인간 항체와<br />
다른 비-인간 포유동물 항체, 인간화 항체, 단일 쇄 항체, 예를 들면, scFv, 카멜바디(camelbody), 나노바디<br />
(nanobody), IgNAR(상어로부터 유래된 단일-쇄 항체), 소형-규격 면역약제(small-modular<br />
immunopharmaceutical, SMIP), 그리고 항체 단편, 예를 들면, Fab, Fab', F(ab')2 등이 포함된다(참조:<br />
Streltsov VA, et al., Structure of a shark IgNAR antibody variable domain and modeling of an early-<br />
developmental isotype, Protein Sci. 2005 Nov;14(11):2901-9. Epub 2005 Sep 30; Greenberg AS, et al., A<br />
new antigen receptor gene family that undergoes rearrangement and extensive somatic diversification in<br />
sharks, Nature. <strong>19</strong>95 Mar 9;374(6518):168-73; Nuttall SD, et al., Isolation of the new antigen receptor<br />
from wobbegong sharks, and use as a scaffold for the display of protein loop libraries, Mol Immunol.<br />
2001 Aug;38(4):313-26; Hamers-Casterman C, et al., Naturally occurring antibodies devoid of light<br />
chains, Nature. <strong>19</strong>93 Jun 3;363(6428):446-8; Gill DS, et al., Biopharmaceutical drug discovery using<br />
novel protein scaffolds, Curr Opin Biotechnol. 2006 Dec;17(6):653-8. Epub 2006 Oct <strong>19</strong>).<br />
가령, 항체, 또는 이들의 항원 결합 단편 또는 변이체는 유전자 조작으로 생산될 수 있다. 이러한 기술에서, 다<br />
른 방법에서처럼, 항체-생산 세포는 원하는 항원 또는 면역원에 민감해진다. 항체 생산 세포로부터 분리된 메신<br />
저 RNA는 PCR 증폭을 이용하여 cDNA를 만드는 주형으로서 이용된다. 각각 초기 항원 특이성을 유지하는 하나의<br />
중쇄 유전자 및 하나의 경쇄 유전자를 포함하는 벡터의 라이브러리는 증폭된 면역글로불린 cDNA의 적절한 구역<br />
의 이들 발현 벡터 내로의 삽입에 의해 생산된다. 조합 라이브러리(combinatorial library)는 중쇄 유전자 라이<br />
브러리를 경쇄 유전자 라이브러리와 통합함으로써 구축된다. 이는 중쇄와 경쇄를 공동-발현하는 클론의 라이브<br />
러리(항체 분자의 Fab 단편 또는 항원 결합 단편과 유사함)를 산출한다. 이들 유전자를 보유하는 벡터는 숙주<br />
세포 내로 공동-형질감염된다. 항체 유전자 합성이 형질감염된 숙주 내에서 유도될 때, 중쇄와 경쇄 단백질은<br />
자가-조립하여 항원 또는 면역원을 이용한 스크리닝에 의해 검출될 수 있는 활성 항체를 생산한다.<br />
목적되는 항체 코딩 서열에는 본래의 서열에 의해 인코딩된 것들, 그리고 유전자 코드의 축중성(degeneracy)으<br />
로 인하여, 이들 개시된 핵산과 서열에서 동일하지 않는 핵산, 그리고 이들의 변이체가 포함된다. 변이체 폴리<br />
펩티드는 아미노산(aa) 치환, 부가 또는 결실을 보유할 수 있다. 아미노산 치환은 보존적 아미노산 치환, 또는<br />
비-필수 아미노산을 제거하는, 예를 들면, 당화 부위를 변화시키거나, 또는 기능에 필요하지 않은 하나 이상의<br />
시스테인 잔기의 치환 또는 결실로 오접힘을 최소화시키는 치환일 수 있다. 변이체는 단백질의 특정 부위(가령,<br />
기능성 도메인, 촉매성 아미노산 잔기 등)의 생물학적 활성을 유지하거나 강화시키도록 설계될 수 있다. 변이체<br />
는 또한, 본 명세서에 기술된 폴리펩티드의 단편, 특히 생물학적 활성 단편 및/또는 기능성 도메인에 상응하는<br />
단편을 포함한다. 클로닝된 유전자의 시험관내 돌연변이유발을 위한 기술은 공지되어 있다. 또한, 본 발명에는<br />
단백분해성 분해에 대한 내성을 개선하거나, 또는 용해도 특성을 최적화하거나, 또는 이들을 치료제로서 더욱<br />
적합하게 만들기 위하여, 통상적인 분자 생물학적 기술을 이용하여 변형된 폴리펩티드가 포함된다.<br />
키메라 항체는 한쪽 종의 항체 생산 세포로부터 획득된 가변 경쇄와 중쇄 영역(VL과 VH)을 다른 종으로부터 불변<br />
경쇄와 중쇄 영역과 통합함으로써 재조합 수단에 의해 만들어질 수 있다. 전형적으로, 키메라 항체는 주로 인간<br />
도메인을 보유하는 항체를 생산하기 위하여, 설치류 또는 토끼 가변 영역 및 인간 불변 영역을 이용한다. 이런<br />
키메라 항체의 생산은 당분야에 널리 공지되어 있고, 그리고 표준 수단(예로써, 본 발명에 참조로서 편입되는<br />
U.S. 특허 No. 5,624,659에서 기술된 바와 같은)에 의해 달성될 수 있다. 게다가, 본 발명의 키메라 항체의 인<br />
간 불변 영역은 IgG1, IgG2, IgG3, IgG4, IgG5, IgG6, IgG7, IgG8, IgG9, IgG10, IgG11, IgG<strong>12</strong>, IgG13,<br />
IgG14, IgG15, IgG16, IgG17, IgG18 또는 IgG<strong>19</strong> 불변 영역에서 선택될 수 있는 것으로 고려된다.<br />
인간화 항체는 더욱 인간-유사한 면역글로불린 도메인을 보유하고, 그리고 동물-유래된 항체의 상보성 결정 영<br />
역만을 통합하도록 조작된다. 이는 단일클론 항체의 가변 영역의 초가변 루프(hyper-variable loop) 서열을 조<br />
심스럽게 조사하고, 그리고 이들을 인간 항체 사슬의 구조에 적합시킴으로써 달성된다. 겉보기에 복잡하지만,<br />
이러한 과정은 실시가 간단하다(참조: 본 발명에 참조로서 편입된 U.S. 특허 No. 6,187,287). 바람직한 구체예<br />
에서, 인간화는 하기에 상세하게 기술된 바와 같이 달성될 수 있다. 이러한 계획은 인간화되는 모 항체에 고도<br />
로 상동성인 인간 FR 상에 CDR을 이식한다.<br />
- 58 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0242]<br />
[0243]<br />
[0244]<br />
[0245]<br />
[0246]<br />
[0247]<br />
[0248]<br />
[0249]<br />
완전한 면역글로불린(또는 이들의 재조합 대응물)에 더하여, 에피토프 결합 부위를 포함하는 면역글로불린 단편<br />
(가령, Fab', F(ab')2, 또는 다른 단편)이 합성될 수 있다. "단편", 또는 최소 면역글로불린은 재조합 면역글로<br />
불린 기술을 이용하여 설계될 수 있다. 가령, 본 발명에 이용되는 "Fv" 면역글로불린은 융합된 가변 경쇄 영역<br />
및 가변 중쇄 영역을 합성함으로써 생산될 수 있다. 항체의 조합, 예를 들면, 2개의 상이한 Fv 특이성을 포함하<br />
는 디아바디(diabody) 역시 목적된다. 본 발명의 또 다른 구체예에서, SMIP(소분자 면역약제), 카멜바디, 나노<br />
바디, 그리고 IgNAR이 면역글로불린 단편에 포함된다.<br />
면역글로불린 및 이들의 단편은 예로써, 이펙터 모이어티, 예를 들면, 화학적 링커, 검출가능 모이어티, 예를<br />
들면, 형광 염료, 효소, 독소, 기질, 생물발광 물질, 방사성 물질, 화학발광 모이어티 등을 추가하기 위하여 번<br />
역후 변형될 수 있고, 또는 특이적 결합 모이어티, 예를 들면, 스트렙타비딘, 아비딘, 또는 비오틴 등이 본 발<br />
명의 방법과 조성물에 이용될 수 있다. 추가의 이펙터 분자의 실례는 하기에 제공된다.<br />
용어 "연장된 기간 동안 원하는 분비된 이종성 폴리펩티드를 안정적으로 발현하거나, 또는 발현하는 배수체 효<br />
모"는 역치 발현 수준, 전형적으로 적어도 10-25 ㎎/ℓ, 바람직하게는 실질적으로 그 이상에서 적어도 수일 내<br />
지 1주일, 더욱 바람직하게는 적어도 1개월, 이보다 더욱 바람직하게는 적어도 1-6개월, 그리고 이보다 더욱 바<br />
람직하게는 1년 이상 동안 상기 폴리펩티드를 분비하는 효모 배양액을 지칭한다.<br />
용어 "원하는 양의 재조합 폴리펩티드를 분비하는 배수체 효모 배양액"은 적어도 10-25 ㎎/ℓ의 이종성 폴리펩<br />
티드, 더욱 바람직하게는 적어도 50-500 ㎎/ℓ, 그리고 가장 바람직하게는 500-1000 ㎎/ℓ 또는 그 이상을 안정<br />
적으로, 또는 연장된 기간 동안 분비하는 배양액을 지칭한다.<br />
유전자 코드에 따른 폴리뉴클레오티드 서열의 번역이 폴리펩티드 서열을 생성시키면(즉, 폴리뉴클레오티드 서열<br />
이 폴리펩티드 서열을 "인코딩하면") 상기 폴리뉴클레오티드 서열은 상기 폴리펩티드 서열에 "상응하고", 그리<br />
고 2개의 폴리뉴클레오티드 서열이 동일한 폴리펩티드 서열을 인코딩하면, 한쪽 폴리뉴클레오티드 서열은 다른<br />
폴리뉴클레오티드 서열에 "상응한다."<br />
DNA 구조체의 "이종성" 영역 또는 도메인은 자연에서 더욱 큰 DNA 분자와 관련하여 관찰되지 않는, 상기 DNA 분<br />
자 내에서 DNA의 확인가능 조각이다. 따라서 이종성 영역이 포유동물 유전자를 인코딩할 때, 상기 유전자는 통<br />
상적으로, 공급원 생물체의 게놈 내에서 포유동물 게놈 DNA에 접하지 않는 DNA가 측면에 위치할 것이다. 이종성<br />
영역의 다른 실례는 코딩 서열 그 자체가 자연에서 관찰되지 않는 구조체(가령, 게놈 코딩 서열이 인트론을 포<br />
함하는 cDNA, 또는 본래의 유전자와 상이한 코돈을 보유하는 합성 서열)이다. 대립유전자 변이 또는 자연-발생<br />
돌연변이 현상은 본 명세서에서 기술된 바와 같은 DNA의 이종성 영역을 발생시키지 못한다.<br />
"코딩 서열"은 (유전자 코드에 비추어) 단백질 또는 펩티드 서열에 상응하거나, 또는 이러한 서열을 인코딩하는<br />
코돈의 인-프레임 서열이다. 2개의 코딩 서열은 이들 서열 또는 이들의 상보성 서열이 동일한 아미노산 서열을<br />
인코딩하면, 서로에 상응한다. 적절한 조절 서열과 공동으로 코딩 서열은 전사되고 폴리펩티드로 번역될 수 있<br />
다. 폴리아데닐화 신호와 전사 종결 서열은 일반적으로, 코딩 서열에 대해 3'에 위치할 것이다. "프로모터<br />
서열"은 세포 내에서 RNA 중합효소에 결합하고 하류(3' 방향) 코딩 서열의 전사를 개시할 수 있는 DNA 조절 영<br />
역이다. 프로모터 서열은 전형적으로, 코딩 서열의 전사에 영향을 주는 조절 분자(가령, 전사 인자)의 결합을<br />
위한 추가 부위를 포함한다. 코딩 서열은 RNA 중합효소가 세포 내에서 프로모터 서열에 결합하고 상기 코딩 서<br />
열을 mRNA로 전사시킬 때 프로모터 서열의 "제어 하에"있거나, 또는 프로모터에 "작동가능하게 연결되고", mRNA<br />
는 이후, 상기 코딩 서열에 의해 인코딩된 단백질로 번역된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
외래 물질, 예를 들면, DNA, RNA 또는 단백질을 생물체 또는 숙주 세포 내로 도입하기 위하여 벡터가 이용된다.<br />
전형적인 벡터에는 재조합 바이러스(폴리뉴클레오티드의 경우) 및 리포좀 또는 다른 지질 응집체(폴리펩티드 및<br />
/또는 폴리뉴클레오티드의 경우)이 포함된다. "DNA 벡터"는 다른 폴리뉴클레오티드 조각이 부착되고 이러한 부<br />
착된 조각의 복제를 유발할 수 있는 레플리콘, 예를 들면, 플라스미드, 파지 또는 코스미드이다. "발현 벡터"는<br />
적절한 숙주 세포에 의한 폴리펩티드 합성을 주동하는 조절 서열을 포함하는 DNA 벡터이다. 이는 일반적으로,<br />
RNA 중합효소에 결합하고 mRNA의 전사를 개시하는 프로모터, 그리고 mRNA의 폴리펩티드로의 번역을 주동하는 리<br />
보솜 결합 부위와 개시 신호를 의미한다. 적절한 부위에서, 그리고 정확한 해독틀 내에서 발현 벡터 내로 폴리<br />
뉴클레오티드 서열의 통합, 그 이후에 상기 벡터에 의한 적절한 숙주 세포의 형질전환은 상기 폴리뉴클레오티드<br />
서열에 의해 인코딩된 폴리펩티드의 생산을 가능하게 한다. 전형적인 발현 벡터 및 이들의 이용을 위한 기술은<br />
아래의 간행물에서 기술된다: Old et al., Principles of Gene Manipulation: An Introduction to Genetic<br />
Engineering, Blackwell Scientific Publications, 4th edition, <strong>19</strong>89; Sambrook et al., Molecular Cloning:<br />
- 59 -
[0250]<br />
[0251]<br />
[0252]<br />
[0253]<br />
A Laboratory Manual, 2nd Edition, Cold Spring Harbor Laboratory Press, <strong>19</strong>89; Sambrook et al.,<br />
Molecular Cloning: A Laboratory Manual, 3rd Edition, Cold Spring Harbor Laboratory Press, 2001;<br />
Gorman, "High Efficiency Gene Transfer into Mammalian Cells," in DNA Cloning, Volume II, Glover, D.<br />
M., Ed., IRL Press, Washington, D.C., pp. 143 <strong>19</strong>0 (<strong>19</strong>85).<br />
가령, 리포좀 또는 다른 지질 집합체는 지질, 예를 들면, 포스파티딜콜린(레시틴)(PC), 포스파티딜에탄올아민<br />
(PE), 리소레시틴, 리소포스파티딜에탄올아민, 포스파티딜세린(PS), 포스파티딜글리세롤(PG), 포스파티딜이노시<br />
톨(PI), 스핑고미엘린, 카디오리핀, 포스파티드산(PA), 지방산, 갱글리오사이드, 글루코리피드, 당지질, 모노-,<br />
디- 또는 트리글리세리드, 세라미드, 세레브로시드 및 이들의 조합; 양이온성 지질(또는 다른 양이온성 양친매<br />
성 물질), 예를 들면, 1,2-디올레일옥시-3-(트리메틸아미노) 프로판(DOTAP); N-콜레스테릴옥시카르바릴-3,7,<strong>12</strong>-<br />
트리아자펜타데칸-1,15-디아민(CTAP); N-[1-(2,3,-디테트라데실옥시)프로필]-N,N-디메틸-N-히드록시에틸암모늄<br />
브롬화물(DMRIE); N-[1-(2,3,-디올레일옥시)프로필]-N,N-디메틸-N-히드록시 에틸암모늄 브롬화물(DORIE); N-<br />
[1-(2,3-디올레일옥시) 프로필]-N,N,N-트리메틸암모늄 염화물(DOTMA); 3 베타 [N-(N',N'-디메틸아미노에탄)카르<br />
바모일] 콜레스테롤(DC-Choi); 그리고 디메틸디옥타데실암모늄(DDAB); 디올레오일포스파티딜 에탄올아민(DOPE),<br />
콜레스테롤-포함 DOPC; 그리고 이들의 조합; 및/또는 친수성 중합체, 예를 들면, 폴리비닐피롤리돈, 폴리비닐메<br />
틸에테르, 폴리메틸옥사졸린, 폴리에틸옥사졸린, 폴리히드록시프로필옥사졸린, 폴리히드록시프로필메타크릴아미<br />
드, 폴리메타크릴아미드, 폴리디메틸아크릴아미드, 폴리히드록시프로필메타크릴레이트, 폴리히드록시에틸아크릴<br />
레이트, 히드록시메틸셀룰로오스, 히드록시에틸셀룰로오스, 폴리에틸렌글리콜, 폴리아스파르타미드 및 이들의<br />
조합을 포함할 수 있다. 다른 적절한 양이온성 지질은 Miller, Angew. Chem. Int. Ed. 37:1768 1785 (<strong>19</strong>98),<br />
그리고 Cooper et al., Chem. Eur. J. 4(1): 137 151 (<strong>19</strong>98)에서 기술된다. 리포좀은 가교되거나, 부분적으로<br />
가교되거나, 또는 가교가 없을 수 있다. 가교된 리포좀은 가교된 성분과 비-가교된 성분을 모두 포함할 수<br />
있다. 적절한 양이온성 리포좀 또는 시토펙틴(cytofectin)은 상업적으로 가용하고, 또한 Sipkins et al.,<br />
Nature Medicine, <strong>19</strong>98, 4(5):(<strong>19</strong>98), 623 626, 또는 Miller, supra에서 기술된 바와 같이 제조될 수 있다. 전<br />
형적인 리포좀은 핵산에 결합하기 적합한 중합가능 짝이온성 또는 중성 지질, 중합가능 인테그린 표적화 지질<br />
및 중합가능 양이온성 지질을 포함한다. 리포좀은 선택적으로, 증가된 효능을 제공하는 펩티드, 예를 들면,<br />
U.S. Pat. No. 7,297,759에서 기술된 바와 같은 펩티드를 포함할 수 있다. 추가의 예시적인 리포좀 및 다른 지<br />
질 집합체는 U.S. Pat. No. 7,166,298에서 기술된다.<br />
폴리뉴클레오티드 서열의 "증폭"은 특정 핵산 서열의 복수 사본의 시험관내 생산이다. 증폭된 서열은 일반적으<br />
로, DNA의 형태이다. 이런 증폭을 수행하기 위한 다양한 기술은 Van Brunt에 의한 서평 논문(<strong>19</strong>90,<br />
Bio/Technol., 8(4):291-294)에서 기술된다. 중합효소 연쇄 반응 또는 PCR은 핵산 증폭의 원형이고, 그리고 본<br />
발명에서 PCR의 이용은 다른 적절한 증폭 기술의 예시인 것으로 간주되어야 한다.<br />
척추동물에서 항체의 일반적인 구조는 현재 충분히 알려져 있다(Edelman, G. M., Ann. N.Y. Acad. Sci., <strong>19</strong>0:<br />
5 (<strong>19</strong>71)). 항체는 대략 23,000 달톤의 분자량을 갖는 2개의 동일한 가벼운 폴리펩티드 사슬("경쇄"), 그리고<br />
53,000-70,000 달톤의 분자량을 갖는 2개의 동일한 무거운 사슬("중쇄")로 구성된다. 이들 4개의 사슬은 "Y" 형<br />
태로 이황화 결합에 의해 연결되고, 여기서 경쇄는 "Y" 형태의 입에서부터 중쇄를 일괄한다. "Y" 형태의 "가지"<br />
부분은 Fab 영역으로 명명된다; "Y" 형태의 굴대 부분은 Fc 영역으로 명명된다. 아미노산 서열 방향은 "Y" 형태<br />
의 꼭대기에서 N-말단 단부로부터 각 사슬의 바닥에서 C-말단 단부로 움직인다. N-말단 단부는 특이성이 유도되<br />
는 항원에 대한 특이성을 갖는 가변 영역을 보유하고, 그리고 대략 100개의 아미노산 길이를 갖는데, 경쇄와 중<br />
쇄 사이에, 그리고 항체마다 약간의 변이가 존재한다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
가변 영역은 각 사슬 내에서, 사슬의 나머지 부분을 전개하고 특정 부류의 항체 내에서 항체의 특이성(즉, 이를<br />
유도하는 항원)에 따라 변하지 않는 불변 영역에 연결된다. 면역글로불린 분자의 부류를 결정하는 5가지 공지된<br />
주요 부류의 불변 영역이 존재한다(γ, μ, α, δ, 그리고 ε(감마, 뮤, 알파, 델타, 또는 엡실론) 중쇄 불변<br />
영역에 상응하는 IgG, IgM, IgA, IgD, 그리고 IgE). 이들 불변 영역 또는 부류는 보체의 활성화(Kabat, E. A.,<br />
Structural Concepts in Immunology and Immunochemistry, 2nd Ed., p. 413-436, Holt, Rinehart, Winston<br />
(<strong>19</strong>76)), 그리고 다른 세포 반응(Andrews, D. W., et al., Clinical Immunobiology, pp 1-18, W. B. Sanders<br />
(<strong>19</strong>80); Kohl, S., et al., Immunology, 48: 187 (<strong>19</strong>83))을 비롯한 항체의 차후 이펙터 기능을 결정한다;<br />
반면, 가변 영역은 자신이 반응할 항원을 결정한다. 경쇄는 κ(카파) 또는 λ(람다)로 분류된다. 각 중쇄 부류<br />
는 카파 또는 람다 경쇄와 짝을 이룰 수 있다. 경쇄와 중쇄는 서로 공유 결합되고, 그리고 2개의 중쇄의 "꼬리"<br />
부분은 면역글로불린이 하이브리도마 또는 B 세포에 의해 산출될 때, 공유 이황화 연쇄에 의해 서로 결합된다.<br />
- 60 -
[0254]<br />
[0255]<br />
[0256]<br />
[0257]<br />
[0258]<br />
[0259]<br />
[0260]<br />
[0261]<br />
[0262]<br />
[0263]<br />
[0264]<br />
[0265]<br />
[0266]<br />
표현 "가변 영역" 또는 "VR"은 항체를 항원에 결합시키는데 직접적으로 관여하는, 항체 내에 경쇄와 중쇄의 각<br />
쌍 내에서 도메인을 지칭한다. 각 중쇄는 한쪽 단부에 가변 도메인(VH)을 보유하고, 그 다음에 다수의 불변 도<br />
메인을 보유한다. 각 경쇄는 한쪽 단부에 가변 도메인(VL), 그리고 다른 단부에 불변 도메인을 보유한다; 경쇄<br />
의 불변 도메인은 중쇄의 첫 번째 불변 도메인과 함께 정렬되고, 그리고 경쇄의 가변 도메인은 중쇄의 가변 도<br />
메인과 함께 정렬된다.<br />
표현 "상보성 결정 영역", "초가변 영역", 또는 "CDR"은 항체의 경쇄 또는 중쇄의 가변 영역에서 관찰되는 하나<br />
이상의 초가변 또는 상보성 결정 영역(CDR)을 지칭한다(참조: Kabat, E. A. et al., Sequences of Proteins of<br />
Immunological Interest, National Institutes of Health, Bethesda, Md., (<strong>19</strong>87)). 이들 표현은 Kabat 등<br />
("Sequences of Proteins of Immunological Interest," Kabat E., et al., US Dept. of Health and Human<br />
Services, <strong>19</strong>83)에 의해 정의된 바와 같은 초가변 영역, 또는 항체의 3-차원 구조에서 초가변 루프(Chothia and<br />
Lesk, J Mol. Biol. <strong>19</strong>6 901-917 (<strong>19</strong>87))를 포함한다. 각 사슬에서 CDR은 골격 영역에 의해 근접하게<br />
유지되고, 그리고 다른 사슬로부터 CDR과 함께, 항원 결합 부위의 형성에 기여한다. 이들 CDR 내에서, 항체-항<br />
원 상호작용에서 CDR에 의해 이용되는 중요한 접촉 잔기를 대표하는 선택성 결정 부위(SDR)로서 기술되는 선택<br />
아미노산이 존재한다(Kashmiri, S., Methods, 36:25-34 (2005)). 예시적인 항-IL-6 항체에 대한 CDR이 본 명세<br />
서에서 제공된다.<br />
표현 "골격 영역" 또는 "FR"은 항체의 경쇄와 중쇄의 가변 영역 내에서 하나 이상의 골격 영역을<br />
지칭한다(참조: Kabat, E. A. et al., Sequences of Proteins of Immunological Interest, National<br />
Institutes of Health, Bethesda, Md., (<strong>19</strong>87)). 이들 표현은 항체의 경쇄와 중쇄의 가변 영역 내에서 CDR 사<br />
이에 개재된 아미노산 서열 영역을 포함한다. 바람직한 구체예에서 언급된 바와 같이, FR은 모 항체(가령 토끼<br />
항체)에 고도로 상동성인 인간 FR을 포함할 것이다.<br />
Ab1 항-IL-6 항체 및 이들의 결합 단편<br />
본 발명은 IL-6에 결합 특이성을 갖고, 그리고 하기에 열거된 서열을 포함하는 가변 경쇄 서열을 보유하는<br />
항체:<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVSAAVGGTVTIKCQASQSINNELSWYQQKPGQRPKLLIYRASTLASGVSSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQQGYSLRNIDNAFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNN (서열 번호: 2) 또는<br />
AIQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPDDFATYYCQQGYSLRNIDNAFG<br />
GGTKVEI<strong>KR</strong> (서열 번호: 709), 그리고 도 2와 34-37에서 열거된 것들과 표 1에서 확인된 것들을 비롯한 이들의<br />
인간화된 이형과 변이체에 관계한다.<br />
본 발명은 또한, IL-6에 결합 특이성을 갖고, 그리고 하기에 열거된 서열을 포함하는 가변 중쇄 서열을 보유하<br />
는 항체:<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSNYYVTWVRQAPGKGLEWIGIIYGSDETAYATWAIGRFTISKTSTTVDLKMTSLT<br />
AADTATYFCARDDSSDWDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK (서열 번호: 3) 또는<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATSAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSS (서열 번호: 657), 그리고 도 2와 34-37에서 열거된 것들과 표 1에서 확인된 것들을 비롯<br />
한 이들의 인간화된 이형과 변이체에 관계한다.<br />
본 발명은 또한, IL-6에 결합 특이성을 갖고, 그리고 하기에 열거된 바와 같이 CDR2 내에서 트립토판 잔기가 세<br />
린으로 변경된 SEQ ID NO: 3의 변형된 이형인 가변 중쇄 서열을 보유하는 항체:<br />
공개특허 10-2011-01<strong>12</strong>308<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSNYYVTWVRQAPGKGLEWIGIIYGSDETAYATSAIGRFTISKTSTTVDLKMTSLT<br />
AADTATYFCARDDSSDWDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK (SEQ ID NO: 658), 그리고 도 2와 34-<br />
37에서 열거된 것들과 표 1에서 확인된 것들을 비롯한 이들의 인간화된 이형과 변이체에 관계한다.<br />
더 나아가, 본 발명에서는 서열 번호: 2의 가변 경쇄 서열의 상보성 결정 영역(CDR, 또는 초가변 영역)에 상응<br />
하는 서열 번호: 4; 서열 번호: 5; 그리고 서열 번호: 6 중에서 하나 이상의 폴리펩티드 서열, 및/또는 서열 번<br />
호: 3 또는 서열 번호: <strong>19</strong>의 가변 중쇄 서열의 상보성 결정 영역(CDR, 또는 초가변 영역)에 상응하는 서열<br />
번호: 7; 서열 번호: 8 또는 서열 번호: <strong>12</strong>0; 그리고 서열 번호: 9 중에서 하나 이상의 폴리펩티드 서열, 또는<br />
- 61 -
[0267]<br />
[0268]<br />
[0269]<br />
[0270]<br />
[0271]<br />
[0272]<br />
[0273]<br />
[0274]<br />
[0275]<br />
이들 폴리펩티드 서열의 조합을 포함하는 항체를 고려한다. 본 발명의 또 다른 구체예에서, 본 발명의 항체는<br />
이들 CDR의 조합 및 앞서 열거된 가변 중쇄와 경쇄 서열을 포함한다.<br />
다른 구체예에서, 본 발명에서는 다른 항체, 예를 들면, 서열 번호: 2의 가변 경쇄 서열의 상보성 결정 영역<br />
(CDR, 또는 초가변 영역)에 상응하는 서열 번호: 4; 서열 번호: 5; 그리고 서열 번호: 6 중에서 하나 이상의 폴<br />
리펩티드 서열, 및/또는 서열 번호: 3 또는 서열 번호: <strong>19</strong>의 가변 중쇄 서열의 상보성 결정 영역(CDR, 또는 초<br />
가변 영역)에 상응하는 서열 번호: 7; 서열 번호: 8 또는 서열 번호: <strong>12</strong>0; 그리고 서열 번호: 9 중에서 하나 이<br />
상의 폴리펩티드 서열, 또는 이들 폴리펩티드 서열의 조합을 포함하는 키메라 항체를 고려한다. 본 발명의 또<br />
다른 구체예에서, 본 발명의 항체는 이들 CDR의 조합 및 앞서 열거된 가변 중쇄와 경쇄 서열의 인간화된 이형을<br />
포함한다.<br />
본 발명에서는 또한, IL-6에 결합 특이성을 갖는 항체의 단편을 고려한다. 본 발명의 한 구체예에서, 본 발명의<br />
항체 단편은 서열 번호: 2, 20, 647, 651, 660, 666, 699, 702, 706 또는 709의 폴리펩티드 서열의 인간화된<br />
이형을 포함하거나, 또는 대안으로 이들로 구성된다. 본 발명의 또 다른 구체예에서, 본 발명의 항체 단편은 서<br />
열 번호: 3, 18, <strong>19</strong>, 652, 656, 657, 658, 661, 664, 665, 704 또는 708의 폴리펩티드 서열의 인간화된 이형을<br />
포함하거나, 또는 대안으로 이들로 구성된다.<br />
본 발명의 추가의 구체예에서, IL-6에 결합 특이성을 갖는 항체의 단편은 서열 번호: 2 또는 709의 가변 경쇄<br />
서열의 상보성 결정 영역(CDR, 또는 초가변 영역)에 상응하는 서열 번호: 4; 서열 번호: 5; 그리고 서열 번호:<br />
6 중에서 하나 이상의 폴리펩티드 서열을 포함하거나, 또는 대안으로 이들로 구성된다.<br />
본 발명의 추가의 구체예에서, IL-6에 결합 특이성을 갖는 항체의 단편은 서열 번호: 3과 서열 번호: 657 또는<br />
<strong>19</strong>의 가변 중쇄 서열의 상보성 결정 영역(CDR, 또는 초가변 영역)에 상응하는 서열 번호: 7; 서열 번호: 8 또는<br />
서열 번호: <strong>12</strong>0; 그리고 서열 번호: 9 중에서 하나 이상의 폴리펩티드 서열을 포함하거나, 또는 대안으로 이들<br />
로 구성된다.<br />
본 발명에서는 또한, 본 명세서에서 기술된 하나 이상의 항체 단편을 포함하는 항체 단편을 고려한다. 본 발명<br />
의 한 구체예에서, IL-6에 결합 특이성을 갖는 항체의 단편은 아래의 항체 단편: 서열 번호: 2의 가변 경쇄 영<br />
역; 서열 번호: 3의 가변 중쇄 영역; 서열 번호: 2의 가변 경쇄 영역의 상보성 결정 영역(서열 번호: 4; 서열<br />
번호: 5; 그리고 서열 번호: 6); 그리고 서열 번호: 3과 서열 번호: 657 또는 <strong>19</strong>의 가변 중쇄 영역의 상보성 결<br />
정 영역(서열 번호: 7; 서열 번호: 8 또는 서열 번호: <strong>12</strong>0; 그리고 서열 번호: 9) 중에서 전부를 비롯하여,<br />
1개, 2개, 3개 또는 그 이상을 포함하거나, 또는 대안으로 이들로 구성된다.<br />
본 발명에서는 또한, 서열 번호: 18 또는 서열 번호: <strong>19</strong>의 중쇄 폴리펩티드 서열 중에서 어느 한쪽이 서열<br />
번호: 3 또는 서열 번호: 657의 중쇄 폴리펩티드 서열을 대체하고; 서열 번호: 20의 경쇄 폴리펩티드 서열이 서<br />
열 번호: 2 또는 서열 번호: 709의 경쇄 폴리펩티드 서열을 대체하고; 그리고 서열 번호: <strong>12</strong>0의 중쇄 CDR 서열<br />
이 서열 번호: 8의 중쇄 CDR 서열을 대체하는 변이체를 고려한다.<br />
본 발명의 바람직한 구체예에서, 항-IL-6 항체는 서열 번호: 2와 서열 번호: 3을 포함하는 Ab1, 또는 더욱 구체<br />
적으로, 서열 번호:657과 서열 번호:709(이들은 각각, 서열 번호:700과 서열 번호:723에서 핵산 서열에 의해 인<br />
코딩된다)를 포함하는 항체, 또는 선행 단락에서 열거된 대안적 서열 번호로 구성되는 항체이고, 그리고 본 명<br />
세서에 열거된 생물학적 활성 중에서 적어도 한 가지를 갖는다. 바람직한 구체예에서, 항-IL-6 항체는 도 34-37<br />
에 도시된 바와 같은 인간화 서열을 포함할 것이다.<br />
본 발명의 항-IL-6 항체의 서열은 표 1에 제시된다. Ab1 내지 Ab7의 중쇄와 경쇄의 다른 대안적 형태의 전형적<br />
인 서열 변이체가 제시된다. 본 발명의 항체는 보존성 치환, 하나 이상의 CDR 서열 및/또는 FR 서열의 치환 등<br />
을 비롯하여, 추가의 서열 변이체를 포함한다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
전형적인 Ab1 구체예에는 경쇄 및/또는 중쇄의 변이체를 포함하는 항체가 포함된다. Ab1의 경쇄의 전형적인 변<br />
이체에는 전체 CDR1 서열이 대체되거나, 또는 CDR1 서열 내에서 하나 이상의 잔기가 열거된 임의의 다른 경쇄<br />
CDR1 서열(즉, 서열 번호: 23, 39, 55, 71, 87, 103, <strong>12</strong>4, 140, 156, 172, 188, 204, 220, 236, 252, 268,<br />
284, 300, 316, 332, 348, 364, 380, 396, 4<strong>12</strong>, 428, 444, 460, 476, 492, 508, 524, 540, 556, 또는 572 중<br />
에서 한 가지)의 상응하는 위치에서 잔기에 의해 치환되고; 및/또는 전체 CDR2 서열이 대체되거나, 또는 CDR2<br />
서열 내에서 하나 이상의 잔기가 열거된 임의의 다른 경쇄 CDR2 서열(즉, 서열 번호: 24, 40, 56, 72, 88, 104,<br />
<strong>12</strong>5, 141, 157, 173, 189, 205, 221, 237, 253, 269, 285, 301, 317, 333, 349, 365, 381, 397, 413, 429,<br />
445, 461, 477, 493, 509, 525, 541, 557, 또는 573 중에서 한 가지)의 상응하는 위치에서 잔기에 의해 치환되<br />
- 62 -
[0276]<br />
[0277]<br />
[0278]<br />
[0279]<br />
[0280]<br />
[0281]<br />
[0282]<br />
고; 및/또는 전체 CDR3 서열이 대체되거나, 또는 CDR3 서열 내에서 하나 이상의 잔기가 열거된 임의의 다른 경<br />
쇄 CDR3 서열(즉, 서열 번호: 25, 41, 57, 73, 89, 105, <strong>12</strong>6, 142, 158, 174, <strong>19</strong>0, 206, 222, 238, 254, 270,<br />
286, 302, 318, 334, 350, 366, 382, 398, 414, 430, 446, 462, 478, 494, 510, 526, 542, 558, 또는 574 중<br />
에서 한 가지)의 상응하는 위치에서 잔기에 의해 치환되는 제시된 임의의 Ab1 경쇄 서열(즉, 서열 번호: 2, 20,<br />
647, 651, 660, 666, 699, 702, 706, 또는 709 중에서 한 가지)이 포함된다.<br />
Ab1의 중쇄의 전형적인 변이체에는 전체 CDR1 서열이 대체되거나, 또는 CDR1 서열 내에서 하나 이상의 잔기가<br />
열거된 임의의 다른 중쇄 CDR1 서열(즉, 서열 번호: 26, 42, 58, 74, 90, 106, <strong>12</strong>7, 143, 159, 175, <strong>19</strong>1, 207,<br />
223, 239, 255, 271, 287, 303, 3<strong>19</strong>, 335, 351, 367, 383, 399, 415, 431, 447, 463, 479, 495, 511, 527,<br />
543, 559, 또는 575 중에서 한 가지)의 상응하는 위치에서 잔기에 의해 치환되고; 및/또는 전체 CDR2 서열이 대<br />
체되거나, 또는 CDR2 서열 내에서 하나 이상의 잔기가 Ab1 중쇄 CDR2, 예를 들면, 표 1에 열거된 것들(즉, 서열<br />
번호: 8, 또는 <strong>12</strong>0 중에서 한 가지) 또는 열거된 임의의 다른 중쇄 CDR2 서열(즉, 서열 번호: 27, 43, 59, 75,<br />
91, 107, <strong>12</strong>1, <strong>12</strong>8, 144, 160, 176, <strong>19</strong>2, 208, 224, 240, 256, 272, 288, 304, 320, 336, 352, 368, 384,<br />
400, 416, 432, 448, 464, 480, 496, 5<strong>12</strong>, 528, 544, 560, 또는 576 중에서 한 가지)의 상응하는 위치에서 잔<br />
기에 의해 치환되고; 및/또는 전체 CDR3 서열이 대체되거나, 또는 CDR3 서열 내에서 하나 이상의 잔기가 열거된<br />
임의의 다른 중쇄 CDR3 서열(즉, 서열 번호: 28, 44, 60, 76, 92, 108, <strong>12</strong>9, 145, 161, 177, <strong>19</strong>3, 209, 225,<br />
241, 257, 273, 289, 305, 321, 337, 353, 369, 385, 401, 417, 433, 449, 465, 481, 497, 513, 529, 545,<br />
561, 또는 577 중에서 한 가지)의 상응하는 위치에서 잔기에 의해 치환되는 제시된 임의의 Ab1 중쇄 서열(즉,<br />
서열 번호: 3, 18, <strong>19</strong>, 652, 656, 657, 658, 661, 664, 665, 704, 또는 708 중에서 한 가지)이 포함된다.<br />
다른 구체예에서, 본 발명에서는 다른 항체, 예를 들면, 서열 번호: 2의 가변 경쇄 서열의 상보성 결정 영역<br />
(CDR, 또는 초가변 영역)에 상응하는 서열 번호: 4; 서열 번호: 5; 그리고 서열 번호: 6 중에서 하나 이상의 폴<br />
리펩티드 서열, 및/또는 서열 번호: 3 또는 서열 번호: <strong>19</strong>의 가변 중쇄 서열의 상보성 결정 영역(CDR, 또는 초<br />
가변 영역)에 상응하는 서열 번호: 7(CDR1); 서열 번호: 8(CDR2); 서열 번호: <strong>12</strong>0(CDR2); 그리고 서열 번호:<br />
9(CDR3) 중에서 하나 이상의 폴리펩티드 서열, 또는 이들 폴리펩티드 서열의 조합을 포함하는 키메라 또는 인간<br />
화 항체를 고려한다. 본 발명의 또 다른 구체예에서, 본 발명의 항체는 이들 CDR의 조합 및 도 2와 34-37에 열<br />
거된 것들, 그리고 표 1에서 확인된 것들을 비롯한 앞서 열거된 가변 중쇄와 경쇄 서열을 포함한다.<br />
다른 구체예에서, 본 발명의 항-IL-6 항체는 서열 번호: <strong>12</strong> 또는 서열 번호: 694에서 서열에 의해 인코딩되는<br />
경쇄 CDR1; 서열 번호: 13에서 서열에 의해 인코딩되는 경쇄 CDR2; 서열 번호: 14 또는 서열 번호: 695에서 서<br />
열에 의해 인코딩되는 경쇄 CDR3; 서열 번호: 15에서 서열에 의해 인코딩되는 중쇄 CDR1; 서열 번호: 16 또는<br />
서열 번호: 696에 의해 인코딩되는 중쇄 CDR2; 그리고 서열 번호: 17 또는 서열 번호: 697에 의해 인코딩되는<br />
중쇄 CDR3 중에서 적어도 하나를 포함한다. 이에 더하여, 본 발명은 이런 핵산 서열 및 이들의 변이체를 포함한<br />
다.<br />
다른 구체예에서, 본 발명은 서열 번호: 4(CDR1), 서열 번호: 5(CDR2), 서열 번호: 6(CDR3), 서열 번호: 7, 서<br />
열 번호: <strong>12</strong>0과 서열 번호: 9에서 선택되는, 상기 항-IL-6 항체의 CDR에 상응하는 아미노산 서열에 관계한다.<br />
다른 구체예에서, 본 발명의 항-IL-6 항체는 서열 번호: 10, 662, 698, 701, 705, 720, 721, 722, 또는 723의<br />
경쇄 핵산 서열; 및/또는 서열 번호: 11, 663, 700, 703, 707, 724, 또는 725의 중쇄 핵산 서열을 포함한다.<br />
이에 더하여, 본 발명은 전술한 핵산 서열 및 이들의 조합 중에서 한 가지에 의해 인코딩되는 상응하는 폴리펩<br />
티드에 관계한다.<br />
본 발명의 특정 구체예에서, 항-IL-6 항체 또는 이들의 일부분은 서열 번호: 10, <strong>12</strong>, 13, 14, 662, 694, 695,<br />
698, 701, 705, 720, 721, 722, 723, 11, 15, 16, 17, 663, 696, 697, 700, 703, 707, 724, 그리고 725에 포<br />
함된 것들에서 선택되는 핵산 서열에 의해 인코딩될 것이다. 가령, 경쇄 내에서 CDR1은 서열 번호: <strong>12</strong> 또는 694<br />
에 의해 인코딩될 수 있고, 경쇄 내에서 CDR2는 서열 번호: 13에 의해 인코딩될 수 있고, 경쇄 내에서 CDR3은<br />
서열 번호: 14 또는 695에 의해 인코딩될 수 있다; 중쇄 내에서 CDR1은 서열 번호: 15에 의해 인코딩될 수<br />
있고, 중쇄 내에서 CDR2는 서열 번호: 16 또는 696에 의해 인코딩될 수 있고, 중쇄 내에서 CDR3은 서열 번호:<br />
17 또는 697에 의해 인코딩될 수 있다. 하기에 논의된 바와 같이, 이들 CDR을 포함하는 항체는 본 명세서에 기<br />
술된 인간화 방법에 기초된 적절한 인간 골격을 이용하여 작제될 수 있다.<br />
본 발명의 다른 특정한 구체예에서, 가변 경쇄는 서열 번호: 10, 662, 698, 701, 705, 720, 721, 722, 또는<br />
723에 의해 인코딩되고, 그리고 항-IL-6 항체의 가변 중쇄는 서열 번호: 11, 663, 700, 703, 707, 724, 또는<br />
725에 의해 인코딩될 것이다.<br />
- 63 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0283]<br />
[0284]<br />
[0285]<br />
[0286]<br />
[0287]<br />
[0288]<br />
[0289]<br />
[0290]<br />
[0291]<br />
[0292]<br />
[0293]<br />
[0294]<br />
[0295]<br />
[0296]<br />
[0297]<br />
[0298]<br />
[0299]<br />
[0300]<br />
더욱 특정한 구체예에서, 항-IL-6 항체의 가변 경쇄와 중쇄는 각각, 서열 번호: 10과 11, 또는 서열 번호: 698<br />
과 서열 번호: 700, 또는 서열 번호: 701과 서열 번호: 703, 또는 서열 번호: 705와 서열 번호: 707에 의해 인<br />
코딩될 것이다.<br />
다른 특정한 구체예에서, 본 발명은 임의의 전술한 핵산 서열과 이들의 조합을 포함하는 핵산 구조체, 그리고<br />
이들 핵산 서열과 구조체를 내포하는 재조합 세포를 커버하고, 여기서 이들 핵산 서열 또는 구조체는 염색체외<br />
이거나, 또는 숙주 세포 게놈 내로 통합될 수 있다.<br />
다른 특정한 구체예에서, 본 발명은 서열 번호: 4, 서열 번호: 5, 서열 번호: 6, 서열 번호: 7, 서열 번호: 8,<br />
서열 번호: <strong>12</strong>0, 서열 번호: 9, 또는 서열 번호: 2, 20, 647, 651, 660, 666, 699, 702, 706, 또는 709에 포함<br />
되는 임의의 가변 경쇄 폴리펩티드 및/또는 서열 번호: 3, 18, <strong>19</strong>, 652, 656, 657, 658, 661, 664, 665, 704,<br />
또는 708에 포함되는 임의의 가변 중쇄 폴리펩티드를 포함하는 폴리펩티드에 열거된 임의의 CDR 또는 이들의 조<br />
합을 포함하는 폴리펩티드를 커버한다. 이들 폴리펩티드는 선택적으로, 다른 면역글로불린 폴리펩티드 또는 이<br />
펙터 모이어티, 예를 들면, 치료 또는 검출 존재물에 직접적으로 또는 간접적으로 부착될 수 있다.<br />
다른 구체예에서, 항-IL-6 항체는 서열 번호: 10 또는 서열 번호: 698 또는 서열 번호: 701 또는 서열 번호:<br />
705에서 서열에 의해 인코딩되는 가변 경쇄, 그리고 서열 번호: 11 또는 서열 번호: 700 또는 서열 번호: 703<br />
또는 서열 번호: 707에서 서열에 의해 인코딩되는 가변 사슬 중에서 적어도 하나를 포함한다.<br />
다른 구체예에서, 항-IL-6 항체는 골격 및/또는 CDR 서열 내에 하나 이상의 치환을 보유하고 시험관내에서 및/<br />
또는 생체내 투여에서 Ab1의 한 가지 이상의 특성을 갖는 전술한 서열의 변이체이다.<br />
이들 시험관내와 생체내 특성은 하기 실시예에서 더욱 상세하게 기술되고, 여기에는 IL-6 및/또는 이의 펩티드<br />
에 결합하는 것에 대하여 Ab1과의 경쟁; 대략 50 피코몰(picomolar) 미만의 IL-6에 대한 결합 친화성(Kd), 및/<br />
또는 10 -4<br />
S -1<br />
이하의 IL-6로부터 해리 속도(Koff); 건강한 인간 개체에서 적어도 대략 22일의 생체내 반감기; 저<br />
알부민혈증(hypoalbunemia)을 예방하거나 치료하는 능력; 상승된 CRP를 예방하거나 치료하는 능력; 비정상적인<br />
응고를 예방하거나 치료하는 능력; 및/또는 혈전증(thrombosis)의 증가된 위험과 연관된 질환 또는 이상을 앓는<br />
개체에서 혈전증의 위험을 감소시키는 능력이 포함된다. 항-IL-6 활성의 추가의 무제한적 실례는 예로써, 표제<br />
"항-IL-6 활성"하에 본 명세서에서 기술된다.<br />
다른 구체예에서, 항-IL-6 항체는 하나 이상의 Ab1 경쇄 및/또는 중쇄 CDR 서열(표 1 참조), 또는 시험관내에서<br />
및/또는 생체내 투여에서 Ab1의 한 가지 이상의 특성(이런 특성의 실례는 전술한 단락에서 제시된다)을 갖는 이<br />
들의 변이체(들)을 포함한다. 당업자는 예로써, 인간 또는 다른 포유동물 골격 서열, 또는 SMIP, 카멜바디, 나<br />
노바디, IgNAR 또는 다른 면역글로불린 또는 다른 조작된 항체로부터 유래된 이들의 기능적 오르토로그<br />
(ortholog)를 포함하는 하나 이상의 뼈대(scaffold)에 연쇄에 의해 이들 CDR 서열을 결합시켜 항원-결합 표면을<br />
형성하는 방법을 이해할 것이다. 가령, 구체예는 특히, 인간 IL-6에 결합하고, 그리고 아래의 CDR 서열 또는 이<br />
들의 변이체 중에서 1개, 2개, 3개, 4개, 5개, 6개, 또는 그 이상을 포함한다:<br />
서열 번호: 4의 경쇄 CDR1에 적어도 72.7%(즉, 11개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 4의 경쇄 CDR1에 적어도 81.8%(즉, 11개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 4의 경쇄 CDR1에 적어도 90.9%(즉, 11개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 4의 경쇄 CDR1에 100%(즉, 11개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 5의 경쇄 CDR2에 적어도 85.7%(즉, 7개 아미노산 중에서 6개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 5의 경쇄 CDR2에 100%(즉, 7개 아미노산 중에서 7개) 동일성을 갖는 폴리펩티드;<br />
공개특허 10-2011-01<strong>12</strong>308<br />
서열 번호: 6의 경쇄 CDR3에 적어도 50%(즉, <strong>12</strong>개 아미노산 중에서 6개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 58.3%(즉, <strong>12</strong>개 아미노산 중에서 7개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드;<br />
- 64 -
[0301]<br />
[0302]<br />
[0303]<br />
[0304]<br />
[0305]<br />
[0306]<br />
[0307]<br />
[0308]<br />
[0309]<br />
[0310]<br />
[0311]<br />
[03<strong>12</strong>]<br />
[0313]<br />
[0314]<br />
[0315]<br />
[0316]<br />
[0317]<br />
[0318]<br />
[03<strong>19</strong>]<br />
[0320]<br />
[0321]<br />
[0322]<br />
[0323]<br />
[0324]<br />
[0325]<br />
[0326]<br />
[0327]<br />
[0328]<br />
[0329]<br />
[0330]<br />
[0331]<br />
[0332]<br />
[0333]<br />
[0334]<br />
[0335]<br />
[0336]<br />
서열 번호: 6의 경쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 7의 중쇄 CDR1에 적어도 80%(즉, 5개 아미노산 중에서 4개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 7의 중쇄 CDR1에 100%(즉, 5개 아미노산 중에서 5개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 50%(즉, 16개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 56.2%(즉, 16개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 62.5%(즉, 16개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 68.7%(즉, 16개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 75%(즉, 16개 아미노산 중에서 <strong>12</strong>개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 81.2%(즉, 16개 아미노산 중에서 13개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 87.5%(즉, 16개 아미노산 중에서 14개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 93.7%(즉, 16개 아미노산 중에서 15개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 100%(즉, 16개 아미노산 중에서 16개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 33.3%(즉, <strong>12</strong>개 아미노산 중에서 4개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 41.6%(즉, <strong>12</strong>개 아미노산 중에서 5개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 50%(즉, <strong>12</strong>개 아미노산 중에서 6개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 58.3%(즉, <strong>12</strong>개 아미노산 중에서 7개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 동일성을 갖는 폴리펩티드;<br />
서열 번호: 4의 경쇄 CDR1에 적어도 90.9%(즉, 11개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 4의 경쇄 CDR1에 100%(즉, 11개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 5의 경쇄 CDR2에 적어도 85.7%(즉, 7개 아미노산 중에서 6개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 5의 경쇄 CDR2에 100%(즉, 7개 아미노산 중에서 7개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 6의 경쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 7의 중쇄 CDR1에 적어도 80%(즉, 5개 아미노산 중에서 4개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 7의 중쇄 CDR1에 100%(즉, 5개 아미노산 중에서 5개) 유사성을 갖는 폴리펩티드;<br />
공개특허 10-2011-01<strong>12</strong>308<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 56.2%(즉, 16개 아미노산 중에서 9개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 62.5%(즉, 16개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 68.7%(즉, 16개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드;<br />
- 65 -
[0337]<br />
[0338]<br />
[0339]<br />
[0340]<br />
[0341]<br />
[0342]<br />
[0343]<br />
[0344]<br />
[0345]<br />
[0346]<br />
[0347]<br />
[0348]<br />
[0349]<br />
[0350]<br />
[0351]<br />
[0352]<br />
[0353]<br />
[0354]<br />
[0355]<br />
[0356]<br />
[0357]<br />
[0358]<br />
[0359]<br />
[0360]<br />
[0361]<br />
[0362]<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 75%(즉, 16개 아미노산 중에서 <strong>12</strong>개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 81.2%(즉, 16개 아미노산 중에서 13개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 87.5%(즉, 16개 아미노산 중에서 14개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 93.7%(즉, 16개 아미노산 중에서 15개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 100%(즉, 16개 아미노산 중에서 16개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 50%(즉, <strong>12</strong>개 아미노산 중에서 6개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 58.3%(즉, <strong>12</strong>개 아미노산 중에서 7개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드;<br />
서열 번호: 9의 중쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 유사성을 갖는 폴리펩티드.<br />
다른 예시적인 구체예에는 전술한 것들 중에서 한 가지를 인코딩하는 하나 이상의 폴리뉴클레오티드, 예를<br />
들면, 인간 IL-6에 특이적으로 결합하고, 그리고 아래의 CDR 서열 또는 이들의 변이체 중에서 1개, 2개, 3개, 4<br />
개, 5개, 6개, 또는 그 이상을 포함하는 폴리펩티드를 인코딩하는 폴리뉴클레오티드가 포함된다:<br />
서열 번호: 4의 경쇄 CDR1에 적어도 72.7%(즉, 11개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 4의 경쇄 CDR1에 적어도 81.8%(즉, 11개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 4의 경쇄 CDR1에 적어도 90.9%(즉, 11개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 4의 경쇄 CDR1에 100%(즉, 11개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드를 인코딩하는 폴<br />
리뉴클레오티드;<br />
서열 번호: 5의 경쇄 CDR2에 적어도 85.7%(즉, 7개 아미노산 중에서 6개) 동일성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 5의 경쇄 CDR2에 100%(즉, 7개 아미노산 중에서 7개) 동일성을 갖는 폴리펩티드를 인코딩하는 폴리<br />
뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 50%(즉, <strong>12</strong>개 아미노산 중에서 6개) 동일성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 58.3%(즉, <strong>12</strong>개 아미노산 중에서 7개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
공개특허 10-2011-01<strong>12</strong>308<br />
서열 번호: 6의 경쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 동일성을 갖는 폴리펩티드를 인코딩하는 폴<br />
- 66 -
[0363]<br />
[0364]<br />
[0365]<br />
[0366]<br />
[0367]<br />
[0368]<br />
[0369]<br />
[0370]<br />
[0371]<br />
[0372]<br />
[0373]<br />
[0374]<br />
[0375]<br />
[0376]<br />
[0377]<br />
[0378]<br />
[0379]<br />
[0380]<br />
[0381]<br />
[0382]<br />
[0383]<br />
리뉴클레오티드;<br />
서열 번호: 7의 중쇄 CDR1에 적어도 80%(즉, 5개 아미노산 중에서 4개) 동일성을 갖는 폴리펩티드를 인코딩하는<br />
폴리뉴클레오티드;<br />
서열 번호: 7의 중쇄 CDR1에 100%(즉, 5개 아미노산 중에서 5개) 동일성을 갖는 폴리펩티드를 인코딩하는 폴리<br />
뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 50%(즉, 16개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 56.2%(즉, 16개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 62.5%(즉, 16개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 68.7%(즉, 16개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 75%(즉, 16개 아미노산 중에서 <strong>12</strong>개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 81.2%(즉, 16개 아미노산 중에서 13개) 동일성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 87.5%(즉, 16개 아미노산 중에서 14개) 동일성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 93.7%(즉, 16개 아미노산 중에서 15개) 동일성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 100%(즉, 16개 아미노산 중에서 16개) 동일성을 갖는 폴리펩티드를 인코딩하는<br />
폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 33.3%(즉, <strong>12</strong>개 아미노산 중에서 4개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 41.6%(즉, <strong>12</strong>개 아미노산 중에서 5개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 50%(즉, <strong>12</strong>개 아미노산 중에서 6개) 동일성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 58.3%(즉, <strong>12</strong>개 아미노산 중에서 7개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 동일성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 동일성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 동일성을 갖는 폴리펩티드를 인코딩하는 폴<br />
리뉴클레오티드;<br />
공개특허 10-2011-01<strong>12</strong>308<br />
서열 번호: 4의 경쇄 CDR1에 적어도 90.9%(즉, 11개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드를 인코딩<br />
- 67 -
[0384]<br />
[0385]<br />
[0386]<br />
[0387]<br />
[0388]<br />
[0389]<br />
[0390]<br />
[0391]<br />
[0392]<br />
[0393]<br />
[0394]<br />
[0395]<br />
[0396]<br />
[0397]<br />
[0398]<br />
[0399]<br />
[0400]<br />
[0401]<br />
[0402]<br />
[0403]<br />
[0404]<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 4의 경쇄 CDR1에 100%(즉, 11개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드를 인코딩하는 폴<br />
리뉴클레오티드;<br />
서열 번호: 5의 경쇄 CDR2에 적어도 85.7%(즉, 7개 아미노산 중에서 6개) 유사성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 5의 경쇄 CDR2에 100%(즉, 7개 아미노산 중에서 7개) 유사성을 갖는 폴리펩티드를 인코딩하는 폴리<br />
뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 유사성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 유사성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 6의 경쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 유사성을 갖는 폴리펩티드를 인코딩하는 폴<br />
리뉴클레오티드;<br />
서열 번호: 7의 중쇄 CDR1에 적어도 80%(즉, 5개 아미노산 중에서 4개) 유사성을 갖는 폴리펩티드를 인코딩하는<br />
폴리뉴클레오티드;<br />
서열 번호: 7의 중쇄 CDR1에 100%(즉, 5개 아미노산 중에서 5개) 유사성을 갖는 폴리펩티드를 인코딩하는 폴리<br />
뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 56.2%(즉, 16개 아미노산 중에서 9개) 유사성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 62.5%(즉, 16개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 68.7%(즉, 16개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 75%(즉, 16개 아미노산 중에서 <strong>12</strong>개) 유사성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 81.2%(즉, 16개 아미노산 중에서 13개) 유사성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 87.5%(즉, 16개 아미노산 중에서 14개) 유사성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 적어도 93.7%(즉, 16개 아미노산 중에서 15개) 유사성을 갖는 폴리펩티드를 인코<br />
딩하는 폴리뉴클레오티드;<br />
서열 번호: <strong>12</strong>0의 중쇄 CDR2에 100%(즉, 16개 아미노산 중에서 16개) 유사성을 갖는 폴리펩티드를 인코딩하는<br />
폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 50%(즉, <strong>12</strong>개 아미노산 중에서 6개) 유사성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 58.3%(즉, <strong>12</strong>개 아미노산 중에서 7개) 유사성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
공개특허 10-2011-01<strong>12</strong>308<br />
서열 번호: 9의 중쇄 CDR3에 적어도 66.6%(즉, <strong>12</strong>개 아미노산 중에서 8개) 유사성을 갖는 폴리펩티드를 인코딩<br />
- 68 -
[0405]<br />
[0406]<br />
[0407]<br />
[0408]<br />
[0409]<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 75%(즉, <strong>12</strong>개 아미노산 중에서 9개) 유사성을 갖는 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 83.3%(즉, <strong>12</strong>개 아미노산 중에서 10개) 유사성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 적어도 91.6%(즉, <strong>12</strong>개 아미노산 중에서 11개) 유사성을 갖는 폴리펩티드를 인코딩<br />
하는 폴리뉴클레오티드;<br />
서열 번호: 9의 중쇄 CDR3에 100%(즉, <strong>12</strong>개 아미노산 중에서 <strong>12</strong>개) 유사성을 갖는 폴리펩티드를 인코딩하는 폴<br />
리뉴클레오티드.<br />
표 1<br />
- 69 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0410]<br />
- 70 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0411]<br />
[04<strong>12</strong>]<br />
[0413]<br />
[0414]<br />
[0415]<br />
[0416]<br />
* 중쇄와 경쇄의 전형적인 서열 변이체 형태는 별도의 라인에 도시된다.<br />
PRT.: 폴리펩티드 서열.<br />
Nuc.: 전형적인 코딩 서열.<br />
참고를 위하여, 표 1에 포함된 것들 이외의 서열 식별자가 표 2에 요약된다.<br />
- 71 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0417]<br />
[0418]<br />
[04<strong>19</strong>]<br />
[0420]<br />
[0421]<br />
[0422]<br />
[0423]<br />
[0424]<br />
표 2<br />
본 출원에서 서열 식별자의 요약<br />
서열 번호: 설명<br />
1 인간 IL-6<br />
586 카파 불변 경쇄 폴리펩티드 서열<br />
587 카파 불변 경쇄 폴리뉴클레오티드 서열<br />
588 감마-1 불변 중쇄 폴리펩티드 서열<br />
589 감마-1 불변 중쇄 폴리뉴클레오티드 서열<br />
590 - 646 인간 IL-6 펩티드(도 <strong>12</strong>와 실시예 14 참조)<br />
7<strong>19</strong> 감마-1 불변 중쇄 폴리펩티드 서열(두 위치에서 서열 번호: 518과 상이함)<br />
726 C-반응성 단백질 폴리펩티드 서열<br />
727 IL-6 수용체 알파<br />
728 IL-6 수용체 베타 / gp130<br />
이런 항체 단편 또는 변이체는 아래의 무제한적 형태: Fab, Fab', F(ab')2, Fv와 단일 쇄 Fv 항체 형태 중에서<br />
한 가지 이상으로 존재할 수 있다. 바람직한 구체예에서, 본 명세서에서 기술된 항-IL-6 항체는 하기에 열거된<br />
서열을 포함하는 카파 불변 경쇄 서열을 추가로 포함한다:<br />
VAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNR<br />
GEC (서열 번호: 586).<br />
다른 바람직한 구체예에서, 본 명세서에서 기술된 항-IL-6 항체는 하기에 열거된 서열 중에서 하나를 포함하는<br />
감마-1 불변 중쇄 폴리펩티드 서열을 추가로 포함한다:<br />
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVD<strong>KR</strong>VEPKS<br />
CDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKC<br />
KVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVF<br />
SCSVMHEALHNHYTQKSLSLSPGK (서열 번호: 588); 그리고<br />
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVD<strong>KR</strong>VEPKS<br />
CDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKC<br />
KVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVF<br />
SCSVMHEALHNHYTQKSLSLSPGK (서열 번호: 7<strong>19</strong>).<br />
본 명세서에서 기술된 항체의 구체예에는 리더 서열, 예를 들면, 토끼 Ig 리더, 알부민 프리-펩티드, 효모 교배<br />
인자 프리 프로(pre pro) 분비 리더 서열(가령, 피치아 파스토리스(P. pastoris) 또는 사카로마이세스 세레비지<br />
애(Saccharomyces cerevisiae) a 또는 알파 인자), 또는 인간 HAS 리더를 포함할 수 있다. 전형적인 리더 서열<br />
은 아래와 같이, 도 36A와 37A에 도시된 폴리펩티드의 N-말단에서 FR1로부터 나란히 도시된다: 서열 번호: 2와<br />
660(MD. . .) 및 서열 번호: 3과 661(ME. . .)에서 토끼 Ig 리더 서열; 그리고, 분비를 용이하게 하는 서열 번<br />
호: 706과 708에서 알부민 프리펩티드. 원하는 특성, 예를 들면, 분비, 개선된 안정성 또는 반감기 등을 제공하<br />
는 당분야에 공지된 다른 리더 서열 역시 중쇄 및/또는 경쇄 상에서, 단독으로 또는 서로 조합으로 이용될 수<br />
있고, 이들은 개체에 투여에 앞서 선택적으로 절단될 수 있다. 가령, 폴리펩티드는 리더 서열을 절단하는 프로<br />
테아제, 예를 들면, 막-결합된 신호 펩티다아제를 발현하거나 포함하는(또는 발현하거나 포함하도록 변형되는)<br />
세포 또는 세포-없는 발현 시스템에서 발현될 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
다른 구체예에서, 본 발명에서는 서열 번호: 3, 18, <strong>19</strong>, 22, 38, 54, 70, 86, 102, 117, 118, <strong>12</strong>3, 139, 155,<br />
171, 187, 203, 2<strong>19</strong>, 235, 251, 267, 283, 299, 315, 331, 347, 363, 379, 395, 411, 427, 443, 459, 475,<br />
491, 507, 523, 539, 555, 571, 652, 656, 657, 658, 661, 664, 665, 668, 672, 676, 680, 684, 688, 691,<br />
692, 704, 또는 708을 포함하는 VH 폴리펩티드 서열을 포함하고; 그리고 서열 번호: 2, 20, 21, 37, 53, 69,<br />
85, 101, 1<strong>19</strong>, <strong>12</strong>2, 138, 154, 170, 186, 202, 218, 234, 250, 266, 282, 298, 314, 330, 346, 362, 378,<br />
394, 410, 426, 442, 458, 474, 490, 506, 522, 538, 554, 570, 647, 651, 660, 666, 667, 671, 675, 679,<br />
683, 687, 693, 699, 702, 706, 또는 709를 포함하는 VL 폴리펩티드 서열을 추가로 포함하는 분리된 항-IL-6 항<br />
체, 또는 상기 VH 또는 VL 폴리펩티드 내에서 하나 이상의 골격 잔기(FR 잔기) 또는 CDR 잔기가 다른 아미노산<br />
- 72 -
[0425]<br />
[0426]<br />
[0427]<br />
[0428]<br />
[0429]<br />
[0430]<br />
잔기로 치환되어 IL-6에 특이적으로 결합하는 항-IL-6 항체를 생성시키는 이의 변이체를 고려한다. 본 발명에서<br />
는 이들 항체의 인간화와 키메라 형태를 고려하고, 여기서 바람직하게는 FR은 모 항체에 고도로 상동성인 인간<br />
FR을 포함할 것이다. 키메라 항체는 IgG1, IgG2, IgG3, IgG4, IgG5, IgG6, IgG7, IgG8, IgG9, IgG10, IgG11,<br />
IgG<strong>12</strong>, IgG13, IgG14, IgG15, IgG16, IgG17, IgG18 또는 IgG<strong>19</strong> 불변 영역으로부터 유래된 Fc, 그리고 특히, 서<br />
열 번호:588과 서열 번호:586 내에 포함된 바와 같은 가변 중쇄와 경쇄 불변 영역을 포함할 수 있다.<br />
본 발명의 한 구체예에서, 이들 항체 또는 VH 또는 VL 폴리펩티드는 본 명세서에 언급된 인간화 과정의 시작에<br />
앞서, 하나 이상의 토끼 B 세포 집단으로부터 기원하거나, 또는 이들로부터 선택된다.<br />
본 발명의 또 다른 구체예에서, 항-IL-6 항체 및 이들의 단편과 변이체는 인간 IL-6 단백질의 영장류 동족체에<br />
대한 결합 특이성을 갖는다. 인간 IL-6 단백질의 영장류 동족체의 무제한적 실례는 게잡이원숭이(Macaca<br />
fascicularis)(일명, 필리핀 원숭이) 및 붉은털원숭이(Rhesus monkey)로부터 획득된 IL-6이다. 본 발명의 또<br />
다른 구체예에서, 항-IL-6 항체 및 이들의 단편과 변이체는 IL-6과 IL-6R의 결합, 및/또는 IL-6/IL-6R/gp130<br />
복합체의 생산 및/또는 IL-6/IL-6R/gp130 멀티머의 생산을 저해하고 및/또는 전술한 한 가지 이상의 생물학적<br />
효과를 중화시킨다.<br />
앞서 언급된 바와 같이, 항체 및 이들의 단편과 변이체는 이펙터 모이어티, 예를 들면, 화학적 링커, 검출가능<br />
모이어티, 예를 들면, 형광 염료, 효소, 기질, 생물발광 물질, 방사성 물질, 그리고 화학발광 모이어티, 또는<br />
기능성 모이어티, 예를 들면, 스트렙타비딘, 아비딘, 비오틴, 세포독소, 세포독성제, 그리고 방사성 물질을 부<br />
가하기 위하여 번역후 변형될 수 있다.<br />
검출가능 모이어티와 관련하여, 추가의 예시적인 효소에는 양고추냉이 과산화효소, 아세틸콜린에스테라아제, 알<br />
칼리성 포스파타아제, 베타-갈락토시다아제와 루시페라아제가 포함되지만 이들에 국한되지 않는다. 추가의 예시<br />
적인 형광 물질에는 로다민, 플루오레세인, 플루오레세인 이소티오시아네이트, 움벨리페론, 디클로로트리아지닐<br />
아민, 피코에리트린과 염화단실이 포함되지만 이들에 국한되지 않는다. 추가의 예시적인 화학발광 모이어티에는<br />
루미놀이 포함되지만 이에 국한되지 않는다. 추가의 예시적인 생물발광 물질에는 루시페린과 에쿼린이 포함되지<br />
만 이들에 국한되지 않는다. 추가의 예시적인 방사성 물질에는 요오드 <strong>12</strong>5( <strong>12</strong>5<br />
I), 탄소 14( 14<br />
C), 황 35( 35<br />
S), 트<br />
리튬( 3<br />
H)과 인 32( 32<br />
P)가 포함되지만 이들에 국한되지 않는다.<br />
기능성 모이어티와 관련하여, 예시적인 세포독성제에는 메토트렉세이트, 아미노프테린, 6-메르캅토퓨린, 6-티오<br />
구아닌, 시타라빈, 5-플루오르우라실 데카르바진; 알킬화제, 예를 들면, 메클로레타민, 티오테파 클로람부실,<br />
멜팔란, 카르무스틴(BSNU), 미토마이신 C, 로무스틴(CCNU), 1-메틸니트로소우레아, 시클로포스파미드, 메클로레<br />
타민, 부설판, 디브로모만니톨, 스트렙토조토신, 미토마이신 C, cis-디클로로디아민 백금(II)(DDP) 시스플라틴<br />
과 카르보플라틴(파라플라틴); 안트라사이클린, 예를 들면, 다우노루비신(이전에 다우노마이신), 독소루비신(아<br />
드리아마이신), 데토루비신, 카르미노마이신, 이다루비신, 에피루비신, 미톡산트론과 비산트렌; 항생제, 예를<br />
들면, 닥티노마이신(악티노마이신 D), 블레오마이신, 칼리케마이신, 미트라마이신, 그리고 안트라마이신(AMC);<br />
그리고 항유사분열제, 예를 들면, 빈카 알칼로이드, 빈크리스틴과 빈블라스틴이 포함되지만 이들에 국한되지 않<br />
는다. 다른 세포독성제에는 파클리탁셀(탁솔), 리신, 슈도모나스 외독소, 젬시타빈, 시토칼라신 B, 그라미시딘<br />
D, 브롬화에티듐, 에메틴, 에토포시드, 테노포시드, 콜히친, 디히드록시 안트라신 디온, 1-데히드로테스토스테<br />
론, 글루코코르티코이드, 프로카인, 테트라카인, 리도카인, 프로파라놀롤, 퓨로마이신, 프로카르바진, 히드록시<br />
우레아, 아스파라기나아제, 코르티코스테로이드, 미토탄(O,P'-(DDD)), 인터페론, 그리고 이들 세포독성제의 혼<br />
합물이 포함되지만 이들에 국한되지 않는다.<br />
추가의 세포독성제에는 화학요법제, 예를 들면, 카르보플라틴, 시스플라틴, 파클리탁셀, 젬시타빈, 칼리케아미<br />
신, 독소루비신, 5-플루오르우라실, 미토마이신 C, 악티노마이신 D, 시클로포스파미드, 빈크리스틴, 블레오마이<br />
신, VEGF 길항제, EGFR 길항제, 플라틴, 탁솔, 이리노테칸, 5-플루오르우라실, 젬시타빈, 류코보린,<br />
스테로이드, 시클로포스파미드, 멜팔란, 빈카 알칼로이드(가령, 빈블라스틴, 빈크리스틴, 빈데신과 비노렐빈),<br />
무스틴, 티로신 키나아제 저해제, 방사선요법, 성 호르몬 길항제, 선택성 안드로겐 수용체 조절제, 선택성 에스<br />
트로겐 수용체 조절제, PDGF 길항제, TNF 길항제, IL-1 길항제, 인터루킨(가령 IL-<strong>12</strong> 또는 IL-2), IL-<strong>12</strong>R 길항<br />
제, 독소 접합된 단일클론 항체, 종양 항원 특이적 단일클론 항체, Erbitux, Avastin, Pertuzumab, 항-<br />
CD20 항체, Rituxan<br />
, 오크렐리주맙, 오파투무맙, DXL625, Herceptin<br />
- 73 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0431]<br />
[0432]<br />
[0433]<br />
[0434]<br />
[0435]<br />
[0436]<br />
[0437]<br />
, 또는 이들의 임의의 조합이 포함되지만 이들에 국한되지 않는다. 식물과 세균으로부터 독성 효소, 예를 들면,<br />
리신, 디프테리아 독소와 슈도모나스(Pseudomonas) 독소는 세포-유형-특이적-사멸 반응물을 생성시키기 위하여<br />
인간화 항체, 또는 이들의 결합 단편에 접합될 수 있다(Youle, et al., Proc. Nat'l Acad. Sci. USA 77:5483<br />
(<strong>19</strong>80); Gilliland, et al., Proc. Nat'l Acad. Sci. USA 77:4539 (<strong>19</strong>80); Krolick, et al., Proc. Nat'l<br />
Acad. Sci. USA 77:54<strong>19</strong> (<strong>19</strong>80)).<br />
다른 세포독성제에는 U.S. Pat. No. 6,653,104에서 Goldenberg에 의해 기술된 바와 같은 세포독성 리보뉴클레아<br />
제가 포함된다. 본 발명의 구체예는 또한, 방사성면역접합체에 관계하고, 여기서 알파 또는 베타 입자를 방출하<br />
는 방사성핵종은 복합체-형성제의 이용으로, 또는 이러한 이용 없이 항체, 또는 이의 결합 단편에 안정적으로<br />
결합된다. 이런 방사성핵종에는 베타-방사체, 예를 들면, 인-32( 32<br />
P), 스칸듐-47( 47<br />
Sc), 구리-67( 67<br />
Cu), 갈륨-<br />
67( 67<br />
Ga), 이트륨-88( 88<br />
Y), 이트륨-90( 90<br />
Y), 요오드-<strong>12</strong>5( <strong>12</strong>5<br />
I), 요오드-131( 131<br />
I), 사마륨-153( 153<br />
Sm), 루테튬-<br />
177( 177<br />
Lu), 레늄-186( 186<br />
Re) 또는 레늄-188( 188<br />
Re), 그리고 알파-방사체, 예를 들면, 아스타틴-211( 211<br />
At), 납-<br />
2<strong>12</strong>( 2<strong>12</strong><br />
Pb), 비스무트-2<strong>12</strong>( 2<strong>12</strong><br />
Bi) 또는 -213( 213<br />
Bi) 또는 악티늄-225( 225<br />
Ac)가 포함된다.<br />
검출가능 모이어티 등에 항체 또는 이의 결합 단편을 접합하는 방법, 예를 들면, Hunter et al, Nature 144:945<br />
(<strong>19</strong>62); David et al, Biochemistry 13:1014 (<strong>19</strong>74); Pain et al, J. Immunol. Meth. 40:2<strong>19</strong> (<strong>19</strong>81); 그리고<br />
Nygren, J., Histochem. and Cytochem. 30:407 (<strong>19</strong>82)에서 기술된 방법은 당분야에 공지되어 있다.<br />
본 명세서에서 기술된 구체예는 본 명세서에 열거된 항체, 항체 단편, 디아바디, SMIP, 카멜바디, 나노바디,<br />
IgNAR, 폴리펩티드, 가변 영역과 CDR에 실질적으로 상동성인 변이체와 등가물을 추가로 포함한다. 이들은 예로<br />
써, 보존성 치환 돌연변이(즉, 하나 이상의 아미노산의 유사한 아미노산에 의한 치환)를 보유할 수 있다. 가령,<br />
보존성 치환은 동일한 보편적 부류 내에서 한 아미노산의 다른 아미노산으로 치환, 예를 들면, 산성 아미노산의<br />
다른 산성 아미노산으로 치환, 염기성 아미노산의 다른 염기성 아미노산으로 치환, 또는 중성 아미노산의 다른<br />
중성 아미노산으로 치환을 지칭한다. 보존적 아미노산 치환에 의해 의도되는 것은 당분야에 널리 공지되어<br />
있다.<br />
다른 구체예에서, 본 발명에서는 본 명세서에 열거된 항체 단편, 가변 영역과 CDR 중에서 하나 이상의 폴리펩티<br />
드 서열에 적어도 90% 이상의 서열 상동성을 갖는 폴리펩티드 서열을 고려한다. 더욱 바람직하게는, 본 발명에<br />
서는 본 명세서에 열거된 항체 단편, 가변 영역과 CDR 중에서 하나 이상의 폴리펩티드 서열에 적어도 95% 이상<br />
의 서열 상동성, 더욱 바람직하게는 적어도 98% 이상의 서열 상동성, 그리고 이보다 더욱 바람직하게는 적어도<br />
99% 이상의 서열 상동성을 갖는 폴리펩티드 서열을 고려한다. 핵산과 아미노산 서열 사이에 상동성을 결정하는<br />
방법은 당업자에게 널리 공지되어 있다.<br />
다른 구체예에서, 본 발명에서는 본 명세서에서 열거되고, 또한 항-IL-6 활성을 갖는, 이들 항체 단편, 가변 영<br />
역과 CDR의 앞서 열거된 폴리펩티드 동족체를 고려한다. 항-IL-6 활성의 무제한적 실례는 예로써, 표제 "항-IL-<br />
6 활성"하에 본 명세서에서 기술된다.<br />
다른 구체예에서, 본 발명에서는 또한, 임의의 전술한 서열에 결합하는 항-이디오타입 항체의 산출과 용도를 고<br />
려한다. 예시적인 구체예에서, 이런 항-이디오타입 항체는 항-IL-6 항체의 효과를 조절, 감소, 또는 중화시키기<br />
위하여, 항-IL-6 항체를 섭취하는 개체에 투여될 수 있다. 이런 항-이디오타입 항체는 또한, 항-IL-6 항체의 존<br />
재로 특징되는 자가면역 질환의 치료에 유용할 수 있다. 이런 항-이디오타입 항체의 추가의 예시적인 용도는 예<br />
로써, 개체의 혈액 또는 다른 체액 내에 존재하는 항-IL-6 항체의 수준을 모니터하기 위한 본 발명의 항-IL-6<br />
항체의 검출이다.<br />
본 발명에서는 또한, 본 명세서에서 기술된 임의의 다른 폴리뉴클레오티드 서열을 대체하는 본 명세서에서 기술<br />
된 임의의 폴리펩티드 또는 폴리뉴클레오티드 서열을 포함하는 항-IL-6 항체를 고려한다. 가령, 한정됨 없이,<br />
본 발명에서는 본 명세서에서 기술된 임의의 가변 경쇄 및 가변 중쇄 서열의 조합을 포함하는 항체를 고려하고,<br />
또한 본 명세서에서 기술된 임의의 다른 CDR 서열에 대한 본 명세서에서 기술된 임의의 CDR 서열의 치환에 기인<br />
하는 항체를 고려한다. 언급된 바와 같이, 선호되는 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 도 34 또는<br />
35에서 도시된 바와 같은 가변 중쇄 및/또는 경쇄 서열, 예를 들면, 서열 번호: 651, 657, 709, 또는 IL-6에 항<br />
체 결합 또는 다른 원하는 기능적 활성에 부정적인 영향을 주지 않으면서 하나 이상의 CDR 또는 FR 잔기가 변형<br />
되는 이들의 변이체를 포함할 수 있다.<br />
- 74 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0438]<br />
[0439]<br />
[0440]<br />
[0441]<br />
[0442]<br />
[0443]<br />
[0444]<br />
[0445]<br />
항-IL-6 항체 폴리펩티드를 인코딩하는 폴리뉴클레오티드<br />
더 나아가, 본 발명은 IL-6에 결합 특이성을 갖는 항체의 폴리펩티드를 인코딩하는 폴리뉴클레오티드에 관계한<br />
다. 본 발명의 한 구체예에서, 본 발명의 폴리뉴클레오티드는 서열 번호: 2의 가변 경쇄 폴리펩티드 서열을 인<br />
코딩하는 아래의 폴리뉴클레오티드 서열:<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCGGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCATTAACAATGAATTATCCTGGTATCAGCAGAAACCAGGGCAGCGTCCCAAGCTC<br />
CTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCTTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTAGCG<br />
GCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTT (서열 번호: 10),<br />
또는 서열 번호: 662, 698, 701 또는 705의 폴리뉴클레오티드 서열을 포함하거나, 또는 대안으로 이러한 서열로<br />
구성된다<br />
본 발명의 다른 구체예에서, 본 발명의 폴리뉴클레오티드는 서열 번호: 3의 가변 중쇄 폴리펩티드 서열을 인코<br />
딩하는 아래의 폴리뉴클레오티드 서열:<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTTATGGTAGTGATGAAACGGCCTACGCGACCTGGGCGATAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACA<br />
GCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCAAAATTTAACTTGTGGGGCCAAGGCACCCTGGTCACCGTCTCGAGC<br />
GCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGG (서열<br />
번호: 11), 또는 서열 번호: 663, 700, 703 또는 707의 폴리뉴클레오티드 서열을 포함하거나, 또는 대안으로 이<br />
러한 서열로 구성된다.<br />
본 발명의 추가의 구체예에서, IL-6에 결합 특이성을 갖는 항체의 단편 또는 변이체를 인코딩하는 폴리뉴클레오<br />
티드는 서열 번호: 2의 경쇄 가변 서열의 상보성 결정 영역(CDR, 또는 초가변 영역)을 인코딩하는 폴리뉴클레오<br />
티드에 상응하는 서열 번호: <strong>12</strong> 또는 694; 서열 번호: 13; 그리고 서열 번호: 14 또는 695 중에서 하나 이상의<br />
폴리뉴클레오티드 서열을 포함하거나, 또는 대안으로 이들로 구성된다.<br />
본 발명의 추가의 구체예에서, IL-6에 결합 특이성을 갖는 항체의 단편 또는 변이체를 인코딩하는 폴리뉴클레오<br />
티드는 서열 번호: 3, 또는 서열 번호: 661 또는 서열 번호: 657, 또는 도 34 또는 35에 도시된 다른 것들의 중<br />
쇄 가변 서열의 상보성 결정 영역(CDR, 또는 초가변 영역)을 인코딩하는 폴리뉴클레오티드에 상응하는 서열 번<br />
호: 15; 서열 번호: 16 또는 696; 그리고 서열 번호: 17 또는 697 중에서 하나 이상의 폴리뉴클레오티드 서열을<br />
포함하거나, 또는 대안으로 이들로 구성된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명에서는 또한, 본 명세서에서 기술된 항체 단편 또는 변이체를 인코딩하는 하나 이상의 폴리뉴클레오티드<br />
서열을 포함하는 폴리뉴클레오티드 서열을 고려한다. 본 발명의 한 구체예에서, IL-6에 결합 특이성을 갖는 항<br />
체의 단편 또는 변이체를 인코딩하는 폴리뉴클레오티드는 항체 단편을 인코딩하는 아래의 폴리뉴클레오티드: 서<br />
열 번호: 2의 경쇄 가변 영역을 인코딩하는 폴리뉴클레오티드 서열 번호: 10; 서열 번호: 3의 중쇄 가변 영역을<br />
인코딩하는 폴리뉴클레오티드 서열 번호: 11; 서열 번호: 20의 경쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드<br />
서열 번호: 720; 서열 번호: 647의 경쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호: 721; 서열<br />
번호: 660의 경쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호: 662; 서열 번호: 666의 경쇄 폴리펩티<br />
드를 인코딩하는 폴리뉴클레오티드 서열 번호: 722; 서열 번호: 699의 경쇄 폴리펩티드를 인코딩하는 폴리뉴클<br />
레오티드 서열 번호: 698; 서열 번호: 702의 경쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호: 701;<br />
서열 번호: 706의 경쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호: 705; 서열 번호: 709의 경쇄 폴<br />
리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호: 723; 서열 번호: <strong>19</strong>의 중쇄 폴리펩티드를 인코딩하는 폴리<br />
뉴클레오티드 서열 번호: 724; 서열 번호: 652의 중쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호:<br />
725; 서열 번호: 657의 중쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호: 700; 서열 번호: 661의 중<br />
쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열 번호: 663; 서열 번호: 704의 중쇄 폴리펩티드를 인코딩하<br />
는 폴리뉴클레오티드 서열 번호: 703; 서열 번호: 708의 중쇄 폴리펩티드를 인코딩하는 폴리뉴클레오티드 서열<br />
번호: 707; 전술한 경쇄 폴리펩티드의 상보성-결정 영역을 인코딩하는 서열 번호: <strong>12</strong>, 13, 14, 694와 695의 폴<br />
리뉴클레오티드; 그리고 전술한 중쇄 폴리펩티드의 상보성-결정 영역을 인코딩하는 서열 번호: 15, 16, 17, 696<br />
과 697의 폴리뉴클레오티드, 그리고 각각, 서열 번호: 657 및 서열 번호: 709에서 가변 중쇄와 경쇄 서열을 인<br />
코딩하는 폴리뉴클레오티드, 예를 들면, 코돈 축중성에 기초된 서열 번호: 700 및 서열 번호: 723에서 핵산 서<br />
- 75 -
[0446]<br />
[0447]<br />
[0448]<br />
[0449]<br />
[0450]<br />
[0451]<br />
[0452]<br />
[0453]<br />
[0454]<br />
열 및 이들의 단편 또는 변이체 중에서 전부를 비롯하여, 1개, 2개, 3개 또는 그 이상을 포함하거나, 또는 대안<br />
으로 이들로 구성된다. 가변 중쇄와 경쇄 서열을 인코딩하는 이들 핵산 서열은 단독으로 또는 조합으로 발현되<br />
고, 그리고 이들 서열은 바람직하게는, 적절한 가변 불변 서열, 예를 들면, 서열 번호: 589 및 서열 번호: 587<br />
에서 서열에 융합된다.<br />
본 발명의 항-IL-6 항체를 인코딩하는 전형적인 뉴클레오티드 서열은 상기 표 1에서 확인된다. 제시된 폴리뉴클<br />
레오티드 서열은 제한이 아닌 예시인 것으로 간주된다. 당업자는 소정의 폴리펩티드를 인코딩하는 폴리뉴클레오<br />
티드 서열을 용이하게 결정할 수 있고, 예로써, 제공된 폴리뉴클레오티드 서열을 개조함으로써 및/또는 이들을<br />
de novo 산출함으로써 소정의 발현 시스템에서 발현에 적합한 코딩 서열을 용이하게 산출할 수 있고, 그리고 예<br />
로써, 공개된 U.S. 특허 출원 no. 2008/0<strong>12</strong>0732에서 기술된 바와 같이, 또는 당분야에 공지된 다른 방법을 이용<br />
하여 코돈-최적화된 발현 서열을 용이하게 생산할 수 있다.<br />
본 발명의 또 다른 구체예에서, 본 발명의 폴리뉴클레오티드는 서열 번호: 586의 카파 불변 경쇄 서열을 인코딩<br />
하는 아래의 폴리뉴클레오티드 서열을 추가로 포함한다:<br />
GTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAG<br />
GCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGC<br />
ACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGG<br />
GGAGAGTGT (서열 번호: 587).<br />
본 발명의 또 다른 구체예에서, 본 발명의 폴리뉴클레오티드는 서열 번호: 588의 감마-1 불변 중쇄 폴리펩티드<br />
서열을 인코딩하는 아래의 폴리뉴클레오티드 서열을 추가로 포함한다:<br />
GCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCC<br />
GAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTG<br />
GTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAGAGTTGAGCCCAAATCT<br />
TGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATC<br />
TCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCC<br />
AAGACAAAGCCGCGGGAGGAGCAGTACGCCAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGC<br />
AAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGG<br />
GAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAAC<br />
AACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTC<br />
TCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAA (서열 번호: 589)<br />
한 구체예에서, 본 발명은 서열 번호: 3, 18, <strong>19</strong>, 652, 656, 657, 658, 661, 664, 665, 704, 또는 708에서 선<br />
택되는 항-IL-6 VH 항체 아미노산 서열, 또는 적어도 하나의 골격 잔기(FR 잔기)가 토끼 항-IL-6 항체 VH 폴리펩<br />
티드 내에서 상응하는 위치에 존재하는 아미노산으로 치환되거나 보존적 아미노산 치환으로 치환된 이의 변이체<br />
를 인코딩하는 폴리뉴클레오티드를 포함하는 분리된 폴리뉴클레오티드에 관계한다. 이에 더하여, 본 발명은 인<br />
간화된 항-Il-6 항체, 또는 이들의 인간화된 항체 결합 단편 또는 변이체, 그리고 도 2 또는 34-37 내에 포함된<br />
서열에서 묘사된 인간화된 가변 중쇄 및/또는 경쇄 폴리펩티드, 또는 표 1에서 확인된 것들, 또는 하나 이상의<br />
골격 또는 CDR 잔기가 변형되는 이들의 변이체를 포함하는 전술한 것을 인코딩하는 핵산 서열을 명확하게 포함<br />
한다. 바람직하게는, 임의의 변형이 도입되면, 이들은 결과의 항-IL-6 항체, 또는 이의 단편 또는 변이체의 결<br />
합 친화성에 부정적인 영향을 주지 않을 것이다.<br />
다른 구체예에서, 본 발명은 서열 번호: 2, 20, 647, 651, 660, 666, 699, 702, 706 또는 709에서 선택되는 항<br />
-IL-6 VL 항체 아미노산 서열, 또는 적어도 하나의 골격 잔기(FR 잔기)가 토끼 항-IL-6 항체 VL 폴리펩티드 내에<br />
서 상응하는 위치에 존재하는 아미노산으로 치환되거나 보존적 아미노산 치환으로 치환된 이의 변이체를 인코딩<br />
하는 폴리뉴클레오티드 서열을 포함하는 분리된 폴리뉴클레오티드에 관계한다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
또 다른 구체예에서, 본 발명은 서열 번호:2 및 서열 번호:3; 서열 번호:2 및 서열 번호:18; 서열 번호:2 및 서<br />
열 번호:<strong>19</strong>; 서열 번호:20 및 서열 번호:3; 서열 번호:20 및 서열 번호:18; 또는 서열 번호:20 및 서열 번호:<strong>19</strong><br />
내에 포함된 폴리펩티드를 인코딩하는 서열을 포함하는 하나 이상의 이종성 폴리뉴클레오티드에 관계한다.<br />
다른 구체예에서, 본 발명은 항-IL-6 항체로부터 유래된 적어도 하나의 CDR 폴리펩티드를 포함하는 폴리펩티드<br />
를 발현하는 분리된 폴리뉴클레오티드에 관계하고, 여기서 상기 발현된 폴리펩티드는 단독으로 IL-6에 특이적으<br />
- 76 -
[0455]<br />
[0456]<br />
[0457]<br />
[0458]<br />
[0459]<br />
로 결합하거나, 또는 항-IL-6 항체로부터 유래된 적어도 하나의 CDR 폴리펩티드를 포함하는 폴리펩티드를 발현<br />
하는 다른 폴리뉴클레오티드 서열과 공동으로 발현될 때 IL-6에 특이적으로 결합하고, 여기서 상기 적어도 하나<br />
의 CDR은 서열 번호: 3, 18, <strong>19</strong>, 652, 656, 657, 658, 661, 664, 665, 704, 708, 2, 20, 647, 651, 660, 666,<br />
699, 702, 706, 또는 709 내에 포함된 VL 또는 VH 폴리펩티드 내에 포함된 것들에서 선택된다.<br />
이들 폴리뉴클레오티드를 포함하는 숙주 세포와 벡터 역시 고려된다.<br />
다른 특정한 구체예에서, 본 발명에서는 전술한 핵산 서열 및 이들의 조합 중에서 한 가지를 포함하는 핵산 구<br />
조체, 그리고 이들 핵산 서열과 구조체를 포함하는 재조합 세포를 커버하고, 여기서 이들 핵산 서열 또는 구조<br />
체는 염색체외이거나, 또는 숙주 세포 게놈 내로 통합될 수 있다.<br />
본 발명에서는 또한, 가변 중쇄와 경쇄 폴리펩티드 서열, 그리고 본 명세서에 열거된 개별 상보성 결정 영역<br />
(CDR, 또는 초가변 영역)을 인코딩하는 폴리뉴클레오티드 서열을 포함하는 벡터, 그리고 이들 서열을 포함하는<br />
숙주 세포를 고려한다. 본 발명의 한 구체예에서, 숙주 세포는 효모 세포이다. 본 발명의 또 다른 구체예에서,<br />
효모 숙주 세포는 피치아(Pichia) 속에 속한다.<br />
일부 경우에, 소정의 폴리펩티드 서열을 인코딩하는 하나 이상의 예시적인 폴리뉴클레오티드가 표 3에 요약된<br />
바와 같이 제공된다.<br />
표 3<br />
특정 폴리펩티드를 인코딩하는 복수의 예시적인 폴리뉴클레오티드.<br />
폴리펩티드 서열 번호: NO 전형적인 코딩 서열 번호: NO<br />
4 <strong>12</strong>, 111, 694<br />
5 13, 1<strong>12</strong>, 389, 501<br />
6 14, 113, 695<br />
9 17, 116, 697<br />
39 47, 260<br />
40 48, 261<br />
60 68, 265<br />
72 80, 325, 565, 581<br />
89 97, 134, 166<br />
103 <strong>12</strong>, 111, 694<br />
104 13, 1<strong>12</strong>, 389, 501<br />
105 14, 113, 695<br />
108 17, 116, 697<br />
<strong>12</strong>6 97, 134, 166<br />
158 97, 134, 166<br />
<strong>19</strong>0 <strong>19</strong>8, 214<br />
<strong>19</strong>1 <strong>19</strong>9, 215<br />
205 213, 469, 485<br />
206 <strong>19</strong>8, 214<br />
207 <strong>19</strong>9, 215<br />
252 47, 260<br />
253 48, 261<br />
257 68, 265<br />
317 80, 325, 565, 581<br />
333 341, 533<br />
381 13, 1<strong>12</strong>, 389, 501<br />
415 423, 439<br />
431 423, 439<br />
461 213, 469, 485<br />
475 483, 499<br />
476 484, 500<br />
477 213, 469, 485<br />
478 486, 502<br />
479 487, 503<br />
- 77 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0460]<br />
[0461]<br />
[0462]<br />
480 488, 504<br />
481 489, 505<br />
491 483, 499<br />
492 484, 500<br />
493 13, 1<strong>12</strong>, 389, 501<br />
494 486, 502<br />
495 487, 503<br />
496 488, 504<br />
497 489, 505<br />
525 341, 533<br />
545 553, 585<br />
554 562, 578<br />
556 564, 580<br />
557 80, 325, 565, 581<br />
558 566, 582<br />
570 562, 578<br />
572 564, 580<br />
573 80, 325, 565, 581<br />
574 566, 582<br />
577 553, 585<br />
일부 경우에, 복수의 서열 식별자는 표 4에 요약된 바와 같이, 동일한 폴리펩티드 또는 폴리뉴클레오티드 서열<br />
을 지칭한다. 이들 서열 식별자에 대한 지시는 달리 명시되는 경우를 제외하고, 교체될 수 있는 것으로 이해된<br />
다.<br />
반복 서열의 서열 번호: NO<br />
4, 103<br />
5, 104, 381, 493<br />
6, 105<br />
9, 108<br />
<strong>12</strong>, 111<br />
13, 1<strong>12</strong><br />
14, 113<br />
17, 116<br />
39, 252<br />
40, 253<br />
48, 261<br />
60, 257<br />
68, 265<br />
72, 317, 557, 573<br />
80, 325, 565, 581<br />
89, <strong>12</strong>6, 158<br />
97, 134, 166<br />
<strong>12</strong>0, 659<br />
<strong>19</strong>0, 206<br />
<strong>19</strong>1, 207<br />
<strong>19</strong>8, 214<br />
<strong>19</strong>9, 215<br />
205, 461, 477<br />
213, 469<br />
표 4<br />
반복 서열. 각 셀은 서열 목록 내에 포함된 일군의 반복 서열을 제공한다.<br />
- 78 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0463]<br />
[0464]<br />
[0465]<br />
333, 525<br />
415, 431<br />
423, 439<br />
475, 491<br />
476, 492<br />
478, 494<br />
479, 495<br />
480, 496<br />
481, 497<br />
483, 499<br />
484, 500<br />
486, 502<br />
487, 503<br />
488, 504<br />
489, 505<br />
545, 577<br />
554, 570<br />
556, 572<br />
558, 574<br />
562, 578<br />
564, 580<br />
566, 582<br />
일정한 예시적인 구체예는 중간으로 또는 고도로 엄밀한 하이브리드화 조건 하에, 표 1에 열거된 예시적인 코딩<br />
서열 중에서 하나를 보유하는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티드를 포함하고, 또한 중간으<br />
로 또는 고도로 엄밀한 하이브리드화 조건 하에, 표 1에 열거된 예시적인 코딩 서열 중에서 하나를 보유하는 폴<br />
리뉴클레오티드와 동일한 폴리펩티드를 인코딩하는 폴리뉴클레오티드에 하이브리드화되는 폴리뉴클레오티드, 또<br />
는 전술한 폴리뉴클레오티드 중에서 하나에 의해 인코딩된 폴리펩티드를 포함한다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
구(句) "높은 엄밀도(stringency) 하이브리드화 조건"은 프로브가 전형적으로, 핵산의 복합 혼합물 내에서 표적<br />
하위서열에 하이브리드화되지만 다른 서열에는 하이브리드화되지 않는 조건을 지칭한다. 높은 엄밀도 조건은 서<br />
열 의존성이고, 그리고 상이한 환경에서 달라질 것이다. 더욱 긴 서열은 특히, 더욱 높은 온도에서 하이브리드<br />
화된다. 핵산의 하이브리드화에 대한 광범위한 보도는 Tijssen, Techniques in Biochemistry and Molecular<br />
Biology--Hybridization with Nucleic Probes, "Overview of principles of hybridization and the strategy<br />
of nucleic acid assays" (<strong>19</strong>93)에서 확인된다. 일반적으로, 높은 엄밀도 조건은 정의된 이온 강도 pH에서 특정<br />
서열에 대한 열용융점(Tm)보다 대략 5-10℃ 낮게 선택된다. Tm은 표적에 상보적인 프로브의 50%가 평형에서 표<br />
적 서열에 하이브리드화되는 온도(정의된 이온 강도, pH, 그리고 핵 농도 하에)이다(표적 서열이 Tm에서 과량으<br />
로 존재하기 때문에, 평형에서 프로브 중에서 50%가 점유된다). 높은 엄밀도 조건은 염 농도가 pH 7.0 내지 8.3<br />
에서 대략 1.0 M 이하 나트륨 이온, 전형적으로 대략 0.01 내지 1.0 M 나트륨 이온 농도(또는 다른 염)이고, 그<br />
리고 온도가 짧은 프로브(가령, 10개 내지 50개 뉴클레오티드)의 경우에 적어도 대략 30℃ 및 긴 프로브(가령,<br />
50개 초과의 뉴클레오티드)의 경우에 적어도 대략 60℃인 조건일 것이다. 높은 엄밀도 조건은 또한, 불안정화제<br />
(destabilizing agent), 예를 들면, 포름아미드의 첨가로 달성될 수 있다. 선택성 또는 특이적 하이브리드화를<br />
위하여, 양성 신호는 배경 하이브리드화의 적어도 2배, 선택적으로 배경 하이브리드화의 10배이다. 전형적인 높<br />
은 엄밀도 하이브리드화 조건은 아래와 같을 수 있다: 50% 포름아미드, 5×SSC, 그리고 1% SDS, 42℃에서 항온<br />
처리, 또는, 5×SSC, 1% SDS, 65℃에서 항온처리, 그리고 65℃에서 0.2×SSC, 그리고 0.1% SDS에서 세척. 이런<br />
하이브리드화와 세척 단계는 예로써, 1, 2, 5, 10, 15, 30, 60분; 또는 그 이상 동안 수행될 수 있다.<br />
높은 엄밀도 조건 하에 서로 하이브리드화되지 않는 핵산은 이들이 인코딩하는 폴리펩티드가 실질적으로 관련되<br />
면, 여전히 실질적으로 관련된다. 이는 예로써, 핵산의 사본이 유전자 코드에 의해 허용되는 최대 코돈 축중성<br />
을 이용하여 산출될 때 발생한다. 이런 경우에, 이들 핵산은 전형적으로, 중간 엄밀도 하이브리드화 조건 하에<br />
하이브리드화된다. 예시적인 "중간 엄밀도 하이브리드화 조건"에는 37℃에서 40% 포름아미드, 1 M NaCl, 1% SDS<br />
의 완충액에서 하이브리드화, 그리고 45℃에서 1×SSC에서 세척이 포함된다. 이런 하이브리드화와 세척 단계는<br />
예로써, 1, 2, 5, 10, 15, 30, 60분, 또는 그 이상 동안 수행될 수 있다. 양성 하이브리드화는 배경의 적어도 2<br />
배이다. 당업자는 유사한 엄밀도의 조건을 제공하기 위하여 대안적 하이브리드화와 세척 조건이 이용될 수 있음<br />
- 79 -
[0466]<br />
[0467]<br />
[0468]<br />
[0469]<br />
[0470]<br />
[0471]<br />
[0472]<br />
[0473]<br />
을 용이하게 인지할 것이다.<br />
본 발명의 추가의 전형적인 구체예<br />
다른 구체예에서, 본 발명에서는 완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는, Ab1을 포함하는<br />
항-IL-6 항체, 그리고 IL-6에 특이적으로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항<br />
체와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포함)과 동일한 선형 또는 입체형태적 에피토프(들)에 특이적<br />
으로 결합하고 및/또는 이러한 선형 또는 입체형태적 에피토프(들)에 결합하는 것에 대해 경쟁하는 하나 이상의<br />
항-IL-6 항체, 또는 이의 항체 단편 또는 변이체를 고려한다. 바람직한 구체예에서, 항-IL-6 항체, 또는 이의<br />
단편 또는 변이체는 완전한 인간 IL-6 폴리펩티드 또는 이의 단편 상에 존재하는, Ab1, 그리고 IL-6에 특이적으<br />
로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된 항체의 하나 이<br />
상의 CDR을 포함)과 동일한 선형 또는 입체형태적 에피토프(들)에 특이적으로 결합하고 및/또는 이러한 선형 또<br />
는 입체형태적 에피토프(들)에 결합하는 것에 대해 경쟁할 수 있다.<br />
본 발명의 다른 구체예에서, Ab1에 의해 특이적으로 결합되는 완전한 IL-6 폴리펩티드 또는 이의 단편 상에 존<br />
재하는 동일한 선형 또는 입체형태적 에피토프에 특이적으로 결합하는 항-IL-6 항체는 본래의 인간 IL-6 폴리펩<br />
티드의 전장에 걸쳐있는 겹쳐지는 선형 펩티드 단편들을 이용한 에피토프 매핑에 의해 확인된 IL-6<br />
에피토프(들)에 결합할 수 있다. 본 발명의 한 구체예에서, IL-6 에피토프는 아미노산 잔기 37-51, 아미노산 잔<br />
기 70-84, 아미노산 잔기 169-183, 아미노산 잔기 31-45 및/또는 아미노산 잔기 58-72를 각각 포함하는 것들에<br />
서 선택되는 IL-6 단편 내에 포함된 하나 이상의 잔기를 포함하거나, 대안으로 이들로 구성된다<br />
본 발명은 또한, Ab1, 그리고 IL-6에 특이적으로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단<br />
일 쇄 항체와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포함)에서 선택되는 항-IL-6 항체가 포함되지만 이들<br />
에 국한되지 않는, 본 명세서에서 기술된 항체 또는 항체 단편과 동일한 IL-6 에피토프에 결합하고 및/또는 IL-<br />
6에 결합하는 것에 대해 경쟁하는 항-IL-6 항체와 경쟁하는 항-IL-6 항체에 관계한다.<br />
또 다른 구체예에서, 본 발명은 또한, 서열 번호: 3, 18, <strong>19</strong>, 22, 38, 54, 70, 86, 102, 117, 118, <strong>12</strong>3, 139,<br />
155, 171, 187, 203, 2<strong>19</strong>, 235, 251, 267, 283, 299, 315, 331, 347, 363, 379, 395, 411, 427, 443, 459,<br />
475, 491, 507, 523, 539, 555, 571, 652, 656, 657, 658, 661, 664, 665, 668, 672, 676, 680, 684, 688,<br />
691, 692, 704, 또는 708을 포함하는 VH 폴리펩티드 서열 내에 포함된 하나 이상의 CDR 및/또는 서열 번호: 2,<br />
20, 21, 37, 53, 69, 85, 101, 1<strong>19</strong>, <strong>12</strong>2, 138, 154, 170, 186, 202, 218, 234, 250, 266, 282, 298, 314,<br />
330, 346, 362, 378, 394, 410, 426, 442, 458, 474, 490, 506, 522, 538, 554, 570, 647, 651, 660, 666,<br />
667, 671, 675, 679, 683, 687, 693, 699, 702, 706, 또는 709로 구성되는 VL 폴리펩티드 서열 내에 포함된 하<br />
나 이상의 CDR, 그리고 본 출원의 도 34-37 내에 포함된 항체 정렬에 묘사된 VH와 VL 서열을 포함하는 분리된<br />
항-IL-6 항체, 또는 이의 항체 단편 또는 변이체에 관계한다.<br />
본 발명의 한 구체예에서, 이들 두 선행 단락에서 논의된 항-IL-6 항체는 Ab1을 포함하는 항-IL-6 항체, 그리고<br />
IL-6에 특이적으로 결합하고, 바람직하게는 비당화되는 이의 키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된<br />
항체의 하나 이상의 CDR을 포함) 내에 포함된 것들과 동일한 가변 경쇄 및 가변 중쇄 영역 각각에서 적어도 2개<br />
의 상보성 결정 영역(CDR)을 포함한다.<br />
바람직한 구체예에서, 앞서 논의된 항-IL-6 항체는 Ab1 내에 포함된 것들과 동일한 가변 경쇄 및 가변 중쇄 영<br />
역 각각에서 적어도 2개의 상보성 결정 영역(CDR)을 포함한다. 다른 구체예에서, 앞서 논의된 항-IL-6 항체의<br />
모든 CDR은 Ab1을 포함하는 항-IL-6 항체, 그리고 IL-6에 특이적으로 결합하고, 바람직하게는 비당화되는 이의<br />
키메라, 인간화, 단일 쇄 항체와 단편(앞서 확인된 항체의 하나 이상의 CDR을 포함) 내에 포함된 CDR과 동일하<br />
다. 본 발명의 바람직한 구체예에서, 앞서 논의된 항-IL-6 항체의 모든 CDR은 Ab1, 예를 들면, 각각 서열 번<br />
호:657과 서열 번호:709 내에 포함된 VH와 VL 서열로 구성되는 항체 내에 포함된 CDR과 동일하다.<br />
본 발명에서는 또한, 앞서 논의된 하나 이상의 항-IL-6 항체가 비당화되고; 이펙터 기능, 반감기, 단백질가수분<br />
해, 및/또는 당화를 변화시키기 위하여 변경된 Fc 영역을 보유하고; 인간, 인간화, 단일 쇄 또는 키메라이고;<br />
그리고, 토끼(모) 항-IL-6 항체로부터 유래된 인간화 항체인 것을 고려한다. 피치아(Pichia) 내에서 비당화된<br />
항체의 생산을 제공하는 전형적인 불변 영역은 각각, 서열 번호:589 및 서열 번호:587에서 핵산 서열에 의해 인<br />
코딩되는 서열 번호:588 및 서열 번호:586 내에 포함된다.<br />
- 80 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0474]<br />
[0475]<br />
[0476]<br />
[0477]<br />
[0478]<br />
[0479]<br />
[0480]<br />
[0481]<br />
[0482]<br />
본 발명에서는 또한, 하나 이상의 항-IL-6 항체를 고려하고, 여기서 상기 항체의 가변 경쇄 영역 및 가변 중쇄<br />
영역 내에 각 골격 영역(FR)은 변형되지 않거나, 또는 가변 경쇄 또는 중쇄 영역 내의 2개 또는 3개 정도의 인<br />
간 FR 잔기를 모 토끼 항체의 상응하는 FR 잔기에 의해 치환함으로써 변형된, 인간 FR이고, 그리고 이들 인간<br />
FR은 인간 생식선 항체 서열의 라이브러리 내에 포함된 다른 인간 생식선 항체 서열에 비하여, 상응하는 토끼<br />
가변 중쇄 또는 경쇄 영역에 대한 높은 상동성 수준에 기초하여 인간 생식선 항체 서열의 라이브러리로부터 선<br />
택된 인간 가변 중쇄와 경쇄 항체 서열로부터 유래된다.<br />
본 발명의 한 구체예에서, 항-IL-6 항체, 또는 이의 단편 또는 변이체는 IL-6을 발현하는 세포와 연관된 질환을<br />
앓는 환자에서 인간 세포 상에서 또는 이들 세포에 의해 발현되는 IL-6을 비롯하여, 생체내에서 IL-6 발현 인간<br />
세포 및/또는 순환 가용성 IL-6 분자에 특이적으로 결합할 수 있다.<br />
다른 구체예에서, 질환은 일반적인 피로, 운동-유발된 피로, 암-관련된 피로, 염증 질환-관련된 피로, 만성 피<br />
로 증후군, 섬유근육통, 암-관련된 악액질, 심장-관련된 악액질, 호흡기-관련된 악액질, 신장-관련된 악액질,<br />
연령-관련된 악액질, 류머티스성 관절염, 전신성 홍반성 루푸스(SLE), 전신성 유년형 특발성 관절염, 건선, 건<br />
선성 관절병증, 강직성 척추염, 염증성 장 질환(IBD), 류머티스성 다발성 근육통, 거대 세포 동맥염, 자가면역<br />
혈관염, 이식편 대(對) 숙주 질환(GVHD), 쇼그렌 증후군, 성인 발병성 스틸병, 류머티스성 관절염, 전신성 유년<br />
형 특발성 관절염, 골관절염, 골다공증, 뼈의 파제트병, 골관절염, 다발성 골수종, 호지킨 림프종, 비-호지킨<br />
림프종, 전립선암, 백혈병, 신장 세포 암, 다발성 캐슬만씨병, 난소암, 암 화학요법에서 약물 내성, 암 화학요<br />
법 독성, 허혈성 심장 질환, 동맥경화증, 비만, 당뇨병, 천식, 다발성 경화증, 알츠하이머병, 뇌혈관 질환, 발<br />
열, 급성기 반응, 알레르기, 빈혈, 염증의 빈혈(만성 질환의 빈혈), 고혈압, 우울증, 만성 질환과 연관된 우울<br />
증, 혈전증, 혈소판증가증, 급성 심장 마비, 대사 증후군, 유산, 비만, 만성 전립선염, 사구체신염, 골반 염증<br />
질환, 재관류 손상, 이식 거부반응, 이식편 대(對) 숙주 질환(GVHD), 조류 인플루엔자, 천연두, 대유행 인플루<br />
엔자, 성인 호흡 곤란 증후군(ARDS), 중증 급성 호흡기 증후군(SARS), 패혈증, 그리고 전신성 염증 반응 증후군<br />
(SIRS)에서 선택된다. 바람직한 구체예에서, 질환은 암, 염증 질환, 바이러스 질환, 또는 자가면역 질환에서 선<br />
택된다. 특히 바람직한 구체예에서, 질환은 관절염, 악액질, 그리고 소모성 증후군이다.<br />
본 발명에서는 또한, 검출가능 라벨 또는 치료제에 직접적으로 또는 간접적으로 부착된 항-IL-6 항체, 또는 이<br />
의 단편 또는 변이체를 고려한다.<br />
본 발명에서는 또한, 효모 또는 인간 선호 코돈을 포함하거나, 또는 대안으로 이들 코돈으로 구성되는 것들을<br />
비롯하여, 앞서 열거된 바와 같은 항-IL-6 항체, 또는 이의 항체 단편 또는 변이체의 발현을 유발하는 하나 이<br />
상의 핵산 서열을 고려한다. 본 발명에서는 또한, 상기 핵산 서열(들)을 포함하는 벡터(플라스미드 또는 재조합<br />
바이러스 벡터 포함)를 고려한다. 본 발명에서는 또한, 포유동물, 효모, 세균, 그리고 곤충 세포를 비롯하여,<br />
앞서 열거된 항체 중에서 적어도 하나를 발현하는 숙주 세포 또는 재조합 숙주 세포를 고려한다. 바람직한 구체<br />
예에서, 숙주 세포는 효모 세포이다. 더욱 바람직한 구체예에서, 효모 세포는 2배체 효모 세포이다. 이보다 더<br />
욱 바람직한 구체예에서, 효모 세포는 피치아(Pichia) 효모이다.<br />
본 발명에서는 또한, IL-6 발현 세포와 연관된 질환 또는 이상을 앓는 환자에 적어도 하나의 항-IL-6 항체, 또<br />
는 이의 단편 또는 변이체의 치료 효과량을 투여하는 단계를 포함하는 치료 방법을 고려한다. 치료될 수 있는<br />
질환은 앞서 열거된 무제한적 목록에서 제공된다. 바람직한 구체예에서, 질환은 암, 자가면역 질환, 또는 염증<br />
장애에서 선택된다. 특히 바람직한 구체예에서, 질환은 암 또는 바이러스 감염이다. 다른 구체예에서, 치료는<br />
화학요법, 방사선요법, 사이토킨 투여 또는 유전자 요법에서 선택되는 다른 치료제 또는 섭생의 투여 단계를 추<br />
가로 포함한다.<br />
본 발명에서는 또한, 적어도 하나의 항-IL-6 항체의 진단 효과량을 투여하는 단계를 포함하는, IL-6을 발현하는<br />
세포의 존재를 검출하는 생체내 화상(imaging) 방법을 고려한다. 한 구체예에서, 상기 투여는 IL-6 발현 질환<br />
부위에서 항체의 검출을 용이하게 하는 방사성핵종 또는 형광단의 투여를 추가로 포함한다. 본 발명의 다른 구<br />
체예에서, 생체내 화상 방법은 IL-6 발현 종양 또는 전이를 검출하는데 이용되거나, 또는 IL-6 발현 세포와 연<br />
관된 자가면역 질환의 부위의 존재를 검출하는데 이용된다. 추가의 구체예에서, 상기 생체내 화상 방법의 결과<br />
는 방사선요법, 화학요법 또는 이들의 조합을 포함하는 치료 섭생(therapeutic regimen)을 비롯한 적절한 치료<br />
섭생의 설계를 용이하게 하는데 이용된다.<br />
항-IL-6 활성<br />
- 81 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0483]<br />
[0484]<br />
[0485]<br />
[0486]<br />
[0487]<br />
[0488]<br />
[0489]<br />
[0490]<br />
[0491]<br />
[0492]<br />
[0493]<br />
[0494]<br />
앞서 언급된 바와 같이, IL-6은 신호-전달 당단백질 gp130의 적어도 하나의 아단위 및 IL-6 수용체(IL-6R)로 구<br />
성되는 수용체 복합체를 통하여 세포 반응을 촉진하는 사이토킨 집단의 구성원이다. IL-6R은 또한, 가용성 형태<br />
(sIL-6R)로 존재할 수 있다. IL-6은 IL-6R에 결합하고, 이는 이후, 신호-전달 수용체 gp130을 이합체화시킨다.<br />
본 발명의 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체는 항-IL-6 활성을 나타냄으로써 유용한 것으<br />
로 생각된다. 본 발명의 무제한적 구체예에서, 본 발명의 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이<br />
체는 가용성 IL-6 또는 세포 표면 발현된 IL-6인 IL-6에 결합함으로써 항-IL-6 활성을 나타내고 및/또는 IL-<br />
6R에 IL-6의 결합 및/또는 gp130 신호-전달 당단백질의 활성화(이합체화)와 IL-6/IL-6R/gp130 멀티머의 형성,<br />
그리고 전술한 것 중 한 가지의 생물학적 효과를 예방하거나 저해할 수 있다. 본 발명의 항-IL-6 항체는 특정<br />
항체가 IL-6에 결합하는 위치(즉, 에피토프) 및/또는 상기 항체가 전술한 IL-6 복합체 및/또는 멀티머의 형성,<br />
그리고 이들의 생물학적 효과에 영향을 주는 방법에 기초하여 상이한 길항 활성을 가질 수 있다. 결과적으로,<br />
본 발명에 따른 상이한 항-IL-6 항체는 예로써, 실질적인 가용성 IL-6의 형성과 축적을 수반하는 이상, 예를 들<br />
면, 류머티스성 관절염을 예방 또는 치료하는데 더욱 적합하고, 반면 다른 항체는 IL-6/IL-6R/gp130 또는 IL-<br />
6/IL-6R/gp130 멀티머의 예방이 바람직한 치료 결과인 치료에 유리할 수 있다. 이는 결합 분석 및 다른 분석에<br />
서 결정될 수 있다.<br />
본 발명의 항-IL-6 항체, 그리고 IL-6에 결합 특이성을 갖는 이들의 단편과 변이체의 항-IL-6 활성은 또한, IL-<br />
6에 대한 결합 강도 또는 친화성으로 기술될 수 있다. 이는 또한, 그들의 치료 특성에 영향을 줄 수 있다. 본<br />
발명의 한 구체예에서, 본 발명의 항-IL-6 항체, 그리고 IL-6에 결합 특이성을 갖는 이들의 단편은 5x10 -7<br />
, 10 -<br />
7<br />
, 5x10 -8<br />
, 10 -8<br />
, 5x10 -9<br />
, 10 -9<br />
, 5x10 -10<br />
, 10 -10<br />
, 5x10 -11<br />
, 10 -11<br />
, 5x10 -<strong>12</strong><br />
, 10 -<strong>12</strong><br />
, 5x10 -13<br />
, 10 -13<br />
, 5x10 -14<br />
, 10 -14<br />
, 5x10 -<br />
15<br />
또는 10 -15<br />
이하의 해리 상수(dissociation constant, KD)로 IL-6에 결합한다. 바람직하게는, 항-IL-6 항체 및<br />
이들의 단편과 변이체는 5x10 -10<br />
이하의 해리 상수로 IL-6에 결합한다.<br />
본 발명의 또 다른 구체예에서, 본 발명의 항-IL-6 항체, 그리고 IL-6에 결합 특이성을 갖는 이들의 단편과 변<br />
이체의 항-IL-6 활성은 10 -4<br />
S -1<br />
, 5x10 -5<br />
S -1<br />
, 10 -5<br />
S -1<br />
, 5x10 -6<br />
S -1<br />
, 10 -6<br />
S -1<br />
, 5x10 -7<br />
S -1<br />
, 또는 10 -7<br />
S -1<br />
이하의 오프<br />
-레이트(off-rate)로 IL-6에 결합한다. 본 발명의 한 구체예에서, 본 발명의 항-IL-6 항체, 그리고 IL-6에 결합<br />
특이성을 갖는 이들의 단편과 변이체는 선형 또는 구조성 IL-6 에피토프에 결합한다.<br />
본 발명의 추가의 구체예에서, 본 발명의 항-IL-6 항체, 그리고 IL-6에 결합 특이성을 갖는 이들의 단편과 변이<br />
체의 항-IL-6 활성은 IL-6과 연관된 질환과 이상의 증상을 개선하거나 감소시키고, 또는 대안으로, 이들 질환과<br />
이상을 치료하거나 예방함으로써 항-IL-6 활성을 나타낸다. IL-6과 연관된 질환과 이상의 무제한적 실례는 하기<br />
에 열거된다. 언급된 바와 같이, 암-관련된 피로, 악액질과 류머티스성 관절염은 본 발명의 항-IL-6 항체에 적<br />
합한 징후이다.<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체<br />
는 IL-6R 또는 gp-130 신호-전달 당단백질에 대한 결합 특이성을 갖지 않는다.<br />
B-세포 스크리닝과 분리<br />
한 구체예에서, 본 발명에서는 적어도 하나의 항원-특이적 세포를 분리하는데 이용될 수 있는 항원-특이적 B 세<br />
포의 클론 집단을 분리하는 방법을 제시한다. 하기에 기술되고 예시된 바와 같이, 이들 방법은 별개로, 공동으<br />
로, 순차적으로, 반복적으로, 또는 주기적으로 이용될 수 있는 일련의 배양과 선별 단계를 포함한다. 바람직하<br />
게는, 이들 방법은 원하는 항원에 특이적인 단일클론 항체, 또는 이러한 항체에 상응하는 핵산 서열을 생산하는<br />
데 이용될 수 있는 적어도 하나의 항원-특이적 세포를 분리하는데 이용된다.<br />
한 구체예에서, 본 발명에서는 아래의 단계를 포함하는 방법을 제시한다:<br />
a. 적어도 하나의 항원-특이적 B 세포를 포함하는 세포 집단을 준비하는 단계;<br />
b. 예로써, 색층분석으로 세포 집단을 농축하여 적어도 하나의 항원-특이적 B 세포를 포함하는 농축된 세포 집<br />
단을 형성하는 단계;<br />
c. 농축된 B 세포 집단으로부터 단일 B 세포를 분리하는 단계; 그리고<br />
- 82 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0495]<br />
[0496]<br />
[0497]<br />
[0498]<br />
[0499]<br />
[0500]<br />
[0501]<br />
[0502]<br />
[0503]<br />
[0504]<br />
[0505]<br />
[0506]<br />
[0507]<br />
[0508]<br />
[0509]<br />
[0510]<br />
d. 단일 B 세포가 항원에 특이적인 항체를 생산하는 지를 결정하는 단계.<br />
다른 구체예에서, 본 발명에서는 단일, 항체-생산 B 세포를 분리하는 방법에 개선을 제시하고, 상기 개선은 면<br />
역화되거나 항원에 자연적으로 노출된 숙주로부터 획득된 B 세포 집단을 농축하는 단계를 포함하고, 여기서 농<br />
축 단계는 임의의 선별 단계를 선행하고, 적어도 하나의 배양 단계를 포함하고, 그리고 상기 항원에 특이적인<br />
단일 단일클론 항체를 생산하는 B 세포의 클론 집단을 산출한다.<br />
본 명세서 전반에서, "B 세포의 클론 집단"은 원하는 항체에 특이적인 단일 항체만을 분비하는 B 세포의 집단을<br />
지칭한다. 다시 말하면, 이들 세포는 원하는 항원에 특이적인 단지 한 가지 유형의 단일클론 항체를 생산한다.<br />
본 출원에서, 세포 집단 세포를 "농축하고"는 혼합된 세포 집단, 예를 들면, 원하는 항원에 대하여 면역화된 숙<br />
주로부터 유래된 B 세포-포함 분리물 내에 포함된 원하는 세포, 전형적으로 항원-특이적 세포의 빈도를 증가시<br />
키는 것을 의미한다. 따라서 농축된 세포 집단은 농축 단계의 결과로서 항원-특이적 세포의 더욱 높은 빈도를<br />
갖는 세포 집단을 포함하지만, 이러한 세포 집단은 상이한 항체를 포함하고 생산할 수 있다.<br />
포괄적인 용어 "세포 집단"은 복수 농축 단계가 수행될 때, 세포 집단이 농축전과 농축후 둘 모두 일 수 있다는<br />
점을 염두에 두고, 농축전과 농축후 세포 집단을 포함한다. 가령, 한 구체예에서, 본 발명은 아래의 단계를 포<br />
함하는 방법을 제시한다:<br />
a. 면역화된 숙주로부터 세포 집단을 수확하여 수확된 세포 집단을 획득하는 단계;<br />
b. 수확된 세포 집단으로부터 적어도 하나의 단일 세포 현탁액을 생성시키는 단계;<br />
c. 적어도 하나의 단일 세포 현탁액을 농축하여 첫 번째 농축된 세포 집단을 형성하는 단계;<br />
d. 첫 번째 농축된 세포 집단을 농축하여 두 번째 농축된 세포 집단을 형성하는 단계;<br />
e. 두 번째 농축된 세포 집단을 농축하여 세 번째 농축된 세포 집단을 형성하는 단계; 그리고<br />
f. 세 번째 농축된 세포 집단의 항원-특이적 세포에 의해 생산된 항체를 선별하는 단계.<br />
각 세포 집단은 다음 단계에 직접 이용되거나, 또는 긴- 또는 짧은-기간 보관 동안 또는 후속 단계 동안 부분적<br />
으로 또는 완전히 동결될 수 있다. 또한, 세포 집단으로부터 세포는 단일 세포 현탁액을 생성시키기 위하여 개<br />
별적으로 현탁될 수 있다. 이러한 단일 세포 현탁액은 농축전 세포 집단으로서 기능하고 농축될 수 있다. 이후,<br />
하나 이상의 항원-특이적 단일 세포 현탁액이 합쳐져 농축된 세포 집단을 형성한다; 이들 항원-특이적 단일 세<br />
포 현탁액은 함께 모아질 수 있다, 가령, 추가의 분석 및/또는 항체 생산을 위하여 재-도말될 수 있다.<br />
한 구체예에서, 본 발명에서는 대략 50% 내지 대략 100%, 또는 그 내에 증분(increment)인 항원-특이적 세포 빈<br />
도를 갖는 농축된 세포 집단을 생성시키기 위하여 세포 집단을 농축하는 방법을 제시한다. 바람직하게는, 농축<br />
된 세포 집단은 대략 50%, 60%, 70%, 75%, 80%, 90%, 95%, 99%, 또는 100% 이상의 항원-특이적 세포 빈도를 갖<br />
는다.<br />
다른 구체예에서, 본 발명에서는 세포 집단을 농축하는 방법을 제시하고, 여기서 항원-특이적 세포의 빈도는 적<br />
어도 대략 2-배, 5-배, 10-배, 20-배, 50-배, 100-배, 또는 그 내에 증분으로 증가된다.<br />
본 명세서 전반에서 용어 "증분"은 다양한 정도의 정밀도, 예를 들면, 10, 1, 0.1, 0.01 반올림 등으로 수치 값<br />
을 정의하는데 이용된다. 이러한 증분은 임의의 측정가능 정도의 정밀도로 반올림될 수 있고, 그리고 범위의 양<br />
측면에서 동일한 정도의 정밀도로 반올림될 필요는 없다. 가령, 범위 1 내지 100 또는 그 내에 증분은 20 내지<br />
80, 5 내지 50, 그리고 0.4 내지 98과 같은 범위를 포함한다. 범위에 제한이 없을 때, 가령, 100 이하의 범위<br />
또는 그 내에 증분은 100 및 측정가능 한계 사이에 증분을 의미한다. 가령, 100 이하 또는 그 내에 증분은<br />
특징, 예를 들면, 온도가 0으로 제한되면, 0 내지 100 또는 그 내에 증분을 의미한다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
항원-특이성은 임의의 항원에 대하여 측정될 수 있다. 항원은 펩티드, 단백질 또는 이들의 단편; 탄수화물; 유<br />
기와 무기 분자; 동물 세포, 세균 세포, 그리고 바이러스에 의해 생산되는 수용체; 효소; 생물학적 경로의 효능<br />
제과 길항제; 호르몬; 그리고 사이토킨이 포함되지만 이들에 국한되지 않는, 항체가 결합할 수 있는 임의의 물<br />
질일 수 있다. 전형적인 항원에는 IL-2, IL-4, IL-6, IL-10, IL-<strong>12</strong>, IL-13, IL-18, IFN-알파, IFN-감마, BAFF,<br />
- 83 -
[0511]<br />
[05<strong>12</strong>]<br />
[0513]<br />
[0514]<br />
[0515]<br />
[0516]<br />
[0517]<br />
[0518]<br />
[05<strong>19</strong>]<br />
CXCL13, IP-10, VEGF, EPO, EGF, HRG, 간세포 성장 인자(HGF)와 헵시딘이 포함되지만 이들에 국한되지 않는다.<br />
바람직한 항원에는 IL-6, IL-13, TNF-알파, VEGF-알파, 간세포 성장 인자(HGF)와 헵시딘이 포함된다. 1회 이상<br />
의 농축 단계를 이용하는 방법에서, 각 농축 단계에 이용되는 항원은 서로 동일하거나 상이할 수 있다. 동일한<br />
항원으로 복수 농축 단계는 항원-특이적 세포의 넓은 및/또는 다양한 집단을 산출할 수 있다; 상이한 항원으로<br />
복수 농축 단계는 이들 상이한 항원에 교차-특이성을 갖는 농축된 세포 집단을 산출할 수 있다.<br />
세포 집단의 농축은 항원-특이적 세포를 분리하기 위한 당분야에 공지된 임의의 세포-선별 수단에 의해 수행될<br />
수 있다. 가령, 세포 집단은 색층분석 기술, 예를 들면, Miltenyi 비드 또는 자석 비드 기술에 의해 농축될 수<br />
있다. 이들 비드는 목적되는 항원에 직접적으로 또는 간접적으로 부착될 수 있다. 바람직한 구체예에서, 세포<br />
집단을 농축하는 방법은 적어도 하나의 색층분석 농축 단계를 포함한다.<br />
세포 집단은 또한, 당분야에 공지된 임의의 항원-특이성 분석 기술, 예를 들면, ELISA 분석 또는 할로 분석에<br />
의해 농축될 수 있다. ELISA 분석에는 선택성 항원 고정화(가령, 스트렙타비딘, 아비딘, 또는 뉴트라비딘 코팅<br />
된 평판에 의한 비오틴화된 항원 포획), 비-특이적 항원 평판 코팅, 그리고 항원 구축 전략(가령, 선택성 항원<br />
포획, 그 이후에 이형(heteromeric) 단백질-항원 복합체를 생성시키기 위한 결합 대응물 첨가)이 포함되지만 이<br />
들에 국한되지 않는다. 항원은 고형 매트릭스 또는 지지체, 예를 들면, 칼럼에 직접적으로 또는 간접적으로 부<br />
착될 수 있다. 할로 분석은 세포를 항원-적하된 비드 및 B 세포를 수확하는데 이용되는 숙주에 특이적인 표지된<br />
항-숙주 항체와 접촉시키는 단계를 포함한다. 라벨은 예로써, 형광단일 수 있다. 한 구체예에서, 적어도 하나의<br />
분석 농축 단계는 적어도 하나의 단일 세포 현탁액 상에서 수행된다. 다른 구체예에서, 세포 집단을 농축하는<br />
방법은 적어도 1회의 색층분석 농축 단계 및 적어도 1회의 분석 농축 단계를 포함한다.<br />
크기 또는 밀도로 세포 집단을 "농축하는" 방법은 당분야에 공지되어 있다(참조: U.S. 특허 5,627,052). 이들<br />
단계는 항원-특이성으로 세포 집단을 농축하는 것에 추가하여, 본 발명의 방법에 이용될 수 있다.<br />
본 발명의 세포 집단은 항원을 인식할 수 있는 적어도 하나의 세포를 포함한다. 항원-인식 세포에는 B 세포, 플<br />
라스마 세포, 그리고 이들의 자손이 포함되지만 이들에 국한되지 않는다. 한 구체예에서, 본 발명에서는 단일<br />
유형의 항원-특이적 B-세포를 포함하는 클론 세포 집단을 제시한다, 다시 말하면, 이러한 세포 집단은 원하는<br />
항원에 특이적인 단일 단일클론 항체를 생산한다.<br />
이런 구체예에서, B 세포의 클론 항원-특이적 집단은 본 명세서에서 제공된 신규한 배양과 선별 프로토콜에 의<br />
해 획득되는 항원-특이적, 항체-분비 세포로 주로 구성되는 것으로 생각된다. 따라서 본 발명에서는 또한, 적어<br />
도 하나의 항원-특이적, 항체-분비 세포를 포함하는 농축된 세포 집단을 획득하기 위한 방법을 제시한다. 한 구<br />
체예에서, 본 발명에서는 대략 50% 내지 대략 100%, 또는 그 내에 증분, 또는 대략 60%, 70%, 80%, 90% 이상,<br />
또는 100%의 항원-특이적, 항체-분비 세포를 포함하는 농축된 세포 집단을 제시한다.<br />
한 구체예에서, 본 발명에서는 예로써, 세포 집단으로부터 특정 B 세포를 선별하고 및/또는 특정 세포에 의해<br />
생산된 항체를 선별하는 임의의 선별 단계 이전에, 숙주로부터 획득된 세포 집단을 농축함으로써 단일 B 세포를<br />
분리하는 방법을 제시한다. 농축 단계는 1, 2, 3 또는 그 이상의 단계에서 수행될 수 있다.<br />
한 구체예에서, 단일 B 세포는 단일 B 세포가 항원-특이성 및/또는 원하는 특성을 갖는 항체를 분비하는 지를<br />
확증하기에 앞서, 농축된 세포 집단으로부터 분리된다.<br />
한 구체예에서, 세포 집단을 농축하는 방법은 항체 생산 및/또는 선별을 위한 방법에 이용된다. 따라서 본 발명<br />
에서는 항체를 선별하기에 앞서 세포 집단을 농축하는 단계를 포함하는 방법을 제시한다. 상기 방법은 아래의<br />
단계를 포함할 수 있다: 적어도 하나의 항원-특이적 세포를 포함하는 세포 집단을 준비하는 단계, 적어도 하나<br />
의 항원-특이적 세포를 분리함으로써 세포 집단을 농축하여 농축된 세포 집단을 형성하는 단계, 그리고 적어도<br />
하나의 항원-특이적 세포로부터 항체 생산을 유도하는 단계. 바람직한 구체예에서, 농축된 세포 집단은 한 가지<br />
이상의 항원-특이적 세포를 포함한다. 한 구체예에서, 농축된 집단의 각 항원-특이적 세포는 이들로부터 항체<br />
생산 세포를 분리하고 및/또는 상기 B 세포를 이용하여 항체를 생산하거나, 또는 이런 항체에 상응하는 핵산 서<br />
열을 생산하기에 앞서, 클론 항원-특이적 B 세포 집단을 생성시키는 조건 하에 배양된다. 항체가 항원-특이적<br />
세포의 낮은 빈도로 세포 집단으로부터 생산되는 이전 기술과 대조적으로, 본 발명은 항원-특이적 세포의 높은<br />
빈도에서 항체 선별을 가능하게 한다. 농축 단계가 항체 선별 이전에 이용되기 때문에, 항체 생산에 이용되는<br />
대다수의 세포, 바람직하게는 실질적으로 모든 세포가 항원-특이적이다. 항원 특이성의 증가된 빈도로 세포 집<br />
단으로부터 항체를 생산함으로써, 항체의 양과 다양성이 증가된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 항체 선별 방법에서, 항체는 바람직하게는, 항원-특이적 B 세포의 클론 집단을 발생시키는 농축 단계<br />
- 84 -
[0520]<br />
[0521]<br />
[0522]<br />
[0523]<br />
[0524]<br />
[0525]<br />
와 배양 단계 이후에 선별된다. 이들 방법은 하나 이상의 분리된, 항원-특이적 세포로부터 선별된 항체 또는 이<br />
의 일부분을 염기서열분석하는 단계를 추가로 포함할 수 있다. 염기서열분석을 위한 당분야에 공지된 임의의 방<br />
법이 이용될 수 있고, 중쇄, 경쇄, 가변 영역(들), 및/또는 상보성 결정 영역(들)(CDR)을 염기서열분석하는 단<br />
계를 포함할 수 있다.<br />
농축 단계에 더하여, 항체 선별을 위한 방법은 또한, 항원 인식 및/또는 항체 기능성에 대하여 세포 집단을 스<br />
크리닝하는 하나 이상의 단계를 포함할 수 있다. 가령, 원하는 항체는 특정한 구조 특징, 예를 들면, 특정 구조<br />
의 특정 에피토프 또는 의태(mimicry)에 결합; 길항제 또는 효능제 활성; 또는 중화 활성, 예를 들면, 항원과<br />
리간드 사이에 결합 저해를 보유할 수 있다. 한 구체예에서, 항체 기능성 스크리닝은 리간드-의존성이다. 항체<br />
기능성에 대한 스크리닝에는 항원 리간드의 재조합 수용체 단백질과의 자연적인 상호작용을 되살리는 시험관내<br />
단백질-단백질 상호작용 분석; 그리고 리간드 의존성이고 용이하게 모니터되는 세포-기초된 반응(가령, 증식반<br />
응)이 포함되지만 이들에 국한되지 않는다. 한 구체예에서, 항체 선별을 위한 방법은 저해 농도(IC50)를 측정함<br />
으로써 항체 기능성에 대하여 세포 집단을 스크리닝하는 단계를 포함한다. 한 구체예에서, 적어도 하나의 분리<br />
된, 항원-특이적 세포는 대략 100, 50, 30, 25, 10 ㎍/㎖ 이하, 또는 그 내에 증분의 IC50을 갖는 항체를 생산<br />
한다.<br />
농축 단계에 더하여, 항체 선별을 위한 방법은 또한, 항체 결합 강도에 대하여 세포 집단을 스크리닝하는 하나<br />
이상의 단계를 포함할 수 있다. 항체 결합 강도는 당분야에 공지된 임의의 방법(가령, Biacore)에 의해 측정<br />
될 수 있다. 한 구체예에서, 적어도 하나의 분리된, 항원-특이적 세포는 높은 항원 친화성, 예를 들면, 대략<br />
5x10 -10<br />
M-1 이하, 바람직하게는 대략 1x10 -13<br />
내지 2x10 -11<br />
, 대략 1.5x10 -11<br />
내지 5x10 -10<br />
, 1x10 -<strong>12</strong><br />
내지 1x10 -10<br />
, 1x10 -<strong>12</strong><br />
내지 7.5x10 -11<br />
, 1x10 -11<br />
또는 그 이하, 또는 그 내에 증분의 해리 상수(Kd)를 갖는 항체를 생산한다. 이러<br />
한 구체예에서, 항체는 친화성 성숙인 것으로 일컬어진다. 바람직한 구체예에서, 항체의 친화성은 Panorex<br />
(에드레콜로맙), Rituxan<br />
(리툭시맙), Herceptin<br />
(트라즈투주맙), Mylotarg<br />
(젠투주맙), Campath<br />
(알렘투주맙), Zevalin(이브리투모맙), Erbitux(세툭시맙), Avastin(베비시주맙),<br />
Raptiva(에팔리주맙), Remicade<br />
(인플릭시맙), Humira(아달리무맙), 그리고 Xolair(오말리주맙) 중에서 한 가지의 친화성에 필적하거나, 또<br />
는 이보다 높다. 바람직하게는, 항체의 친화성은 Humira의 친화성에 필적하거나, 또는 이보다 높다. 항체의<br />
친화성은 또한, 공지된 친화성 성숙 기술에 의해 증가될 수 있다. 한 구체예에서, 적어도 하나의 세포 집단은<br />
항체 기능성과 항체 결합 강도 중에서 적어도 하나, 바람직하게는 둘 모두에 대하여 스크리닝된다.<br />
농축 단계에 더하여, 항체 선별을 위한 방법은 또한, 항체 서열 상동성, 특히 인간 상동성에 대하여 세포 집단<br />
을 스크리닝하는 하나 이상의 단계를 포함할 수 있다. 한 구체예에서, 적어도 하나의 분리된, 항원-특이적 세포<br />
는 인간 항체에 대하여, 대략 50% 내지 대략 100%, 또는 그 내에 증분, 또는 대략 60%, 70%, 80%, 85%, 90%,<br />
또는 95% 이상의 상동성을 갖는 항체를 생산한다. 이들 항체는 당분야에 공지된 기술, 예를 들면, CDR 이식<br />
(grafting) 또는 선택성 결정 잔기 이식(SDR)에 의해, 인간 서열에 대한 상동성을 증가시키기 위하여 인간화될<br />
수 있다.<br />
다른 구체예에서, 본 발명에서는 또한, IC50, Kd, 및/또는 상동성의 관점에서 앞서 기술된 임의의 구체예에 따<br />
른 항체 자체를 제시한다.<br />
본 명세서에 기술된 B 세포 선별 프로토콜은 항체-분비 B 세포 및 원하는 표적 항원에 특이적인 단일클론 항체<br />
를 획득하기 위한 다른 방법과 대비하여 다수의 본질적인 이점을 갖는다. 이들 이점에는 아래가 포함되지만 이<br />
들에 국한되지 않는다:<br />
공개특허 10-2011-01<strong>12</strong>308<br />
첫째, 이들 선별 절차가 원하는 항원, 예를 들면, IL-6 또는 TNF-알파와 함께 이용될 때, 이들 방법은 항체의<br />
- 85 -
[0526]<br />
[0527]<br />
[0528]<br />
[0529]<br />
[0530]<br />
[0531]<br />
[0532]<br />
[0533]<br />
[0534]<br />
[0535]<br />
[0536]<br />
실질적으로 포괄적인 보체, 다시 말하면, 항원의 다양한 별개의 에피토프에 결합하는 항체인 것으로 보이는 것<br />
을 생산할 수 있는 항원-특이적 B 세포를 재현적으로 발생시키는 것으로 밝혀졌다. 이론에 한정됨 없이, 포괄적<br />
인 보체는 최초 B 세포 회수에 앞서 수행되는 항원 농축 단계에 기인하는 것으로 가정된다. 게다가, 이러한 이<br />
점은 이들 특성이 특정 항체의 에피토프 특이성에 따라 변할 수 있기 때문에, 상이한 특성을 갖는 항체의 분리<br />
와 선별을 가능하게 한다.<br />
둘째, 상기 B 세포 선별 프로토콜은 단일 B 세포, 또는 이의 자손을 포함하고, 전반적으로, 상대적으로 높은 결<br />
합 친화성, 다시 말하면, 피코몰(picomolar) 또는 더욱 우수한 항원 결합 친화성으로 원하는 항원에 결합하는<br />
단일 단일클론 항체를 분비하는 클론 B 세포 배양액을 재현적으로 생성시키는 것으로 밝혀졌다. 대조적으로, 기<br />
존의 항체 선별 방법은 상대적으로 적은 높은 친화성 항체를 생성시키고, 따라서 치료 잠재력을 갖는 항체를 분<br />
리하기 위하여 광범위한 스크리닝 절차를 필요로 하는 경향이 있다. 이론에 한정됨 없이, 상기 프로토콜은 숙주<br />
의 생체내 B 세포 면역화(일차 면역화), 그 이후에 항원 표적에 특이적인 단일 높은 친화성 단일클론 항체를 분<br />
비하는 회수된 클론 B 세포의 능력과 성향을 강화시키는 두 번째 시험관내 B 세포 자극(이차 항원 프라이밍 단<br />
계)을 유발하는 것으로 가정된다.<br />
셋째, 상기 B 세포 선별 프로토콜은 평균적으로, 원하는 표적에 고도로 선택성(항원 특이적)인 IgG를 생산하는<br />
농축된 B 세포를 재현적으로 생성시키는 것으로 밝혀졌다(IL-6 특이적 B 세포로 본 발명에서 확인된 바와 같<br />
이). 이들 방법에 의해 회수된 항원-농축된 B 세포는 앞서 논의된 바와 같은 에피토프 특이성의 원하는 완전한<br />
보체를 산출할 수 있는 B 세포를 포함하는 것으로 생각된다.<br />
넷째, 소형 항원, 다시 말하면, 100개 이하의 아미노산, 예를 들면, 5-50개 아미노산 길이의 펩티드와 함께 이<br />
용될 때에도 이들 B 세포 선별 프로토콜은 소형 항원, 예를 들면, 펩티드에 대한 단일 높은 친화성 항체를 분비<br />
하는 클론 B 세포 배양액을 재현적으로 발생시키는 것으로 밝혀졌다. 이는 소형 펩티드에 대해 높은 친화성 항<br />
체를 생산하는 것이 일반적으로 매우 어렵고, 노동 집중적이고, 그리고 때때로, 가능하지도 않다는 점에서, 매<br />
우 놀랍다. 따라서 본 발명은 원하는 펩티드 표적, 예를 들면, 바이러스, 세균 또는 자기항원 펩티드에 대한 치<br />
료 항체를 생산하는데 이용될 수 있고, 따라서 매우 상이한 결합 특성을 갖는 단일클론 항체의 생산 또는 심지<br />
어, 상이한 펩티드 표적들, 가령, 상이한 바이러스 균주들에 대한 단일클론 항체의 칵테일의 생산을 가능하게<br />
한다. 이러한 이점은 원하는 결합가(valency)를 갖는 치료 또는 예방 백신, 예를 들면, 상이한 HPV 균주에 대한<br />
보호 면역(protective immunity)을 유도하는 HPV 백신의 생산의 배경에서 특히 유용하다.<br />
다섯 번째, 이들 B 세포 선별 프로토콜은 특히, 토끼로부터 유래된 B 세포와 함께 이용될 때, 내인성 인간 면역<br />
글로불린에 매우 유사하고(아미노산 수준에서 대략 90% 유사한) 인간 면역글로불린에 매우 유사한 길이를 갖는<br />
CDR을 포함하고, 따라서 잠재적인 면역원성 우려를 제거하기 위한 서열 변형을 거의 또는 전혀 필요로 하지 않<br />
는(전형적으로, 기껏해야 소수의 CDR 잔기가 모 항체 서열 내에서 변형되고 골격 외인성 잔기가 도입되지 않은)<br />
항원-특이적 항체 서열을 재현적으로 생성시키는 경향이 있다. 특히, 바람직하게는 이러한 재조합 항체는 항원<br />
인식에 요구되는 숙주(토끼) CDR1과 CDR2 잔기, 그리고 전체 CDR3만을 포함할 것이다. 이로 인하여, 상기 B 세<br />
포와 항체 선별 프로토콜에 따라 생산된 회수된 항체 서열의 높은 항원 결합 친화성은 심지어 인간화 이후에도<br />
본래 상태로, 또는 실질적으로 본래 상태로 남아있다.<br />
종합하면, 이들 방법은 기존에 알려졌던 것보다 더욱 효과적인 프로토콜의 이용에 의해 더욱 많은 별개의 에피<br />
토프에 대해 더욱 높은 결합 친화성을 나타내는 항체를 생산하는데 이용될 수 있다.<br />
특정한 구체예에서, 본 발명에서는 아래의 단계를 포함하는 방법으로, 원하는 항원에 특이적인 항체를 분비하고<br />
적어도 하나의 원하는 기능적 특성, 예를 들면, 친화성, 친화력(avidity), 세포용해 활성 등을 선택적으로 갖는<br />
단일 B 세포를 확인하는 방법을 제시한다:<br />
a. 항원에 대하여 숙주를 면역화시키는 단계;<br />
b. 숙주로부터 B 세포를 회수하는 단계;<br />
c. 수확된 B 세포를 농축하여 항원-특이적 세포의 빈도를 증가시키는 단계;<br />
d. 적어도 하나의 단일 세포 현탁액을 생성시키는 단계;<br />
e. 배양 웰에 대해 단일 항원-특이적 B 세포의 생존에 우호적인 조건 하에 단일 세포 현탁액으로부터 하위-집단<br />
을 배양하는 단계;<br />
- 86 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0537]<br />
[0538]<br />
[0539]<br />
[0540]<br />
[0541]<br />
[0542]<br />
[0543]<br />
[0544]<br />
f. 하위-집단으로부터 B 세포를 분리하는 단계; 그리고<br />
g. 단일 B 세포가 상기 항원에 특이적인 항체를 생산하는 지를 결정하는 단계.<br />
전형적으로, 이들 방법은 원하는 항체를 인코딩하는 폴리펩티드와 핵산 서열을 전체적으로 또는 부분적으로, 분<br />
리하고 염기서열분석하는 추가적인 단계를 추가로 포함할 것이다. 이들 서열, 또는 이들의 변형된 이형 또는 일<br />
부분은 원하는 항원에 대한 재조합 항체를 생산하기 위하여 원하는 숙주 세포 내에서 발현될 수 있다.<br />
앞서 언급된 바와 같이, B 세포의 클론 집단은 원하는 항원에 대한 항체를 생산하는 항체-분비 B 세포를 주로<br />
포함하는 것으로 생각된다. 또한, 여러 항원, 그리고 상이한 B 세포 집단으로 획득된 실험 결과에 기초하여, 클<br />
론성으로 생산된 B 세포 및 본 발명에 따라 생산된 이들로부터 유래된 분리된 항원-특이적 B 세포는 배양된 항<br />
원-특이적 B 세포로부터 단일클론 항체를 도출하는 다른 방법과 비교하여, 전형적으로 상대적으로 높은 친화성<br />
을 나타내고 게다가, 더욱 높은 에피토프 변이성의 단일클론 항체의 선별체를 효과적으로 및 재현적으로 생산할<br />
수 있는 단일클론 항체를 분비하는 것으로 생각된다. 예시적인 구체예에서, 이런 B 세포 선별 방법에 이용되는<br />
면역 세포의 집단은 토끼로부터 유래될 것이다. 하지만, 비-인간과 인간 숙주를 비롯하여, 항체를 생산하는 다<br />
른 숙주가 면역 B 세포의 공급원으로서 대안으로 이용될 수 있다. B 세포의 공급원으로서 토끼의 이용은 이들<br />
방법에 의해 도출될 수 있는 단일클론 항체의 다양성을 강화시키는 것으로 생각된다. 또한, 본 발명에 따라 토<br />
끼로부터 유래된 항체 서열은 전형적으로, 인간 항체 서열에 높은 서열 동일성을 갖는 서열을 보유하고, 따라서<br />
항원성을 거의 나타내지 않기 때문에 인간에 이용하기 적합하다. 인간화의 과정에서, 최종 인간화 항체는 일반<br />
적으로 이식에 이용되는 인간 표적 서열과 대비하여 성질이 극히 상이한 숙주 CDR 잔기의 부분집합에 한정되는<br />
더욱 적은 외래/숙주 잔기 함량을 갖는다. 이는 인간화된 항체 단백질에서 완전한 활성 회복의 가능성을 증진시<br />
킨다.<br />
본 명세서에 기술된 농축 단계를 이용한 항체 선별의 방법은 면역화된 숙주로부터 면역 세포-포함 세포 집단을<br />
획득하는 단계를 포함한다. 면역화된 숙주로부터 면역 세포-포함 세포 집단을 획득하는 방법은 당분야에 공지되<br />
어 있고, 그리고 일반적으로, 숙주에서 면역 반응을 유도하는 단계 및 숙주로부터 세포를 수확하여 하나 이상의<br />
세포 집단을 획득하는 단계를 포함한다. 상기 반응은 원하는 항원에 대하여 숙주를 면역화함으로서 유도될 수<br />
있다. 대안으로, 이런 면역 세포의 공급원으로서 이용되는 숙주는 원하는 항원, 예를 들면, 특정 병원균, 예를<br />
들면, 세균 또는 바이러스로 감염되거나, 또는 대안으로 개체를 괴롭히는 암에 대한 특이적 항체 반응을 적재하<br />
는 개체에 자연적으로 노출될 수 있다.<br />
숙주 동물은 당분야에 널리 공지되어 있고, 여기에는 기니 피그, 토끼, 생쥐, 쥐, 비-인간 영장류, 인간, 그리<br />
고 다른 포유동물과 설치류, 닭, 소, 돼지, 염소, 그리고 양이 포함되지만 이들에 국한되지 않는다. 바람직하게<br />
는, 숙주는 포유동물, 더욱 바람직하게는, 토끼, 생쥐, 쥐, 또는 인간이다. 항원에 노출될 때, 숙주는 상기 항<br />
원에 대한 본래의 면역 반응의 일부로서 항체를 생산한다. 앞서 언급된 바와 같이, 면역 반응은 질환의 결과로<br />
서 자연적으로 발생하거나, 또는 항원으로 면역화에 의해 유도될 수 있다. 면역화는 당분야에 공지된 임의의 방<br />
법, 예를 들면, 면역 반응을 강화시키는 작용제, 예를 들면, 완전 또는 불완전 Freund 어쥬번트와 함께 또는 이<br />
러한 어쥬번트 없이, 항원의 1회 이상 주입에 의해 수행될 수 있다. 다른 구체예에서, 본 발명에서는 또한, 비<br />
장내(intrasplenic) 면역화를 고려한다. 숙주 동물의 생체내 면역화의 대안으로서, 상기 방법은 숙주 세포 배양<br />
액을 시험관내에서 면역화시키는 단계를 포함할 수 있다.<br />
면역 반응(가령, 혈청 항체 검출에 의해 측정됨)을 위한 충분한 시간 이후에, 숙주 동물 세포는 하나 이상의 세<br />
포 집단을 획득하기 위하여 수확된다. 바람직한 구체예에서, 수확된 세포 집단은 항체 결합 강도 및/또는 항체<br />
기능성에 대하여 스크리닝된다. 수확된 세포 집단은 바람직하게는, 비장, 림프절, 골수, 및/또는 말초혈 단핵<br />
세포(peripheral blood mononuclear cell, PBMC) 중에서 적어도 하나로부터 유래된다. 이들 세포는 한 가지 이<br />
상의 공급원으로부터 수확되고 집합될 수 있다. 일정한 항원의 경우에 일정한 공급원이 바람직할 수 있다.<br />
가령, IL-6의 경우에 비장, 림프절, 그리고 PBMC가 바람직하다; 그리고 TNF의 경우에 림프절이 바람직하다. 세<br />
포 집단은 면역화 이후, 대략 20일 내지 대략 90일 또는 그 내에 증분, 바람직하게는 대략 50일 내지 대략 60일<br />
시점에 수확된다. 수확된 세포 집단 및/또는 이로부터 단일 세포 현탁액은 항체 선별을 위하여 농축되고, 스크<br />
리닝되고, 및/또는 배양될 수 있다. 수확된 세포 집단 내에서 항원-특이적 세포의 빈도는 일반적으로, 대략 1%<br />
내지 대략 5%, 또는 그 내에 증분이다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
한 구체예에서, 수확된 세포 집단으로부터 단일 세포 현탁액은 바람직하게는, Miltenyi 비드를 이용함으로써 농<br />
축된다. 대략 1% 내지 대략 5%의 항원-특이적 세포의 빈도를 갖는 수확된 세포 집단으로부터, 100%에 근접하는<br />
- 87 -
[0545]<br />
[0546]<br />
[0547]<br />
[0548]<br />
[0549]<br />
[0550]<br />
[0551]<br />
[0552]<br />
[0553]<br />
[0554]<br />
항원-특이적 세포의 빈도를 갖는 농축된 세포 집단이 도출된다.<br />
농축 단계를 이용한 항체 선별 방법은 농축된 세포 집단으로부터 적어도 하나의 항원-특이적 세포로부터 항체를<br />
생산하는 단계를 포함한다. 시험관내에서 항체를 생산하는 방법은 당분야에 널리 공지되어 있고, 그리고 임의의<br />
적절한 방법이 이용될 수 있다. 한 구체예에서, 수확된 세포 집단으로부터 농축된 세포 집단, 예를 들면, 항원-<br />
특이적 단일 세포 현탁액은 다양한 세포 밀도, 예를 들면, 웰(well)당 50, 100, 250, 500개, 또는 1개 내지<br />
1000개 세포 사이의 다른 증분으로 도말된다. 바람직하게는, 하위-집단은 대략 10,000개 이하의 항원-특이적,<br />
항체-분비 세포, 더욱 바람직하게는 대략 50-10,000개, 대략 50-5,000개, 대략 50-1,000개, 대략 50-500개, 대<br />
략 50-250개, 또는 그 내에 증분의 항원-특이적, 항체-분비 세포를 포함한다. 이후, 이들 하위-집단은 영양 세<br />
포층 상에서, 바람직하게는 배양 웰마다 단일 증식 항체-분비 세포의 생존에 우호적인 조건 하에 적절한 배지<br />
(가령, 활성화된 T 세포 조건 배지, 특히 1-5% 활성화된 토끼 T 세포 조건 배지)로 배양된다. 일반적으로 조사<br />
(照射)된 세포 물질, 예를 들면, EL4B 세포로 구성되는 영양 세포층은 세포 집단의 일부를 구성하지 않는다. 이<br />
들 세포는 항체 생산을 위한 충분한 시간, 예를 들면, 대략 1일 내지 대략 2주, 대략 1일 내지 대략 10일, 적어<br />
도 대략 3일, 대략 3일 내지 대략 5일, 대략 5일 내지 대략 7일, 적어도 대략 7일, 또는 그 내에 다른 증분 동<br />
안 적절한 배지 내에서 배양된다. 한 구체예에서, 하나 이상의 하위-집단이 동시에 배양된다. 바람직하게는, 단<br />
일 항체-생산 세포 및 이의 자손은 각 웰에서 생존하고, 따라서 각 웰에서 항원-특이적 B 세포의 클론 집단을<br />
제공한다. 이 단계에서, 상기 클론 집단에 의해 생산된 면역글로불린 G(IgG)는 항원 특이성과 고도로 상관된다.<br />
바람직한 구체예에서, 이들 IgG는 대략 50% 이상, 더욱 바람직하게는 70%, 85%, 90%, 95%, 99% 이상, 또는 그<br />
내에 증분인 항원 특이성으로 상관관계를 나타낸다. IL-6에 대한 예시적인 상관관계를 증명하는 도 3을 참조한<br />
다. 이들 상관관계는 웰(well)당 단일 항원-특이적 항체 산물을 확립하기 위한 제한 조건 하에 B 세포 배양액을<br />
셋업함으로써 증명되었다. 항원-특이적 대(對) 일반적 IgG 합성이 비교되었다. 3가지 집단이 관찰되었다: 단일<br />
형식의 항원(비오틴화되고 직접적인 코팅)을 인식하는 IgG, 고정화에 상관없이 검출가능 IgG와 항원 인식, 그리<br />
고 IgG 생산 단독. IgG 생산은 항원-특이성과 고도로 상관되었다.<br />
항체를 포함하는 상층액은 선택적으로 수집되고, 이는 앞서 기술된 단계에 따른 항체 선별을 위하여 농축되고,<br />
스크리닝되고, 및/또는 배양될 수 있다. 한 구체예에서, 상층액은 농축되고(바람직하게는, 항원-특이성 분석,<br />
특히 ELISA 분석에 의해) 및/또는 항체 기능성에 대하여 스크리닝된다.<br />
다른 구체예에서, 원하는 분비된 단일클론 항체의 존재를 검출하기 위하여 앞서 기술된 상층액이 선택적으로 스<br />
크리닝되는 농축된, 바람직하게는 클론성, 항원-특이적 B 세포 집단은 소수의 B 세포, 바람직하게는 단일 B 세<br />
포의 분리에 이용되고, 이는 이후, 클론 B 세포 집단 내에서 단일 항체-생산 B 세포의 존재를 확증하기 위하여<br />
적절한 분석법으로 조사된다. 한 구체예에서 대략 1개 내지 대략 20개의 세포, 바람직하게는 대략 15, <strong>12</strong>, 10,<br />
5, 또는 3개 이하, 또는 그 내에 증분의 세포, 가장 바람직하게는 단일 세포가 클론 B 세포 집단으로부터 분리<br />
된다. 스크리닝은 바람직하게는, 항원-특이성 분석, 특히 할로 분석에 의해 달성된다. 할로 분석은 전장<br />
단백질, 또는 이의 단편으로 수행될 수 있다. 항체-포함 상층액은 또한, 항원 결합 친화성; 항원-리간드 결합의<br />
작동 또는 길항, 특정한 표적 세포 유형의 증식의 유도 또는 저해; 표적 세포의 용해의 유도 또는 저해, 그리고<br />
항원을 수반하는 생물학적 경로의 유도 또는 저해 중에서 적어도 하나에 대하여 스크리닝될 수 있다.<br />
확인된 항원-특이적 세포는 원하는 단일클론 항체를 인코딩하는 상응하는 핵산 서열을 도출하는데 이용될 수 있<br />
다(AluI 다이제스트는 웰마다 단일 단일클론 항체 유형만 생산된다는 것을 확증할 수 있다). 앞서 언급된 바와<br />
같이, 이들 서열은 인간 약제에서 이용에 적합해지도록 예로써, 인간화에 의해 돌연변이될 수 있다.<br />
앞서 언급된 바와 같이, 이러한 과정에 이용되는 농축된 B 세포 집단 역시 반복되거나 상이한 순서로 수행될 수<br />
있는 앞서 기술된 단계에 따른 항체 선별을 위하여 더욱 농축되고, 스크리닝되고, 및/또는 배양될 수 있다. 바<br />
람직한 구체예에서, 농축된, 바람직하게는 클론성, 항원-특이적 세포 집단의 적어도 하나의 세포는 분리되고,<br />
배양되고, 그리고 항체 선별에 이용된다.<br />
따라서 한 구체예에서, 본 발명에서는 아래의 단계를 포함하는 방법을 제시한다:<br />
a. 면역화된 숙주로부터 세포 집단을 수확하여 수확된 세포 집단을 획득하는 단계;<br />
b. 수확된 세포 집단으로부터 적어도 하나의 단일 세포 현탁액을 생성시키는 단계;<br />
c. 적어도 하나의 단일 세포 현탁액을 바람직하게는, 색층분석으로 농축하여 첫 번째 농축된 세포 집단을 형성<br />
하는 단계;<br />
공개특허 10-2011-01<strong>12</strong>308<br />
d. 첫 번째 농축된 세포 집단을 바람직하게는, ELISA 분석으로 농축하여 두 번째 농축된 세포 집단을 형성하는<br />
- 88 -
[0555]<br />
[0556]<br />
[0557]<br />
[0558]<br />
[0559]<br />
[0560]<br />
[0561]<br />
[0562]<br />
[0563]<br />
[0564]<br />
[0565]<br />
[0566]<br />
[0567]<br />
[0568]<br />
[0569]<br />
[0570]<br />
[0571]<br />
[0572]<br />
단계, 상기 세포 집단은 바람직하게는, 클론성이다, 다시 말하면, 이는 단일 유형의 항원-특이적 B 세포만을 포<br />
함한다;<br />
e. 두 번째 농축된 세포 집단을 바람직하게는, 할로 분석으로 농축하여 원하는 항원에 특이적인 항체를 생산하<br />
는 단일 또는 소수의 세포를 포함하는 세 번째 농축된 세포 집단을 형성하는 단계; 그리고<br />
f. 세 번째 농축된 세포 집단으로부터 분리된 항원-특이적 세포에 의해 생산된 항체를 선별하는 단계.<br />
상기 방법은 수확된 세포 집단을 항체 결합 강도(친화성, 친화력) 및/또는 항체 기능성에 대하여 스크리닝하는<br />
하나 이상의 단계를 추가로 포함할 수 있다. 적절한 스크리닝 단계에는 확인된 항원-특이적 B 세포에 의해 생산<br />
된 항체가 최소 항원 결합 친화성을 갖는 항체를 생산하는 지의 여부; 상기 항체가 리간드에 대한 원하는 항원<br />
의 결합을 작동하거나, 또는 길항하는 지의 여부; 상기 항체가 특이적 세포 유형의 증식을 유도하거나, 또는 저<br />
해하는 지의 여부; 상기 항체가 표적 세포에 대한 세포용해 반응을 유도하거나, 또는 도출하는 지의 여부; 상기<br />
항체가 특이적 에피토프에 결합하는 지의 여부; 그리고 상기 항체가 항원을 수반하는 특정한 생물학적 경로<br />
(들)를 조절(저해 또는 작동)하는 지의 여부를 검출하는 분석 방법이 포함되지만 이들에 국한되지 않는다.<br />
유사하게, 상기 방법은 두 번째 농축된 세포 집단을 항체 결합 강도 및/또는 항체 기능성에 대하여 스크리닝하<br />
는 하나 이상의 단계를 포함할 수 있다.<br />
상기 방법은 선별된 항체의 폴리펩티드 서열 또는 상응하는 핵산 서열을 염기서열분석하는 단계를 추가로 포함<br />
할 수 있다. 상기 방법은 또한, 선별된 항체의 서열, 이의 단편, 또는 유전적으로 변형된 이형을 이용하여 재조<br />
합 항체를 생산하는 단계를 포함한다. 원하는 특성을 유지시키기 위하여 항체 서열을 돌연변이시키는 방법은 당<br />
업자에게 널리 공지되어 있고, 여기에는 인간화, 키메라화, 단일 쇄 항체의 생산이 포함된다; 이들 돌연변이 방<br />
법은 원하는 이펙터 기능, 면역원성, 안정성, 당화의 제거 또는 부가 등을 갖는 재조합 항체를 산출할 수 있다.<br />
재조합 항체는 포유동물 세포, 예를 들면, CHO, COS, BHK, HEK-293, 세균 세포, 효모 세포, 식물 세포, 곤충 세<br />
포, 그리고 양서류 세포가 포함되지만 이들에 국한되지 않는 임의의 적절한 재조합 세포에 의해 생산될 수<br />
있다. 한 구체예에서, 이들 항체는 배수체 효모 세포, 다시 말하면, 2배체 효모 세포, 특히 피치아(Pichia)에서<br />
발현된다.<br />
한 구체예에서, 상기 방법은 아래의 단계를 포함한다:<br />
a. 항원에 대하여 숙주를 면역화시켜 숙주 항체를 생성시키는 단계;<br />
b. 숙주 항체를 항원 특이성과 중화에 대하여 스크리닝하는 단계;<br />
c. 숙주로부터 B 세포를 수확하는 단계;<br />
d. 수확된 B 세포를 농축하여 항원-특이적 세포의 증가된 빈도를 갖는 농축된 세포 집단을 생성시키는 단계;<br />
e. 적어도 하나의 배양 웰에서 클론 집단을 생산하기 위하여 단일 B 세포의 생존에 우호적인 조건 하에, 농축된<br />
세포 집단으로부터 하나 이상의 하위-집단을 배양하는 단계;<br />
f. 클론 집단이 항원에 특이적인 항체를 생산하는 지를 결정하는 단계;<br />
g. 단일 B 세포를 분리하는 단계; 그리고<br />
h. 단일 B 세포에 의해 생산된 항체의 핵산 서열을 염기서열분석하는 단계.<br />
항체를 인간화시키는 방법<br />
본 발명의 또 다른 구체예에서, 항체 중쇄와 경쇄를 인간화시키는 방법이 제시된다. 이러한 구체예에서, 중쇄와<br />
경쇄의 인간화를 위하여 아래의 방법이 수행된다:<br />
경쇄<br />
1. 신호 펩티드 서열 다음에 첫 번째 아미노산을 확인한다. 이는 골격 1의 시작이다. 토끼 경쇄 단백질 서열에<br />
대한 신호 펩티드는 첫 번째 개시 메티오닌에서 시작되고 전형적으로, 22개 아미노산 길이를 갖지만 반드시 그<br />
러한 것은 아니다. 성숙 폴리펩티드의 시작은 또한, N-말단 단백질 염기서열분석에 의해 경험적으로<br />
결정되거나, 또는 예측 알고리즘(prediction algorithm)을 이용하여 예측될 수 있다. 이는 또한, 당업자에 의해<br />
고전적으로 정의되는 골격 1의 시작이다.<br />
- 89 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0573]<br />
[0574]<br />
[0575]<br />
[0576]<br />
[0577]<br />
[0578]<br />
[0579]<br />
[0580]<br />
[0581]<br />
[0582]<br />
[0583]<br />
[0584]<br />
[0585]<br />
[0586]<br />
[0587]<br />
실례: 'AYDM…'으로 시작되는 도 2에서 RbtVL 아미노산 잔기<br />
2. 골격 3의 끝을 확인한다. 이는 전형적으로, 골격 1의 시작 다음에 86-90개 아미노산이고, 그리고<br />
전형적으로, 2개의 티로신 잔기가 선행하는 시스테인 잔기이다. 이는 당업자에 의해 고전적으로 정의되는 골격<br />
3의 끝이다.<br />
실례: 'TYYC'로 끝나는 도 2에서 RbtVL 아미노산 잔기 88<br />
3. 앞서 정의된 바와 같은 골격 1의 시작에서부터 골격 3의 끝까지 폴리펩티드의 토끼 경쇄 서열을 이용하고 가<br />
장 유사한 인간 항체 단백질 서열에 대한 서열 상동성 검색을 수행한다. 이는 전형적으로, 면역원성의 가능성을<br />
감소시키기 위하여 항체 성숙 이전에 인간 생식세포 서열의 데이터베이스에 대한 검색이긴 하지만, 임의의 인간<br />
서열이 이용될 수 있다. 전형적으로, 서열 데이터베이스를 최대 상동성에 대하여 검색하는데 BLAST와 같은 프로<br />
그램이 이용될 수 있다. 인간 항체 서열의 데이터베이스는 다양한 출처, 예를 들면, NCBI(National Center for<br />
Biotechnology Information)로부터 확인될 수 있다.<br />
실례: 도 2에서 1번 내지 88번 잔기로부터 RbtVL 아미노산 서열은 인간 항체 생식세포 데이터베이스에 대하여<br />
BLAST된다. 상위 3개의 독특한 답변된 서열은 도 2에서 L<strong>12</strong>A, V1과 Vx02로서 도시된다.<br />
4. 일반적으로, 최대 상동성 인간 생식세포 가변 경쇄 서열은 이후, 인간화를 위한 기초로서 이용된다. 하지만,<br />
당업자는 서열 갭 및 골격 유사성을 비롯한 다른 인자에 기초하여, 상동성 알고리즘에 의한 결정에서 최대 상동<br />
성이 아닌 다른 서열의 이용을 결정할 수도 있다.<br />
실례: 도 2에서, L<strong>12</strong>A는 최대 상동성 인간 생식세포 가변 경쇄 서열이고 RbtVL의 인간화를 위한 기초로서 이용<br />
된다.<br />
5. 경쇄 인간화에 이용되는 인간 동족체에 대한 골격과 CDR 배열(FR1, FR2, FR3, CDR1 & CDR2)을 결정한다. 이<br />
는 당분야에서 기술된 바와 같은 전통적인 배치(layout)를 이용한다. 골격과 CDR 영역의 배치를 유지하면서 토<br />
끼 가변 경쇄 서열과 인간 동족체를 정렬한다.<br />
실례: 도 2에서, RbtVL 서열은 인간 상동성 서열 L<strong>12</strong>A와 함께 정렬되고, 그리고 골격과 CDR 도메인이<br />
표시된다.<br />
6. 인간 상동성 경쇄 서열 CDR1과 CDR2 영역을 토끼 서열로부터 CDR1과 CDR2 서열로 대체한다. 토끼와 인간 CDR<br />
서열 간에 길이 차이가 존재하면, 전체 토끼 CDR 서열 및 이들의 길이를 이용한다. 결과의 인간화된 항체의 특<br />
이성, 친화성 및/또는 면역원성은 더욱 작은 또는 더욱 큰 서열 교환이 수행되거나, 또는 특정한 잔기(들)가 변<br />
경되면, 변화되지 않는 것이 가능하고, 기술된 이들 교환이 성공적으로 이용되긴 했지만 다른 변화가 허용될 수<br />
있는 가능성을 배제시키지 않는다.<br />
실례: 도 2에서, 인간 상동성 가변 경쇄 L<strong>12</strong>A의 CDR1과 CDR2 아미노산 잔기는 RbtVL 토끼 항체 경쇄 서열로부<br />
터 CDR1과 CDR2 아미노산 서열로 대체된다. 인간 L<strong>12</strong>A 골격 1, 2와 3은 변경되지 않는다. 결과의 인간화된 서열<br />
은 하기에, 1번 내지 88번 잔기로부터 VLh로서 도시된다. 주의: L<strong>12</strong>A 인간 서열과 상이한 잔기만 밑줄로 표시되<br />
고, 따라서 토끼-유래된 아미노산 잔기이다. 본 실례에서, 88개 잔기 중에서 8개만 인간 서열과 상이하다.<br />
7. 단계 6에서 산출된 새로운 하이브리드 서열의 골격 3 다음에, 토끼 경쇄 항체 서열의 전체 CDR3을 부착한다.<br />
CDR3 서열은 다양한 길이일 수 있지만, 전형적으로 9개 내지 15개 아미노산 잔기 길이를 갖는다. CDR3 영역 및<br />
그 뒤에 오는 골격 4 영역의 시작은 당업자에 의해 고전적으로 정의되고 확인가능하다. 전형적으로, 골격 4의<br />
시작, 그리고 따라서 CDR3의 끝 다음은 서열 'FGGG…'로 구성되지만, 이들 잔기에 일부 변이가 존재할 수 있다.<br />
실례: 도 2에서, RbtVL의 CDR3(89번 내지 100번 아미노산 잔기)이 VLh로 표시된 인간화 서열 내에서 골격 3의<br />
끝 다음에 추가된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
8. 전형적으로, 가변 경쇄의 최종 11개 아미노산 잔기이고 상기 단계 7에서 지시된 바와 같이 시작되고 전형적<br />
으로, 아미노산 서열 '…VV<strong>KR</strong>'로 끝나는 토끼 경쇄 골격 4는 일반적으로, 생식세포 서열로부터 최근접 인간 경<br />
쇄 골격 4 동족체로 대체된다. 빈번하게, 인간 경쇄 골격 4는 서열 'FGGGTKVEI<strong>KR</strong>'을 보유한다. 최대 상동성이<br />
아닌, 또는 달리 상이한 다른 인간 경쇄 골격 4 서열이 결과의 인간화된 항체의 특이성, 친화성 및/또는 면역원<br />
성에 영향을 주지 않으면서 이용될 수 있다. 인간 경쇄 골격 4 서열은 상기 단계 7로부터 CDR3 서열 바로 다음<br />
에, 가변 경쇄 인간화된 서열의 끝에 추가된다. 이는 가변 경쇄 인간화된 아미노산 서열의 끝이다.<br />
실례: 도 2에서, RbtVL 토끼 경쇄 서열의 골격 4(FR4)는 상동성 인간 FR4 서열 위에 도시된다. 인간 FR4 서열<br />
- 90 -
[0588]<br />
[0589]<br />
[0590]<br />
[0591]<br />
[0592]<br />
[0593]<br />
[0594]<br />
[0595]<br />
[0596]<br />
[0597]<br />
[0598]<br />
[0599]<br />
[0600]<br />
은 상기 단계 7에서 추가된 CD3 영역의 끝 바로 다음에, 인간화된 가변 경쇄 서열(VLh)에 추가된다.<br />
이에 더하여, 도 34와 35에서는 본 발명에 따른 Ab1에서 가변 중쇄와 경쇄 영역으로부터 인간화된 선호되는 항-<br />
IL-6 가변 중쇄 및 가변 경쇄 서열을 도시한다. 이들 인간화된 경쇄와 중쇄 영역은 각각, 서열 번호: 647 또는<br />
651, 그리고 서열 번호: 652, 656, 657 또는 658 내에 포함된 폴리펩티드 내에 포함된다. 서열 번호: 657에서<br />
인간화된 가변 중쇄 영역의 CDR2(CDR2에서 세린 치환을 포함)는 서열 번호: 658 내에 포함된다. 경쇄와 중쇄의<br />
변이체를 예시하는 정렬은 각각, 도 36과 37에서 도시되는데, 이들 CDR 영역 내에서 서열 차이는 강조된다. CDR<br />
서열과 전형적 코딩 서열의 서열 식별자는 상기 표 1에 요약된다.<br />
중쇄<br />
1. 신호 펩티드 서열 다음에 첫 번째 아미노산을 확인한다. 이는 골격 1의 시작이다. 토끼 중쇄 단백질 서열에<br />
대한 신호 펩티드는 첫 번째 개시 메티오닌에서 시작되고 전형적으로, <strong>19</strong>개 아미노산 길이를 갖는다. 항상 그러<br />
한 것은 아니지만 전형적으로, 토끼 중쇄 신호 펩티드의 최종 3개의 아미노산 잔기는 '…VQC'이고, 그 다음에<br />
골격 1의 시작이다. 성숙 폴리펩티드의 시작은 또한, N-말단 단백질 염기서열분석에 의해 경험적으로 결정되거<br />
나, 또는 예측 알고리즘(prediction algorithm)을 이용하여 예측될 수 있다. 이는 또한, 당업자에 의해 고전적<br />
으로 정의되는 골격 1의 시작이다<br />
실례: 'QEQL…'로 시작되는 도 2에서 RbtVH 아미노산 잔기<br />
2. 골격 3의 끝을 확인한다. 이는 전형적으로, 골격 1의 시작 다음에 95-100개 아미노산이고, 그리고 전형적으<br />
로, '…CAR'(알라닌은 발린일 수도 있다)의 최종 서열을 보유한다. 이는 당업자에 의해 고전적으로 정의되는 골<br />
격 3의 끝이다.<br />
실례: '…FCVR'로 끝나는 도 2에서 RbtVH 아미노산 잔기 98<br />
3. 앞서 정의된 바와 같은 골격 1의 시작에서부터 골격 3의 끝까지 폴리펩티드의 토끼 중쇄 서열을 이용하고 가<br />
장 유사한 인간 항체 단백질 서열에 대한 서열 상동성 검색을 수행한다. 이는 전형적으로, 면역원성의 가능성을<br />
감소시키기 위하여 항체 성숙 이전에 인간 생식세포 서열의 데이터베이스에 대한 검색이긴 하지만, 임의의 인간<br />
서열이 이용될 수 있다. 전형적으로, 서열 데이터베이스를 최대 상동성에 대하여 검색하는데 BLAST와 같은 프로<br />
그램이 이용될 수 있다. 인간 항체 서열의 데이터베이스는 다양한 출처, 예를 들면, NCBI(National Center for<br />
Biotechnology Information)로부터 확인될 수 있다.<br />
실례: 도 2에서 1번 내지 98번 잔기로부터 RbtVH 아미노산 서열은 인간 항체 생식세포 데이터베이스에 대하여<br />
BLAST된다. 상위 3개의 독특한 답변된 서열은 도 2에서 3-64-04, 3-66-04, 그리고 3-53-02로서 도시된다.<br />
4. 일반적으로, 최대 상동성 인간 생식세포 가변 중쇄 서열은 이후, 인간화를 위한 기초로서 이용된다. 하지만,<br />
당업자는 서열 갭 및 골격 유사성을 비롯한 다른 인자에 기초하여, 상동성 알고리즘에 의한 결정에서 최대 상동<br />
성이 아닌 다른 서열의 이용을 결정할 수도 있다.<br />
실례: 도 2에서 3-64-04는 최대 상동성 인간 생식세포 가변 중쇄 서열이고 RbtVH의 인간화를 위한 기초로서 이<br />
용된다.<br />
5. 중쇄 인간화에 이용되는 인간 동족체에 대한 골격과 CDR 배열(FR1, FR2, FR3, CDR1 & CDR2)을 결정한다. 이<br />
는 당분야에서 기술된 바와 같은 전통적인 배치(layout)를 이용한다. 골격과 CDR 영역의 배치를 유지하면서 토<br />
끼 가변 중쇄 서열과 인간 동족체를 정렬한다.<br />
실례: 도 2에서, RbtVH 서열은 인간 상동성 서열 3-64-04와 함께 정렬되고, 그리고 골격과 CDR 도메인이 표시<br />
된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
6. 인간 상동성 중쇄 서열 CDR1과 CDR2 영역을 토끼 서열로부터 CDR1과 CDR2 서열로 대체한다. 토끼와 인간 CDR<br />
서열 간에 길이 차이가 존재하면, 전체 토끼 CDR 서열 및 이들의 길이를 이용한다. 이에 더하여, 인간 중쇄 골<br />
격 1 영역의 최종 3개의 아미노산을 토끼 중쇄 골격 1의 최종 3개의 아미노산으로 대체하는 것이 필요할 수도<br />
있다. 항상 그러한 것은 아니지만 전형적으로, 토끼 중쇄 골격 1 내에서, 이들 3개의 잔기는 세린 잔기가 선행<br />
하는 글리신 잔기 다음에 위치한다. 이에 더하여, 인간 중쇄 골격 2 영역의 최종 아미노산을 토끼 중쇄 골격 2<br />
의 최종 아미노산으로 대체하는 것이 필요할 수도 있다. 항상 그러한 것은 아니지만 전형적으로, 이는 토끼 중<br />
쇄 골격 2 내에서 이소류신 잔기가 선행하는 글리신 잔기이다. 결과의 인간화된 항체의 특이성, 친화성 및/또는<br />
- 91 -
[0601]<br />
[0602]<br />
[0603]<br />
[0604]<br />
[0605]<br />
[0606]<br />
[0607]<br />
[0608]<br />
면역원성은 더욱 작은 또는 더욱 큰 서열 교환이 수행되거나, 또는 특정한 잔기(들)가 변경되면, 변화되지 않는<br />
것이 가능하고, 기술된 이들 교환이 성공적으로 이용되긴 했지만 다른 변화가 허용될 수 있는 가능성을 배제시<br />
키지 않는다. 가령, 트립토판 아미노산 잔기는 전형적으로, 토끼 중쇄 CDR2 영역의 끝에서부터 4개 잔기 앞에서<br />
발생하는 반면, 인간 중쇄 CDR2 내에서 이러한 잔기는 전형적으로, 세린 잔기이다. 상기 위치에서 토끼 트립토<br />
판 잔기의 인간 세린 잔기로의 변화는 인간화된 항체의 특이성 또는 친화성에 거의 또는 전혀 영향을 주지 않는<br />
것으로 증명되었고, 따라서 인간화된 서열 내에서 토끼 서열-유래된 아미노산 잔기의 함량을 더욱 감소시킨다.<br />
실례: 도 2에서, 인간 상동성 가변 중쇄의 CDR1과 CDR2 아미노산 잔기는 토끼 서열(63번 위치) 내에서 트립토<br />
판 및 인간 서열 내에서 동일한 위치에서 세린이고, 그리고 인간 세린 잔기로서 유지되는 상자로 표시된 잔기를<br />
제외하고, RbtVH 토끼 항체 경쇄 서열로부터 CDR1과 CDR2 아미노산 서열로 대체된다. 이들 CDR1과 CDR2 변화에<br />
더하여, 골격 1의 최종 3개의 아미노산(위치 28-30) 및 골격 2의 최종 잔기(위치 49)는 인간이 아닌 토끼 아미<br />
노산 잔기로서 유지된다. 결과의 인간화된 서열은 하기에, 1번 내지 98번 잔기로부터 VHh로서 도시된다. 주의:<br />
3-64-04 인간 서열과 상이한 잔기만 밑줄로 표시되고, 따라서 토끼-유래된 아미노산 잔기이다. 본 실례에서, 98<br />
개 잔기 중에서 15개만 인간 서열과 상이하다<br />
7. 단계 6에서 산출된 새로운 하이브리드 서열의 골격 3 다음에, 토끼 중쇄 항체 서열의 전체 CDR3을 부착한다.<br />
CDR3 서열은 다양한 길이일 수 있지만, 전형적으로 5개 내지 <strong>19</strong>개 아미노산 잔기 길이를 갖는다. CDR3 영역 및<br />
그 뒤에 오는 골격 4 영역의 시작은 당업자에 의해 고전적으로 정의되고 확인가능하다. 전형적으로, 골격 4의<br />
시작, 그리고 따라서 CDR3의 끝 다음은 서열 WGXG…(여기서 X는 일반적으로, Q 또는 P)로 구성되지만, 이들 잔<br />
기에 일부 변이가 존재할 수 있다<br />
실례: RbtVH의 CDR3(99번 내지 110번 아미노산 잔기)이 VHh로 표시된 인간화 서열 내에서 골격 3의 끝 다음에<br />
추가된다.<br />
8. 전형적으로, 가변 중쇄의 최종 11개 아미노산 잔기이고 상기 단계 7에서 지시된 바와 같이 시작되고 전형적<br />
으로, 아미노산 서열 '…TVSS'로 끝나는 토끼 중쇄 골격 4는 일반적으로, 생식세포 서열로부터 최근접 인간 중<br />
쇄 골격 4 동족체로 대체된다. 빈번하게, 인간 중쇄 골격 4는 서열 WGQGTLVTVSS'을 보유한다. 최대 상동성이 아<br />
닌, 또는 달리 상이한 다른 인간 중쇄 골격 4 서열이 결과의 인간화된 항체의 특이성, 친화성 및/또는 면역원성<br />
에 영향을 주지 않으면서 이용될 수 있다. 인간 중쇄 골격 4 서열은 상기 단계 7로부터 CDR3 서열 바로 다음에,<br />
가변 중쇄 인간화된 서열의 끝에 추가된다. 이는 가변 중쇄 인간화된 아미노산 서열의 끝이다<br />
실례: 도 2에서, RbtVH 토끼 중쇄 서열의 골격 4(FR4)는 상동성 인간 중쇄 FR4 서열 위에 도시된다. 인간 FR4<br />
서열은 상기 단계 7에서 추가된 CD3 영역의 끝 바로 다음에, 인간화된 가변 중쇄 서열(VHh)에 추가된다.<br />
항체 및 이들의 단편을 생산하는 방법<br />
본 발명은 또한, 본 명세서에서 기술된 항체 또는 이들의 단편의 생산에 관계한다. 본 명세서에서 기술된 항체<br />
또는 이들의 단편에 상응하는 재조합 폴리펩티드는 교배 적격성 효모의 배수체, 바람직하게는 2배체 또는 4배체<br />
균주로부터 분비된다. 예시적인 구체예에서, 본 발명은 배수체 효모를 포함하는 배양액을 이용하여 연장된<br />
기간, 다시 말하면, 적어도 수일 내지 1주일, 더욱 바람직하게는 적어도 1개월 또는 수개월, 그리고 이보다 더<br />
욱 바람직하게는 적어도 6개월 내지 1년 이상 동안, 분비된 형태로 이들 재조합 폴리펩티드를 생산하는 방법에<br />
관계한다. 이들 배수체 효모 배양액은 적어도 10-25 ㎎/ℓ, 더욱 바람직하게는 적어도 50-250 ㎎/ℓ, 이보다 더<br />
욱 바람직하게는 적어도 500-1000 ㎎/ℓ, 그리고 가장 바람직하게는 1 gram/ℓ 이상의 재조합 폴리펩티드(들)를<br />
발현할 것이다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 한 쌍의 유전적으로 명료한 효모 반수체 세포가 원하는 이형멀티머 단백질의 아단위<br />
를 포함하는 발현 벡터로 형질전환된다. 한쪽 반수체 세포는 첫 번째 발현 벡터를 포함하고, 그리고 두 번째 반<br />
수체 세포는 두 번째 발현 벡터를 포함한다. 다른 구체예에서, 2배체 효모 세포는 하나 이상의 재조합 폴리펩티<br />
드의 발현과 분비를 제공하는 하나 이상의 발현 벡터로 형질전환될 것이다. 또 다른 구체예에서, 단일 반수체<br />
세포는 하나 이상의 벡터로 형질전환되고 융합 또는 교배 전략으로 배수체 효모를 생산하는데 이용될 수 있다.<br />
또 다른 구체예에서, 이배체 효모 배양액은 원하는 폴리펩티드 또는 폴리펩티드의 발현과 분비를 제공하는 하나<br />
이상의 벡터로 형질전환될 수 있다. 이들 벡터는 상동성 재조합을 통해, 또는 리콤비나아제(recombinase), 예를<br />
들면, Cre/Lox 또는 Flp/Frt를 이용하여 효모 세포의 게놈 내로 무작위로 통합되는 벡터, 예를 들면, 선형화된<br />
플라스미드 또는 다른 선형 DNA 산물을 포함할 수 있다. 선택적으로, 추가의 발현 벡터가 반수체 또는 2배체 세<br />
- 92 -
[0609]<br />
[0610]<br />
[0611]<br />
[06<strong>12</strong>]<br />
[0613]<br />
[0614]<br />
[0615]<br />
[0616]<br />
포 내로 도입될 수 있다; 또는 첫 번째 또는 두 번째 발현 벡터가 이형삼합체(heterotrimer), 이형사합체<br />
(heterotetramer) 등의 합성을 위한 추가의 코딩 서열을 포함할 수 있다. 비-동일성 폴리펩티드의 발현 수준은<br />
개별적으로 측정되고, 그리고 적절한 선별, 벡터 사본수, 프로모터 강도 및/또는 유도 등을 통해 조정될 수 있<br />
다. 형질전환된 반수체 세포는 유전적으로 교배되거나 융합된다. 결과의 2배체 또는 4배체 균주는 완전하게 조<br />
립되고 생물학적 기능성인 단백질, 본 명세서에서 기술된 인간화된 항체, 또는 이들의 단편을 생산하고 분비하<br />
는데 이용된다.<br />
단백질 생산을 위한 2배체 또는 4배체 세포의 이용은 예상치 못한 이점을 제공한다. 이들 세포는 반수체 세포<br />
의 성장에 유해할 수 있는 조건에서, 그리고 연장된 기간 동안 생산 목적으로 증대, 다시 말하면, 확대될 수 있<br />
고, 이들 조건은 높은 세포 밀도; 최소 배지에서 성장; 낮은 온도에서 성장; 선택성 압력의 부재에서 안정적인<br />
성장을 포함하고, 그리고 시간의 흐름에서 이종성 유전자 서열 일체성의 유지 및 높은 수준 발현의 유지를 제공<br />
할 수 있다. 이론에 한정됨 없이, 본 발명자들은 이들 이점이 적어도 부분적으로, 2가지 별개의 모 반수체 균주<br />
로부터 2배체 균주의 산출로부터 발생한다고 이론화한다. 이들 반수체 균주는 다수의 사소한 자가영양 돌연변이<br />
를 포함할 수 있고, 이들 돌연변이는 2배체 또는 4배체에서 보완되고, 높은 선택성 조건 하에 성장 및 강화된<br />
생산을 가능하게 한다.<br />
형질전환된 교배 적격성 반수체 효모 세포는 원하는 단백질의 아단위 편성(subunit pairing)을 가능하게 하는<br />
유전학적 방법을 제공한다. 반수체 효모 균주는 2가지 발현 벡터: 한쪽 폴리펩티드 사슬의 합성을 주동하는 첫<br />
번째 벡터 및 두 번째, 비-동일성 폴리펩티드 사슬의 합성을 주동하는 두 번째 벡터 각각으로 형질전환된다. 이<br />
들 2개의 반수체 균주는 최적화된 표적 단백질 생산이 달성될 수 있는 2배체 숙주를 제공하기 위하여 교배된다.<br />
선택적으로, 추가의 비-동일성 코딩 서열(들)이 제시된다. 이런 서열은 추가의 발현 벡터 상에, 또는 첫 번째<br />
또는 두 번째 발현 벡터 내에 존재할 수 있다. 당분야에 공지된 바와 같이, 복합 코딩 서열은 개별 프로모터로<br />
부터 독립적으로 발현되거나, 또는 시스트론(단백질 인코딩 부위)의 개시 코돈, 예를 들면, ATG에 직접적인 내<br />
부 리보솜 결합을 촉진하고, 따라서 유전자의 캡(cap)-독립성 번역을 유발하는 요소인 "내부 리보솜 결합 부위"<br />
또는 "IRES"의 포함을 통해 통합적으로 발현될 수 있다. 효모에서 기능하는 IRES 요소는 Thompson et al.<br />
(2001) P.N.A.S. 98:<strong>12</strong>866-<strong>12</strong>868에서 기술된다.<br />
본 발명의 한 구체예에서, IgA의 강화된 안정성을 제공하는 항체 서열은 분비 J 사슬과 공동으로<br />
생산된다(참조: U.S. 특허 No. 5,959,177; 그리고 5,202,422).<br />
바람직한 구체예에서, 이들 2개의 반수체 효모 균주는 각각 영양요구성이고, 그리고 이들 반수체 세포의 성장을<br />
위하여 배지의 보완을 필요로 한다. 이들 한 쌍의 영양요구체는 상보적이고, 따라서 2배체 산물은 반수체 세포<br />
에 요구되는 보완물질의 부재에서 성장할 것이다. 효모에서 아미노산(가령, met, lys, his, arg 등), 뉴클레오<br />
시드(가령, ura3, ade1 등) 등에 대한 요구를 비롯하여 많은 유전자 마커가 공지되어 있다. 아미노산 마커가 본<br />
발명의 방법에 바람직할 수 있다. 대안으로, 원하는 벡터를 포함하는 2배체 세포는 다른 수단에 의해, 예를 들<br />
면, 다른 마커, 예를 들면, 녹색 형광 단백질, 항생제 내성 유전자, 다양한 우성 선별가능 마커 등의 이용에 의<br />
해 선별될 수 있다.<br />
2개의 형질전환된 반수체 세포는 유전적으로 교배되고, 그리고 이러한 교배 사건으로부터 발생하는 2배체 균주<br />
는 그들의 하이브리드 영양 요구 및/또는 항생제 내성 스펙트럼에 의해 선별될 수 있다. 대안으로, 이들 2개의<br />
형질전환된 반수체 균주의 집단은 스페로플라스트화되고 융합되고, 그리고 2배체 자손이 재생되고 선별된다. 어<br />
느 한쪽 방법에 의해, 2배체 균주는 그들의 모와 상이한 배지에서 성장하는 능력에 기초하여, 확인되고 선별적<br />
으로 성장될 수 있다. 가령, 이들 2배체 세포는 항생제를 포함하는 최소 배지에서 성장될 수 있다. 이러한 2배<br />
체 합성 전략은 일정한 이점을 갖는다. 2배체 균주는 재조합 단백질의 생산 및/또는 분비에 영향을 줄 수 있는,<br />
기초 돌연변이에 더욱 넓은 보완을 통하여 강화된 수준의 이종성 단백질을 생산하는 잠재력을 갖는다. 게다가,<br />
일단 안정적인 균주가 획득되면, 이들 균주를 선별하는데 이용되는 임의의 항생제는 성장 배지 내에 반드시 연<br />
속적으로 존재할 필요가 없다.<br />
앞서 언급된 바와 같이, 일부 구체예에서, 반수체 효모는 단일 또는 복합 벡터로 형질전환되고, 그리고 상기 벡<br />
터(들)를 포함하는 2배체 세포를 생산하기 위하여 비-형질전환된 세포와 교배되거나 융합될 수 있다. 다른 구체<br />
예에서, 배수체 효모 세포는 2배체 효모 세포에 의한 원하는 이종성 폴리펩티드의 발현과 분비를 제공하는 하나<br />
이상의 벡터로 형질전환될 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 2개의 반수체 균주는 폴리펩티드의 라이브러리, 예를 들면, 항체 중쇄 또는 경쇄의<br />
- 93 -
[0617]<br />
[0618]<br />
[06<strong>19</strong>]<br />
[0620]<br />
[0621]<br />
[0622]<br />
라이브러리로 형질전환된다. 이들 폴리펩티드를 합성하는 형질전환된 반수체 세포는 상보성 반수체 세포와 교배<br />
된다. 결과의 2배체 세포는 기능성 단백질에 대하여 스크리닝된다. 이들 2배체 세포는 기능 검사를 위한 다수의<br />
폴리펩티드 조합을 신속하고, 편의하고, 저렴하게 확보하는 수단을 제공한다. 이러한 기술은 특히, 최적화된 아<br />
단위 합성 수준이 기능성 단백질 발현과 분비에 결정적인 이형이합체 단백질 산물의 산출에 적용가능하다.<br />
본 발명의 또 다른 구체예에서, 2개의 아단위의 발현 수준 비율은 산물 산출을 최대화시키기 위하여 조절된다.<br />
이형이합체 아단위 단백질 수준은 이전에, 최종 산물 산출에 영향을 주는 것으로 밝혀졌다(Simmons LC, J<br />
Immunol Methods. 2002 May 1;263(1-2):133-47). 조절은 발현 벡터 상에 존재하는 마커에 대한 선별에 의해 교<br />
배 단계에 앞서 달성될 수 있다. 벡터의 사본수를 안정적으로 증가시킴으로써, 발현 수준이 증가될 수 있다. 일<br />
부 사례에서, 폴리펩티드의 아단위 간에 균형된 비율에 도달하기 위하여 다른 사슬에 비하여 한쪽 사슬의 수준<br />
을 증가시키는 것이 바람직할 수 있다. 항생제 내성 마커, 예를 들면, Zeocin(플레오마이신) 내성 마커, G418<br />
내성 등이 이런 목적에 유용하고 더욱 높은 수준의 Zeocin(플레오마이신) 또는 G418에 내성인 형질전환체를<br />
선별함으로써 균주 내에서 발현 벡터의 복수 통합된 사본을 포함하는 균주에 대한 농축 수단을 제공한다. 아단<br />
위 유전자의 적절한 비율, 예를 들면, 1:1; 1:2 등은 효과적인 단백질 생산에 중요할 수 있다. 심지어 양쪽 아<br />
단위를 전사하기 위하여 동일한 프로모터가 이용될 때, 많은 다른 인자가 발현된 단백질의 최종 수준에 기여하<br />
고, 이런 이유로 다른 쪽에 비하여 한쪽 인코딩된 유전자의 사본의 숫자를 증가시키는 것이 유용할 수 있다. 대<br />
안으로, 단일 사본 벡터 균주에 비하여 더욱 높은 수준의 폴리펩티드를 생산하는 2배체 균주는 발현 벡터의 복<br />
수 사본을 보유하는 2개의 반수체 균주를 교배함으로써 산출된다.<br />
숙주 세포는 앞서 기술된 발현 벡터로 형질전환되고, 교배되어 2배체 균주를 형성하고, 그리고 프로모터를 유도<br />
하거나, 형질전환체를 선별하거나, 또는 원하는 서열을 인코딩하는 유전자를 증폭하기 위하여 적절하게 변형된<br />
전통적인 영양 배지에서 배양된다. 효모의 성장에 적합한 다수의 최소 배지는 당분야에 공지되어 있다. 이들<br />
배지는 필요에 따라, 염(가령, 염화나트륨, 칼슘, 마그네슘, 그리고 인산염), 완충제(가령, 인산염, HEPES), 뉴<br />
클레오시드(가령, 아데노신과 티미딘), 항생제, 미량 원소, 그리고 글루코오스 또는 등가의 에너지 공급원으로<br />
보충될 수 있다. 임의의 다른 필요 보충물질 역시 당업자에게 공지되어 있는 적절한 농도로 포함될 수 있다. 배<br />
양 조건, 예를 들면, 온도, pH 등은 발현을 위하여 선별된 숙주 세포에서 기존에 이용된 것들이고, 그리고 당업<br />
자에게 명백할 것이다.<br />
분비된 단백질은 배양 배지로부터 회수된다. 프로테아제 저해제, 예를 들면, 페닐 메틸 설포닐 플루오르화물<br />
(PMSF)은 정제 동안 단백질 분해(proteolytic degradation)를 저해하는데 유용하고, 그리고 항생제는 외래의 오<br />
염물질의 성장을 예방하기 위하여 포함될 수 있다. 조성물은 당분야에 공지된 방법을 이용하여 농축, 여과, 분<br />
석 등이 수행될 수 있다.<br />
본 발명의 2배체 세포는 생산 목적으로 성장된다. 이런 생산 목적에는 바람직하게는, 미리-형성된 아미노산 및<br />
다른 복합적 생물분자가 결핍되는 최소 배지, 예를 들면, 질소 공급원으로서 암모니아, 그리고 에너지와 탄소<br />
공급원으로서 글루코오스, 그리고 인산염, 칼슘 등의 공급원으로서 염을 포함하는 배지에서 성장이 포함된다.<br />
바람직하게는, 이런 생산 배지는 선택성 작용제, 예를 들면, 항생제, 아미노산, 퓨린, 피리미딘 등이 결핍된다.<br />
2배체 세포는 높은 세포 밀도, 예를 들면, 적어도 대략 50 g/ℓ; 더욱 일반적으로, 적어도 대략 100 g/ℓ로 성<br />
장될 수 있고, 그리고 적어도 대략 300, 대략 400, 대략 500 g/ℓ 또는 그 이상이다.<br />
본 발명의 한 구체예에서, 생산 목적을 위한 개체 세포의 성장은 낮은 온도에서 수행되고, 이들 온도는 로그 상<br />
(phase) 동안, 정지 상(phase) 동안, 또는 둘 모두에서 낮아질 수 있다. 용어 "낮은 온도"는 적어도 대략 15℃,<br />
더욱 일반적으로 적어도 대략 17℃의 온도를 지칭하고, 그리고 대략 20℃, 일반적으로 대략 25℃ 이하, 더욱 일<br />
반적으로 대략 22℃ 이하이다. 본 발명의 또 다른 구체예에서, 낮은 온도는 일반적으로 대략 28℃ 이하이다. 성<br />
장 온도는 생산 배양액에서 전장 분비된 단백질의 생산에 영향을 줄 수 있고, 그리고 배양 성장 온도가 하락하<br />
면 본래 산물 수율이 강하게 증가될 수 있다. 하락된 온도는 세포 프로테아제 분해의 감소와 함께, 표적 산물을<br />
생성시키기 위하여 숙주에 의해 이용되는 접힘과 번역후 처리 경로를 통해 세포내 이동(intracellular<br />
trafficking)을 돕는 것으로 보인다.<br />
본 발명의 방법은 분비된, 활성 단백질, 바람직하게는 포유동물 단백질의 발현을 제공한다. 본 명세서에서, 한<br />
구체예에서, 분비된, "활성 항체"는 동계 항원에 정확하게 결합하는 적어도 2개의 적절하게 편성된 사슬의 정확<br />
하게 접힘된 멀티머를 지칭한다. 활성 단백질의 발현 수준은 일반적으로 적어도 대략 10-50 ㎎/ℓ, 더욱 일반적<br />
으로 적어도 대략 100 ㎎/ℓ, 바람직하게는 적어도 대략 500 ㎎/ℓ 배양액이고, 그리고 1000 ㎎/ℓ 배양액 또는<br />
그 이상일 수 있다.<br />
- 94 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0623]<br />
[0624]<br />
[0625]<br />
[0626]<br />
[0627]<br />
[0628]<br />
[0629]<br />
[0630]<br />
[0631]<br />
[0632]<br />
[0633]<br />
[0634]<br />
본 발명의 방법은 생산 동안 숙주와 이종성 코딩 서열의 증가된 안정성을 제공할 수 있다. 이러한 안정성은 예<br />
로써, 높은 수준의 발현 기간의 유지에 의해 증명되고, 여기서 발현의 출발 수준은 많아야 대략 20%, 많아야<br />
10% 감소되고, 그리고 대략 20 배증(doubling), 50 배증, 100 배증, 또는 그 이상에서 많아야 대략 5% 감소될<br />
수 있다.<br />
균주 안정성은 또한, 시간의 흐름에서 이종성 유전자 서열 일체성의 유지를 제공하고, 여기서 활성 코딩 서열과<br />
필수 전사 조절 요소의 서열은 적어도 대략 99%의 2배체 세포, 일반적으로 적어도 대략 99.9%의 2배체 세포, 그<br />
리고 바람직하게는 대략 20 배증, 50 배증, 100 배증, 또는 그 이상에서 적어도 대략 99.99%의 2배체 세포에서<br />
유지된다. 바람직하게는, 실질적으로 모든 2배체 세포는 활성 코딩 서열과 필수 전사 조절 요소의 서열을 유지<br />
한다.<br />
항체를 생산하는 다른 방법은 당업자에게 널리 공지되어 있다. 가령, 키메라 항체를 생산하는 방법은 당분야에<br />
널리 공지되어 있다(참조: U.S. 특허 No. 4,816,567(Cabilly et al.); Morrison et al., P.N.A.S. USA,<br />
81:8651-55 (<strong>19</strong>84); Neuberger, M.S. et al., Nature, 314:268-270 (<strong>19</strong>85); Boulianne, G.L. et al., Nature,<br />
3<strong>12</strong>:643-46 (<strong>19</strong>84), 이들 각각의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
유사하게, 인간화된 항체를 생산하는 다른 방법은 당분야에 널리 공지되어 있다(참조: U.S. 특허 No.<br />
5,530,101, 5,585,089, 5,693,762와 6,180,370(Queen et al); U.S. 특허 No. 5,225,539와 6,548,640(Winter);<br />
U.S. 특허 No. 6,054,297, 6,407,213과 6,639,055(Carter et al); U.S. 특허 No. 6,632,927(Adair); Jones,<br />
P.T. et al, Nature, 321:522-525 (<strong>19</strong>86); Reichmann, L., et al, Nature, 332:323-327 (<strong>19</strong>88); Verhoeyen,<br />
M, et al, Science, 239:1534-36 (<strong>19</strong>88), 이들 각각의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
IL-6 결합 특이성을 갖는 본 발명의 항체 폴리펩티드는 또한, 당업자에게 널리 공지된 전통적인 기술을 이용하<br />
여, 오페론 및 항체 중쇄를 인코딩하는 DNA 서열을 포함하는 발현 벡터를 작제함으로써 생산될 수 있고, 여기서<br />
항체 특이성을 위하여 요구되는 CDR을 인코딩하는 DNA 서열은 비-인간 세포 공급원, 바람직하게는 토끼 B-세포<br />
공급원으로부터 유래되고, 반면 항체 사슬의 나머지 부분을 인코딩하는 DNA 서열은 인간 세포 공급원으로부터<br />
유래된다.<br />
두 번째 발현 벡터는 당업자에게 널리 공지된 동일한 전통적인 수단을 이용하여 생산되고, 상기 발현 벡터는 오<br />
페론 및 항체 경쇄를 인코딩하는 DNA 서열을 포함하고, 여기서 항체 특이성에 요구되는 CDR을 인코딩하는 DNA<br />
서열은 비-인간 세포 공급원, 바람직하게는 토끼 B-세포 공급원으로부터 유래되고, 반면 항체 사슬의 나머지 부<br />
분을 인코딩하는 DNA 서열은 인간 세포 공급원으로부터 유래된다.<br />
이들 발현 벡터는 형질감염된 숙주 세포를 생산하기 위하여 당업자에게 널리 공지된 전통적인 기술에 의해 숙주<br />
세포 내로 형질감염되고, 상기 형질감염된 숙주 세포는 항체 폴리펩티드를 생산하기 위한 당업자에게 널리 공지<br />
된 전통적인 기술에 의해 배양된다.<br />
숙주 세포는 앞서 기술된 2가지 발현 벡터: 오페론 및 경쇄-유래된 폴리펩티드를 인코딩하는 DNA를 포함하는 첫<br />
번째 발현 벡터, 그리고 오페론 및 중쇄-유래된 폴리펩티드를 인코딩하는 DNA를 포함하는 두 번째 벡터로 공동-<br />
형질감염될 수 있다. 이들 2가지 벡터는 상이한 선별가능 마커를 포함하지만, 바람직하게는 중쇄와 경쇄 폴리펩<br />
티드의 실질적으로 동등한 발현을 달성한다. 대안으로, 단일 벡터가 이용될 수 있고, 상기 벡터는 중쇄와 경쇄<br />
폴리펩티드 둘 모두를 인코딩하는 DNA를 포함한다. 중쇄와 경쇄에 대한 코딩 서열은 cDNA를 포함할 수 있다.<br />
항체 폴리펩티드를 발현하는데 이용되는 숙주 세포는 세균 세포, 예를 들면, 대장균(E. coli), 또는 진핵 세포<br />
일 수 있다. 본 발명의 특히 바람직한 구체예에서, 이러한 목적을 위한 충분히-정의된 유형의 포유동물 세포,<br />
예를 들면, 골수종 세포 또는 중국 햄스터 난소(Chinese hamster ovary, CHO) 세포주가 이용될 수 있다.<br />
벡터가 작제되는 일반적인 방법, 숙주 세포를 생산하는데 요구되는 형질감염 방법, 그리고 이들 숙주 세포로부<br />
터 항체 폴리펩티드를 생산하는데 요구되는 배양 방법 모두 전통적인 기술을 포함한다. 항체를 생산하는데 이용<br />
되는 세포주는 바람직하게는, 포유동물 세포주이지만, 임의의 다른 적합한 세포주, 예를 들면, 세균 세포주, 예<br />
를 들면, 대장균(E. coli)-유래된 세균 균주, 또는 효모 세포주가 대용될 수 있다.<br />
유사하게, 일단 생산된 항체 폴리펩티드는 당분야의 표준 절차, 예를 들면, 십자-흐름 여과(cross-flow<br />
filtration), 황산암모늄 침전, 친화성 칼럼 색층분석 등에 따라 정제될 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 명세서에서 기술된 항체 폴리펩티드는 본 발명의 항체 폴리펩티드와 동일한 치료 적용에 유용한 펩티드 또는<br />
비-펩티드 모방체의 설계와 합성에도 이용될 수 있다(참조: Saragobi et al, Science, 253:792-795 (<strong>19</strong>91), 이<br />
- 95 -
[0635]<br />
[0636]<br />
[0637]<br />
[0638]<br />
[0639]<br />
[0640]<br />
의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
중쇄와 경쇄 폴리펩티드와 폴리뉴클레오티드의 전형적인 구체예<br />
본 섹션에서는 중쇄와 경쇄 폴리펩티드, 그리고 이런 폴리펩티드를 인코딩하는 예시적인 폴리뉴클레오티드의 예<br />
시적인 구체예를 열거한다. 이들 예시적인 폴리뉴클레오티드는 개시된 피치아(Pichia) 발현 시스템에서 발현에<br />
적합하다.<br />
일정한 구체예에서, 본 발명은 본 출원에서 열거되거나, 또는 본 출원에서 열거된 폴리펩티드를 인코딩하는 폴<br />
리뉴클레오티드, 또는 낮은-엄밀도 조건, 중간-엄밀도 조건, 또는 높은-엄밀도 조건 하에 상기 폴리뉴클레오티<br />
드에 하이브리드화되는 폴리뉴클레오티드에 적어도 70%, 예를 들면, 적어도 75%, 적어도 80%, 적어도 85%, 적어<br />
도 90%, 적어도 91%, 적어도 92%, 적어도 93%, 적어도 94%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%,<br />
적어도 99%, 또는 100% 동일성을 갖는 폴리뉴클레오티드, 바람직하게는 IL-6 폴리펩티드에 특이적 결합이 포함<br />
되지만 이에 국한되지 않는 본 명세서에 열거된 생물학적 활성 중에서 적어도 한 가지를 갖는 폴리펩티드(가령<br />
면역글로불린 중쇄와 경쇄, 단일-쇄 항체, 항체 단편 등)를 인코딩하는 것들을 포함한다. 또 다른 측면에서, 본<br />
발명은 이런 폴리뉴클레오티드 및/또는 이런 폴리뉴클레오티드에 의해 인코딩되는 폴리펩티드를 포함하는 조성<br />
물을 포함한다. 또 다른 측면에서, 본 발명은 IL-6과 연관되거나, 또는 IL-6 길항제, 예를 들면, Ab1로 예방,<br />
치료 또는 개선될 수 있는 질환 또는 이상(가령, 악액질, 암 피로, 관절염 등)의 치료 방법을 포함하고, 상기<br />
방법은 이런 폴리뉴클레오티드 및/또는 폴리펩티드를 포함하는 조성물을 투여하는 단계를 포함한다.<br />
일정한 바람직한 구체예에서, 중쇄 폴리펩티드는 도 2와 34-37 또는 표 1에 묘사되고, 그리고 본 명세서에서 열<br />
거된 중쇄와 경쇄 폴리펩티드 서열 내에 포함된 것들을 비롯하여, 본 명세서에서 열거된 중쇄 및/또는 경쇄 폴<br />
리펩티드의 하나 이상의 CDR 서열(본 명세서에서 열거된 중쇄와 경쇄 폴리펩티드 내에 포함된 것들 포함) 및 본<br />
명세서에서 열거된 하나 이상의 골격 영역 폴리펩티드를 포함할 것이다. 일정한 바람직한 구체예에서, 중쇄 폴<br />
리펩티드는 도 2와 34-37 또는 표 1에서 묘사된 바와 같은, 또는 본 명세서에서 열거된 중쇄 또는 경쇄 폴리펩<br />
티드 내에 포함된 바와 같은 하나 이상의 골격 4 영역 서열을 포함할 것이다.<br />
일정한 바람직한 구체예에서, 경쇄 폴리펩티드는 도 2와 34-37 또는 표 1에 묘사되고, 그리고 본 명세서에서 열<br />
거된 중쇄와 경쇄 폴리펩티드 서열 내에 포함된 것들을 비롯하여, 본 명세서에서 열거된 중쇄 및/또는 경쇄 폴<br />
리펩티드의 하나 이상의 CDR 서열(본 명세서에서 열거된 중쇄와 경쇄 폴리펩티드 내에 포함된 것들 포함) 및 본<br />
명세서에서 열거된 하나 이상의 골격 영역 폴리펩티드를 포함할 것이다. 일정한 바람직한 구체예에서, 경쇄 폴<br />
리펩티드는 도 2와 34-37 또는 표 1에서 묘사된 바와 같은, 또는 본 명세서에서 열거된 중쇄 또는 경쇄 폴리펩<br />
티드 내에 포함된 바와 같은 하나 이상의 골격 4 영역 서열을 포함할 것이다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 명세서에서 열거된 임의의 구체예에서, 열거된 일정한 서열은 달리 명시되지 않으면, 서로를 치환할 수<br />
있다. 특정 서열이 서로를 치환할 수 있다는 상술은 이런 상술이 어디에서 만들어지는 지에 상관없이, 한정이<br />
아닌 예시인 것으로 이해되고, 그리고 이런 치환은 치환의 예시적인 실례가 열거되지 않을 때에도 포함되는 것<br />
으로 이해된다. 가령, 하나 이상의 Ab1 경쇄 폴리펩티드, 예를 들면, 서열 번호: 2, 20, 647, 651, 660, 666,<br />
699, 702, 706, 또는 709 중에서 한 가지가 열거되는 경우에, 달리 명시되지 않으면 다른 Ab1 경쇄 폴리펩티드<br />
가 치환될 수 있다. 유사하게, Ab1 중쇄 폴리펩티드 중에서 한 가지, 예를 들면, 서열 번호: 3, 18, <strong>19</strong>, 652,<br />
656, 657, 658, 661, 664, 665, 704, 또는 708 중에서 한 가지가 열거되는 경우에, 달리 명시되지 않으면 다른<br />
Ab1 중쇄 폴리펩티드가 치환될 수 있다. 유사하게, Ab1 경쇄 폴리뉴클레오티드 중에서 한 가지, 예를 들면, 서<br />
열 번호: 10, 662, 698, 701, 또는 705 중에서 한 가지가 열거되는 경우에, 달리 명시되지 않으면 다른 Ab1 경<br />
쇄 폴리뉴클레오티드가 치환될 수 있다. 유사하게, Ab1 중쇄 폴리뉴클레오티드 중에서 한 가지, 예를 들면, 서<br />
열 번호: 11, 663, 700, 703, 또는 707 중에서 한 가지가 열거되는 경우에, 달리 명시되지 않으면 다른 Ab1 중<br />
쇄 폴리뉴클레오티드가 치환될 수 있다. 부가적으로, 아래의 군 중에서 하나의 임의의 구성원에 관한 상술은 아<br />
래와 같은, 상기 군의 다른 구성원에 의한 치환을 포함하는 것으로 이해된다: Ab2 경쇄 폴리펩티드(서열 번호:<br />
21과 667); Ab2 경쇄 폴리뉴클레오티드(서열 번호: 29와 669); Ab2 중쇄 폴리펩티드(서열 번호: 22와 668);<br />
Ab2 중쇄 폴리뉴클레오티드(서열 번호: 30과 670); Ab3 경쇄 폴리펩티드(서열 번호: 37과 671); Ab3 경쇄 폴리<br />
뉴클레오티드(서열 번호: 45와 673); Ab3 중쇄 폴리펩티드(서열 번호: 38과 672); Ab3 중쇄 폴리뉴클레오티드<br />
(서열 번호: 46과 674); Ab4 경쇄 폴리펩티드(서열 번호: 53과 675); Ab4 경쇄 폴리뉴클레오티드(서열 번호: 61<br />
과 677); Ab4 중쇄 폴리펩티드(서열 번호: 54와 676); Ab4 중쇄 폴리뉴클레오티드(서열 번호: 62와 678); Ab5<br />
경쇄 폴리펩티드(서열 번호: 69와 679); Ab5 경쇄 폴리뉴클레오티드(서열 번호: 77과 681); Ab5 중쇄 폴리펩티<br />
- 96 -
[0641]<br />
[0642]<br />
[0643]<br />
[0644]<br />
[0645]<br />
[0646]<br />
[0647]<br />
[0648]<br />
[0649]<br />
[0650]<br />
[0651]<br />
[0652]<br />
[0653]<br />
드(서열 번호: 70과 680); Ab5 중쇄 폴리뉴클레오티드(서열 번호: 78과 682); Ab6 경쇄 폴리펩티드(서열 번호:<br />
85와 683); Ab6 경쇄 폴리뉴클레오티드(서열 번호: 93과 685); Ab6 중쇄 폴리펩티드(서열 번호: 86과 684);<br />
Ab6 중쇄 폴리뉴클레오티드(서열 번호: 94와 686); Ab7 경쇄 폴리펩티드(서열 번호: 101, 1<strong>19</strong>, 687, 693); Ab7<br />
경쇄 폴리뉴클레오티드(서열 번호: 109와 689); Ab7 중쇄 폴리펩티드(서열 번호: 102, 117, 118, 688, 691, 그<br />
리고 692); Ab7 중쇄 폴리뉴클레오티드(서열 번호: 110과 690); Ab1 경쇄 CDR1 폴리뉴클레오티드(서열 번호: <strong>12</strong><br />
와 694); Ab1 경쇄 CDR3 폴리뉴클레오티드(서열 번호: 14와 695); Ab1 중쇄 CDR2 폴리뉴클레오티드(서열 번호:<br />
16과 696), 그리고 Ab1 중쇄 CDR3 폴리뉴클레오티드(서열 번호: 17과 697).<br />
전형적인 Ab1-인코딩 폴리뉴클레오티드 서열은 아래와 같이 열거된다:<br />
서열 번호: 662:<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCGGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCATTAACAATGAATTATCCTGGTATCAGCAGAAACCAGGGCAGCGTCCCAAGCTC<br />
CTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCT<br />
서열 번호: 663:<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTTATGGTAGTGATGAAACGGCCTACGCGACCTGGGCGATAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACA<br />
GCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCAAAATTTAACTTG<br />
서열 번호: 698:<br />
GCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCC<br />
TGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGG<br />
ACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGC<br />
GGAGGGACCAAGGTGGAAATCAAACGTACG<br />
서열 번호: 700:<br />
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGGTCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTG<br />
ACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATCATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACC<br />
ATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGCCTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGAC<br />
TGGGATGCAAAGTTCAACTTGTGGGGCCAAGGGACCCTCGTCACCGTCTCGAGC<br />
서열 번호: 701:<br />
GCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCC<br />
TGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGG<br />
ACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGC<br />
GGAGGGACCAAGGTGGAAATCAAACGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTG<br />
TGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGAC<br />
AGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTG<br />
AGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT<br />
서열 번호: 703:<br />
공개특허 10-2011-01<strong>12</strong>308<br />
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGGTCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTG<br />
ACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATCATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACC<br />
ATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGCCTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGAC<br />
TGGGATGCAAAGTTCAACTTGTGGGGCCAAGGGACCCTCGTCACCGTCTCGAGCGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAG<br />
AGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTG<br />
CACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAAC<br />
GTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAGAGTTGAGCCCAAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTG<br />
- 97 -
[0654]<br />
[0655]<br />
[0656]<br />
[0657]<br />
[0658]<br />
[0659]<br />
[0660]<br />
[0661]<br />
[0662]<br />
[0663]<br />
GGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAA<br />
GACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACGCCAGCACGTACCGTGTGGTC<br />
AGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCC<br />
AAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGC<br />
TTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTC<br />
CTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAG<br />
AGCCTCTCCCTGTCTCCGGGTAAA<br />
서열 번호: 705:<br />
ATGAAGTGGGTAACCTTTATTTCCCTTCTGTTTCTCTTTAGCAGCGCTTATTCCGCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGA<br />
GACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCCTGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGG<br />
GCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGGACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCA<br />
ACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGCGGAGGGACCAAGGTGGAAATCAAACGTACGGTGGCTGCACCATCTGTC<br />
TTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAG<br />
GTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAA<br />
GCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT<br />
서열 번호: 707:<br />
ATGAAGTGGGTAACCTTTATTTCCCTTCTGTTTCTCTTTAGCAGCGCTTATTCCGAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGG<br />
TCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATC<br />
ATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACCATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGC<br />
CTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGACTGGGATGCAAAGTTCAACTTGTGGGGCCAAGGGACCCTCGTCACCGTC<br />
TCGAGCGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTAC<br />
TTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGC<br />
AGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAGAGTTGAGCCC<br />
AAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTC<br />
ATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCAT<br />
AATGCCAAGACAAAGCCGCGGGAGGAGCAGTACGCCAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTAC<br />
AAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCA<br />
TCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCG<br />
GAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAAC<br />
GTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAA<br />
서열 번호: 720:<br />
ATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCCTGG<br />
TATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGGACA<br />
GACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCT<br />
서열 번호: 721:<br />
GCCTATGATATGACCCAGACTCCAGCCTCGGTGTCTGCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCATTAACAATGAATTATCC<br />
TGGTATCAGCAGAAACCAGGGCAGCGTCCCAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGG<br />
ACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGTGCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCTTTCGGC<br />
GGAGGGACCGAGGTGGTGGTCAAACGT<br />
서열 번호: 722:<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCCTGG<br />
TATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGGACA<br />
GACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGCGGA<br />
GGGACCAAGGTGGAAATCAAACGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGC<br />
CTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGC<br />
AAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGC<br />
- 98 -
[0664]<br />
[0665]<br />
[0666]<br />
[0667]<br />
[0668]<br />
[0669]<br />
[0670]<br />
[0671]<br />
[0672]<br />
[0673]<br />
[0674]<br />
[0675]<br />
[0676]<br />
[0677]<br />
TCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT<br />
서열 번호: 723:<br />
GCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCC<br />
TGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGG<br />
ACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGC<br />
GGAGGGACCAAGGTGGAAATCAAACGT<br />
서열 번호: 724:<br />
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGGTCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTG<br />
ACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATCATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACC<br />
ATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGCCTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGAC<br />
TGGGATGCAAAGTTCAACTTG<br />
서열 번호: 725:<br />
CAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACACCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACC<br />
TGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATCATTTATGGTAGTGATGAAACGGCCTACGCGACCTGGGCGATAGGCCGATTCACCATC<br />
TCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACAGCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCA<br />
AAATTTAACTTGTGGGGCCAAGGCACCCTGGTCACCGTCTCGAGC<br />
스크리닝 분석<br />
본 발명은 또한, IL-6 연관된 질환 또는 이상의 증상을 보이는 환자에서 IL-6과 연관된 질환과 이상의 확인을<br />
보조하도록 설계된 스크리닝 분석법에 관계한다.<br />
본 발명의 한 구체예에서, 본 발명의 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체는 IL-6과 연관된<br />
질환 또는 이상의 증상을 보이는 환자로부터 획득된 생물학적 시료에서 IL-6의 존재를 검출하는데 이용된다.<br />
IL-6의 존재, 또는 비교되는 생물학적 시료에서 IL-6의 질환전 수준과 비교하여 이의 상승된 수준은 IL-6과 연<br />
관된 질환 또는 이상을 진단하는데 유익할 수 있다.<br />
본 발명의 다른 구체예는 확인된 IL-6 연관된 질환 또는 이상의 증상을 보이는 환자에서 IL-6과 연관된 질환 또<br />
는 이상의 진단을 보조하는 진단 또는 스크리닝 분석법을 제시하고, 상기 분석법은 번역후 변형된 항-IL-6<br />
항체, 또는 이의 결합 단편 또는 변이체를 이용하여 상기 환자로부터 생물학적 시료에서 IL-6 발현의 수준을 분<br />
석하는 단계를 포함한다. 항-IL-6 항체, 또는 이의 결합 단편 또는 변이체는 예로써, 본 명세서에 앞서 기술된<br />
검출가능 모이어티를 포함하도록 번역후 변형될 수 있다.<br />
생물학적 시료에서 IL-6 수준은 본 명세서에서 기술된 변형된 항-IL-6 항체, 또는 이의 결합 단편 또는 변이체<br />
를 이용하여 결정되고, 그리고 생물학적 시료에서 IL-6의 수준은 IL-6의 표준 수준(가령, 정상적인 생물학적 시<br />
료에서 수준)과 비교된다. 당업자가 인지하는 바와 같이, 정상적인 생물학적 시료 간에 다소간 변이성이 존재하<br />
고, 그리고 결과를 평가할 때 이러한 변이성이 고려되어야 한다.<br />
앞서 예시된 분석법은 또한, 질환 또는 이상을 모니터하는데 유용한데, 여기서 IL-6 연관된 질환 또는 이상을<br />
앓는 것으로 생각되는 환자로부터 생물학적 시료에서 획득된 IL-6의 수준은 상기 환자에서 IL-6 수준이 예로써,<br />
치료 섭생으로 변하는 지를 확인하기 위하여, 동일한 환자로부터 이전 생물학적 시료에서 IL-6의 수준과 비교된<br />
다.<br />
본 발명은 또한, 진단 조성물의 진단 효과량을 투여하는 단계를 포함하는, IL-6을 발현하는 세포의 존재를 검출<br />
하는 생체내 화상 방법에 관계한다. 상기 생체내 화상은 예로써, IL-6 발현 종양 또는 전이, 그리고 IL-6 발현<br />
염증 부위의 검출과 화상에 유용하고, 그리고 효과적인 암 또는 관절염 치료 프로토콜의 설계를 위한 계획 섭생<br />
(planning regimen)의 일부로서 이용될 수 있다. 이러한 치료 프로토콜은 항-IL-6 항체, 또는 이의 단편 또는<br />
변이체 뿐만 아니라 예로써, 방사선, 화학요법, 사이토킨 요법, 유전자 요법, 그리고 항체 요법 중에서 한 가지<br />
이상을 포함할 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
당업자가 인지하는 바와 같이, 생물학적 시료에는 혈청, 혈장, 소변, 타액, 점액, 흉수(pleural fluid), 활액<br />
- 99 -
[0678]<br />
[0679]<br />
[0680]<br />
[0681]<br />
[0682]<br />
[0683]<br />
(synovial fluid)과 척수액(spinal fluid)이 포함되지만 이들에 국한되지 않는다.<br />
IL-6과 연관된 질환과 이상의 증상을 개선하거나 감소시키는, 또는 이들 질환과 이상을 치료하거나 예방하는 방<br />
법<br />
본 발명의 한 구체예에서, 본 명세서에서 기술된 IL-6 길항제, 예를 들면, Ab1은 IL-6과 연관된 질환과 이상의<br />
증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유용하다. 본 명세서에서 기<br />
술된 IL-6 길항제(가령, Ab1)는 또한, 하기에 더욱 상세하게 기술된 바와 같은 제약학적 조성물의 형태로, IL-6<br />
과 연관된 질환과 이상의 치료가 필요한 환자에 치료 효과량으로 투여될 수 있다.<br />
본 발명의 한 구체예에서, 본 명세서에서 기술된 IL-6 길항제(가령, Ab1)는 상승된 C-반응성 단백질(CRP)과 연<br />
관된 질환과 이상의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유용하<br />
다. 이런 질환에는 만성 염증을 나타내는 임의의 질환, 예를 들면, 류머티스성 관절염, 유년형 류머티스성 관절<br />
염, 건선, 건선성 관절병증, 강직성 척추염, 전신성 홍반성 루푸스, 크론병, 궤양성 대장염, 천포창, 피부근염,<br />
다발근육염, 류머티스성 다발성 근육통, 거대 세포 동맥염, 혈관염, 결절성 다발동맥염, 베게너 육아종증, 가와<br />
사키병, 고립형 CNS 혈관염, Churg-Strauss 관절염, 현미경적 다발동맥염, 현미경적 다발혈관염, 헤노호-쉐라인<br />
자반증, 본태성 한랭글로불린혈증성 혈관염, 류머티스성 혈관염, 한랭글로불린혈증, 재발성 다발연골염, 베체트<br />
병, 다까야수 동맥염, 허혈성 심장 질환, 발작, 다발성 경화증, 패혈증, 바이러스 감염(가령, B형 간염, C형 간<br />
염, HIV, 거대세포바이러스, 엡스타인-바 바이러스, 파보바이러스 B<strong>19</strong> 등)에 속발성인 혈관염, 버거스씨병, 암,<br />
진행된 암, 골관절염, 전신 경화증, CREST 증후군, 라이터병, 뼈의 파제트병, 쇼그렌 증후군, 1형 당뇨병, 2형<br />
당뇨병, 가족성 지중해열, 자가면역 혈소판감소증, 자가면역 용혈성 빈혈, 자가면역 갑상선 질환, 악성 빈혈,<br />
백반, 원형탈모증, 원발성 담도 경화증, 자가면역 만성 활성 간염, 알코올성 간경화증, B형과 C형 간염을 비롯<br />
한 바이러스 간염, 다른 장기 특이적 자가면역 질환, 화상, 특발성 폐 섬유증, 만성 폐쇄성 폐 질환, 알레르기<br />
천식, 다른 알레르기 질환 또는 이들의 임의의 조합이 포함된다.<br />
본 발명의 한 구체예에서, 본 명세서에서 기술된 IL-6 길항제, 예를 들면, 항-IL-6 항체(가령, Ab1), 이들의 변<br />
이체 또는 이들의 단편은 감소된 혈청 알부민과 연관된 질환과 이상, 예를 들면, 류머티스성 관절염, 암, 진행<br />
된 암, 간 질환, 신장 질환, 염증성 장 질환, 셀리악병, 외상, 화상, 감소된 혈청 알부민과 연관된 기타 질환,<br />
또는 이들의 임의의 조합의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데<br />
유용하다.<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 IL-6 길항제는 다른 활성제와 공동으로 환자에 투여된다.<br />
가령, IL-6 길항제, 예를 들면, Ab1은 하나 이상의 화학요법제, 예를 들면, VEGF 길항제, EGFR 길항제, 플라틴,<br />
탁솔, 이리노테칸, 5-플루오르우라실, 젬시타빈, 류코보린, 스테로이드, 시클로포스파미드, 멜팔란, 빈카 알칼<br />
로이드(가령, 빈블라스틴, 빈크리스틴, 빈데신과 비노렐빈), 무스틴, 티로신 키나아제 저해제, 방사선요법, 성<br />
호르몬 길항제, 선택성 안드로겐 수용체 조절제, 선택성 에스트로겐 수용체 조절제, PDGF 길항제, TNF 길항제,<br />
IL-1 길항제, 인터루킨(가령, IL-<strong>12</strong> 또는 IL-2), IL-<strong>12</strong>R 길항제, 독소 접합된 단일클론 항체, 종양 항원 특이적<br />
단일클론 항체, Erbitux, Avastin, Pertuzumab, 항-CD20 항체, Rituxan<br />
, 오크렐리주맙, 오파투무맙, DXL625, Herceptin<br />
, 또는 이들의 임의의 조합과 공동-투여될 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 피로와 연관된<br />
질환과 이상의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유용하다. 피<br />
로와 연관된 질환과 이상에는 일반적인 피로, 운동-유발된 피로, 암-관련된 피로, 섬유근육통, 염증 질환-관련<br />
된 피로와 만성 피로 증후군이 포함되지만 이들에 국한되지 않는다(참조: Esper DH, et al, The cancer<br />
cachexia syndrome: a review of metabolic and clinical manifestations, Nutr Clin Pract., 2005 Aug;20<br />
(4):369-76; Vgontzas AN, et al, IL-6 and its circadian secretion in humans, Neuroimmunomodulation,<br />
2005;<strong>12</strong>(3):131-40; Robson-Ansley, PJ, et al, Acute interleukin-6 administration impairs athletic<br />
performance in healthy, trained male runners, Can J Appl Physiol., 2004 Aug;29(4):411-8; Shephard RJ.,<br />
Cytokine responses to physical activity, with particular reference to IL-6: sources, actions, and<br />
clinical implications, Crit Rev Immunol., 2002;22(3):165-82; Arnold, MC, et al, Using an interleukin-6<br />
- 100 -
[0684]<br />
[0685]<br />
challenge to evaluate neuropsychological performance in chronic fatigue syndrome, Psychol Med., 2002<br />
Aug;32(6):1075-89; Kurzrock R., The role of cytokines in cancer-related fatigue, Cancer, 2001 Sep<br />
15;92(6 Suppl):1684-8; Nishimoto N, et al, Improvement in Castleman's disease by humanized anti-<br />
interleukin-6 receptor antibody therapy, Blood, 2000 Jan 1; 95 (1):56-61; Vgontzas AN, et al,<br />
Circadian interleukin-6 secretion and quantity and depth of sleep, J Clin Endocrinol Metab., <strong>19</strong>99<br />
Aug;84(8):2603-7; 그리고 Spath-Schwalbe E, et al, Acute effects of recombinant human interleukin 6 on<br />
endocrine and central nervous sleep functions in healthy men, J Clin Endocrinol Metab., <strong>19</strong>98<br />
May;83(5):1573-9; 이들 각각의 내용은 본 발명에서 그 전체가 참조로서 편입된다).<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 바람직한 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 악액질<br />
의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유용하다. 악액질과 연관<br />
된 질환과 이상에는 암-관련된 악액질, 심장-관련된 악액질, 호흡기-관련된 악액질, 신장-관련된 악액질과 연령<br />
-관련된 악액질이 포함되지만 이들에 국한되지 않는다(참조: Barton, BE., Interleukin-6 and new strategies<br />
for the treatment of cancer, hyperproliferative diseases and paraneoplastic syndromes, Expert Opin<br />
Ther Targets, 2005 Aug;9(4):737-52; Zaki MH, et al, CNTO 328, a monoclonal antibody to IL-6, inhibits<br />
human tumor-induced cachexia in nude mice, Int J Cancer, 2004 Sep 10;111(4):592-5; Trikha M, et al,<br />
Targeted anti-interleukin-6 monoclonal antibody therapy for cancer: a review of the rationale and<br />
clinical evidence, Clin Cancer Res., 2003 Oct 15;9(13):4653-65; Lelli G, et al, Treatment of the<br />
cancer anorexia-cachexia syndrome: a critical reappraisal, J Chemother., 2003 Jun;15(3):220-5; Argiles<br />
JM, et al, Cytokines in the pathogenesis of cancer cachexia, Curr Opin Clin Nutr Metab Care, 2003<br />
Jul;6(4):401-6; Barton BE., IL-6-like cytokines and cancer cachexia: consequences of chronic<br />
inflammation, Immunol Res., 2001;23(1):41-58; Yamashita JI, et al, Medroxyprogesterone acetate and<br />
cancer cachexia: interleukin-6 involvement, Breast Cancer, 2000;7(2):130-5; Yeh SS, et al, Geriatric<br />
cachexia: the role of cytokines, Am J Clin Nutr., <strong>19</strong>99 Aug;70(2):183-97; Strassmann G, et al,<br />
Inhibition of experimental cancer cachexia by anti-cytokine and anti-cytokine-receptor therapy,<br />
Cytokines Mol Ther., <strong>19</strong>95 Jun;1(2):107-13; Fujita J, et al, Anti-interleukin-6 receptor antibody<br />
prevents muscle atrophy in colon-26 adenocarcinoma-bearing mice with modulation of lysosomal and ATP-<br />
ubiquitin-dependent proteolytic pathways, Int J Cancer, <strong>19</strong>96 Nov 2768(5):637-43; Tsujinaka T, et al,<br />
Interleukin 6 receptor antibody inhibits muscle atrophy and modulates proteolytic systems in<br />
interleukin 6 transgenic mice, J Clin Invest., <strong>19</strong>96 Jan l;97(l):244-9; Emilie D, et al, Administration<br />
of an anti-interleukin-6 monoclonal antibody to patients with acquired immunodeficiency syndrome and<br />
lymphoma: effect on lymphoma growth and on B clinical Symptoms, Blood, <strong>19</strong>94 Oct 1584 (8):2472-9; 그리<br />
고 Strassmann G, et al, Evidence for the involvement of interleukin 6 in experimental cancer cachexia,<br />
J Clin Invest., <strong>19</strong>92 May;89(5):1681-4; 이들 각각의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 자가면역<br />
질환과 이상의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유용하다. 자<br />
가면역과 연관된 질환과 이상에는 류머티스성 관절염, 전신성 홍반성 루푸스(SLE), 전신성 유년형 특발성 관절<br />
염, 건선, 건선성 관절병증, 강직성 척추염, 염증성 장 질환(IBD), 류머티스성 다발성 근육통, 거대 세포 동맥<br />
염, 자가면역 혈관염, 이식편 대(對) 숙주 질환(GVHD), 쇼그렌 증후군, 성인 발병성 스틸병이 포함되지만 이들<br />
에 국한되지 않는다. 본 발명의 바람직한 구체예에서, 본 명세서에서 기술된 인간화된 항-IL-6 항체, 또는 이들<br />
의 단편 또는 변이체는 류머티스성 관절염과 전신성 유년형 특발성 관절염의 증상을 개선하거나 감소시키는데,<br />
또는 이들 질환과 이상을 치료하거나 예방하는데 유용하다(참조: Nishimoto N., Clinical studies in patients<br />
with Castleman's disease, Crohn's disease, and rheumatoid arthritis in Japan, Clin Rev Allergy<br />
Immunol., 2005 Jun;28(3):221-30; Nishimoto N, et al, Treatment of rheumatoid arthritis with humanized<br />
anti-interleukin-6 receptor antibody: a multicenter, double-blind, placebo-controlled trial, Arthritis<br />
Rheum., 2004 Jun;50(6):1761-9; Choy E., Interleukin 6 receptor as a target for the treatment of<br />
rheumatoid arthritis, Ann Rheum Dis., 2003 Nov;62 Suppl 2:ii68-9; Nishimoto N, et al, Toxicity,<br />
pharmacokinetics, and dose-finding study of repetitive treatment with the humanized anti-interleukin 6<br />
receptor antibody MRA in rheumatoid arthritis. Phase I/II clinical study, J Rheumatol., 2003<br />
Jul;30(7):1426-35; Mihara M, et al, Humanized antibody to human interleukin-6 receptor inhibits the<br />
development of collagen arthritis in cynomolgus monkeys, Clin Immunol., 2001 Mar;98(3):3<strong>19</strong>-26;<br />
- 101 -
공개특허 10-2011-01<strong>12</strong>308<br />
Nishimoto N, et al, Anti-interleukin 6 receptor antibody treatment in rheumatic disease, Ann Rheum<br />
Dis., 2000 Nov;59 Suppl 1:i21-7; Tackey E, et al, Rationale for interleukin-6 blockade in systemic<br />
lupus erythematosus, Lupus, 200413(5):339-43; Finck BK, et al, Interleukin 6 promotes murine lupus in<br />
NZB/NZW Fl mice, J Clin Invest., <strong>19</strong>94 Aug;94 (2):585-91; Kitani A, et al, Autostimulatory effects of<br />
IL-6 on excessive B cell differentiation in patients with systemic lupus erythematosus: analysis of<br />
IL-6 production and IL-6R expression, Clin Exp Immunol., <strong>19</strong>92 Apr;88(1):75-83; Stuart RA, et al,<br />
Elevated serum interleukin-6 levels associated with active disease in systemic connective tissue<br />
disorders, Clin Exp Rheumatol., <strong>19</strong>95 Jan-Feb;l3 (1):17-22; Mihara M, et al, IL-6 receptor blockage<br />
inhibits the onset of autoimmune kidney disease in NZB/W Fl mice, Clin Exp Immunol., <strong>19</strong>98<br />
Jun;<strong>12</strong>(3):397-402; Woo P, et al, Open label phase II trial of single, ascending doses of MRA in<br />
Caucasian children with severe systemic juvenile idiopathic arthritis: proof of principle of the<br />
efficacy of IL-6 receptor blockade in this type of arthritis and demonstration of prolonged clinical<br />
improvement, Arthritis Res Ther., 2005;7(6):RI281-8. Epub 2005 Sep 15; Yokota S, et al, Clinical study<br />
of tocilizumab in children with systemic-onset juvenile idiopathic arthritis, Clin Rev Allergy<br />
Immunol., 2005 Jun;28(3):231-8; Yokota S, et al, Therapeutic efficacy of humanized recombinant anti-<br />
interleukin-6 receptor antibody in children with systemic-onset juvenile idiopathic arthritis,<br />
Arthritis Rheum., 2005 Mar;52(3):818-25; de Benedetti F, et al, Targeting the interleukin-6 receptor:<br />
a new treatment for systemic juvenile idiopathic arthritis?, Arthritis Rheum., 2005 Mar;52(3):687-93;<br />
De Benedetti F, et al, Is systemic juvenile rheumatoid arthritis an interleukin 6 mediated disease?, J<br />
Rheumatol., <strong>19</strong>98 Feb;25(2):203-7; Ishihara K, et al, IL-6 in autoimmune disease and chronic<br />
inflammatory proliferative disease, Cytokine Growth Factor Rev., 2002 Aug-Oct;13 (4-5):357- 68; Gilhar<br />
A, et al, In vivo effects of cytokines on psoriatic skin grafted on nude mice :involvement of the<br />
tumor necrosis factor (TNF) receptor, Clin Exp Immunol., <strong>19</strong>96 Oct;106(1):134-42; Spadaro A, et al,<br />
Interleukin-6 and soluble interleukin-2 receptor in psoriatic arthritis: correlations with clinical<br />
and laboratory parameters, Clin Exp Rheumatol., <strong>19</strong>96 Jul-Aug;14 (4):413-6; Ameglio F, et al,<br />
Interleukin-6 and tumor necrosis factor levels decrease in the suction blister fluids of psoriatic<br />
patients during effective therapy, Dermatology, <strong>19</strong>94189(4):359-63; Wendling D, et al, Combination<br />
therapy of anti-CD4 and anti-IL-6 monoclonal antibodies in a case of severe spondylarthropathy, Br J<br />
Rheumatol., <strong>19</strong>96 Dec;35(<strong>12</strong>):1330; Gratacos J, et al, Serum cytokines (IL-6, TNF-alpha, IL-1 beta and<br />
IFN-gamma) in ankylosing spondylitis: a close correlation between serum IL-6 and disease activity and<br />
severity, Br J Rheumatol., <strong>19</strong>94 Oct;33(10):927-31; Ito H., Treatment of Crohn's disease with anti-IL-6<br />
receptor antibody, J Gastroenterol., 2005 Mar;40 Suppl 16:32-4; Ito H, et al, A pilot randomized trial<br />
of a human anti-interleukin-6 receptor monoclonal antibody in active Crohn's disease,<br />
Gastroenterology, 2004 Apr;<strong>12</strong>6(4):989-96; discussion 947; Ito H., IL-6 and Crohn's disease, Curr Drug<br />
Targets Inflamm Allergy, 2003 Jun;2(2):<strong>12</strong>5 Ito H, et al, Anti-IL-6 receptor monoclonal antibody<br />
inhibits leukocyte recruitment and promotes T-cell apoptosis in a murine model of Crohn's disease, J<br />
Gastroenterol., 2002 Nov;37 Suppl 14:56-61; Ito H., Anti-interleukin-6 therapy for Crohn's disease,<br />
Curr Pharm Des., 20039(4):295-305; Salvarani C, et al, Acute-phase reactants and the risk of<br />
relapse/recurrence in polymyalgia rheumatica: a prospective follow-up study, Arthritis Rheum., 2005<br />
Feb 1553(1):33-8; Roche NE, et al, Correlation of interleukin-6 production and disease activity in<br />
polymyalgia rheumatica and giant cell arteritis, Arthritis Rheum., <strong>19</strong>93 Sep;36(9):<strong>12</strong>86-94; Gupta M, et<br />
al, Cytokine modulation with immune gamma-globulin in peripheral blood of normal children and its<br />
implications in Kawasaki disease treatment, J Clin Immunol., 2001 May;21(3):<strong>19</strong>3-9; Noris M, et al,<br />
Interleukin-6 and RANTES in Takayasu arteritis: a guide for therapeutic decisions?, Circulation, <strong>19</strong>99<br />
Jul 6100(1):55-60; Besbas N, et al, The role of cytokines in Henoch Schonlein purpura, Scand J<br />
Rheumatol., <strong>19</strong>9726(6):456-60; Hirohata S, et al, Cerebrospinal fluid interleukin-6 in progressive<br />
Neuro-Behcet's syndrome, Clin Immunol Immunopathol., <strong>19</strong>97 Jan;82(1):<strong>12</strong>-7; Yamakawa Y, et al,<br />
Interleukin-6 (IL-6) in patients with Behcet's disease, J Dermatol Sci., <strong>19</strong>96 Mar;11(3):189-95; Kim<br />
DS., Serum interleukin-6 in Kawasaki disease, Yonsei Med J., <strong>19</strong>92 Jun;33(2):183-8; Lange, A., et al,<br />
Cytokines, adhesion molecules (E-selectin and VCAM-l) and graft-versus-host disease, Arch. Immunol<br />
Ther Exp., <strong>19</strong>95, 43(2):99-105; Tanaka, J., et al, Cytokine gene expression after allogeneic bone<br />
- 102 -
[0686]<br />
[0687]<br />
marrow transplantation, Leuk. Lymphoma, <strong>19</strong>95 16(5-6):413-418; Dickenson, AM, et al, Predicting outcome<br />
in hematological stem cell transplantation, Arch Immunol Ther Exp., 2002 50(6):371-8; Zeiser, R, et<br />
al, Immunopathogenesis of acute graft-versus-host disease: implications for novel preventive and<br />
therapeutic strategies, Ann Hematol., 2004 83(9):551-65; Dickinson, AM, et al, Genetic polymorphisms<br />
predicting the outcome of bone marrow transplants, Br. J Haematol., 2004 <strong>12</strong>7(5):479- and Scheinberg<br />
MA, et al, Interleukin 6: a possible marker of disease activity in adult onset Still's disease, Clin<br />
Exp Rheumatol., <strong>19</strong>96 Nov-Dec;14 (6):653-5, 이들 각각의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 골격계와<br />
연관된 질환과 이상의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유용<br />
하다. 골격계와 연관된 질환과 이상에는 골관절염, 골다공증과 뼈의 파제트병이 포함되지만 이들에 국한되지 않<br />
는다. 본 발명의 바람직한 구체예에서, 본 명세서에서 기술된 인간화된 항-IL-6 항체, 또는 이들의 단편 또는<br />
변이체는 골관절염의 증상을 개선하거나 감소시키는데, 또는 골관절염을 치료하거나 예방하는데 유용하다(참조:<br />
Malemud CJ., Cytokines as therapeutic targets for osteoarthritis, BioDrugs, 2004;18(1):23-35;<br />
Westacott CI, et al, Cytokines in osteoarthritis: mediators or markers of joint destruction?, Semin<br />
Arthritis Rheum., <strong>19</strong>96 Feb;25(4):254-72; Sugiyama T., Involvement of interleukin-6 and prostaglandin<br />
E2 in particular osteoporosis of postmenopausal women with rheumatoid arthritis, J Bone Miner Metab.,<br />
2001;<strong>19</strong>(2):89-96; Abrahamsen B, et al, Cytokines and bone loss in a 5-year longitudinal study -<br />
hormone replacement therapy suppresses serum soluble interleukin-6 receptorand increases interleukin-<br />
1-receptor antagonist: the Danish Osteoporosis Prevention Study, J Bone Miner Res., 2000<br />
Aug;15(8):1545-54; Straub RH, et al, Hormone replacement therapy and interrelation between serum<br />
interleukin-6 and body mass index in postmenopausal women: a population-based study, J Clin Endocrinol<br />
Metab., 2000 Mar;85(3):1340-4; Manolagas SC, The role of IL-6 type cytokines and their receptors in<br />
bone, Ann N Y Acad Sci., <strong>19</strong>98 May 1840:<strong>19</strong>4-204; Ershler WB, et al, Immunologic aspects of<br />
osteoporosis, Dev Comp Immunol., <strong>19</strong>97 Nov-Dec;21(6):487-99; Jilka RL, et al, Increased osteoclast<br />
development after estrogen loss: mediation by interleukin-6, Science, <strong>19</strong>92 Jul 3;257(5066):88-91;<br />
Kallen KJ, et al, New developments in IL-6 dependent biology and therapy: where do we stand and what<br />
are the options?, Expert Opin Investig Drugs, <strong>19</strong>99 Sep;8(9):1327-49; Neale SD, et al, The influence of<br />
serum cytokines and growth factors on osteoclast formation in Paget's disease, QJM, 2002 Apr;95<br />
(4):233 - 40; Roodman GD, Osteoclast function In Paget's disease and multiple myeloma, Bone, <strong>19</strong>95<br />
Aug;17(2 Suppl):57S-61S; Hoyland JA, et al, Interleukin-6, IL-6 receptor, and IL-6 nuclear factor gene<br />
expression in Paget's disease, J Bone Miner Res., <strong>19</strong>94 Jan;9(1):75-80; 그리고 Roodman GD, et al,<br />
Interleukin 6. A potential autocrine/paracrine factor in Paget's disease of bone, J Clin Invest., <strong>19</strong>92<br />
Jan;89(1):46-52; 이들 각각의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 암과 연<br />
관된 질환과 이상의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유용하<br />
다. 암과 연관된 질환과 이상에는 가시세포종, 선방 세포 암종, 청신견종, 선단 흑자성 흑색종, 선단한선종, 급<br />
성 호산성 백혈병, 급성 림프모구성 백혈병, 급성 거핵모구성 백혈병, 급성 단구성 백혈병, 성숙을 동반한 급성<br />
골수모구성 백혈병, 급성 골수성 수상돌기 세포 백혈병, 급성 골수성 백혈병, 급성 전골수성 백혈병, 사기질종,<br />
선암종, 선양 낭성 암종, 선종, 선양 치성 종양, 부신피질 암종, 성체 T-세포 백혈병, 공격성 NK-세포 백혈병,<br />
AIDS-관련된 암, AIDS-관련된 림프종, 포상 연부 육종, 법랑아세포 섬유치아종, 항문 암, 퇴행성 대세포<br />
림프종, 역형성 갑상선 암, 혈관면역모세포형 T-세포 림프종, 혈관근육지방종, 맥관육종, 충수 암, 별아교세포<br />
종, 비정형 기형 횡문근양 종양, 기저 세포 암종, 기저-유사 암종, B-세포 백혈병, B-세포 림프종, 집합관<br />
암종, 담관 암, 방광 암, 모세포종, 골 암, 골 종양, 뇌간 교종, 뇌 종양, 유방암, 브렌너 종양, 기관지 종양,<br />
세기관지폐포 암종, 갈색 종양, 버킷 림프종, 원발부위 불명암, 유암종, 암종, in situ 암종, 음경 암종, 원발<br />
부위 불명 암종, 암육종, 캐슬만씨병, 중추신경계 배양 종양, 소뇌 별아교세포종, 대뇌 별아교세포종, 자궁경부<br />
암, 담관암, 연골종, 연골육종, 척삭종, 융모막암종, 맥락막총 유두종, 만성 림프성 백혈병, 만성 단구성 백혈<br />
병, 만성 골수성 백혈병, 만성 골수증식성 질환, 만성 호중구성 백혈병, 투명-세포 종양, 대장 암, 결장직장<br />
암, 머리인두종, 피부 T-세포 림프종, Degos 질환, 융기성 피부섬유육종, 유피낭종, 복부 결합조직형성 소원형<br />
세포 종양, 미만성 거대 B 세포 림프종, 배아형성장애 신경상피 종양, 배아 암종, 내배엽동 종양, 자궁내막 암,<br />
자궁내막 자궁 암, 자궁내막양 종양, 장병증 연관 T-세포 림프종, 상의모세포종, 상의세포종, 상피양 육종, 적<br />
- 103 -
공개특허 10-2011-01<strong>12</strong>308<br />
백혈병, 식도 암, 감각신경모세포종, 유잉 계통 종양, 유잉 계통 육종, 유잉 육종, 두개외 생식세포 종양, 생식<br />
샘외 생식세포 종양, 간외 담도 암, 유방외성 파제트병, 난관 암, 태아속 태아, 섬유종, 섬유육종, 소포성 림프<br />
종, 소포성 갑상선 암, 담낭 암, 담낭 암, 신경절교종, 신경절신경종, 위 암, 위 림프종, 위장 암, 위장<br />
유암종, 위장 기질 종양, 위장 기질 종양, 생식세포 종양, 배세포종, 임신성 융모막암종, 임신성 융모성 종양,<br />
뼈의 거대 세포 종양, 다형성교모세포종, 신경교종, 대뇌신경교종증, 사구 종양, 글루카곤종, 생식아세포종, 과<br />
립층 세포 종양, 모상 세포 백혈병, 모상 세포 백혈병, 두경부 암, 두경부 암, 심장 암, 혈관모세포종, 혈관주<br />
위세포종, 혈관육종, 혈액학적 악성, 간세포 암종, 간비 T-세포 림프종, 유전성 유방-난소암 증후군, 호지킨 림<br />
프종, 호지킨 림프종, 하인두 암, 시상하부 신경교종, 염증 유방암, 안구내 흑색종, 섬 세포 암종, 섬 세포 종<br />
양, 연소형 골수단구성 백혈병, 카포시 육종, 카포시 육종, 신장 암, 클라츠킨씨 종양, 크루켄버그 종양, 후두<br />
암, 후두 암, 악성 흑자 흑색종, 백혈병, 백혈병, 입술과 구강 암, 지방육종, 폐암, 황체종, 림프관종, 림프관<br />
육종, 림프상피종, 림프성 백혈병, 림프종, 마크로글로불린혈증, 악성 섬유성 조직구종, 악성 섬유성 조직구종,<br />
뼈의 악성 섬유성 조직구종, 악성 신경교종, 악성 중피종, 악성 말초신경초 종양, 악성 횡문근양 종양, 악성 트<br />
리톤 종양, MALT 림프종, 덮개 세포 림프종, 비만 세포 백혈병, 종격동 생식세포 종양, 종격동 종양, 갑상선 수<br />
질암, 속질모세포종, 속질모세포종, 속질상피종, 흑색종, 흑색종, 수막종, 메르켈 세포 암종, 중피종, 중피종,<br />
잠복원발성 전이성 편평 목 암, 전이성 요로상피 암종, 혼합 뮬러 종양, 단구성 백혈병, 구강 암, 점액 종양,<br />
다발성 캐슬만씨 병, 다발성 내분비 종양 증후군, 다발성 골수종, 다발성 골수종, 균상식육종, 균상식육종, 골<br />
수형성이상 질환, 골수형성이상 증후군, 골수성 백혈병, 골수성 육종, 골수증식 질환, 점액종, 비강 암, 코인두<br />
암, 코인두 암종, 신생물, 신경집종, 신경모세포종, 신경모세포종, 신경섬유종, 신경종, 결절성 흑색종, 비-호<br />
지킨 림프종, 비-호지킨 림프종, 비-흑색종 피부 암, 비-소세포 폐암, 안종양, 희소별아교세포종, 핍지교종, 호<br />
산성세포종, 시신경초 수막종, 구강 암, 구강 암, 입인두 암, 골육종, 골육종, 난소암, 난소암, 난소 상피 암,<br />
난소 생식세포 종양, 난소 저급성 악성 종양, 유방의 파제트병, 판코스트 종양, 췌장암, 췌장암, 갑상샘 유두<br />
암, 유두종증, 곁신경절종, 부비동 암, 부갑상선 암, 음경 암, 혈관주위 상피모양 세포 종양, 인두 암, 갈색세<br />
포종, 중간 분화의 송과체 실질 종양, 송과체모세포종, 하수체세포종, 뇌하수체 선종, 뇌하수체 종양, 플라스마<br />
세포 신생물, 흉막폐아세포종, 다배아종, 전구 T-림프모구성 림프종, 원발성 중추신경계 림프종, 원발성 삼출성<br />
림프종, 원발성 간세포 암, 원발성 간 암, 원발성 복막 암, 원시 신경외배엽 종양, 전립선암, 복막가성점액종,<br />
직장 암, 신장 세포 암종, 염색체 15에서 NUT 유전자가 관련된 호흡기 암종, 망막모세포종, 횡문근종, 횡문근육<br />
종, 리히터 변형, 천미골 기형종, 타액선 암, 육종, 다발성신경초종, 피지선 암종, 속발성 신생물, 정상피종,<br />
장액 종양, 세르톨리 라이디히 세포 종양, 성삭-기질 종양, 세자리 증후군, 인환 세포 암종, 피부 암, 청색 소<br />
원형세포 종양, 소세포 암종, 소세포 폐암, 소세포 림프종, 소장 암, 연부 조직 육종, 소마토스타틴종, 매연 사<br />
마귀, 척추 종양, 척추 종양, 비장 번연 림프종, 편평 세포 암종, 위 암, 표재 확장성 흑색종, 천막위 원시 신<br />
경외배엽 종양, 표면 상피-기질 종양, 활액 육종, T-세포 급성 림프모구성 백혈병, T-세포 큰 과립성 림프구 백<br />
혈병, T-세포 백혈병, T-세포 림프종, T-세포 전림프성 백혈병, 기형종, 말기 림프성 암, 고환 암, 난포막종,<br />
인후 암, 흉선 암종, 가슴샘종, 갑상선 암, 신우 요관의 이행 세포 암, 이행 세포 암종, 요막관 암, 요도 암,<br />
비뇨생식기 신생물, 자궁 육종, 포도막 흑색종, 질 암, 버너-모리슨 증후군, 사마귀모양 암종, 시각경로 신경교<br />
종, 외음부 암, 왈덴스트룀 마크로글로불린혈증, 바르틴 종양, 윌름 종양, 또는 이들의 임의의 조합, 그리고 암<br />
화학요법에서 약물 내성 및 암 화학요법 독성이 포함되지만 이들에 국한되지 않는다(참조: Hirata T, et al,<br />
Humanized anti-interleukin-6 receptor monoclonal antibody induced apoptosis of fresh and cloned human<br />
myeloma cells in vitro, Leuk Res., 2003 Apr;27(4):343-9, Bataille R, et al, Biologic effects of anti-<br />
interleukin-6 murine monoclonal antibody in advanced multiple myeloma, Blood, <strong>19</strong>95 Jul 15;86 (2):685-<br />
91; Goto H, et al, Mouse anti-human interleukin-6 receptor monoclonal antibody inhibits proliferation<br />
of fresh human myeloma cells in vitro, Jpn J Cancer Res., <strong>19</strong>94 Sep;85(9):958-65; Klein B, et al,<br />
Murine anti-interleukin-6 monoclonal antibody therapy for a patient with plasma cell leukemia, Blood,<br />
<strong>19</strong>91 Sep 1;78(5):1<strong>19</strong>8-204; Mauray S, et al, Epstein-Barr virus-dependent lymphoproliferative disease:<br />
critical role of IL-6, Eur J Immunol., 2000 Jul;30(7):2065-73; Tsunenari T, et al, New xenograft model<br />
of multiple myeloma and efficacy of a humanized antibody against human interleukin-6 receptor, Blood,<br />
<strong>19</strong>97 Sep 15;90(6):2437-44; Emilie D, et al, Interleukin-6 production in high-grade B lymphomas:<br />
correlation with the presence of malignant immunoblasts in acquired immunodeficiency syndrome and in<br />
human immunodeficiency virus-seronegative patients, Blood, <strong>19</strong>92 Jul 15;80(2):498-504; Emilie D, et al,<br />
Administration of an anti-interleukin-6 monoclonal antibody to patients with acquired immunodeficiency<br />
syndrome and lymphoma: effect on lymphoma growth and on B clinical Symptoms, Blood, <strong>19</strong>94 Oct 15;<br />
84(8):2472-9; Smith PC, et al, Anti-interleukin-6 monoclonal antibody induces regression of human<br />
- 104 -
[0688]<br />
prostate cancer xenografts in nude mice, Prostate, 2001 Jun 15;48(1):47-53; Smith PC, et al,<br />
Interleukin-6 and prostate cancer progression, Cytokine Growth Factor Rev., 2001 Mar;<strong>12</strong>(1):33-40;<br />
Chung TD, et al, Characterization of the role of IL-6 in the progression of prostate cancer, Prostate,<br />
<strong>19</strong>99 Feb 15;38(3):<strong>19</strong>9-207; Okamoto M, et al, Interleukin-6 as a paracrine and autocrine growth factor<br />
in human prostatic carcinoma cells in vitro, Cancer Res., <strong>19</strong>97 Jan 1;57(1):141-6; Reittie JE, et al,<br />
Interleukin-6 inhibits apoptosis and tumor necrosis factor induced proliferation of B-chronic<br />
lymphocytic leukemia, Leuk Lymphoma, <strong>19</strong>96 Jun;22(1-2):83-90, follow 186, color plate VI; Sugiyama H,<br />
et al, The expression of IL-6 and its related genes in acute leukemia, Leuk Lymphoma, <strong>19</strong>96 Mar;21(1-<br />
2):49-52; Bataille R, et al, Effects of an anti-interleukin-6 (IL-6) murine monoclonal antibody in a<br />
patient with acute monoblastic leukemia, Med Oncol Tumor Pharmacother., <strong>19</strong>93;10(4):185-8; Kedar I, et<br />
al, Thalidomide reduces serum C-reactive protein and interleukin-6 and induces response to IL-2 in a<br />
fraction of metastatic renal cell cancer patients who failed IL-2-based therapy, Int J Cancer, 2004<br />
Jun 10;110(2):260-5; Angelo LS, Talpaz M, Kurzrock R, Autocrine interleukin-6 production in renal cell<br />
carcinoma: evidence for the involvement of p53, Cancer Res., 2002 Feb 1;62(3):932-40; Nishimoto N,<br />
Humanized anti-interleukin-6 receptor antibody treatment of multicentric Castleman disease, Blood,<br />
2005 Oct 15;106(8):2627-32, Epub 2005 Jul 5; Katsume A, et al, Anti-interleukin 6 (IL-6) receptor<br />
antibody suppresses Castleman's disease like symptoms emerged in IL-6 transgenic mice, Cytokine, 2002<br />
Dec 21;20(6):304-11; Nishimoto N, et al, Improvement in Castleman's disease by humanized anti-<br />
interleukin-6 receptor antibody therapy, Blood, 2000 Jan 1;95(1):56-61; Screpanti I, Inactivation of<br />
the IL-6 gene prevents development of multicentric Castleman's disease in C/EBP betamice, J Exp Med.,<br />
<strong>19</strong>96 Oct 1;184(4):1561-6; Hsu SM, et al, Expression of interleukin-6 in Castleman's disease, Hum<br />
Pathol., <strong>19</strong>93 Aug;24(8):833-9; Yoshizaki K, et al, Pathogenic significance of interleukin-6 (IL 6/BSF-<br />
2) in Castleman's disease, Blood, <strong>19</strong>89 Sep;74(4):1360-7; Nilsson MB, et al, Interleukin-6, secreted by<br />
human ovarian carcinoma cells, is a potent proangiogenic cytokine, Cancer Res., 2005 Dec<br />
1;65(23):10794-800; Toutirais O, et al, Constitutive expression of TGF-betal, interleukin-6 and<br />
interleukin-8 by tumor cells as a major component of immune escape in human ovarian carcinoma, Eur<br />
Cytokine Netw., 2003 Oct-Dec;14(4):246-55; Obata NH, et al, Effects of interleukin 6 on in vitro cell<br />
attachment, migration and invasion of human ovarian carcinoma, Anticancer Res., <strong>19</strong>97 Jan-Feb;17<br />
(lA):337-42; Dedoussis GV, et al, Endogenous interleukin 6 conveys resistance to cis-<br />
diamminedichloroplatinum-mediated apoptosis of the K562 human leukemic cell line, Exp Cell Res., <strong>19</strong>99<br />
Jun 15;249(2):269-78; Borsellino N, et al, Blocking signaling through the Gp130 receptor chain by<br />
interleukin-6 and oncostatin M inhibits PC-3 cell growth and sensitizes the tumor cells to etoposide<br />
and cisplatin-mediated cytotoxicity, Cancer, <strong>19</strong>99 Jan 1;85(1):134-44; Borsellino N, et al, Endogenous<br />
interleukin 6 is a resistance factor for cis-diamminedichloroplatinum and etoposide-mediated<br />
cytotoxicity of human prostate carcinoma cell lines, Cancer Res., <strong>19</strong>95 Oct 15;55(20):4633-9; Mizutani<br />
Y, et al, Sensitization of human renal cell carcinoma cells to cis-diamminedichloroplatinum(II) by<br />
anti-interleukin 6 monoclonal antibody or anti-interleukin 6 receptor monoclonal antibody; Cancer<br />
Res., <strong>19</strong>95 Feb 1;55(3):590-6; Yusuf RZ, et al, Paclitaxel resistance: molecular mechanisms and<br />
pharmacologic manipulation, Curr Cancer Drug Targets, 2003 Feb;3(1):1-<strong>19</strong>; Duan Z, et al,<br />
Overexpression of IL-6 but not IL-8 increases paclitaxel resistance of U-20S human osteosarcoma cells,<br />
Cytokine, 2002 Mar 7;17(5):234-42; Conze D, et al, Autocrine production of interleukin 6 causes<br />
multidrug resistance in breast cancer cells, Cancer Res., 2001 Dec 15;61(24):8851-8; Rossi JF, et al,<br />
Optimizing the use of anti-interleukin-6 monoclonal antibody with dexamethasone and 140 mg/m2 of<br />
melphalan in multiple myeloma: results of a pilot study including biological aspects, Bone Marrow<br />
Transplant, 2005 Nov;36(9):771-9; 그리고 Tonini G, et al, Oxaliplatin may induce cytokine-release<br />
syndrome in colorectal cancer patients, J BiolRegul Homeost Agents, 2002 Apr-Jun;16 (2):105-9; 이들 각<br />
각의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 허혈성<br />
심장 질환, 동맥경화증, 비만, 당뇨병, 천식, 다발성 경화증, 알츠하이머병, 뇌혈관 질환, 발열, 급성기 반응,<br />
알레르기, 빈혈, 염증의 빈혈(만성 질환의 빈혈), 고혈압, 우울증, 만성 질환과 연관된 우울증, 혈전증, 혈소판<br />
- 105 -
증가증, 급성 심장 마비, 대사 증후군, 유산, 비만, 만성 전립선염, 사구체신염, 골반 염증 질환, 재관류 손상,<br />
그리고 이식 거부반응의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료하거나 예방하는데 유<br />
용하다(참조: Tzoulaki I, et al, C-reactive protein, interleukin-6, and soluble adhesion molecules as<br />
predictors of progressive peripheral atherosclerosis in the general population: Edinburgh Artery<br />
Study, Circulation, 2005 Aug 16;l<strong>12</strong>(7):976-83, Epub 2005 Aug 8; Rattazzi M, et al, C-reactive protein<br />
and interleukin-6 in vascular disease: culprits or passive bystanders?, J Hypertens., 2003<br />
Oct;21(10):1787-803; Ito T, et al, HMG-CoA reductase inhibitors reduce interleukin-6 synthesis in<br />
human vascular smooth muscle cells, Cardiovasc Drugs Ther., 2002 Mar;16(2):<strong>12</strong>1-6; Stenvinkel P, et al,<br />
Mortality, malnutrition, and atherosclerosis in ESRD: what is the role of interleukin-6?, Kidney Int<br />
Suppl., 2002 May;(80):103-8; Yudkin JS, et al, Inflammation, obesity, stress and coronary heart<br />
disease: is interleukin-6 the link?, Atherosclerosis, 2000 Feb;148(2):209-14; Huber SA, et al,<br />
Interleukin-6 exacerbates early atherosclerosis in mice, Arterioscler Thromb Vasc Biol., <strong>19</strong>99<br />
Oct;<strong>19</strong>(10):2364-7; Kado S, et al, Circulating levels of interleukin-6, its soluble receptor and<br />
interleukin-6/interleukin-6 receptor complexes in patients with type 2 diabetes mellitus, Acta<br />
Diabetol.,<strong>19</strong>99 Jun;36(1-2):67-72; Sukovich DA, et al, Expression of interleukin-6 in atherosclerotic<br />
lesions of male ApoE-knockout mice: inhibition by 17beta-estradiol, Arterioscler Thromb Vasc<br />
Biol.,<strong>19</strong>98 Sept;8(9):1498-505; Klover PJ, et al, Interleukin-6 depletion selectively improves hepatic<br />
insulin action in obesity, Endocrinology, 2005 Aug;146(8):3417-27, Epub 2005 Apr 21; Lee YH, et al,<br />
The evolving role of inflammation in obesity and the metabolic syndrome, Curr Diab Rep., 2005<br />
Feb;5(1):70-5; Diamant M, et al, The association between abdominal visceral fat and carotid stiffness<br />
is mediated by circulating inflammatory markers in uncomplicated type 2 diabetes, J Clin Endocrinol<br />
Metab., 2005 Mar;90(3):1495-501, Epub 2004 Dec 21; Bray GA, Medical consequences of obesity, J Clin<br />
Endocrinol Metab., 2004 Jun;89(6):2583 9; Klover PJ, et al, Chronic exposure to interleukin-6 causes<br />
hepatic insulin resistance in mice, Diabetes, 2003 Nov;52 (11):2784-9; Yudkin JS, et al, Inflammation,<br />
obesity, stress and coronary heart disease: is interleukin-6 the link?, Atherosclerosis, 2000<br />
Feb;148(2):209-14; Doganci A, et al, Pathological role of IL-6 in the experimental allergic bronchial<br />
asthma in mice, Clin Rev Allergy Immunol., 2005 Jun;28(3):257-70; Doganci A, et al, The IL-6R alpha<br />
chain controls lung CD4+CD25+ Treg development and function during allergic airway inflammation in<br />
vivo, J Clin Invest., 2005 Feb;l15(2):313 25, (Erratum in: J Clin Invest., 2005 May;l15(5):1388, Lehr,<br />
Hans A [added]); Stelmasiak Z, et al, IL 6 and sIL-6R concentration in the cerebrospinal fluid and<br />
serum of MS patients, Med Sci Monit., 2001 Sep-Oct;7(5):914-8; Tilgner J, et al, Continuous<br />
interleukin-6 application in vivo via macroencapsulation of interleukin-6-expressing COS-7 cells<br />
induces massive gliosis, Glia, 2001 Sep;35(3):234-45, Brunello AG, et al, Astrocytic alterations in<br />
interleukin-6 Soluble interleukin-6 receptor alpha double-transgenic mice, Am J Pathol., 2000<br />
Nov;157(5):1485-93; Hampel H, et al, Pattern of interleukin-6 receptor complex immunoreactivity<br />
between cortical regions of rapid autopsy normal and Alzheimer's disease brain, Eur Arch Psychiatry<br />
Clin Neurosci., 2005 Aug;255(4):269-78, Epub 2004 Nov 26; Cacquevel M, et al, Cytokines in<br />
neuroinflammation and Alzheimer's disease, Curr Drug Targets, 2004 Aug;5(6):529-34; Quintanilla RA, et<br />
al, Interleukin 6 induces Alzheimer-type phosphorylation of tau protein by deregulating the cdk5/p35<br />
pathway, Exp Cell Res., 2004 Apr 15; 295 (1):245-57; Gadient RA, et al, Interleukin-6 (IL-6)--a<br />
molecule with both beneficial and destructive potentials, Prog Neurobiol., <strong>19</strong>97 Aug;52(5):379-90; Hull<br />
M, et al, Occurrence of interleukin-6 in cortical plaques of Alzheimer's disease patients may precede<br />
transformation of diffuse into neuritic plaques, Ann N Y Acad Sci., <strong>19</strong>96 Jan 17;777:205-<strong>12</strong>; Rallidis<br />
LS, et al, Inflammatory markers and in-hospital mortality in acute ischaemic stroke, Atherosclerosis,<br />
2005 Dec 30; Emsley HC, et al, Interleukin-6 and acute ischaemic stroke, Acta Neurol Scand., 2005<br />
Oct;1<strong>12</strong>(4):273-4; Smith CJ, et al, Peak plasma interleukin-6 and other peripheral markers of<br />
inflammation in the first week of ischaemic stroke correlate with brain infarct volume, stroke<br />
severity and long-term outcome, BMC Neurol., 2004 Jan 15;4:2; Vila N, et al, Proinflammatory cytokines<br />
and early neurological worsening in ischemic stroke, Stroke, 2000 Oct;31(10):2325-9; 그리고 Tarkowski<br />
E, et al, Early intrathecal production of interleukin-6 predicts the size of brain lesion in stroke,<br />
Stroke, <strong>19</strong>95 Aug;26(8):1393-8; 이들 각각의 내용은 본 발명에 그 전체가 참조로서 편입된다).<br />
- 106 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0689]<br />
[0690]<br />
[0691]<br />
[0692]<br />
[0693]<br />
[0694]<br />
[0695]<br />
[0696]<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 사이토킨<br />
폭풍(cytokine storm)과 연관된 질환과 이상의 증상을 개선하거나 감소시키는데, 또는 이들 질환과 이상을 치료<br />
하거나 예방하는데 유용하다. 사이토킨 폭풍과 연관된 질환과 이상에는 이식편 대(對) 숙주 질환(GVHD), 조류<br />
인플루엔자, 천연두, 대유행 인플루엔자, 성인 호흡 곤란 증후군(ARDS), 중증 급성 호흡기 증후군(SARS), 패혈<br />
증, 그리고 전신성 염증 반응 증후군(SIRS)이 포함되지만 이들에 국한되지 않는다(참조: Cecil, R. L.,<br />
Goldman, L., & Bennett, J. C. (2000). Cecil textbook of medicine. Philadelphia: W.B. Saunders; Ferrara<br />
JL, et al.,Cytokine storm of graft-versus-host disease: a critical effector role for interleukin-1,<br />
Transplant Proc. <strong>19</strong>93 Feb;25(1 Pt 2):<strong>12</strong>16-7; Osterholm MT, Preparing for the Next Pandemic, N Engl J<br />
Med. 2005 May 5;352(18):1839-42; Huang KJ, et al., An interferon-gamma-related cytokine storm in SARS<br />
patients, J Med Virol. 2005 Feb;75(2):185-94; 그리고 Cheung CY, et al., Induction of proinflammatory<br />
cytokines in human macrophages by influenza A (H5N1) viruses: a mechanism for the unusual severity of<br />
human disease? Lancet. 2002 Dec 7;360(9348):1831-7).<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 단편 또는 변이체는 각성 보<br />
조제(wakefulness aid)로서 유용하다.<br />
투여<br />
본 발명의 한 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체, 그리<br />
고 이들 항체 단편 또는 변이체의 조합은 수용자 개체 체중의 대략 0.1 내지 20 ㎎/㎏, 예를 들면, 대략 0.4 ㎎<br />
/㎏, 대략 0.8 ㎎/㎏, 대략 1.6 ㎎/㎏, 또는 대략 4 ㎎/㎏의 농도로 개체에 투여된다. 본 발명의 바람직한 구체<br />
예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체, 그리고 이들 항체 단편<br />
또는 변이체의 조합은 수용자 개체 체중의 대략 0.4 ㎎/㎏의 농도로 개체에 투여된다. 본 발명의 바람직한 구체<br />
예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체, 그리고 이들 항체 단편<br />
또는 변이체의 조합은 26주 이하마다 1회, 예를 들면, 16주 이하마다 1회, 8주 이하마다 1회, 또는 4주 이하마<br />
다 1회의 빈도로, 수용자 개체에 투여된다. 본 발명의 다른 바람직한 구체예에서, 본 명세서에서 기술된 항-IL-<br />
6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체, 그리고 이들의 조합은 대략 1주의 기간 마다 많아야 1회, 예<br />
를 들면, 대략 2주의 기간 마다 많아야 1회, 예를 들면, 대략 4주의 기간 마다 많아야 1회, 예를 들면, 대략 8<br />
주의 기간 마다 많아야 1회, 예를 들면, 대략 <strong>12</strong>주의 기간 마다 많아야 1회, 예를 들면, 대략 16주의 기간 마다<br />
많아야 1회, 예를 들면, 대략 24주의 기간 마다 많아야 1회의 빈도로, 수용자 개체에 투여된다.<br />
효과량은 수용자 개체 속성, 예를 들면, 연령, 성별, 임신 상태, 체질량 지수, 제지방량, 조성물이 제공되는 조<br />
건(들), 조성물의 물질대사 또는 내성에 영향을 주는 수용자 개체의 다른 건강 조건, 수용자 개체에서 IL-6의<br />
수준, 그리고 조성물에 대한 내성(가령, 상기 조성물에 대한 항체를 발생시키는 환자에서 발생)에 좌우되는 것<br />
으로 이해된다. 당업자는 예로써 본 명세서 및 Goodman, L. S., Gilman, A., Brunton, L. L., Lazo, J. S., &<br />
Parker, K. L. (2006). Goodman & Gilman's the pharmacological basis of therapeutics. New York: McGraw-<br />
Hill; Howland, R. D., Mycek, M. J., Harvey, R. A., Champe, P. C., & Mycek, M. J. (2006). Pharmacology.<br />
Lippincott's illustrated reviews. Philadelphia: Lippincott Williams & Wilkins; 그리고 Golan, D. E.<br />
(2008). Principles of pharmacology: the pathophysiologic basis of drug therapy. Philadelphia, Pa.,<br />
[etc.]: Lippincott Williams & Wilkins에서 교시에 의해 보도된 일과적인 실험을 통해 투여의 효과량과 빈도<br />
를 결정할 수 있을 것이다.<br />
본 발명의 또 다른 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체,<br />
그리고 이들 항체 단편 또는 변이체의 조합은 제약학적 제제에 담겨 개체에 투여된다.<br />
"제약학적 조성물"은 포유동물에 투여하기 적합한 화학적 또는 생물학적 조성물을 지칭한다. 이런 조성물은 특<br />
히, 협측, 피부 표면, 경막외, 흡입, 동맥내, 심장내, 뇌실내, 피내, 근육내, 비내, 안구내, 복막내, 척추관내,<br />
척수강내, 정맥내, 경구, 비경구, 관장제 또는 좌약을 통해 직장, 피하, 피하, 설하, 경피, 그리고 경점막이 포<br />
함되지만 이들에 국한되지 않는 다수의 경로 중에서 한 가지 이상을 통한 투여를 위하여 조제된다. 또한, 투여<br />
는 주사, 분말, 액체, 겔, 점안약, 또는 다른 투여 수단에 의해 달성될 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
본 발명의 한 구체예에서, 본 명세서에서 기술된 항-IL-6 항체, 또는 이들의 IL-6 결합 단편 또는 변이체, 그리<br />
고 이들 항체 단편 또는 변이체의 조합은 선택적으로, 하나 이상의 활성제와 공동으로 투여된다. 이런 활성제에<br />
- 107 -
[0697]<br />
[0698]<br />
는 진통제, 해열제, 소염제, 항생제, 항바이러스제, 그리고 항-사이토킨제가 포함된다. 활성제에는 TNF-알파,<br />
IL-2, IL-4, IL-6, IL-10, IL-<strong>12</strong>, IL-13, IL-18, IFN-알파, IFN-감마, BAFF, CXCL13, IP-10, VEGF, EPO, EGF,<br />
HRG, 간세포 성장 인자(HGF), 헵시딘 중에서 한 가지에 반응성인 항체, 그리고 이들의 수용체 중에서 한 가지에<br />
반응성인 항체를 비롯하여, 이들의 효능제, 길항제, 그리고 조절제가 포함된다. 활성제에는 또한, 2-아릴프로피<br />
온산, 아세클로페낙, 아세메타신, 아세틸살리실산(아스피린), 알클로페낙, 알미노프로펜, 아목시프린, 암피론,<br />
아릴알카노산, 아자프로파존, 베노릴레이트, 베녹사프로펜, 브롬페낙, 카르프로펜, 셀레콕시브, 콜린 마그네슘<br />
살리실레이트, 클로페존, COX-2 저해제, 덱시부프로펜, 덱스케토프로펜, 디클로페낙, 디플루니살, 드록시캄, 에<br />
텐자미드, 에토돌락, 에토리콕시브, 파이슬라민, 페남산, 펜부펜, 페노프로펜, 플루페남산, 플루녹사프로펜, 플<br />
루비프로펜, 이부프로펜, 이부프록삼, 인도메타신, 인도프로펜, 케부존, 케토프로펜, 케토롤락, 로르녹시캄, 록<br />
소프로펜, 루미라콕시브, 마그네슘 살리실레이트, 메클로페남산, 메페남산, 멜록시캄, 메타미졸, 메틸 살리실레<br />
이트, 모페부타존, 나부메톤, 나프록센, N-아릴안트라닐산, 옥사메타신, 옥사프로진, 옥시캄, 옥시펜부타존, 파<br />
레콕시브, 페나존, 페닐부타존, 페닐부타존, 피록시캄, 피르프로펜, 프로펜, 프로글루메타신, 피라졸리딘 유도<br />
체, 로페콕시브, 살리실 살리실레이트, 살리실아미드, 살리실레이트, 설핀피라존, 설린닥, 수프로펜, 테녹시캄,<br />
티아프로펜산, 톨페남산, 톨메틴, 그리고 발데콕시브가 포함된다. 항생제에는 아미카신, 아미노글리코시드, 아<br />
목시리린, 암피실린, 안사마이신, 아르스페나민, 아지트로마이신, 아즐로실린, 아즈트레오남, 바시트라신, 카르<br />
바세펨, 카르바페넴, 카르베니실린, 세파클로르, 세파드록실, 세팔렉신, 세팔로틴, 세팔로틴, 세파만돌, 세파졸<br />
린, 세프디니르, 세프디토렌, 세페핌, 세픽심, 세토페라존, 세포탁심, 세폭시틴, 세프포독심, 세프프로질, 세프<br />
타지딤, 세프티부텐, 세프티족심, 세프토비프롤, 세프트리악손, 세푸록심, 세팔로스포린, 클로람페니콜, 실라스<br />
타틴, 시프로플록사신, 클라리트로마이신, 클린다마이신, 클록사실린, 콜리스틴, 코-트리목사졸, 달포프리스틴,<br />
데메클로사이클린, 디클록사실린, 디리트로마이신, 도리페넴, 독시사이클린, 에녹사신, 에르타페넴, 에리트로마<br />
이신, 에탐부톨, 플루클록사실린, 포스포마이신, 푸라졸리돈, 퓨시드산, 가티플록사신, 겔다나마이신, 젠타마이<br />
신, 글리코펩티드, 헤르비마이신, 이미페넴, 이소니아지드, 카나마이신, 레보플록사신, 린코마이신,<br />
리네졸리드, 로메플록사신, 로라카르베프, 마크롤리드, 마페니드, 메로페넴, 메티실린, 메트로니다졸, 메즐로실<br />
린, 미노사이클린, 모노박탐, 목시플록사신, 무피로신, 나프실린, 네오마이신, 네틸마이신, 니트로푸란토인, 노<br />
르플록사신, 오플록사신, 옥사실린, 옥시테트라사이클린, 파로모마이신, 페니실린, 페니실린, 피페라실린, 플라<br />
텐시마이신, 폴리믹신 B, 폴리펩티드, 프론토실, 피라진아미드, 퀴놀론, 퀴누프리스틴, 리팜피신, 리팜핀, 록시<br />
트로마이신, 스펙티노마이신, 스트렙토마이신, 설파세타미드, 설파메티졸, 설파닐아미드, 설파살라진, 설피속사<br />
졸, 설폰아미드, 테이코플라닌, 텔리트로마이신, 테트라사이클린, 테트라사이클린, 티카르실린, 티니다졸, 토브<br />
라마이신, 트리메토프림, 트리메토프림-설파메톡사졸, 트롤레안도마이신, 트로바플록사신, 그리고 반코마이신이<br />
포함된다. 활성제에는 또한, 알도스테론, 베클로메타손, 베타메타손, 코르티코스테로이드, 코르티솔, 코르티손<br />
아세테이트, 디옥시코르티코스테론 아세테이트, 덱사메타손, 플루드로코르티손 아세테이트,<br />
글루코코르티코이드, 하이드로코르티손, 메틸프레드니솔론, 프레드니솔론, 프레드니손, 스테로이드, 그리고 트<br />
리암시놀론이 포함된다. 항바이러스제에는 아바카비르, 아시클로비르, 아시클로비르, 아데포비르, 아만타딘, 암<br />
프레나비르, 항레트로바이러스 고정 용량 복합제, 항레트로바이러스 상승작용 강화제, 아르비돌, 아타자나비르,<br />
아트리플라, 브리부딘, 시도포비르, 콤비비르, 다루나비르, 델라비르딘, 디다노신, 도코사놀, 에독수딘, 에파비<br />
렌즈, 엠트리시타빈, 엔푸비르티드, 엔테카비르, 침입 저해제, 팜시클로비르, 포미비르센, 포삼프레나비르, 포<br />
스카르네트, 포스포네트, 융합 저해제, 간시클로비르, 가르다실, 이바시타빈, 이독수리딘, 이미퀴모드, 이무노<br />
비르, 인디나비르, 이노신, 인테그라아제 저해제, 인터페론, I형 인터페론, II형 인터페론, III형 인터페론, 라<br />
미부딘, 로피나비르, 로비리드, 마라비록, MK-0518, 모록시딘, 넬피나비르, 네비라핀, 넥사비르, 뉴클레오시드<br />
유사체, 오셀타미비르, 펜시클로비르, 페라미비르, 플레코나릴, 포도필로독소, 프로테아제 저해제, 역전사효소<br />
저해제, 리바비린, 리만타딘, 리토나비르, 사퀴나비르, 스타부딘, 테노포비르, 테노포비르, 디소프록실, 티프라<br />
나비르, 트리플루리딘, 트리지비르, 트로만타딘, 트루바다, 발라시클로비르, 발간시클로비르, 비크리비록, 비다<br />
라빈, 비라미딘, 잘시타빈, 자나미비르, 그리고 지도부딘이 포함된다. 이들 활성제의 임의의 적절한 조합 역시<br />
고려된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
"제약학적 부형제" 또는 "제약학적으로 허용되는 부형제"는 담체, 일반적으로, 액체이고, 여기서 활성 치료제가<br />
조제된다. 본 발명의 한 구체예에서, 활성 치료제는 본 명세서에서 기술된 인간화된 항체, 또는 이들의 하나 이<br />
상의 단편 또는 변이체이다. 부형제는 화학적 및/또는 생물학적 안정성, 그리고 방출 특징을 제공하긴 하지만,<br />
일반적으로, 제제에 어떤 약리학적 활성도 제공하지 않는다. 전형적인 제제는 예로써, 본 발명에 참조로서 편입<br />
되는 Remington's Pharmaceutical Sciences, <strong>19</strong>th Ed., Grennaro, A., Ed., <strong>19</strong>95에서 확인될 수 있다.<br />
본 명세서에서 "제약학적으로 허용되는 담체" 또는 "부형제"는 생리학적으로 융화성인 모든 용매, 분산 매체,<br />
- 108 -
[0699]<br />
[0700]<br />
[0701]<br />
[0702]<br />
[0703]<br />
[0704]<br />
[0705]<br />
[0706]<br />
[0707]<br />
코팅, 항균제와 항진균제, 등장성화제 및 흡수 지연제를 포함한다. 한 구체예에서, 담체는 비경구 투여에 적합<br />
하다. 대안으로, 담체는 정맥내, 복막내, 근육내, 또는 설하 투여에 적합할 수 있다. 제약학적으로 허용되는 담<br />
체에는 무균 수용액 또는 분산액, 그리고 무균 주사가능 용액 또는 분산액의 즉석 제조를 위한 무균 분말이 포<br />
함된다. 제약학적 활성 물질에 대한 이런 매체와 작용제의 이용은 당분야에 널리 공지되어 있다. 임의의 전통적<br />
인 매체 또는 작용제가 활성 화합물에 부적합한 경우를 제외하고, 본 발명의 제약학적 조성물에서 이용이 고려<br />
된다. 보조 활성 화합물 역시 조성물 내로 통합될 수 있다.<br />
암 징후를 위하여 Ab1을 비롯한 본 발명의 항체를 정맥내 투여하는데 이용될 수 있는 본 발명의 한 구체예에서,<br />
투여 제제는 대략 10.5 ㎎/㎖의 항체, 25 mM 히스티딘 염기, pH 6까지 인산 q.s., 그리고 250 mM 소르비톨을 포<br />
함하거나, 또는 대안으로 이들로 구성된다.<br />
암 징후를 위하여 Ab1을 비롯한 본 발명의 항체를 정맥내 투여하는데 이용될 수 있는 본 발명의 다른 구체예에<br />
서, 투여 제제는 대략 10.5 ㎎/㎖의 항체, <strong>12</strong>.5 mM 히스티딘 염기, <strong>12</strong>.5 mM 히스티딘 HCl(또는 25 mM 히스티딘<br />
염기 및 pH 6까지 염화수소산 q.s.), 250 mM 소르비톨, 그리고 0.015% (w/w) 폴리소르베이트 80을 포함하거나,<br />
또는 대안으로 이들로 구성된다.<br />
류머티스성 관절염 징후를 위하여 Ab1을 비롯한 본 발명의 항체를 피하 투여하는데 이용될 수 있는 본 발명의<br />
한 구체예에서, 투여 제제는 대략 50 또는 100 ㎎/㎖의 항체, 대략 5 mM 히스티딘 염기, 최종 pH 6을 만들기 위<br />
한 대략 5 mM 히스티딘 HCl, 250 mM 소르비톨, 그리고 0.015%(w/w) 폴리소르베이트 80을 포함하거나, 또는 대안<br />
으로 이들로 구성된다.<br />
류머티스성 관절염 징후를 위하여 Ab1을 비롯한 본 발명의 항체를 피하 투여하는데 이용될 수 있는 본 발명의<br />
다른 구체예에서, 투여 제제는 대략 20 또는 100 ㎎/㎖의 항체, 대략 5 mM 히스티딘 염기, 최종 pH 6을 만들기<br />
위한 대략 5 mM 히스티딘 HCl, 250 내지 280 mM 소르비톨(또는 수크로오스와 공동으로 소르비톨), 그리고<br />
0.015%(w/w) 폴리소르베이트 80을 포함하거나, 또는 대안으로 이들로 구성되고, 상기 제제는 수송 바이알<br />
(shipping vial) 내에서 질소 헤드스페이스를 갖는다.<br />
제약학적 조성물은 전형적으로, 제조와 보관의 조건 하에 무균이고 안정적이어야 한다. 본 발명에서는 제약학적<br />
조성물이 동결 건조된 형태로 존재하는 것을 고려한다. 조성물은 용액, 마이크로에멀젼, 리포좀, 또는 고농도<br />
농도에 적합한 다른 정연한 구조로서 조제될 수 있다. 담체는 예로써, 물, 에탄올, 폴리올(가령, 글리세롤, 프<br />
로필렌 글리콜, 그리고 액상 폴리에틸렌 글리콜), 그리고 이들의 적절한 혼합물을 포함하는 용매 또는 분산 매<br />
체일 수 있다. 더 나아가, 본 발명에서는 제약학적 조성물 내에서 안정화제의 포함을 고려한다.<br />
많은 사례에서, 조성물 내에 등장성화제, 예를 들면, 당류, 폴리알코올, 예를 들면, 만니톨, 소르비톨, 또는 염<br />
화나트륨을 포함하는 것이 바람직할 수 있다. 주사가능 조성물의 연장된 흡수는 흡수를 지연시키는 작용제, 예<br />
를 들면, 모노스테아레이트 염과 젤라틴을 조성물 내에 포함시킴으로써 달성될 수 있다. 게다가, 알칼리성 폴리<br />
펩티드는 예로써, 느린 방출 중합체를 포함하는 조성물 내에서 시한 방출 제제로 조제될 수 있다. 이들 활성 화<br />
합물, 예를 들면, 이식물과 마이크로캡슐화된 전달 시스템을 비롯한 조절 방출 제제는 신속 방출로부터 화합물<br />
을 보호하는 담체로 만들어질 수 있다. 생물분해성, 생물적합성 중합체, 예를 들면, 에틸렌 비닐 아세테이트,<br />
폴리무수물, 폴리글리콜산, 콜라겐, 폴리오르토에스테르, 폴리락트산, 그리고 폴리락트산, 폴리글리콜산 공중합<br />
체(PLG)가 이용될 수 있다. 이런 제제의 조제를 위한 많은 방법이 당업자에게 공지되어 있다.<br />
앞서 열거된 각 구체예에서, 화합물은 다양한 제형(dosage form)으로 투여될 수 있다. 당업자에게 공지된 임의<br />
의 생물학적으로 허용되는 제형, 그리고 이들의 조합이 고려된다. 이런 제형의 실례에는 제한 없이, 재구성가능<br />
분말, 엘릭시르, 액체, 용액, 현탁액, 에멀젼, 분말, 과립, 입자, 마이크로입자, 분산가능 과립, 교갑, 흡입제,<br />
에어로졸 흡입제, 패치, 입자 흡입제, 이식물, 저장소 이식물, 주사가능물질(피하, 근육내, 정맥내, 그리고 피<br />
내 포함), 주입물, 그리고 이들의 조합이 포함된다.<br />
본 발명의 다양한 예시된 구체예에 관한 상기 설명은 철저하거나, 또는 본 발명을 개시된 정확한 형태에 한정하<br />
는 것으로 의도되지 않는다. 본 발명에 대한 특정 구체예, 그리고 실례는 예시의 목적으로 본 명세서에서 기술<br />
되지만, 당업자가 인지하는 바와 같이 본 발명의 범위 내에서 다양한 등가의 변형이 가능하다. 본 발명의 명세<br />
서에 제공된 교시는 앞서 기술된 실례 이외에 다른 목적에도 적용될 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
이들 변화는 상기 상세한 설명을 감안하여, 본 발명에서 수행될 수 있다. 일반적으로, 아래의 특허청구범위에서<br />
이용되는 용어는 본 발명을 명세서와 특허청구범위에서 개시된 특정 구체예에 한정시키는 것으로 간주되지 않는<br />
다. 따라서 본 발명은 이러한 개시에 의해 한정되지 않고, 그 대신에 본 발명의 범위는 아래의 특허청구범위에<br />
- 109 -
[0708]<br />
[0709]<br />
[0710]<br />
[0711]<br />
[07<strong>12</strong>]<br />
[0713]<br />
[0714]<br />
[0715]<br />
[0716]<br />
[0717]<br />
의해 전적으로 결정된다.<br />
본 발명은 특히, 상기 상세한 설명과 실례에서 기술된 것들 이외의 방식으로 실행될 수 있다. 본 발명의 다수의<br />
개변은 상기 교시에 비추어 가능하고, 이런 이유로 첨부된 특허청구범위의 범위 내에 있다.<br />
항원-특이적 B 세포의 클론 집단을 획득하기 위한 방법에 관련된 교시는 2006년 5월 <strong>19</strong>일 제출된 U.S. 가출원<br />
no. 60/801,4<strong>12</strong>에서 개시되었고, 이의 내용은 본 발명에 그 전체가 참조로서 편입된다.<br />
토끼-유래된 단일클론 항체의 인간화 및 항원 결합 친화성을 유지하기 위한 바람직한 서열 변형에 관련된 교시<br />
는 2008년 5월 21일 제출된 국제 출원 No. <strong>12</strong>/<strong>12</strong>4,723(발명의 명칭: "신규한 토끼 항체 인간화 방법 및 인간화<br />
된 토끼 항체"; Attorney Docket No. 67858.704001에 대응함)에서 개시되었고, 이의 내용은 본 발명에 그 전체<br />
가 참조로서 편입된다.<br />
교배 적격성 효모 및 부합하는 방법을 이용하여 항체 또는 이들의 단편을 생산하는 것에 관련된 교시는 2006년<br />
5월 8일 제출된 U.S. 특허 출원 no. 11/429,053(U.S. 특허 출원 공개 No. US2006/0270045)에서 개시되었고, 이<br />
의 내용은 본 발명에 그 전체가 참조로서 편입된다.<br />
항-IL-6 항체, 그리고 교배 적격성 효모 및 부합하는 방법을 이용하여 항체 또는 이들의 단편을 생산하는 방법<br />
에 관련된 교시는 2007년 5월 21일 제출된 U.S. 가출원 no. 60/924,550에서 개시되었고, 이의 내용은 본 발명에<br />
그 전체가 참조로서 편입된다.<br />
항-IL-6 항체, 그리고 일정한 질환 및/또는 질병을 해결하기 위하여 이들 항체 또는 이들의 단편을 이용하는 방<br />
법에 관련된 교시는 2008년 11월 25일자 제출된 U.S. 가출원 no. 61/117,839, 61/117,861, 그리고 61/117,811<br />
에서 개시되었고, 이들 각각의 내용은 본 발명에 그 전체가 참조로서 편입된다.<br />
일정한 항-IL-6 항체 폴리뉴클레오티드와 폴리펩티드는 본 특허 출원서에 동반된 서열 목록에서 개시되고, 그리<br />
고 상기 서열 목록의 내용은 본 발명에서 그 전체가 참조로서 편입된다.<br />
본 명세서에서 인용된 각 문헌(특허, 특허 출원, 학술지 기사, 초록, 매뉴얼, 서적, 또는 다른 간행물 포함)의<br />
전체 내용은 본 발명에서 그 전체가 참조로서 편입된다.<br />
아래의 실시예는 본 발명을 생성시키고 이용하는 방법에 관한 완벽한 개시와 설명을 당업자에게 제공하기 위하<br />
여 기술되고, 그리고 본 발명으로서 간주되는 것의 범위를 한정하는 것으로 의도되지 않는다. 이용된<br />
숫자(가령, 양, 온도, 농도 등)에 대하여 정확성을 담보하기 위한 노력이 필요하지만, 다소의 실험 오차와 편차<br />
는 허용되어야 한다. 달리 지시되지 않으면, 분율(part)은 중량 분율(part by weight)이고, 분자량은 평균 분자<br />
량이고, 온도는 섭씨이고, 그리고 압력은 대기압이거나 대기압에 가깝다.<br />
도면의 간단한 설명<br />
도면의 간단한 설명<br />
도 1에서는 다수의 독특한 에피토프가 항체 선별 프로토콜에 의해 제조된 항-IL-6 항체의 집합에 의해 인식된다<br />
는 것을 보여준다. 에피토프 변이성은 항체-IL-6 결합 경쟁 연구(ForteBio Octet)에 의해 확증되었다.<br />
도 2에서는 토끼 항체 가변 경쇄와 가변 중쇄 및 상동성 인간 서열 및 인간화된 서열 사이에 가변 경쇄와 가변<br />
중쇄의 정렬을 도시한다. 골격 영역은 FR1-FR4로서 확인된다. 상보성 결정 영역은 CDR1-CDR3으로서 확인된다.<br />
아미노산 잔기는 도시된 바와 같이 번호가 매겨진다. 최초 토끼 서열은 가변 경쇄와 가변 중쇄에 대하여 각각<br />
RbtVL과 RbtVH로 불린다. 골격 1에서부터 골격 3의 말단까지 걸쳐있는 가장 유사한 인간 생식세포 항체 서열 중<br />
에서 3가지가 토끼 서열 아래에 정렬된다. 토끼 서열에 가장 유사한 것으로 간주되는 인간 서열이 가장 먼저 도<br />
시된다. 이러한 실례에서, 가장 유사한 서열은 경쇄의 경우에 L<strong>12</strong>A, 그리고 중쇄의 경우에 3-64-04이다. 인간<br />
CDR3 서열은 도시되지 않는다. 가장 가까운 인간 골격 4 서열이 토끼 골격 4 서열 아래에 정렬된다. 수직선은<br />
토끼 잔기가 동일한 위치에서 하나 이상의 인간 잔기와 일치하는 잔기를 지시한다. 굵게 표시된 잔기는 이 위치<br />
에서 인간 잔기가 동일한 위치에서 토끼 잔기와 일치한다는 것을 지시한다. 최종 인간화된 서열은 가변 경쇄와<br />
가변 중쇄에 대하여 각각 VLh와 VHh로 불린다. 밑줄로 표시된 잔기는 이 위치에서 잔기가 토끼 잔기와 동일하지<br />
만 3개의 정렬된 인간 서열 내에 상기 위치에서 인간 잔기와 상이하다는 것을 지시한다.<br />
도 3에서는 생산된 IgG 및 예시적인 IL-6 프로토콜에 대한 항원 특이성 사이에 높은 상관관계를 증명한다. 11개<br />
의 웰(well) 중에서 9개가 항원 인식과의 특이적 IgG 상관관계를 보였다.<br />
- 110 -<br />
공개특허 10-2011-01<strong>12</strong>308
도 4에서는 인간 IL-6의 100 ㎍/㎏ s.c. 투약후 1시간 시점에, 상이한 용량에서 정맥내 투여된 항체 Ab1에 대한<br />
알파-2-마크로글로불린(A2M) 용량 반응 곡선을 도시한다.<br />
도 5에서는 항체 Ab1 진행 군 대(對) 대조 군에 대한 생존 데이터를 제공한다.<br />
도 6에서는 항체 Ab1 역행 군 대(對) 대조 군에 대한 추가의 생존 데이터를 제공한다.<br />
도 7에서는 3일마다 10 ㎎/㎏ i.v.에서 다중클론 인간 IgG(270-320 ㎎ 종양 크기) 대(對) 3일마다 10 ㎎/㎏<br />
i.v.에서 항체 Ab1(270-320 ㎎ 종양 크기)에 대한 생존 데이터를 제공한다.<br />
도 8에서는 3일마다 10 ㎎/㎏ i.v.에서 다중클론 인간 IgG(400-527 ㎎ 종양 크기) 대(對) 3일마다 10 ㎎/㎏<br />
i.v.에서 항체 Ab1(400-527 ㎎ 종양 크기)에 대한 생존 데이터를 제공한다.<br />
도 9에서는 필리핀 원숭이에서 항체 Ab1의 약동학적 프로필을 제공한다. 항체 Ab1의 혈장 수준은 항원 포획<br />
ELISA를 통해 정량되었다. 상기 단백질은 다른 전장 인간화된 항체와 일치하는 <strong>12</strong>일 내지 17일의 반감기를 보인<br />
다.<br />
도 10(A-D)에서는 각각, 항체 Ab4, Ab3, Ab8과 Ab2에 대한 결합 데이터를 제공한다. 도 10E에서는 항체 Ab1,<br />
Ab6과 Ab7에 대한 결합 데이터를 제공한다.<br />
도 11에서는 표 형태로, 도 10(A-E)의 결합 데이터를 요약한다.<br />
도 <strong>12</strong>에서는 실시예 14의 펩티드 맵핑 실험에 이용된 15개 아미노산 펩티드의 서열을 제공한다.<br />
도 13에서는 실시예 14에서 준비된 블롯(blot)의 결과를 제공한다.<br />
도 14에서는 실시예 14에서 준비된 블롯의 결과를 제공한다.<br />
도 15A에서는 다양한 종의 IL-6에 대한 Ab1의 친화성과 결합 동역학을 도시한다.<br />
도 15B에서는 T1165 세포 증식 분석에서 Ab1에 의한 IL-6의 저해를 증명한다.<br />
도 16에서는 여러 용량 군에서 건강한 수컷 개체에 Ab1의 단일 투여에 기인하는 Ab1의 평균 혈장 농도를 도시한<br />
다.<br />
도 17에서는 도 16에 도시된 용량 군에 대한 혈장 Ab1 농도 시간 곡선 아래 평균 면적(AUC)을 도시한다.<br />
도 18에서는 도 16에서 도시된 용량 군에 대한 평균 피크 혈장 Ab1 농도(Cmax)를 도시한다.<br />
도 <strong>19</strong>에서는 도 16에 도시된 용량 군의 Ab1 약동학적 치수를 요약한다.<br />
도 20에서는 진행된 암 환자에 Ab1의 단일 투여에 기인하는 Ab1의 평균 혈장 농도를 도시한다.<br />
도 21에서는 다른 항-IL-6 항체와 비교하여 Ab1의 선례가 없는 소실 반감기를 도시한다.<br />
도 22에서는 진행된 암 환자에 Ab1의 투여 이후에, 증가된 헤모글로빈 농도를 도시한다.<br />
도 23에서는 진행된 암 환자에 Ab1의 투여 이후에, 평균 혈장 지질 농도를 도시한다.<br />
도 24에서는 진행된 암 환자에 Ab1의 투여 이후에, 평균 호중구 숫자를 도시한다.<br />
도 25에서는 건강한 개체에서 혈청 CRP 수준의 억제를 증명한다.<br />
도 26(A-B)에서는 진행된 암 환자에서 혈청 CRP 수준의 억제를 증명한다.<br />
도 27에서는 생쥐 암 악액질 모형에서 Ab1에 의한 체중 감소의 예방을 증명한다.<br />
도 28에서는 암 악액질 모형에서 대표적인 Ab1-치료된 생쥐와 대조 생쥐의 신체 외관을 도시한다.<br />
도 29에서는 Ab1이 진행된 암 환자에서 체중 증가를 촉진한다는 것을 증명한다.<br />
도 30에서는 Ab1이 진행된 암 환자에서 피로를 감소시킨다는 것을 증명한다.<br />
도 31에서는 Ab1이 진행된 암 환자에서 손 악력을 증진한다는 것을 증명한다.<br />
도 32에서는 Ab1이 생쥐에서 급성기 단백질(혈청 아밀로이드 A)을 억제한다는 것을 증명한다.<br />
도 33에서는 Ab1이 진행된 암 환자에서 혈장 알부민 농도를 증가시킨다는 것을 증명한다.<br />
- 111 -<br />
공개특허 10-2011-01<strong>12</strong>308
도 34와 35에서는 토끼 항체 경쇄와 가변 중쇄 및 상동성 인간 서열 및 최종 인간화된 서열 사이에 정렬을 도시<br />
한다. 골격 영역은 FR1-FR4로서 확인된다. 상보성 결정 영역은 CDR1-CDR3으로서 확인된다.<br />
도 36과 37에서는 각각, 상이한 형태의 Ab1의 경쇄와 가변 중쇄 사이에 정렬을 도시한다. 골격 영역은 FR1-<br />
FR4로서 확인된다. 상보성 결정 영역은 CDR1-CDR3으로서 확인된다. CDR 영역 내에서 서열 차이는 강조된다.<br />
도 38에서는 Ab1 단일클론 항체의 각 투약 농도(위약, 80 ㎎, 160 ㎎, 그리고 320 ㎎)에 대한 평균 CRP 값을 도<br />
시한다.<br />
도 39에서는 도 38에 상응하는 각 투약 농도 군으로부터 CRP의 중앙 값(median value)에서 변화를 도시한다.<br />
도 40에서는 80, 160 또는 320 ㎎으로 <strong>12</strong>주 동안 투약후, 다양한 암을 앓는 환자에서 혈청 CRP 수준의 감소를<br />
도시한다.<br />
도 41에서는 80, 160과 320 ㎎으로 <strong>12</strong>주 동안 투약후, 류머티스성 관절염을 앓는 환자 집단에서 혈청 CRP 수준<br />
의 감소를 도시한다.<br />
도 42에서는 80, 160과 320 ㎎으로 <strong>12</strong>주 동안 투약후, Ab1이 평균 헤모글로빈을 증가시킨다는 것을 증명한다.<br />
도 43에서는 도 42에 제공된 데이터에 대한 기준선 헤모글로빈으로부터 평균 변화를 도시한다.<br />
도 44에서는 11 g/ℓ 미만의 기준선 헤모글로빈을 갖는 환자에서 160과 320 ㎎으로 <strong>12</strong>주 동안 투약후, Ab1이 평<br />
균 헤모글로빈을 증가시킨다는 것을 증명한다.<br />
도 45에서는 80, 160과 320 ㎎으로 16주 동안 투약후, Ab1이 평균 헤모글로빈을 증가시킨다는 것을 증명한다.<br />
도 46에서는 80, 160과 320 ㎎으로 <strong>12</strong>주 동안 투약후, Ab1이 평균 알부민 농도를 증가시킨다는 것을 증명한다.<br />
도 47에서는 도 46에 상응하는 각 투약 농도 군으로부터 평균 알부민 농도에 대한 기준선으로부터 변화를 도시<br />
한다.<br />
도 48에서는 35 g/ℓ 미만의 기준선 알부민을 갖는 환자에서 160과 320 ㎎으로 <strong>12</strong>주 동안 투약후, Ab1이 평균<br />
알부민 농도에서 지속적인 증가를 제공한다는 것을 증명한다.<br />
도 49에서는 <strong>12</strong>주 동안 Ab1 단일클론 항체의 각 투약 농도 군(위약, 80 ㎎, 160 ㎎, 그리고 320 ㎎)으로부터 평<br />
균화된 체중 변화 데이터를 제공한다.<br />
도 50에서는 도 49에 상응하는 각 투약 농도 군으로부터 체중의 평균화된 변화 비율을 제공한다.<br />
도 51에서는 도 49에 상응하는 투약 농도 군에 대한 평균화된 제지방량(lean body mass) 데이터에서 변화를 제<br />
공한다.<br />
도 52에서는 80, 160과 320 ㎎으로 8주 동안 투약후, 환자 집단에서 일부 투약 농도 군에 대한 평균 Facit-F FS<br />
하위척도 점수(subscale score)의 증가를 증명한다.<br />
도 53에서는 도 52에 상응하는 기준선 Facit-F FS 하위척도 점수로부터 변화를 도시한다.<br />
도 54에서는 Ab1이 80, 160과 320 ㎎에서 16주간 투약후, 위약에 비하여 D-이합체 수준을 하락시킨다는 것을 증<br />
명한다.<br />
도 55에서는 도 54에 상응하는 각 투약 농도 군으로부터 D-이합체 농도에서 기준선으로부터 변화 비율을 도시한<br />
다.<br />
도 56에서는 류머티스성 관절염 환자의 치료가 ACR 계량에 기초하여 위약에 비하여 현저한 개선을 산출한다는<br />
것을 증명한다.<br />
도 57에서는 80, 160, 그리고 320 ㎎에서 16주간 투약후, 위약에 비하여 ACR 20을 달성하는 환자를 보여준다.<br />
도 58에서는 80, 160, 그리고 320 ㎎에서 16주간 투약후, 위약에 비하여 ACR 50을 달성하는 환자를 보여준다.<br />
도 59에서는 80, 160, 그리고 320 ㎎에서 16주간 투약후, 위약에 비하여 ACR 70을 달성하는 환자를 보여준다.<br />
도 60에서는 위약, 80, 160, 그리고 320 ㎎ 투약 농도 군에 대한 ACR 계량의 구성요소의 기준선으로부터 변화를<br />
도시한다.<br />
- 1<strong>12</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
[0718]<br />
[07<strong>19</strong>]<br />
[0720]<br />
[0721]<br />
[0722]<br />
[0723]<br />
[0724]<br />
[0725]<br />
[0726]<br />
[0727]<br />
도 61에서는 위약, 80, 160, 그리고 320 ㎎ 투약 농도 군에 대한 HAQ-DI 스코어에서 변화를 도시한다.<br />
도 62에서는 위약, 80, 160, 그리고 320 ㎎ 투약 농도 군에 대한 DAS28 스코어에서 변화를 도시한다.<br />
도 63에서는 위약, 80, 160, 그리고 320 ㎎ 투약 농도 군에서 EULAR 우수한 또는 온건한 반응을 달성하는 환자<br />
의 비율에서 변화를 도시한다.<br />
발명을 실시하기 위한 구체적인 내용<br />
실시예<br />
아래의 실시예에서, 용어 "Ab1"은 달리 명시되는 경우를 제외하고, 서열 번호: 702의 경쇄 서열 및 서열 번호:<br />
704의 중쇄 서열을 포함하는 항체를 지칭한다.<br />
실시예 1 농축된 항원-특이적 B 세포 항체 배양액의 생산<br />
항체의 패널은 목적되는 표적 항원에 대한 본래의 면역 반응을 유도하기 위하여 전통적인 항체 숙주 동물을 면<br />
역화시킴으로써 도출된다. 전형적으로, 면역화에 이용되는 숙주는 토끼, 또는 유사한 성숙 과정을 이용하여 항<br />
체를 생산하고 필적하는 다양성, 예를 들면, 에피토프 다양성의 항체를 생산하는 항원-특이적 B 세포의 집단을<br />
제공하는 다른 숙주이다. 최초 항원 면역화는 완전 Freund 어쥬번트(CFA)를 이용하여 수행될 수 있고, 그리고<br />
차후 부스트(boost)는 불완전 어쥬번트로 달성될 수 있다. 면역화후 대략 50-60일, 바람직하게는 55일 시점에,<br />
항체 역가가 조사되고, 그리고 적절한 역가가 확립되면 항체 선별(ABS) 과정이 시작된다. ABS 시작을 위한 2가<br />
지 핵심 기준은 강력한 항원 인식 및 다중클론 혈청 내에서 기능-변화 활성이다.<br />
양성 항체 역가가 확립되는 시점에서, 동물은 희생되고 B 세포 공급원이 분리된다. 이들 공급원에는 비장, 림프<br />
절, 골수, 그리고 말초혈 단핵 세포(PBMC)가 포함된다. 단일 세포 현탁액이 산출되고, 그리고 이들 세포 현탁액<br />
은 낮은 온도 장기 보관에 적합하도록 세척된다. 이들 세포는 이후, 전형적으로 동결된다.<br />
항체 확인 과정을 시작하기 위하여, 적은 분획물의 동결된 세포 현탁액은 해동되고, 세척되고, 그리고 조직 배<br />
양액 배지에 배치된다. 이들 현탁액은 이후, 동물 면역 반응을 생성시키는데 이용되는 항원의 비오틴화된 형태<br />
와 혼합되고, 그리고 항원-특이적 세포는 Miltenyi 자석 비드 세포 선별 방법을 이용하여 회수된다. 스트렙타비<br />
딘 비드를 이용하여 특이적 농축이 수행된다. 농축된 집단은 회수되고 특이적 B 세포 분리의 다음 단계에서 처<br />
리된다.<br />
실시예 2 클론성, 항원-특이적 B 세포-포함 배양액의 생산<br />
실시예 1에 따라 생산된 농축된 B 세포는 이후, 96웰 마이크로역가 평판에서 웰당 다양한 세포 밀도에서 도말된<br />
다. 일반적으로, 이는 군당 10개 평판으로 웰당 50, 100, 250, 또는 500개 세포이다. 배지는 50K 동결되고 조사<br />
된 EL4B 지지 세포(feeder cell)와 함께, 4% 활성화된 토끼 T 세포 조건 배지로 보충된다. 이들 배양액은 5-7일<br />
동안 방해 없이 방치되고, 이 시점에서 상층액-포함 분비된 항체가 수집되고 독립된 분석 환경에서 표적 특성에<br />
대하여 평가된다. 나머지 상층액은 본래대로 방치되고, 그리고 평판은 -70℃에서 동결된다. 이들 조건 하에, 배<br />
양 과정은 전형적으로, 항원-특이적 B 세포의 클론 집단을 포함하는 혼합된 세포 집단을 포함하는 웰을 발생시<br />
킨다, 다시 말하면, 단일 웰은 원하는 항원에 특이적인 단일 단일클론 항체만을 포함할 것이다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
실시예 3 원하는 특이성 및/또는 기능적 특성의 단일클론 항체에 대한 항체 상층액의 스크리닝<br />
실시예 2에 따라 생산된 클론 항원-특이적 B 세포 집단을 포함하는 웰로부터 유래된 항체-포함 상층액은<br />
초기에, ELISA 방법을 이용하여 항원 인식에 대하여 스크리닝된다. 이는 선택성 항원 고정화(가령, 스트렙타비<br />
딘 코팅된 평판에 의한 비오틴화된 항원 포획), 비-특이적 항원 평판 코팅, 또는 대안으로, 항원 구축 전략(가<br />
령, 선택성 항원 포획, 그 이후에 이형(heteromeric) 단백질-항원 복합체를 생성시키기 위한 결합 파트너 부<br />
가)을 포함한다. 항원-양성 웰 상층액은 이후, 리간드에 엄격하게 의존하는 기능-변화 분석에서 선택적으로 조<br />
사된다. 이와 같은 한 가지 실례는 재조합 수용체 단백질로 항원 리간드의 자연적인 상호작용을 재현하는 시험<br />
관내 단백질-단백질 상호작용 분석이다. 대안으로, 리간드 의존성이고 용이하게 모니터되는 세포-기초된 반응<br />
(가령, 증식반응)이 이용된다. 현저한 항원 인식과 효능을 보이는 상층액은 양성 웰인 것으로 간주된다. 최초<br />
- 113 -
[0728]<br />
[0729]<br />
[0730]<br />
[0731]<br />
[0732]<br />
[0733]<br />
[0734]<br />
[0735]<br />
[0736]<br />
양성 웰로부터 유래된 세포는 이후, 항체 회수 상(phase)으로 이전된다.<br />
실시예 4 원하는 항원 특이성의 단일, 항체-생산 B 세포의 회수<br />
세포는 단일 항체 서열을 분비하는 항원-특이적 B 세포의 클론 집단(실시예 2 또는 3에 따라 생산됨)을 포함하<br />
는 웰로부터 분리된다. 분리된 세포는 이후, 단일, 항체-분비 세포를 분리하기 위하여 분석된다. Dynal 스트렙<br />
타비딘 비드는 세포 생존능과 적합한 항원-포함 마이크로비드를 준비하기 위하여 완충 매체 하에, 비오틴화된<br />
표적 항원으로 코팅된다. 그 다음, 항원-적하된 비드, 양성 웰로부터 항체-생산 세포, 그리고 플루오레세인 이<br />
소티오시아네이트(FITC)-표지된 항-숙주 H&L IgG 항체(언급된 바와 같이, 숙주는 임의의 포유동물 숙주, 예를<br />
들면, 토끼, 생쥐, 쥐 등일 수 있다)는 37℃에서 함께 배양된다. 생성된 혼합물은 이후, 유리 슬라이드 상에서<br />
분취량(aliquot)으로 재-피펫팅되고, 따라서 각 분취량은 평균적으로, 단일, 항체-생산 B-세포를 보유한다. 항<br />
원-특이적, 항체-분비 세포는 이후, 형광 현미경을 통해 검출된다. 분비된 항체는 결합된 항원으로 인하여 인접<br />
한 비드 상에 국지적으로 집중되고, 그리고 강한 형광 신호에 기초하여 국지화 정보를 제공한다. 항체-분비 세<br />
포는 이들 분비 세포에 인접하게 형성된 항체-항원 복합체의 FITC 검출을 통해 확인된다. 이러한 복합체의 중심<br />
에서 관찰되는 단일 세포는 이후, 미세조작기(micromanipulator)를 이용하여 회수된다. 세포는 항체 서열 회수<br />
가 시작될 때까지 -80℃에서 보관 동안 에펜도르프 PCR 튜브에서 순간-동결된다.<br />
실시예 5 항원-특이적 B 세포로부터 항체 서열의 분리<br />
항체 서열은 실시예 4에 따라 생산된 단일 분리된 B-세포로부터, 또는 실시예 2에 따라 획득된 클론 B 세포 집<br />
단으로부터 분리된 항원 특이적 B 세포로부터 통합 RT-PCR 기초된 방법을 이용하여 회수된다. 표적 면역글로불<br />
린 유전자(중쇄와 경쇄)의 보존 영역과 불변 영역, 예를 들면, 토끼 면역글로불린 서열에 어닐링하는 프라이머<br />
가 설계되고, 그리고 항체 서열을 획득하기 위하여 2-단계 이중(nested) PCR 회수 단계가 이용된다. 각 웰로부<br />
터 앰플리콘은 회수와 크기 일체성에 대하여 분석된다. 결과의 단편은 이후, 서열 클론형성능(sequence<br />
clonality)을 핑거프린팅(fingerprinting)하기 위하여 AluI로 절단된다. 동일한 서열은 그들의 전기영동 분석에<br />
서 공통의 단편화 패턴을 보인다. 유의하게는, 세포 클론형성능을 입증하는 이러한 공통의 단편화 패턴은 일반<br />
적으로, 초기에 1000개 세포/웰까지 도말된 웰에서도 관찰된다. 최초 중쇄와 경쇄 앰플리콘 단편은 이후, 클로<br />
닝을 위한 DNA의 개별 조각을 준비하기 위하여 HindIII과 XhoI, 또는 HindIII과 BsiWI로 제한 효소 절단된다.<br />
결과의 절단물은 이후, 플라스미드 증식과 생산을 위하여 발현 벡터 내로 결찰되고 세균 내로 형질전환된다. 콜<br />
로니는 서열 특성화를 위하여 선별된다.<br />
실시예 6 원하는 항원 특이성 및/또는 기능적 특성의 단일클론 항체의 재조합 생산<br />
단일 단일클론 항체를 포함하는 각 웰에 대한 정확한 전장 항체 서열이 확립되고, Qiagen 고체-상 방법을 이용<br />
하여 miniprep DNA가 준비된다. 상기 DNA는 이후, 재조합 전장 항체를 생산하기 위하여 포유동물 세포를 형질감<br />
염시키는데 이용된다. 가공되지 않은 항체 산물은 항원 인식에 대하여 조사되고, 그리고 재조합 항체 단백질에<br />
서 최초 특징을 확증하기 위한 기능적 특성이 확인된다. 적절한 경우에, 대규모 일시적 포유동물 형질감염이 완<br />
결되고, 그리고 항체가 단백질 A 친화성 색층분석을 통해 정제된다. Kd는 표준 방법(가령, Biacore) 및 효능<br />
분석에서 IC50을 이용하여 평가된다.<br />
실시예 7 인간 IL-6에 결합하는 항체의 준비<br />
본 명세서에서 기술된 항체 선별 프로토콜을 이용함으로써, 항체의 광범위한 패널을 산출할 수 있다. 상기 항체<br />
는 IL-6에 대하여 높은 친화성(한 자리 내지 두 자리 pM Kd)을 갖고 복수 세포-기초된 스크리닝 시스템(T1165와<br />
HepG2)에서 IL-6의 강력한 길항을 나타낸다. 게다가, 이러한 항체 수집물은 IL-6-주동된 과정에 대하여 상이한<br />
길항 양식을 보인다.<br />
면역화 전략<br />
- 114 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0737]<br />
[0738]<br />
[0739]<br />
[0740]<br />
[0741]<br />
[0742]<br />
[0743]<br />
토끼는 huIL-6(R&R)으로 면역화되었다. 면역화는 완전 Freund 어쥬번트(CFA)(Sigma)에서 100 ㎍의 일차 피하<br />
(sc) 주사, 그 이후에 불완전 Freund 어쥬번트(IFA)(Sigma)에서 각각 50 ㎍의 2주 간격 2회 부스트(boost)로<br />
구성되었다. 동물은 55일 자에 채혈되고, 그리고 혈청 역가가 T1165 세포주를 이용하여 ELISA(항원 인식) 및 비<br />
-방사성 증식 분석(Promega)에 의해 결정되었다.<br />
항체 선별 역가 평가<br />
항원 인식은 4℃에서 하룻밤동안 인산염 완충된 염수(PBS, Hyclone)에서 Immulon 4 평판(Thermo)을 1 ㎍/㎖의<br />
huIL-6(50 ㎕/웰)으로 코팅함으로써 결정되었다. 분석 당일에, 평판은 PBS /Tween 20(PBST tablets,<br />
Calbiochem)로 3회 세척되었다. 평판은 이후, 37℃에서 30분 동안 PBS에서 200 ㎕/웰의 0.5% 비늘 젤라틴(FSG,<br />
Sigma)으로 차단되었다. 차단 용액은 제거되고, 그리고 평판은 블롯팅(blotting)되었다. 혈청 시료는 1:100의<br />
출발 희석도(채혈 및 채혈전)(모든 희석액은 FSG 50 ㎕/웰에서 만들어졌다)에서, 그 이후에 평판을 교차하여<br />
1:10 희석도에서 만들어졌다(칼럼 <strong>12</strong>는 배경 대조를 위하여 공백으로 남겨졌다). 평판은 37℃에서 30분 동안 배<br />
양되었다. 평판은 PBS/Tween 20으로 3회 세척되었다. 1:5000 희석된 염소 항-토끼 Fc-HRP(Pierce)는 모든 웰<br />
(50 ㎕/웰)에 첨가되고, 그리고 평판은 7℃에서 30분 동안 배양되었다. 평판은 앞서 기술된 바와 같이 세척되었<br />
다. 평판은 50 ㎕/웰의 TMB-Stable stop(Fitzgerald Industries)이 첨가되고, 그리고 일반적으로 3 내지 5분<br />
동안 현색되었다. 현색 반응은 50 ㎕/웰 0.5 M HCl로 중단되었다. 평판은 450 nm에서 판독되었다. 광학 밀도<br />
(OD) 대(對) 희석도가 Graph Pad Prizm 소프트웨어를 이용하여 플롯팅(plotting)되고, 그리고 역가가 결정되었<br />
다.<br />
기능적 역가 평가<br />
시료의 기능적 활성은 T1165 증식 분석에 의해 결정되었다. T1165 세포는 HEPES, 피루브산나트륨,<br />
중탄산나트륨, L-글루타민, 고농도 글루코오스, 페니실린/스트렙토마이신, 10% 열 불활성화된 소 태아 혈청<br />
(FBS)(모든 보충물은 Hyclone으로부터), 2-메르캅토에탄올(Sigma), 그리고 10 ng/㎖의 huIL-6(R&D)으로 보충된<br />
변형된 RPMI 배지(Hyclone)에서 일과적으로 유지되었다. 분석 당일에, 세포 생존능은 트립판 블루(Invitrogen)<br />
에 의해 결정되고, 그리고 세포는 20,000개 세포/웰의 고정 밀도로 접종되었다. 접종에 앞서, 세포는 인간-IL-6<br />
이 없는(5분 동안 13000 rpm에서 원심분리하고 상층액을 버림으로써) 앞서 기술된 배지에서 2회 세척되었다. 최<br />
종 세척후, 세포는 50 ㎕/웰에 동등한 부피에서 세척을 위하여 이용된 동일한 배지에서 재현탁되었다. 세포는<br />
실온에서 방치되었다.<br />
둥근-바닥, 96-웰 평판(Costar)에서, 혈청 시료는 시작 시점에 1:100, 그 이후에 5개의 복제물(열 B 내지 F: 희<br />
석은 huIL-6이 없는 앞서 기술된 배지에서 달성됨)에서 30 ㎕/웰에서 평판을 교차하여(칼럼 2 내지 10) 1:10 희<br />
석도로 첨가되었다. 칼럼 11은 IL-6 대조에 대한 배지이었다. 최종 EC50(이전에 결정된 농도)의 4x 농도에서 30<br />
㎕/웰의 huIL-6이 모든 웰에 첨가되었다(huIL-6은 앞서 기술된 배지에서 희석되었다). 웰은 항체 결합이 발생하<br />
도록 37℃에서 1시간 동안 배양되었다. 1시간후, 50 ㎕/웰의 항체-항원(Ab-Ag) 복합체가 둥근-바닥 평판에 배치<br />
된 평판 지도 형식(plate map format)에 따라, 편평-바닥, 96-웰 평판(Costar)으로 이전되었다. 열 G에서, 50<br />
㎕/웰의 배지가 배경 대조를 위하여 모든 웰(칼럼 2 내지 11)에 첨가되었다. 유보된 50 ㎕/웰의 세포 현탁액이<br />
모든 웰(칼럼 2 내지 11, 열 B 내지 G)에 첨가되었다. 칼럼 1과 <strong>12</strong>, 그리고 열 A와 H에서, 검사 웰의 증발을 예<br />
방하고 가장자리 효과(edge effect)를 최소화시키기 위하여 200 ㎕/웰의 배지가 첨가되었다. 평판은 37℃에서<br />
72시간 동안 4% CO2에서 배양되었다. 72시간 시점에, 20 ㎕/웰의 CellTiter96(Promega) 시약이 제조업체 프로토<br />
콜에 따라 모든 검사 웰에 첨가되고, 그리고 평판은 37℃에서 2시간 동안 배양되었다. 2시간 시점에, 평판은 검<br />
사 웰에서 세포를 분산시키고 균질성을 가능하게 하기 위하여 오비탈 진탕기(orbital shaker)에서 온화하게 혼<br />
합되었다. 평판은 490 nm 파장에서 판독되었다. 광학 밀도(OD) 대(對) 희석도가 Graph Pad Prizm 소프트웨어를<br />
이용하여 플롯팅(plotting)되고, 그리고 기능적 역가가 결정되었다. 양성 분석 대조 평판은 1 ㎍/㎖의 출발 농<br />
도(최종 농도), 그 이후에 평판을 교차하여 1:3 희석도에서 MAB2061(R&D Systems)을 이용하여 앞서 기술된 바와<br />
같이 수행되었다.<br />
조직 수확<br />
- 115 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0744]<br />
[0745]<br />
[0746]<br />
[0747]<br />
[0748]<br />
[0749]<br />
[0750]<br />
일단 허용가능 역가가 확립되면, 토끼(들)는 희생되었다. 비장, 림프절, 그리고 전혈이 수확되고 아래와 같이<br />
처리되었다:<br />
비장과 림프절은 20 cc 주사기의 플런저로 조직을 분리시키고 70 ㎛에서 무균 와이어 메시(wire mesh)(Fisher)<br />
에 밀어 넣음으로써 단일 세포 현탁액으로 처리되었다. 세포는 huIL-6이 없지만 소량의 글루코오스가 존재하는<br />
앞서 기술된 변형된 RPMI 배지에서 수집되었다. 세포는 원심분리에 의해 2회 세척되었다. 최종 세척후, 세포 밀<br />
도는 트립판 블루에 의해 결정되었다. 세포는 1500 rpm에서 10분 동안 원심분리되었다; 상층액은 폐기되었다.<br />
세포는 FBS(Hyclone)에서 적절한 부피의 10% 디메틸 설폭시드(DMSO, Sigma)에서 재현탁되고 1 ㎖/바이알로 분배<br />
되었다. 바이알은 이후, 장기 보관을 위한 액체 질소(LN2) 탱크에 배치되기에 앞서 -70℃에서 24시간 동안 보관<br />
되었다.<br />
말초혈 단핵 세포(PBMC)는 전혈을 각 분율의 FBS-없는 앞서 기술된 저농도 글루코오스 배지와 혼합함으로써 분<br />
리되었다. 35 ㎖의 전혈 혼합물은 45 ㎖ 원뿔형 튜브(Corning) 내로 8 ㎖의 Lympholyte Rabbit(Cedarlane) 상<br />
에 조심스럽게 층으로 쌓아지고 중단 없이 2500 rpm에서 실온에서 30분 동안 원심분리되었다. 원심분리후, PBMC<br />
층은 유리 Pasteur 피펫(VWR)을 이용하여 조심스럽게 제거되고, 합쳐지고, 그리고 깨끗한 50 ㎖ 바이알 내에 배<br />
치되었다. 세포는 1500 rpm에서 실온에서 10분 동안 원심분리에 의해 앞서 기술된 변형된 배지로 2회 세척되고,<br />
그리고 세포 밀도가 트립판 블루 염색에 의해 결정되었다. 최종 세척후, 세포는 적절한 부피의 10% DMSO/FBS 배<br />
지에서 재현탁되고 앞서 기술된 바와 같이 동결되었다.<br />
B 세포 배양<br />
B 세포 배양을 셋업한 당일에, PBMC, 비장세포, 또는 림프절 바이알은 이용을 위해 해동되었다. 바이알은 LN2<br />
탱크로부터 제거되고 해동될 때까지 37℃ 물 중탕에 배치되었다. 바이알의 내용물은 15 ㎖ 원뿔형 원심분리 튜<br />
브(Corning) 내로 이전되고, 그리고 앞서 기술된 10 ㎖의 변형된 RPMI가 상기 튜브에 천천히 첨가되었다. 세포<br />
는 1.5K rpm에서 5분 동안 원심분리되고, 그리고 상층액이 폐기되었다. 세포는 10 ㎖의 새로운 배지에서 재현탁<br />
되었다. 세포 밀도 및 생존능이 트립판 블루에 의해 결정되었다. 세포는 다시 세척되고 1E07 세포/80 ㎕ 배지에<br />
서 재현탁되었다. 세포 현탁액은 3 ㎍/㎖의 최종 농도에서 비오틴화된 huIL-6(B huIL-6)이 첨가되고 4℃에서 30<br />
분 동안 배양되었다. 결합되지 않은 B huIL-6은 인산염-완충된 (PBF):Ca/Mg 없는 PBS(Hyclone), 2 mM 에틸렌디<br />
아민 테트라아세트산(EDTA), 0.5% 소 혈청 알부민(BSA)(Sigma-비오틴 없음)의 10 ㎖ 세척액으로 2회<br />
제거되었다. 두 번째 세척후, 세포는 1E07 세포/80 ㎕ PBF에서 재현탁되었다. 20 ㎕의 MACS<br />
스트렙타비딘 비드(Milteni)/10E7 세포가 세포 현탁액에 첨가되었다. 세포는 4℃에서 15분 동안 배양되었다.<br />
세포는 2 ㎖의 PBF/10E7 세포로 1회 세척되었다. 세척후, 이들 세포는 1E08 세포/500 ㎕의 PBF에서 재현탁되고<br />
유보되었다. MACS<br />
MS 칼럼(Milteni)은 자석 스탠드(Milteni) 상에서 500 ㎖의 PBF로 미리 헹굼되었다. 세포 현탁액은 프리-필터<br />
를 통해 칼럼에 적용되고, 그리고 결합되지 않은 분획물이 수집되었다. 상기 칼럼은 1.5 ㎖의 PBF 완충액으로<br />
세척되었다. 상기 칼럼은 자석 스탠드로부터 제거되고 깨끗한 무균 5 ㎖ 폴리프로필렌 Falcon 튜브 상에 배치되<br />
었다. 1 ㎖의 PBF 완충액이 칼럼의 상부에 첨가되고, 그리고 양성 선별된 세포는 수집되었다. 양성과 음성 세포<br />
분획물의 수율과 생존능이 트립판 블루 염색에 의해 결정되었다. 양성 선별은 출발 세포 농도의 평균 1%를 생성<br />
시키였다.<br />
배양액에 대한 접종 수준에 관한 정보를 제공하기 위하여 파일럿 세포 스크린이 확립되었다. 3가지 10개-평판<br />
군(총 30개 평판)은 50, 100, 그리고 200개 농축된 B 세포/웰로 접종되었다. 또한, 각 웰은 고농도 글루코오스<br />
변형된 RPMI 배지 내에서 250 ㎕/웰의 최종 부피에서 50K 세포/웰의 조사(照射)된 EL-4.B5 세포(5,000 Rad) 및<br />
적절한 수준의 T 세포 상층액(준비에 따라 1-5% 범위)을 포함하였다. 배양액은 37℃에서 4% CO2에서 5 내지 7일<br />
동안 배양되었다.<br />
선택성 항체 분비 B 세포의 확인<br />
- 116 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0751]<br />
[0752]<br />
[0753]<br />
[0754]<br />
[0755]<br />
[0756]<br />
[0757]<br />
[0758]<br />
[0759]<br />
[0760]<br />
[0761]<br />
[0762]<br />
[0763]<br />
배양액은 5일 내지 7일 사이에 항원 인식 및 기능적 활성에 대하여 조사되었다.<br />
항원 인식 스크리닝<br />
이용된 ELISA 형식은 B 세포 배양액(BCC) 웰(모두 30개 평판)로부터 50 ㎕의 상층액이 항체의 공급원으로서 이<br />
용된 점을 제외하고 앞서 기술된 바와 동일하다. 상기 조건 배지는 항원-코팅된 평판으로 이동되었다. 양성 웰<br />
이 확인된 이후, 상층액은 제거되고 96-웰 마스터 평판(들)으로 이동되었다. 이들 초기 배양액 평판은 이후, 40<br />
㎕/웰을 제외하고 모든 상층액을 제거하고 FBS에서 60 ㎕/웰의 16% DMSO를 첨가함으로써 동결되었다. 평판은 동<br />
결을 지연시키기 위하여 종이 타월로 감싸지고 -70℃에 배치되었다.<br />
기능적 활성 스크리닝<br />
마스터 평판은 이후, 열 B가 배경 대조에 대한 배지이고, 열 C가 양성 증식 대조에 대한 배지 + IL-6이고, 그리<br />
고 열 D-G 및 칼럼 2-11이 BCC(50 ㎕/웰, 단일 점)로부터 웰인 점을 제외하고, 앞서 기술된 바와 같은 T1165 증<br />
식 분석에서 기능적 활성에 대하여 스크리닝되었다. 40 ㎕의 IL-6이 상기 분석에서 결정된 EC50 농도의<br />
2.5배로, 상기 배지 열을 제외한 모든 웰에 첨가되었다. 1시간 배양후, Ab/Ag 복합체는 조직 배양액(TC)<br />
처리된, 96-웰, 편평-바닥 평판으로 이동되었다. huIL-6(20,000개 세포/웰에서 T1165)이 없는 변형된 RPMI 배지<br />
에서 20 ㎕의 세포 현탁액이 모든 웰(웰당 100 ㎕ 최종 부피)에 첨가되었다. 배경은 뺄셈되고, 그리고 관찰된<br />
OD 값은 저해 %로 변환되었다.<br />
B 세포 회수<br />
목적되는 웰을 포함하는 평판은 -70℃로부터 이전되고, 그리고 각 웰로부터 세포는 5-200 ㎕ 배지/웰의 세척액<br />
으로 회수되었다. 이들 세척액은 1.5 ㎖ 무균 원심분리 튜브 내에 모아지고, 그리고 세포는 1500 rpm에서 2분<br />
동안 작은 알로 뭉쳐졌다.<br />
상기 튜브는 뒤집어지고, 회전은 반복되고, 그리고 상층액은 조심스럽게 제거되었다. 세포는 100 ㎕/튜브의 배<br />
지에서 재현탁되었다. 배지에서 1:100 희석된 100 ㎕ 비오틴화된 IL-6 코팅된 스트렙타비딘 M280<br />
dynabead(Invitrogen) 및 16 ㎕의 염소 항-토끼 H&L IgG-FITC가 세포 현탁액에 첨가되었다.<br />
20 ㎕의 세포/비드/FITC 현탁액은 제거되고, 그리고 Sigmacote(Sigma)로 미리 처리된 유리 슬라이드(Corning)<br />
상에서 5 ㎕ 비말이 35 내지 40개 비말/슬라이드로 만들어졌다. 이들 비말을 물에 담그기 위하여 파라핀 오일<br />
(JT Baker)의 불침투성 장벽이 첨가되고, 그리고 37℃, 4% CO2에서 어둠 하에 90분 동안 상기 슬라이드가 배양<br />
되었다.<br />
항체를 생산하는 특이적 B 세포는 항체 분비로 인한 그들 주변에 형광 고리, 비드-결합된 비오틴화된 항원의 인<br />
식, 그리고 형광-IgG 검출 시약에 의한 차후 검출에 의해 확인될 수 있다. 일단 목적되는 세포가 확인되면, 형<br />
광 고리의 중심에서 세포는 미세조작기(Eppendorf)를 통해 회수되었다. 항체를 합성하고 이출하는 단일 세포는<br />
250 ㎕ 마이크로원심분리 튜브 내로 이전되고 드라이아이스에 배치되었다. 목적되는 모든 세포를 회수한 이후,<br />
이들은 장기 보관을 위하여 -70℃로 이전되었다.<br />
실시예 8 효모 세포 발현<br />
공개특허 10-2011-01<strong>12</strong>308<br />
항체 유전자: 키메라 인간화된 토끼 단일클론 항체의 합성을 주동하는 유전자가 클로닝되고 작제되었다.<br />
발현 벡터: 본 벡터는 아래의 기능적 성분을 포함한다: 1) 대장균(Escherichia coli)의 세포 내에서 플라스미드<br />
벡터의 복제를 조장하는 돌연변이 ColE1 복제 기점; 2) 항생제 Zeocin(플레오마이신)에 대한 내성을<br />
공여하고, 그리고 대장균(E. coli)과 피치아 파스토리스(P. pastoris) 둘 모두의 형질전환에 대한 선별가능 마<br />
커로서 기능하는 세균 Sh ble 유전자; 3) 사카로마이세스 세레비지애(Saccharomyces cerevisiae) 알파 교배 인<br />
자 프리 프로 분비 리더 서열을 인코딩하는 서열, 그 다음에 피치아 파스토리스(P. pastoris) 알코올 산화효소<br />
I 유전자(AOX1)로부터 피치아 파스토리스(P. pastoris) 전사 종결 신호를 인코딩하는 서열에 융합된 글리세르알<br />
데히드 탈수소효소(glyceraldehyde dehydrogenase) 유전자(GAP 유전자) 프로모터로 구성되는 발현 카세트.<br />
- 117 -
[0764]<br />
[0765]<br />
[0766]<br />
[0767]<br />
[0768]<br />
[0769]<br />
[0770]<br />
Zeocin(플레오마이신) 내성 마커 유전자는 더욱 높은 수준의 Zeocin(플레오마이신)에 내성을 갖는 형질전환<br />
체를 선별함으로써, 균주 내에서 발현 벡터의 복수 통합된 사본을 포함하는 균주에 대한 농축의 수단을 제공한<br />
다.<br />
피치아 파스토리스(P. pastoris) 균주: 피치아 파스토리스(P. pastoris) 균주 met1, lys3, ura3과 ade1이 이용<br />
될 수 있다. 임의의 2가지 상보성 세트의 영양요구성 균주가 2배체 균주의 작제와 유지에 이용될 수 있긴 하지<br />
만, 이들 두 균주는 2가지 이유로 본 발명의 방법에 특히 적합하다. 첫째, 이들 균주는 그들의 교배 또는 융합<br />
의 결과물인 2배체 균주보다 더욱 느리게 성장한다. 따라서 적은 숫자의 반수체 ade1 또는 ura3 세포가 배양액<br />
내에 존재하거나, 또는 감수분열 또는 다른 기전을 통하여 발생하면, 2배체 균주는 배양액 내에서 이들보다 빨<br />
리 자란다.<br />
둘째, 교배로부터 발생하는 2배체 Ade+ 콜로니는 정상적인 백색 또는 크림색인 반면, 반수체 ade1 돌연변이체인<br />
임의의 균주의 세포는 독특한 핑크색을 갖는 콜로니를 형성할 것이기 때문에, 이들 균주의 성적 상태를 모니터<br />
하는 것이 용이하다. 이에 더하여, 반수체 ura3 돌연변이체인 임의의 균주는 약물 5-플루오르-오로틴산(FOA)에<br />
내성이고 FOA를 포함하는 최소 배지 + 우라실 평판 상에 배양액의 시료를 도말함으로써 민감하게 확인될 수 있<br />
다. 이들 평판에서, 우라실-요구 ura3 돌연변이(아마도 반수체) 균주만 성장하고 콜로니를 형성할 수 있다. 따<br />
라서 ade1과 ura3으로 표기된 반수체 모 균주로, 결과의 항체-생산 2배체 균주의 성적 상태를 용이하게 모니터<br />
할 수 있다(반수체 대(對) 2배체)<br />
방법<br />
경쇄와 중쇄 항체 유전자의 전사를 위한 pGAPZ-알파 발현 벡터의 작제. 인간화된 경쇄와 중쇄 단편은 PCR 주동<br />
된 과정을 통해 pGAPZ 발현 벡터 내로 클로닝되었다. 회수된 인간화된 구조체는 아래의 프라이머 (1) 경쇄 전방<br />
AGCGCTTATTCCGCTATCCAGATGACCCAGTC(AfeI 부위는 단일 밑줄로 표시됨)를 이용하는 표준 KOD 중합효소(Novagen)<br />
키트 조건((1) 94℃, 2분; (2) 94℃, 30초; (3) 55℃, 30초; (4) 72℃, 30초-35회 동안 단계 2-4 사이클링;<br />
(5) 72℃ 2분) 하에 증폭에 종속되었다. HSA 신호 서열의 끝은 이중 밑줄로 표시되고, 그 다음에 성숙 가변 경<br />
쇄에 대한 서열(밑줄로 표시되지 않음); 역방 CGTACGTTTGATTTCCACCTTG가 위치한다.<br />
가변 경쇄 후방 프라이머. BsiWI 부위가 밑줄로 표시되고, 그 다음에 가변 경쇄의 3' 말단에 대한 역방 보체가<br />
위치한다. AfeI와 BsiWI로 제한 효소 절단 시에, 이는 이출을 위한 인간 카파 경쇄 불변 영역과 인 프레임(in<br />
frame)으로 인간 HAS 리더 서열을 이용하여 pGAPZ 벡터와 인-프레임으로 삽입을 가능하게 한다. (2) 중쇄에 대<br />
하여 유사한 전략이 수행된다. 이용된 전방 프라이머는 AGCGCTTATTCCGAGGTGCAGCTGGTGGAGTC이다. AfeI 부위는<br />
단일 밑줄로 표시된다. HSA 신호 서열의 끝은 이중 밑줄로 표시되고, 그 다음에 성숙 가변 중쇄에 대한 서열(밑<br />
줄로 표시되지 않음)이 위치한다. 역방 중쇄 프라이머는 CTCGAGACGGTGACGAGGGT이다. XhoI 부위는 밑줄로 표시되<br />
고, 그 다음에 가변 중쇄의 3' 말단에 대한 역방 보체가 존재한다. 이는 비교 지향성 클로닝 전략(comparable<br />
directional cloning strategy)을 이용하여 pGAPZ 내에 앞서 삽입된 IgG-γ1 CH1-CH2-CH3 부위와 인-프레임으<br />
로 중쇄의 클로닝을 가능하게 한다.<br />
피치아 파스토리스(P. pastoris)의 반수체 ade1, ura3, met1과 lys3 숙주 균주 내로 발현 벡터의 형질전환. 반<br />
수체 피치아 파스토리스(P. pastoris) 균주의 형질전환 및 피치아 파스토리스(P. pastoris) 유성 주기의 유전자<br />
조작에 이용된 모든 방법은 Higgins, D. R., and Cregg, J. M., Eds. <strong>19</strong>98. Pichia Protocols. Methods in<br />
Molecular Biology. Humana Press, Totowa, NJ에서 기술된다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
형질전환에 앞서, 각 발현 벡터는 피치아 파스토리스(P. pastoris) 게놈의 GAP 프로모터 좌위 내로 이들 벡터의<br />
통합을 유도하기 위하여, GAP 프로모터 서열 내에서 AvrII로 선형화된다. 각 벡터의 시료는 이후, 전기천공<br />
(electroporation)에 의해 ade1, ura3, met1과 lys3 균주의 전기적격성 배양액 내로 개별적으로 형질전환되고,<br />
그리고 성공적인 형질전환체는 상기 항생제에 대한 그들의 내성에 의해 YPD Zeocin(플레오마이신) 평판 상에<br />
서 선별되었다. 결과의 콜로니는 선별되고, YPD Zeocin(플레오마이신) 평판 상에서 단일 콜로니에 대하여 스<br />
트리킹(streaking)되고, 이후 적절한 항체 유전자 삽입물에 대한 각 균주로부터 추출된 게놈 DNA 상에서 PCR 분<br />
석에 의해 및/또는 콜로니 리프트/면역블롯 방법으로 항체 사슬을 합성하는 각 균주의 능력에 의해, 항체 유전<br />
자 삽입물의 존재에 대하여 조사되었다(Wung et al. Biotechniques 21 808-8<strong>12</strong> (<strong>19</strong>96)). 3가지 중쇄 구조체 중<br />
에서 한 가지를 발현하는 반수체 ade1, met1과 lys3 균주는 반수체 ura3 균주 발현 경쇄 유전자와 함께 2배체<br />
작제를 위하여 수집된다. 이들 반수체 발현 중쇄 유전자는 2배체 분비 단백질을 생성시키기 위하여, 적절한 경<br />
- 118 -
[0771]<br />
[0772]<br />
[0773]<br />
[0774]<br />
[0775]<br />
[0776]<br />
[0777]<br />
[0778]<br />
쇄 반수체 ura3과 교배된다.<br />
단일 항체 사슬을 합성하는 반수체 균주의 교배 및 사합체 기능적 항체를 합성하는 2배체 유도체의 선별. 피치<br />
아 파스토리스(P. pastoris) 반수체 균주를 교배하기 위하여, 교배되는 각각의 ade1(또는 met1 또는 lys3) 중쇄<br />
생산 균주는 풍부한 YPD 평판을 교차하여 스트리킹되고, 그리고 ura3 경쇄 생산 균주는 두 번째 YPD 평판을 교<br />
차하여 스트리킹된다(평판당 ~10개 스트리킹). 30℃에서 1일 또는 2일 배양후, 중쇄 균주를 포함하는 하나의 평<br />
판 및 ura3 경쇄 균주를 포함하는 하나의 평판으로부터 세포는 각각의 중쇄 균주가 각 경쇄 균주와 혼합된 세포<br />
의 패치를 포함하도록 하기 위하여, 교차 해치드 패턴(cross hatched pattern)으로 복제-도말 블록 상에서 무균<br />
벨벳 천으로 이전되었다. 교차-스트리킹된 복제 도말된 세포는 이후, 교배 평판으로 이전되고 균주 간에 교배의<br />
시작을 촉진하기 위하여 25℃에서 배양되었다. 2일후, 이들 교배 평판 상에서 세포는 복제-도말 블록 상에서 무<br />
균 벨벳으로 다시 이전되고, 이후 최소 배지 평판으로 이전되었다. 이들 평판은 독립영양성 2배체 균주의 콜로<br />
니의 선택성 성장을 가능하게 하기 위하여, 3일 동안 30℃에서 배양되었다. 발생된 콜로니는 정선되고, 그리고<br />
콜로니 분리물을 선별하고 각각의 2배체 균주를 정제하기 위하여 두 번째 최소 배지 평판 상에 스트리킹된다.<br />
결과의 2배체 세포주는 이후, 항체 생산에 대하여 조사된다.<br />
추정 2배체 균주는 그들이 2배체이고 항체 생산을 위한 양쪽 발현 벡터를 포함한다는 것을 증명하기 위하여 시<br />
험된다. 2배수성의 경우에, 균주의 시료는 이들 균주가 감수분열을 겪고 포자를 형성하도록 촉진하기 위하여 교<br />
배 평판 상에 발라진다. 반수체 포자 산물은 수집되고 표현형에 대하여 조사된다. 결과의 포자 산물 중에서 유<br />
의한 비율이 단일 또는 이중 영양요구체이면, 최초 균주는 2배체인 것으로 결론될 수 있다. 2배체 균주는 각각<br />
으로부터 게놈 DNA를 추출하고 각 유전자에 특이적인 PCR 반응에 이러한 DNA를 이용함으로써 양쪽 항체 유전자<br />
의 존재에 대하여 조사된다.<br />
단일 항체 사슬을 합성하는 반수체 균주의 융합 및 사합체 기능적 항체를 합성하는 2배체 유도체의 선별. 앞서<br />
기술된 교배 절차에 대한 대안으로, 단일-사슬 항체 생산 반수체 ade1과 ura3 균주의 개별 배양액은 스페로플라<br />
스트화되고, 그들의 결과의 스페로플라스트는 폴리에틸렌 글리콜/CaCl2를 이용하여 융합된다. 융합된 반수체 균<br />
주는 이후, 2배체 균주가 그들의 세포 벽을 재생시키고 가시적인 콜로니로 성장할 수 있도록 하기 위하여, 1 M<br />
소르비톨과 최소 배지를 포함하는 아가에 끼워 넣어진다. 결과의 콜로니는 아가로부터 정선되고, 최소 배지 평<br />
판 상에 스트리킹되고, 그리고 이들 평판은 2배체 세포주의 단일 세포로부터 콜로니를 생성시키기 위하여 30℃<br />
에서 2일 동안 배양된다. 결과의 추정 2배체 세포주는 이후, 앞서 기술된 바와 같이 2배수성 및 항체 생산에 대<br />
하여 조사된다.<br />
항체의 정제와 분석. 전장 항체의 생산을 위한 2배체 균주는 앞서 기술된 방법을 이용하여 met1 경쇄와 lys3 중<br />
쇄의 교배를 통하여 도출된다. 2배체 피치아 파스토리스(P. pastoris) 발현 균주의 진탕-플라스크 또는 발효기<br />
배양액으로부터 배양액 배지는 수집되고, 그리고 SDS-PAGE 및 인간 IgG의 중쇄와 경쇄, 또는 특히, IgG의 중쇄<br />
에 대한 항체를 이용한 면역블롯팅(immunoblotting)을 통해 항체 단백질의 존재에 대하여 조사된다.<br />
효모 분비된 항체를 정제하기 위하여, 항체 생산 배양액으로부터 정화된 배지는 단백질 A 칼럼에 통과되고, 그<br />
리고 20 mM 나트륨 인산염, pH 7.0, 결합 완충액으로 세척후, 단백질 A 결합된 단백질이 0.1 M 글리신 HCl 완충<br />
액, pH 3.0을 이용하여 용출된다. 가장 많은 전체 단백질을 포함하는 분획물은 항체 단백질에 대하여 Coomasie<br />
blue 염색된 SDS-PAGE 및 면역블롯팅에 의해 조사된다. 항체는 IL-6 인식을 위한 앞서 기술된 ELISA를 이용하여<br />
특성화된다.<br />
항체 활성의 분석. 재조합 효모-유래된 인간화된 항체는 앞서 기술된 IL-6 주동된 T1165 세포 증식 분석 및 IL-<br />
6 촉진된 HepG2 합토글로빈 분석을 통하여 기능적 활성에 대하여 평가된다.<br />
실시예 9 항-IL-6 항체 Ab1의 정맥내 투여에 의한 급성기 반응 중화<br />
인간 IL-6은 쥐에서 급성기 반응을 유발할 수 있고, 그리고 쥐에서 자극되는 주요 급성기 단백질 중에서 한 가<br />
지는 알파-2 마크로글로불린(A2M)이다. 상이한 용량(0.03, 0.1, 0.3, 1, 그리고 3 ㎎/㎏)의 항체 Ab1(n=10 쥐/<br />
용량 수준) 또는 대조로서 다중클론 인간 IgG1(n=10마리 쥐)의 정맥내 투여후 1시간 시점에 제공된 100 ㎍의 인<br />
간 IL-6의 단일 s.c. 주사에 대한 A2M 반응을 제거하는데 필요한 항체 Ab1의 용량을 평가하는 연구가 설계되었<br />
다. 혈장은 회수되고, 그리고 A2M은 상업적 샌드위치 ELISA 키트(ICL Inc., Newberg OR; cat. no.- E-25A2M)를<br />
통해 통해 정량되었다. 종점은 24시간 시점(post-Ab1)에서 A2M의 혈장 농도에서 차이이었다. 획득된 결과는 도<br />
4에 제공된다.<br />
- 1<strong>19</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
[0779]<br />
[0780]<br />
[0781]<br />
[0782]<br />
[0783]<br />
[0784]<br />
[0785]<br />
[0786]<br />
[0787]<br />
[0788]<br />
[0789]<br />
[0790]<br />
[0791]<br />
[0792]<br />
항체 Ab1에 대한 ID50은 0.1 ㎎/㎏이고, 그리고 0.3 ㎎/㎏에서 A2M 반응이 완전히 억제되었다. 이는 인간 IL-<br />
6의 생체내 중화가 항체 Ab1에 의해 달성될 수 있다는 것을 명백하게 증명한다.<br />
실시예 10 RXF393 악액질 모형 연구 1.<br />
도입<br />
인간 신장 세포 암 세포주, RXF393은 무흉선 누드 생쥐 내로 이식될 때, 현저한 체중 감소를 유발한다. 체중 감<br />
소는 이식후 대략 15일 시점에 시작되고, 그리고 80%의 동물이 이식후 18 - 20일 시점에 전체 체중의 적어도<br />
30%를 상실한다. RXF393은 인간 IL-6을 분비하고, 그리고 이들 동물에서 인간 IL-6의 혈장 농도는 대략 10 ng/<br />
㎖에서 매우 높다. 인간 IL-6은 뮤린 가용성 IL-6 수용체에 결합하고 생쥐 내에서 IL-6 반응을 활성화시킨다.<br />
인간 IL-6은 생쥐에서 IL-6 반응을 활성화시키는데 있어서 뮤린 IL-6보다 대략 10배 덜 강력하다. 본 연구의 목<br />
적은 인간 신장 세포 암 세포주, RXF393으로 이식된 무흉선 누드 생쥐 내에서 생존, 체중, 혈청 아밀로이드 A<br />
단백질, 혈액 파라미터, 그리고 종양 성장에 대한 항체 Ab1의 효과를 결정하는 것이었다.<br />
방법<br />
80마리, 6주령, 수컷 무흉선 누드 생쥐는 오른쪽 옆구리에서 RXF393 종양 단편(30-40 ㎎)이 피하 이식되었다.<br />
동물은 이후, 10마리 생쥐의 8개 군으로 분할되었다. 3마리 군은 이식후 1일, 8일, 15일과 22일자에 주1회씩 3<br />
㎎/㎏, 10 ㎎/㎏, 또는 30 ㎎/㎏의 항체 Ab1이 정맥내 투약되었다(진행 군). 다른 3마리 군은 이식후 8일, 15일<br />
과 22일자에 주1회씩 3 ㎎/㎏, 또는 10 ㎎/㎏, 또는 30 ㎎/㎏의 항체 Ab1이 정맥내 투약되었다(역행 군). 최종<br />
적으로, 하나의 대조 군은 다중클론 인간 IgG 30 ㎎/㎏이, 그리고 두 번째 대조 군은 인산염 완충된 염수가 이<br />
식후 1일, 8일, 15일과 22일자에 주1회씩 정맥내 제공되었다.<br />
동물은 28일자에, 종양이 4,000 mm 3<br />
에 도달할 때, 또는 그들이 쇠약해지면(체중의 >30% 상실) 안락사되었다. 동<br />
물은 이식후 1일, 6일, 그리고 9일부터 28일까지 매일 칭량되었다. 평균 체중 비율(Mean Percent Body Weight,<br />
MPBW)이 본 연구 동안 체중 감소를 모니터하기 위한 일차 파라미터로서 이용되었다. 이는 아래와 같이 계산되었<br />
다: (체중 - 종양 중량)/기준선 체중 x 100. 종양 중량은 이식후 1, 6, 9, <strong>12</strong>, 15, 18, 22, 25와 28일자에 측<br />
정되었다. 혈액은 5일과 13일자에 각 군에서 5마리 생쥐로부터 마취 하에 채취되고, 그리고 안락사될 때(대부분<br />
의 경우에 28일자 시점) 각 군에서 10마리 생쥐 모두에서 채취되었다. 혈액은 혈액학과 혈청 아밀로이드 A 단백<br />
질(SAA) 농도에 대하여 분석되었다. 10마리 비-종양 보유 6주령, 무흉선 누드 수컷 생쥐의 추가 군은 기준선 값<br />
으로 기능하는 혈액학과 SAA 농도 평가를 위하여 혈액 시료가 채취되었다.<br />
결과 - 생존<br />
항체 Ab1 군의 동물은 28일의 연구 종결일 이전에, 안락사되거나 폐사하지 않았다. 2가지 대조 군에서, 15마리<br />
동물(다중클론 인간 IgG 군에서 7/9 및 인산염 완충된 염수 군에서 8/10)이 폐사하거나, 또는 매우 쇠약해져(체<br />
중의 >30% 상실) 안락사되었다. 양쪽 대조 군에서 평균 생존 기간은 20일이었다.<br />
이들 두 대조 군 및 항체 Ab1 진행(본 연구의 1일자부터 투약됨) 군에 대한 생존 곡선은 도 5에 제공된다.<br />
이들 두 대조 군 및 항체 Ab1 역행(본 연구의 8일자부터 투약됨) 군에 대한 생존 곡선은 도 6에 제공된다.<br />
다중클론 인간 IgG(p=0.0038)와 인산염 완충된 염수(p=0.0003) 대조 군에 대한 생존 곡선 및 6가지 항체 Ab1 군<br />
에 대한 생존 곡선 사이에 통계학적으로 유의한 차이가 존재하였다. 두 대조 군 사이에 통계학적으로 유의한 차<br />
이는 존재하지 않았다(p=0.97).<br />
결과 - 종양 크기<br />
공개특허 10-2011-01<strong>12</strong>308<br />
생존 생쥐에서 종양 크기는 촉진에 의해 평가되었다. 본 연구의 첫 15일 동안, 임의의 군에서 어떤 생쥐도 폐사<br />
하거나 안락사되지 않았고, 따라서 이들 일자에서 군간에 종양 크기의 비교는 샘플링 치우침(sampling bias)이<br />
없었다. 15일자까지 항체 Ab1 진행 군 또는 역행 군 및 대조 군 사이에 종양 크기에서 차이가 관찰되지 않았다.<br />
- <strong>12</strong>0 -
[0793]<br />
[0794]<br />
[0795]<br />
[0796]<br />
[0797]<br />
[0798]<br />
[0799]<br />
[0800]<br />
[0801]<br />
대조에서 폐사의 발생(15일자) 다음에 대조 군과 치료 군에서 생존 생쥐 사이에 종양 크기의 비교는 진행되지<br />
않았는데, 그 이유는 생존하는 대조 생쥐의 종양 크기가 치우친 것으로 추정되고, 따라서 이런 비교의 결과가<br />
무의미했기 때문이다.<br />
항체 Ab1의 투여가 종양 크기에서 명백한 감소 없이 생존을 촉진했기 때문에, 상승된 혈청 IL-6은 종양 성장과<br />
독립적인 기전을 통하여 폐사의 원인이 될 수 있다. 이들 관찰 결과는 항체 Ab1이 아마도 환자의 전반적인 복지<br />
를 강화시킴으로써, 종양 성장에 직접적인 영향을 주지 않으면서 암 환자 생존력을 증진할 수 있다는 가설을 뒷<br />
받침한다.<br />
결과 - 체중 감소<br />
평균 체중 비율(MPBW)(±SEM) 대(對) 시간은 도 27에 도시된다. 대조와 비교하여, Ab1이 투약된 생쥐는 체중 감<br />
소로부터 보호되었다. 18일자에, 대조 생쥐에서 MPBW는 75%이고, 25%의 평균 체중 감소에 상응하였다. 대조적으<br />
로, 동일자에, Ab-1 치료 군에서 MPBW는 변화가 미미하였다(97% 내지 103%). 대조(다중클론 인간 IgG 또는 PBS<br />
가 투여됨) 및 10 ㎎/㎏ 용량 군(p
[0802]<br />
[0803]<br />
[0804]<br />
[0805]<br />
[0806]<br />
[0807]<br />
[0808]<br />
[0809]<br />
[0810]<br />
[0811]<br />
[08<strong>12</strong>]<br />
[0813]<br />
[0814]<br />
항체 Ab1이 생체내 효능을 나타낸다는 주장을 더욱 뒷받침한다.<br />
실시예 11 RXF393 악액질 모형 2.<br />
도입<br />
두 번째 연구는 항체 Ab1로 치료가 후기 단계(이식후 10일과 13일자)에서 시작되고 치료 기간이 더욱 연장(이식<br />
후 49일자까지)된 RXF-393 악액질 모형에서 수행되었다. 항체 Ab1로 투약 간격(dosing interval)이 7일에서 3일<br />
로 단축되고, 그리고 일일 사료 소비 역시 측정되었다. 또한, 항체 Ab1로 최초 투약 시점에 종양 크기를 표준화<br />
하려는 시도가 있었다.<br />
방법<br />
80마리, 6주령, 수컷 무흉선 누드 생쥐는 오른쪽 옆구리에서 RXF393 종양 단편(30-40 ㎎)이 피하 이식되었다.<br />
종양이 270 - 320 ㎎ 크기에 도달한 20마리 생쥐가 선별되고 2가지 군으로 분할되었다. 한쪽 군은 10 ㎎/㎏ 항<br />
체 Ab1이 3일마다, 그리고 다른 군은 10 ㎎/㎏ 다중클론 인간 IgG가 3일마다, 상기 시점(이식후 10일)부터 i.v.<br />
투여되었다. 종양 크기가 400 - 527 ㎎에 도달한 다른 20마리 생쥐가 선별되고 2가지 군으로 분할되었다. 한쪽<br />
군은 10 ㎎/㎏ 항체 Ab1이 3일마다, 그리고 다른 군은 10 ㎎/㎏ 다중클론 인간 IgG가 3일마다, 상기 시점(이식<br />
후 13일)부터 i.v. 투여되었다. 나머지 40마리 생쥐는 본 연구에 더 이상 참여되지 않고 49일자에, 종양이<br />
4,000 mm 3<br />
에 도달할 때, 또는 매우 쇠약해지면(체중의 >30% 상실) 안락사되었다.<br />
동물은 이식후 1일 내지 49일까지 3-4일마다 칭량되었다. 평균 체중 비율(MPBW)은 본 연구 동안 체중 감소를 모<br />
니터하기 위한 일차 파라미터로서 이용되었다. 이는 아래와 같이 계산되었다: ((체중 - 종양 중량)/기준선<br />
체중) x 100. 종양 중량은 이식후 5일 내지 49일까지 3-4일마다 측정되었다. 사료 소비는 270-320 ㎎ 종양 군의<br />
경우에 10일자부터, 그리고 400-527 ㎎ 종양 군의 경우에 13일자부터 매일 측정되었다(각 치료 군에 의해 중량<br />
으로 24시간 동안 소비된 양(g))<br />
결과-생존<br />
3일마다 10 ㎎/㎏ 항체 Ab1 i.v.(270-320 ㎎ 종양 크기), 그리고 3일마다 10 ㎎/㎏ 다중클론 인간 IgG<br />
i.v.(270-320 ㎎ 종양 크기)에 대한 생존 곡선은 도 7에 제공된다.<br />
3일마다 10 ㎎/㎏ 항체 Ab1 i.v.(270-320 ㎎ 종양 크기), 그리고 3일마다 10 ㎎/㎏ 다중클론 인간 IgG<br />
i.v.(270-320 ㎎ 종양 크기)에 대한 평균 생존은 각각, 46일과 32.5일이었다(p=0.0071).<br />
3일마다 10 ㎎/㎏ 항체 Ab1 i.v.(400-527 ㎎ 종양 크기), 그리고 3일마다 10 ㎎/㎏ 다중클론 인간 IgG<br />
i.v.(400-527 ㎎ 종양 크기)에 대한 생존 곡선은 도 8에 제공되다. 3일마다 10 ㎎/㎏ 항체 Ab1 i.v.(400-527<br />
㎎ 종양 크기), 그리고 3일마다 10 ㎎/㎏ 다중클론 인간 IgG i.v.(400-527 ㎎ 종양 크기)에 대한 평균 생존은<br />
각각, 46.5일과 27일이었다(p=0.0481).<br />
실시예 <strong>12</strong> 비-인간 영장류에서 항체 Ab1의 복수-투약 약동학적 평가<br />
항체 Ab1은 인산염 완충된 염수에 담겨, 1마리의 수컷과 1마리의 암컷 필리핀 원숭이(cynomolgus monkey)에 단<br />
일 일시 주사로 투약되었다. 혈장 시료는 고정된 시간 간격에서 채취되고, 그리고 항체 Ab1의 수준은 항원 포획<br />
ELISA 분석의 이용을 통해 정량되었다. 비오틴화된 IL-6(50 ㎕의 3 ㎍/㎖)은 스트렙타비딘 코팅된 96 웰 마이크<br />
로역가 평판 상에 포획되었다. 이들 평판은 세척되고 0.5% 비늘 젤라틴으로 차단되었다. 적절하게 희석된 혈장<br />
시료가 첨가되고 실온에서 1시간 동안 배양되었다. 상층액이 제거되고 항-hFc-HRP 접합된 이차 항체가 적용되고<br />
실온에서 방치되었다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
이들 평판은 이후, 흡출되고 항체의 양을 가시화시키기 위하여 TMB가 첨가되었다. 이후, 표준 곡선의 이용을 통<br />
해 특이적 수준이 결정되었다. 항체 Ab1의 이차 용량이 35일자에 이들 동일한 2마리 필리핀 원숭이에 투여되고,<br />
그리고 이러한 실험은 동일한 샘플링 계획을 이용하여 반복되었다. 결과의 농도는 이후, 도 9에 도시된 바와 같<br />
- <strong>12</strong>2 -
[0815]<br />
[0816]<br />
[0817]<br />
[0818]<br />
[08<strong>19</strong>]<br />
[0820]<br />
[0821]<br />
[0822]<br />
[0823]<br />
[0824]<br />
[0825]<br />
[0826]<br />
[0827]<br />
이 시간과 대비하여 플롯팅된다.<br />
피치아 파스토리스(Pichia pastoris) 발현되고 정제된 이러한 인간화된 전장 비당화된 항체는 포유동물 발현된<br />
단백질에 필적하는 특징을 나타낸다. 이에 더하여, 이러한 산물의 복수 투약은 재현가능한 반감기를 보이고, 이<br />
는 이러한 생산 플랫폼이 강화된 면역원성을 나타내는 산물을 생성시키지 않는다는 것을 암시한다.<br />
실시예 13 항체 단백질의 Octet 기계적 특성화<br />
IL-6 신호전달은 IL-6 및 2가지 수용체: IL-6R1(CD<strong>12</strong>6)과 gp130(IL-6 신호전달체) 사이에 상호작용에<br />
의존한다. 항체의 작용 기전을 결정하기 위하여, Octet QK 기구(ForteBio; Menlo Park, CA)를 이용한 생물-층<br />
간섭법(bio-layer interferometry)에 의해 기계적 연구가 수행되었다. 연구는 2가지 상이한 형태로 수행되었다.<br />
첫 번째 방침에서, 비오틴화된 IL-6(R&D systems 부품 번호 206-IL-001MG/CF, 제조업체의 프로토콜에 따라<br />
Pierce EZ-링크 설포-NHS-LC-LC-비오틴 제품 번호 21338을 이용하여 비오틴화됨)이 스트렙타비딘 코팅된 바이오<br />
센서(ForteBio 제품 번호 18-5006)에 초기에 결합되었다. 결합은 신호에서 증가로서 모니터된다.<br />
상기 센서에 결합된 IL-6은 이후, 문제되는 항체, 또는 희석 용액 단독과 함께 배양되었다. 상기 센서는 이후,<br />
가용성 IL-6R1(R&D systems 제품 번호 227-SR-025/CF) 분자와 함께 배양되었다. IL-6R1 분자가 결합하지 못하<br />
면, 상기 항체는 IL-6/IL-6R1 상호작용을 차단하는 것으로 간주되었다. 이들 복합체는 안정성 목적으로, IL-6R1<br />
의 존재에서 gp130(R&D systems 228-GP-010/CF)과 함께 배양되었다. gp130이 결합하지 않으면, 상기 항체는<br />
gp130과 IL-6의 상호작용을 차단하는 것으로 결론되었다.<br />
두 번째 방침에서, 항체는 항-인간 IgG1 Fc-특이적 시약(ForteBio 부품 번호 18-5001)으로 코팅된 바이오센서에<br />
결합되었다. IL-6이 상기 고정된 항체에 결합되고, 그리고 상기 센서가 IL-6R1과 함께 배양되었다. IL-6R1이<br />
IL-6과 상호작용하지 않으면, 상기 IL-6 결합 항체는 IL-6/IL-6R1 상호작용을 차단하는 것으로 결론되었다. 항<br />
체/IL-6/IL-6R1이 관찰되는 상황에서, 상기 복합체는 IL-6R1의 존재에서 gp130과 함께 배양되었다. gp130이 상<br />
호작용하지 않으면, 상기 항체는 IL-6/gp130 상호작용을 차단하는 것으로 결론되었다. 모든 연구는 30℃와 1000<br />
rpm에서, 200 ㎕ 최종 부피로 수행되었다. 이들 연구를 위하여, 모든 단백질은 ForteBio의 시료 희석 완충액(부<br />
품 번호 18-5028)을 이용하여 희석되었다.<br />
결과는 도 10(A-E)과 도 11에 제공된다.<br />
실시예 14 펩티드 맵핑.<br />
인간 IL-6 상에서 Ab1에 의해 인식되는 에피토프를 결정하기 위하여, 상기 항체가 웨스턴-블롯 기초된 분석에<br />
이용되었다. 본 실시예에서 이용된 인간 IL-6의 형태는 183개 아미노산 길이의 서열(하기에 도시됨)을 보유하였<br />
다. 이러한 서열을 포함하는 중복되는 15개 아미노산 펩티드의 57개-구성원 라이브러리가 상업적으로 합성되었<br />
고 PepSpots 니트로셀룰로오스 막(JPT 펩티드 technologies, Berlin, Germany)에 공유 결합되었다. 중복되는<br />
15개 아미노산 펩티드의 서열은 도 <strong>12</strong>에 도시되고 서열 번호: 590-646에 상응한다. 제조업체의 권고에 따라 블<br />
롯(blot)이 준비되고 탐침되었다.<br />
간단히 말하면, 블롯은 메탄올에서 미리 적셔지고, PBS에서 헹굼되고, 그리고 PBS/0.05% Tween에서 10% 탈지 우<br />
유(차단 용액)에서 2시간 동안 차단되었다. Ab1 항체는 1 ㎎/㎖ 최종 희석도에서 이용되고, 그리고 HRP-접합된<br />
생쥐 항-인간-카파 이차 항체(Southern BioTech #9220-05)는 1:5000 희석도에서 이용되었다. 항체 희석/배양은<br />
차단 용액에서 수행되었다. 블롯은 Amersham ECL advance 시약(GE# RPN2135)을 이용하여 현색되고, 그리고 화학<br />
발광 신호는 CCD 카메라(AlphaInnotec)를 이용하여 기록되었다. 이들 블롯의 결과는 도 13과 도 14에 도시된다.<br />
펩티드 라이브러리를 생성시키는데 이용된 형태의 인간 IL-6 서열은 하기에 열거된다:<br />
VPPGEDSKDVAAPHRQPLTSSERIDKQIRYILDGISALRKETCNKSNMCESSKEALAENNLNLPKMAEKDGCFQSGFNEETCLVKIITGLLEFEVYLEYLQN<br />
RFESSEEQARAVQMSTKVLIQFLQKKAKNLDAITTPDPTTNASLLTKLQAQNQWLQDMTTHLILRSFKEFLQSSLRALRQM (서열 번호: 1).<br />
실시예 15 Ab1은 IL-6에 대한 높은 친화성을 갖는다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
25℃에서, 쥐, 생쥐, 개, 인간, 그리고 필리핀 원숭이로부터 IL-6에 대한 Ab1의 결합 속도(Ka), 분리 속도(Kd)<br />
- <strong>12</strong>3 -
[0828]<br />
[0829]<br />
[0830]<br />
[0831]<br />
[0832]<br />
[0833]<br />
[0834]<br />
[0835]<br />
[0836]<br />
[0837]<br />
및 해리 상수(KD)를 측정하기 위하여 표면 플라즈몬 공명(surface plasmon resonance)이 이용되었다(도 15A).<br />
인간 IL-6에 대한 해리 상수는 4 pM이었는데, 이는 매우 높은 친화성을 지시하였다. 예상된 바와 같이, 친화성<br />
은 일반적으로, 인간으로부터 계통발생적 거리에 비례하여 감소하였다. 필리핀 원숭이, 쥐, 그리고 생쥐의 IL-6<br />
에 대한 Ab1의 해리 상수는 각각, 31 pM, 1.4 nM, 그리고 0.4 nM이었다. 개 IL-6에 대한 Ab1 친화성은 본 실험<br />
의 정량 한계 미만이었다.<br />
생쥐, 쥐, 그리고 필리핀 원숭이 IL-6에 대한 Ab1의 높은 친화성은 Ab1이 이들 종의 IL-6을 저해하는데 이용될<br />
수 있음을 암시한다. 이러한 가설은 세포 증식 분석을 이용하여 시험되었다. 간단히 말하면, T1165 세포의 증식<br />
을 촉진하기 위하여 각 종의 IL-6이 이용되었고, 그리고 Ab1이 50%의 증식을 저해하는 농도(IC50)가<br />
측정되었다. 저해는 측정된 해리 상수와 일치하였다(도 15B). 이들 결과는 Ab1이 이들 종의 본래의 IL-6을 저해<br />
할 수 있음을 증명하고, 그리고 Ab1에 의한 IL-6 저해의 시험관내 또는 생체내 모델링을 위한 이들 생물체의 유<br />
용성을 암시한다.<br />
실시예 16 건강한 인간 지원자에서 항체 Ab1의 복수-투약 약동학적 평가.<br />
항체 Ab1은 히스티딘과 소르비톨에 담겨, 건강한 인간 지원자에 단일 일시 주사로 투약되었다. 1 ㎎, 3 ㎎, 10<br />
㎎, 30 ㎎ 또는 100 ㎎의 용량이 5명 내지 6명 개체를 포함하는 투약 군에서 각 개체에 투여되었다. 혈장 시료<br />
는 최대 <strong>12</strong>주 동안 고정된 시간 간격에서 채취되었다. 인간 혈장은 정맥천자(venipuncture)를 통해, EDTA를 포<br />
함하는 진공 수집 튜브 내로 수집되었다. 혈장은 분리되고 아래와 같이, Ab1에 특이적인 단일클론 항체를 이용<br />
하여 Ab1의 순환 수준을 평가하는데 이용되었다. 96 웰 마이크로역가 평판은 1X PBS에서 4℃에서 하룻밤동안,<br />
Ab1에 특이적인 단일클론 항체로 하룻밤동안 코팅되었다. 나머지 단계는 실온에서 수행되었다. 웰은 흡출되고<br />
1X PBS에서 60분 동안 0.5% 비늘 젤라틴(FSG)(Sigma)을 이용하여 차후에 차단되었다. 이후, 인간 혈장 시료가<br />
첨가되고, 60분 동안 배양되고, 이후 흡출되고, 50 ㎕의 1 ㎍/㎖ 비오틴화된 IL-6이 각 웰에 첨가되고, 그리고<br />
60분 동안 배양되었다. 이들 웰은 흡출되고, 그리고 0.5% FSG/PBS에서 1:5,000 희석된 50 ㎕ 스트렙타비딘-<br />
HRP(Pharmingen)가 첨가되고 45분 동안 배양되었다. 현색은 검출을 위하여 TMB를 이용하는 표준 방법에 의해 수<br />
행되었다. 수준은 이후, 필적하는 형식에서 준비된 표준 곡선에 비교를 통해 결정되었다.<br />
각 투약 군에 대한 Ab1의 평균 혈장 농도 대(對) 시간은 도 16에 도시된다. 평균 AUC와 Cmax는 용량에 비례하여<br />
선형으로 증가하였다(각각, 도 17과 도 18). 30 ㎎ 이상의 용량의 경우에, 각 투약 군에서 평균 Ab1 반감기는<br />
대략 25일 내지 30일이었다(도 <strong>19</strong>).<br />
실시예 17 진행된 암 환자에서 Ab1의 약물동역학.<br />
항체 Ab1은 인산염 완충된 염수에 담겨, 진행된 암을 앓는 5명의 개체에 단일 일시 주사로 투약되었다. 각 개체<br />
는 80 ㎎(n=2) 또는 160 ㎎(n=3) 용량의 Ab1을 섭취하였다. 혈장 시료는 주1회 채취되고, 그리고 항체 Ab1의 수<br />
준은 실시예 16에서처럼 정량되었다.<br />
시간의 함수로서, 이들 개체에서 Ab1의 평균 혈장 농도는 도 20에 도시된다. 평균 Ab1 반감기는 대략 31일이었<br />
다.<br />
실시예 18 Ab1의 선례가 없는 반감기.<br />
전체적으로, Ab1의 평균 반감기는 인간(10 ㎎ 이상의 용량의 경우에)에서 대략 31일이고, 그리고 필리핀 원숭이<br />
에서 대략 15-21일이었다. 인간과 필리핀 원숭이에서 이러한 Ab1 반감기는 다른 항-IL-6 항체의 반감기와 비교<br />
하여 선례가 없다(도 21). 앞서 기술된 바와 같이, Ab1은 토끼 항체의 인간화로부터 유래되고 비당화된 형태로<br />
피치아 파스토리스(Pichia pastoris)에서 생산된다. 이들 특징은 인간에서 매우 낮은 면역원성을 갖는 항체를<br />
발생시킨다. 게다가, 당화의 부재는 Ab1이 Fc 수용체 또는 보체와 상호작용하는 것을 예방한다. 이론에 한정됨<br />
없이, Ab1의 선례가 없는 반감기는 적어도 부분적으로, 인간화 및/또는 당화의 부재에 기인하는 것으로 생각된<br />
다. 항원 결합 표면의 특정 서열 및/또는 구조 역시 Ab1의 반감기에 기여할 수 있다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
실시예 <strong>19</strong> 진행된 암을 앓는 환자에서 헤모글로빈 농도, 혈장 지질 농도, 그리고 호중구 숫자에 대한 Ab1<br />
- <strong>12</strong>4 -
[0838]<br />
[0839]<br />
[0840]<br />
[0841]<br />
[0842]<br />
[0843]<br />
[0844]<br />
[0845]<br />
[0846]<br />
[0847]<br />
[0848]<br />
[0849]<br />
[0850]<br />
효과.<br />
항체 Ab1은 인산염 완충된 염수에 담겨, 진행된 암(NSCLC, 결장직장 암, 담관암, 또는 중피종)을 앓는 8명의 개<br />
체에 단일 일시 주사로 투약되었다. 각 개체는 80 ㎎, 160 ㎎, 또는 320 ㎎ 용량의 Ab1을 섭취하였다. 혈액 시<br />
료는 주사 직전에, 그리고 6주 동안 고정된 시간 간격에서 채취되고, 그리고 헤모글로빈 농도, 혈장 지질 농도,<br />
그리고 호중구 숫자가 측정되었다. 평균 헤모글로빈 농도는 약간 상승하고(도 22), 전체 콜레스테롤과 트리글리<br />
세리드 역시 약간 상승하고(도 23), 반면 평균 호중구 숫자는 약간 하락하였다(도 24).<br />
이들 결과는 만성적으로 아픈 개체에 Ab1의 투여의 유익한 효과 중에서 일부를 더욱 증명한다. IL-6이 만성 질<br />
환의 빈혈(암-관련된 빈혈 포함)의 원인이 되는 주요 사이토킨이기 때문에, Ab1에 의한 IL-6의 중화는 이들 개<br />
체에서 헤모글로빈 농도를 증가시킨다. 유사하게, IL-6이 염증에서 증가하는 호중구 숫자에서 중심적으로 중요<br />
하기 때문에, 호중구 숫자에서 관찰된 약간의 감소는 Ab1이 IL-6을 저해한다는 것을 더욱 확증한다.<br />
최종적으로, IL-6은 이들 환자에서 악액질뿐만 아니라 식욕부진을 유발한다; Ab1에 의한 IL-6의 중화는 식욕의<br />
회복 및 악액질의 반전을 유발한다. 혈장 지질 농도에서 증가는 환자의 개선된 영양 상태를 반영한다.<br />
종합하면, 이들 결과는 Ab1이 이들 환자에서 IL-6의 유해한 결과를 효과적으로 반전시킨다는 것을 더욱 증명한<br />
다.<br />
실시예 20 Ab1은 건강한 지원자 및 진행된 암을 앓는 환자에서 혈청 CRP를 억제한다.<br />
도입<br />
혈청 CRP 농도는 일정한 형태의 암을 앓는 환자에서 강한 예후 지시자로서 확인되었다. 가령, Hashimoto 등은<br />
생존 및 질환 재발에 영향을 주는 인자를 확인하기 위하여, 간세포 암종을 앓는 환자에서 수술전 혈청 CRP 농도<br />
의 단일변량(univariate)과 다변량(multivariate) 분석을 수행하였다(Hashimoto, K., et al., Cancer,<br />
103(9):1856-1864 (2005)). 환자는 2가지 군: 혈청 CRP 수준 > 1.0 ㎎/dL을 갖는 군("CRP 양성 군") 및 혈청<br />
CRP 수준 < 1.0 ㎎/dL을 갖는 군("CRP 음성 군")으로 분류되었다. 이들 저자는 "수술전 혈청 CRP 수준과 종양<br />
크기 사이에 유의한 상관관계"를 확인하였다(Id). 더 나아가, 이들 저자는 "CRP-양성 군에서 전반적인 생존과<br />
재발-없는 생존율이 CRP-음성 군에서 생존율과 비교하여 훨씬 낮다."라는 것을 확인하였다(Id). 이들 저자는 환<br />
자의 수술전 CRP 수준이 독립적이고 간세포 암종을 앓는 환자에서 불량한 예후와 조기 재발의 유의한 예측 지시<br />
자라고 결론하였다.<br />
다른 연구자들에 의해 유사한 상관관계가 확인되었다. 가령, Karakiewicz 등은 혈청 CRP가 독립적이고 신장 세<br />
포 암종-특이적 사망의 유익한 예측자라는 것을 확인하였다(Karakiewicz, P.I., et al., Cancer, 110(6):<strong>12</strong>41-<br />
<strong>12</strong>47 (2007)). 따라서 암 환자, 특히 진행된 암을 앓는 환자에서 혈청 C-반응성 단백질(CRP) 농도를 감소시키는<br />
방법 및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
건강한 지원자는 100 ㎎(5명의 환자), 30 ㎎(5명의 환자), 10 ㎎(6명의 환자), 3 ㎎(6명의 환자) 또는 1 ㎎(6명<br />
의 환자)의 Ab1 단일클론 항체의 단일 1-시간 정맥내(IV) 주사가 투약되고, 반면 다른 14명의 건강한 지원자는<br />
정맥내 위약이 투약되었다. 비교를 위하여, 진행된 형태의 결장직장 암을 앓는 2명의 환자는 80 ㎎의 Ab1 단일<br />
클론 항체의 단일 1-시간 정맥내(IV) 주사가 투약되었다. Ab1 단일클론 항체의 다른 용량은 상기 검사 집단에<br />
투여되지 않았다.<br />
환자는 투약 이전에, 그리고 투약후 적어도 5주 동안 주1회 평가되었다. 각 평가의 시점에서, 환자는 혈청 CRP<br />
농도에 대하여 스크리닝되었다.<br />
결과<br />
건강한 지원자<br />
공개특허 10-2011-01<strong>12</strong>308<br />
앞서 언급된 바와 같이, 혈청 CRP 수준은 염증의 마커이다; 따라서 기준선 CRP 수준은 전형적으로, 건강한 개체<br />
에서 낮다. 이러한 낮은 기준선 CRP 수준은 CRP 수준에서 추가의 감소를 검출하기 어렵게 만들 수 있다. 그럼에<br />
도 불구하고, 혈청 CRP 농도에서 실질적인 감소는 대조와 비교하여, 모든 농도의 Ab1 단일클론 항체를 섭취하는<br />
건강한 지원자에서 검출가능하였다(도 25). 혈청 CRP 수준에서 감소는 급속하고, 항체 투여후 1주 이내에 발생<br />
- <strong>12</strong>5 -
[0851]<br />
[0852]<br />
[0853]<br />
[0854]<br />
[0855]<br />
[0856]<br />
[0857]<br />
[0858]<br />
[0859]<br />
[0860]<br />
[0861]<br />
[0862]<br />
[0863]<br />
[0864]<br />
[0865]<br />
[0866]<br />
[0867]<br />
하고, 그리고 연장된 점감된 수준은 적어도 최종 측정이 수행될 때(항체 투여후 8 또는 <strong>12</strong>주)까지 지속되었다.<br />
암 환자<br />
상승된 혈청 CRP 수준을 갖는 5명의 진행된 암 환자(결장직장 암, 담관암, 또는 NSCLC)는 80 ㎎ 또는 160 ㎎의<br />
Ab1가 투약되었다. 혈청 CRP 수준은 이들 환자에서 매우 감소하였다(도 26A). 혈청 CRP 수준에서 감소는 급속하<br />
고, 90%의 감소가 Ab1 투여후 1주 이내에 발생하고, 그리고 연장된 점감된 수준은 적어도 최종 측정이 수행될<br />
때(최대 <strong>12</strong>주)까지 지속되었다. 2명의 대표적인 개체의 CRP 수준이 도 26B에 도시된다. 이들 개체에서, CRP 수<br />
준은 1주 이내에 정상 참고 범위(5 - 6 ㎎/ℓ 이하) 미만으로 하락하였다. 따라서 진행된 암 환자에 Ab1의 투여<br />
는 혈청 CRP 수준의 급속하고 지속된 억제를 유발할 수 있다.<br />
실시예 21 진행된 암을 앓는 환자에서 Ab1 개선된 근력, 개선된 체중, 그리고 감소된 피로<br />
도입<br />
체중 감소와 피로(여기에 동반된 근육 쇠약)는 진행된 형태의 암을 앓는 환자의 매우 공통적인 증상이고, 그리<br />
고 이들 증상은 암이 계속 진행됨에 따라 악화될 수 있다. 피로, 체중 감소 및 근육 쇠약은 예로써 생활방식과<br />
인간관계를 파괴함으로써, 그리고 암 치료를 지속하는 환자의 의지 또는 능력에 영향을 줌으로써 진행된 형태의<br />
암을 앓는 환자의 회복에 현저한 부정적인 영향을 줄 수 있다. 피로, 체중 감소와 근육 쇠약을 해결하는 공지된<br />
방법에는 체력과 운동의 규칙적인 일과, 환자의 활동력을 보존하는 방법, 그리고 빈혈-유도된 피로와 근육 쇠약<br />
을 해결하는 치료가 포함된다. 그럼에도 불구하고, 암 환자에서 피로, 체중 감소와 근육 쇠약을 개선하는 방법<br />
및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
진행된 형태의 암을 앓는 4명의 환자(결장직장 암(2), NSCLC(1), 담관암(1))는 80 ㎎ 또는 160 ㎎의 Ab1 단일클<br />
론 항체의 단일 1-시간 정맥내(IV) 주사가 투약되었다. Ab1 단일클론 항체의 다른 용량은 상기 검사 집단에 투<br />
여되지 않았다.<br />
환자는 투약 이전에, 그리고 투약후 적어도 6주 동안 평가되었다. 각 평가의 시점에서, 환자는 아래에 대하여<br />
스크리닝되었다: a.) 체중에서 변화; b.) 피로를 평가하기 위한 의학적으로 인정된 검사법인 Facit-F 피로 하위<br />
척도 조사표를 이용하여 측정된 피로(참조: Cella, D., Lai, J.S., Chang, C.H., Peterman, A., & Slavin, M.<br />
(2002). Fatigue in cancer patients compared with fatigue in the general population. Cancer, 94(2),<br />
528-538; Cella, D., Eton, D.T., Lai,F J-S., Peterman, A.H & Merkel, D.E. (2002). Combining anchor and<br />
distribution based methods to derive minimal clinically important differences on the Functional<br />
Assessment of Cancer Therapy anemia and fatigue scales. Journal of Pain & Symptom Management, 24 (6)<br />
547-561.); 그리고 손-악력(전형적으로 악력계를 이용하여 근력을 평가하기 위한 의학적으로 인정된 검사법).<br />
결과<br />
체중 변화<br />
Ab1 단일클론 항체의 양쪽 투약 농도(80 ㎎과 160 ㎎)에 대한 평균화된 데이터는 6주 기간 동안 환자당 대략 2<br />
㎏의 체중 증가를 증명하였다(도 29).<br />
피로<br />
Ab1 단일클론 항체의 양쪽 투약 농도(80 ㎎과 160 ㎎)에 대한 평균화된 데이터는 6주 기간 동안 환자 집단에서<br />
적어도 대략 10 점의 평균 Facit-F FS 하위척도 점수에서 증가를 증명하였다(도 30).<br />
손-악력<br />
Ab1 단일클론 항체의 양쪽 투약 농도(80 ㎎과 160 ㎎)에 대한 평균화된 데이터는 6주 기간 동안 환자 집단에서<br />
적어도 대략 10%의 평균 손-악력에서 증가를 증명하였다(도 31).<br />
실시예 22 혈전증의 예방을 위한 Ab1<br />
공개특허 10-2011-01<strong>12</strong>308<br />
이전 연구에서, 항-IL-6 항체의 투여가 감소된 혈소판 수를 유발할 수 있는 것으로 밝혀졌다(Emilie, D. et<br />
- <strong>12</strong>6 -
[0868]<br />
[0869]<br />
[0870]<br />
[0871]<br />
[0872]<br />
[0873]<br />
[0874]<br />
[0875]<br />
[0876]<br />
[0877]<br />
[0878]<br />
[0879]<br />
al., Blood, 84(8):2472-9 (<strong>19</strong>94); Blay et al., Int JCancer, 72(3):424-30 (<strong>19</strong>97)). 이들 결과는 명백하게,<br />
잠재적 위험의 지시자로서 간주되었는데, 그 이유는 혈소판 수에서 추가의 감소가 출혈과 같은 합병증을 유발할<br />
수 있기 때문이다. 하지만, 출원인은 IL-6의 저해가 정상적인 혈액응고 프로필을 복원한다는 것을 인식하고, 이<br />
것이 혈전증을 예방할 것으로 예측한다. IL-6의 저해에 기인하는 감소된 혈소판 수는 잠재적 위험의 징후가 아<br />
니며, 정상적인 혈액응고의 유익한 복원을 반영한다.<br />
정상적인 혈액응고가 복원되는 기전은 IL-6 및 급성기 반응 사이에 상호작용에 기인하는 것으로 생각된다. 예로<br />
써, 암 환자에서처럼 상승된 IL-6 수준에 응하여, 간은 급성기 단백질을 생산한다. 이들 급성기 단백질에는 혈<br />
액응고 인자, 예를 들면, 인자 II, 인자 V, 인자 VIII, 인자 IX, 인자 XI, 인자 XII, F/피브린 분해 산물, 트롬<br />
빈-항트롬빈 III 복합체, 피브리노겐, 플라스미노겐, 프로트롬빈, 그리고 폰 빌레브란드 인자가 포함된다. 혈액<br />
응고 인자에서 이러한 증가는 직접적으로 측정되거나, 또는 응고 능력의 기능적 측정으로부터 추론될 수 있다.<br />
IL-6의 길항제, 예를 들면, Ab1은 급성기 단백질, 예를 들면, 혈청 아밀로이드 A를 억제한다(도 32 및 실시예<br />
10 참조). 출원인은 급성기 단백질의 이러한 억제가 정상적인 혈액응고 프로필을 복원하고, 따라서 혈전증을 예<br />
방할 것으로 예측한다. 정상적인 혈액응고의 복원은 혈소판 수에서 약간 감소를 유발할 수 있지만, 그럼에도 불<br />
구하고 환자는 정상적인 혈액응고 능력을 유지하고, 따라서 출혈의 증가된 위험에 노출되지 않을 것이다. 이런<br />
치료는 유용성이 유해한 부작용, 예를 들면, 대량 출혈의 위험에 의해 제한되는 현재 가용한 항혈액응고 요법에<br />
비하여 현저한 개선을 대표할 것이다.<br />
출원인은 IL-6을 저해하는 동일한 유익한 효과가 저해 방법에 상관없이 획득될 것이라고 고려한다. IL-6을 저해<br />
하는 적절한 방법에는 개별적으로 또는 조합으로, 항-IL-6 항체, 안티센스 요법, 가용성 IL-6 수용체 등의 투여<br />
가 포함된다.<br />
실시예 23 Ab1은 진행된 암을 앓는 환자에서 혈장 알부민 농도를 증가시킨다.<br />
도입<br />
혈청 알부민 농도는 암 환자의 생존 및/또는 회복 성공의 예측 지시자로서 인정된다. 저알부민혈증은 다양한 형<br />
태의 암에서 불량한 환자 성과와 강하게 상관된다. 가령, 한 연구에서, 전이성 췌장 선암종에 대한 전신 화학요<br />
법을 받고 있고 3.5 g/dL 이하의 혈청 알부민 수준을 갖는 어떤 환자도 전신 화학요법에 성공적으로 반응하지<br />
않았다(Fujishiro, M., et al., Hepatogastroenterology, 47(36):1744-46 (2000)). 이들 저자는 "… 저알부민<br />
혈증 …을 앓는 환자가 전신 화학요법의 후보로서 적합하지 않고 다른 실험적 접근법 또는 지지 간호로 치료될<br />
수도 있을 것이다."라고 결론한다(Id).<br />
유사하게, Senior와 Maroni는 "저알부민혈증이 최종-단계 신장 질환에서 사망의 가장 강력한 예언자라는 최근의<br />
판단은 이러한 환자 집단에서 적절한 단백질 섭취를 담보하는 것의 결정적인 중요성을 강조한다."라고 주장한다<br />
(J.R. Senior and B.J. Maroni, Am. Soc. Nutr. Sci., <strong>12</strong>9:313S-314S (<strong>19</strong>99)).<br />
적어도 하나의 연구에서, 정상적인 혈청 알부민 수준(>3.5 g/dL)이 달성될 때까지 20 g의 매일 정맥내 알부민<br />
주사로 27명의 전이성 암 환자에서 저알부민혈증을 교정하려는 시도는 성공하지 못하였다. 이들 저자는 "진행된<br />
단계 암 환자에 대한 알부민 주사는 임상적 실시에서 제한적 가치를 갖는다. PS 4와 저알부민혈증을 앓는 환자<br />
는 더욱 불량한 예후를 갖는다."라고 강조한다(Demirkazik, A., et al., Proc. Am. Soc. Clin. Oncol.,<br />
21:Abstr 2892 (2002)).<br />
따라서 암 환자에서 혈청 알부민 농도를 개선하고 암 환자, 특히 진행된 암 환자에서 저알부민혈증 상태를 해결<br />
하는 방법 및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
진행된 형태의 암을 앓는 4명의 환자(결장직장 암(2), NSCLC(1), 담관암(1))는 80 ㎎ 또는 160 ㎎의 Ab1 단일클<br />
론 항체의 단일 1-시간 정맥내(IV) 주사가 투약되었다. Ab1 단일클론 항체의 다른 용량은 상기 검사 집단에 투<br />
여되지 않았다.<br />
환자는 투약 이전에, 그리고 투약후 적어도 6주 동안 평가되었다. 각 평가의 시점에서, 환자는 혈장 알부민 농<br />
도에 대하여 스크리닝되었다.<br />
결과<br />
- <strong>12</strong>7 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0880]<br />
[0881]<br />
[0882]<br />
[0883]<br />
[0884]<br />
[0885]<br />
[0886]<br />
[0887]<br />
[0888]<br />
[0889]<br />
[0890]<br />
[0891]<br />
[0892]<br />
Ab1 단일클론 항체의 양쪽 투약 농도(80 ㎎과 160 ㎎)에 대한 평균화된 데이터는 6주 기간 동안 환자당 대략 5<br />
g/ℓ의 혈장 알부민 농도의 증가를 증명하였다(도 33).<br />
실시예 24 Ab1은 진행된 암을 앓는 환자에서 혈청 CRP를 억제한다.<br />
도입<br />
혈청 CRP 농도는 일정한 형태의 암을 앓는 환자에서 강한 예후 지시자로서 확인되었다. 가령, Hashimoto 등은<br />
생존과 질환 재발에 영향을 주는 인자를 확인하기 위하여 간세포 암종을 앓는 환자에서 수술전 혈청 CRP 농도의<br />
단일변량(univariate)과 다변량(multivariate) 분석을 수행하였다(Hashimoto, K., et al., Cancer,<br />
103(9):1856-1864 (2005)). 환자는 2가지 군: 혈청 CRP 수준 > 1.0 ㎎/dL을 갖는 군("CRP 양성 군") 및 혈청<br />
CRP 수준 < 1.0 ㎎/dL을 갖는 군("CRP 음성 군")으로 분류되었다. 이들 저자는 "수술전 혈청 CRP 수준과 종양<br />
크기 사이에 유의한 상관관계"를 확인하였다(Id). 더 나아가, 이들 저자는 "CRP-양성 군에서 전반적인 생존과<br />
재발-없는 생존율이 CRP-음성 군에서 생존율과 비교하여 훨씬 낮다."라는 것을 확인하였다(Id). 이들 저자는 환<br />
자의 수술전 CRP 수준이 독립적이고 간세포 암종을 앓는 환자에서 불량한 예후와 조기 재발의 유의한 예측 지시<br />
자라고 결론하였다.<br />
다른 연구자들에 의해 유사한 상관관계가 확인되었다. 가령, Karakiewicz 등은 혈청 CRP가 독립적이고 신장 세<br />
포 암종-특이적 사망의 유익한 예측자라는 것을 확인하였다(Karakiewicz, P.I., et al., Cancer, 110(6):<strong>12</strong>41-<br />
<strong>12</strong>47 (2007)). 따라서 암 환자, 특히 진행된 암을 앓는 환자에서 혈청 C-반응성 단백질(CRP) 농도를 감소시키는<br />
방법 및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
비-소세포 폐암(NSCLC)을 앓는 <strong>12</strong>4명의 환자는 4가지 치료 군으로 분할되었다. 하나의 군에서 환자는 총 3회 투<br />
약을 위하여 24주 기간 동안 8주마다 위약(n=31), 80 ㎎(n=29), 160 ㎎(n=32), 또는 320 ㎎(n=32)의 Ab1 단일<br />
클론 항체의 1-시간 정맥내(IV) 주사가 투약되었다. CRP 농도는 라텍스-부착된 항-CRP 항체(즉, Roche CRP<br />
Tinaquant<br />
)를 이용한 C-반응성 단백질 입자-증대된 면역비탁법에 의해 정량되었다. 간단히 말하면, 대략 1.0 ㎖의 환자<br />
시료 혈청이 수집되고 플라스틱 수집 튜브에서 보관되었다. 시료는 적절한 완충액 내로 배치되고, 그리고 반응<br />
을 시작시키기 위하여 라텍스 미세입자에 결합된 항-CRP 항체가 상기 시료에 첨가되었다. 접합된 라텍스 미세입<br />
자를 보유하는 이들 항-CRP 항체는 시료 내에서 항원과 반응하여 항원/항체 복합체를 형성한다. 응집 이후에,<br />
이는 Roche/Hitachi Modular P 검광자를 이용하여 혼탁도에 대하여 측정되었다.<br />
환자는 투약 이전에, 그리고 투약후 2, 4, 8과 <strong>12</strong>주 시점에 평가되었다. 각 평가 시점에서, 환자는 혈청 CRP 농<br />
도에 대하여 스크리닝되었다.<br />
결과<br />
Ab1 단일클론 항체의 각 투약 농도(위약, 80 ㎎, 160 ㎎, 그리고 320 ㎎)에 대한 평균화된 데이터는 도 38에 플<br />
롯팅된다. 모든 용량 수준의 Ab1 항체는 <strong>12</strong>주 기간 동안 위약에 비하여 CRP 농도에서 즉시 하락을 나타냈다.<br />
CRP 수준은 투약후 8주 시점에 돌파구를 보였다. CRP 수준은 <strong>12</strong>주 시점에 5 ㎎/ℓ 미만으로 하락하였다. CRP의<br />
중앙 값은 위약에 비하여 모든 투약 농도에 대한 급속하고 지속된 감소를 나타냈다(도 39). 따라서 진행된 암<br />
환자에 Ab1의 투여는 혈청 CRP 수준의 급속하고 지속된 억제를 유발할 수 있다.<br />
실시예 25 Ab1은 진행된 암을 앓는 환자에서 혈청 CRP를 억제한다.<br />
도입<br />
공개특허 10-2011-01<strong>12</strong>308<br />
혈청 CRP 농도는 일정한 형태의 암을 앓는 환자에서 강한 예후 지시자로서 확인되었다. 가령, Hashimoto 등은<br />
생존과 질환 재발에 영향을 주는 인자를 확인하기 위하여 간세포 암종을 앓는 환자에서 수술전 혈청 CRP 농도의<br />
단일변량(univariate)과 다변량(multivariate) 분석을 수행하였다(Hashimoto, K., et al., Cancer,<br />
103(9):1856-1864 (2005)). 환자는 2가지 군: 혈청 CRP 수준 > 1.0 ㎎/dL을 갖는 군("CRP 양성 군") 및 혈청<br />
CRP 수준 < 1.0 ㎎/dL을 갖는 군("CRP 음성 군")으로 분류되었다. 이들 저자는 "수술전 혈청 CRP 수준과 종양<br />
- <strong>12</strong>8 -
[0893]<br />
[0894]<br />
[0895]<br />
[0896]<br />
[0897]<br />
[0898]<br />
[0899]<br />
[0900]<br />
[0901]<br />
[0902]<br />
[0903]<br />
크기 사이에 유의한 상관관계"를 확인하였다(Id). 더 나아가, 이들 저자는 "CRP-양성 군에서 전반적인 생존과<br />
재발-없는 생존율이 CRP-음성 군에서 생존율과 비교하여 훨씬 낮다."라는 것을 확인하였다(Id). 이들 저자는 환<br />
자의 수술전 CRP 수준이 독립적이고 간세포 암종을 앓는 환자에서 불량한 예후와 조기 재발의 유의한 예측 지시<br />
자라고 결론하였다.<br />
다른 연구자들에 의해 유사한 상관관계가 확인되었다. 가령, Karakiewicz 등은 혈청 CRP가 독립적이고 신장 세<br />
포 암종-특이적 사망의 유익한 예측자라는 것을 확인하였다(Karakiewicz, P.I., et al., Cancer, 110(6):<strong>12</strong>41-<br />
<strong>12</strong>47 (2007)). 따라서 암 환자, 특히 진행된 암을 앓는 환자에서 혈청 C-반응성 단백질(CRP) 농도를 감소시키는<br />
방법 및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
다양한 형태의 진행된 암을 앓는 8명의 환자(결장직장암(3), NSCLC(1), 담관암(1), 그리고 중피종(2))는 80 ㎎<br />
(2명의 환자), 160 ㎎(3명의 환자) 또는 320 ㎎(3명의 환자)의 Ab1 단일클론 항체의 단일 1-시간 정맥내 주사가<br />
투약되었다. Ab1 단일클론 항체의 다른 용량은 상기 검사 집단에 투여되지 않았다.<br />
환자는 투약 이전에, 그리고 투약후 적어도 8주 동안 주1회 평가되었다. 각 평가 시점에서, 환자는 혈청 CRP 농<br />
도에 대하여 스크리닝되었다. CRP 농도는 라텍스-부착된 항-CRP 항체(즉, Roche CRP Tinaquant<br />
)를 이용한 C-반응성 단백질 입자-증대된 면역비탁법에 의해 정량되었다. 간단히 말하면, 대략 1.0 ㎖의 환자<br />
시료 혈청이 수집되고 플라스틱 수집 튜브에서 보관되었다. 시료는 적절한 완충액 내로 배치되고, 그리고 반응<br />
을 시작시키기 위하여 라텍스 미세입자에 결합된 항-CRP 항체가 상기 시료에 첨가되었다. 접합된 라텍스 미세입<br />
자를 보유하는 이들 항-CRP 항체는 시료 내에서 항원과 반응하여 항원/항체 복합체를 형성한다. 응집 이후에,<br />
이는 Roche/Hitachi Modular P 검광자를 이용하여 혼탁도에 대하여 측정되었다.<br />
결과<br />
혈청 CRP 수준은 조사된 모든 환자에서 상당히 감소하였다(도 40). 혈청 CRP 수준에서 감소는 급속하고, 이러한<br />
감소의 대략 90%가 Ab1 투여후 1주 이내에 발생하고, 그리고 연장된 점감된 수준이 적어도 최종 측정이 수행될<br />
때(최대 <strong>12</strong>주)까지 지속되었다. 결장직장 암을 앓는 1명의 환자를 제외하고 모든 사례에서, CRP 수준은 1주 이<br />
내에 정상 참고 범위(5-6 ㎎/ℓ이하) 이하로 하락하였다. 상기 결장직장 암 환자는 본 연구의 4주 시점에 유사<br />
한 정상적인 수준을 달성하였다. 따라서 진행된 암 환자에 Ab1의 투여는 혈청 CRP 수준의 급속하고 지속된 억제<br />
를 유발할 수 있다.<br />
실시예 26 Ab1은 류머티스성 관절염을 앓는 환자에서 혈청 CRP를 억제한다.<br />
도입<br />
혈청 CRP 농도는 류머티스성 관절염을 앓는 환자에서 강한 예후 지시자로서 확인되었다. 높은 수준의 CRP를 갖<br />
는 류머티스성 관절염을 앓는 환자는 거의 보편적인 악화를 보였다(Amos et al., 1 Br. Med. J. <strong>19</strong>5-97<br />
(<strong>19</strong>77)). 반대로, 낮은 CRP 수준을 갖는 환자는 질환 진행을 보이지 않았는데, 이는 류머티스성 관절염을 효과<br />
적으로 치료하기 위하여 낮은 수준의 CRP를 유지하는 것이 필요하다는 것을 암시하였다(Id). 금, D-페니실아민,<br />
클로로퀸, 또는 댑손의 류머티스성 관절염 치료 섭생 동안 CRP의 추적은 CRP 수준이 지속적으로 통제될 때, 첫<br />
6개월의 치료후 방사선학적 악화가 저해된다는 것을 지시하였다(Dawes et al., 25 Rheumatology 44-49<br />
(<strong>19</strong>86)). CRP 생산과 방사선학적 진행 간에 고도로 유의한 상관관계가 확인되었다(van Leeuwen et al., 32<br />
(Supp. 3) Rheumatology 9-13 (<strong>19</strong>97). 다른 연구에서, 활성 류머티스성 관절염을 앓는 환자의 경우에, 비정상<br />
적으로 상승된 CRP의 억제는 기능적 검사 측정규준에서 개선을 유발하는 반면, 지속된 CRP 상승은 동일한 측정<br />
규준에서 악화와 연관되는 것으로 밝혀졌다(Devlin et al., 24 J. Rheumatol. 9-13 (<strong>19</strong>97)). CRP 재-상승이 없<br />
으면 추가의 악화는 관찰되지 않았는데, 이는 류머티스성 관절염 치료에 대한 실용적인 후보로서 CRP 억제를 지<br />
시하였다(Id). 따라서 류머티스성 관절염 환자에서 혈청 C-반응성 단백질(CRP) 농도를 감소시키는 방법 및/또는<br />
치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
공개특허 10-2011-01<strong>12</strong>308<br />
활성 류머티스성 관절염을 앓고 CRP ≥10 ㎎/ℓ를 갖는 <strong>12</strong>7명의 환자는 4가지 치료 군으로 분할되었다. 하나의<br />
군에서 환자는 16주 시험의 시작 시점에 한 번, 그리고 8주 시점에 다시 한 번, 위약(n=33), 80 ㎎(n=32), 160<br />
- <strong>12</strong>9 -
[0904]<br />
[0905]<br />
[0906]<br />
[0907]<br />
[0908]<br />
[0909]<br />
[0910]<br />
[0911]<br />
[09<strong>12</strong>]<br />
[0913]<br />
[0914]<br />
[0915]<br />
[0916]<br />
㎎(n=34), 또는 320 ㎎(n=28)의 Ab1 단일클론 항체의 1-시간 정맥내(IV) 주사가 투약되었다. CRP 농도는 라텍스<br />
-부착된 항-CRP 항체(즉, Roche CRP Tinaquant<br />
)를 이용한 C-반응성 단백질 입자-증대된 면역비탁법에 의해 정량되었다. 간단히 말하면, 대략 1.0 ㎖의 환자<br />
시료 혈청이 수집되고 플라스틱 수집 튜브에서 보관되었다. 시료는 적절한 완충액 내로 배치되고, 그리고 반응<br />
을 시작시키기 위하여 라텍스 미세입자에 결합된 항-CRP 항체가 상기 시료에 첨가되었다. 접합된 라텍스 미세입<br />
자를 보유하는 이들 항-CRP 항체는 시료 내에서 항원과 반응하여 항원/항체 복합체를 형성한다. 응집 이후에,<br />
이는 Roche/Hitachi Modular P 검광자를 이용하여 혼탁도에 대하여 측정되었다. CRP 농도에 관한 데이터는 첫4<br />
주 동안 매주, 4주와 <strong>12</strong>주 사이에 격주, 그리고 16주에서 시험의 종결 시점에서 수집되었다.<br />
결과<br />
혈청 CRP 수준은 조사된 모든 환자에서 상당히 감소하였다(도 41). 혈청 CRP 수준에서 감소는 Ab1 투여후 1주<br />
이내에 위약에 비하여 CRP 수준의 즉시 감소로 급속하고, 그리고 연장된 점감된 수준은 적어도 최종 측정이 수<br />
행될 때(최대 16주)까지 지속되었다. 모든 사례에서, CRP 수준이 1주 이내에 정상 참고 범위(5-6 ㎎/ℓ 이하)<br />
이하로 하락하였다. 따라서 류머티스성 관절염 환자에 Ab1의 투여는 혈청 CRP 수준의 급속하고 지속된 억제를<br />
유발할 수 있고 효과적인 치료 섭생을 제공한다.<br />
실시예 27 Ab1은 진행된 암을 앓는 환자에서 헤모글로빈을 증가시킨다.<br />
항체 Ab1은 인산염 완충된 염수에서 80 ㎎, 160 ㎎, 또는 320 ㎎이 비-소세포 폐 암종을 앓는 93명의 개체에 투<br />
약되었다. 비-소세포 폐 암종을 앓는 31명 개체의 위약 군은 인산염 완충된 염수만 투약되었다. 혈액 시료는 투<br />
약 직전(0주)에, 그리고 투약후 2, 4, 8과 <strong>12</strong>주 시점에 채취되고, 그리고 헤모글로빈 농도가 측정되었다. 평균<br />
헤모글로빈 농도는 항체 Ab1을 섭취하는 개체에서 상승하는 반면, 위약을 섭취하는 개체의 평균 헤모글로빈 농<br />
도는 투약 직전(0주)에 농도와 비교할 때 <strong>12</strong>주후 상승하지 않았다(도 42와 43).<br />
상기 집단의 부분집합은 11 g/ℓ 미만의 기준선 헤모글로빈 농도로서 정의된, 낮은 수준의 헤모글로빈으로 연구<br />
를 시작하였다. 평균 헤모글로빈 농도는 160 ㎎과 320 ㎎의 용량에서 항체 Ab1을 섭취하는 개체에서 8주후 11<br />
g/ℓ를 초과하여 상승하는 반면, 80 ㎎의 용량에서 항체 Ab1 또는 위약을 섭취하는 개체의 평균 헤모글로빈 농<br />
도는 8주후 11 g/ℓ를 초과하여 상승하지 못하였다(도 44).<br />
이들 결과는 만성적으로 아픈 개체에 Ab1의 투여의 유익한 효과 중에서 일부를 더욱 증명한다. IL-6이 만성 질<br />
환의 빈혈(암-관련된 빈혈 포함)의 원인이 되는 주요 사이토킨이기 때문에, Ab1에 의한 IL-6의 중화는 이들 개<br />
체에서 헤모글로빈 농도를 증가시킨다.<br />
실시예 28 Ab1은 류머티스성 관절염을 앓는 환자에서 헤모글로빈을 증가시킨다.<br />
헤모글로빈 수준은 Ab1 항체로 치료 동안 류머티스성 관절염을 앓는 환자에서 분석되었다. Ab1 항체는 인산염<br />
완충된 염수에서 80 ㎎, 160 ㎎, 또는 320 ㎎이 류머티스성 관절염을 앓는 94명의 개체에 투약되었다. 류머티스<br />
성 관절염을 앓는 33명 개체의 위약 군은 인산염 완충된 염수만 투약되었다. 혈액 시료는 투약 직전(0주)에, 그<br />
리고 투약후 1, 2, 3, 4, 6, 8, 10, <strong>12</strong>와 16주 시점에 채취되고, 그리고 헤모글로빈 농도가 측정되었다. 평균<br />
헤모글로빈 농도는 항체 Ab1을 섭취하는 개체에서 상승하는 반면, 위약을 섭취하는 개체의 평균 헤모글로빈 농<br />
도는 투약 직전(0주)에 농도와 비교할 때 16주후 뚜렷하게 상승하지 못하였다(도 45).<br />
이들 결과는 만성적으로 아픈 개체에 Ab1의 투여의 유익한 효과 중에서 일부를 더욱 증명한다. IL-6이 만성 질<br />
환의 빈혈(암-관련된 빈혈 포함)의 원인이 되는 주요 사이토킨이기 때문에, Ab1에 의한 IL-6의 중화는 이들 개<br />
체에서 헤모글로빈 농도를 증가시킨다.<br />
실시예 29 Ab1은 진행된 암을 앓는 환자에서 알부민을 증가시킨다.<br />
도입<br />
공개특허 10-2011-01<strong>12</strong>308<br />
혈청 알부민 농도는 암 환자의 생존 및/또는 회복 성공의 예측 지시자로서 인정된다. 저알부민혈증은 다양한 형<br />
태의 암에서 불량한 환자 성과와 강하게 상관된다. 가령, 한 연구에서, 전이성 췌장 선암종에 대한 전신 화학요<br />
- 130 -
[0917]<br />
[0918]<br />
[09<strong>19</strong>]<br />
[0920]<br />
[0921]<br />
[0922]<br />
[0923]<br />
[0924]<br />
[0925]<br />
[0926]<br />
[0927]<br />
[0928]<br />
[0929]<br />
[0930]<br />
법을 받고 있고 3.5 g/dL 이하의 혈청 알부민 수준을 갖는 어떤 환자도 전신 화학요법에 성공적으로 반응하지<br />
않았다(Fujishiro, M., et al., Hepatogastroenterology, 47(36):1744-46 (2000)). 이들 저자는 "… 저알부민<br />
혈증 …을 앓는 환자가 전신 화학요법의 후보로서 적합하지 않고 다른 실험적 접근법 또는 지지 간호로 치료될<br />
수도 있을 것이다."라고 결론한다(Id).<br />
유사하게, Senior와 Maroni는 "저알부민혈증이 최종-단계 신장 질환에서 사망의 가장 강력한 예언자라는 최근의<br />
판단은 이러한 환자 집단에서 적절한 단백질 섭취를 담보하는 것의 결정적인 중요성을 강조한다."라고 주장한다<br />
(J.R. Senior and B.J. Maroni, Am. Soc. Nutr. Sci., <strong>12</strong>9:313S-314S (<strong>19</strong>99)).<br />
적어도 하나의 연구에서, 정상적인 혈청 알부민 수준(>3.5 g/dL)이 달성될 때까지 20 g의 매일 정맥내 알부민<br />
주사로 27명의 전이성 암 환자에서 저알부민혈증을 교정하려는 시도는 성공하지 못하였다. 이들 저자는 "진행된<br />
단계 암 환자에 대한 알부민 주사는 임상적 실시에서 제한적 가치를 갖는다. PS 4와 저알부민혈증을 앓는 환자<br />
는 더욱 불량한 예후를 갖는다."라고 강조한다(Demirkazik, A., et al., Proc. Am. Soc. Clin. Oncol.,<br />
21:Abstr 2892 (2002)).<br />
따라서 암 환자에서 혈청 알부민 농도를 개선하고 암 환자, 특히 진행된 암 환자에서 저알부민혈증 상태를 해결<br />
하는 방법 및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
항체 Ab1은 인산염 완충된 염수에서 80 ㎎, 160 ㎎, 또는 320 ㎎이 비-소세포 폐 암종을 앓는 93명의 개체에 투<br />
약되었다. 비-소세포 폐 암종을 앓는 31명 개체의 위약 군은 인산염 완충된 염수만 투약되었다. 혈액 시료는 투<br />
약 직전(0주)에, 그리고 투약후 2, 4, 8과 <strong>12</strong>주 시점에 채취되고, 그리고 알부민 농도가 측정되었다.<br />
결과<br />
평균 알부민 농도는 항체 Ab1을 섭취하는 개체에서 상승하는 반면, 위약을 섭취하는 개체의 평균 알부민 농도는<br />
투약 직전(0주)에 농도와 비교할 때 <strong>12</strong>주후 상승하지 않았다(도 46). 모든 투약 농도 군에 대한 기준선 알부민<br />
값으로부터 변화는 도 47에 플롯팅된다.<br />
상기 연구 집단의 부분집합은 35 g/ℓ 이하의 기준선 알부민 농도로서 정의되는 낮은 수준의 알부민으로 연구를<br />
시작하였다. 평균 알부민 농도는 초기에, 위약에 비하여 모든 용량의 항체 Ab1로 상승하지만, 160 ㎎ 또는 320<br />
㎎을 섭취하는 환자만 8주 연구 기간 동안 35 g/ℓ를 초과하는 지속된 알부민 수준을 보였다(도 48). 80 ㎎ 용<br />
량 군에서 알부민 수준은 최초 증가를 보이긴 하지만, 2주후 점진적으로 감소하고 데이터가 가용한 8주 동안 35<br />
g/ℓ를 초과하여 상승하지 못하였다(Id.).<br />
실시예 30 Ab1은 진행된 암을 앓는 환자에서 체중을 증가시키고 피로를 감소시켰다.<br />
도입<br />
체중 감소와 피로는 진행된 형태의 암을 앓는 환자의 매우 공통적인 증상이고, 그리고 이들 증상은 암이 계속<br />
진행됨에 따라 악화될 수 있다. 피로와 체중 감소는 예로써 생활방식과 인간관계를 파괴함으로써, 그리고 암 치<br />
료를 지속하는 환자의 의지 또는 능력에 영향을 줌으로써 진행된 형태의 암을 앓는 환자의 회복에 현저한 부정<br />
적인 영향을 줄 수 있다. 피로와 체중 감소를 해결하는 공지된 방법에는 체력과 운동의 규칙적인 일과, 환자의<br />
활동력을 보존하는 방법, 그리고 빈혈-유도된 피로를 해결하는 치료가 포함된다. 그럼에도 불구하고, 암 환자에<br />
서 피로와 체중 감소를 개선하는 방법 및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
비-소세포 폐암(NSCLC)을 앓는 <strong>12</strong>4명의 환자는 4가지 치료 군으로 분할되었다. 하나의 군에서 환자는 총 3회 투<br />
약을 위하여 24주 기간 동안 8주마다 위약(n=31), 80 ㎎(n=29), 160 ㎎(n=32), 또는 320 ㎎(n=32)의 Ab1 단일<br />
클론 항체의 1-시간 정맥내(IV) 주사가 투약되었다.<br />
공개특허 10-2011-01<strong>12</strong>308<br />
환자는 투약 이전에, 그리고 투약후 적어도 <strong>12</strong>주 동안 평가되었다. 각 평가의 시점에서, 환자는 아래에 대하여<br />
스크리닝되었다: a.) 체중에서 변화; 그리고 b.) 피로를 평가하기 위한 의학적으로 인정된 검사법인 Facit-F 피<br />
로 하위척도 조사표를 이용하여 측정된 피로(참조: Cella, D., Lai, J.S., Chang, C.H., Peterman, A., &<br />
Slavin, M. (2002). Fatigue in cancer patients compared with fatigue in the general population. Cancer,<br />
- 131 -
[0931]<br />
[0932]<br />
[0933]<br />
[0934]<br />
[0935]<br />
[0936]<br />
[0937]<br />
[0938]<br />
[0939]<br />
[0940]<br />
[0941]<br />
[0942]<br />
[0943]<br />
94(2), 528-538; Cella, D., Eton, D.T., Lai,F J-S., Peterman, A.H & Merkel, D.E. (2002). Combining<br />
anchor and distribution based methods to derive minimal clinically important differences on the<br />
Functional Assessment of Cancer Therapy anemia and fatigue scales. Journal of Pain & Symptom<br />
Management, 24 (6) 547-561.).<br />
결과<br />
체중 변화<br />
<strong>12</strong>주 동안 Ab1 단일클론 항체의 각 투약 농도 군(위약, 80 ㎎, 160 ㎎, 그리고 320 ㎎)으로부터 평균화된 체중<br />
변화 데이터는 도 49에 플롯팅된다. 각 투약 농도 군으로부터 체중에서 평균 변화 비율은 도 50에 플롯팅된다.<br />
이들 투약 농도 군에 대한 평균화된 제지방량 데이터는 도 51에 플롯팅된다.<br />
피로<br />
Ab1 단일클론 항체의 각 투약 농도 군(위약, 80 ㎎, 160 ㎎, 그리고 320 ㎎)으로부터 평균화된 피로는 8주 기간<br />
동안 상기 환자 집단의 일부 투약 농도 군에 대한 평균 Facit-F FS 하위척도 점수에서 증가를 증명하였다(도<br />
52). 기준선 Facit-F 하위척도 점수로부터 변화는 도 53에 플롯팅된다.<br />
실시예 31 Ab1은 진행된 암 환자에서 D-이합체 수준을 감소시킨다.<br />
도입<br />
D-이합체 농도는 환자에서 혈전성 사건의 위험을 예측하는데 유용한 진단 도구로서 인정된다(Adam et al., 113<br />
Blood 2878-87 (2009)). D-이합체에 음성인 환자는 혈전증의 가능성이 낮다. 가령, D-이합체 분석은 환자에서<br />
의심되는 하지 심부 정맥 혈전증을 배제할 수 있다(Wells et al., 349 N. Engl. J. Med. <strong>12</strong>27-35 (2003)). 음<br />
성 D-이합체 검사와 공동으로 임상 평가는 폐 색전증의 사례를 0.5%까지 효과적으로 낮출 수 있다(Van Belle et<br />
al., 295 JAMA 172-79 (2006); Kruip et al., 162 Arch. Intern. Med. 1631-35 (2002); Wells et al., 135<br />
Ann. Intern. Med. 98-107 (2001)).<br />
D-이합체 분석은 혈액응고 질환의 치료 진행을 추적하는데 유용하다. 한 연구에서, 급성 정맥성 혈전 색전증에<br />
대한 항혈액응고 치료는 D-이합체 농도에서 점진적인 감소를 유발하는 것으로 지시되었다(Adam et al., 113<br />
Blood 2878-87 (2009); Schutgens et al., 144 J. Lab. Clin. Med. 100-07 (2004)). 이러한 발견은 D-이합체<br />
수준 모니터링이 치료 민감성을 평가하는데 이용될 수 있다는 결론으로 이어졌다(Adam et al., 113 Blood at<br />
2883).<br />
암 환자의 경우에, D-이합체 분석은 암이 혈전증의 이환율을 증가시키기 때문에, 추가의 의미를 가질 수 있다<br />
(Adam et al., 113 Blood 2878-87 (2009)). 종양 환자를 대상으로 하는 한 연구에서, D-이합체 농도는 높은 음<br />
성 예측 값 및 폐 색전증의 진단에서 높은 민감도를 갖는 것으로 지시되었다(King et al., 247 Radiology 854-<br />
61 (2008)). 심부 정맥 혈전증의 발병 가능성이 낮고 D-이합체에 대한 음성 결과를 갖는 암 환자의 경우에, 비<br />
록 이런 조합이 종양 환자에서 발생할 가능성이 낮긴 하지만, 심부 정맥 혈전증이 유사하게 배제될 수 있다(Lee<br />
et al., <strong>12</strong>3 Thromb. Res. 177-83 (2008)). 음성 D-이합체 결과에 대한 더욱 높은 역치가 암 환자에서 필요할<br />
수도 있다(Righini et al., 95 Haemost. 715-<strong>19</strong> (2006)).<br />
따라서 암 환자에서 D-이합체 농도를 개선하고 암 환자, 특히 진행된 암 환자에서 상승된 D-이합체 상태를 해결<br />
하는 혈전증의 치료 방법 및/또는 치료제가 당분야에서 여전히 요구된다.<br />
방법<br />
공개특허 10-2011-01<strong>12</strong>308<br />
비-소세포 폐 암(NSCLC)을 앓는 <strong>12</strong>4명의 환자는 4가지 치료 군으로 분할되었다. 하나의 군에서 환자는 총 3회<br />
투약을 위하여 24주 기간 동안 8주마다 위약(n=31), 80 ㎎(n=29), 160 ㎎(n=32), 또는 320 ㎎(n=32)의 Ab1 단<br />
일클론 항체의 1-시간 정맥내(IV) 주사가 투약되었다. D-이합체 농도에 관한 데이터는 첫 8주간의 치료 동안 수<br />
집되었다. D-이합체 데이터 농도는 D-이합체 면역비탁법에 의해 정량되었다. 간단히 말하면, 상기 분석법은 광<br />
도측정법(photometry)으로 측정되는 마이크로입자 현탁액의 탁도에서 변화에 기초된다. 대략 1.5 ㎖의 환자 시<br />
료 구연산나트륨 혈장이 수집되고 플라스틱 수집 튜브 내에 보관되었다. D-이합체에 특이적인 단일클론 항체로<br />
공유 결합에 의해 코팅된 라텍스 마이크로입자(latex microparticle)의 현탁액은 D-이합체 수준이 분석되는 검<br />
사 혈장과 혼합되었다. 라텍스 마이크로입자의 응집을 유발하는 항원-항체 반응은 반응 매체의 탁도에서 증가를<br />
- 132 -
[0944]<br />
[0945]<br />
[0946]<br />
[0947]<br />
[0948]<br />
[0949]<br />
[0950]<br />
[0951]<br />
[0952]<br />
[0953]<br />
[0954]<br />
[0955]<br />
[0956]<br />
[0957]<br />
유발하였다. 탁도에서 이러한 증가는 흡광도에서 증가로 반영되고, 후자는 STAGO STA 분석기를 이용하여 광도측<br />
정법으로 측정되었다. 흡광도에서 증가는 검사 시료 내에 존재하는 D-이합체 수준의 함수이었다.<br />
결과<br />
Ab1 단일클론 항체의 각 투약 농도(위약, 80 ㎎, 160 ㎎, 그리고 320 ㎎)에 대한 평균화된 데이터는 도 54에 플<br />
롯팅된다. 오차 막대는 명료하게 하기 위하여 그래프로부터 생략되었다. D-이합체 농도에서 기준선으로부터 변<br />
화 비율은 도 55에 플롯팅된다. 모든 용량 수준의 Ab1 항체는 8주의 기간 동안 위약에 비하여 D-이합체 수준에<br />
서 감소를 나타냈다.<br />
실시예 32 Ab1은 류머티스성 관절염을 앓는 환자에서 ACR 20/50/70을 달성하였다.<br />
도입<br />
류머티스성 관절염은 주로, 관절의 활액막을 공격하는 만성 전신성 염증 질환이다. 상기 질환은 고통스럽고, 그<br />
리고 잠재적으로 무능화 염증을 유발하고, 전형적으로, 40세와 50세 사이에 발병한다. 류머티스성 관절염에서<br />
약물 치료 효능의 해석은 수년에 걸쳐 가용해진 무수한 주관적 및 객관적 평가 도구로 인하여 난해하다.<br />
American College of Rheumatology("ACR")에서는 임상 시험에서 상기 질환의 개선의 평가를 용이하게 하는 류<br />
머티스성 관절염 척도의 표준화된 세트를 발표하였다(Felson et al., 36 Arthritis & Rheumatism 729-40<br />
(<strong>19</strong>93)).<br />
방법<br />
활성 류머티스성 관절염을 앓고 CRP ≥10 ㎎/ℓ를 갖는 <strong>12</strong>7명의 환자는 4가지 치료 군으로 분할되었다. 하나의<br />
군에서 환자는 16주 시험의 시작 시점에 한 번, 그리고 8주 시점에 다시 한 번, 위약(n=33), 80 ㎎(n=32), 160<br />
㎎(n=34), 또는 320 ㎎(n=28)의 Ab1 단일클론 항체의 1-시간 정맥내(IV) 주사가 투약되었다. CRP 농도에 관한<br />
데이터는 첫 4주 동안 매주, 4주와 <strong>12</strong>주 사이에 격주, 그리고 16주에 시험의 종결 시점에서 수집되었다.<br />
American College of Rheumatology로부터 표준화된 프로토콜 하에 평가는 임상 시험 동안 환자의 개선 비율을<br />
결정하는데 활용되고, 그리고 류머티스성 관절염을 평가하는데 숙련된 인력에 의해 수행되었다. 이러한 평가는<br />
유약 관절 수, 종창 관절 수, 환자의 통증 평가, 환자와 의사의 전체적인 질병 활성 평가, 그리고 적혈구 침강<br />
속도 또는 CRP 수준의 실험실 평가를 비롯한 활성 척도에 기초되었다(Id). 환자의 통증 평가는 Stanford Health<br />
Assessment Questionnaire Disability Index(HAQ DI)에 기초되었다. 임상 시험 동안 류머티스성 관절염에 대한<br />
활성 척도에서 20% 증가를 달성하는 환자는 ACR 20을 달성하는 것으로 분류된다. 유사하게, 50%와 70% 개선을<br />
달성하는 환자는 각각, ACR 50과 ACR 70으로 분류된다.<br />
결과<br />
류머티스성 관절염을 앓는 환자 중에서 상당수가 연구 과정 동안 ACR 20 이상을 달성하였다(도 56). 환자는 연<br />
구의 첫 4주 이내에 체계에서 신속한 개선이 관찰되고, 16주 평가 과정 내내 안정적인 개선이 지속되었다(도<br />
57, 58, 그리고 59). 최고 결과는 320 ㎎ 용량 수준이 투약된 환자에서 관찰되고, 연구 동안 43%가 ACR 70 상태<br />
를 달성하였다(도 59).<br />
ACR 평가의 개별 구성요소의 분석은 모든 구성요소에서 증가를 증명하였다(도 60). HAQ DI 스코어는 평가 과정<br />
동안 위약에 비하여 임상적으로 유의한 변화를 보였다(도 61). 혈청 CRP 수준은 조사된 모든 환자에서 상당히<br />
감소되었다(도 41). 혈청 CRP 수준에서 감소는 Ab1 투여후 1주 이내에 위약에 비하여 CRP 수준에서 즉각적인 감<br />
소로 인하여 급속하고, 그리고 연장된 감소된 수준은 적어도 최종 측정이 수행될 때(16주)까지 지속되었다. 모<br />
든 경우에, CRP 수준은 1주 이내에 정상적인 참고 범위(5-6 ㎎/ℓ 미만) 이하로 하락하였다. 따라서 Ab1의 투여<br />
는 임상 평가 동안 ACR 스코어의 유의한 개선에 의해 증명되는 바와 같이, 류머티스성 관절염 환자에서 신속하<br />
고 지속된 개선을 유발할 수 있고, 그리고 효과적인 치료 섭생(treatment regime)을 제공한다.<br />
실시예 33 Ab1은 류머티스성 관절염을 앓는 환자에서 개선된 DAS28과 EULAR 스코어를 달성하였다.<br />
도입<br />
공개특허 10-2011-01<strong>12</strong>308<br />
류머티스성 관절염은 주로, 관절의 활액막을 공격하는 만성 전신성 염증 질환이다. 상기 질환은 고통스럽고, 그<br />
- 133 -
[0958]<br />
[0959]<br />
[0960]<br />
[0961]<br />
[0962]<br />
[0963]<br />
[0964]<br />
[0965]<br />
[0966]<br />
[0967]<br />
[0968]<br />
[0969]<br />
[0970]<br />
[0971]<br />
[0972]<br />
[0973]<br />
[0974]<br />
[0975]<br />
리고 잠재적으로 무능화 염증을 유발하고, 전형적으로, 40세와 50세 사이에 발병한다. 류머티스성 관절염에서<br />
약물 치료 효능의 해석은 수년에 걸쳐 가용해진 무수한 주관적 및 객관적 평가 도구로 인하여 난해하다.<br />
American College of Rheumatology("ACR")에서는 임상 시험에서 상기 질환의 개선의 평가를 용이하게 하는 류<br />
머티스성 관절염 척도의 표준화된 세트를 발표하였다(Felson et al., 36 Arthritis & Rheumatism 729-40<br />
(<strong>19</strong>93)).<br />
류머티스성 관절염과 연관된 염증 활성은 검증된 반응 기준, 예를 들면, 질병 활성 스코어(DAS), DAS28과 EULAR<br />
을 통하여 다수의 변수를 이용하여 측정된다. DAS는 종창 관절, 유약 관절, 급성기 반응, 그리고 전반적인 건강<br />
으로부터 정보를 통합하는 류머티스성 관절염 질병 활성의 임상 지수이다(Fransen, J., et al., Clin. Exp.<br />
Rheumatol., 23 (Suppl. 39): S93-S99 (2005)). DAS 28은 본래 DAS와 유사한 지수이지만, 28 유약 관절 수(0-<br />
28 범위), 28 종창 관절 수(0-28 범위), ESR(적혈구 침강 속도), 그리고 시각 통증 등급(visual analogue<br />
scale)에서 선택적인 전반적인 건강 평가(0-100 범위)를 이용한다(Id). European League against<br />
Rheumatism(EULAR) 반응 기준은 DAS에서 변화의 개별 결과 및 도달된 DAS 값(낮음, 중간, 높음)을 이용하여, 환<br />
자를 아래의 분류: 우수한 반응자; 중간 반응자; 또는 비-반응자 중에서 한 가지로 분류한다(Id).<br />
방법<br />
활성 류머티스성 관절염을 앓는 <strong>12</strong>7명의 환자는 4가지 치료 군으로 분할되었다. 하나의 군에서 환자는 16주 시<br />
험의 시작 시점에 한 번, 그리고 8주 시점에 다시 한 번, 위약(n=33), 80 ㎎(n=32), 160 ㎎(n=34), 또는 320<br />
㎎(n=28)의 Ab1 단일클론 항체의 1-시간 정맥내(IV) 주사가 투약되었다. DAS28과 EULAR 스코어에 관한 데이터는<br />
첫 4주 동안 매주, 4주와 <strong>12</strong>주 사이에 격주, 그리고 16주에 시험의 종결 시점에서 수집되었다. 표준화된 DAS28<br />
과 EULAR 프로토콜 하에 평가는 임상 시험 동안 환자의 개별 스코어를 결정하는데 활용되고, 그리고 류머티스성<br />
관절염을 평가하는데 숙련된 인력에 의해 수행되었다.<br />
결과<br />
80 ㎎, 160 ㎎ 또는 320 ㎎의 Ab1이 투약된 환자는 도 62에서 기준선 DAS28 스코어로부터 평균 변화로서 제시된<br />
바와 같이, 16주 과정 동안 위약이 투약된 환자에 비하여 개선된 DAS28 스코어를 보였다. 더 나아가, 80 ㎎,<br />
160 ㎎ 또는 320 ㎎의 Ab1이 투약된 환자의 유의한 비율이 16주 과정 동안 위약이 투약된 환자에 비하여 "우수<br />
한" 또는 "중간" 분류를 달성하였다(도 63).<br />
따라서 Ab1의 투약은 위약이 투약된 환자와 비교할 때, 류머티스성 관절염에서 개선된 DAS28과 EULAR 스코어를<br />
유발할 수 있다.<br />
서열 목록<br />
본 명세서에 언급된 생물학적 서열은 하기에 제공된다:<br />
서열 번호: 1<br />
VPPGEDSKDVAAPHRQPLTSSERIDKQIRYILDGISALRKETCNKSNMCESSKEALAENNLNLPKMAEKDGCFQSGFNEETCLVKIITGLLEFEVYLEYLQN<br />
RFESSEEQARAVQMSTKVLIQFLQKKAKNLDAITTPDPTTNASLLTKLQAQNQWLQDMTTHLILRSFKEFLQSSLRALRQM<br />
서열 번호: 2<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVSAAVGGTVTIKCQASQSINNELSWYQQKPGQRPKLLIYRASTLASGVSSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQQGYSLRNIDNAFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNN<br />
서열 번호: 3<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSNYYVTWVRQAPGKGLEWIGIIYGSDETAYATWAIGRFTISKTSTTVDLKMTSLT<br />
AADTATYFCARDDSSDWDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK<br />
서열 번호: 4<br />
QASQSINNELS<br />
서열 번호: 5<br />
RASTLAS<br />
- 134 -<br />
공개특허 10-2011-01<strong>12</strong>308
[0976]<br />
[0977]<br />
[0978]<br />
[0979]<br />
[0980]<br />
[0981]<br />
[0982]<br />
[0983]<br />
[0984]<br />
[0985]<br />
[0986]<br />
[0987]<br />
[0988]<br />
[0989]<br />
[0990]<br />
[0991]<br />
[0992]<br />
[0993]<br />
[0994]<br />
[0995]<br />
[0996]<br />
[0997]<br />
[0998]<br />
[0999]<br />
[1000]<br />
[1001]<br />
[1002]<br />
[1003]<br />
[1004]<br />
서열 번호: 6<br />
QQGYSLRNIDNA<br />
서열 번호: 7<br />
NYYVT<br />
서열 번호: 8<br />
IIYGSDETAYATWAIG<br />
서열 번호: 9<br />
DDSSDWDAKFNL<br />
서열 번호: 10<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCGGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCATTAACAATGAATTATCCTGGTATCAGCAGAAACCAGGGCAGCGTCCCAAGCTC<br />
CTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCTTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTAGCG<br />
GCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTT<br />
서열 번호: 11<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTTATGGTAGTGATGAAACGGCCTACGCGACCTGGGCGATAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACA<br />
GCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCAAAATTTAACTTGTGGGGCCAAGGCACCCTGGTCACCGTCTCGAGC<br />
GCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGG<br />
서열 번호: <strong>12</strong><br />
CAGGCCAGTCAGAGCATTAACAATGAATTATCC<br />
서열 번호: 13<br />
AGGGCATCCACTCTGGCATCT<br />
서열 번호: 14<br />
CAACAGGGTTATAGTCTGAGGAATATTGATAATGCT<br />
서열 번호: 15<br />
AACTACTACGTGACC<br />
서열 번호: 16<br />
ATCATTTATGGTAGTGATGAAACGGCCTACGCGACCTGGGCGATAGGC<br />
서열 번호: 17<br />
GATGATAGTAGTGACTGGGATGCAAAATTTAACTTG<br />
서열 번호: 18<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATWAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNL<br />
서열 번호: <strong>19</strong><br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATSAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNL<br />
서열 번호: 20<br />
- 135 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1005]<br />
[1006]<br />
[1007]<br />
[1008]<br />
[1009]<br />
[1010]<br />
[1011]<br />
[10<strong>12</strong>]<br />
[1013]<br />
[1014]<br />
[1015]<br />
[1016]<br />
[1017]<br />
[1018]<br />
[10<strong>19</strong>]<br />
[1020]<br />
[1021]<br />
[1022]<br />
[1023]<br />
[1024]<br />
[1025]<br />
[1026]<br />
[1027]<br />
[1028]<br />
[1029]<br />
[1030]<br />
[1031]<br />
[1032]<br />
IQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPDDFATYYCQQGYSLRNIDNA<br />
서열 번호: 21<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVEVAVGGTVTINCQASETIYSWLSWYQQKPGQPPKLLIYQASDLASGVPSRFSGSGAGTEYTLTISGVQC<br />
DDAATYYCQQGYSGSNVDNVFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAK<br />
서열 번호: 22<br />
METGLRWLLLVAVLKGVQCQEQLKESGGRLVTPGTPLTLTCTASGFSLNDHAMGWVRQAPGKGLEYIGFINSGGSARYASWAEGRFTISRTSTTVDLKMTSL<br />
TTEDTATYFCVRGGAVWSIHSFDPWGPGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK<br />
서열 번호: 23<br />
QASETIYSWLS<br />
서열 번호: 24<br />
QASDLAS<br />
서열 번호: 25<br />
QQGYSGSNVDNV<br />
서열 번호: 26<br />
DHAMG<br />
서열 번호: 27<br />
FINSGGSARYASWAEG<br />
서열 번호: 28<br />
GGAVWSIHSFDP<br />
서열 번호: 29<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCTGTGGAG<br />
GTAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTGAGACCATTTACAGTTGGTTATCCTGGTATCAGCAGAAGCCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTACCAGGCATCCGATCTGGCATCTGGGGTCCCATCGCGATTCAGCGGCAGTGGGGCTGGGACAGAGTACACTCTCACCATCAGCGGCGTGCAGTGT<br />
GACGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTGGTAGTAATGTTGATAATGTTTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTAGCG<br />
GCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAA<br />
G<br />
서열 번호: 30<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGGAGCAGCTGAAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGG<br />
ACACCCCTGACACTTACCTGCACAGCCTCTGGATTCTCCCTCAATGACCATGCAATGGGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATACATCGGA<br />
TTCATTAATAGTGGTGGTAGCGCACGCTACGCGAGCTGGGCAGAAGGCCGATTCACCATCTCCAGAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTG<br />
ACAACCGAGGACACGGCCACCTATTTCTGTGTCAGAGGGGGTGCTGTTTGGAGTATTCATAGTTTTGATCCCTGGGGCCCAGGGACCCTGGTCACCGTCTCG<br />
AGCGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAG<br />
서열 번호: 31<br />
CAGGCCAGTGAGACCATTTACAGTTGGTTATCC<br />
서열 번호: 32<br />
CAGGCATCCGATCTGGCATCT<br />
서열 번호: 33<br />
CAACAGGGTTATAGTGGTAGTAATGTTGATAATGTT<br />
서열 번호: 34<br />
- 136 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1033]<br />
[1034]<br />
[1035]<br />
[1036]<br />
[1037]<br />
[1038]<br />
[1039]<br />
[1040]<br />
[1041]<br />
[1042]<br />
[1043]<br />
[1044]<br />
[1045]<br />
[1046]<br />
[1047]<br />
[1048]<br />
[1049]<br />
[1050]<br />
[1051]<br />
[1052]<br />
[1053]<br />
[1054]<br />
[1055]<br />
[1056]<br />
[1057]<br />
[1058]<br />
[1059]<br />
[1060]<br />
[1061]<br />
GACCATGCAATGGGC<br />
서열 번호: 35<br />
TTCATTAATAGTGGTGGTAGCGCACGCTACGCGAGCTGGGCAGAAGGC<br />
서열 번호: 36<br />
GGGGGTGCTGTTTGGAGTATTCATAGTTTTGATCCC<br />
서열 번호: 37<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSAAVGGTVSISCQASQSVYDNNYLSWFQQKPGQPPKLLIYGASTLASGVPSRFVGSGSGTQFTLTITDV<br />
QCDDAATYYCAGVYDDDSDNAFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNF<br />
서열 번호: 38<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSVYYMNWVRQAPGKGLEWIGFITMSDNINYASWAKGRFTISKTSTTVDLKMTSPT<br />
TEDTATYFCARSRGWGTMGRLDLWGPGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK<br />
서열 번호: 39<br />
QASQSVYDNNYLS<br />
서열 번호: 40<br />
GASTLAS<br />
서열 번호: 41<br />
AGVYDDDSDNA<br />
서열 번호: 42<br />
VYYMN<br />
서열 번호: 43<br />
FITMSDNINYASWAKG<br />
서열 번호: 44<br />
SRGWGTMGRLDL<br />
서열 번호: 45<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCGCCGTGCTGACCCAGACTCCATCTCCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGGCCAGTCAGAGTGTTTATGACAACAACTACTTATCCTGGTTTCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCGTGGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCACAGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTATTGTGCAGGCGTTTATGATGATGATAGTGATAATGCCTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTA<br />
GCGGCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCT<br />
서열 번호: 46<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTGGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACCCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTGTCTACTACATGAACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGATTC<br />
ATTACAATGAGTGATAATATAAATTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGGAGTCGTGGCTGGGGTACAATGGGTCGGTTGGATCTCTGGGGCCCAGGCACCCTCGTCACCGTCTCGAGC<br />
GCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGG<br />
서열 번호: 47<br />
CAGGCCAGTCAGAGTGTTTATGACAACAACTACTTATCC<br />
서열 번호: 48<br />
GGTGCATCCACTCTGGCATCT<br />
- 137 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1062]<br />
[1063]<br />
[1064]<br />
[1065]<br />
[1066]<br />
[1067]<br />
[1068]<br />
[1069]<br />
[1070]<br />
[1071]<br />
[1072]<br />
[1073]<br />
[1074]<br />
[1075]<br />
[1076]<br />
[1077]<br />
[1078]<br />
[1079]<br />
[1080]<br />
[1081]<br />
[1082]<br />
[1083]<br />
[1084]<br />
[1085]<br />
[1086]<br />
[1087]<br />
[1088]<br />
[1089]<br />
[1090]<br />
서열 번호: 49<br />
GCAGGCGTTTATGATGATGATAGTGATAATGCC<br />
서열 번호: 50<br />
GTCTACTACATGAAC<br />
서열 번호: 51<br />
TTCATTACAATGAGTGATAATATAAATTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 52<br />
AGTCGTGGCTGGGGTACAATGGGTCGGTTGGATCTC<br />
서열 번호: 53<br />
MDTRAPTQLLGLLLLWLPGAICDPVLTQTPSPVSAPVGGTVSISCQASQSVYENNYLSWFQQKPGQPPKLLIYGASTLDSGVPSRFKGSGSGTQFTLTITDV<br />
QCDDAATYYCAGVYDDDSDDAFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNN<br />
서열 번호: 54<br />
METGLRWLLLVAVLKGVQCQEQLKESGGGLVTPGGTLTLTCTASGFSLNAYYMNWVRQAPGKGLEWIGFITLNNNVAYANWAKGRFTFSKTSTTVDLKMTSP<br />
TPEDTATYFCARSRGWGAMGRLDLWGHGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK<br />
서열 번호: 55<br />
QASQSVYENNYLS<br />
서열 번호: 56<br />
GASTLDS<br />
서열 번호: 57<br />
AGVYDDDSDDA<br />
서열 번호: 58<br />
AYYMN<br />
서열 번호: 59<br />
FITLNNNVAYANWAKG<br />
서열 번호: 60<br />
SRGWGAMGRLDL<br />
서열 번호: 61<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCATATGTGACCCTGTGCTGACCCAGACTCCATCTCCCGTATCT<br />
GCACCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGGCCAGTCAGAGTGTTTATGAGAACAACTATTTATCCTGGTTTCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCATCCACTCTGGATTCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATTACAGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTATTGTGCAGGCGTTTATGATGATGATAGTGATGATGCCTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTA<br />
GCGGCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTT<br />
서열 번호: 62<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTGGCTGTGCTCAAAGGTGTCCAGTGTCAGGAGCAGCTGAAGGAGTCCGGAGGAGGCCTGGTAACGCCTGGA<br />
GGAACCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAATGCCTACTACATGAACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGA<br />
TTCATTACTCTGAATAATAATGTAGCTTACGCGAACTGGGCGAAAGGCCGATTCACCTTCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCCG<br />
ACACCCGAGGACACGGCCACCTATTTCTGTGCCAGGAGTCGTGGCTGGGGTGCAATGGGTCGGTTGGATCTCTGGGGCCATGGCACCCTGGTCACCGTCTCG<br />
AGCGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGG<br />
서열 번호: 63<br />
- 138 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1091]<br />
[1092]<br />
[1093]<br />
[1094]<br />
[1095]<br />
[1096]<br />
[1097]<br />
[1098]<br />
[1099]<br />
[1100]<br />
[1101]<br />
[1102]<br />
[1103]<br />
[1104]<br />
[1105]<br />
[1106]<br />
[1107]<br />
[1108]<br />
[1109]<br />
[1110]<br />
[1111]<br />
[11<strong>12</strong>]<br />
[1113]<br />
[1114]<br />
[1115]<br />
[1116]<br />
[1117]<br />
[1118]<br />
[11<strong>19</strong>]<br />
[1<strong>12</strong>0]<br />
[1<strong>12</strong>1]<br />
CAGGCCAGTCAGAGTGTTTATGAGAACAACTATTTATCC<br />
서열 번호: 64<br />
GGTGCATCCACTCTGGATTCT<br />
서열 번호: 65<br />
GCAGGCGTTTATGATGATGATAGTGATGATGCC<br />
서열 번호: 66<br />
GCCTACTACATGAAC<br />
서열 번호: 67<br />
TTCATTACTCTGAATAATAATGTAGCTTACGCGAACTGGGCGAAAGGC<br />
서열 번호: 68<br />
AGTCGTGGCTGGGGTGCAATGGGTCGGTTGGATCTC<br />
서열 번호: 69<br />
MDTRAPTQLLGLLLLWLPGATFAQVLTQTPSPVSAAVGGTVTINCQASQSVDDNNWLGWYQQ<strong>KR</strong>GQPPKYLIYSASTLASGVPSRFKGSGSGTQFTLTISDL<br />
ECDDAATYYCAGGFSGNIFAFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNF<br />
서열 번호: 70<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGFSLSSYAMSWVRQAPGKGLEWIGIIGGFGTTYYATWAKGRFTISKTSTTVDLRITSPT<br />
TEDTATYFCARGGPGNGGDIWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKD<br />
서열 번호: 71<br />
QASQSVDDNNWLG<br />
서열 번호: 72<br />
SASTLAS<br />
서열 번호: 73<br />
AGGFSGNIFA<br />
서열 번호: 74<br />
SYAMS<br />
서열 번호: 75<br />
IIGGFGTTYYATWAKG<br />
서열 번호: 76<br />
GGPGNGGDI<br />
서열 번호: 77<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCCAAGTGCTGACCCAGACTCCATCGCCTGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAACTGCCAGGCCAGTCAGAGTGTTGATGATAACAACTGGTTAGGCTGGTATCAGCAGAAACGAGGGCAGCCTCCC<br />
AAGTACCTGATCTATTCTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACCTG<br />
GAGTGTGACGATGCTGCCACTTACTACTGTGCAGGCGGTTTTAGTGGTAATATCTTTGCTTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTAGCG<br />
GCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCT<br />
서열 번호: 78<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGCTTCTCCCTCAGTAGCTATGCAATGAGCTGGGTCCGCCAGGCTCCAGGAAAGGGGCTGGAGTGGATCGGAATC<br />
- 139 -
[1<strong>12</strong>2]<br />
[1<strong>12</strong>3]<br />
[1<strong>12</strong>4]<br />
[1<strong>12</strong>5]<br />
[1<strong>12</strong>6]<br />
[1<strong>12</strong>7]<br />
[1<strong>12</strong>8]<br />
[1<strong>12</strong>9]<br />
[1130]<br />
[1131]<br />
[1132]<br />
[1133]<br />
[1134]<br />
[1135]<br />
[1136]<br />
[1137]<br />
[1138]<br />
[1139]<br />
[1140]<br />
[1141]<br />
[1142]<br />
[1143]<br />
[1144]<br />
[1145]<br />
[1146]<br />
[1147]<br />
[1148]<br />
[1149]<br />
[1150]<br />
[1151]<br />
ATTGGTGGTTTTGGTACCACATACTACGCGACCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAGAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGGTGGTCCTGGTAATGGTGGTGACATCTGGGGCCAAGGGACCCTGGTCACCGTCTCGAGCGCCTCCACC<br />
AAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACT<br />
서열 번호: 79<br />
CAGGCCAGTCAGAGTGTTGATGATAACAACTGGTTAGGC<br />
서열 번호: 80<br />
TCTGCATCCACTCTGGCATCT<br />
서열 번호: 81<br />
GCAGGCGGTTTTAGTGGTAATATCTTTGCT<br />
서열 번호: 82<br />
AGCTATGCAATGAGC<br />
서열 번호: 83<br />
ATCATTGGTGGTTTTGGTACCACATACTACGCGACCTGGGCGAAAGGC<br />
서열 번호: 84<br />
GGTGGTCCTGGTAATGGTGGTGACATC<br />
서열 번호: 85<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSVPVGGTVTIKCQSSQSVYNNFLSWYQQKPGQPPKLLIYQASKLASGVPDRFSGSGSGTQFTLTISGVQ<br />
CDDAATYYCLGGYDDDADNAFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNF<br />
서열 번호: 86<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGIDLSDYAMSWVRQAPGKGLEWIGIIYAGSGSTWYASWAKGRFTISKTSTTVDLKITSP<br />
TTEDTATYFCARDGYDDYGDFDRLDLWGPGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKD<br />
서열 번호: 87<br />
QSSQSVYNNFLS<br />
서열 번호: 88<br />
QASKLAS<br />
서열 번호: 89<br />
LGGYDDDADNA<br />
서열 번호: 90<br />
DYAMS<br />
서열 번호: 91<br />
IIYAGSGSTWYASWAKG<br />
서열 번호: 92<br />
DGYDDYGDFDRLDL<br />
서열 번호: 93<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCAGCCGTGCTGACCCAGACACCATCGCCCGTGTCT<br />
GTACCTGTGGGAGGCACAGTCACCATCAAGTGCCAGTCCAGTCAGAGTGTTTATAATAATTTCTTATCGTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAG<br />
CTCCTGATCTACCAGGCATCCAAACTGGCATCTGGGGTCCCAGATAGGTTCAGCGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGGCGTGCAG<br />
TGTGACGATGCTGCCACTTACTACTGTCTAGGCGGTTATGATGATGATGCTGATAATGCTTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTAGCG<br />
- 140 -
[1152]<br />
[1153]<br />
[1154]<br />
[1155]<br />
[1156]<br />
[1157]<br />
[1158]<br />
[1159]<br />
[1160]<br />
[1161]<br />
[1162]<br />
[1163]<br />
[1164]<br />
[1165]<br />
[1166]<br />
[1167]<br />
[1168]<br />
[1169]<br />
[1170]<br />
[1171]<br />
[1172]<br />
[1173]<br />
[1174]<br />
[1175]<br />
[1176]<br />
[1177]<br />
[1178]<br />
[1179]<br />
[1180]<br />
[1181]<br />
GCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTC<br />
서열 번호: 94<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACGCTCACCTGCACAGTCTCTGGAATCGACCTCAGTGACTATGCAATGAGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTTATGCTGGTAGTGGTAGCACATGGTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATCACCAGTCCG<br />
ACAACCGAGGACACGGCCACCTATTTCTGTGCCAGAGATGGATACGATGACTATGGTGATTTCGATCGATTGGATCTCTGGGGCCCAGGCACCCTCGTCACC<br />
GTCTCGAGCGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGAC<br />
T<br />
서열 번호: 95<br />
CAGTCCAGTCAGAGTGTTTATAATAATTTCTTATCG<br />
서열 번호: 96<br />
CAGGCATCCAAACTGGCATCT<br />
서열 번호: 97<br />
CTAGGCGGTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 98<br />
GACTATGCAATGAGC<br />
서열 번호: 99<br />
ATCATTTATGCTGGTAGTGGTAGCACATGGTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 100<br />
GATGGATACGATGACTATGGTGATTTCGATCGATTGGATCTC<br />
서열 번호: 101<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVSAAVGGTVTIKCQASQSINNELSWYQQKSGQRPKLLIYRASTLASGVSSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQQGYSLRNIDNAFGGGTEVVV<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNF<br />
서열 번호: 102<br />
METGLRWLLLVAVLSGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSNYYMTWVRQAPGKGLEWIGMIYGSDETAYANWAIGRFTISKTSTTVDLKMTSLT<br />
AADTATYFCARDDSSDWDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK<br />
서열 번호: 103<br />
QASQSINNELS<br />
서열 번호: 104<br />
RASTLAS<br />
서열 번호: 105<br />
QQGYSLRNIDNA<br />
서열 번호: 106<br />
NYYMT<br />
서열 번호: 107<br />
MIYGSDETAYANWAIG<br />
서열 번호: 108<br />
DDSSDWDAKFNL<br />
- 141 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1182]<br />
[1183]<br />
[1184]<br />
[1185]<br />
[1186]<br />
[1187]<br />
[1188]<br />
[1189]<br />
[1<strong>19</strong>0]<br />
[1<strong>19</strong>1]<br />
[1<strong>19</strong>2]<br />
[1<strong>19</strong>3]<br />
[1<strong>19</strong>4]<br />
[1<strong>19</strong>5]<br />
[1<strong>19</strong>6]<br />
[1<strong>19</strong>7]<br />
[1<strong>19</strong>8]<br />
[1<strong>19</strong>9]<br />
[<strong>12</strong>00]<br />
[<strong>12</strong>01]<br />
[<strong>12</strong>02]<br />
[<strong>12</strong>03]<br />
[<strong>12</strong>04]<br />
[<strong>12</strong>05]<br />
[<strong>12</strong>06]<br />
[<strong>12</strong>07]<br />
[<strong>12</strong>08]<br />
[<strong>12</strong>09]<br />
서열 번호: 109<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCGGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAATGCCAGGCCAGTCAGAGCATTAACAATGAATTATCCTGGTATCAGCAGAAATCAGGGCAGCGTCCCAAGCTC<br />
CTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCTTTCGGCGGAGGGACCGAGGTGGTGGTCAAACGTACGGTAGCG<br />
GCCCCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTC<br />
서열 번호: 110<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCTCAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACATGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATG<br />
ATTTATGGTAGTGATGAAACAGCCTACGCGAACTGGGCGATAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACA<br />
GCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCAAAATTTAACTTGTGGGGCCAAGGGACCCTCGTCACCGTCTCGAGC<br />
GCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGG<br />
서열 번호: 111<br />
CAGGCCAGTCAGAGCATTAACAATGAATTATCC<br />
서열 번호: 1<strong>12</strong><br />
AGGGCATCCACTCTGGCATCT<br />
서열 번호: 113<br />
CAACAGGGTTATAGTCTGAGGAATATTGATAATGCT<br />
서열 번호: 114<br />
AACTACTACATGACC<br />
서열 번호: 115<br />
ATGATTTATGGTAGTGATGAAACAGCCTACGCGAACTGGGCGATAGGC<br />
서열 번호: 116<br />
GATGATAGTAGTGACTGGGATGCAAAATTTAACTTG<br />
서열 번호: 117<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYMTWVRQAPGKGLEWVGMIYGSDETAYANWAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNL<br />
서열 번호: 118<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYMTWVRQAPGKGLEWVGMIYGSDETAYANSAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNL<br />
서열 번호: 1<strong>19</strong><br />
DIQMTQSPSTLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTEFTLTISSLQPDDFATYYCQQGYSLRNIDNA<br />
서열 번호: <strong>12</strong>0<br />
IIYGSDETAYATSAIG<br />
서열 번호: <strong>12</strong>1<br />
MIYGSDETAYANSAIG<br />
서열 번호: <strong>12</strong>2<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSAAVGGTVTISCQSSQSVGNNQDLSWFQQRPGQPPKLLIYEISKLESGVPSRFSGSGSGTHFTLTISGV<br />
QCDDAATYYCLGGYDDDADNA<br />
- 142 -<br />
공개특허 10-2011-01<strong>12</strong>308
[<strong>12</strong>10]<br />
[<strong>12</strong>11]<br />
[<strong>12</strong><strong>12</strong>]<br />
[<strong>12</strong>13]<br />
[<strong>12</strong>14]<br />
[<strong>12</strong>15]<br />
[<strong>12</strong>16]<br />
[<strong>12</strong>17]<br />
[<strong>12</strong>18]<br />
[<strong>12</strong><strong>19</strong>]<br />
[<strong>12</strong>20]<br />
[<strong>12</strong>21]<br />
[<strong>12</strong>22]<br />
[<strong>12</strong>23]<br />
[<strong>12</strong>24]<br />
[<strong>12</strong>25]<br />
[<strong>12</strong>26]<br />
[<strong>12</strong>27]<br />
[<strong>12</strong>28]<br />
[<strong>12</strong>29]<br />
[<strong>12</strong>30]<br />
[<strong>12</strong>31]<br />
[<strong>12</strong>32]<br />
[<strong>12</strong>33]<br />
[<strong>12</strong>34]<br />
[<strong>12</strong>35]<br />
[<strong>12</strong>36]<br />
[<strong>12</strong>37]<br />
[<strong>12</strong>38]<br />
[<strong>12</strong>39]<br />
[<strong>12</strong>40]<br />
서열 번호: <strong>12</strong>3<br />
METGLRWLLLVAVLKGVQCHSVEESGGRLVTPGTPLTLTCTVSGFSLSSRTMSWVRQAPGKGLEWIGYIWSGGSTYYATWAKGRFTISKTSTTVDLKITSPT<br />
TEDTATYFCARLGDTGGHAYATRLNL<br />
서열 번호: <strong>12</strong>4<br />
QSSQSVGNNQDLS<br />
서열 번호: <strong>12</strong>5<br />
EISKLES<br />
서열 번호: <strong>12</strong>6<br />
LGGYDDDADNA<br />
서열 번호: <strong>12</strong>7<br />
SRTMS<br />
서열 번호: <strong>12</strong>8<br />
YIWSGGSTYYATWAKG<br />
서열 번호: <strong>12</strong>9<br />
LGDTGGHAYATRLNL<br />
서열 번호: 130<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCAGCCGTGCTGACCCAGACACCATCACCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAGTTGCCAGTCCAGTCAGAGTGTTGGTAATAACCAGGACTTATCCTGGTTTCAGCAGAGACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTACGAAATATCCAAACTGGAATCTGGGGTCCCATCGCGGTTCAGCGGCAGTGGATCTGGGACACACTTCACTCTCACCATCAGCGGCGTA<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCTAGGCGGTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 131<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCACTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGATTCTCCCTCAGTAGTCGTACAATGTCCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATCGGATAC<br />
ATTTGGAGTGGTGGTAGCACATACTACGCGACCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGATTGGGCGATACTGGTGGTCACGCTTATGCTACTCGCTTAAATCTC<br />
서열 번호: 132<br />
CAGTCCAGTCAGAGTGTTGGTAATAACCAGGACTTATCC<br />
서열 번호: 133<br />
GAAATATCCAAACTGGAATCT<br />
서열 번호: 134<br />
CTAGGCGGTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 135<br />
AGTCGTACAATGTCC<br />
서열 번호: 136<br />
TACATTTGGAGTGGTGGTAGCACATACTACGCGACCTGGGCGAAAGGC<br />
서열 번호: 137<br />
TTGGGCGATACTGGTGGTCACGCTTATGCTACTCGCTTAAATCTC<br />
서열 번호: 138<br />
- 143 -<br />
공개특허 10-2011-01<strong>12</strong>308
[<strong>12</strong>41]<br />
[<strong>12</strong>42]<br />
[<strong>12</strong>43]<br />
[<strong>12</strong>44]<br />
[<strong>12</strong>45]<br />
[<strong>12</strong>46]<br />
[<strong>12</strong>47]<br />
[<strong>12</strong>48]<br />
[<strong>12</strong>49]<br />
[<strong>12</strong>50]<br />
[<strong>12</strong>51]<br />
[<strong>12</strong>52]<br />
[<strong>12</strong>53]<br />
[<strong>12</strong>54]<br />
[<strong>12</strong>55]<br />
[<strong>12</strong>56]<br />
[<strong>12</strong>57]<br />
[<strong>12</strong>58]<br />
[<strong>12</strong>59]<br />
[<strong>12</strong>60]<br />
[<strong>12</strong>61]<br />
[<strong>12</strong>62]<br />
[<strong>12</strong>63]<br />
[<strong>12</strong>64]<br />
[<strong>12</strong>65]<br />
[<strong>12</strong>66]<br />
[<strong>12</strong>67]<br />
[<strong>12</strong>68]<br />
[<strong>12</strong>69]<br />
[<strong>12</strong>70]<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSSVSAAVGGTVSISCQSSQSVYSNKYLAWYQQKPGQPPKLLIYWTSKLASGAPSRFSGSGSGTQFTLTISGV<br />
QCDDAATYYCLGAYDDDADNA<br />
서열 번호: 139<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVKPDETLTLTCTASGFSLEGGYMTWVRQAPGKGLEWIGISYDSGSTYYASWAKGRFTISKTSSTTVDLKMTSL<br />
TTEDTATYFCVRSLKYPTVTSDDL<br />
서열 번호: 140<br />
QSSQSVYSNKYLA<br />
서열 번호: 141<br />
WTSKLAS<br />
서열 번호: 142<br />
LGAYDDDADNA<br />
서열 번호: 143<br />
GGYMT<br />
서열 번호: 144<br />
ISYDSGSTYYASWAKG<br />
서열 번호: 145<br />
SLKYPTVTSDDL<br />
서열 번호: 146<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCAGCCGTGCTGACCCAGACACCATCGTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGTCCAGTCAGAGTGTTTATAGTAATAAGTACCTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTACTGGACATCCAAACTGGCATCTGGGGCCCCATCACGGTTCAGCGGCAGTGGATCTGGGACACAATTCACTCTCACCATCAGCGGCGTG<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCTAGGCGCTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 147<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAAGAGTCCGGGGGTCGCCTGGTCAAGCCTGACGAA<br />
ACCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTGGAGGGCGGCTACATGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
AGTTATGATAGTGGTAGCACATACTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAGACCTCGTCGACCACGGTGGATCTGAAAATGACCAGTCTG<br />
ACAACCGAGGACACGGCCACCTATTTCTGCGTCAGATCACTAAAATATCCTACTGTTACTTCTGATGACTTG<br />
서열 번호: 148<br />
CAGTCCAGTCAGAGTGTTTATAGTAATAAGTACCTAGCC<br />
서열 번호: 149<br />
TGGACATCCAAACTGGCATCT<br />
서열 번호: 150<br />
CTAGGCGCTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 151<br />
GGCGGCTACATGACC<br />
서열 번호: 152<br />
ATCAGTTATGATAGTGGTAGCACATACTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 153<br />
- 144 -<br />
공개특허 10-2011-01<strong>12</strong>308
[<strong>12</strong>71]<br />
[<strong>12</strong>72]<br />
[<strong>12</strong>73]<br />
[<strong>12</strong>74]<br />
[<strong>12</strong>75]<br />
[<strong>12</strong>76]<br />
[<strong>12</strong>77]<br />
[<strong>12</strong>78]<br />
[<strong>12</strong>79]<br />
[<strong>12</strong>80]<br />
[<strong>12</strong>81]<br />
[<strong>12</strong>82]<br />
[<strong>12</strong>83]<br />
[<strong>12</strong>84]<br />
[<strong>12</strong>85]<br />
[<strong>12</strong>86]<br />
[<strong>12</strong>87]<br />
[<strong>12</strong>88]<br />
[<strong>12</strong>89]<br />
[<strong>12</strong>90]<br />
[<strong>12</strong>91]<br />
[<strong>12</strong>92]<br />
[<strong>12</strong>93]<br />
[<strong>12</strong>94]<br />
[<strong>12</strong>95]<br />
[<strong>12</strong>96]<br />
[<strong>12</strong>97]<br />
[<strong>12</strong>98]<br />
[<strong>12</strong>99]<br />
[1300]<br />
TCACTAAAATATCCTACTGTTACTTCTGATGACTTG<br />
서열 번호: 154<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSAAVGGTVTISCQSSQSVYNNNDLAWYQQKPGQPPKLLIYYASTLASGVPSRFKGSGSGTQFTLTISGV<br />
QCDDAAAYYCLGGYDDDADNA<br />
서열 번호: 155<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGLSLSSNTINWVRQAPGKGLEWIGYIWSGGSTYYASWVNGRFTISKTSTTVDLKITSPT<br />
TEDTATYFCARGGYASGGYPYATRLDL<br />
서열 번호: 156<br />
QSSQSVYNNNDLA<br />
서열 번호: 157<br />
YASTLAS<br />
서열 번호: 158<br />
LGGYDDDADNA<br />
서열 번호: 159<br />
SNTIN<br />
서열 번호: 160<br />
YIWSGGSTYYASWVNG<br />
서열 번호: 161<br />
GGYASGGYPYATRLDL<br />
서열 번호: 162<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCAGCCGTGCTGACCCAGACACCATCACCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAGTTGCCAGTCCAGTCAGAGTGTTTATAATAATAACGACTTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCT<br />
AAACTCCTGATCTATTATGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGGCGTG<br />
CAGTGTGACGATGCTGCCGCTTACTACTGTCTAGGCGGTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 163<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTATCTGGATTATCCCTCAGTAGCAATACAATAAACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATCGGATAC<br />
ATTTGGAGTGGTGGTAGTACATACTACGCGAGCTGGGTGAATGGTCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGGGGGTTACGCTAGTGGTGGTTATCCTTATGCCACTCGGTTGGATCTC<br />
서열 번호: 164<br />
CAGTCCAGTCAGAGTGTTTATAATAATAACGACTTAGCC<br />
서열 번호: 165<br />
TATGCATCCACTCTGGCATCT<br />
서열 번호: 166<br />
CTAGGCGGTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 167<br />
AGCAATACAATAAAC<br />
서열 번호: 168<br />
- 145 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1301]<br />
[1302]<br />
[1303]<br />
[1304]<br />
[1305]<br />
[1306]<br />
[1307]<br />
[1308]<br />
[1309]<br />
[1310]<br />
[1311]<br />
[13<strong>12</strong>]<br />
[1313]<br />
[1314]<br />
[1315]<br />
[1316]<br />
[1317]<br />
[1318]<br />
[13<strong>19</strong>]<br />
[1320]<br />
[1321]<br />
[1322]<br />
[1323]<br />
[1324]<br />
[1325]<br />
[1326]<br />
[1327]<br />
[1328]<br />
[1329]<br />
[1330]<br />
TACATTTGGAGTGGTGGTAGTACATACTACGCGAGCTGGGTGAATGGT<br />
서열 번호: 169<br />
GGGGGTTACGCTAGTGGTGGTTATCCTTATGCCACTCGGTTGGATCTC<br />
서열 번호: 170<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSSVSAAVGGTVTINCQSSQSVYNNDYLSWYQQRPGQRPKLLIYGASKLASGVPSRFKGSGSGKQFTLTISGV<br />
QCDDAATYYCLGDYDDDADNT<br />
서열 번호: 171<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTVSGFTLSTNYYLSWVRQAPGKGLEWIGIIYPSGNTYCAKWAKGRFTISKTSSTTVDLKMTS<br />
PTTEDTATYFCARNYGGDESL<br />
서열 번호: 172<br />
QSSQSVYNNDYLS<br />
서열 번호: 173<br />
GASKLAS<br />
서열 번호: 174<br />
LGDYDDDADNT<br />
서열 번호: 175<br />
TNYYLS<br />
서열 번호: 176<br />
IIYPSGNTYCAKWAKG<br />
서열 번호: 177<br />
NYGGDESL<br />
서열 번호: 178<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCAGCCGTGCTGACCCAGACACCATCCTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGTCCAGTCAGAGTGTTTATAATAACGACTACTTATCCTGGTATCAACAGAGGCCAGGGCAACGTCCC<br />
AAGCTCCTAATCTATGGTGCTTCCAAACTGGCATCTGGGGTCCCGTCACGGTTCAAAGGCAGTGGATCTGGGAAACAGTTTACTCTCACCATCAGCGGCGTG<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCTGGGCGATTATGATGATGATGCTGATAATACT<br />
서열 번호: 179<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACTTGCACAGTCTCTGGATTCACCCTCAGTACCAACTACTACCTGAGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTAGAATGGATCGGA<br />
ATCATTTATCCTAGTGGTAACACATATTGCGCGAAGTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGTCGACCACGGTGGATCTGAAAATGACCAGT<br />
CCGACAACCGAGGACACAGCCACGTATTTCTGTGCCAGAAATTATGGTGGTGATGAAAGTTTG<br />
서열 번호: 180<br />
CAGTCCAGTCAGAGTGTTTATAATAACGACTACTTATCC<br />
서열 번호: 181<br />
GGTGCTTCCAAACTGGCATCT<br />
서열 번호: 182<br />
CTGGGCGATTATGATGATGATGCTGATAATACT<br />
서열 번호: 183<br />
- 146 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1331]<br />
[1332]<br />
[1333]<br />
[1334]<br />
[1335]<br />
[1336]<br />
[1337]<br />
[1338]<br />
[1339]<br />
[1340]<br />
[1341]<br />
[1342]<br />
[1343]<br />
[1344]<br />
[1345]<br />
[1346]<br />
[1347]<br />
[1348]<br />
[1349]<br />
[1350]<br />
[1351]<br />
[1352]<br />
[1353]<br />
[1354]<br />
[1355]<br />
[1356]<br />
[1357]<br />
[1358]<br />
[1359]<br />
[1360]<br />
ACCAACTACTACCTGAGC<br />
서열 번호: 184<br />
ATCATTTATCCTAGTGGTAACACATATTGCGCGAAGTGGGCGAAAGGC<br />
서열 번호: 185<br />
AATTATGGTGGTGATGAAAGTTTG<br />
서열 번호: 186<br />
MDTRAPTQLLGLLLLWLPGARCDVVMTQTPASVEAAVGGTVTIKCQASETIGNALAWYQQKSGQPPKLLIYKASKLASGVPSRFKGSGSGTEYTLTISDLEC<br />
ADAATYYCQWCYFGDSV<br />
서열 번호: 187<br />
METGLRWLLLVTVLKGVQCQEQLVESGGGLVQPEGSLTLTCTASGFDFSSGYYMCWVRQAPGKGLEWIACIFTITTNTYYASWAKGRFTISKTSSTTVTLQM<br />
TSLTAADTATYLCARGIYSDNNYYAL<br />
서열 번호: 188<br />
QASETIGNALA<br />
서열 번호: 189<br />
KASKLAS<br />
서열 번호: <strong>19</strong>0<br />
QWCYFGDSV<br />
서열 번호: <strong>19</strong>1<br />
SGYYMC<br />
서열 번호: <strong>19</strong>2<br />
CIFTITTNTYYASWAKG<br />
서열 번호: <strong>19</strong>3<br />
GIYSDNNYYAL<br />
서열 번호: <strong>19</strong>4<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGATGTTGTGATGACCCAGACTCCAGCCTCCGTGGAG<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTGAGACCATTGGCAATGCATTAGCCTGGTATCAGCAGAAATCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTACAAGGCATCCAAACTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTACACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAATGGTGTTATTTTGGTGATAGTGTT<br />
서열 번호: <strong>19</strong>5<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCACTGTGCTCAAAGGTGTCCAGTGTCAGGAGCAGCTGGTGGAGTCCGGGGGAGGCCTGGTCCAGCCTGAG<br />
GGATCCCTGACACTCACCTGCACAGCCTCTGGATTCGACTTCAGTAGCGGCTACTACATGTGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATC<br />
GCGTGTATTTTCACTATTACTACTAACACTTACTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAGACCTCGTCGACCACGGTGACTCTGCAAATG<br />
ACCAGTCTGACAGCCGCGGACACGGCCACCTATCTCTGTGCGAGAGGGATTTATTCTGATAATAATTATTATGCCTTG<br />
서열 번호: <strong>19</strong>6<br />
CAGGCCAGTGAGACCATTGGCAATGCATTAGCC<br />
서열 번호: <strong>19</strong>7<br />
AAGGCATCCAAACTGGCATCT<br />
서열 번호: <strong>19</strong>8<br />
- 147 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1361]<br />
[1362]<br />
[1363]<br />
[1364]<br />
[1365]<br />
[1366]<br />
[1367]<br />
[1368]<br />
[1369]<br />
[1370]<br />
[1371]<br />
[1372]<br />
[1373]<br />
[1374]<br />
[1375]<br />
[1376]<br />
[1377]<br />
[1378]<br />
[1379]<br />
[1380]<br />
[1381]<br />
[1382]<br />
[1383]<br />
[1384]<br />
[1385]<br />
[1386]<br />
[1387]<br />
[1388]<br />
[1389]<br />
[1390]<br />
CAATGGTGTTATTTTGGTGATAGTGTT<br />
서열 번호: <strong>19</strong>9<br />
AGCGGCTACTACATGTGC<br />
서열 번호: 200<br />
TGTATTTTCACTATTACTACTAACACTTACTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 201<br />
GGGATTTATTCTGATAATAATTATTATGCCTTG<br />
서열 번호: 202<br />
MDTRAPTQLLGLLLLWLPGARCDVVMTQTPASVEAAVGGTVTIKCQASESIGNALAWYQQKPGQPPKLLIYKASTLASGVPSRFSGSGSGTEFTLTISGVQC<br />
ADAAAYYCQWCYFGDSV<br />
서열 번호: 203<br />
METGLRWLLLVAVLKGVQCQQQLVESGGGLVKPGASLTLTCKASGFSFSSGYYMCWVRQAPGKGLESIACIFTITDNTYYANWAKGRFTISKPSSPTVTLQM<br />
TSLTAADTATYFCARGIYSTDNYYAL<br />
서열 번호: 204<br />
QASESIGNALA<br />
서열 번호: 205<br />
KASTLAS<br />
서열 번호: 206<br />
QWCYFGDSV<br />
서열 번호: 207<br />
SGYYMC<br />
서열 번호: 208<br />
CIFTITDNTYYANWAKG<br />
서열 번호: 209<br />
GIYSTDNYYAL<br />
서열 번호: 210<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGATGTTGTGATGACCCAGACTCCAGCCTCCGTGGAG<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTGAGAGCATTGGCAATGCATTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTACAAGGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAGCGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGGCGTGCAGTGT<br />
GCCGATGCTGCCGCTTACTACTGTCAATGGTGTTATTTTGGTGATAGTGTT<br />
서열 번호: 211<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGCAGCAGCTGGTGGAGTCCGGGGGAGGCCTGGTCAAGCCGGGG<br />
GCATCCCTGACACTCACCTGCAAAGCCTCTGGATTCTCCTTCAGTAGCGGCTACTACATGTGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTCGATC<br />
GCATGCATTTTTACTATTACTGATAACACTTACTACGCGAACTGGGCGAAAGGCCGATTCACCATCTCCAAGCCCTCGTCGCCCACGGTGACTCTGCAAATG<br />
ACCAGTCTGACAGCCGCGGACACGGCCACCTATTTCTGTGCGAGGGGGATTTATTCTACTGATAATTATTATGCCTTG<br />
서열 번호: 2<strong>12</strong><br />
CAGGCCAGTGAGAGCATTGGCAATGCATTAGCC<br />
서열 번호: 213<br />
- 148 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1391]<br />
[1392]<br />
[1393]<br />
[1394]<br />
[1395]<br />
[1396]<br />
[1397]<br />
[1398]<br />
[1399]<br />
[1400]<br />
[1401]<br />
[1402]<br />
[1403]<br />
[1404]<br />
[1405]<br />
[1406]<br />
[1407]<br />
[1408]<br />
[1409]<br />
[1410]<br />
[1411]<br />
[14<strong>12</strong>]<br />
[1413]<br />
[1414]<br />
[1415]<br />
[1416]<br />
[1417]<br />
[1418]<br />
[14<strong>19</strong>]<br />
[1420]<br />
AAGGCATCCACTCTGGCATCT<br />
서열 번호: 214<br />
CAATGGTGTTATTTTGGTGATAGTGTT<br />
서열 번호: 215<br />
AGCGGCTACTACATGTGC<br />
서열 번호: 216<br />
TGCATTTTTACTATTACTGATAACACTTACTACGCGAACTGGGCGAAAGGC<br />
서열 번호: 217<br />
GGGATTTATTCTACTGATAATTATTATGCCTTG<br />
서열 번호: 218<br />
MDTRAPTQLLGLLLLWLPGARCDVVMTQTPASVEAAVGGTVTIKCQASQSVSSYLNWYQQKPGQPPKLLIYRASTLESGVPSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQCTYGTSSSYGAA<br />
서열 번호: 2<strong>19</strong><br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGISLSSNAISWVRQAPGKGLEWIGIISYSGTTYYASWAKGRFTISKTSSTTVDLKITSP<br />
TTEDTATYFCARDDPTTVMVMLIPFGAGMDL<br />
서열 번호: 220<br />
QASQSVSSYLN<br />
서열 번호: 221<br />
RASTLES<br />
서열 번호: 222<br />
QCTYGTSSSYGAA<br />
서열 번호: 223<br />
SNAIS<br />
서열 번호: 224<br />
IISYSGTTYYASWAKG<br />
서열 번호: 225<br />
DDPTTVMVMLIPFGAGMDL<br />
서열 번호: 226<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGATGTTGTGATGACCCAGACTCCAGCCTCCGTGGAG<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCGTTAGTAGCTACTTAAACTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTACAGGGCATCCACTCTGGAATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAATGTACTTATGGTACTAGTAGTAGTTATGGTGCTGCT<br />
서열 번호: 227<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACCGTCTCTGGTATCTCCCTCAGTAGCAATGCAATAAGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTAGTTATAGTGGTACCACATACTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGTCGACCACGGTGGATCTGAAAATCACTAGTCCG<br />
ACAACCGAGGACACGGCCACCTACTTCTGTGCCAGAGATGACCCTACGACAGTTATGGTTATGTTGATACCTTTTGGAGCCGGCATGGACCTC<br />
서열 번호: 228<br />
- 149 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1421]<br />
[1422]<br />
[1423]<br />
[1424]<br />
[1425]<br />
[1426]<br />
[1427]<br />
[1428]<br />
[1429]<br />
[1430]<br />
[1431]<br />
[1432]<br />
[1433]<br />
[1434]<br />
[1435]<br />
[1436]<br />
[1437]<br />
[1438]<br />
[1439]<br />
[1440]<br />
[1441]<br />
[1442]<br />
[1443]<br />
[1444]<br />
[1445]<br />
[1446]<br />
[1447]<br />
[1448]<br />
[1449]<br />
[1450]<br />
[1451]<br />
CAGGCCAGTCAGAGCGTTAGTAGCTACTTAAAC<br />
서열 번호: 229<br />
AGGGCATCCACTCTGGAATCT<br />
서열 번호: 230<br />
CAATGTACTTATGGTACTAGTAGTAGTTATGGTGCTGCT<br />
서열 번호: 231<br />
AGCAATGCAATAAGC<br />
서열 번호: 232<br />
ATCATTAGTTATAGTGGTACCACATACTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 233<br />
GATGACCCTACGACAGTTATGGTTATGTTGATACCTTTTGGAGCCGGCATGGACCTC<br />
서열 번호: 234<br />
MDTRAPTQLLGLLLLWLPGATFAQVLTQTASPVSAAVGGTVTINCQASQSVYKNNYLSWYQQKPGQPPKGLIYSASTLDSGVPLRFSGSGSGTQFTLTISDV<br />
QCDDAATYYCLGSYDCSSGDCYA<br />
서열 번호: 235<br />
METGLRWLLLVAVLKGVQCQSLEESGGDLVKPEGSLTLTCTASGFSFSSYWMCWVRQAPGKGLEWIACIVTGNGNTYYANWAKGRFTISKTSSTTVTLQMTS<br />
LTAADTATYFCAKAYDL<br />
서열 번호: 236<br />
QASQSVYKNNYLS<br />
서열 번호: 237<br />
SASTLDS<br />
서열 번호: 238<br />
LGSYDCSSGDCYA<br />
서열 번호: 239<br />
SYWMC<br />
서열 번호: 240<br />
CIVTGNGNTYYANWAKG<br />
서열 번호: 241<br />
AYDL<br />
서열 번호: 242<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCCAAGTGCTGACCCAGACTGCATCGCCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAACTGCCAGGCCAGTCAGAGTGTTTATAAGAACAACTACTTATCCTGGTATCAGCAGAAACCAGGGCAGCCTCCC<br />
AAAGGCCTGATCTATTCTGCATCGACTCTAGATTCTGGGGTCCCATTGCGGTTCAGCGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCTAGGCAGTTATGATTGTAGTAGTGGTGATTGTTATGCT<br />
서열 번호: 243<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGTTGGAGGAGTCCGGGGGAGACCTGGTCAAGCCTGAGGGA<br />
TCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCTTCAGTAGCTACTGGATGTGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATCGCATGC<br />
ATTGTTACTGGTAATGGTAACACTTACTACGCGAACTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGTCGACCACGGTGACTCTGCAAATGACCAGT<br />
- 150 -
[1452]<br />
[1453]<br />
[1454]<br />
[1455]<br />
[1456]<br />
[1457]<br />
[1458]<br />
[1459]<br />
[1460]<br />
[1461]<br />
[1462]<br />
[1463]<br />
[1464]<br />
[1465]<br />
[1466]<br />
[1467]<br />
[1468]<br />
[1469]<br />
[1470]<br />
[1471]<br />
[1472]<br />
[1473]<br />
[1474]<br />
[1475]<br />
[1476]<br />
[1477]<br />
[1478]<br />
[1479]<br />
[1480]<br />
[1481]<br />
[1482]<br />
CTGACAGCCGCGGACACGGCCACCTATTTTTGTGCGAAAGCCTATGACTTG<br />
서열 번호: 244<br />
CAGGCCAGTCAGAGTGTTTATAAGAACAACTACTTATCC<br />
서열 번호: 245<br />
TCTGCATCGACTCTAGATTCT<br />
서열 번호: 246<br />
CTAGGCAGTTATGATTGTAGTAGTGGTGATTGTTATGCT<br />
서열 번호: 247<br />
AGCTACTGGATGTGC<br />
서열 번호: 248<br />
TGCATTGTTACTGGTAATGGTAACACTTACTACGCGAACTGGGCGAAAGGC<br />
서열 번호: 249<br />
GCCTATGACTTG<br />
서열 번호: 250<br />
MDTRAPTQLLGLLLLWLPGSTFAAVLTQTPSPVSAAVGGTVSISCQASQSVYDNNYLSWYQQKPGQPPKLLIYGASTLASGVPSRFKGTGSGTQFTLTITDV<br />
QCDDAATYYCAGVFNDDSDDA<br />
서열 번호: 251<br />
METGLRWLLLVAVPKGVQCQSLEESGGRLVTPGTPLTLTCTLSGFSLSAYYMSWVRQAPGKGLEWIGFITLSDHISYARWAKGRFTISKTSTTVDLKMTSPT<br />
TEDTATYFCARSRGWGAMGRLDL<br />
서열 번호: 252<br />
QASQSVYDNNYLS<br />
서열 번호: 253<br />
GASTLAS<br />
서열 번호: 254<br />
AGVFNDDSDDA<br />
서열 번호: 255<br />
AYYMS<br />
서열 번호: 256<br />
FITLSDHISYARWAKG<br />
서열 번호: 257<br />
SRGWGAMGRLDL<br />
서열 번호: 258<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTTCCACATTTGCCGCCGTGCTGACCCAGACTCCATCTCCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGGCCAGTCAGAGTGTTTATGACAACAACTATTTATCCTGGTATCAGCAGAAACCAGGACAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCACGGGATCTGGGACACAGTTCACTCTCACCATCACAGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTATTGTGCAGGCGTTTTTAATGATGATAGTGATGATGCC<br />
서열 번호: 259<br />
- 151 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1483]<br />
[1484]<br />
[1485]<br />
[1486]<br />
[1487]<br />
[1488]<br />
[1489]<br />
[1490]<br />
[1491]<br />
[1492]<br />
[1493]<br />
[1494]<br />
[1495]<br />
[1496]<br />
[1497]<br />
[1498]<br />
[1499]<br />
[1500]<br />
[1501]<br />
[1502]<br />
[1503]<br />
[1504]<br />
[1505]<br />
[1506]<br />
[1507]<br />
[1508]<br />
[1509]<br />
[1510]<br />
[1511]<br />
[15<strong>12</strong>]<br />
[1513]<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCCCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACACTCTCTGGATTCTCCCTCAGTGCATACTATATGAGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGATTC<br />
ATTACTCTGAGTGATCATATATCTTACGCGAGGTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGGAGTCGTGGCTGGGGTGCAATGGGTCGGTTGGATCTC<br />
서열 번호: 260<br />
CAGGCCAGTCAGAGTGTTTATGACAACAACTATTTATCC<br />
서열 번호: 261<br />
GGTGCATCCACTCTGGCATCT<br />
서열 번호: 262<br />
GCAGGCGTTTTTAATGATGATAGTGATGATGCC<br />
서열 번호: 263<br />
GCATACTATATGAGC<br />
서열 번호: 264<br />
TTCATTACTCTGAGTGATCATATATCTTACGCGAGGTGGGCGAAAGGC<br />
서열 번호: 265<br />
AGTCGTGGCTGGGGTGCAATGGGTCGGTTGGATCTC<br />
서열 번호: 266<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSAAVGGTVTISCQASQSVYNNKNLAWYQQKSGQPPKLLIYWASTLASGVSSRFSGSGSGTQFTLTVSGV<br />
QCDDAATYYCLGVFDDDADNA<br />
서열 번호: 267<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTASGFSLSSYSMTWVRQAPGKGLEYIGVIGTSGSTYYATWAKGRFTISRTSTTVALKITSPT<br />
TEDTATYFCVRSLSSITFL<br />
서열 번호: 268<br />
QASQSVYNNKNLA<br />
서열 번호: 269<br />
WASTLAS<br />
서열 번호: 270<br />
LGVFDDDADNA<br />
서열 번호: 271<br />
SYSMT<br />
서열 번호: 272<br />
VIGTSGSTYYATWAKG<br />
서열 번호: 273<br />
SLSSITFL<br />
서열 번호: 274<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTCGCAGCCGTGCTGACCCAGACACCATCGCCCGTGTCT<br />
GCGGCTGTGGGAGGCACAGTCACCATCAGTTGCCAGGCCAGTCAGAGTGTTTATAACAACAAAAATTTAGCCTGGTATCAGCAGAAATCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTACTGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAGCGGCAGTGGATCTGGGACACAGTTCACTCTCACCGTCAGCGGCGTG<br />
- 152 -
[1514]<br />
[1515]<br />
[1516]<br />
[1517]<br />
[1518]<br />
[15<strong>19</strong>]<br />
[1520]<br />
[1521]<br />
[1522]<br />
[1523]<br />
[1524]<br />
[1525]<br />
[1526]<br />
[1527]<br />
[1528]<br />
[1529]<br />
[1530]<br />
[1531]<br />
[1532]<br />
[1533]<br />
[1534]<br />
[1535]<br />
[1536]<br />
[1537]<br />
[1538]<br />
[1539]<br />
[1540]<br />
[1541]<br />
[1542]<br />
[1543]<br />
[1544]<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCTAGGCGTTTTTGATGATGATGCTGATAATGCT<br />
서열 번호: 275<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAATGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAGCTACTCCATGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATATATCGGAGTC<br />
ATTGGTACTAGTGGTAGCACATACTACGCGACCTGGGCGAAAGGCCGATTCACCATCTCCAGAACCTCGACCACGGTGGCTCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGTCAGGAGTCTTTCTTCTATTACTTTCTTG<br />
서열 번호: 276<br />
CAGGCCAGTCAGAGTGTTTATAACAACAAAAATTTAGCC<br />
서열 번호: 277<br />
TGGGCATCCACTCTGGCATCT<br />
서열 번호: 278<br />
CTAGGCGTTTTTGATGATGATGCTGATAATGCT<br />
서열 번호: 279<br />
AGCTACTCCATGACC<br />
서열 번호: 280<br />
GTCATTGGTACTAGTGGTAGCACATACTACGCGACCTGGGCGAAAGGC<br />
서열 번호: 281<br />
AGTCTTTCTTCTATTACTTTCTTG<br />
서열 번호: 282<br />
MDTRAPTQLLGLLLLWLPGARCAFELTQTPASVEAAVGGTVTINCQASQNIYRYLAWYQQKPGQPPKFLIYLASTLASGVPSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQSYYSSNSVA<br />
서열 번호: 283<br />
METGLRWLLLVAVLKGVQCQEQLVESGGDLVQPEGSLTLTCTASELDFSSGYWICWVRQVPGKGLEWIGCIYTGSSGSTFYASWAKGRFTISKTSSTTVTLQ<br />
MTSLTAADTATYFCARGYSGFGYFKL<br />
서열 번호: 284<br />
QASQNIYRYLA<br />
서열 번호: 285<br />
LASTLAS<br />
서열 번호: 286<br />
QSYYSSNSVA<br />
서열 번호: 287<br />
SGYWIC<br />
서열 번호: 288<br />
CIYTGSSGSTFYASWAKG<br />
서열 번호: 289<br />
GYSGFGYFKL<br />
서열 번호: 290<br />
- 153 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1545]<br />
[1546]<br />
[1547]<br />
[1548]<br />
[1549]<br />
[1550]<br />
[1551]<br />
[1552]<br />
[1553]<br />
[1554]<br />
[1555]<br />
[1556]<br />
[1557]<br />
[1558]<br />
[1559]<br />
[1560]<br />
[1561]<br />
[1562]<br />
[1563]<br />
[1564]<br />
[1565]<br />
[1566]<br />
[1567]<br />
[1568]<br />
[1569]<br />
[1570]<br />
[1571]<br />
[1572]<br />
[1573]<br />
[1574]<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCATTCGAATTGACCCAGACTCCAGCCTCCGTGGAG<br />
GCAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTCAGAACATTTATAGATACTTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGTTC<br />
CTGATCTATCTGGCATCTACTCTGGCATCTGGGGTCCCATCGCGGTTTAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAAAGTTATTATAGTAGTAATAGTGTCGCT<br />
서열 번호: 291<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGGAGCAGCTGGTGGAGTCCGGGGGAGACCTGGTCCAGCCTGAG<br />
GGATCCCTGACACTCACCTGCACAGCTTCTGAGTTAGACTTCAGTAGCGGCTACTGGATATGCTGGGTCCGCCAGGTTCCAGGGAAGGGGCTGGAGTGGATC<br />
GGATGCATTTATACTGGTAGTAGTGGTAGCACTTTTTACGCGAGTTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGTCGACCACGGTGACTCTGCAA<br />
ATGACCAGTCTGACAGCCGCGGACACGGCCACCTATTTCTGTGCGAGAGGTTATAGTGGCTTTGGTTACTTTAAGTTG<br />
서열 번호: 292<br />
CAGGCCAGTCAGAACATTTATAGATACTTAGCC<br />
서열 번호: 293<br />
CTGGCATCTACTCTGGCATCT<br />
서열 번호: 294<br />
CAAAGTTATTATAGTAGTAATAGTGTCGCT<br />
서열 번호: 295<br />
AGCGGCTACTGGATATGC<br />
서열 번호: 296<br />
TGCATTTATACTGGTAGTAGTGGTAGCACTTTTTACGCGAGTTGGGCGAAAGGC<br />
서열 번호: 297<br />
GGTTATAGTGGCTTTGGTTACTTTAAGTTG<br />
서열 번호: 298<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVEVAVGGTVTIKCQASEDIYRLLAWYQQKPGQPPKLLIYDSSDLASGVPSRFKGSGSGTEFTLAISGVQC<br />
DDAATYYCQQAWSYSDIDNA<br />
서열 번호: 299<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTASGFSLSSYYMSWVRQAPGKGLEWIGIITTSGNTFYASWAKGRLTISRTSTTVDLKITSPT<br />
TEDTATYFCARTSDIFYYRNL<br />
서열 번호: 300<br />
QASEDIYRLLA<br />
서열 번호: 301<br />
DSSDLAS<br />
서열 번호: 302<br />
QQAWSYSDIDNA<br />
서열 번호: 303<br />
SYYMS<br />
서열 번호: 304<br />
IITTSGNTFYASWAKG<br />
서열 번호: 305<br />
- 154 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1575]<br />
[1576]<br />
[1577]<br />
[1578]<br />
[1579]<br />
[1580]<br />
[1581]<br />
[1582]<br />
[1583]<br />
[1584]<br />
[1585]<br />
[1586]<br />
[1587]<br />
[1588]<br />
[1589]<br />
[1590]<br />
[1591]<br />
[1592]<br />
[1593]<br />
[1594]<br />
[1595]<br />
[1596]<br />
[1597]<br />
[1598]<br />
[1599]<br />
[1600]<br />
[1601]<br />
[1602]<br />
[1603]<br />
[1604]<br />
TSDIFYYRNL<br />
서열 번호: 306<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCTGTGGAG<br />
GTAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTGAGGACATTTATAGGTTATTGGCCTGGTATCAACAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTATGATTCATCCGATCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCGCCATCAGCGGTGTGCAGTGT<br />
GACGATGCTGCCACTTACTACTGTCAACAGGCTTGGAGTTATAGTGATATTGATAATGCT<br />
서열 번호: 307<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCGGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAGCTACTACATGAGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTACTACTAGTGGTAATACATTTTACGCGAGCTGGGCGAAAGGCCGGCTCACCATCTCCAGAACCTCGACCACGGTGGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAACTTCTGATATTTTTTATTATCGTAACTTG<br />
서열 번호: 308<br />
CAGGCCAGTGAGGACATTTATAGGTTATTGGCC<br />
서열 번호: 309<br />
GATTCATCCGATCTGGCATCT<br />
서열 번호: 310<br />
CAACAGGCTTGGAGTTATAGTGATATTGATAATGCT<br />
서열 번호: 311<br />
AGCTACTACATGAGC<br />
서열 번호: 3<strong>12</strong><br />
ATCATTACTACTAGTGGTAATACATTTTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 313<br />
ACTTCTGATATTTTTTATTATCGTAACTTG<br />
서열 번호: 314<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTASPVSAAVGATVTINCQSSQSVYNDMDLAWFQQKPGQPPKLLIYSASTLASGVPSRFSGSGSGTEFTLTISGV<br />
QCDDAATYYCLGAFDDDADNT<br />
서열 번호: 315<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGFSLTRHAITWVRQAPGKGLEWIGCIWSGGSTYYATWAKGRFTISKTSTTVDLRITSPT<br />
TEDTATYFCARVIGDTAGYAYFTGLDL<br />
서열 번호: 316<br />
QSSQSVYNDMDLA<br />
서열 번호: 317<br />
SASTLAS<br />
서열 번호: 318<br />
LGAFDDDADNT<br />
서열 번호: 3<strong>19</strong><br />
RHAIT<br />
서열 번호: 320<br />
- 155 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1605]<br />
[1606]<br />
[1607]<br />
[1608]<br />
[1609]<br />
[1610]<br />
[1611]<br />
[16<strong>12</strong>]<br />
[1613]<br />
[1614]<br />
[1615]<br />
[1616]<br />
[1617]<br />
[1618]<br />
[16<strong>19</strong>]<br />
[1620]<br />
[1621]<br />
[1622]<br />
[1623]<br />
[1624]<br />
[1625]<br />
[1626]<br />
[1627]<br />
[1628]<br />
[1629]<br />
[1630]<br />
[1631]<br />
[1632]<br />
[1633]<br />
[1634]<br />
CIWSGGSTYYATWAKG<br />
서열 번호: 321<br />
VIGDTAGYAYFTGLDL<br />
서열 번호: 322<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACGTTTGCAGCCGTGCTGACCCAGACTGCATCACCCGTGTCT<br />
GCCGCTGTGGGAGCCACAGTCACCATCAACTGCCAGTCCAGTCAGAGTGTTTATAATGACATGGACTTAGCCTGGTTTCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATTCTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAGCGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGGCGTG<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCTAGGCGCTTTTGATGATGATGCTGATAATACT<br />
서열 번호: 323<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGATTCTCCCTCACTAGGCATGCAATAACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGATGC<br />
ATTTGGAGTGGTGGTAGCACATACTACGCGACCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTCAGAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTACTTCTGTGCCAGAGTCATTGGCGATACTGCTGGTTATGCTTATTTTACGGGGCTTGACTTG<br />
서열 번호: 324<br />
CAGTCCAGTCAGAGTGTTTATAATGACATGGACTTAGCC<br />
서열 번호: 325<br />
TCTGCATCCACTCTGGCATCT<br />
서열 번호: 326<br />
CTAGGCGCTTTTGATGATGATGCTGATAATACT<br />
서열 번호: 327<br />
AGGCATGCAATAACC<br />
서열 번호: 328<br />
TGCATTTGGAGTGGTGGTAGCACATACTACGCGACCTGGGCGAAAGGC<br />
서열 번호: 329<br />
GTCATTGGCGATACTGCTGGTTATGCTTATTTTACGGGGCTTGACTTG<br />
서열 번호: 330<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVEVAVGGTVTIKCQASQSVYNWLSWYQQKPGQPPKLLIYTASSLASGVPSRFSGSGSGTEFTLTISGVEC<br />
ADAATYYCQQGYTSDVDNV<br />
서열 번호: 331<br />
METGLRWLLLVAVLKGVQCQSLEEAGGRLVTPGTPLTLTCTVSGIDLSSYAMGWVRQAPGKGLEYIGIISSSGSTYYATWAKGRFTISQASSTTVDLKITSP<br />
TTEDSATYFCARGGAGSGGVWLLDGFDP<br />
서열 번호: 332<br />
QASQSVYNWLS<br />
서열 번호: 333<br />
TASSLAS<br />
서열 번호: 334<br />
QQGYTSDVDNV<br />
서열 번호: 335<br />
- 156 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1635]<br />
[1636]<br />
[1637]<br />
[1638]<br />
[1639]<br />
[1640]<br />
[1641]<br />
[1642]<br />
[1643]<br />
[1644]<br />
[1645]<br />
[1646]<br />
[1647]<br />
[1648]<br />
[1649]<br />
[1650]<br />
[1651]<br />
[1652]<br />
[1653]<br />
[1654]<br />
[1655]<br />
[1656]<br />
[1657]<br />
[1658]<br />
[1659]<br />
[1660]<br />
[1661]<br />
[1662]<br />
[1663]<br />
[1664]<br />
SYAMG<br />
서열 번호: 336<br />
IISSSGSTYYATWAKG<br />
서열 번호: 337<br />
GGAGSGGVWLLDGFDP<br />
서열 번호: 338<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCTGTGGAG<br />
GTAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGTGTTTATAATTGGTTATCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTATACTGCATCCAGTCTGGCATCTGGGGTCCCATCGCGGTTCAGTGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGGCGTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAACAGGGTTATACTAGTGATGTTGATAATGTT<br />
서열 번호: 339<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGGCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGAATCGACCTCAGTAGCTATGCAATGGGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATACATCGGAATC<br />
ATTAGTAGTAGTGGTAGCACATACTACGCGACCTGGGCGAAAGGCCGATTCACCATCTCACAAGCCTCGTCGACCACGGTGGATCTGAAAATTACCAGTCCG<br />
ACAACCGAGGACTCGGCCACATATTTCTGTGCCAGAGGGGGTGCTGGTAGTGGTGGTGTTTGGCTGCTTGATGGTTTTGATCCC<br />
서열 번호: 340<br />
CAGGCCAGTCAGAGTGTTTATAATTGGTTATCC<br />
서열 번호: 341<br />
ACTGCATCCAGTCTGGCATCT<br />
서열 번호: 342<br />
CAACAGGGTTATACTAGTGATGTTGATAATGTT<br />
서열 번호: 343<br />
AGCTATGCAATGGGC<br />
서열 번호: 344<br />
ATCATTAGTAGTAGTGGTAGCACATACTACGCGACCTGGGCGAAAGGC<br />
서열 번호: 345<br />
GGGGGTGCTGGTAGTGGTGGTGTTTGGCTGCTTGATGGTTTTGATCCC<br />
서열 번호: 346<br />
MDTRAPTQLLGLLLLWLPGAKCADVVMTQTPASVSAAVGGTVTINCQASENIYNWLAWYQQKPGQPPKLLIYTVGDLASGVSSRFKGSGSGTEFTLTISDLE<br />
CADAATYYCQQGYSSSYVDNV<br />
서열 번호: 347<br />
METGLRWLLLVAVLKGVQCQEQLKESGGRLVTPGTPLTLTCTVSGFSLNDYAVGWFRQAPGKGLEWIGYIRSSGTTAYATWAKGRFTISATSTTVDLKITSP<br />
TTEDTATYFCARGGAGSSGVWILDGFAP<br />
서열 번호: 348<br />
QASENIYNWLA<br />
서열 번호: 349<br />
TVGDLAS<br />
서열 번호: 350<br />
- 157 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1665]<br />
[1666]<br />
[1667]<br />
[1668]<br />
[1669]<br />
[1670]<br />
[1671]<br />
[1672]<br />
[1673]<br />
[1674]<br />
[1675]<br />
[1676]<br />
[1677]<br />
[1678]<br />
[1679]<br />
[1680]<br />
[1681]<br />
[1682]<br />
[1683]<br />
[1684]<br />
[1685]<br />
[1686]<br />
[1687]<br />
[1688]<br />
[1689]<br />
[1690]<br />
[1691]<br />
[1692]<br />
[1693]<br />
[1694]<br />
QQGYSSSYVDNV<br />
서열 번호: 351<br />
DYAVG<br />
서열 번호: 352<br />
YIRSSGTTAYATWAKG<br />
서열 번호: 353<br />
GGAGSSGVWILDGFAP<br />
서열 번호: 354<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAAATGTGCCGATGTTGTGATGACCCAGACTCCAGCCTCCGTG<br />
TCTGCAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTGAGAACATTTATAATTGGTTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAG<br />
CTCCTGATCTATACTGTAGGCGATCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAG<br />
TGTGCCGATGCTGCCACTTACTATTGTCAACAGGGTTATAGTAGTAGTTATGTTGATAATGTT<br />
서열 번호: 355<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGGAGCAGCTGAAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGG<br />
ACACCCCTGACACTCACCTGCACAGTCTCTGGATTCTCCCTCAATGACTATGCAGTGGGCTGGTTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGA<br />
TACATTCGTAGTAGTGGTACCACAGCCTACGCGACCTGGGCGAAAGGCCGATTCACCATCTCCGCTACCTCGACCACGGTGGATCTGAAAATCACCAGTCCG<br />
ACAACCGAGGACACGGCCACCTATTTCTGTGCCAGAGGGGGTGCTGGTAGTAGTGGTGTGTGGATCCTTGATGGTTTTGCTCCC<br />
서열 번호: 356<br />
CAGGCCAGTGAGAACATTTATAATTGGTTAGCC<br />
서열 번호: 357<br />
ACTGTAGGCGATCTGGCATCT<br />
서열 번호: 358<br />
CAACAGGGTTATAGTAGTAGTTATGTTGATAATGTT<br />
서열 번호: 359<br />
GACTATGCAGTGGGC<br />
서열 번호: 360<br />
TACATTCGTAGTAGTGGTACCACAGCCTACGCGACCTGGGCGAAAGGC<br />
서열 번호: 361<br />
GGGGGTGCTGGTAGTAGTGGTGTGTGGATCCTTGATGGTTTTGCTCCC<br />
서열 번호: 362<br />
MDTRAPTQLLGLLLLWLPGATFAQVLTQTPSSVSAAVGGTVTINCQASQSVYQNNYLSWFQQKPGQPPKLLIYGAATLASGVPSRFKGSGSGTQFTLTISDL<br />
ECDDAATYYCAGAYRDVDS<br />
서열 번호: 363<br />
METGLRWLLLVAVLKGVQCQSLEESGGDLVKPGASLTLTCTASGFSFTSTYYIYWVRQAPGKGLEWIACIDAGSSGSTYYATWVNGRFTISKTSSTTVTLQM<br />
TSLTAADTATYFCAKWDYGGNVGWGYDL<br />
서열 번호: 364<br />
QASQSVYQNNYLS<br />
서열 번호: 365<br />
- 158 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1695]<br />
[1696]<br />
[1697]<br />
[1698]<br />
[1699]<br />
[1700]<br />
[1701]<br />
[1702]<br />
[1703]<br />
[1704]<br />
[1705]<br />
[1706]<br />
[1707]<br />
[1708]<br />
[1709]<br />
[1710]<br />
[1711]<br />
[17<strong>12</strong>]<br />
[1713]<br />
[1714]<br />
[1715]<br />
[1716]<br />
[1717]<br />
[1718]<br />
[17<strong>19</strong>]<br />
[1720]<br />
[1721]<br />
[1722]<br />
[1723]<br />
[1724]<br />
GAATLAS<br />
서열 번호: 366<br />
AGAYRDVDS<br />
서열 번호: 367<br />
STYYIY<br />
서열 번호: 368<br />
CIDAGSSGSTYYATWVNG<br />
서열 번호: 369<br />
WDYGGNVGWGYDL<br />
서열 번호: 370<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCTCAAGTGCTGACCCAGACTCCATCCTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTCAGAGTGTTTATCAGAACAACTACTTATCCTGGTTTCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCGGCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACCTG<br />
GAGTGTGACGATGCTGCCACTTACTACTGTGCAGGCGCTTATAGGGATGTGGATTCT<br />
서열 번호: 371<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGTTGGAGGAGTCCGGGGGAGACCTGGTCAAGCCTGGGGCA<br />
TCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCTTTACTAGTACCTACTACATCTACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATCGCA<br />
TGTATTGATGCTGGTAGTAGTGGTAGCACTTACTACGCGACCTGGGTGAATGGCCGATTCACCATCTCCAAAACCTCGTCGACCACGGTGACTCTGCAAATG<br />
ACCAGTCTGACAGCCGCGGACACGGCCACCTATTTCTGTGCGAAATGGGATTATGGTGGTAATGTTGGTTGGGGTTATGACTTG<br />
서열 번호: 372<br />
CAGGCCAGTCAGAGTGTTTATCAGAACAACTACTTATCC<br />
서열 번호: 373<br />
GGTGCGGCCACTCTGGCATCT<br />
서열 번호: 374<br />
GCAGGCGCTTATAGGGATGTGGATTCT<br />
서열 번호: 375<br />
AGTACCTACTACATCTAC<br />
서열 번호: 376<br />
TGTATTGATGCTGGTAGTAGTGGTAGCACTTACTACGCGACCTGGGTGAATGGC<br />
서열 번호: 377<br />
TGGGATTATGGTGGTAATGTTGGTTGGGGTTATGACTTG<br />
서열 번호: 378<br />
MDTRAPTQLLGLLLLWLPGARCAFELTQTPSSVEAAVGGTVTIKCQASQSISSYLAWYQQKPGQPPKFLIYRASTLASGVPSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQSYYDSVSNP<br />
서열 번호: 379<br />
METGLRWLLLVAVLKGVQCQSLEESGGDLVKPEGSLTLTCKASGLDLGTYWFMCWVRQAPGKGLEWIACIYTGSSGSTFYASWVNGRFTISKTSSTTVTLQM<br />
TSLTAADTATYFCARGYSGYGYFKL<br />
서열 번호: 380<br />
- 159 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1725]<br />
[1726]<br />
[1727]<br />
[1728]<br />
[1729]<br />
[1730]<br />
[1731]<br />
[1732]<br />
[1733]<br />
[1734]<br />
[1735]<br />
[1736]<br />
[1737]<br />
[1738]<br />
[1739]<br />
[1740]<br />
[1741]<br />
[1742]<br />
[1743]<br />
[1744]<br />
[1745]<br />
[1746]<br />
[1747]<br />
[1748]<br />
[1749]<br />
[1750]<br />
[1751]<br />
[1752]<br />
[1753]<br />
[1754]<br />
[1755]<br />
QASQSISSYLA<br />
서열 번호: 381<br />
RASTLAS<br />
서열 번호: 382<br />
QSYYDSVSNP<br />
서열 번호: 383<br />
TYWFMC<br />
서열 번호: 384<br />
CIYTGSSGSTFYASWVNG<br />
서열 번호: 385<br />
GYSGYGYFKL<br />
서열 번호: 386<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCATTCGAATTGACCCAGACTCCATCCTCCGTGGAG<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCATTAGTAGTTACTTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGTTC<br />
CTGATCTACAGGGCGTCCACTCTGGCATCTGGGGTCCCATCGCGATTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAAAGCTATTATGATAGTGTTTCAAATCCT<br />
서열 번호: 387<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGTTGGAGGAGTCCGGGGGAGACCTGGTCAAGCCTGAGGGA<br />
TCCCTGACACTCACCTGCAAAGCCTCTGGACTCGACCTCGGTACCTACTGGTTCATGTGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATCGCT<br />
TGTATTTATACTGGTAGTAGTGGTTCCACTTTCTACGCGAGCTGGGTGAATGGCCGATTCACCATCTCCAAAACCTCGTCGACCACGGTGACTCTGCAAATG<br />
ACCAGTCTGACAGCCGCGGACACGGCCACTTATTTTTGTGCGAGAGGTTATAGTGGTTATGGTTATTTTAAGTTG<br />
서열 번호: 388<br />
CAGGCCAGTCAGAGCATTAGTAGTTACTTAGCC<br />
서열 번호: 389<br />
AGGGCGTCCACTCTGGCATCT<br />
서열 번호: 390<br />
CAAAGCTATTATGATAGTGTTTCAAATCCT<br />
서열 번호: 391<br />
ACCTACTGGTTCATGTGC<br />
서열 번호: 392<br />
TGTATTTATACTGGTAGTAGTGGTTCCACTTTCTACGCGAGCTGGGTGAATGGC<br />
서열 번호: 393<br />
GGTTATAGTGGTTATGGTTATTTTAAGTTG<br />
서열 번호: 394<br />
MDTRAPTQLLGLLLLWLPGVTFAIEMTQSPFSVSAAVGGTVSISCQASQSVYKNNQLSWYQQKSGQPPKLLIYGASALASGVPSRFKGSGSGTEFTLTISDV<br />
QCDDAATYYCAGAITGSIDTDG<br />
서열 번호: 395<br />
공개특허 10-2011-01<strong>12</strong>308<br />
METGLRWLLLVAVLKGVQCQSLEESGGDLVKPGASLTLTCTTSGFSFSSSYFICWVRQAPGKGLEWIACIYGGDGSTYYASWAKGRFTISKTSSTTVTLQMT<br />
- 160 -
[1756]<br />
[1757]<br />
[1758]<br />
[1759]<br />
[1760]<br />
[1761]<br />
[1762]<br />
[1763]<br />
[1764]<br />
[1765]<br />
[1766]<br />
[1767]<br />
[1768]<br />
[1769]<br />
[1770]<br />
[1771]<br />
[1772]<br />
[1773]<br />
[1774]<br />
[1775]<br />
[1776]<br />
[1777]<br />
[1778]<br />
[1779]<br />
[1780]<br />
[1781]<br />
[1782]<br />
[1783]<br />
[1784]<br />
[1785]<br />
SLTAADTATYFCAREWAYSQGYFGAFDL<br />
서열 번호: 396<br />
QASQSVYKNNQLS<br />
서열 번호: 397<br />
GASALAS<br />
서열 번호: 398<br />
AGAITGSIDTDG<br />
서열 번호: 399<br />
SSYFIC<br />
서열 번호: 400<br />
CIYGGDGSTYYASWAKG<br />
서열 번호: 401<br />
EWAYSQGYFGAFDL<br />
서열 번호: 402<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGTCACATTTGCCATCGAAATGACCCAGAGTCCATTCTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGGCCAGTCAGAGTGTTTATAAGAACAACCAATTATCCTGGTATCAGCAGAAATCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCATCGGCTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTACTGTGCAGGCGCTATTACTGGTAGTATTGATACGGATGGT<br />
서열 번호: 403<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGTTGGAGGAGTCCGGGGGAGACCTGGTCAAGCCTGGGGCA<br />
TCCCTGACACTCACCTGCACAACTTCTGGATTCTCCTTCAGTAGCAGCTACTTCATTTGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATCGCA<br />
TGCATTTATGGTGGTGATGGCAGCACATACTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGTCGACCACGGTGACGCTGCAAATGACC<br />
AGTCTGACAGCCGCGGACACGGCCACCTATTTCTGTGCGAGAGAATGGGCATATAGTCAAGGTTATTTTGGTGCTTTTGATCTC<br />
서열 번호: 404<br />
CAGGCCAGTCAGAGTGTTTATAAGAACAACCAATTATCC<br />
서열 번호: 405<br />
GGTGCATCGGCTCTGGCATCT<br />
서열 번호: 406<br />
GCAGGCGCTATTACTGGTAGTATTGATACGGATGGT<br />
서열 번호: 407<br />
AGCAGCTACTTCATTTGC<br />
서열 번호: 408<br />
TGCATTTATGGTGGTGATGGCAGCACATACTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 409<br />
GAATGGGCATATAGTCAAGGTTATTTTGGTGCTTTTGATCTC<br />
서열 번호: 410<br />
MDTRAPTQLLGLLLLWLPGARCDVVMTQTPASVEAAVGGTVTIKCQASEDISSYLAWYQQKPGQPPKLLIYAASNLESGVSSRFKGSGSGTEYTLTISDLEC<br />
ADAATYYCQCTYGTISISDGNA<br />
- 161 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1786]<br />
[1787]<br />
[1788]<br />
[1789]<br />
[1790]<br />
[1791]<br />
[1792]<br />
[1793]<br />
[1794]<br />
[1795]<br />
[1796]<br />
[1797]<br />
[1798]<br />
[1799]<br />
[1800]<br />
[1801]<br />
[1802]<br />
[1803]<br />
[1804]<br />
[1805]<br />
[1806]<br />
[1807]<br />
[1808]<br />
[1809]<br />
[1810]<br />
[1811]<br />
[18<strong>12</strong>]<br />
[1813]<br />
[1814]<br />
[1815]<br />
[1816]<br />
서열 번호: 411<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGFSLSSYFMTWVRQAPGEGLEYIGFINPGGSAYYASWVKGRFTISKSSTTVDLKITSPT<br />
TEDTATYFCARVLIVSYGAFTI<br />
서열 번호: 4<strong>12</strong><br />
QASEDISSYLA<br />
서열 번호: 413<br />
AASNLES<br />
서열 번호: 414<br />
QCTYGTISISDGNA<br />
서열 번호: 415<br />
SYFMT<br />
서열 번호: 416<br />
FINPGGSAYYASWVKG<br />
서열 번호: 417<br />
VLIVSYGAFTI<br />
서열 번호: 418<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGATGTTGTGATGACCCAGACTCCAGCCTCCGTGGAG<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTGAGGATATTAGTAGCTACTTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTATGCTGCATCCAATCTGGAATCTGGGGTCTCATCGCGATTCAAAGGCAGTGGATCTGGGACAGAGTACACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACCTATTACTGTCAATGTACTTATGGTACTATTTCTATTAGTGATGGTAATGCT<br />
서열 번호: 4<strong>19</strong><br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAATGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGATTCTCCCTCAGTAGCTACTTCATGACCTGGGTCCGCCAGGCTCCAGGGGAGGGGCTGGAATACATCGGATTC<br />
ATTAATCCTGGTGGTAGCGCTTACTACGCGAGCTGGGTGAAAGGCCGATTCACCATCTCCAAGTCCTCGACCACGGTAGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGGGTTCTGATTGTTTCTTATGGAGCCTTTACCATC<br />
서열 번호: 420<br />
CAGGCCAGTGAGGATATTAGTAGCTACTTAGCC<br />
서열 번호: 421<br />
GCTGCATCCAATCTGGAATCT<br />
서열 번호: 422<br />
CAATGTACTTATGGTACTATTTCTATTAGTGATGGTAATGCT<br />
서열 번호: 423<br />
AGCTACTTCATGACC<br />
서열 번호: 424<br />
TTCATTAATCCTGGTGGTAGCGCTTACTACGCGAGCTGGGTGAAAGGC<br />
서열 번호: 425<br />
GTTCTGATTGTTTCTTATGGAGCCTTTACCATC<br />
서열 번호: 426<br />
- 162 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1817]<br />
[1818]<br />
[18<strong>19</strong>]<br />
[1820]<br />
[1821]<br />
[1822]<br />
[1823]<br />
[1824]<br />
[1825]<br />
[1826]<br />
[1827]<br />
[1828]<br />
[1829]<br />
[1830]<br />
[1831]<br />
[1832]<br />
[1833]<br />
[1834]<br />
[1835]<br />
[1836]<br />
[1837]<br />
[1838]<br />
[1839]<br />
[1840]<br />
[1841]<br />
[1842]<br />
[1843]<br />
[1844]<br />
[1845]<br />
[1846]<br />
MDTRAPTQLLGLLLLWLPGARCDVVMTQTPASVSAAVGGTVTIKCQASEDIESYLAWYQQKPGQPPKLLIYGASNLESGVSSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQCTYGIISISDGNA<br />
서열 번호: 427<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGFSLSSYFMTWVRQAPGEGLEYIGFMNTGDNAYYASWAKGRFTISKTSTTVDLKITSPT<br />
TEDTATYFCARVLVVAYGAFNI<br />
서열 번호: 428<br />
QASEDIESYLA<br />
서열 번호: 429<br />
GASNLES<br />
서열 번호: 430<br />
QCTYGIISISDGNA<br />
서열 번호: 431<br />
SYFMT<br />
서열 번호: 432<br />
FMNTGDNAYYASWAKG<br />
서열 번호: 433<br />
VLVVAYGAFNI<br />
서열 번호: 434<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGATGTTGTGATGACCCAGACTCCAGCCTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTGAGGACATTGAAAGCTATCTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTATGGTGCATCCAATCTGGAATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTATTGTCAATGCACTTATGGTATTATTAGTATTAGTGATGGTAATGCT<br />
서열 번호: 435<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTGTCTGGATTCTCCCTCAGTAGCTACTTCATGACCTGGGTCCGCCAGGCTCCAGGGGAGGGGCTGGAATACATCGGATTC<br />
ATGAATACTGGTGATAACGCATACTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGGGTTCTTGTTGTTGCTTATGGAGCCTTTAACATC<br />
서열 번호: 436<br />
CAGGCCAGTGAGGACATTGAAAGCTATCTAGCC<br />
서열 번호: 437<br />
GGTGCATCCAATCTGGAATCT<br />
서열 번호: 438<br />
CAATGCACTTATGGTATTATTAGTATTAGTGATGGTAATGCT<br />
서열 번호: 439<br />
AGCTACTTCATGACC<br />
서열 번호: 440<br />
TTCATGAATACTGGTGATAACGCATACTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 441<br />
- 163 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1847]<br />
[1848]<br />
[1849]<br />
[1850]<br />
[1851]<br />
[1852]<br />
[1853]<br />
[1854]<br />
[1855]<br />
[1856]<br />
[1857]<br />
[1858]<br />
[1859]<br />
[1860]<br />
[1861]<br />
[1862]<br />
[1863]<br />
[1864]<br />
[1865]<br />
[1866]<br />
[1867]<br />
[1868]<br />
[1869]<br />
[1870]<br />
[1871]<br />
[1872]<br />
[1873]<br />
[1874]<br />
[1875]<br />
[1876]<br />
GTTCTTGTTGTTGCTTATGGAGCCTTTAACATC<br />
서열 번호: 442<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSEPVGGTVSISCQSSKSVMNNNYLAWYQQKPGQPPKLLIYGASNLASGVPSRFSGSGSGTQFTLTISDV<br />
QCDDAATYYCQGGYTGYSDHGT<br />
서열 번호: 443<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVKPDETLTLTCTVSGIDLSSYPMNWVRQAPGKGLEWIGFINTGGTIVYASWAKGRFTISKTSTTVDLKMTSPT<br />
TEDTATYFCARGSYVSSGYAYYFNV<br />
서열 번호: 444<br />
QSSKSVMNNNYLA<br />
서열 번호: 445<br />
GASNLAS<br />
서열 번호: 446<br />
QGGYTGYSDHGT<br />
서열 번호: 447<br />
SYPMN<br />
서열 번호: 448<br />
FINTGGTIVYASWAKG<br />
서열 번호: 449<br />
GSYVSSGYAYYFNV<br />
서열 번호: 450<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCGCCGTGCTGACCCAGACTCCATCTCCCGTGTCT<br />
GAACCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGTCCAGTAAGAGTGTTATGAATAACAACTACTTAGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCATCCAATCTGGCATCTGGGGTCCCATCACGGTTCAGCGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCAAGGCGGTTATACTGGTTATAGTGATCATGGGACT<br />
서열 번호: 451<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCAAGCCTGACGAA<br />
ACCCTGACACTCACCTGCACAGTCTCTGGAATCGACCTCAGTAGCTATCCAATGAACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGATTC<br />
ATTAATACTGGTGGTACCATAGTCTACGCGAGCTGGGCAAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGGCAGTTATGTTTCATCTGGTTATGCCTACTATTTTAATGTC<br />
서열 번호: 452<br />
CAGTCCAGTAAGAGTGTTATGAATAACAACTACTTAGCC<br />
서열 번호: 453<br />
GGTGCATCCAATCTGGCATCT<br />
서열 번호: 454<br />
CAAGGCGGTTATACTGGTTATAGTGATCATGGGACT<br />
서열 번호: 455<br />
AGCTATCCAATGAAC<br />
서열 번호: 456<br />
- 164 -<br />
공개특허 10-2011-01<strong>12</strong>308
[1877]<br />
[1878]<br />
[1879]<br />
[1880]<br />
[1881]<br />
[1882]<br />
[1883]<br />
[1884]<br />
[1885]<br />
[1886]<br />
[1887]<br />
[1888]<br />
[1889]<br />
[1890]<br />
[1891]<br />
[1892]<br />
[1893]<br />
[1894]<br />
[1895]<br />
[1896]<br />
[1897]<br />
[1898]<br />
[1899]<br />
[<strong>19</strong>00]<br />
[<strong>19</strong>01]<br />
[<strong>19</strong>02]<br />
[<strong>19</strong>03]<br />
[<strong>19</strong>04]<br />
[<strong>19</strong>05]<br />
[<strong>19</strong>06]<br />
TTCATTAATACTGGTGGTACCATAGTCTACGCGAGCTGGGCAAAAGGC<br />
서열 번호: 457<br />
GGCAGTTATGTTTCATCTGGTTATGCCTACTATTTTAATGTC<br />
서열 번호: 458<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSAAVGGTVSISCQSSQSVYNNNWLSWFQQKPGQPPKLLIYKASTLASGVPSRFKGSGSGTQFTLTISDV<br />
QCDDVATYYCAGGYLDSVI<br />
서열 번호: 459<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGFSLSTYSINWVRQAPGKGLEWIGIIANSGTTFYANWAKGRFTVSKTSTTVDLKITSPT<br />
TEDTATYFCARESGMYNEYGKFNI<br />
서열 번호: 460<br />
QSSQSVYNNNWLS<br />
서열 번호: 461<br />
KASTLAS<br />
서열 번호: 462<br />
AGGYLDSVI<br />
서열 번호: 463<br />
TYSIN<br />
서열 번호: 464<br />
IIANSGTTFYANWAKG<br />
서열 번호: 465<br />
ESGMYNEYGKFNI<br />
서열 번호: 466<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCGCCGTGCTGACCCAGACTCCATCTCCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGTCCAGTCAGAGTGTTTATAATAACAACTGGTTATCCTGGTTTCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTACAAGGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACGTG<br />
CAGTGTGACGATGTTGCCACTTACTACTGTGCGGGCGGTTATCTTGATAGTGTTATT<br />
서열 번호: 467<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGATTCTCCCTCAGTACCTATTCAATAAACTGGGTCCGCCAGGCTCCAGGGAAGGGCCTGGAATGGATCGGAATC<br />
ATTGCTAATAGTGGTACCACATTCTACGCGAACTGGGCGAAAGGCCGATTCACCGTCTCCAAAACCTCGACCACGGTGGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGAGAGTGGAATGTACAATGAATATGGTAAATTTAACATC<br />
서열 번호: 468<br />
CAGTCCAGTCAGAGTGTTTATAATAACAACTGGTTATCC<br />
서열 번호: 469<br />
AAGGCATCCACTCTGGCATCT<br />
서열 번호: 470<br />
GCGGGCGGTTATCTTGATAGTGTTATT<br />
서열 번호: 471<br />
- 165 -<br />
공개특허 10-2011-01<strong>12</strong>308
[<strong>19</strong>07]<br />
[<strong>19</strong>08]<br />
[<strong>19</strong>09]<br />
[<strong>19</strong>10]<br />
[<strong>19</strong>11]<br />
[<strong>19</strong><strong>12</strong>]<br />
[<strong>19</strong>13]<br />
[<strong>19</strong>14]<br />
[<strong>19</strong>15]<br />
[<strong>19</strong>16]<br />
[<strong>19</strong>17]<br />
[<strong>19</strong>18]<br />
[<strong>19</strong><strong>19</strong>]<br />
[<strong>19</strong>20]<br />
[<strong>19</strong>21]<br />
[<strong>19</strong>22]<br />
[<strong>19</strong>23]<br />
[<strong>19</strong>24]<br />
[<strong>19</strong>25]<br />
[<strong>19</strong>26]<br />
[<strong>19</strong>27]<br />
[<strong>19</strong>28]<br />
[<strong>19</strong>29]<br />
[<strong>19</strong>30]<br />
[<strong>19</strong>31]<br />
[<strong>19</strong>32]<br />
[<strong>19</strong>33]<br />
[<strong>19</strong>34]<br />
[<strong>19</strong>35]<br />
[<strong>19</strong>36]<br />
ACCTATTCAATAAAC<br />
서열 번호: 472<br />
ATCATTGCTAATAGTGGTACCACATTCTACGCGAACTGGGCGAAAGGC<br />
서열 번호: 473<br />
GAGAGTGGAATGTACAATGAATATGGTAAATTTAACATC<br />
서열 번호: 474<br />
MDTRAPTQLLGLLLLWLPGARCASDMTQTPSSVSAAVGGTVTINCQASENIYSFLAWYQQKPGQPPKLLIFKASTLASGVSSRFKGSGSGTQFTLTISDLEC<br />
DDAATYYCQQGATVYDIDNN<br />
서열 번호: 475<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTVSGIDLSAYAMIWVRQAPGEGLEWITIIYPNGITYYANWAKGRFTVSKTSTAMDLKITSPT<br />
TEDTATYFCARDAESSKNAYWGYFNV<br />
서열 번호: 476<br />
QASENIYSFLA<br />
서열 번호: 477<br />
KASTLAS<br />
서열 번호: 478<br />
QQGATVYDIDNN<br />
서열 번호: 479<br />
AYAMI<br />
서열 번호: 480<br />
IIYPNGITYYANWAKG<br />
서열 번호: 481<br />
DAESSKNAYWGYFNV<br />
서열 번호: 482<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTCTGATATGACCCAGACTCCATCCTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTGAGAACATTTATAGCTTTTTGGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTTCAAGGCTTCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GACGATGCTGCCACTTACTACTGTCAACAGGGTGCTACTGTGTATGATATTGATAATAAT<br />
서열 번호: 483<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTTTCTGGAATCGACCTCAGTGCCTATGCAATGATCTGGGTCCGCCAGGCTCCAGGGGAGGGGCTGGAATGGATCACAATC<br />
ATTTATCCTAATGGTATCACATACTACGCGAACTGGGCGAAAGGCCGATTCACCGTCTCCAAAACCTCGACCGCGATGGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGATGCAGAAAGTAGTAAGAATGCTTATTGGGGCTACTTTAACGTC<br />
서열 번호: 484<br />
CAGGCCAGTGAGAACATTTATAGCTTTTTGGCC<br />
서열 번호: 485<br />
AAGGCTTCCACTCTGGCATCT<br />
서열 번호: 486<br />
- 166 -<br />
공개특허 10-2011-01<strong>12</strong>308
[<strong>19</strong>37]<br />
[<strong>19</strong>38]<br />
[<strong>19</strong>39]<br />
[<strong>19</strong>40]<br />
[<strong>19</strong>41]<br />
[<strong>19</strong>42]<br />
[<strong>19</strong>43]<br />
[<strong>19</strong>44]<br />
[<strong>19</strong>45]<br />
[<strong>19</strong>46]<br />
[<strong>19</strong>47]<br />
[<strong>19</strong>48]<br />
[<strong>19</strong>49]<br />
[<strong>19</strong>50]<br />
[<strong>19</strong>51]<br />
[<strong>19</strong>52]<br />
[<strong>19</strong>53]<br />
[<strong>19</strong>54]<br />
[<strong>19</strong>55]<br />
[<strong>19</strong>56]<br />
[<strong>19</strong>57]<br />
[<strong>19</strong>58]<br />
[<strong>19</strong>59]<br />
[<strong>19</strong>60]<br />
[<strong>19</strong>61]<br />
[<strong>19</strong>62]<br />
[<strong>19</strong>63]<br />
[<strong>19</strong>64]<br />
[<strong>19</strong>65]<br />
[<strong>19</strong>66]<br />
CAACAGGGTGCTACTGTGTATGATATTGATAATAAT<br />
서열 번호: 487<br />
GCCTATGCAATGATC<br />
서열 번호: 488<br />
ATCATTTATCCTAATGGTATCACATACTACGCGAACTGGGCGAAAGGC<br />
서열 번호: 489<br />
GATGCAGAAAGTAGTAAGAATGCTTATTGGGGCTACTTTAACGTC<br />
서열 번호: 490<br />
MDTRAPTQLLGLLLLWLPGARCASDMTQTPSSVSAAVGGTVTINCQASENIYSFLAWYQQKPGQPPKLLIFRASTLASGVSSRFKGSGSGTQFTLTISDLEC<br />
DDAATYYCQQGATVYDIDNN<br />
서열 번호: 491<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTVSGIDLSAYAMIWVRQAPGEGLEWITIIYPNGITYYANWAKGRFTVSKTSTAMDLKITSPT<br />
TEDTATYFCARDAESSKNAYWGYFNV<br />
서열 번호: 492<br />
QASENIYSFLA<br />
서열 번호: 493<br />
RASTLAS<br />
서열 번호: 494<br />
QQGATVYDIDNN<br />
서열 번호: 495<br />
AYAMI<br />
서열 번호: 496<br />
IIYPNGITYYANWAKG<br />
서열 번호: 497<br />
DAESSKNAYWGYFNV<br />
서열 번호: 498<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTCTGATATGACCCAGACTCCATCCTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTGAGAACATTTATAGCTTTTTGGCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTTCAGGGCTTCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GACGATGCTGCCACTTACTACTGTCAACAGGGTGCTACTGTGTATGATATTGATAATAAT<br />
서열 번호: 499<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTTTCTGGAATCGACCTCAGTGCCTATGCAATGATCTGGGTCCGCCAGGCTCCAGGGGAGGGGCTGGAATGGATCACAATC<br />
ATTTATCCTAATGGTATCACATACTACGCGAACTGGGCGAAAGGCCGATTCACCGTCTCCAAAACCTCGACCGCGATGGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGATGCAGAAAGTAGTAAGAATGCTTATTGGGGCTACTTTAACGTC<br />
서열 번호: 500<br />
CAGGCCAGTGAGAACATTTATAGCTTTTTGGCC<br />
서열 번호: 501<br />
- 167 -<br />
공개특허 10-2011-01<strong>12</strong>308
[<strong>19</strong>67]<br />
[<strong>19</strong>68]<br />
[<strong>19</strong>69]<br />
[<strong>19</strong>70]<br />
[<strong>19</strong>71]<br />
[<strong>19</strong>72]<br />
[<strong>19</strong>73]<br />
[<strong>19</strong>74]<br />
[<strong>19</strong>75]<br />
[<strong>19</strong>76]<br />
[<strong>19</strong>77]<br />
[<strong>19</strong>78]<br />
[<strong>19</strong>79]<br />
[<strong>19</strong>80]<br />
[<strong>19</strong>81]<br />
[<strong>19</strong>82]<br />
[<strong>19</strong>83]<br />
[<strong>19</strong>84]<br />
[<strong>19</strong>85]<br />
[<strong>19</strong>86]<br />
[<strong>19</strong>87]<br />
[<strong>19</strong>88]<br />
[<strong>19</strong>89]<br />
[<strong>19</strong>90]<br />
[<strong>19</strong>91]<br />
[<strong>19</strong>92]<br />
[<strong>19</strong>93]<br />
[<strong>19</strong>94]<br />
[<strong>19</strong>95]<br />
[<strong>19</strong>96]<br />
AGGGCTTCCACTCTGGCATCT<br />
서열 번호: 502<br />
CAACAGGGTGCTACTGTGTATGATATTGATAATAAT<br />
서열 번호: 503<br />
GCCTATGCAATGATC<br />
서열 번호: 504<br />
ATCATTTATCCTAATGGTATCACATACTACGCGAACTGGGCGAAAGGC<br />
서열 번호: 505<br />
GATGCAGAAAGTAGTAAGAATGCTTATTGGGGCTACTTTAACGTC<br />
서열 번호: 506<br />
MDTRAPTQLLGLLLLWLPGATFAIEMTQTPSPVSAAVGGTVTINCQASESVFNNMLSWYQQKPGHSPKLLIYDASDLASGVPSRFKGSGSGTQFTLTISGVE<br />
CDDAATYYCAGYKSDSNDGDNV<br />
서열 번호: 507<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTVSGFSLNRNSITWVRQAPGEGLEWIGIITGSGRTYYANWAKGRFTISKTSTTVDLKMTSPT<br />
TEDTATYFCARGHPGLGSGNI<br />
서열 번호: 508<br />
QASESVFNNMLS<br />
서열 번호: 509<br />
DASDLAS<br />
서열 번호: 510<br />
AGYKSDSNDGDNV<br />
서열 번호: 511<br />
RNSIT<br />
서열 번호: 5<strong>12</strong><br />
IITGSGRTYYANWAKG<br />
서열 번호: 513<br />
GHPGLGSGNI<br />
서열 번호: 514<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCATTGAAATGACCCAGACTCCATCCCCCGTGTCT<br />
GCCGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTGAGAGTGTTTTTAATAATATGTTATCCTGGTATCAGCAGAAACCAGGGCACTCTCCTAAG<br />
CTCCTGATCTATGATGCATCCGATCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGTGGCGTGGAG<br />
TGTGACGATGCTGCCACTTACTATTGTGCAGGGTATAAAAGTGATAGTAATGATGGCGATAATGTT<br />
서열 번호: 515<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGATTCTCCCTCAACAGGAATTCAATAACCTGGGTCCGCCAGGCTCCAGGGGAGGGGCTGGAATGGATCGGAATC<br />
ATTACTGGTAGTGGTAGAACGTACTACGCGAACTGGGCAAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGGCCATCCTGGTCTTGGTAGTGGTAACATC<br />
서열 번호: 516<br />
- 168 -<br />
공개특허 10-2011-01<strong>12</strong>308
[<strong>19</strong>97]<br />
[<strong>19</strong>98]<br />
[<strong>19</strong>99]<br />
[2000]<br />
[2001]<br />
[2002]<br />
[2003]<br />
[2004]<br />
[2005]<br />
[2006]<br />
[2007]<br />
[2008]<br />
[2009]<br />
[2010]<br />
[2011]<br />
[20<strong>12</strong>]<br />
[2013]<br />
[2014]<br />
[2015]<br />
[2016]<br />
[2017]<br />
[2018]<br />
[20<strong>19</strong>]<br />
[2020]<br />
[2021]<br />
[2022]<br />
[2023]<br />
[2024]<br />
[2025]<br />
[2026]<br />
[2027]<br />
CAGGCCAGTGAGAGTGTTTTTAATAATATGTTATCC<br />
서열 번호: 517<br />
GATGCATCCGATCTGGCATCT<br />
서열 번호: 518<br />
GCAGGGTATAAAAGTGATAGTAATGATGGCGATAATGTT<br />
서열 번호: 5<strong>19</strong><br />
AGGAATTCAATAACC<br />
서열 번호: 520<br />
ATCATTACTGGTAGTGGTAGAACGTACTACGCGAACTGGGCAAAAGGC<br />
서열 번호: 521<br />
GGCCATCCTGGTCTTGGTAGTGGTAACATC<br />
서열 번호: 522<br />
MDTRAPTQLLGLLLLWLPGATFAQVLTQTASSVSAAVGGTVTINCQSSQSVYNNYLSWYQQKPGQPPKLLIYTASSLASGVPSRFKGSGSGTQFTLTISEVQ<br />
CDDAATYYCQGYYSGPIIT<br />
서열 번호: 523<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLNNYYIQWVRQAPGEGLEWIGIIYAGGSAYYATWANGRFTIAKTSSTTVDLKMTSL<br />
TTEDTATYFCARGTFDGYEL<br />
서열 번호: 524<br />
QSSQSVYNNYLS<br />
서열 번호: 525<br />
TASSLAS<br />
서열 번호: 526<br />
QGYYSGPIIT<br />
서열 번호: 527<br />
NYYIQ<br />
서열 번호: 528<br />
IIYAGGSAYYATWANG<br />
서열 번호: 529<br />
GTFDGYEL<br />
서열 번호: 530<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCGCAAGTGCTGACCCAGACTGCATCGTCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGTCCAGTCAGAGTGTTTATAATAACTACTTATCCTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAG<br />
CTCCTGATCTATACTGCATCCAGCCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGAAGTGCAG<br />
TGTGACGATGCTGCCACTTACTACTGTCAAGGCTATTATAGTGGTCCTATAATTACT<br />
서열 번호: 531<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAATAACTACTACATACAATGGGTCCGCCAGGCTCCAGGGGAGGGGCTGGAATGGATCGGGATC<br />
ATTTATGCTGGTGGTAGCGCATACTACGCGACCTGGGCAAACGGCCGATTCACCATCGCCAAAACCTCGTCGACCACGGTGGATCTGAAGATGACCAGTCTG<br />
- 169 -
[2028]<br />
[2029]<br />
[2030]<br />
[2031]<br />
[2032]<br />
[2033]<br />
[2034]<br />
[2035]<br />
[2036]<br />
[2037]<br />
[2038]<br />
[2039]<br />
[2040]<br />
[2041]<br />
[2042]<br />
[2043]<br />
[2044]<br />
[2045]<br />
[2046]<br />
[2047]<br />
[2048]<br />
[2049]<br />
[2050]<br />
[2051]<br />
[2052]<br />
[2053]<br />
[2054]<br />
[2055]<br />
[2056]<br />
[2057]<br />
[2058]<br />
ACAACCGAGGACACGGCCACCTATTTCTGTGCCAGAGGGACATTTGATGGTTATGAGTTG<br />
서열 번호: 532<br />
CAGTCCAGTCAGAGTGTTTATAATAACTACTTATCC<br />
서열 번호: 533<br />
ACTGCATCCAGCCTGGCATCT<br />
서열 번호: 534<br />
CAAGGCTATTATAGTGGTCCTATAATTACT<br />
서열 번호: 535<br />
AACTACTACATACAA<br />
서열 번호: 536<br />
ATCATTTATGCTGGTGGTAGCGCATACTACGCGACCTGGGCAAACGGC<br />
서열 번호: 537<br />
GGGACATTTGATGGTTATGAGTTG<br />
서열 번호: 538<br />
MDTRAPTQLLGLLLLWLPGATFAQVLTQTPSPVSVPVGDTVTISCQSSESVYSNNLLSWYQQKPGQPPKLLIYRASNLASGVPSRFKGSGSGTQFTLTISGA<br />
QCDDAATYYCQGYYSGVINS<br />
서열 번호: 539<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGFSLSSYFMSWVRQAPGEGLEYIGFINPGGSAYYASWASGRLTISKTSTTVDLKITSPT<br />
TEDTATYFCARILIVSYGAFTI<br />
서열 번호: 540<br />
QSSESVYSNNLLS<br />
서열 번호: 541<br />
RASNLAS<br />
서열 번호: 542<br />
QGYYSGVINS<br />
서열 번호: 543<br />
SYFMS<br />
서열 번호: 544<br />
FINPGGSAYYASWASG<br />
서열 번호: 545<br />
ILIVSYGAFTI<br />
서열 번호: 546<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCCAAGTGCTGACCCAGACTCCATCCCCTGTGTCT<br />
GTCCCTGTGGGAGACACAGTCACCATCAGTTGCCAGTCCAGTGAGAGCGTTTATAGTAATAACCTCTTATCCTGGTATCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTACAGGGCATCCAATCTGGCATCTGGTGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGGCGCA<br />
CAGTGTGACGATGCTGCCACTTACTACTGTCAAGGCTATTATAGTGGTGTCATTAATAGT<br />
서열 번호: 547<br />
- 170 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2059]<br />
[2060]<br />
[2061]<br />
[2062]<br />
[2063]<br />
[2064]<br />
[2065]<br />
[2066]<br />
[2067]<br />
[2068]<br />
[2069]<br />
[2070]<br />
[2071]<br />
[2072]<br />
[2073]<br />
[2074]<br />
[2075]<br />
[2076]<br />
[2077]<br />
[2078]<br />
[2079]<br />
[2080]<br />
[2081]<br />
[2082]<br />
[2083]<br />
[2084]<br />
[2085]<br />
[2086]<br />
[2087]<br />
[2088]<br />
[2089]<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTGTCTGGATTCTCCCTCAGTAGCTACTTCATGAGCTGGGTCCGCCAGGCTCCAGGGGAGGGGCTGGAATACATCGGATTC<br />
ATTAATCCTGGTGGTAGCGCATACTACGCGAGCTGGGCGAGTGGCCGACTCACCATCTCCAAAACCTCGACCACGGTAGATCTGAAAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGGATTCTTATTGTTTCTTATGGAGCCTTTACCATC<br />
서열 번호: 548<br />
CAGTCCAGTGAGAGCGTTTATAGTAATAACCTCTTATCC<br />
서열 번호: 549<br />
AGGGCATCCAATCTGGCATCT<br />
서열 번호: 550<br />
CAAGGCTATTATAGTGGTGTCATTAATAGT<br />
서열 번호: 551<br />
AGCTACTTCATGAGC<br />
서열 번호: 552<br />
TTCATTAATCCTGGTGGTAGCGCATACTACGCGAGCTGGGCGAGTGGC<br />
서열 번호: 553<br />
ATTCTTATTGTTTCTTATGGAGCCTTTACCATC<br />
서열 번호: 554<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVEVAVGGTVTIKCQATESIGNELSWYQQKPGQAPKLLIYSASTLASGVPSRFKGSGSGTQFTLTITGVEC<br />
DDAATYYCQQGYSSANIDNA<br />
서열 번호: 555<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTVSGFSLSKYYMSWVRQAPEKGLKYIGYIDSTTVNTYYATWARGRFTISKTSTTVDLKITSP<br />
TSEDTATYFCARGSTYFTDGGHRLDL<br />
서열 번호: 556<br />
QATESIGNELS<br />
서열 번호: 557<br />
SASTLAS<br />
서열 번호: 558<br />
QQGYSSANIDNA<br />
서열 번호: 559<br />
KYYMS<br />
서열 번호: 560<br />
YIDSTTVNTYYATWARG<br />
서열 번호: 561<br />
GSTYFTDGGHRLDL<br />
서열 번호: 562<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCTGTGGAG<br />
GTAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCACTGAGAGCATTGGCAATGAGTTATCCTGGTATCAGCAGAAACCAGGGCAGGCTCCCAAGCTC<br />
CTGATCTATTCTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCACCGGCGTGGAGTGT<br />
- 171 -
[2090]<br />
[2091]<br />
[2092]<br />
[2093]<br />
[2094]<br />
[2095]<br />
[2096]<br />
[2097]<br />
[2098]<br />
[2099]<br />
[2100]<br />
[2101]<br />
[2102]<br />
[2103]<br />
[2104]<br />
[2105]<br />
[2106]<br />
[2107]<br />
[2108]<br />
[2109]<br />
[2110]<br />
[2111]<br />
[21<strong>12</strong>]<br />
[2113]<br />
[2114]<br />
[2115]<br />
[2116]<br />
[2117]<br />
[2118]<br />
[21<strong>19</strong>]<br />
[2<strong>12</strong>0]<br />
GATGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTAGTGCTAATATTGATAATGCT<br />
서열 번호: 563<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACCGTCTCTGGATTCTCCCTCAGTAAGTACTACATGAGCTGGGTCCGCCAGGCTCCAGAGAAGGGGCTGAAATACATCGGATAC<br />
ATTGATAGTACTACTGTTAATACATACTACGCGACCTGGGCGAGAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAGATCACCAGTCCG<br />
ACAAGTGAGGACACGGCCACCTATTTCTGTGCCAGAGGAAGTACTTATTTTACTGATGGAGGCCATCGGTTGGATCTC<br />
서열 번호: 564<br />
CAGGCCACTGAGAGCATTGGCAATGAGTTATCC<br />
서열 번호: 565<br />
TCTGCATCCACTCTGGCATCT<br />
서열 번호: 566<br />
CAACAGGGTTATAGTAGTGCTAATATTGATAATGCT<br />
서열 번호: 567<br />
AAGTACTACATGAGC<br />
서열 번호: 568<br />
TACATTGATAGTACTACTGTTAATACATACTACGCGACCTGGGCGAGAGGC<br />
서열 번호: 569<br />
GGAAGTACTTATTTTACTGATGGAGGCCATCGGTTGGATCTC<br />
서열 번호: 570<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVEVAVGGTVTIKCQATESIGNELSWYQQKPGQAPKLLIYSASTLASGVPSRFKGSGSGTQFTLTITGVEC<br />
DDAATYYCQQGYSSANIDNA<br />
서열 번호: 571<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTVSGFSLSTYNMGWVRQAPGKGLEWIGSITIDGRTYYASWAKGRFTVSKSSTTVDLKMTSLT<br />
TGDTATYFCARILIVSYGAFTI<br />
서열 번호: 572<br />
QATESIGNELS<br />
서열 번호: 573<br />
SASTLAS<br />
서열 번호: 574<br />
QQGYSSANIDNA<br />
서열 번호: 575<br />
TYNMG<br />
서열 번호: 576<br />
SITIDGRTYYASWAKG<br />
서열 번호: 577<br />
ILIVSYGAFTI<br />
서열 번호: 578<br />
- 172 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2<strong>12</strong>1]<br />
[2<strong>12</strong>2]<br />
[2<strong>12</strong>3]<br />
[2<strong>12</strong>4]<br />
[2<strong>12</strong>5]<br />
[2<strong>12</strong>6]<br />
[2<strong>12</strong>7]<br />
[2<strong>12</strong>8]<br />
[2<strong>12</strong>9]<br />
[2130]<br />
[2131]<br />
[2132]<br />
[2133]<br />
[2134]<br />
[2135]<br />
[2136]<br />
[2137]<br />
[2138]<br />
[2139]<br />
[2140]<br />
[2141]<br />
[2142]<br />
[2143]<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCTGTGGAG<br />
GTAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCACTGAGAGCATTGGCAATGAGTTATCCTGGTATCAGCAGAAACCAGGGCAGGCTCCCAAGCTC<br />
CTGATCTATTCTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCACCGGCGTGGAGTGT<br />
GATGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTAGTGCTAATATTGATAATGCT<br />
서열 번호: 579<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTAACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGATTCTCCCTCAGTACCTACAACATGGGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAAGT<br />
ATTACTATTGATGGTCGCACATACTACGCGAGCTGGGCGAAAGGCCGATTCACCGTCTCCAAAAGCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACA<br />
ACCGGGGACACGGCCACCTATTTCTGTGCCAGGATTCTTATTGTTTCTTATGGGGCCTTTACCATC<br />
서열 번호: 580<br />
CAGGCCACTGAGAGCATTGGCAATGAGTTATCC<br />
서열 번호: 581<br />
TCTGCATCCACTCTGGCATCT<br />
서열 번호: 582<br />
CAACAGGGTTATAGTAGTGCTAATATTGATAATGCT<br />
서열 번호: 583<br />
ACCTACAACATGGGC<br />
서열 번호: 584<br />
AGTATTACTATTGATGGTCGCACATACTACGCGAGCTGGGCGAAAGGC<br />
서열 번호: 585<br />
ATTCTTATTGTTTCTTATGGGGCCTTTACCATC<br />
서열 번호: 586<br />
VAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNR<br />
GEC<br />
서열 번호: 587<br />
GTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAG<br />
GCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGC<br />
ACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGG<br />
GGAGAGTGT<br />
서열 번호: 588<br />
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVD<strong>KR</strong>VEPKS<br />
CDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKC<br />
KVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVF<br />
SCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 589<br />
공개특허 10-2011-01<strong>12</strong>308<br />
GCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCC<br />
GAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTG<br />
GTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAGAGTTGAGCCCAAATCT<br />
TGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATC<br />
TCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCC<br />
AAGACAAAGCCGCGGGAGGAGCAGTACGCCAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGC<br />
- 173 -
[2144]<br />
[2145]<br />
[2146]<br />
[2147]<br />
[2148]<br />
[2149]<br />
[2150]<br />
[2151]<br />
[2152]<br />
[2153]<br />
[2154]<br />
[2155]<br />
[2156]<br />
[2157]<br />
[2158]<br />
[2159]<br />
[2160]<br />
[2161]<br />
[2162]<br />
[2163]<br />
[2164]<br />
[2165]<br />
[2166]<br />
[2167]<br />
[2168]<br />
[2169]<br />
[2170]<br />
[2171]<br />
[2172]<br />
[2173]<br />
[2174]<br />
[2175]<br />
[2176]<br />
AAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGG<br />
GAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAAC<br />
AACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTC<br />
TCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAA<br />
서열 번호: 590<br />
VPPGEDSKDVAAPHR<br />
서열 번호: 591<br />
GEDSKDVAAPHRQPL<br />
서열 번호: 592<br />
SKDVAAPHRQPLTSS<br />
서열 번호: 593<br />
VAAPHRQPLTSSERI<br />
서열 번호: 594<br />
PHRQPLTSSERIDKQ<br />
서열 번호: 595<br />
QPLTSSERIDKQIRY<br />
서열 번호: 596<br />
TSSERIDKQIRYILD<br />
서열 번호: 597<br />
ERIDKQIRYILDGIS<br />
서열 번호: 598<br />
DKQIRYILDGISALR<br />
서열 번호: 599<br />
IRYILDGISALRKET<br />
서열 번호: 600<br />
ILDGISALRKETCNK<br />
서열 번호: 601<br />
GISALRKETCNKSNM<br />
서열 번호: 602<br />
ALRKETCNKSNMCES<br />
서열 번호: 603<br />
KETCNKSNMCESSKE<br />
서열 번호: 604<br />
CNKSNMCESSKEALA<br />
서열 번호: 605<br />
SNMCESSKEALAENN<br />
서열 번호: 606<br />
- 174 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2177]<br />
[2178]<br />
[2179]<br />
[2180]<br />
[2181]<br />
[2182]<br />
[2183]<br />
[2184]<br />
[2185]<br />
[2186]<br />
[2187]<br />
[2188]<br />
[2189]<br />
[2<strong>19</strong>0]<br />
[2<strong>19</strong>1]<br />
[2<strong>19</strong>2]<br />
[2<strong>19</strong>3]<br />
[2<strong>19</strong>4]<br />
[2<strong>19</strong>5]<br />
[2<strong>19</strong>6]<br />
[2<strong>19</strong>7]<br />
[2<strong>19</strong>8]<br />
[2<strong>19</strong>9]<br />
[2200]<br />
[2201]<br />
[2202]<br />
[2203]<br />
[2204]<br />
[2205]<br />
[2206]<br />
[2207]<br />
[2208]<br />
[2209]<br />
[2210]<br />
[2211]<br />
[22<strong>12</strong>]<br />
CESSKEALAENNLNL<br />
서열 번호: 607<br />
SKEALAENNLNLPKM<br />
서열 번호: 608<br />
ALAENNLNLPKMAEK<br />
서열 번호: 609<br />
ENNLNLPKMAEKDGC<br />
서열 번호: 610<br />
LNLPKMAEKDGCFQS<br />
서열 번호: 611<br />
PKMAEKDGCFQSGFN<br />
서열 번호: 6<strong>12</strong><br />
AEKDGCFQSGFNEET<br />
서열 번호: 613<br />
DGCFQSGFNEETCLV<br />
서열 번호: 614<br />
FQSGFNEETCLVKII<br />
서열 번호: 615<br />
GFNEETCLVKIITGL<br />
서열 번호: 616<br />
EETCLVKIITGLLEF<br />
서열 번호: 617<br />
CLVKIITGLLEFEVY<br />
서열 번호: 618<br />
KIITGLLEFEVYLEY<br />
서열 번호: 6<strong>19</strong><br />
TGLLEFEVYLEYLQN<br />
서열 번호: 620<br />
LEFEVYLEYLQNRFE<br />
서열 번호: 621<br />
EVYLEYLQNRFESSE<br />
서열 번호: 622<br />
LEYLQNRFESSEEQA<br />
서열 번호: 623<br />
LQNRFESSEEQARAV<br />
서열 번호: 624<br />
- 175 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2213]<br />
[2214]<br />
[2215]<br />
[2216]<br />
[2217]<br />
[2218]<br />
[22<strong>19</strong>]<br />
[2220]<br />
[2221]<br />
[2222]<br />
[2223]<br />
[2224]<br />
[2225]<br />
[2226]<br />
[2227]<br />
[2228]<br />
[2229]<br />
[2230]<br />
[2231]<br />
[2232]<br />
[2233]<br />
[2234]<br />
[2235]<br />
[2236]<br />
[2237]<br />
[2238]<br />
[2239]<br />
[2240]<br />
[2241]<br />
[2242]<br />
[2243]<br />
[2244]<br />
[2245]<br />
[2246]<br />
[2247]<br />
[2248]<br />
RFESSEEQARAVQMS<br />
서열 번호: 625<br />
SSEEQARAVQMSTKV<br />
서열 번호: 626<br />
EQARAVQMSTKVLIQ<br />
서열 번호: 627<br />
RAVQMSTKVLIQFLQ<br />
서열 번호: 628<br />
QMSTKVLIQFLQKKA<br />
서열 번호: 629<br />
TKVLIQFLQKKAKNL<br />
서열 번호: 630<br />
LIQFLQKKAKNLDAI<br />
서열 번호: 631<br />
FLQKKAKNLDAITTP<br />
서열 번호: 632<br />
KKAKNLDAITTPDPT<br />
서열 번호: 633<br />
KNLDAITTPDPTTNA<br />
서열 번호: 634<br />
DAITTPDPTTNASLL<br />
서열 번호: 635<br />
TTPDPTTNASLLTKL<br />
서열 번호: 636<br />
DPTTNASLLTKLQAQ<br />
서열 번호: 637<br />
TNASLLTKLQAQNQW<br />
서열 번호: 638<br />
SLLTKLQAQNQWLQD<br />
서열 번호: 639<br />
TKLQAQNQWLQDMTT<br />
서열 번호: 640<br />
QAQNQWLQDMTTHLI<br />
서열 번호: 641<br />
NQWLQDMTTHLILRS<br />
서열 번호: 642<br />
- 176 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2249]<br />
[2250]<br />
[2251]<br />
[2252]<br />
[2253]<br />
[2254]<br />
[2255]<br />
[2256]<br />
[2257]<br />
[2258]<br />
[2259]<br />
[2260]<br />
[2261]<br />
[2262]<br />
[2263]<br />
[2264]<br />
[2265]<br />
[2266]<br />
[2267]<br />
[2268]<br />
[2269]<br />
[2270]<br />
[2271]<br />
[2272]<br />
[2273]<br />
[2274]<br />
[2275]<br />
[2276]<br />
[2277]<br />
[2278]<br />
[2279]<br />
[2280]<br />
LQDMTTHLILRSFKE<br />
서열 번호: 643<br />
MTTHLILRSFKEFLQ<br />
서열 번호: 644<br />
HLILRSFKEFLQSSL<br />
서열 번호: 645<br />
LRSFKEFLQSSLRAL<br />
서열 번호: 646<br />
FKEFLQSSLRALRQM<br />
서열 번호: 647<br />
AYDMTQTPASVSAAVGGTVTIKCQASQSINNELSWYQQKPGQRPKLLIYRASTLASGVSSRFKGSGSGTEFTLTISDLECADAATYYCQQGYSLRNIDNAFG<br />
GGTEVVV<strong>KR</strong><br />
서열 번호: 648<br />
AIQMTQSPSSLSASVGDRVTITCRASQGIRNDLGWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYC<br />
서열 번호: 649<br />
DIQMTQSPSSLSASVGDRVTITCRASQGISNYLAWYQQKPGKVPKLLIYAASTLQSGVPSRFSGSGSGTDFTLTISSLQPEDVATYYC<br />
서열 번호: 650<br />
DIQMTQSPSTLSASVGDRVTITCRASQSISSWLAWYQQKPGKAPKLLIYKASSLESGVPSRFSGSGSGTEFTLTISSLQPDDFATYYC<br />
서열 번호: 651<br />
AIQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQGYSLRNIDNAFG<br />
GGTKVEI<strong>KR</strong><br />
서열 번호: 652<br />
QSLEESGGRLVTPGTPLTLTCTASGFSLSNYYVTWVRQAPGKGLEWIGIIYGSDETAYATWAIGRFTISKTSTTVDLKMTSLTAADTATYFCARDDSSDWDA<br />
KFNLWGQGTLVTVSS<br />
서열 번호: 653<br />
EVQLVESGGGLVQPGGSLRLSCAASGFTVSSNYMSWVRQAPGKGLEWVSVIYSGGSTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAR<br />
서열 번호: 654<br />
EVQLVESGGGLIQPGGSLRLSCAASGFTVSSNYMSWVRQAPGKGLEWVSVIYSGGSTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAR<br />
서열 번호: 655<br />
EVQLLESGGGLVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSVIYSGGSSTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAK<br />
서열 번호: 656<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATWAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSS<br />
서열 번호: 657<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATSAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSS<br />
서열 번호: 658<br />
- 177 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2281]<br />
[2282]<br />
[2283]<br />
[2284]<br />
[2285]<br />
[2286]<br />
[2287]<br />
[2288]<br />
[2289]<br />
[2290]<br />
[2291]<br />
[2292]<br />
[2293]<br />
[2294]<br />
[2295]<br />
[2296]<br />
[2297]<br />
[2298]<br />
[2299]<br />
[2300]<br />
[2301]<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSNYYVTWVRQAPGKGLEWIGIIYGSDETAYATSAIGRFTISKTSTTVDLKMTSLT<br />
AADTATYFCARDDSSDWDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVK<br />
서열 번호: 659<br />
IIYGSDETAYATSAIG<br />
서열 번호: 660<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVSAAVGGTVTIKCQASQSINNELSWYQQKPGQRPKLLIYRASTLASGVSSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQQGYSLRNIDNA<br />
서열 번호: 661<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSNYYVTWVRQAPGKGLEWIGIIYGSDETAYATWAIGRFTISKTSTTVDLKMTSLT<br />
AADTATYFCARDDSSDWDAKFNL<br />
서열 번호: 662<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCGGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCATTAACAATGAATTATCCTGGTATCAGCAGAAACCAGGGCAGCGTCCCAAGCTC<br />
CTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
GCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCT<br />
서열 번호: 663<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTTATGGTAGTGATGAAACGGCCTACGCGACCTGGGCGATAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACA<br />
GCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCAAAATTTAACTTG<br />
서열 번호: 664<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATWAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICN<br />
VNHKPSNTKVD<strong>KR</strong>VEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVV<br />
SVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFF<br />
LYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 665<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATSAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICN<br />
VNHKPSNTKVD<strong>KR</strong>VEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVV<br />
SVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFF<br />
LYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 666<br />
IQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPDDFATYYCQQGYSLRNIDNAFGG<br />
GTKVEI<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLS<br />
SPVTKSFNRGEC<br />
서열 번호: 667<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVEVAVGGTVTINCQASETIYSWLSWYQQKPGQPPKLLIYQASDLASGVPSRFSGSGAGTEYTLTISGVQC<br />
DDAATYYCQQGYSGSNVDNV<br />
서열 번호: 668<br />
METGLRWLLLVAVLKGVQCQEQLKESGGRLVTPGTPLTLTCTASGFSLNDHAMGWVRQAPGKGLEYIGFINSGGSARYASWAEGRFTISRTSTTVDLKMTSL<br />
TTEDTATYFCVRGGAVWSIHSFDP<br />
- 178 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2302]<br />
[2303]<br />
[2304]<br />
[2305]<br />
[2306]<br />
[2307]<br />
[2308]<br />
[2309]<br />
[2310]<br />
[2311]<br />
[23<strong>12</strong>]<br />
[2313]<br />
[2314]<br />
[2315]<br />
[2316]<br />
[2317]<br />
[2318]<br />
[23<strong>19</strong>]<br />
[2320]<br />
[2321]<br />
서열 번호: 669<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCTGTGGAG<br />
GTAGCTGTGGGAGGCACAGTCACCATCAATTGCCAGGCCAGTGAGACCATTTACAGTTGGTTATCCTGGTATCAGCAGAAGCCAGGGCAGCCTCCCAAGCTC<br />
CTGATCTACCAGGCATCCGATCTGGCATCTGGGGTCCCATCGCGATTCAGCGGCAGTGGGGCTGGGACAGAGTACACTCTCACCATCAGCGGCGTGCAGTGT<br />
GACGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTGGTAGTAATGTTGATAATGTT<br />
서열 번호: 670<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGGAGCAGCTGAAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGG<br />
ACACCCCTGACACTTACCTGCACAGCCTCTGGATTCTCCCTCAATGACCATGCAATGGGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATACATCGGA<br />
TTCATTAATAGTGGTGGTAGCGCACGCTACGCGAGCTGGGCAGAAGGCCGATTCACCATCTCCAGAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTG<br />
ACAACCGAGGACACGGCCACCTATTTCTGTGTCAGAGGGGGTGCTGTTTGGAGTATTCATAGTTTTGATCCC<br />
서열 번호: 671<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSAAVGGTVSISCQASQSVYDNNYLSWFQQKPGQPPKLLIYGASTLASGVPSRFVGSGSGTQFTLTITDV<br />
QCDDAATYYCAGVYDDDSDNA<br />
서열 번호: 672<br />
METGLRWLLLVAVLKGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSVYYMNWVRQAPGKGLEWIGFITMSDNINYASWAKGRFTISKTSTTVDLKMTSPT<br />
TEDTATYFCARSRGWGTMGRLDL<br />
서열 번호: 673<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCGCCGTGCTGACCCAGACTCCATCTCCCGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGGCCAGTCAGAGTGTTTATGACAACAACTACTTATCCTGGTTTCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCGTGGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCACAGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTATTGTGCAGGCGTTTATGATGATGATAGTGATAATGCC<br />
서열 번호: 674<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTGGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACCCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTGTCTACTACATGAACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGATTC<br />
ATTACAATGAGTGATAATATAAATTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGGAGTCGTGGCTGGGGTACAATGGGTCGGTTGGATCTC<br />
서열 번호: 675<br />
MDTRAPTQLLGLLLLWLPGAICDPVLTQTPSPVSAPVGGTVSISCQASQSVYENNYLSWFQQKPGQPPKLLIYGASTLDSGVPSRFKGSGSGTQFTLTITDV<br />
QCDDAATYYCAGVYDDDSDDA<br />
서열 번호: 676<br />
METGLRWLLLVAVLKGVQCQEQLKESGGGLVTPGGTLTLTCTASGFSLNAYYMNWVRQAPGKGLEWIGFITLNNNVAYANWAKGRFTFSKTSTTVDLKMTSP<br />
TPEDTATYFCARSRGWGAMGRLDL<br />
서열 번호: 677<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCATATGTGACCCTGTGCTGACCCAGACTCCATCTCCCGTATCT<br />
GCACCTGTGGGAGGCACAGTCAGCATCAGTTGCCAGGCCAGTCAGAGTGTTTATGAGAACAACTATTTATCCTGGTTTCAGCAGAAACCAGGGCAGCCTCCC<br />
AAGCTCCTGATCTATGGTGCATCCACTCTGGATTCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATTACAGACGTG<br />
CAGTGTGACGATGCTGCCACTTACTATTGTGCAGGCGTTTATGATGATGATAGTGATGATGCC<br />
서열 번호: 678<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTGGCTGTGCTCAAAGGTGTCCAGTGTCAGGAGCAGCTGAAGGAGTCCGGAGGAGGCCTGGTAACGCCTGGA<br />
GGAACCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAATGCCTACTACATGAACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGA<br />
TTCATTACTCTGAATAATAATGTAGCTTACGCGAACTGGGCGAAAGGCCGATTCACCTTCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCCG<br />
ACACCCGAGGACACGGCCACCTATTTCTGTGCCAGGAGTCGTGGCTGGGGTGCAATGGGTCGGTTGGATCTC<br />
- 179 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2322]<br />
[2323]<br />
[2324]<br />
[2325]<br />
[2326]<br />
[2327]<br />
[2328]<br />
[2329]<br />
[2330]<br />
[2331]<br />
[2332]<br />
[2333]<br />
[2334]<br />
[2335]<br />
[2336]<br />
[2337]<br />
[2338]<br />
[2339]<br />
[2340]<br />
[2341]<br />
[2342]<br />
[2343]<br />
서열 번호: 679<br />
MDTRAPTQLLGLLLLWLPGATFAQVLTQTPSPVSAAVGGTVTINCQASQSVDDNNWLGWYQQ<strong>KR</strong>GQPPKYLIYSASTLASGVPSRFKGSGSGTQFTLTISDL<br />
ECDDAATYYCAGGFSGNIFA<br />
서열 번호: 680<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGFSLSSYAMSWVRQAPGKGLEWIGIIGGFGTTYYATWAKGRFTISKTSTTVDLRITSPT<br />
TEDTATYFCARGGPGNGGDI<br />
서열 번호: 681<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCCCAAGTGCTGACCCAGACTCCATCGCCTGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAACTGCCAGGCCAGTCAGAGTGTTGATGATAACAACTGGTTAGGCTGGTATCAGCAGAAACGAGGGCAGCCTCCC<br />
AAGTACCTGATCTATTCTGCATCCACTCTGGCATCTGGGGTCCCATCGCGGTTCAAAGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGACCTG<br />
GAGTGTGACGATGCTGCCACTTACTACTGTGCAGGCGGTTTTAGTGGTAATATCTTTGCT<br />
서열 번호: 682<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGTCTCTGGCTTCTCCCTCAGTAGCTATGCAATGAGCTGGGTCCGCCAGGCTCCAGGAAAGGGGCTGGAGTGGATCGGAATC<br />
ATTGGTGGTTTTGGTACCACATACTACGCGACCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAGAATCACCAGTCCGACA<br />
ACCGAGGACACGGCCACCTATTTCTGTGCCAGAGGTGGTCCTGGTAATGGTGGTGACATC<br />
서열 번호: 683<br />
MDTRAPTQLLGLLLLWLPGATFAAVLTQTPSPVSVPVGGTVTIKCQSSQSVYNNFLSWYQQKPGQPPKLLIYQASKLASGVPDRFSGSGSGTQFTLTISGVQ<br />
CDDAATYYCLGGYDDDADNA<br />
서열 번호: 684<br />
METGLRWLLLVAVLKGVQCQSVEESGGRLVTPGTPLTLTCTVSGIDLSDYAMSWVRQAPGKGLEWIGIIYAGSGSTWYASWAKGRFTISKTSTTVDLKITSP<br />
TTEDTATYFCARDGYDDYGDFDRLDL<br />
서열 번호: 685<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCACATTTGCAGCCGTGCTGACCCAGACACCATCGCCCGTGTCT<br />
GTACCTGTGGGAGGCACAGTCACCATCAAGTGCCAGTCCAGTCAGAGTGTTTATAATAATTTCTTATCGTGGTATCAGCAGAAACCAGGGCAGCCTCCCAAG<br />
CTCCTGATCTACCAGGCATCCAAACTGGCATCTGGGGTCCCAGATAGGTTCAGCGGCAGTGGATCTGGGACACAGTTCACTCTCACCATCAGCGGCGTGCAG<br />
TGTGACGATGCTGCCACTTACTACTGTCTAGGCGGTTATGATGATGATGCTGATAATGCT<br />
서열 번호: 686<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCAAAGGTGTCCAGTGTCAGTCGGTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACGCTCACCTGCACAGTCTCTGGAATCGACCTCAGTGACTATGCAATGAGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATC<br />
ATTTATGCTGGTAGTGGTAGCACATGGTACGCGAGCTGGGCGAAAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATCACCAGTCCG<br />
ACAACCGAGGACACGGCCACCTATTTCTGTGCCAGAGATGGATACGATGACTATGGTGATTTCGATCGATTGGATCTC<br />
서열 번호: 687<br />
MDTRAPTQLLGLLLLWLPGARCAYDMTQTPASVSAAVGGTVTIKCQASQSINNELSWYQQKSGQRPKLLIYRASTLASGVSSRFKGSGSGTEFTLTISDLEC<br />
ADAATYYCQQGYSLRNIDNA<br />
서열 번호: 688<br />
METGLRWLLLVAVLSGVQCQSLEESGGRLVTPGTPLTLTCTASGFSLSNYYMTWVRQAPGKGLEWIGMIYGSDETAYANWAIGRFTISKTSTTVDLKMTSLT<br />
AADTATYFCARDDSSDWDAKFNL<br />
서열 번호: 689<br />
공개특허 10-2011-01<strong>12</strong>308<br />
ATGGACACGAGGGCCCCCACTCAGCTGCTGGGGCTCCTGCTGCTCTGGCTCCCAGGTGCCAGATGTGCCTATGATATGACCCAGACTCCAGCCTCGGTGTCT<br />
GCAGCTGTGGGAGGCACAGTCACCATCAAATGCCAGGCCAGTCAGAGCATTAACAATGAATTATCCTGGTATCAGCAGAAATCAGGGCAGCGTCCCAAGCTC<br />
CTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGGACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGT<br />
- 180 -
[2344]<br />
[2345]<br />
[2346]<br />
[2347]<br />
[2348]<br />
[2349]<br />
[2350]<br />
[2351]<br />
[2352]<br />
[2353]<br />
[2354]<br />
[2355]<br />
[2356]<br />
[2357]<br />
[2358]<br />
[2359]<br />
[2360]<br />
[2361]<br />
[2362]<br />
[2363]<br />
[2364]<br />
[2365]<br />
GCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCT<br />
서열 번호: 690<br />
ATGGAGACTGGGCTGCGCTGGCTTCTCCTGGTCGCTGTGCTCTCAGGTGTCCAGTGTCAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACA<br />
CCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACATGACCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATG<br />
ATTTATGGTAGTGATGAAACAGCCTACGCGAACTGGGCGATAGGCCGATTCACCATCTCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACA<br />
GCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCAAAATTTAACTTG<br />
서열 번호: 691<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYMTWVRQAPGKGLEWVGMIYGSDETAYANWAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICN<br />
VNHKPSNTKVD<strong>KR</strong>VEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVV<br />
SVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFF<br />
LYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 692<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYMTWVRQAPGKGLEWVGMIYGSDETAYANSAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICN<br />
VNHKPSNTKVD<strong>KR</strong>VEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVV<br />
SVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFF<br />
LYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 693<br />
DIQMTQSPSTLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTEFTLTISSLQPDDFATYYCQQGYSLRNIDNAFG<br />
GGTKVEI<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGL<br />
SSPVTKSFNRGEC<br />
서열 번호: 694<br />
CAGGCCAGTCAGAGCATTAACAATGAGTTATCC<br />
서열 번호: 695<br />
CAACAGGGTTATAGTCTGAGGAACATTGATAATGCT<br />
서열 번호: 696<br />
ATCATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGC<br />
서열 번호: 697<br />
GATGATAGTAGTGACTGGGATGCAAAGTTCAACTTG<br />
서열 번호: 698<br />
GCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCC<br />
TGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGG<br />
ACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGC<br />
GGAGGGACCAAGGTGGAAATCAAACGTACG<br />
서열 번호: 699<br />
AIQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPDDFATYYCQQGYSLRNIDNAFG<br />
GGTKVEI<strong>KR</strong>T<br />
서열 번호: 700<br />
공개특허 10-2011-01<strong>12</strong>308<br />
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGGTCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTG<br />
ACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATCATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACC<br />
ATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGCCTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGAC<br />
- 181 -
[2366]<br />
[2367]<br />
[2368]<br />
[2369]<br />
[2370]<br />
[2371]<br />
[2372]<br />
[2373]<br />
[2374]<br />
[2375]<br />
[2376]<br />
[2377]<br />
TGGGATGCAAAGTTCAACTTGTGGGGCCAAGGGACCCTCGTCACCGTCTCGAGC<br />
서열 번호: 701<br />
GCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCC<br />
TGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGG<br />
ACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGC<br />
GGAGGGACCAAGGTGGAAATCAAACGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTG<br />
TGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGAC<br />
AGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTG<br />
AGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT<br />
서열 번호: 702<br />
AIQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPDDFATYYCQQGYSLRNIDNAFG<br />
GGTKVEI<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGL<br />
SSPVTKSFNRGEC<br />
서열 번호: 703<br />
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGGTCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTG<br />
ACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATCATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACC<br />
ATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGCCTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGAC<br />
TGGGATGCAAAGTTCAACTTGTGGGGCCAAGGGACCCTCGTCACCGTCTCGAGCGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAG<br />
AGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTG<br />
CACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAAC<br />
GTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAGAGTTGAGCCCAAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTG<br />
GGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAA<br />
GACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACGCCAGCACGTACCGTGTGGTC<br />
AGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCC<br />
AAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGC<br />
TTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTC<br />
CTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAG<br />
AGCCTCTCCCTGTCTCCGGGTAAA<br />
서열 번호: 704<br />
EVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATSAIGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARDDSSD<br />
WDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICN<br />
VNHKPSNTKVD<strong>KR</strong>VEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVV<br />
SVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFF<br />
LYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 705<br />
ATGAAGTGGGTAACCTTTATTTCCCTTCTGTTTCTCTTTAGCAGCGCTTATTCCGCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGA<br />
GACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCCTGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGG<br />
GCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGGACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCA<br />
ACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGCGGAGGGACCAAGGTGGAAATCAAACGTACGGTGGCTGCACCATCTGTC<br />
TTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAG<br />
GTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAA<br />
GCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT<br />
서열 번호: 706<br />
공개특허 10-2011-01<strong>12</strong>308<br />
MKWVTFISLLFLFSSAYSAIQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPDDFA<br />
TYYCQQGYSLRNIDNAFGGGTKVEI<strong>KR</strong>TVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSK<br />
- 182 -
[2378]<br />
[2379]<br />
[2380]<br />
[2381]<br />
[2382]<br />
[2383]<br />
[2384]<br />
[2385]<br />
[2386]<br />
[2387]<br />
[2388]<br />
[2389]<br />
[2390]<br />
[2391]<br />
[2392]<br />
[2393]<br />
[2394]<br />
[2395]<br />
[2396]<br />
[2397]<br />
[2398]<br />
[2399]<br />
ADYEKHKVYACEVTHQGLSSPVTKSFNRGEC<br />
서열 번호: 707<br />
ATGAAGTGGGTAACCTTTATTTCCCTTCTGTTTCTCTTTAGCAGCGCTTATTCCGAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGG<br />
TCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATC<br />
ATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACCATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGC<br />
CTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGACTGGGATGCAAAGTTCAACTTGTGGGGCCAAGGGACCCTCGTCACCGTC<br />
TCGAGCGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTAC<br />
TTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGC<br />
AGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAGAGTTGAGCCC<br />
AAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTC<br />
ATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCAT<br />
AATGCCAAGACAAAGCCGCGGGAGGAGCAGTACGCCAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTAC<br />
AAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCA<br />
TCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCG<br />
GAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAAC<br />
GTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAA<br />
서열 번호: 708<br />
MKWVTFISLLFLFSSAYSEVQLVESGGGLVQPGGSLRLSCAASGFSLSNYYVTWVRQAPGKGLEWVGIIYGSDETAYATSAIGRFTISRDNSKNTLYLQMNS<br />
LRAEDTAVYYCARDDSSDWDAKFNLWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLS<br />
SVVTVPSSSLGTQTYICNVNHKPSNTKVD<strong>KR</strong>VEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVH<br />
NAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQP<br />
ENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 709<br />
AIQMTQSPSSLSASVGDRVTITCQASQSINNELSWYQQKPGKAPKLLIYRASTLASGVPSRFSGSGSGTDFTLTISSLQPDDFATYYCQQGYSLRNIDNAFG<br />
GGTKVEI<strong>KR</strong><br />
서열 번호: 710<br />
RASQGIRNDLG<br />
서열 번호: 711<br />
RASQGISNYLA<br />
서열 번호: 7<strong>12</strong><br />
RASQSISSWLA<br />
서열 번호: 713<br />
AASSLQS<br />
서열 번호: 714<br />
AASTLQS<br />
서열 번호: 715<br />
KASSLES<br />
서열 번호: 716<br />
SNYMS<br />
서열 번호: 717<br />
VIYSGGSTYYADSVKG<br />
- 183 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2400]<br />
[2401]<br />
[2402]<br />
[2403]<br />
[2404]<br />
[2405]<br />
[2406]<br />
[2407]<br />
[2408]<br />
[2409]<br />
[2410]<br />
[2411]<br />
[24<strong>12</strong>]<br />
[2413]<br />
[2414]<br />
[2415]<br />
[2416]<br />
[2417]<br />
서열 번호: 718<br />
VIYSGGSSTYYADSVKG<br />
서열 번호: 7<strong>19</strong><br />
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVD<strong>KR</strong>VEPKS<br />
CDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKC<br />
KVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVF<br />
SCSVMHEALHNHYTQKSLSLSPGK<br />
서열 번호: 720<br />
ATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCCTGG<br />
TATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGGACA<br />
GACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCT<br />
서열 번호: 721<br />
GCCTATGATATGACCCAGACTCCAGCCTCGGTGTCTGCAGCTGTGGGAGGCACAGTCACCATCAAGTGCCAGGCCAGTCAGAGCATTAACAATGAATTATCC<br />
TGGTATCAGCAGAAACCAGGGCAGCGTCCCAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCTCATCGCGGTTCAAAGGCAGTGGATCTGGG<br />
ACAGAGTTCACTCTCACCATCAGCGACCTGGAGTGTGCCGATGCTGCCACTTACTACTGTCAACAGGGTTATAGTCTGAGGAATATTGATAATGCTTTCGGC<br />
GGAGGGACCGAGGTGGTGGTCAAACGT<br />
서열 번호: 722<br />
ATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCCTGG<br />
TATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGGACA<br />
GACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGCGGA<br />
GGGACCAAGGTGGAAATCAAACGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGC<br />
CTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGC<br />
AAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGC<br />
TCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT<br />
서열 번호: 723<br />
GCTATCCAGATGACCCAGTCTCCTTCCTCCCTGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGCCAGGCCAGTCAGAGCATTAACAATGAGTTATCC<br />
TGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGCTCCTGATCTATAGGGCATCCACTCTGGCATCTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGG<br />
ACAGACTTCACTCTCACCATCAGCAGCCTGCAGCCTGATGATTTTGCAACTTATTACTGCCAACAGGGTTATAGTCTGAGGAACATTGATAATGCTTTCGGC<br />
GGAGGGACCAAGGTGGAAATCAAACGT<br />
서열 번호: 724<br />
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGGTCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCCTCAGTAACTACTACGTG<br />
ACCTGGGTCCGTCAGGCTCCAGGGAAGGGGCTGGAGTGGGTCGGCATCATCTATGGTAGTGATGAAACCGCCTACGCTACCTCCGCTATAGGCCGATTCACC<br />
ATCTCCAGAGACAATTCCAAGAACACCCTGTATCTTCAAATGAACAGCCTGAGAGCTGAGGACACTGCTGTGTATTACTGTGCTAGAGATGATAGTAGTGAC<br />
TGGGATGCAAAGTTCAACTTG<br />
서열 번호: 725<br />
CAGTCGCTGGAGGAGTCCGGGGGTCGCCTGGTCACGCCTGGGACACCCCTGACACTCACCTGCACAGCCTCTGGATTCTCCCTCAGTAACTACTACGTGACC<br />
TGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAATGGATCGGAATCATTTATGGTAGTGATGAAACGGCCTACGCGACCTGGGCGATAGGCCGATTCACCATC<br />
TCCAAAACCTCGACCACGGTGGATCTGAAAATGACCAGTCTGACAGCCGCGGACACGGCCACCTATTTCTGTGCCAGAGATGATAGTAGTGACTGGGATGCA<br />
AAATTTAACTTGTGGGGCCAAGGCACCCTGGTCACCGTCTCGAGC<br />
서열 번호: 726<br />
MEKLLCFLVLTSLSHAFGQTDMSRKAFVFPKESDTSYVSLKAPLTKPLKAFTVCLHFYTELSSTRGYSIFSYAT<strong>KR</strong>QDNEILIFWSKDIGYSFTVGGSEILF<br />
EVPEVTVAPVHICTSWESASGIVEFWVDGKPRVRKSLKKGYTVGAEASIILGQEQDSFGGNFEGSQSLVGDIGNVNMWDFVLSPDEINTIYLGGPFSPNVLN<br />
WRALKYEVQGEVFTKPQLWP<br />
- 184 -<br />
공개특허 10-2011-01<strong>12</strong>308
[2418]<br />
[24<strong>19</strong>]<br />
[2420]<br />
[2421]<br />
서열 번호: 727<br />
MLAVGCALLAALLAAPGAALAPRRCPAQEVARGVLTSLPGDSVTLTCPGVEPEDNATVHWVLRKPAAGSHPSRWAGMGRRLLLRSVQLHDSGNYSCYRAGRP<br />
AGTVHLLVDVPPEEPQLSCFRKSPLSNVVCEWGPRSTPSLTTKAVLLVRKFQNSPAEDFQEPCQYSQESQKFSCQLAVPEGDSSFYIVSMCVASSVGSKFSK<br />
TQTFQGCGILQPDPPANITVTAVARNPRWLSVTWQDPHSWNSSFYRLRFELRYRAERSKTFTTWMVKDLQHHCVIHDAWSGLRHVVQLRAQEEFGQGEWSEW<br />
SPEAMGTPWTESRSPPAENEVSTPMQALTTNKDDDNILFRDSANATSLPVQDSSSVPLPTFLVAGGSLAFGTLLCIAIVLRFKKTWKLRALKEGKTSMHPPY<br />
SLGQLVPERPRPTPVLVPLISPPVSPSSLGSDNTSSHNRPDARDPRSPYDISNTDYFFPR<br />
서열 번호: 728<br />
공개특허 10-2011-01<strong>12</strong>308<br />
MLTLQTWVVQALFIFLTTESTGELLDPCGYISPESPVVQLHSNFTAVCVLKEKCMDYFHVNANYIVWKTNHFTIPKEQYTIINRTASSVTFTDIASLNIQLT<br />
CNILTFGQLEQNVYGITIISGLPPEKPKNLSCIVNEGKKMRCEWDGGRETHLETNFTLKSEWATHKFADCKA<strong>KR</strong>DTPTSCTVDYSTVYFVNIEVWVEAENAL<br />
GKVTSDHINFDPVYKVKPNPPHNLSVINSEELSSILKLTWTNPSIKSVIILKYNIQYRTKDASTWSQIPPEDTASTRSSFTVQDLKPFTEYVFRIRCMKEDG<br />
KGYWSDWSEEASGITYEDRPSKAPSFWYKIDPSHTQGYRTVQLVWKTLPPFEANGKILDYEVTLTRWKSHLQNYTVNATKLTVNLTNDRYLATLTVRNLVGK<br />
SDAAVLTIPACDFQATHPVMDLKAFPKDNMLWVEWTTPRESVKKYILEWCVLSDKAPCITDWQQEDGTVHRTYLRGNLAESKCYLITVTPVYADGPGSPESI<br />
KAYLKQAPPSKGPTVRTKKVGKNEAVLEWDQLPVDVQNGFIRNYTIFYRTIIGNETAVNVDSSHTEYTLSSLTSDTLYMVRMAAYTDEGGKDGPEFTFTTPK<br />
FAQGEIEAIVVPVCLAFLLTTLLGVLFCFN<strong>KR</strong>DLIKKHIWPNVPDPSKSHIAQWSPHTPPRHNFNSKDQMYSDGNFTDVSVVEIEANDKKPFPEDLKSLDLF<br />
KKEKINTEGHSSGIGGSSCMSSSRPSISSSDENESSQNTSSTVQYSTVVHSGYRHQVPSVQVFSRSESTQPLLDSEERPEDLQLVDHVDGGDGILPRQQYFK<br />
QNCSQHESSPDISHFERSKQVSSVNEEDFVRLKQQISDHISQSCGSGQMKMFQEVSAADAFGPGTEGQVERFETVGMEAATDEGMPKSYLPQTVRQGGYMPQ<br />
- 185 -
도면<br />
도면1<br />
- 186 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면2<br />
- 187 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면3<br />
- 188 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면4<br />
- 189 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면5<br />
- <strong>19</strong>0 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면6<br />
- <strong>19</strong>1 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면7<br />
- <strong>19</strong>2 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면8<br />
- <strong>19</strong>3 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면9<br />
- <strong>19</strong>4 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면10a<br />
- <strong>19</strong>5 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면10b<br />
- <strong>19</strong>6 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면10c<br />
- <strong>19</strong>7 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면10d<br />
- <strong>19</strong>8 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면10e<br />
- <strong>19</strong>9 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면11<br />
- 200 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면<strong>12</strong><br />
- 201 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면13<br />
- 202 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면14<br />
- 203 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면15<br />
- 204 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면16<br />
- 205 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면17<br />
- 206 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면18<br />
- 207 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면<strong>19</strong><br />
- 208 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면20<br />
- 209 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면21<br />
- 210 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면22<br />
- 211 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면23<br />
- 2<strong>12</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
도면24<br />
- 213 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면25<br />
- 214 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면26a<br />
도면26b<br />
- 215 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면27<br />
- 216 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면28<br />
- 217 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면29<br />
- 218 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면30<br />
도면31<br />
- 2<strong>19</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
도면32<br />
- 220 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면33<br />
- 221 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면34<br />
- 222 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면35<br />
- 223 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면36a<br />
- 224 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면36b<br />
- 225 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면37a<br />
- 226 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면37b<br />
- 227 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면38<br />
- 228 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면39<br />
- 229 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면40<br />
- 230 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면41<br />
- 231 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면42<br />
- 232 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면43<br />
- 233 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면44<br />
- 234 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면45<br />
- 235 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면46<br />
- 236 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면47<br />
- 237 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면48<br />
- 238 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면49<br />
- 239 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면50<br />
- 240 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면51<br />
- 241 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면52<br />
- 242 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면53<br />
- 243 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면54<br />
도면55<br />
- 244 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면56<br />
도면57<br />
- 245 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면58<br />
도면59<br />
- 246 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면60<br />
도면61<br />
- 247 -<br />
공개특허 10-2011-01<strong>12</strong>308
도면62<br />
도면63<br />
서 열 목 록<br />
- 248 -<br />
공개특허 10-2011-01<strong>12</strong>308
Smith, Jeffrey T.L.<br />
Schatzman, Randall C.<br />
Litton, Mark J.<br />
Latham, John<br />
Garcia, Leon<br />
SEQUENCE LISTING<br />
Jensen, Anne Elisabeth Carvalho<br />
Olson, Katie<br />
Dutzar, Ben<br />
Kovacevich, Brian<br />
ANTIBODIES TO IL-6 AND USE THEREOF<br />
67858.706002<br />
PCT/US2009/006274<br />
2009-11-24<br />
61/117,861<br />
2008-11-25<br />
61/117,839<br />
2008-11-25<br />
61/117,811<br />
2008-11-25<br />
<strong>12</strong>/502,581<br />
2009-07-14<br />
<strong>12</strong>/399,156<br />
2009-03-06<br />
<strong>12</strong>/391,717<br />
2009-02-24<br />
<strong>12</strong>/366,567<br />
2009-02-05<br />
728<br />
PatentIn version 3.5<br />
1<br />
183<br />
PRT<br />
Homo sapiens<br />
- 249 -<br />
공개특허 10-2011-01<strong>12</strong>308
1<br />
Val Pro Pro Gly Glu Asp Ser Lys Asp Val Ala Ala Pro His Arg Gln<br />
1 5 10 15<br />
Pro Leu Thr Ser Ser Glu Arg Ile Asp Lys Gln Ile Arg Tyr Ile Leu<br />
20 25 30<br />
Asp Gly Ile Ser Ala Leu Arg Lys Glu Thr Cys Asn Lys Ser Asn Met<br />
35 40 45<br />
Cys Glu Ser Ser Lys Glu Ala Leu Ala Glu Asn Asn Leu Asn Leu Pro<br />
50 55 60<br />
Lys Met Ala Glu Lys Asp Gly Cys Phe Gln Ser Gly Phe Asn Glu Glu<br />
65 70 75 80<br />
Thr Cys Leu Val Lys Ile Ile Thr Gly Leu Leu Glu Phe Glu Val Tyr<br />
85 90 95<br />
Leu Glu Tyr Leu Gln Asn Arg Phe Glu Ser Ser Glu Glu Gln Ala Arg<br />
100 105 110<br />
Ala Val Gln Met Ser Thr Lys Val Leu Ile Gln Phe Leu Gln Lys Lys<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Ala Lys Asn Leu Asp Ala Ile Thr Thr Pro Asp Pro Thr Thr Asn Ala<br />
130 135 140<br />
Ser Leu Leu Thr Lys Leu Gln Ala Gln Asn Gln Trp Leu Gln Asp Met<br />
145 150 155 160<br />
Thr Thr His Leu Ile Leu Arg Ser Phe Lys Glu Phe Leu Gln Ser Ser<br />
Leu Arg Ala Leu Arg Gln Met<br />
2<br />
163<br />
PRT<br />
180<br />
Oryctolagus cuniculus<br />
2<br />
165 170 175<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
- 250 -<br />
공개특허 10-2011-01<strong>12</strong>308
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Ile Asn Asn Glu Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Arg Pro Lys Leu Leu Ile Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Ser Leu Arg Asn Ile Asp Asn Ala Phe Gly Gly Gly Thr Glu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Val Val Val Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro<br />
130 135 140<br />
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu<br />
145 150 155 160<br />
Leu Asn Asn<br />
3<br />
166<br />
PRT<br />
Oryctolagus cuniculus<br />
3<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
- 251 -<br />
공개특허 10-2011-01<strong>12</strong>308
Asn Tyr Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Ile Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
130 135 140<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
145 150 155 160<br />
Leu Gly Cys Leu Val Lys<br />
4<br />
11<br />
PRT<br />
165<br />
Oryctolagus cuniculus<br />
4<br />
Gln Ala Ser Gln Ser Ile Asn Asn Glu Leu Ser<br />
1 5 10<br />
5<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
5<br />
Arg Ala Ser Thr Leu Ala Ser<br />
1 5<br />
6<br />
<strong>12</strong><br />
- 252 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
6<br />
Gln Gln Gly Tyr Ser Leu Arg Asn Ile Asp Asn Ala<br />
1 5 10<br />
7<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
7<br />
Asn Tyr Tyr Val Thr<br />
1 5<br />
8<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
8<br />
Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Trp Ala Ile Gly<br />
1 5 10 15<br />
9<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
9<br />
Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
1 5 10<br />
10<br />
491<br />
DNA<br />
Oryctolagus cuniculus<br />
10<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctcggtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
- 253 -<br />
공개특허 10-2011-01<strong>12</strong>308
gtcaccatca agtgccaggc cagtcagagc attaacaatg aattatcctg gtatcagcag 180<br />
aaaccagggc agcgtcccaa gctcctgatc tatagggcat ccactctggc atctggggtc 240<br />
tcatcgcggt tcaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caacagggtt atagtctgag gaatattgat 360<br />
aatgctttcg gcggagggac cgaggtggtg gtcaaacgta cggtagcggc cccatctgtc 420<br />
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 480<br />
ctgaataact t 491<br />
11<br />
499<br />
DNA<br />
Oryctolagus cuniculus<br />
11<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtaactac tacgtgacct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatcatttat ggtagtgatg aaacggccta cgcgacctgg 240<br />
gcgataggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ctgacagccg cggacacggc cacctatttc tgtgccagag atgatagtag tgactgggat 360<br />
gcaaaattta acttgtgggg ccaaggcacc ctggtcaccg tctcgagcgc ctccaccaag 420<br />
ggcccatcgg tcttccccct ggcaccctcc tccaagagca cctctggggg cacagcggcc 480<br />
ctgggctgcc tggtcaagg 499<br />
<strong>12</strong><br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
<strong>12</strong><br />
caggccagtc agagcattaa caatgaatta tcc 33<br />
13<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
13<br />
- 254 -<br />
공개특허 10-2011-01<strong>12</strong>308
agggcatcca ctctggcatc t 21<br />
14<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
14<br />
caacagggtt atagtctgag gaatattgat aatgct 36<br />
15<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
15<br />
aactactacg tgacc 15<br />
16<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
16<br />
atcatttatg gtagtgatga aacggcctac gcgacctggg cgataggc 48<br />
17<br />
36<br />
DNA<br />
<br />
Oryctolagus cuniculus<br />
17<br />
gatgatagta gtgactggga tgcaaaattt aacttg 36<br />
18<br />
109<br />
PRT<br />
Oryctolagus cuniculus<br />
18<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
- 255 -<br />
공개특허 10-2011-01<strong>12</strong>308
20 25 30<br />
Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Trp Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
<strong>19</strong><br />
109<br />
PRT<br />
100 105<br />
Oryctolagus cuniculus<br />
<strong>19</strong><br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
<br />
20<br />
100 105<br />
- 256 -<br />
공개특허 10-2011-01<strong>12</strong>308
99<br />
PRT<br />
Oryctolagus cuniculus<br />
20<br />
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp<br />
1 5 10 15<br />
Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu Leu<br />
20 25 30<br />
Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr<br />
35 40 45<br />
Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser<br />
50 55 60<br />
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp<br />
65 70 75 80<br />
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn Ile<br />
Asp Asn Ala<br />
21<br />
170<br />
PRT<br />
Oryctolagus cuniculus<br />
21<br />
85 90 95<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Val Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Glu Thr Ile Tyr Ser Trp Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Gln Ala Ser Asp Leu Ala Ser Gly Val<br />
- 257 -<br />
공개특허 10-2011-01<strong>12</strong>308
65 70 75 80<br />
Pro Ser Arg Phe Ser Gly Ser Gly Ala Gly Thr Glu Tyr Thr Leu Thr<br />
85 90 95<br />
Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Ser Gly Ser Asn Val Asp Asn Val Phe Gly Gly Gly Thr Glu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Val Val Val Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro<br />
130 135 140<br />
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu<br />
145 150 155 160<br />
Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys<br />
22<br />
167<br />
PRT<br />
165 170<br />
Oryctolagus cuniculus<br />
22<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Glu Gln Leu Lys Glu Ser Gly Gly Arg Leu Val Thr<br />
20 25 30<br />
Pro Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu<br />
35 40 45<br />
Asn Asp His Ala Met Gly Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Tyr Ile Gly Phe Ile Asn Ser Gly Gly Ser Ala Arg Tyr Ala Ser<br />
65 70 75 80<br />
Trp Ala Glu Gly Arg Phe Thr Ile Ser Arg Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Met Thr Ser Leu Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
- 258 -<br />
공개특허 10-2011-01<strong>12</strong>308
100 105 110<br />
Val Arg Gly Gly Ala Val Trp Ser Ile His Ser Phe Asp Pro Trp Gly<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Pro Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser<br />
130 135 140<br />
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala<br />
145 150 155 160<br />
Ala Leu Gly Cys Leu Val Lys<br />
23<br />
11<br />
PRT<br />
165<br />
Oryctolagus cuniculus<br />
23<br />
Gln Ala Ser Glu Thr Ile Tyr Ser Trp Leu Ser<br />
1 5 10<br />
24<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
24<br />
Gln Ala Ser Asp Leu Ala Ser<br />
1 5<br />
25<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
25<br />
Gln Gln Gly Tyr Ser Gly Ser Asn Val Asp Asn Val<br />
1 5 10<br />
26<br />
5<br />
PRT<br />
- 259 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
26<br />
Asp His Ala Met Gly<br />
1 5<br />
27<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
27<br />
Phe Ile Asn Ser Gly Gly Ser Ala Arg Tyr Ala Ser Trp Ala Glu Gly<br />
1 5 10 15<br />
28<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
28<br />
Gly Gly Ala Val Trp Ser Ile His Ser Phe Asp Pro<br />
1 5 10<br />
29<br />
511<br />
DNA<br />
Oryctolagus cuniculus<br />
29<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctctgtgg aggtagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccaggc cagtgagacc atttacagtt ggttatcctg gtatcagcag 180<br />
aagccagggc agcctcccaa gctcctgatc taccaggcat ccgatctggc atctggggtc 240<br />
ccatcgcgat tcagcggcag tggggctggg acagagtaca ctctcaccat cagcggcgtg 300<br />
cagtgtgacg atgctgccac ttactactgt caacagggtt atagtggtag taatgttgat 360<br />
aatgttttcg gcggagggac cgaggtggtg gtcaaacgta cggtagcggc cccatctgtc 420<br />
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 480<br />
ctgaataact tctatcccag agaggccaaa g 511<br />
30<br />
- 260 -<br />
공개특허 10-2011-01<strong>12</strong>308
501<br />
DNA<br />
Oryctolagus cuniculus<br />
30<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
gagcagctga aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacacttacc <strong>12</strong>0<br />
tgcacagcct ctggattctc cctcaatgac catgcaatgg gctgggtccg ccaggctcca 180<br />
gggaaggggc tggaatacat cggattcatt aatagtggtg gtagcgcacg ctacgcgagc 240<br />
tgggcagaag gccgattcac catctccaga acctcgacca cggtggatct gaaaatgacc 300<br />
agtctgacaa ccgaggacac ggccacctat ttctgtgtca gagggggtgc tgtttggagt 360<br />
attcatagtt ttgatccctg gggcccaggg accctggtca ccgtctcgag cgcctccacc 420<br />
aagggcccat cggtcttccc cctggcaccc tcctccaaga gcacctctgg gggcacagcg 480<br />
gccctgggct gcctggtcaa g 501<br />
31<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
31<br />
caggccagtg agaccattta cagttggtta tcc 33<br />
32<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
32<br />
caggcatccg atctggcatc t 21<br />
33<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
33<br />
caacagggtt atagtggtag taatgttgat aatgtt 36<br />
34<br />
15<br />
- 261 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
34<br />
gaccatgcaa tgggc 15<br />
35<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
35<br />
ttcattaata gtggtggtag cgcacgctac gcgagctggg cagaaggc 48<br />
36<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
36<br />
gggggtgctg tttggagtat tcatagtttt gatccc 36<br />
37<br />
165<br />
PRT<br />
Oryctolagus cuniculus<br />
37<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asp Asn Asn Tyr Leu Ser Trp Phe Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Val Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
- 262 -<br />
공개특허 10-2011-01<strong>12</strong>308
85 90 95<br />
Leu Thr Ile Thr Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Val Tyr Asp Asp Asp Ser Asp Asn Ala Phe Gly Gly Gly Thr<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Glu Val Val Val Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe<br />
130 135 140<br />
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys<br />
145 150 155 160<br />
Leu Leu Asn Asn Phe<br />
38<br />
166<br />
PRT<br />
165<br />
Oryctolagus cuniculus<br />
38<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Val Tyr Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Phe Ile Thr Met Ser Asp Asn Ile Asn Tyr Ala Ser Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Ser Arg Gly Trp Gly Thr Met Gly Arg Leu Asp Leu Trp Gly Pro<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
- 263 -<br />
공개특허 10-2011-01<strong>12</strong>308
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
130 135 140<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
145 150 155 160<br />
Leu Gly Cys Leu Val Lys<br />
39<br />
13<br />
PRT<br />
165<br />
Oryctolagus cuniculus<br />
39<br />
Gln Ala Ser Gln Ser Val Tyr Asp Asn Asn Tyr Leu Ser<br />
1 5 10<br />
40<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
40<br />
Gly Ala Ser Thr Leu Ala Ser<br />
1 5<br />
41<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
41<br />
Ala Gly Val Tyr Asp Asp Asp Ser Asp Asn Ala<br />
1 5 10<br />
42<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
42<br />
Val Tyr Tyr Met Asn<br />
- 264 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5<br />
43<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
43<br />
Phe Ile Thr Met Ser Asp Asn Ile Asn Tyr Ala Ser Trp Ala Lys Gly<br />
1 5 10 15<br />
44<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
44<br />
Ser Arg Gly Trp Gly Thr Met Gly Arg Leu Asp Leu<br />
1 5 10<br />
45<br />
496<br />
DNA<br />
Oryctolagus cuniculus<br />
45<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccg ccgtgctgac ccagactcca tctcccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccaggc cagtcagagt gtttatgaca acaactactt atcctggttt 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctatg gtgcatccac tctggcatct 240<br />
ggggtcccat cgcggttcgt gggcagtgga tctgggacac agttcactct caccatcaca 300<br />
gacgtgcagt gtgacgatgc tgccacttac tattgtgcag gcgtttatga tgatgatagt 360<br />
gataatgcct tcggcggagg gaccgaggtg gtggtcaaac gtacggtagc ggccccatct 420<br />
gtcttcatct tcccgccatc tgatgagcag ttgaaatctg gaactgcctc tgttgtgtgc 480<br />
ctgctgaata acttct 496<br />
46<br />
499<br />
DNA<br />
Oryctolagus cuniculus<br />
- 265 -<br />
공개특허 10-2011-01<strong>12</strong>308
46<br />
atggagactg ggctgcgctg gcttctcctg gtggctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acccctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtgtctac tacatgaact gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg attcattaca atgagtgata atataaatta cgcgagctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagga gtcgtggctg gggtacaatg 360<br />
ggtcggttgg atctctgggg cccaggcacc ctcgtcaccg tctcgagcgc ctccaccaag 420<br />
ggcccatcgg tcttccccct ggcaccctcc tccaagagca cctctggggg cacagcggcc 480<br />
ctgggctgcc tggtcaagg 499<br />
47<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
47<br />
caggccagtc agagtgttta tgacaacaac tacttatcc 39<br />
48<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
48<br />
ggtgcatcca ctctggcatc t 21<br />
49<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
49<br />
gcaggcgttt atgatgatga tagtgataat gcc 33<br />
50<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
50<br />
- 266 -<br />
공개특허 10-2011-01<strong>12</strong>308
gtctactaca tgaac 15<br />
51<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
51<br />
ttcattacaa tgagtgataa tataaattac gcgagctggg cgaaaggc 48<br />
52<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
52<br />
agtcgtggct ggggtacaat gggtcggttg gatctc 36<br />
53<br />
164<br />
PRT<br />
Oryctolagus cuniculus<br />
53<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Ile Cys Asp Pro Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Pro Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Glu Asn Asn Tyr Leu Ser Trp Phe Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Thr Leu Asp Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Thr Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
- 267 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ala Gly Val Tyr Asp Asp Asp Ser Asp Asp Ala Phe Gly Gly Gly Thr<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Glu Val Val Val Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe<br />
130 135 140<br />
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys<br />
145 150 155 160<br />
Leu Leu Asn Asn<br />
54<br />
167<br />
PRT<br />
Oryctolagus cuniculus<br />
54<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Glu Gln Leu Lys Glu Ser Gly Gly Gly Leu Val Thr<br />
20 25 30<br />
Pro Gly Gly Thr Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu<br />
35 40 45<br />
Asn Ala Tyr Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Trp Ile Gly Phe Ile Thr Leu Asn Asn Asn Val Ala Tyr Ala Asn<br />
65 70 75 80<br />
Trp Ala Lys Gly Arg Phe Thr Phe Ser Lys Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Met Thr Ser Pro Thr Pro Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Ser Arg Gly Trp Gly Ala Met Gly Arg Leu Asp Leu Trp Gly<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
His Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser<br />
130 135 140<br />
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala<br />
- 268 -<br />
공개특허 10-2011-01<strong>12</strong>308
145 150 155 160<br />
Ala Leu Gly Cys Leu Val Lys<br />
55<br />
13<br />
PRT<br />
165<br />
Oryctolagus cuniculus<br />
55<br />
Gln Ala Ser Gln Ser Val Tyr Glu Asn Asn Tyr Leu Ser<br />
1 5 10<br />
56<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
56<br />
Gly Ala Ser Thr Leu Asp Ser<br />
1 5<br />
57<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
57<br />
Ala Gly Val Tyr Asp Asp Asp Ser Asp Asp Ala<br />
1 5 10<br />
58<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
58<br />
Ala Tyr Tyr Met Asn<br />
1 5<br />
59<br />
16<br />
- 269 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
59<br />
Phe Ile Thr Leu Asn Asn Asn Val Ala Tyr Ala Asn Trp Ala Lys Gly<br />
1 5 10 15<br />
60<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
60<br />
Ser Arg Gly Trp Gly Ala Met Gly Arg Leu Asp Leu<br />
1 5 10<br />
61<br />
494<br />
DNA<br />
Oryctolagus cuniculus<br />
61<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
atatgtgacc ctgtgctgac ccagactcca tctcccgtat ctgcacctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccaggc cagtcagagt gtttatgaga acaactattt atcctggttt 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctatg gtgcatccac tctggattct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccattaca 300<br />
gacgtgcagt gtgacgatgc tgccacttac tattgtgcag gcgtttatga tgatgatagt 360<br />
gatgatgcct tcggcggagg gaccgaggtg gtggtcaaac gtacggtagc ggccccatct 420<br />
gtcttcatct tcccgccatc tgatgagcag ttgaaatctg gaactgcctc tgttgtgtgc 480<br />
ctgctgaata actt 494<br />
62<br />
502<br />
DNA<br />
Oryctolagus cuniculus<br />
62<br />
atggagactg ggctgcgctg gcttctcctg gtggctgtgc tcaaaggtgt ccagtgtcag 60<br />
- 270 -<br />
공개특허 10-2011-01<strong>12</strong>308
gagcagctga aggagtccgg aggaggcctg gtaacgcctg gaggaaccct gacactcacc <strong>12</strong>0<br />
tgcacagcct ctggattctc cctcaatgcc tactacatga actgggtccg ccaggctcca 180<br />
gggaaggggc tggaatggat cggattcatt actctgaata ataatgtagc ttacgcgaac 240<br />
tgggcgaaag gccgattcac cttctccaaa acctcgacca cggtggatct gaaaatgacc 300<br />
agtccgacac ccgaggacac ggccacctat ttctgtgcca ggagtcgtgg ctggggtgca 360<br />
atgggtcggt tggatctctg gggccatggc accctggtca ccgtctcgag cgcctccacc 420<br />
aagggcccat cggtcttccc cctggcaccc tcctccaaga gcacctctgg gggcacagcg 480<br />
gccctgggct gcctggtcaa gg 502<br />
63<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
63<br />
caggccagtc agagtgttta tgagaacaac tatttatcc 39<br />
64<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
64<br />
ggtgcatcca ctctggattc t 21<br />
65<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
65<br />
gcaggcgttt atgatgatga tagtgatgat gcc 33<br />
66<br />
15<br />
DNA<br />
<br />
Oryctolagus cuniculus<br />
66<br />
gcctactaca tgaac 15<br />
- 271 -<br />
공개특허 10-2011-01<strong>12</strong>308
67<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
67<br />
ttcattactc tgaataataa tgtagcttac gcgaactggg cgaaaggc 48<br />
68<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
68<br />
agtcgtggct ggggtgcaat gggtcggttg gatctc 36<br />
69<br />
164<br />
PRT<br />
Oryctolagus cuniculus<br />
69<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Gln Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Asp Asp Asn Asn Trp Leu Gly Trp Tyr Gln Gln Lys Arg<br />
50 55 60<br />
Gly Gln Pro Pro Lys Tyr Leu Ile Tyr Ser Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Asp Leu Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Gly Phe Ser Gly Asn Ile Phe Ala Phe Gly Gly Gly Thr Glu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
- 272 -<br />
공개특허 10-2011-01<strong>12</strong>308
Val Val Val Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro<br />
130 135 140<br />
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu<br />
145 150 155 160<br />
Leu Asn Asn Phe<br />
70<br />
164<br />
PRT<br />
Oryctolagus cuniculus<br />
70<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Gly Gly Phe Gly Thr Thr Tyr Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Arg Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Gly Gly Pro Gly Asn Gly Gly Asp Ile Trp Gly Gln Gly Thr Leu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu<br />
130 135 140<br />
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys<br />
145 150 155 160<br />
- 273 -<br />
공개특허 10-2011-01<strong>12</strong>308
Leu Val Lys Asp<br />
71<br />
13<br />
PRT<br />
Oryctolagus cuniculus<br />
71<br />
Gln Ala Ser Gln Ser Val Asp Asp Asn Asn Trp Leu Gly<br />
1 5 10<br />
72<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
72<br />
Ser Ala Ser Thr Leu Ala Ser<br />
1 5<br />
73<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
73<br />
Ala Gly Gly Phe Ser Gly Asn Ile Phe Ala<br />
1 5 10<br />
74<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
74<br />
Ser Tyr Ala Met Ser<br />
1 5<br />
75<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
- 274 -<br />
공개특허 10-2011-01<strong>12</strong>308
75<br />
Ile Ile Gly Gly Phe Gly Thr Thr Tyr Tyr Ala Thr Trp Ala Lys Gly<br />
1 5 10 15<br />
76<br />
9<br />
PRT<br />
Oryctolagus cuniculus<br />
76<br />
Gly Gly Pro Gly Asn Gly Gly Asp Ile<br />
1 5<br />
77<br />
493<br />
DNA<br />
Oryctolagus cuniculus<br />
77<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccc aagtgctgac ccagactcca tcgcctgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca actgccaggc cagtcagagt gttgatgata acaactggtt aggctggtat 180<br />
cagcagaaac gagggcagcc tcccaagtac ctgatctatt ctgcatccac tctggcatct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccatcagc 300<br />
gacctggagt gtgacgatgc tgccacttac tactgtgcag gcggttttag tggtaatatc 360<br />
tttgctttcg gcggagggac cgaggtggtg gtcaaacgta cggtagcggc cccatctgtc 420<br />
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 480<br />
ctgaataact tct 493<br />
78<br />
493<br />
DNA<br />
Oryctolagus cuniculus<br />
78<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gcttctccct cagtagctat gcaatgagct gggtccgcca ggctccagga 180<br />
- 275 -<br />
공개특허 10-2011-01<strong>12</strong>308
aaggggctgg agtggatcgg aatcattggt ggttttggta ccacatacta cgcgacctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgag aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag gtggtcctgg taatggtggt 360<br />
gacatctggg gccaagggac cctggtcacc gtctcgagcg cctccaccaa gggcccatcg 420<br />
gtcttccccc tggcaccctc ctccaagagc acctctgggg gcacagcggc cctgggctgc 480<br />
ctggtcaagg act 493<br />
79<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
79<br />
caggccagtc agagtgttga tgataacaac tggttaggc 39<br />
80<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
80<br />
tctgcatcca ctctggcatc t 21<br />
81<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
81<br />
gcaggcggtt ttagtggtaa tatctttgct 30<br />
82<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
82<br />
agctatgcaa tgagc 15<br />
83<br />
48<br />
DNA<br />
- 276 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
83<br />
atcattggtg gttttggtac cacatactac gcgacctggg cgaaaggc 48<br />
84<br />
27<br />
DNA<br />
Oryctolagus cuniculus<br />
84<br />
ggtggtcctg gtaatggtgg tgacatc 27<br />
85<br />
164<br />
PRT<br />
Oryctolagus cuniculus<br />
85<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Val Pro Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asn Phe Leu Ser Trp Tyr Gln Gln Lys Pro Gly<br />
50 55 60<br />
Gln Pro Pro Lys Leu Leu Ile Tyr Gln Ala Ser Lys Leu Ala Ser Gly<br />
65 70 75 80<br />
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu<br />
85 90 95<br />
Thr Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Leu<br />
100 105 110<br />
Gly Gly Tyr Asp Asp Asp Ala Asp Asn Ala Phe Gly Gly Gly Thr Glu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Val Val Val Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro<br />
130 135 140<br />
- 277 -<br />
공개특허 10-2011-01<strong>12</strong>308
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu<br />
145 150 155 160<br />
Leu Asn Asn Phe<br />
86<br />
170<br />
PRT<br />
Oryctolagus cuniculus<br />
86<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser<br />
35 40 45<br />
Asp Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Tyr Ala Gly Ser Gly Ser Thr Trp Tyr Ala Ser<br />
65 70 75 80<br />
Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Asp Gly Tyr Asp Asp Tyr Gly Asp Phe Asp Arg Leu Asp Leu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Trp Gly Pro Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly<br />
130 135 140<br />
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly<br />
145 150 155 160<br />
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp<br />
87<br />
165 170<br />
- 278 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
87<br />
Gln Ser Ser Gln Ser Val Tyr Asn Asn Phe Leu Ser<br />
1 5 10<br />
88<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
88<br />
Gln Ala Ser Lys Leu Ala Ser<br />
1 5<br />
89<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
89<br />
Leu Gly Gly Tyr Asp Asp Asp Ala Asp Asn Ala<br />
1 5 10<br />
90<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
90<br />
Asp Tyr Ala Met Ser<br />
1 5<br />
91<br />
17<br />
PRT<br />
Oryctolagus cuniculus<br />
91<br />
Ile Ile Tyr Ala Gly Ser Gly Ser Thr Trp Tyr Ala Ser Trp Ala Lys<br />
1 5 10 15<br />
- 279 -<br />
공개특허 10-2011-01<strong>12</strong>308
Gly<br />
92<br />
14<br />
PRT<br />
Oryctolagus cuniculus<br />
92<br />
Asp Gly Tyr Asp Asp Tyr Gly Asp Phe Asp Arg Leu Asp Leu<br />
1 5 10<br />
93<br />
492<br />
DNA<br />
Oryctolagus cuniculus<br />
93<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcag ccgtgctgac ccagacacca tcgcccgtgt ctgtacctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccagtc cagtcagagt gtttataata atttcttatc gtggtatcag 180<br />
cagaaaccag ggcagcctcc caagctcctg atctaccagg catccaaact ggcatctggg 240<br />
gtcccagata ggttcagcgg cagtggatct gggacacagt tcactctcac catcagcggc 300<br />
gtgcagtgtg acgatgctgc cacttactac tgtctaggcg gttatgatga tgatgctgat 360<br />
aatgctttcg gcggagggac cgaggtggtg gtcaaacgta cggtagcggc cccatctgtc 420<br />
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 480<br />
ctgaataact tc 492<br />
94<br />
511<br />
DNA<br />
Oryctolagus cuniculus<br />
94<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac gctcacctgc <strong>12</strong>0<br />
acagtctctg gaatcgacct cagtgactat gcaatgagct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatcatttat gctggtagtg gtagcacatg gtacgcgagc 240<br />
- 280 -<br />
공개특허 10-2011-01<strong>12</strong>308
tgggcgaaag gccgattcac catctccaaa acctcgacca cggtggatct gaaaatcacc 300<br />
agtccgacaa ccgaggacac ggccacctat ttctgtgcca gagatggata cgatgactat 360<br />
ggtgatttcg atcgattgga tctctggggc ccaggcaccc tcgtcaccgt ctcgagcgcc 420<br />
tccaccaagg gcccatcggt cttccccctg gcaccctcct ccaagagcac ctctgggggc 480<br />
acagcggccc tgggctgcct ggtcaaggac t 511<br />
95<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
95<br />
cagtccagtc agagtgttta taataatttc ttatcg 36<br />
96<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
96<br />
caggcatcca aactggcatc t 21<br />
97<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
97<br />
ctaggcggtt atgatgatga tgctgataat gct 33<br />
98<br />
15<br />
DNA<br />
<br />
Oryctolagus cuniculus<br />
98<br />
gactatgcaa tgagc 15<br />
99<br />
51<br />
DNA<br />
Oryctolagus cuniculus<br />
- 281 -<br />
공개특허 10-2011-01<strong>12</strong>308
99<br />
atcatttatg ctggtagtgg tagcacatgg tacgcgagct gggcgaaagg c 51<br />
100<br />
42<br />
DNA<br />
Oryctolagus cuniculus<br />
100<br />
gatggatacg atgactatgg tgatttcgat cgattggatc tc 42<br />
101<br />
164<br />
PRT<br />
Oryctolagus cuniculus<br />
101<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Ile Asn Asn Glu Leu Ser Trp Tyr Gln Gln Lys Ser Gly Gln<br />
50 55 60<br />
Arg Pro Lys Leu Leu Ile Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Ser Leu Arg Asn Ile Asp Asn Ala Phe Gly Gly Gly Thr Glu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Val Val Val Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro<br />
130 135 140<br />
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu<br />
- 282 -<br />
공개특허 10-2011-01<strong>12</strong>308
145 150 155 160<br />
Leu Asn Asn Phe<br />
102<br />
166<br />
PRT<br />
Oryctolagus cuniculus<br />
102<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Ser Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Asn Tyr Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Trp<br />
65 70 75 80<br />
Ala Ile Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
130 135 140<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
145 150 155 160<br />
Leu Gly Cys Leu Val Lys<br />
103<br />
11<br />
165<br />
- 283 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
103<br />
Gln Ala Ser Gln Ser Ile Asn Asn Glu Leu Ser<br />
1 5 10<br />
104<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
104<br />
Arg Ala Ser Thr Leu Ala Ser<br />
1 5<br />
105<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
105<br />
Gln Gln Gly Tyr Ser Leu Arg Asn Ile Asp Asn Ala<br />
1 5 10<br />
106<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
106<br />
Asn Tyr Tyr Met Thr<br />
1 5<br />
107<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
107<br />
Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Trp Ala Ile Gly<br />
1 5 10 15<br />
108<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
108<br />
Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
1 5 10<br />
109<br />
492<br />
DNA<br />
Oryctolagus cuniculus<br />
109<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctcggtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca aatgccaggc cagtcagagc attaacaatg aattatcctg gtatcagcag 180<br />
aaatcagggc agcgtcccaa gctcctgatc tatagggcat ccactctggc atctggggtc 240<br />
tcatcgcggt tcaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caacagggtt atagtctgag gaatattgat 360<br />
aatgctttcg gcggagggac cgaggtggtg gtcaaacgta cggtagcggc cccatctgtc 420<br />
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 480<br />
ctgaataact tc 492<br />
110<br />
499<br />
DNA<br />
Oryctolagus cuniculus<br />
110<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tctcaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtaactac tacatgacct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatgatttat ggtagtgatg aaacagccta cgcgaactgg 240<br />
gcgataggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ctgacagccg cggacacggc cacctatttc tgtgccagag atgatagtag tgactgggat 360<br />
gcaaaattta acttgtgggg ccaagggacc ctcgtcaccg tctcgagcgc ctccaccaag 420<br />
- 285 -<br />
공개특허 10-2011-01<strong>12</strong>308
ggcccatcgg tcttccccct ggcaccctcc tccaagagca cctctggggg cacagcggcc 480<br />
ctgggctgcc tggtcaagg 499<br />
111<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
111<br />
caggccagtc agagcattaa caatgaatta tcc 33<br />
1<strong>12</strong><br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
1<strong>12</strong><br />
agggcatcca ctctggcatc t 21<br />
113<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
113<br />
caacagggtt atagtctgag gaatattgat aatgct 36<br />
114<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
114<br />
aactactaca tgacc 15<br />
115<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
115<br />
atgatttatg gtagtgatga aacagcctac gcgaactggg cgataggc 48<br />
116<br />
- 286 -<br />
공개특허 10-2011-01<strong>12</strong>308
36<br />
DNA<br />
Oryctolagus cuniculus<br />
116<br />
gatgatagta gtgactggga tgcaaaattt aacttg 36<br />
117<br />
109<br />
PRT<br />
Oryctolagus cuniculus<br />
117<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Trp Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
118<br />
109<br />
PRT<br />
100 105<br />
Oryctolagus cuniculus<br />
118<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
- 287 -<br />
공개특허 10-2011-01<strong>12</strong>308
20 25 30<br />
Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Ser Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
1<strong>19</strong><br />
100<br />
PRT<br />
100 105<br />
Oryctolagus cuniculus<br />
1<strong>19</strong><br />
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu<br />
20 25 30<br />
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn<br />
Ile Asp Asn Ala<br />
<strong>12</strong>0<br />
16<br />
100<br />
85 90 95<br />
- 288 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
<strong>12</strong>0<br />
Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser Ala Ile Gly<br />
1 5 10 15<br />
<strong>12</strong>1<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>12</strong>1<br />
Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Ser Ala Ile Gly<br />
1 5 10 15<br />
<strong>12</strong>2<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>12</strong>2<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Ser Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Gly Asn Asn Gln Asp Leu Ser Trp Phe Gln Gln Arg Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Glu Ile Ser Lys Leu Glu Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr His Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Leu Gly Gly Tyr Asp Asp Asp Ala Asp Asn Ala<br />
- 289 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong>3<br />
<strong>12</strong>8<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
<strong>12</strong>3<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys His Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Arg Thr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Tyr Ile Trp Ser Gly Gly Ser Thr Tyr Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Leu Gly Asp Thr Gly Gly His Ala Tyr Ala Thr Arg Leu Asn Leu<br />
<strong>12</strong>4<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
<strong>12</strong>4<br />
Gln Ser Ser Gln Ser Val Gly Asn Asn Gln Asp Leu Ser<br />
1 5 10<br />
<strong>12</strong>5<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
- 290 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong>5<br />
Glu Ile Ser Lys Leu Glu Ser<br />
1 5<br />
<strong>12</strong>6<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>12</strong>6<br />
Leu Gly Gly Tyr Asp Asp Asp Ala Asp Asn Ala<br />
1 5 10<br />
<strong>12</strong>7<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>12</strong>7<br />
Ser Arg Thr Met Ser<br />
1 5<br />
<strong>12</strong>8<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>12</strong>8<br />
Tyr Ile Trp Ser Gly Gly Ser Thr Tyr Tyr Ala Thr Trp Ala Lys Gly<br />
1 5 10 15<br />
<strong>12</strong>9<br />
15<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>12</strong>9<br />
Leu Gly Asp Thr Gly Gly His Ala Tyr Ala Thr Arg Leu Asn Leu<br />
1 5 10 15<br />
130<br />
369<br />
- 291 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
130<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcag ccgtgctgac ccagacacca tcacccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca gttgccagtc cagtcagagt gttggtaata accaggactt atcctggttt 180<br />
cagcagagac cagggcagcc tcccaagctc ctgatctacg aaatatccaa actggaatct 240<br />
ggggtcccat cgcggttcag cggcagtgga tctgggacac acttcactct caccatcagc 300<br />
ggcgtacagt gtgacgatgc tgccacttac tactgtctag gcggttatga tgatgatgct 360<br />
gataatgct 369<br />
131<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
131<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcac 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gattctccct cagtagtcgt acaatgtcct gggtccgcca ggctccaggg 180<br />
aaggggctgg agtggatcgg atacatttgg agtggtggta gcacatacta cgcgacctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagat tgggcgatac tggtggtcac 360<br />
gcttatgcta ctcgcttaaa tctc 384<br />
132<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
132<br />
cagtccagtc agagtgttgg taataaccag gacttatcc 39<br />
133<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
- 292 -<br />
공개특허 10-2011-01<strong>12</strong>308
133<br />
gaaatatcca aactggaatc t 21<br />
134<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
134<br />
ctaggcggtt atgatgatga tgctgataat gct 33<br />
135<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
135<br />
agtcgtacaa tgtcc 15<br />
136<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
136<br />
tacatttgga gtggtggtag cacatactac gcgacctggg cgaaaggc 48<br />
137<br />
45<br />
DNA<br />
Oryctolagus cuniculus<br />
137<br />
ttgggcgata ctggtggtca cgcttatgct actcgcttaa atctc 45<br />
138<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
138<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Ser<br />
- 293 -<br />
공개특허 10-2011-01<strong>12</strong>308
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Ser Asn Lys Tyr Leu Ala Trp Tyr Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp Thr Ser Lys Leu Ala Ser<br />
65 70 75 80<br />
Gly Ala Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Leu Gly Ala Tyr Asp Asp Asp Ala Asp Asn Ala<br />
139<br />
<strong>12</strong>6<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
139<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Lys Pro<br />
20 25 30<br />
Asp Glu Thr Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Glu<br />
35 40 45<br />
Gly Gly Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ser Tyr Asp Ser Gly Ser Thr Tyr Tyr Ala Ser Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Met Thr Ser Leu Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
- 294 -<br />
공개특허 10-2011-01<strong>12</strong>308
100 105 110<br />
Val Arg Ser Leu Lys Tyr Pro Thr Val Thr Ser Asp Asp Leu<br />
140<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
140<br />
Gln Ser Ser Gln Ser Val Tyr Ser Asn Lys Tyr Leu Ala<br />
1 5 10<br />
141<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
141<br />
Trp Thr Ser Lys Leu Ala Ser<br />
1 5<br />
142<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
142<br />
Leu Gly Ala Tyr Asp Asp Asp Ala Asp Asn Ala<br />
1 5 10<br />
143<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
143<br />
Gly Gly Tyr Met Thr<br />
1 5<br />
144<br />
16<br />
PRT<br />
- 295 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
144<br />
Ile Ser Tyr Asp Ser Gly Ser Thr Tyr Tyr Ala Ser Trp Ala Lys Gly<br />
1 5 10 15<br />
145<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
145<br />
Ser Leu Lys Tyr Pro Thr Val Thr Ser Asp Asp Leu<br />
1 5 10<br />
146<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
146<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcag ccgtgctgac ccagacacca tcgtccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccagtc cagtcagagt gtttatagta ataagtacct agcctggtat 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctact ggacatccaa actggcatct 240<br />
ggggccccat cacggttcag cggcagtgga tctgggacac aattcactct caccatcagc 300<br />
ggcgtgcagt gtgacgatgc tgccacttac tactgtctag gcgcttatga tgatgatgct 360<br />
gataatgct 369<br />
147<br />
378<br />
DNA<br />
Oryctolagus cuniculus<br />
147<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggaag agtccggggg tcgcctggtc aagcctgacg aaaccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct ggagggcggc tacatgacct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatcagttat gatagtggta gcacatacta cgcgagctgg 240<br />
- 296 -<br />
공개특허 10-2011-01<strong>12</strong>308
gcgaaaggcc gattcaccat ctccaagacc tcgtcgacca cggtggatct gaaaatgacc 300<br />
agtctgacaa ccgaggacac ggccacctat ttctgcgtca gatcactaaa atatcctact 360<br />
gttacttctg atgacttg 378<br />
148<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
148<br />
cagtccagtc agagtgttta tagtaataag tacctagcc 39<br />
149<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
149<br />
tggacatcca aactggcatc t 21<br />
150<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
150<br />
ctaggcgctt atgatgatga tgctgataat gct 33<br />
151<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
151<br />
ggcggctaca tgacc 15<br />
152<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
152<br />
atcagttatg atagtggtag cacatactac gcgagctggg cgaaaggc 48<br />
- 297 -<br />
공개특허 10-2011-01<strong>12</strong>308
153<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
153<br />
tcactaaaat atcctactgt tacttctgat gacttg 36<br />
154<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
154<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Ser Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asn Asn Asp Leu Ala Trp Tyr Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Ala Tyr Tyr Cys<br />
100 105 110<br />
Leu Gly Gly Tyr Asp Asp Asp Ala Asp Asn Ala<br />
155<br />
<strong>12</strong>9<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
155<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
- 298 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Leu Ser Leu Ser<br />
35 40 45<br />
Ser Asn Thr Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Tyr Ile Trp Ser Gly Gly Ser Thr Tyr Tyr Ala Ser Trp<br />
65 70 75 80<br />
Val Asn Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Gly Gly Tyr Ala Ser Gly Gly Tyr Pro Tyr Ala Thr Arg Leu Asp<br />
Leu<br />
156<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
156<br />
Gln Ser Ser Gln Ser Val Tyr Asn Asn Asn Asp Leu Ala<br />
1 5 10<br />
157<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
157<br />
Tyr Ala Ser Thr Leu Ala Ser<br />
1 5<br />
158<br />
- 299 -<br />
공개특허 10-2011-01<strong>12</strong>308
11<br />
PRT<br />
Oryctolagus cuniculus<br />
158<br />
Leu Gly Gly Tyr Asp Asp Asp Ala Asp Asn Ala<br />
1 5 10<br />
159<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
159<br />
Ser Asn Thr Ile Asn<br />
1 5<br />
160<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
160<br />
Tyr Ile Trp Ser Gly Gly Ser Thr Tyr Tyr Ala Ser Trp Val Asn Gly<br />
1 5 10 15<br />
161<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
161<br />
Gly Gly Tyr Ala Ser Gly Gly Tyr Pro Tyr Ala Thr Arg Leu Asp Leu<br />
1 5 10 15<br />
162<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
162<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcag ccgtgctgac ccagacacca tcacccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
- 300 -<br />
공개특허 10-2011-01<strong>12</strong>308
gtcaccatca gttgccagtc cagtcagagt gtttataata ataacgactt agcctggtat 180<br />
cagcagaaac cagggcagcc tcctaaactc ctgatctatt atgcatccac tctggcatct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccatcagc 300<br />
ggcgtgcagt gtgacgatgc tgccgcttac tactgtctag gcggttatga tgatgatgct 360<br />
gataatgct 369<br />
163<br />
387<br />
DNA<br />
Oryctolagus cuniculus<br />
163<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtatctg gattatccct cagtagcaat acaataaact gggtccgcca ggctccaggg 180<br />
aaggggctgg agtggatcgg atacatttgg agtggtggta gtacatacta cgcgagctgg 240<br />
gtgaatggtc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag ggggttacgc tagtggtggt 360<br />
tatccttatg ccactcggtt ggatctc 387<br />
164<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
164<br />
cagtccagtc agagtgttta taataataac gacttagcc 39<br />
165<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
165<br />
tatgcatcca ctctggcatc t 21<br />
166<br />
33<br />
DNA<br />
- 301 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
166<br />
ctaggcggtt atgatgatga tgctgataat gct 33<br />
167<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
167<br />
agcaatacaa taaac 15<br />
168<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
168<br />
tacatttgga gtggtggtag tacatactac gcgagctggg tgaatggt 48<br />
169<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
169<br />
gggggttacg ctagtggtgg ttatccttat gccactcggt tggatctc 48<br />
170<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
170<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asn Asp Tyr Leu Ser Trp Tyr Gln Gln Arg Pro<br />
- 302 -<br />
공개특허 10-2011-01<strong>12</strong>308
50 55 60<br />
Gly Gln Arg Pro Lys Leu Leu Ile Tyr Gly Ala Ser Lys Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Lys Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Leu Gly Asp Tyr Asp Asp Asp Ala Asp Asn Thr<br />
171<br />
<strong>12</strong>3<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
171<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Thr Leu Ser<br />
35 40 45<br />
Thr Asn Tyr Tyr Leu Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Trp Ile Gly Ile Ile Tyr Pro Ser Gly Asn Thr Tyr Cys Ala Lys<br />
65 70 75 80<br />
Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr Thr Val<br />
85 90 95<br />
Asp Leu Lys Met Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe<br />
100 105 110<br />
Cys Ala Arg Asn Tyr Gly Gly Asp Glu Ser Leu<br />
172<br />
13<br />
115 <strong>12</strong>0<br />
- 303 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
172<br />
Gln Ser Ser Gln Ser Val Tyr Asn Asn Asp Tyr Leu Ser<br />
1 5 10<br />
173<br />
7<br />
<br />
PRT<br />
Oryctolagus cuniculus<br />
173<br />
Gly Ala Ser Lys Leu Ala Ser<br />
1 5<br />
174<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
174<br />
Leu Gly Asp Tyr Asp Asp Asp Ala Asp Asn Thr<br />
1 5 10<br />
175<br />
6<br />
PRT<br />
Oryctolagus cuniculus<br />
175<br />
Thr Asn Tyr Tyr Leu Ser<br />
1 5<br />
176<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
176<br />
Ile Ile Tyr Pro Ser Gly Asn Thr Tyr Cys Ala Lys Trp Ala Lys Gly<br />
1 5 10 15<br />
- 304 -<br />
공개특허 10-2011-01<strong>12</strong>308
177<br />
8<br />
PRT<br />
Oryctolagus cuniculus<br />
177<br />
Asn Tyr Gly Gly Asp Glu Ser Leu<br />
1 5<br />
178<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
178<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcag ccgtgctgac ccagacacca tcctccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccagtc cagtcagagt gtttataata acgactactt atcctggtat 180<br />
caacagaggc cagggcaacg tcccaagctc ctaatctatg gtgcttccaa actggcatct 240<br />
ggggtcccgt cacggttcaa aggcagtgga tctgggaaac agtttactct caccatcagc 300<br />
ggcgtgcagt gtgacgatgc tgccacttac tactgtctgg gcgattatga tgatgatgct 360<br />
gataatact 369<br />
179<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
179<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacttgc <strong>12</strong>0<br />
acagtctctg gattcaccct cagtaccaac tactacctga gctgggtccg ccaggctcca 180<br />
gggaaggggc tagaatggat cggaatcatt tatcctagtg gtaacacata ttgcgcgaag 240<br />
tgggcgaaag gccgattcac catctccaaa acctcgtcga ccacggtgga tctgaaaatg 300<br />
accagtccga caaccgagga cacagccacg tatttctgtg ccagaaatta tggtggtgat 360<br />
gaaagtttg 369<br />
180<br />
39<br />
- 305 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
180<br />
cagtccagtc agagtgttta taataacgac tacttatcc 39<br />
181<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
181<br />
ggtgcttcca aactggcatc t 21<br />
182<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
182<br />
ctgggcgatt atgatgatga tgctgataat act 33<br />
183<br />
18<br />
DNA<br />
Oryctolagus cuniculus<br />
183<br />
accaactact acctgagc 18<br />
184<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
184<br />
atcatttatc ctagtggtaa cacatattgc gcgaagtggg cgaaaggc 48<br />
185<br />
24<br />
DNA<br />
Oryctolagus cuniculus<br />
185<br />
- 306 -<br />
공개특허 10-2011-01<strong>12</strong>308
aattatggtg gtgatgaaag tttg 24<br />
186<br />
1<strong>19</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
186<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Asp Val Val Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Glu Thr Ile Gly Asn Ala Leu Ala Trp Tyr Gln Gln Lys Ser Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Lys Ala Ser Lys Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Trp<br />
100 105 110<br />
Cys Tyr Phe Gly Asp Ser Val<br />
115<br />
187<br />
<strong>12</strong>8<br />
PRT<br />
Oryctolagus cuniculus<br />
187<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Thr Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Glu Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln<br />
20 25 30<br />
Pro Glu Gly Ser Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Asp Phe<br />
- 307 -<br />
공개특허 10-2011-01<strong>12</strong>308
35 40 45<br />
Ser Ser Gly Tyr Tyr Met Cys Trp Val Arg Gln Ala Pro Gly Lys Gly<br />
50 55 60<br />
Leu Glu Trp Ile Ala Cys Ile Phe Thr Ile Thr Thr Asn Thr Tyr Tyr<br />
65 70 75 80<br />
Ala Ser Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr<br />
85 90 95<br />
Thr Val Thr Leu Gln Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr<br />
100 105 110<br />
Tyr Leu Cys Ala Arg Gly Ile Tyr Ser Asp Asn Asn Tyr Tyr Ala Leu<br />
188<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
188<br />
Gln Ala Ser Glu Thr Ile Gly Asn Ala Leu Ala<br />
1 5 10<br />
<br />
189<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
189<br />
Lys Ala Ser Lys Leu Ala Ser<br />
1 5<br />
<strong>19</strong>0<br />
9<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>19</strong>0<br />
Gln Trp Cys Tyr Phe Gly Asp Ser Val<br />
1 5<br />
<strong>19</strong>1<br />
- 308 -<br />
공개특허 10-2011-01<strong>12</strong>308
6<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>19</strong>1<br />
Ser Gly Tyr Tyr Met Cys<br />
1 5<br />
<strong>19</strong>2<br />
17<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>19</strong>2<br />
Cys Ile Phe Thr Ile Thr Thr Asn Thr Tyr Tyr Ala Ser Trp Ala Lys<br />
1 5 10 15<br />
Gly<br />
<strong>19</strong>3<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
<strong>19</strong>3<br />
Gly Ile Tyr Ser Asp Asn Asn Tyr Tyr Ala Leu<br />
1 5 10<br />
<strong>19</strong>4<br />
357<br />
DNA<br />
Oryctolagus cuniculus<br />
<strong>19</strong>4<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgatg ttgtgatgac ccagactcca gcctccgtgg aggcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtgagacc attggcaatg cattagcctg gtatcagcag 180<br />
aaatcagggc agcctcccaa gctcctgatc tacaaggcat ccaaactggc atctggggtc 240<br />
ccatcgcggt tcaaaggcag tggatctggg acagagtaca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caatggtgtt attttggtga tagtgtt 357<br />
- 309 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>19</strong>5<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
<strong>19</strong>5<br />
atggagactg ggctgcgctg gcttctcctg gtcactgtgc tcaaaggtgt ccagtgtcag 60<br />
gagcagctgg tggagtccgg gggaggcctg gtccagcctg agggatccct gacactcacc <strong>12</strong>0<br />
tgcacagcct ctggattcga cttcagtagc ggctactaca tgtgctgggt ccgccaggct 180<br />
ccagggaagg ggctggagtg gatcgcgtgt attttcacta ttactactaa cacttactac 240<br />
gcgagctggg cgaaaggccg attcaccatc tccaagacct cgtcgaccac ggtgactctg 300<br />
caaatgacca gtctgacagc cgcggacacg gccacctatc tctgtgcgag agggatttat 360<br />
tctgataata attattatgc cttg 384<br />
<strong>19</strong>6<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
<strong>19</strong>6<br />
caggccagtg agaccattgg caatgcatta gcc 33<br />
<strong>19</strong>7<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
<strong>19</strong>7<br />
aaggcatcca aactggcatc t 21<br />
<strong>19</strong>8<br />
27<br />
DNA<br />
Oryctolagus cuniculus<br />
<strong>19</strong>8<br />
caatggtgtt attttggtga tagtgtt 27<br />
<strong>19</strong>9<br />
18<br />
DNA<br />
- 310 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
<strong>19</strong>9<br />
agcggctact acatgtgc 18<br />
200<br />
51<br />
DNA<br />
Oryctolagus cuniculus<br />
200<br />
tgtattttca ctattactac taacacttac tacgcgagct gggcgaaagg c 51<br />
201<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
201<br />
gggatttatt ctgataataa ttattatgcc ttg 33<br />
202<br />
1<strong>19</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
202<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Asp Val Val Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Glu Ser Ile Gly Asn Ala Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Lys Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
- 311 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ile Ser Gly Val Gln Cys Ala Asp Ala Ala Ala Tyr Tyr Cys Gln Trp<br />
100 105 110<br />
Cys Tyr Phe Gly Asp Ser Val<br />
115<br />
203<br />
<strong>12</strong>8<br />
PRT<br />
Oryctolagus cuniculus<br />
203<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Gln Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys<br />
20 25 30<br />
Pro Gly Ala Ser Leu Thr Leu Thr Cys Lys Ala Ser Gly Phe Ser Phe<br />
35 40 45<br />
Ser Ser Gly Tyr Tyr Met Cys Trp Val Arg Gln Ala Pro Gly Lys Gly<br />
50 55 60<br />
Leu Glu Ser Ile Ala Cys Ile Phe Thr Ile Thr Asp Asn Thr Tyr Tyr<br />
65 70 75 80<br />
Ala Asn Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Pro Ser Ser Pro<br />
85 90 95<br />
Thr Val Thr Leu Gln Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr<br />
100 105 110<br />
Tyr Phe Cys Ala Arg Gly Ile Tyr Ser Thr Asp Asn Tyr Tyr Ala Leu<br />
204<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
204<br />
Gln Ala Ser Glu Ser Ile Gly Asn Ala Leu Ala<br />
1 5 10<br />
- 3<strong>12</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
205<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
205<br />
Lys Ala Ser Thr Leu Ala Ser<br />
1 5<br />
206<br />
9<br />
PRT<br />
Oryctolagus cuniculus<br />
206<br />
Gln Trp Cys Tyr Phe Gly Asp Ser Val<br />
1 5<br />
207<br />
6<br />
PRT<br />
Oryctolagus cuniculus<br />
207<br />
Ser Gly Tyr Tyr Met Cys<br />
1 5<br />
208<br />
17<br />
PRT<br />
Oryctolagus cuniculus<br />
208<br />
Cys Ile Phe Thr Ile Thr Asp Asn Thr Tyr Tyr Ala Asn Trp Ala Lys<br />
1 5 10 15<br />
Gly<br />
209<br />
11<br />
PRT<br />
- 313 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
209<br />
Gly Ile Tyr Ser Thr Asp Asn Tyr Tyr Ala Leu<br />
1 5 10<br />
210<br />
357<br />
DNA<br />
Oryctolagus cuniculus<br />
210<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgatg ttgtgatgac ccagactcca gcctccgtgg aggcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtgagagc attggcaatg cattagcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gctcctgatc tacaaggcat ccactctggc atctggggtc 240<br />
ccatcgcggt tcagcggcag tggatctggg acagagttca ctctcaccat cagcggcgtg 300<br />
cagtgtgccg atgctgccgc ttactactgt caatggtgtt attttggtga tagtgtt 357<br />
211<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
211<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
cagcagctgg tggagtccgg gggaggcctg gtcaagccgg gggcatccct gacactcacc <strong>12</strong>0<br />
tgcaaagcct ctggattctc cttcagtagc ggctactaca tgtgctgggt ccgccaggct 180<br />
ccagggaagg ggctggagtc gatcgcatgc atttttacta ttactgataa cacttactac 240<br />
gcgaactggg cgaaaggccg attcaccatc tccaagccct cgtcgcccac ggtgactctg 300<br />
caaatgacca gtctgacagc cgcggacacg gccacctatt tctgtgcgag ggggatttat 360<br />
tctactgata attattatgc cttg 384<br />
2<strong>12</strong><br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
2<strong>12</strong><br />
caggccagtg agagcattgg caatgcatta gcc 33<br />
- 314 -<br />
공개특허 10-2011-01<strong>12</strong>308
213<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
213<br />
aaggcatcca ctctggcatc t 21<br />
214<br />
27<br />
DNA<br />
Oryctolagus cuniculus<br />
214<br />
caatggtgtt attttggtga tagtgtt 27<br />
215<br />
18<br />
DNA<br />
Oryctolagus cuniculus<br />
215<br />
agcggctact acatgtgc 18<br />
216<br />
51<br />
DNA<br />
Oryctolagus cuniculus<br />
216<br />
tgcattttta ctattactga taacacttac tacgcgaact gggcgaaagg c 51<br />
217<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
217<br />
gggatttatt ctactgataa ttattatgcc ttg 33<br />
218<br />
<strong>12</strong>3<br />
PRT<br />
- 315 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
218<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Asp Val Val Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Arg Ala Ser Thr Leu Glu Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Cys<br />
100 105 110<br />
Thr Tyr Gly Thr Ser Ser Ser Tyr Gly Ala Ala<br />
2<strong>19</strong><br />
133<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
2<strong>19</strong><br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Ser Leu Ser<br />
35 40 45<br />
Ser Asn Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Ser Tyr Ser Gly Thr Thr Tyr Tyr Ala Ser Trp<br />
- 316 -<br />
공개특허 10-2011-01<strong>12</strong>308
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Asp Asp Pro Thr Thr Val Met Val Met Leu Ile Pro Phe Gly<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Ala Gly Met Asp Leu<br />
130<br />
220<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
220<br />
Gln Ala Ser Gln Ser Val Ser Ser Tyr Leu Asn<br />
1 5 10<br />
221<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
221<br />
Arg Ala Ser Thr Leu Glu Ser<br />
1 5<br />
222<br />
13<br />
PRT<br />
Oryctolagus cuniculus<br />
222<br />
Gln Cys Thr Tyr Gly Thr Ser Ser Ser Tyr Gly Ala Ala<br />
1 5 10<br />
223<br />
5<br />
PRT<br />
- 317 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
223<br />
Ser Asn Ala Ile Ser<br />
1 5<br />
224<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
224<br />
Ile Ile Ser Tyr Ser Gly Thr Thr Tyr Tyr Ala Ser Trp Ala Lys Gly<br />
1 5 10 15<br />
225<br />
<strong>19</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
225<br />
Asp Asp Pro Thr Thr Val Met Val Met Leu Ile Pro Phe Gly Ala Gly<br />
1 5 10 15<br />
Met Asp Leu<br />
226<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
226<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgatg ttgtgatgac ccagactcca gcctccgtgg aggcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtcagagc gttagtagct acttaaactg gtatcagcag 180<br />
aaaccagggc agcctcccaa gctcctgatc tacagggcat ccactctgga atctggggtc 240<br />
ccatcgcggt tcaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caatgtactt atggtactag tagtagttat 360<br />
ggtgctgct 369<br />
227<br />
- 318 -<br />
공개특허 10-2011-01<strong>12</strong>308
399<br />
DNA<br />
Oryctolagus cuniculus<br />
227<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
accgtctctg gtatctccct cagtagcaat gcaataagct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatcattagt tatagtggta ccacatacta cgcgagctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgtcgacca cggtggatct gaaaatcact 300<br />
agtccgacaa ccgaggacac ggccacctac ttctgtgcca gagatgaccc tacgacagtt 360<br />
atggttatgt tgataccttt tggagccggc atggacctc 399<br />
228<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
228<br />
caggccagtc agagcgttag tagctactta aac 33<br />
229<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
229<br />
agggcatcca ctctggaatc t 21<br />
230<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
230<br />
caatgtactt atggtactag tagtagttat ggtgctgct 39<br />
231<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
- 3<strong>19</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
231<br />
agcaatgcaa taagc 15<br />
232<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
232<br />
atcattagtt atagtggtac cacatactac gcgagctggg cgaaaggc 48<br />
233<br />
57<br />
DNA<br />
Oryctolagus cuniculus<br />
233<br />
gatgacccta cgacagttat ggttatgttg ataccttttg gagccggcat ggacctc 57<br />
234<br />
<strong>12</strong>5<br />
PRT<br />
Oryctolagus cuniculus<br />
234<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Gln Val Leu Thr Gln Thr Ala Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Lys Asn Asn Tyr Leu Ser Trp Tyr Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Gly Leu Ile Tyr Ser Ala Ser Thr Leu Asp Ser<br />
65 70 75 80<br />
Gly Val Pro Leu Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
- 320 -<br />
공개특허 10-2011-01<strong>12</strong>308
100 105 110<br />
Leu Gly Ser Tyr Asp Cys Ser Ser Gly Asp Cys Tyr Ala<br />
235<br />
1<strong>19</strong><br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
235<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Asp Leu Val Lys Pro<br />
20 25 30<br />
Glu Gly Ser Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Phe Ser<br />
35 40 45<br />
Ser Tyr Trp Met Cys Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Ala Cys Ile Val Thr Gly Asn Gly Asn Thr Tyr Tyr Ala Asn<br />
65 70 75 80<br />
Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr Thr Val<br />
85 90 95<br />
Thr Leu Gln Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr Phe<br />
100 105 110<br />
Cys Ala Lys Ala Tyr Asp Leu<br />
115<br />
236<br />
13<br />
PRT<br />
Oryctolagus cuniculus<br />
236<br />
Gln Ala Ser Gln Ser Val Tyr Lys Asn Asn Tyr Leu Ser<br />
1 5 10<br />
237<br />
- 321 -<br />
공개특허 10-2011-01<strong>12</strong>308
7<br />
PRT<br />
Oryctolagus cuniculus<br />
237<br />
Ser Ala Ser Thr Leu Asp Ser<br />
1 5<br />
238<br />
13<br />
PRT<br />
Oryctolagus cuniculus<br />
238<br />
Leu Gly Ser Tyr Asp Cys Ser Ser Gly Asp Cys Tyr Ala<br />
1 5 10<br />
239<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
239<br />
Ser Tyr Trp Met Cys<br />
1 5<br />
240<br />
17<br />
PRT<br />
Oryctolagus cuniculus<br />
240<br />
Cys Ile Val Thr Gly Asn Gly Asn Thr Tyr Tyr Ala Asn Trp Ala Lys<br />
1 5 10 15<br />
Gly<br />
241<br />
4<br />
PRT<br />
Oryctolagus cuniculus<br />
241<br />
- 322 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ala Tyr Asp Leu<br />
1<br />
242<br />
375<br />
DNA<br />
Oryctolagus cuniculus<br />
242<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccc aagtgctgac ccagactgca tcgcccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca actgccaggc cagtcagagt gtttataaga acaactactt atcctggtat 180<br />
cagcagaaac cagggcagcc tcccaaaggc ctgatctatt ctgcatcgac tctagattct 240<br />
ggggtcccat tgcggttcag cggcagtgga tctgggacac agttcactct caccatcagc 300<br />
gacgtgcagt gtgacgatgc tgccacttac tactgtctag gcagttatga ttgtagtagt 360<br />
ggtgattgtt atgct 375<br />
243<br />
357<br />
DNA<br />
Oryctolagus cuniculus<br />
243<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgttggagg agtccggggg agacctggtc aagcctgagg gatccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctcctt cagtagctac tggatgtgct gggtccgcca ggctccaggg 180<br />
aaggggctgg agtggatcgc atgcattgtt actggtaatg gtaacactta ctacgcgaac 240<br />
tgggcgaaag gccgattcac catctccaaa acctcgtcga ccacggtgac tctgcaaatg 300<br />
accagtctga cagccgcgga cacggccacc tatttttgtg cgaaagccta tgacttg 357<br />
244<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
244<br />
caggccagtc agagtgttta taagaacaac tacttatcc 39<br />
245<br />
- 323 -<br />
공개특허 10-2011-01<strong>12</strong>308
21<br />
DNA<br />
Oryctolagus cuniculus<br />
245<br />
tctgcatcga ctctagattc t 21<br />
246<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
246<br />
ctaggcagtt atgattgtag tagtggtgat tgttatgct 39<br />
247<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
247<br />
agctactgga tgtgc 15<br />
248<br />
51<br />
DNA<br />
Oryctolagus cuniculus<br />
248<br />
tgcattgtta ctggtaatgg taacacttac tacgcgaact gggcgaaagg c 51<br />
249<br />
<strong>12</strong><br />
DNA<br />
Oryctolagus cuniculus<br />
249<br />
gcctatgact tg <strong>12</strong><br />
250<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
250<br />
- 324 -<br />
공개특허 10-2011-01<strong>12</strong>308
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ser Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asp Asn Asn Tyr Leu Ser Trp Tyr Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Thr Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Thr Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Val Phe Asn Asp Asp Ser Asp Asp Ala<br />
251<br />
<strong>12</strong>5<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
251<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Pro Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Leu Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ala Tyr Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Phe Ile Thr Leu Ser Asp His Ile Ser Tyr Ala Arg Trp<br />
65 70 75 80<br />
- 325 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Ser Arg Gly Trp Gly Ala Met Gly Arg Leu Asp Leu<br />
252<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
252<br />
Gln Ala Ser Gln Ser Val Tyr Asp Asn Asn Tyr Leu Ser<br />
1 5 10<br />
253<br />
<<br />
211> 7<br />
PRT<br />
Oryctolagus cuniculus<br />
253<br />
Gly Ala Ser Thr Leu Ala Ser<br />
1 5<br />
254<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
254<br />
Ala Gly Val Phe Asn Asp Asp Ser Asp Asp Ala<br />
1 5 10<br />
255<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
255<br />
Ala Tyr Tyr Met Ser<br />
- 326 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5<br />
256<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
256<br />
Phe Ile Thr Leu Ser Asp His Ile Ser Tyr Ala Arg Trp Ala Lys Gly<br />
1 5 10 15<br />
257<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
257<br />
Ser Arg Gly Trp Gly Ala Met Gly Arg Leu Asp Leu<br />
1 5 10<br />
258<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
258<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggttcc 60<br />
acatttgccg ccgtgctgac ccagactcca tctcccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccaggc cagtcagagt gtttatgaca acaactattt atcctggtat 180<br />
cagcagaaac caggacagcc tcccaagctc ctgatctatg gtgcatccac tctggcatct 240<br />
ggggtcccat cgcggttcaa aggcacggga tctgggacac agttcactct caccatcaca 300<br />
gacgtgcagt gtgacgatgc tgccacttac tattgtgcag gcgtttttaa tgatgatagt 360<br />
gatgatgcc 369<br />
259<br />
375<br />
DNA<br />
Oryctolagus cuniculus<br />
259<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc ccaaaggtgt ccagtgtcag 60<br />
- 327 -<br />
공개특허 10-2011-01<strong>12</strong>308
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acactctctg gattctccct cagtgcatac tatatgagct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg attcattact ctgagtgatc atatatctta cgcgaggtgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagga gtcgtggctg gggtgcaatg 360<br />
ggtcggttgg atctc 375<br />
260<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
260<br />
caggccagtc agagtgttta tgacaacaac tatttatcc 39<br />
261<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
261<br />
ggtgcatcca ctctggcatc t 21<br />
262<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
262<br />
gcaggcgttt ttaatgatga tagtgatgat gcc 33<br />
263<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
263<br />
gcatactata tgagc 15<br />
264<br />
48<br />
- 328 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
264<br />
ttcattactc tgagtgatca tatatcttac gcgaggtggg cgaaaggc 48<br />
265<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
265<br />
agtcgtggct ggggtgcaat gggtcggttg gatctc 36<br />
266<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
266<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Ser Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asn Lys Asn Leu Ala Trp Tyr Gln Gln Lys Ser<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Ser Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Val Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Leu Gly Val Phe Asp Asp Asp Ala Asp Asn Ala<br />
267<br />
115 <strong>12</strong>0<br />
- 329 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong>1<br />
PRT<br />
Oryctolagus cuniculus<br />
267<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Tyr Ser Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Tyr Ile Gly Val Ile Gly Thr Ser Gly Ser Thr Tyr Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Arg Thr Ser Thr Thr Val Ala Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Val<br />
100 105 110<br />
Arg Ser Leu Ser Ser Ile Thr Phe Leu<br />
268<br />
13<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
268<br />
Gln Ala Ser Gln Ser Val Tyr Asn Asn Lys Asn Leu Ala<br />
1 5 10<br />
269<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
269<br />
- 330 -<br />
공개특허 10-2011-01<strong>12</strong>308
Trp Ala Ser Thr Leu Ala Ser<br />
1 5<br />
270<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
270<br />
Leu Gly Val Phe Asp Asp Asp Ala Asp Asn Ala<br />
1 5 10<br />
271<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
271<br />
Ser Tyr Ser Met Thr<br />
1 5<br />
272<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
272<br />
Val Ile Gly Thr Ser Gly Ser Thr Tyr Tyr Ala Thr Trp Ala Lys Gly<br />
1 5 10 15<br />
273<br />
8<br />
PRT<br />
Oryctolagus cuniculus<br />
273<br />
Ser Leu Ser Ser Ile Thr Phe Leu<br />
1 5<br />
274<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
- 331 -<br />
공개특허 10-2011-01<strong>12</strong>308
274<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acattcgcag ccgtgctgac ccagacacca tcgcccgtgt ctgcggctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca gttgccaggc cagtcagagt gtttataaca acaaaaattt agcctggtat 180<br />
cagcagaaat cagggcagcc tcccaagctc ctgatctact gggcatccac tctggcatct 240<br />
ggggtctcat cgcggttcag cggcagtgga tctgggacac agttcactct caccgtcagc 300<br />
ggcgtgcagt gtgacgatgc tgccacttac tactgtctag gcgtttttga tgatgatgct 360<br />
gataatgct 369<br />
275<br />
363<br />
DNA<br />
Oryctolagus cuniculus<br />
275<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccaatgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtagctac tccatgacct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatatatcgg agtcattggt actagtggta gcacatacta cgcgacctgg 240<br />
gcgaaaggcc gattcaccat ctccagaacc tcgaccacgg tggctctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgtcagga gtctttcttc tattactttc 360<br />
ttg 363<br />
276<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
276<br />
caggccagtc agagtgttta taacaacaaa aatttagcc 39<br />
277<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
277<br />
tgggcatcca ctctggcatc t 21<br />
- 332 -<br />
공개특허 10-2011-01<strong>12</strong>308
278<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
278<br />
ctaggcgttt ttgatgatga tgctgataat gct 33<br />
279<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
279<br />
agctactcca tgacc 15<br />
280<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
280<br />
gtcattggta ctagtggtag cacatactac gcgacctggg cgaaaggc 48<br />
281<br />
24<br />
DNA<br />
Oryctolagus cuniculus<br />
281<br />
agtctttctt ctattacttt cttg 24<br />
282<br />
<strong>12</strong>0<br />
PRT<br />
Oryctolagus cuniculus<br />
282<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Phe Glu Leu Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
- 333 -<br />
공개특허 10-2011-01<strong>12</strong>308
Val Glu Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Gln Asn Ile Tyr Arg Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Phe Leu Ile Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Ser<br />
100 105 110<br />
Tyr Tyr Ser Ser Asn Ser Val Ala<br />
283<br />
<strong>12</strong>8<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
283<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Glu Gln Leu Val Glu Ser Gly Gly Asp Leu Val Gln<br />
20 25 30<br />
Pro Glu Gly Ser Leu Thr Leu Thr Cys Thr Ala Ser Glu Leu Asp Phe<br />
35 40 45<br />
Ser Ser Gly Tyr Trp Ile Cys Trp Val Arg Gln Val Pro Gly Lys Gly<br />
50 55 60<br />
Leu Glu Trp Ile Gly Cys Ile Tyr Thr Gly Ser Ser Gly Ser Thr Phe<br />
65 70 75 80<br />
Tyr Ala Ser Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser<br />
85 90 95<br />
Thr Thr Val Thr Leu Gln Met Thr Ser Leu Thr Ala Ala Asp Thr Ala<br />
100 105 110<br />
Thr Tyr Phe Cys Ala Arg Gly Tyr Ser Gly Phe Gly Tyr Phe Lys Leu<br />
- 334 -<br />
공개특허 10-2011-01<strong>12</strong>308
284<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
284<br />
Gln Ala Ser Gln Asn Ile Tyr Arg Tyr Leu Ala<br />
1 5 10<br />
<br />
285<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
285<br />
Leu Ala Ser Thr Leu Ala Ser<br />
1 5<br />
286<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
286<br />
Gln Ser Tyr Tyr Ser Ser Asn Ser Val Ala<br />
1 5 10<br />
287<br />
6<br />
PRT<br />
Oryctolagus cuniculus<br />
287<br />
Ser Gly Tyr Trp Ile Cys<br />
1 5<br />
288<br />
18<br />
PRT<br />
Oryctolagus cuniculus<br />
- 335 -<br />
공개특허 10-2011-01<strong>12</strong>308
288<br />
Cys Ile Tyr Thr Gly Ser Ser Gly Ser Thr Phe Tyr Ala Ser Trp Ala<br />
1 5 10 15<br />
Lys Gly<br />
289<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
289<br />
Gly Tyr Ser Gly Phe Gly Tyr Phe Lys Leu<br />
1 5 10<br />
290<br />
360<br />
DNA<br />
Oryctolagus cuniculus<br />
290<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcat tcgaattgac ccagactcca gcctccgtgg aggcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccaggc cagtcagaac atttatagat acttagcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gttcctgatc tatctggcat ctactctggc atctggggtc 240<br />
ccatcgcggt ttaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caaagttatt atagtagtaa tagtgtcgct 360<br />
291<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
291<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
gagcagctgg tggagtccgg gggagacctg gtccagcctg agggatccct gacactcacc <strong>12</strong>0<br />
tgcacagctt ctgagttaga cttcagtagc ggctactgga tatgctgggt ccgccaggtt 180<br />
ccagggaagg ggctggagtg gatcggatgc atttatactg gtagtagtgg tagcactttt 240<br />
- 336 -<br />
공개특허 10-2011-01<strong>12</strong>308
tacgcgagtt gggcgaaagg ccgattcacc atctccaaaa cctcgtcgac cacggtgact 300<br />
ctgcaaatga ccagtctgac agccgcggac acggccacct atttctgtgc gagaggttat 360<br />
agtggctttg gttactttaa gttg 384<br />
292<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
292<br />
caggccagtc agaacattta tagatactta gcc 33<br />
293<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
293<br />
ctggcatcta ctctggcatc t 21<br />
294<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
294<br />
caaagttatt atagtagtaa tagtgtcgct 30<br />
295<br />
18<br />
DNA<br />
Oryctolagus cuniculus<br />
295<br />
agcggctact ggatatgc 18<br />
296<br />
54<br />
DNA<br />
Oryctolagus cuniculus<br />
296<br />
tgcatttata ctggtagtag tggtagcact ttttacgcga gttgggcgaa aggc 54<br />
- 337 -<br />
공개특허 10-2011-01<strong>12</strong>308
297<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
297<br />
ggttatagtg gctttggtta ctttaagttg 30<br />
298<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
298<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Val Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Glu Asp Ile Tyr Arg Leu Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Asp Ser Ser Asp Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Ala<br />
85 90 95<br />
Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Ala Trp Ser Tyr Ser Asp Ile Asp Asn Ala<br />
299<br />
<strong>12</strong>3<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
299<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
- 338 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Tyr Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Thr Thr Ser Gly Asn Thr Phe Tyr Ala Ser Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Leu Thr Ile Ser Arg Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Thr Ser Asp Ile Phe Tyr Tyr Arg Asn Leu<br />
300<br />
11<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
300<br />
Gln Ala Ser Glu Asp Ile Tyr Arg Leu Leu Ala<br />
1 5 10<br />
301<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
301<br />
Asp Ser Ser Asp Leu Ala Ser<br />
1 5<br />
302<br />
<strong>12</strong><br />
PRT<br />
- 339 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
302<br />
Gln Gln Ala Trp Ser Tyr Ser Asp Ile Asp Asn Ala<br />
1 5 10<br />
303<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
303<br />
Ser Tyr Tyr Met Ser<br />
1 5<br />
304<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
304<br />
Ile Ile Thr Thr Ser Gly Asn Thr Phe Tyr Ala Ser Trp Ala Lys Gly<br />
1 5 10 15<br />
305<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
305<br />
Thr Ser Asp Ile Phe Tyr Tyr Arg Asn Leu<br />
1 5 10<br />
306<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
306<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctctgtgg aggtagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtgaggac atttataggt tattggcctg gtatcaacag 180<br />
- 340 -<br />
공개특허 10-2011-01<strong>12</strong>308
aaaccagggc agcctcccaa gctcctgatc tatgattcat ccgatctggc atctggggtc 240<br />
ccatcgcggt tcaaaggcag tggatctggg acagagttca ctctcgccat cagcggtgtg 300<br />
cagtgtgacg atgctgccac ttactactgt caacaggctt ggagttatag tgatattgat 360<br />
aatgct 366<br />
307<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
307<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgccgggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtagctac tacatgagct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatcattact actagtggta atacatttta cgcgagctgg 240<br />
gcgaaaggcc ggctcaccat ctccagaacc tcgaccacgg tggatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagaa cttctgatat tttttattat 360<br />
cgtaacttg 369<br />
308<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
308<br />
caggccagtg aggacattta taggttattg gcc 33<br />
309<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
309<br />
gattcatccg atctggcatc t 21<br />
310<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
310<br />
- 341 -<br />
공개특허 10-2011-01<strong>12</strong>308
caacaggctt ggagttatag tgatattgat aatgct 36<br />
311<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
311<br />
agctactaca tgagc 15<br />
3<strong>12</strong><br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
3<strong>12</strong><br />
atcattacta ctagtggtaa tacattttac gcgagctggg cgaaaggc 48<br />
313<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
313<br />
acttctgata ttttttatta tcgtaacttg 30<br />
314<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
314<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Ala Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Ala Thr Val Thr Ile Asn Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asp Met Asp Leu Ala Trp Phe Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Ala Ser Thr Leu Ala Ser<br />
- 342 -<br />
공개특허 10-2011-01<strong>12</strong>308
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Leu Gly Ala Phe Asp Asp Asp Ala Asp Asn Thr<br />
315<br />
<strong>12</strong>9<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
315<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr<br />
35 40 45<br />
Arg His Ala Ile Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Cys Ile Trp Ser Gly Gly Ser Thr Tyr Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Arg Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Val Ile Gly Asp Thr Ala Gly Tyr Ala Tyr Phe Thr Gly Leu Asp<br />
Leu<br />
316<br />
13<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
- 343 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
316<br />
Gln Ser Ser Gln Ser Val Tyr Asn Asp Met Asp Leu Ala<br />
1 5 10<br />
317<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
317<br />
Ser Ala Ser Thr Leu Ala Ser<br />
1 5<br />
318<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
318<br />
Leu Gly Ala Phe Asp Asp Asp Ala Asp Asn Thr<br />
1 5 10<br />
3<strong>19</strong><br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
3<strong>19</strong><br />
Arg His Ala Ile Thr<br />
1 5<br />
320<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
<<br />
400> 320<br />
Cys Ile Trp Ser Gly Gly Ser Thr Tyr Tyr Ala Thr Trp Ala Lys Gly<br />
1 5 10 15<br />
- 344 -<br />
공개특허 10-2011-01<strong>12</strong>308
321<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
321<br />
Val Ile Gly Asp Thr Ala Gly Tyr Ala Tyr Phe Thr Gly Leu Asp Leu<br />
1 5 10 15<br />
322<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
322<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acgtttgcag ccgtgctgac ccagactgca tcacccgtgt ctgccgctgt gggagccaca <strong>12</strong>0<br />
gtcaccatca actgccagtc cagtcagagt gtttataatg acatggactt agcctggttt 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctatt ctgcatccac tctggcatct 240<br />
ggggtcccat cgcggttcag cggcagtgga tctgggacag agttcactct caccatcagc 300<br />
ggcgtgcagt gtgacgatgc tgccacttac tactgtctag gcgcttttga tgatgatgct 360<br />
gataatact 369<br />
323<br />
387<br />
DNA<br />
Oryctolagus cuniculus<br />
323<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gattctccct cactaggcat gcaataacct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg atgcatttgg agtggtggta gcacatacta cgcgacctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctcag aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctacttc tgtgccagag tcattggcga tactgctggt 360<br />
tatgcttatt ttacggggct tgacttg 387<br />
324<br />
- 345 -<br />
공개특허 10-2011-01<strong>12</strong>308
39<br />
DNA<br />
Oryctolagus cuniculus<br />
324<br />
cagtccagtc agagtgttta taatgacatg gacttagcc 39<br />
325<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
325<br />
tctgcatcca ctctggcatc t 21<br />
326<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
326<br />
ctaggcgctt ttgatgatga tgctgataat act 33<br />
327<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
327<br />
aggcatgcaa taacc 15<br />
328<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
328<br />
tgcatttgga gtggtggtag cacatactac gcgacctggg cgaaaggc 48<br />
329<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
329<br />
- 346 -<br />
공개특허 10-2011-01<strong>12</strong>308
gtcattggcg atactgctgg ttatgcttat tttacggggc ttgacttg 48<br />
330<br />
<strong>12</strong>1<br />
PRT<br />
Oryctolagus cuniculus<br />
330<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Val Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Trp Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Thr Ala Ser Ser Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Gly Val Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Thr Ser Asp Val Asp Asn Val<br />
331<br />
130<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
331<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ala Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser<br />
- 347 -<br />
공개특허 10-2011-01<strong>12</strong>308
35 40 45<br />
Ser Tyr Ala Met Gly Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Tyr Ile Gly Ile Ile Ser Ser Ser Gly Ser Thr Tyr Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Gln Ala Ser Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Ile Thr Ser Pro Thr Thr Glu Asp Ser Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Gly Gly Ala Gly Ser Gly Gly Val Trp Leu Leu Asp Gly Phe<br />
Asp Pro<br />
130<br />
332<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
332<br />
Gln Ala Ser Gln Ser Val Tyr Asn Trp Leu Ser<br />
1 5 10<br />
333<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
333<br />
Thr Ala Ser Ser Leu Ala Ser<br />
1 5<br />
334<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
334<br />
Gln Gln Gly Tyr Thr Ser Asp Val Asp Asn Val<br />
- 348 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10<br />
<<br />
210> 335<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
335<br />
Ser Tyr Ala Met Gly<br />
1 5<br />
336<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
336<br />
Ile Ile Ser Ser Ser Gly Ser Thr Tyr Tyr Ala Thr Trp Ala Lys Gly<br />
1 5 10 15<br />
337<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
337<br />
Gly Gly Ala Gly Ser Gly Gly Val Trp Leu Leu Asp Gly Phe Asp Pro<br />
1 5 10 15<br />
338<br />
363<br />
DNA<br />
Oryctolagus cuniculus<br />
338<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctctgtgg aggtagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtcagagt gtttataatt ggttatcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gctcctgatc tatactgcat ccagtctggc atctggggtc 240<br />
ccatcgcggt tcagtggcag tggatctggg acagagttca ctctcaccat cagcggcgtg 300<br />
- 349 -<br />
공개특허 10-2011-01<strong>12</strong>308
gagtgtgccg atgctgccac ttactactgt caacagggtt atactagtga tgttgataat 360<br />
gtt 363<br />
339<br />
390<br />
DNA<br />
Oryctolagus cuniculus<br />
339<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg aggccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gaatcgacct cagtagctat gcaatgggct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatacatcgg aatcattagt agtagtggta gcacatacta cgcgacctgg 240<br />
gcgaaaggcc gattcaccat ctcacaagcc tcgtcgacca cggtggatct gaaaattacc 300<br />
agtccgacaa ccgaggactc ggccacatat ttctgtgcca gagggggtgc tggtagtggt 360<br />
ggtgtttggc tgcttgatgg ttttgatccc 390<br />
340<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
340<br />
caggccagtc agagtgttta taattggtta tcc 33<br />
341<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
341<br />
actgcatcca gtctggcatc t 21<br />
342<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
342<br />
caacagggtt atactagtga tgttgataat gtt 33<br />
- 350 -<br />
공개특허 10-2011-01<strong>12</strong>308
343<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
343<br />
agctatgcaa tgggc 15<br />
344<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
344<br />
atcattagta gtagtggtag cacatactac gcgacctggg cgaaaggc 48<br />
345<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
345<br />
gggggtgctg gtagtggtgg tgtttggctg cttgatggtt ttgatccc 48<br />
346<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
346<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Lys Cys Ala Asp Val Val Met Thr Gln Thr Pro Ala<br />
20 25 30<br />
Ser Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala<br />
35 40 45<br />
Ser Glu Asn Ile Tyr Asn Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly<br />
50 55 60<br />
Gln Pro Pro Lys Leu Leu Ile Tyr Thr Val Gly Asp Leu Ala Ser Gly<br />
65 70 75 80<br />
- 351 -<br />
공개특허 10-2011-01<strong>12</strong>308
Val Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu<br />
85 90 95<br />
Thr Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln<br />
100 105 110<br />
Gln Gly Tyr Ser Ser Ser Tyr Val Asp Asn Val<br />
347<br />
130<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
347<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Glu Gln Leu Lys Glu Ser Gly Gly Arg Leu Val Thr<br />
20 25 30<br />
Pro Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu<br />
35 40 45<br />
Asn Asp Tyr Ala Val Gly Trp Phe Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Trp Ile Gly Tyr Ile Arg Ser Ser Gly Thr Thr Ala Tyr Ala Thr<br />
65 70 75 80<br />
Trp Ala Lys Gly Arg Phe Thr Ile Ser Ala Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Gly Gly Ala Gly Ser Ser Gly Val Trp Ile Leu Asp Gly Phe<br />
Ala Pro<br />
130<br />
348<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
- 352 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
348<br />
Gln Ala Ser Glu Asn Ile Tyr Asn Trp Leu Ala<br />
1 5 10<br />
349<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
349<br />
Thr Val Gly Asp Leu Ala Ser<br />
1 5<br />
350<br />
<strong>12</strong><br />
PRT<br />
<br />
Oryctolagus cuniculus<br />
350<br />
Gln Gln Gly Tyr Ser Ser Ser Tyr Val Asp Asn Val<br />
1 5 10<br />
351<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
351<br />
Asp Tyr Ala Val Gly<br />
1 5<br />
352<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
352<br />
Tyr Ile Arg Ser Ser Gly Thr Thr Ala Tyr Ala Thr Trp Ala Lys Gly<br />
1 5 10 15<br />
353<br />
16<br />
- 353 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
353<br />
Gly Gly Ala Gly Ser Ser Gly Val Trp Ile Leu Asp Gly Phe Ala Pro<br />
1 5 10 15<br />
354<br />
369<br />
DNA<br />
Oryctolagus cuniculus<br />
354<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
aaatgtgccg atgttgtgat gacccagact ccagcctccg tgtctgcagc tgtgggaggc <strong>12</strong>0<br />
acagtcacca tcaattgcca ggccagtgag aacatttata attggttagc ctggtatcag 180<br />
cagaaaccag ggcagcctcc caagctcctg atctatactg taggcgatct ggcatctggg 240<br />
gtctcatcgc ggttcaaagg cagtggatct gggacagagt tcactctcac catcagcgac 300<br />
ctggagtgtg ccgatgctgc cacttactat tgtcaacagg gttatagtag tagttatgtt 360<br />
gataatgtt 369<br />
355<br />
390<br />
DNA<br />
Oryctolagus cuniculus<br />
355<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
gagcagctga aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc <strong>12</strong>0<br />
tgcacagtct ctggattctc cctcaatgac tatgcagtgg gctggttccg ccaggctcca 180<br />
gggaaggggc tggaatggat cggatacatt cgtagtagtg gtaccacagc ctacgcgacc 240<br />
tgggcgaaag gccgattcac catctccgct acctcgacca cggtggatct gaaaatcacc 300<br />
agtccgacaa ccgaggacac ggccacctat ttctgtgcca gagggggtgc tggtagtagt 360<br />
ggtgtgtgga tccttgatgg ttttgctccc 390<br />
356<br />
33<br />
DNA<br />
- 354 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
356<br />
caggccagtg agaacattta taattggtta gcc 33<br />
357<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
357<br />
actgtaggcg atctggcatc t 21<br />
358<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
358<br />
caacagggtt atagtagtag ttatgttgat aatgtt 36<br />
359<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
359<br />
gactatgcag tgggc 15<br />
360<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
360<br />
tacattcgta gtagtggtac cacagcctac gcgacctggg cgaaaggc 48<br />
361<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
361<br />
gggggtgctg gtagtagtgg tgtgtggatc cttgatggtt ttgctccc 48<br />
- 355 -<br />
공개특허 10-2011-01<strong>12</strong>308
362<br />
<strong>12</strong>1<br />
PRT<br />
Oryctolagus cuniculus<br />
362<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Gln Val Leu Thr Gln Thr Pro Ser Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Gln Asn Asn Tyr Leu Ser Trp Phe Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ala Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Asp Leu Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Ala Tyr Arg Asp Val Asp Ser<br />
363<br />
130<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
363<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Asp Leu Val Lys Pro<br />
20 25 30<br />
Gly Ala Ser Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Phe Thr<br />
35 40 45<br />
- 356 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ser Thr Tyr Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Trp Ile Ala Cys Ile Asp Ala Gly Ser Ser Gly Ser Thr Tyr Tyr<br />
65 70 75 80<br />
Ala Thr Trp Val Asn Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr<br />
85 90 95<br />
Thr Val Thr Leu Gln Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr<br />
100 105 110<br />
Tyr Phe Cys Ala Lys Trp Asp Tyr Gly Gly Asn Val Gly Trp Gly Tyr<br />
Asp Leu<br />
130<br />
364<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
364<br />
Gln Ala Ser Gln Ser Val Tyr Gln Asn Asn Tyr Leu Ser<br />
1 5 10<br />
365<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
365<br />
Gly Ala Ala Thr Leu Ala Ser<br />
1 5<br />
366<br />
9<br />
PRT<br />
Oryctolagus cuniculus<br />
366<br />
Ala Gly Ala Tyr Arg Asp Val Asp Ser<br />
1 5<br />
- 357 -<br />
공개특허 10-2011-01<strong>12</strong>308
367<br />
6<br />
PRT<br />
Oryctolagus cuniculus<br />
367<br />
Ser Thr Tyr Tyr Ile Tyr<br />
1 5<br />
368<br />
18<br />
PRT<br />
Oryctolagus cuniculus<br />
368<br />
Cys Ile Asp Ala Gly Ser Ser Gly Ser Thr Tyr Tyr Ala Thr Trp Val<br />
1 5 10 15<br />
Asn Gly<br />
369<br />
13<br />
PRT<br />
Oryctolagus cuniculus<br />
369<br />
Trp Asp Tyr Gly Gly Asn Val Gly Trp Gly Tyr Asp Leu<br />
1 5 10<br />
370<br />
363<br />
DNA<br />
Oryctolagus cuniculus<br />
370<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgctc aagtgctgac ccagactcca tcctccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccaggc cagtcagagt gtttatcaga acaactactt atcctggttt 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctatg gtgcggccac tctggcatct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccatcagc 300<br />
- 358 -<br />
공개특허 10-2011-01<strong>12</strong>308
gacctggagt gtgacgatgc tgccacttac tactgtgcag gcgcttatag ggatgtggat 360<br />
tct 363<br />
371<br />
390<br />
DNA<br />
Oryctolagus cuniculus<br />
371<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgttggagg agtccggggg agacctggtc aagcctgggg catccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctcctt tactagtacc tactacatct actgggtccg ccaggctcca 180<br />
gggaaggggc tggagtggat cgcatgtatt gatgctggta gtagtggtag cacttactac 240<br />
gcgacctggg tgaatggccg attcaccatc tccaaaacct cgtcgaccac ggtgactctg 300<br />
caaatgacca gtctgacagc cgcggacacg gccacctatt tctgtgcgaa atgggattat 360<br />
ggtggtaatg ttggttgggg ttatgacttg 390<br />
372<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
372<br />
caggccagtc agagtgttta tcagaacaac tacttatcc 39<br />
373<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
373<br />
ggtgcggcca ctctggcatc t 21<br />
374<br />
27<br />
DNA<br />
Oryctolagus cuniculus<br />
374<br />
gcaggcgctt atagggatgt ggattct 27<br />
375<br />
- 359 -<br />
공개특허 10-2011-01<strong>12</strong>308
18<br />
DNA<br />
Oryctolagus cuniculus<br />
375<br />
agtacctact acatctac 18<br />
376<br />
54<br />
DNA<br />
Oryctolagus cuniculus<br />
376<br />
tgtattgatg ctggtagtag tggtagcact tactacgcga cctgggtgaa tggc 54<br />
377<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
377<br />
tgggattatg gtggtaatgt tggttggggt tatgacttg 39<br />
378<br />
<strong>12</strong>0<br />
PRT<br />
Oryctolagus cuniculus<br />
378<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Phe Glu Leu Thr Gln Thr Pro Ser Ser<br />
20 25 30<br />
Val Glu Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Ile Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Phe Leu Ile Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
- 360 -<br />
공개특허 10-2011-01<strong>12</strong>308
Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Ser<br />
100 105 110<br />
Tyr Tyr Asp Ser Val Ser Asn Pro<br />
379<br />
<strong>12</strong>7<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
379<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Asp Leu Val Lys Pro<br />
20 25 30<br />
Glu Gly Ser Leu Thr Leu Thr Cys Lys Ala Ser Gly Leu Asp Leu Gly<br />
35 40 45<br />
Thr Tyr Trp Phe Met Cys Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Trp Ile Ala Cys Ile Tyr Thr Gly Ser Ser Gly Ser Thr Phe Tyr<br />
65 70 75 80<br />
Ala Ser Trp Val Asn Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr<br />
85 90 95<br />
Thr Val Thr Leu Gln Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr<br />
100 105 110<br />
Tyr Phe Cys Ala Arg Gly Tyr Ser Gly Tyr Gly Tyr Phe Lys Leu<br />
380<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
380<br />
- 361 -<br />
공개특허 10-2011-01<strong>12</strong>308
Gln Ala Ser Gln Ser Ile Ser Ser Tyr Leu Ala<br />
1 5 10<br />
381<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
381<br />
Arg Ala Ser Thr Leu Ala Ser<br />
1 5<br />
382<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
382<br />
Gln Ser Tyr Tyr Asp Ser Val Ser Asn Pro<br />
1 5 10<br />
383<br />
6<br />
PRT<br />
Oryctolagus cuniculus<br />
383<br />
Thr Tyr Trp Phe Met Cys<br />
1 5<br />
384<br />
18<br />
PRT<br />
Oryctolagus cuniculus<br />
384<br />
Cys Ile Tyr Thr Gly Ser Ser Gly Ser Thr Phe Tyr Ala Ser Trp Val<br />
1 5 10 15<br />
Asn Gly<br />
385<br />
- 362 -<br />
공개특허 10-2011-01<strong>12</strong>308
10<br />
PRT<br />
Oryctolagus cuniculus<br />
385<br />
Gly Tyr Ser Gly Tyr Gly Tyr Phe Lys Leu<br />
1 5 10<br />
386<br />
360<br />
DNA<br />
Oryctolagus cuniculus<br />
386<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcat tcgaattgac ccagactcca tcctccgtgg aggcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtcagagc attagtagtt acttagcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gttcctgatc tacagggcgt ccactctggc atctggggtc 240<br />
ccatcgcgat tcaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caaagctatt atgatagtgt ttcaaatcct 360<br />
387<br />
381<br />
DNA<br />
Oryctolagus cuniculus<br />
387<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgttggagg agtccggggg agacctggtc aagcctgagg gatccctgac actcacctgc <strong>12</strong>0<br />
aaagcctctg gactcgacct cggtacctac tggttcatgt gctgggtccg ccaggctcca 180<br />
gggaaggggc tggagtggat cgcttgtatt tatactggta gtagtggttc cactttctac 240<br />
gcgagctggg tgaatggccg attcaccatc tccaaaacct cgtcgaccac ggtgactctg 300<br />
caaatgacca gtctgacagc cgcggacacg gccacttatt tttgtgcgag aggttatagt 360<br />
ggttatggtt attttaagtt g 381<br />
388<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
- 363 -<br />
공개특허 10-2011-01<strong>12</strong>308
388<br />
caggccagtc agagcattag tagttactta gcc 33<br />
389<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
389<br />
agggcgtcca ctctggcatc t 21<br />
390<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
390<br />
caaagctatt atgatagtgt ttcaaatcct 30<br />
391<br />
18<br />
DNA<br />
Oryctolagus cuniculus<br />
391<br />
acctactggt tcatgtgc 18<br />
392<br />
54<br />
DNA<br />
Oryctolagus cuniculus<br />
392<br />
tgtatttata ctggtagtag tggttccact ttctacgcga gctgggtgaa tggc 54<br />
393<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
393<br />
ggttatagtg gttatggtta ttttaagttg 30<br />
394<br />
- 364 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong>4<br />
PRT<br />
Oryctolagus cuniculus<br />
394<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Val Thr Phe Ala Ile Glu Met Thr Gln Ser Pro Phe Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Lys Asn Asn Gln Leu Ser Trp Tyr Gln Gln Lys Ser<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Ala Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Ala Ile Thr Gly Ser Ile Asp Thr Asp Gly<br />
395<br />
130<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
395<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Asp Leu Val Lys Pro<br />
20 25 30<br />
Gly Ala Ser Leu Thr Leu Thr Cys Thr Thr Ser Gly Phe Ser Phe Ser<br />
35 40 45<br />
Ser Ser Tyr Phe Ile Cys Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
- 365 -<br />
공개특허 10-2011-01<strong>12</strong>308
50 55 60<br />
Glu Trp Ile Ala Cys Ile Tyr Gly Gly Asp Gly Ser Thr Tyr Tyr Ala<br />
65 70 75 80<br />
Ser Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Ser Thr Thr<br />
85 90 95<br />
Val Thr Leu Gln Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr<br />
100 105 110<br />
Phe Cys Ala Arg Glu Trp Ala Tyr Ser Gln Gly Tyr Phe Gly Ala Phe<br />
Asp Leu<br />
130<br />
396<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
396<br />
Gln Ala Ser Gln Ser Val Tyr Lys Asn Asn Gln Leu Ser<br />
1 5 10<br />
397<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
397<br />
Gly Ala Ser Ala Leu Ala Ser<br />
1 5<br />
398<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
398<br />
Ala Gly Ala Ile Thr Gly Ser Ile Asp Thr Asp Gly<br />
1 5 10<br />
399<br />
- 366 -<br />
공개특허 10-2011-01<strong>12</strong>308
6<br />
PRT<br />
Oryctolagus cuniculus<br />
399<br />
Ser Ser Tyr Phe Ile Cys<br />
1 5<br />
400<br />
17<br />
PRT<br />
Oryctolagus cuniculus<br />
400<br />
Cys Ile Tyr Gly Gly Asp Gly Ser Thr Tyr Tyr Ala Ser Trp Ala Lys<br />
1 5 10 15<br />
Gly<br />
401<br />
14<br />
PRT<br />
Oryctolagus cuniculus<br />
401<br />
Glu Trp Ala Tyr Ser Gln Gly Tyr Phe Gly Ala Phe Asp Leu<br />
1 5 10<br />
402<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
402<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgtc 60<br />
acatttgcca tcgaaatgac ccagagtcca ttctccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccaggc cagtcagagt gtttataaga acaaccaatt atcctggtat 180<br />
cagcagaaat cagggcagcc tcccaagctc ctgatctatg gtgcatcggc tctggcatct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacag agttcactct caccatcagc 300<br />
gacgtgcagt gtgacgatgc tgccacttac tactgtgcag gcgctattac tggtagtatt 360<br />
- 367 -<br />
공개특허 10-2011-01<strong>12</strong>308
gatacggatg gt 372<br />
403<br />
390<br />
DNA<br />
Oryctolagus cuniculus<br />
403<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgttggagg agtccggggg agacctggtc aagcctgggg catccctgac actcacctgc <strong>12</strong>0<br />
acaacttctg gattctcctt cagtagcagc tacttcattt gctgggtccg ccaggctcca 180<br />
gggaaggggc tggagtggat cgcatgcatt tatggtggtg atggcagcac atactacgcg 240<br />
agctgggcga aaggccgatt caccatctcc aaaacctcgt cgaccacggt gacgctgcaa 300<br />
atgaccagtc tgacagccgc ggacacggcc acctatttct gtgcgagaga atgggcatat 360<br />
agtcaaggtt attttggtgc ttttgatctc 390<br />
404<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
404<br />
caggccagtc agagtgttta taagaacaac caattatcc 39<br />
405<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
405<br />
ggtgcatcgg ctctggcatc t 21<br />
406<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
406<br />
gcaggcgcta ttactggtag tattgatacg gatggt 36<br />
407<br />
18<br />
- 368 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
407<br />
agcagctact tcatttgc 18<br />
408<br />
51<br />
DNA<br />
Oryctolagus cuniculus<br />
408<br />
tgcatttatg gtggtgatgg cagcacatac tacgcgagct gggcgaaagg c 51<br />
409<br />
42<br />
DNA<br />
Oryctolagus cuniculus<br />
409<br />
gaatgggcat atagtcaagg ttattttggt gcttttgatc tc 42<br />
410<br />
<strong>12</strong>4<br />
PRT<br />
Oryctolagus cuniculus<br />
410<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Asp Val Val Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Glu Asp Ile Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Val<br />
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr<br />
- 369 -<br />
공개특허 10-2011-01<strong>12</strong>308
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Cys<br />
100 105 110<br />
Thr Tyr Gly Thr Ile Ser Ile Ser Asp Gly Asn Ala<br />
411<br />
<strong>12</strong>4<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
411<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Tyr Phe Met Thr Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu<br />
50 55 60<br />
Tyr Ile Gly Phe Ile Asn Pro Gly Gly Ser Ala Tyr Tyr Ala Ser Trp<br />
65 70 75 80<br />
Val Lys Gly Arg Phe Thr Ile Ser Lys Ser Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Val Leu Ile Val Ser Tyr Gly Ala Phe Thr Ile<br />
4<strong>12</strong><br />
11<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
4<strong>12</strong><br />
Gln Ala Ser Glu Asp Ile Ser Ser Tyr Leu Ala<br />
- 370 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10<br />
413<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
413<br />
Ala Ala Ser Asn Leu Glu Ser<br />
1 5<br />
414<br />
14<br />
PRT<br />
Oryctolagus cuniculus<br />
414<br />
Gln Cys Thr Tyr Gly Thr Ile Ser Ile Ser Asp Gly Asn Ala<br />
1 5 10<br />
415<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
415<br />
Ser Tyr Phe Met Thr<br />
1 5<br />
416<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
416<br />
Phe Ile Asn Pro Gly Gly Ser Ala Tyr Tyr Ala Ser Trp Val Lys Gly<br />
1 5 10 15<br />
417<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
417<br />
- 371 -<br />
공개특허 10-2011-01<strong>12</strong>308
Val Leu Ile Val Ser Tyr Gly Ala Phe Thr Ile<br />
1 5 10<br />
418<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
418<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgatg ttgtgatgac ccagactcca gcctccgtgg aggcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtgaggat attagtagct acttagcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gctcctgatc tatgctgcat ccaatctgga atctggggtc 240<br />
tcatcgcgat tcaaaggcag tggatctggg acagagtaca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ctattactgt caatgtactt atggtactat ttctattagt 360<br />
gatggtaatg ct 372<br />
4<strong>19</strong><br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
4<strong>19</strong><br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccaatgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gattctccct cagtagctac ttcatgacct gggtccgcca ggctccaggg 180<br />
gaggggctgg aatacatcgg attcattaat cctggtggta gcgcttacta cgcgagctgg 240<br />
gtgaaaggcc gattcaccat ctccaagtcc tcgaccacgg tagatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccaggg ttctgattgt ttcttatgga 360<br />
gcctttacca tc 372<br />
420<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
420<br />
caggccagtg aggatattag tagctactta gcc 33<br />
- 372 -<br />
공개특허 10-2011-01<strong>12</strong>308
421<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
421<br />
gctgcatcca atctggaatc t 21<br />
422<br />
42<br />
DNA<br />
Oryctolagus cuniculus<br />
422<br />
caatgtactt atggtactat ttctattagt gatggtaatg ct 42<br />
423<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
423<br />
agctacttca tgacc 15<br />
424<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
424<br />
ttcattaatc ctggtggtag cgcttactac gcgagctggg tgaaaggc 48<br />
425<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
425<br />
gttctgattg tttcttatgg agcctttacc atc 33<br />
426<br />
<strong>12</strong>4<br />
PRT<br />
- 373 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
426<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Asp Val Val Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Glu Asp Ile Glu Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Asn Leu Glu Ser Gly Val<br />
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Cys<br />
100 105 110<br />
Thr Tyr Gly Ile Ile Ser Ile Ser Asp Gly Asn Ala<br />
427<br />
<strong>12</strong>4<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
427<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Tyr Phe Met Thr Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu<br />
50 55 60<br />
Tyr Ile Gly Phe Met Asn Thr Gly Asp Asn Ala Tyr Tyr Ala Ser Trp<br />
- 374 -<br />
공개특허 10-2011-01<strong>12</strong>308
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Val Leu Val Val Ala Tyr Gly Ala Phe Asn Ile<br />
428<br />
11<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
428<br />
Gln Ala Ser Glu Asp Ile Glu Ser Tyr Leu Ala<br />
1 5 10<br />
429<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
429<br />
Gly Ala Ser Asn Leu Glu Ser<br />
1 5<br />
430<br />
14<br />
PRT<br />
Oryctolagus cuniculus<br />
430<br />
Gln Cys Thr Tyr Gly Ile Ile Ser Ile Ser Asp Gly Asn Ala<br />
1 5 10<br />
431<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
431<br />
- 375 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ser Tyr Phe Met Thr<br />
1 5<br />
432<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
432<br />
Phe Met Asn Thr Gly Asp Asn Ala Tyr Tyr Ala Ser Trp Ala Lys Gly<br />
1 5 10 15<br />
433<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
433<br />
Val Leu Val Val Ala Tyr Gly Ala Phe Asn Ile<br />
1 5 10<br />
434<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
434<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgatg ttgtgatgac ccagactcca gcctccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtgaggac attgaaagct atctagcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gctcctgatc tatggtgcat ccaatctgga atctggggtc 240<br />
tcatcgcggt tcaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactattgt caatgcactt atggtattat tagtattagt 360<br />
gatggtaatg ct 372<br />
435<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
435<br />
- 376 -<br />
공개특허 10-2011-01<strong>12</strong>308
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtgtctg gattctccct cagtagctac ttcatgacct gggtccgcca ggctccaggg 180<br />
gaggggctgg aatacatcgg attcatgaat actggtgata acgcatacta cgcgagctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccaggg ttcttgttgt tgcttatgga 360<br />
gcctttaaca tc 372<br />
436<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
436<br />
caggccagtg aggacattga aagctatcta gcc 33<br />
437<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
437<br />
ggtgcatcca atctggaatc t 21<br />
438<br />
42<br />
DNA<br />
Oryctolagus cuniculus<br />
438<br />
caatgcactt atggtattat tagtattagt gatggtaatg ct 42<br />
439<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
439<br />
agctacttca tgacc 15<br />
440<br />
48<br />
- 377 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
440<br />
ttcatgaata ctggtgataa cgcatactac gcgagctggg cgaaaggc 48<br />
441<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
441<br />
gttcttgttg ttgcttatgg agcctttaac atc 33<br />
442<br />
<strong>12</strong>4<br />
PRT<br />
Oryctolagus cuniculus<br />
442<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Glu Pro Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ser Ser<br />
35 40 45<br />
Lys Ser Val Met Asn Asn Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Asn Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Gln Gly Gly Tyr Thr Gly Tyr Ser Asp His Gly Thr<br />
443<br />
115 <strong>12</strong>0<br />
- 378 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong>7<br />
PRT<br />
Oryctolagus cuniculus<br />
443<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Lys Pro<br />
20 25 30<br />
Asp Glu Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser<br />
35 40 45<br />
Ser Tyr Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Phe Ile Asn Thr Gly Gly Thr Ile Val Tyr Ala Ser Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Gly Ser Tyr Val Ser Ser Gly Tyr Ala Tyr Tyr Phe Asn Val<br />
444<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
444<br />
Gln Ser Ser Lys Ser Val Met Asn Asn Asn Tyr Leu Ala<br />
1 5 10<br />
445<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
445<br />
Gly Ala Ser Asn Leu Ala Ser<br />
- 379 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5<br />
446<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
446<br />
Gln Gly Gly Tyr Thr Gly Tyr Ser Asp His Gly Thr<br />
1 5 10<br />
447<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
447<br />
Ser Tyr Pro Met Asn<br />
1 5<br />
448<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
448<br />
Phe Ile Asn Thr Gly Gly Thr Ile Val Tyr Ala Ser Trp Ala Lys Gly<br />
1 5 10 15<br />
449<br />
14<br />
PRT<br />
Oryctolagus cuniculus<br />
449<br />
Gly Ser Tyr Val Ser Ser Gly Tyr Ala Tyr Tyr Phe Asn Val<br />
1 5 10<br />
450<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
- 380 -<br />
공개특허 10-2011-01<strong>12</strong>308
450<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccg ccgtgctgac ccagactcca tctcccgtgt ctgaacctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccagtc cagtaagagt gttatgaata acaactactt agcctggtat 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctatg gtgcatccaa tctggcatct 240<br />
ggggtcccat cacggttcag cggcagtgga tctgggacac agttcactct caccatcagc 300<br />
gacgtgcagt gtgacgatgc tgccacttac tactgtcaag gcggttatac tggttatagt 360<br />
gatcatggga ct 372<br />
451<br />
381<br />
DNA<br />
Oryctolagus cuniculus<br />
451<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc aagcctgacg aaaccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gaatcgacct cagtagctat ccaatgaact gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg attcattaat actggtggta ccatagtcta cgcgagctgg 240<br />
gcaaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag gcagttatgt ttcatctggt 360<br />
tatgcctact attttaatgt c 381<br />
452<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
452<br />
cagtccagta agagtgttat gaataacaac tacttagcc 39<br />
453<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
453<br />
ggtgcatcca atctggcatc t 21<br />
- 381 -<br />
공개특허 10-2011-01<strong>12</strong>308
454<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
454<br />
caaggcggtt atactggtta tagtgatcat gggact 36<br />
455<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
455<br />
agctatccaa tgaac 15<br />
456<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
456<br />
ttcattaata ctggtggtac catagtctac gcgagctggg caaaaggc 48<br />
457<br />
42<br />
DNA<br />
Oryctolagus cuniculus<br />
457<br />
ggcagttatg tttcatctgg ttatgcctac tattttaatg tc 42<br />
458<br />
<strong>12</strong>1<br />
PRT<br />
Oryctolagus cuniculus<br />
458<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
- 382 -<br />
공개특허 10-2011-01<strong>12</strong>308
Val Ser Ala Ala Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asn Asn Trp Leu Ser Trp Phe Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Lys Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Asp Val Gln Cys Asp Asp Val Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Gly Tyr Leu Asp Ser Val Ile<br />
459<br />
<strong>12</strong>6<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
459<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Thr Tyr Ser Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Ala Asn Ser Gly Thr Thr Phe Tyr Ala Asn Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Val Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Glu Ser Gly Met Tyr Asn Glu Tyr Gly Lys Phe Asn Ile<br />
- 383 -<br />
공개특허 10-2011-01<strong>12</strong>308
460<br />
13<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
460<br />
Gln Ser Ser Gln Ser Val Tyr Asn Asn Asn Trp Leu Ser<br />
1 5 10<br />
<br />
461<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
461<br />
Lys Ala Ser Thr Leu Ala Ser<br />
1 5<br />
462<br />
9<br />
PRT<br />
Oryctolagus cuniculus<br />
462<br />
Ala Gly Gly Tyr Leu Asp Ser Val Ile<br />
1 5<br />
463<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
463<br />
Thr Tyr Ser Ile Asn<br />
1 5<br />
464<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
464<br />
- 384 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ile Ile Ala Asn Ser Gly Thr Thr Phe Tyr Ala Asn Trp Ala Lys Gly<br />
1 5 10 15<br />
465<br />
13<br />
PRT<br />
Oryctolagus cuniculus<br />
465<br />
Glu Ser Gly Met Tyr Asn Glu Tyr Gly Lys Phe Asn Ile<br />
1 5 10<br />
466<br />
363<br />
DNA<br />
Oryctolagus cuniculus<br />
466<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccg ccgtgctgac ccagactcca tctcccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccagtc cagtcagagt gtttataata acaactggtt atcctggttt 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctaca aggcatccac tctggcatct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccatcagc 300<br />
gacgtgcagt gtgacgatgt tgccacttac tactgtgcgg gcggttatct tgatagtgtt 360<br />
att 363<br />
467<br />
378<br />
DNA<br />
Oryctolagus cuniculus<br />
467<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gattctccct cagtacctat tcaataaact gggtccgcca ggctccaggg 180<br />
aagggcctgg aatggatcgg aatcattgct aatagtggta ccacattcta cgcgaactgg 240<br />
gcgaaaggcc gattcaccgt ctccaaaacc tcgaccacgg tggatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag agagtggaat gtacaatgaa 360<br />
- 385 -<br />
공개특허 10-2011-01<strong>12</strong>308
tatggtaaat ttaacatc 378<br />
468<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
468<br />
cagtccagtc agagtgttta taataacaac tggttatcc 39<br />
469<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
469<br />
aaggcatcca ctctggcatc t 21<br />
470<br />
27<br />
DNA<br />
Oryctolagus cuniculus<br />
470<br />
gcgggcggtt atcttgatag tgttatt 27<br />
471<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
471<br />
acctattcaa taaac 15<br />
472<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
472<br />
atcattgcta atagtggtac cacattctac gcgaactggg cgaaaggc 48<br />
473<br />
39<br />
- 386 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
473<br />
gagagtggaa tgtacaatga atatggtaaa tttaacatc 39<br />
474<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
474<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Ser Asp Met Thr Gln Thr Pro Ser Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Glu Asn Ile Tyr Ser Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Phe Lys Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Ala Thr Val Tyr Asp Ile Asp Asn Asn<br />
475<br />
<strong>12</strong>8<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
475<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
- 387 -<br />
공개특허 10-2011-01<strong>12</strong>308
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser<br />
35 40 45<br />
Ala Tyr Ala Met Ile Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu<br />
50 55 60<br />
Trp Ile Thr Ile Ile Tyr Pro Asn Gly Ile Thr Tyr Tyr Ala Asn Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Val Ser Lys Thr Ser Thr Ala Met Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Asp Ala Glu Ser Ser Lys Asn Ala Tyr Trp Gly Tyr Phe Asn Val<br />
476<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
476<br />
Gln Ala Ser Glu Asn Ile Tyr Ser Phe Leu Ala<br />
1 5 10<br />
<br />
477<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
477<br />
Lys Ala Ser Thr Leu Ala Ser<br />
1 5<br />
478<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
- 388 -<br />
공개특허 10-2011-01<strong>12</strong>308
478<br />
Gln Gln Gly Ala Thr Val Tyr Asp Ile Asp Asn Asn<br />
1 5 10<br />
479<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
479<br />
Ala Tyr Ala Met Ile<br />
1 5<br />
480<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
480<br />
Ile Ile Tyr Pro Asn Gly Ile Thr Tyr Tyr Ala Asn Trp Ala Lys Gly<br />
1 5 10 15<br />
481<br />
15<br />
PRT<br />
Oryctolagus cuniculus<br />
481<br />
Asp Ala Glu Ser Ser Lys Asn Ala Tyr Trp Gly Tyr Phe Asn Val<br />
1 5 10 15<br />
482<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
482<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct ctgatatgac ccagactcca tcctccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccaggc cagtgagaac atttatagct ttttggcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gctcctgatc ttcaaggctt ccactctggc atctggggtc 240<br />
- 389 -<br />
공개특허 10-2011-01<strong>12</strong>308
tcatcgcggt tcaaaggcag tggatctggg acacagttca ctctcaccat cagcgacctg 300<br />
gagtgtgacg atgctgccac ttactactgt caacagggtg ctactgtgta tgatattgat 360<br />
aataat 366<br />
483<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
483<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtttctg gaatcgacct cagtgcctat gcaatgatct gggtccgcca ggctccaggg 180<br />
gaggggctgg aatggatcac aatcatttat cctaatggta tcacatacta cgcgaactgg 240<br />
gcgaaaggcc gattcaccgt ctccaaaacc tcgaccgcga tggatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag atgcagaaag tagtaagaat 360<br />
gcttattggg gctactttaa cgtc 384<br />
484<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
484<br />
caggccagtg agaacattta tagctttttg gcc 33<br />
485<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
485<br />
aaggcttcca ctctggcatc t 21<br />
486<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
486<br />
caacagggtg ctactgtgta tgatattgat aataat 36<br />
- 390 -<br />
공개특허 10-2011-01<strong>12</strong>308
487<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
487<br />
gcctatgcaa tgatc 15<br />
488<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
488<br />
atcatttatc ctaatggtat cacatactac gcgaactggg cgaaaggc 48<br />
489<br />
45<br />
DNA<br />
Oryctolagus cuniculus<br />
489<br />
gatgcagaaa gtagtaagaa tgcttattgg ggctacttta acgtc 45<br />
490<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
490<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Ser Asp Met Thr Gln Thr Pro Ser Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Glu Asn Ile Tyr Ser Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Phe Arg Ala Ser Thr Leu Ala Ser Gly Val<br />
- 391 -<br />
공개특허 10-2011-01<strong>12</strong>308
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Ala Thr Val Tyr Asp Ile Asp Asn Asn<br />
491<br />
<strong>12</strong>8<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
491<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser<br />
35 40 45<br />
Ala Tyr Ala Met Ile Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu<br />
50 55 60<br />
Trp Ile Thr Ile Ile Tyr Pro Asn Gly Ile Thr Tyr Tyr Ala Asn Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Val Ser Lys Thr Ser Thr Ala Met Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Asp Ala Glu Ser Ser Lys Asn Ala Tyr Trp Gly Tyr Phe Asn Val<br />
492<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
- 392 -<br />
공개특허 10-2011-01<strong>12</strong>308
492<br />
Gln Ala Ser Glu Asn Ile Tyr Ser Phe Leu Ala<br />
1 5 10<br />
493<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
493<br />
Arg Ala Ser Thr Leu Ala Ser<br />
1 5<br />
494<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
494<br />
Gln Gln Gly Ala Thr Val Tyr Asp Ile Asp Asn Asn<br />
1 5 10<br />
495<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
495<br />
Ala Tyr Ala Met Ile<br />
1 5<br />
496<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
496<br />
Ile Ile Tyr Pro Asn Gly Ile Thr Tyr Tyr Ala Asn Trp Ala Lys Gly<br />
1 5 10 15<br />
497<br />
15<br />
PRT<br />
- 393 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
497<br />
Asp Ala Glu Ser Ser Lys Asn Ala Tyr Trp Gly Tyr Phe Asn Val<br />
1 5 10 15<br />
498<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
498<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct ctgatatgac ccagactcca tcctccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccaggc cagtgagaac atttatagct ttttggcctg gtatcagcag 180<br />
aaaccagggc agcctcccaa gctcctgatc ttcagggctt ccactctggc atctggggtc 240<br />
tcatcgcggt tcaaaggcag tggatctggg acacagttca ctctcaccat cagcgacctg 300<br />
gagtgtgacg atgctgccac ttactactgt caacagggtg ctactgtgta tgatattgat 360<br />
aataat 366<br />
499<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
499<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtttctg gaatcgacct cagtgcctat gcaatgatct gggtccgcca ggctccaggg 180<br />
gaggggctgg aatggatcac aatcatttat cctaatggta tcacatacta cgcgaactgg 240<br />
gcgaaaggcc gattcaccgt ctccaaaacc tcgaccgcga tggatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag atgcagaaag tagtaagaat 360<br />
gcttattggg gctactttaa cgtc 384<br />
500<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
- 394 -<br />
공개특허 10-2011-01<strong>12</strong>308
500<br />
caggccagtg agaacattta tagctttttg gcc 33<br />
501<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
501<br />
agggcttcca ctctggcatc t 21<br />
502<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
502<br />
caacagggtg ctactgtgta tgatattgat aataat 36<br />
503<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
503<br />
gcctatgcaa tgatc 15<br />
504<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
504<br />
atcatttatc ctaatggtat cacatactac gcgaactggg cgaaaggc 48<br />
505<br />
45<br />
DNA<br />
Oryctolagus cuniculus<br />
505<br />
gatgcagaaa gtagtaagaa tgcttattgg ggctacttta acgtc 45<br />
506<br />
- 395 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong>4<br />
PRT<br />
Oryctolagus cuniculus<br />
506<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ile Glu Met Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Glu Ser Val Phe Asn Asn Met Leu Ser Trp Tyr Gln Gln Lys Pro Gly<br />
50 55 60<br />
His Ser Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asp Leu Ala Ser Gly<br />
65 70 75 80<br />
Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu<br />
85 90 95<br />
Thr Ile Ser Gly Val Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Ala<br />
100 105 110<br />
Gly Tyr Lys Ser Asp Ser Asn Asp Gly Asp Asn Val<br />
507<br />
<strong>12</strong>3<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
507<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Asn<br />
35 40 45<br />
Arg Asn Ser Ile Thr Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu<br />
- 396 -<br />
공개특허 10-2011-01<strong>12</strong>308
50 55 60<br />
Trp Ile Gly Ile Ile Thr Gly Ser Gly Arg Thr Tyr Tyr Ala Asn Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Gly His Pro Gly Leu Gly Ser Gly Asn Ile<br />
508<br />
<strong>12</strong><br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
508<br />
Gln Ala Ser Glu Ser Val Phe Asn Asn Met Leu Ser<br />
1 5 10<br />
509<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
509<br />
Asp Ala Ser Asp Leu Ala Ser<br />
1 5<br />
510<br />
13<br />
PRT<br />
Oryctolagus cuniculus<br />
510<br />
Ala Gly Tyr Lys Ser Asp Ser Asn Asp Gly Asp Asn Val<br />
1 5 10<br />
511<br />
5<br />
PRT<br />
- 397 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
511<br />
Arg Asn Ser Ile Thr<br />
1 5<br />
5<strong>12</strong><br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
5<strong>12</strong><br />
Ile Ile Thr Gly Ser Gly Arg Thr Tyr Tyr Ala Asn Trp Ala Lys Gly<br />
1 5 10 15<br />
513<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
513<br />
Gly His Pro Gly Leu Gly Ser Gly Asn Ile<br />
1 5 10<br />
514<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
514<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcca ttgaaatgac ccagactcca tcccccgtgt ctgccgctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccaggc cagtgagagt gtttttaata atatgttatc ctggtatcag 180<br />
cagaaaccag ggcactctcc taagctcctg atctatgatg catccgatct ggcatctggg 240<br />
gtcccatcgc ggttcaaagg cagtggatct gggacacagt tcactctcac catcagtggc 300<br />
gtggagtgtg acgatgctgc cacttactat tgtgcagggt ataaaagtga tagtaatgat 360<br />
ggcgataatg tt 372<br />
515<br />
369<br />
DNA<br />
- 398 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
515<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gattctccct caacaggaat tcaataacct gggtccgcca ggctccaggg 180<br />
gaggggctgg aatggatcgg aatcattact ggtagtggta gaacgtacta cgcgaactgg 240<br />
gcaaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag gccatcctgg tcttggtagt 360<br />
ggtaacatc 369<br />
516<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
516<br />
caggccagtg agagtgtttt taataatatg ttatcc 36<br />
517<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
517<br />
gatgcatccg atctggcatc t 21<br />
518<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
518<br />
gcagggtata aaagtgatag taatgatggc gataatgtt 39<br />
5<strong>19</strong><br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
5<strong>19</strong><br />
aggaattcaa taacc 15<br />
- 399 -<br />
공개특허 10-2011-01<strong>12</strong>308
520<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
520<br />
atcattactg gtagtggtag aacgtactac gcgaactggg caaaaggc 48<br />
521<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
521<br />
ggccatcctg gtcttggtag tggtaacatc 30<br />
522<br />
<strong>12</strong>1<br />
PRT<br />
Oryctolagus cuniculus<br />
522<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Gln Val Leu Thr Gln Thr Ala Ser Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asn Tyr Leu Ser Trp Tyr Gln Gln Lys Pro Gly<br />
50 55 60<br />
Gln Pro Pro Lys Leu Leu Ile Tyr Thr Ala Ser Ser Leu Ala Ser Gly<br />
65 70 75 80<br />
Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu<br />
85 90 95<br />
Thr Ile Ser Glu Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln<br />
100 105 110<br />
Gly Tyr Tyr Ser Gly Pro Ile Ile Thr<br />
- 400 -<br />
공개특허 10-2011-01<strong>12</strong>308
523<br />
<strong>12</strong>2<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
523<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Asn<br />
35 40 45<br />
Asn Tyr Tyr Ile Gln Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Tyr Ala Gly Gly Ser Ala Tyr Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Asn Gly Arg Phe Thr Ile Ala Lys Thr Ser Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Met Thr Ser Leu Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Gly Thr Phe Asp Gly Tyr Glu Leu<br />
524<br />
<strong>12</strong><br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
524<br />
Gln Ser Ser Gln Ser Val Tyr Asn Asn Tyr Leu Ser<br />
1 5 10<br />
525<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
- 401 -<br />
공개특허 10-2011-01<strong>12</strong>308
525<br />
Thr Ala Ser Ser Leu Ala Ser<br />
1 5<br />
526<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
526<br />
Gln Gly Tyr Tyr Ser Gly Pro Ile Ile Thr<br />
1 5 10<br />
527<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
527<br />
Asn Tyr Tyr Ile Gln<br />
1 5<br />
528<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
528<br />
Ile Ile Tyr Ala Gly Gly Ser Ala Tyr Tyr Ala Thr Trp Ala Asn Gly<br />
1 5 10 15<br />
529<br />
8<br />
PRT<br />
Oryctolagus cuniculus<br />
529<br />
Gly Thr Phe Asp Gly Tyr Glu Leu<br />
1 5<br />
530<br />
363<br />
- 402 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
530<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcgc aagtgctgac ccagactgca tcgtccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccagtc cagtcagagt gtttataata actacttatc ctggtatcag 180<br />
cagaaaccag ggcagcctcc caagctcctg atctatactg catccagcct ggcatctggg 240<br />
gtcccatcgc ggttcaaagg cagtggatct gggacacagt tcactctcac catcagcgaa 300<br />
gtgcagtgtg acgatgctgc cacttactac tgtcaaggct attatagtgg tcctataatt 360<br />
act 363<br />
531<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
531<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct caataactac tacatacaat gggtccgcca ggctccaggg 180<br />
gaggggctgg aatggatcgg gatcatttat gctggtggta gcgcatacta cgcgacctgg 240<br />
gcaaacggcc gattcaccat cgccaaaacc tcgtcgacca cggtggatct gaagatgacc 300<br />
agtctgacaa ccgaggacac ggccacctat ttctgtgcca gagggacatt tgatggttat 360<br />
gagttg 366<br />
532<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
532<br />
cagtccagtc agagtgttta taataactac ttatcc 36<br />
533<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
533<br />
- 403 -<br />
공개특허 10-2011-01<strong>12</strong>308
actgcatcca gcctggcatc t 21<br />
534<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
534<br />
caaggctatt atagtggtcc tataattact 30<br />
535<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
535<br />
aactactaca tacaa 15<br />
536<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
536<br />
atcatttatg ctggtggtag cgcatactac gcgacctggg caaacggc 48<br />
537<br />
24<br />
DNA<br />
Oryctolagus cuniculus<br />
537<br />
gggacatttg atggttatga gttg 24<br />
538<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
538<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Gln Val Leu Thr Gln Thr Pro Ser Pro<br />
- 404 -<br />
공개특허 10-2011-01<strong>12</strong>308
20 25 30<br />
Val Ser Val Pro Val Gly Asp Thr Val Thr Ile Ser Cys Gln Ser Ser<br />
35 40 45<br />
Glu Ser Val Tyr Ser Asn Asn Leu Leu Ser Trp Tyr Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Arg Ala Ser Asn Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Gly Ala Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Gln Gly Tyr Tyr Ser Gly Val Ile Asn Ser<br />
539<br />
<strong>12</strong>4<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
539<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Tyr Phe Met Ser Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu<br />
50 55 60<br />
Tyr Ile Gly Phe Ile Asn Pro Gly Gly Ser Ala Tyr Tyr Ala Ser Trp<br />
65 70 75 80<br />
Ala Ser Gly Arg Leu Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
- 405 -<br />
공개특허 10-2011-01<strong>12</strong>308
100 105 110<br />
Arg Ile Leu Ile Val Ser Tyr Gly Ala Phe Thr Ile<br />
540<br />
13<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
540<br />
Gln Ser Ser Glu Ser Val Tyr Ser Asn Asn Leu Leu Ser<br />
1 5 10<br />
541<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
541<br />
Arg Ala Ser Asn Leu Ala Ser<br />
1 5<br />
542<br />
10<br />
PRT<br />
Oryctolagus cuniculus<br />
542<br />
Gln Gly Tyr Tyr Ser Gly Val Ile Asn Ser<br />
1 5 10<br />
543<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
543<br />
Ser Tyr Phe Met Ser<br />
1 5<br />
544<br />
16<br />
PRT<br />
- 406 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
544<br />
Phe Ile Asn Pro Gly Gly Ser Ala Tyr Tyr Ala Ser Trp Ala Ser Gly<br />
1 5 10 15<br />
545<br />
<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
545<br />
Ile Leu Ile Val Ser Tyr Gly Ala Phe Thr Ile<br />
1 5 10<br />
546<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
546<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccc aagtgctgac ccagactcca tcccctgtgt ctgtccctgt gggagacaca <strong>12</strong>0<br />
gtcaccatca gttgccagtc cagtgagagc gtttatagta ataacctctt atcctggtat 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctaca gggcatccaa tctggcatct 240<br />
ggtgtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccatcagc 300<br />
ggcgcacagt gtgacgatgc tgccacttac tactgtcaag gctattatag tggtgtcatt 360<br />
aatagt 366<br />
547<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
547<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtgtctg gattctccct cagtagctac ttcatgagct gggtccgcca ggctccaggg 180<br />
gaggggctgg aatacatcgg attcattaat cctggtggta gcgcatacta cgcgagctgg 240<br />
- 407 -<br />
공개특허 10-2011-01<strong>12</strong>308
gcgagtggcc gactcaccat ctccaaaacc tcgaccacgg tagatctgaa aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagga ttcttattgt ttcttatgga 360<br />
gcctttacca tc 372<br />
548<br />
39<br />
DNA<br />
Oryctolagus cuniculus<br />
548<br />
cagtccagtg agagcgttta tagtaataac ctcttatcc 39<br />
549<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
549<br />
agggcatcca atctggcatc t 21<br />
550<br />
30<br />
DNA<br />
Oryctolagus cuniculus<br />
550<br />
caaggctatt atagtggtgt cattaatagt 30<br />
551<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
551<br />
agctacttca tgagc 15<br />
552<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
552<br />
ttcattaatc ctggtggtag cgcatactac gcgagctggg cgagtggc 48<br />
- 408 -<br />
공개특허 10-2011-01<strong>12</strong>308
553<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
553<br />
attcttattg tttcttatgg agcctttacc atc 33<br />
554<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
554<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Val Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Thr<br />
35 40 45<br />
Glu Ser Ile Gly Asn Glu Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr<br />
85 90 95<br />
Ile Thr Gly Val Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Ser Ser Ala Asn Ile Asp Asn Ala<br />
555<br />
<strong>12</strong>8<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
555<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
- 409 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Lys Tyr Tyr Met Ser Trp Val Arg Gln Ala Pro Glu Lys Gly Leu Lys<br />
50 55 60<br />
Tyr Ile Gly Tyr Ile Asp Ser Thr Thr Val Asn Thr Tyr Tyr Ala Thr<br />
65 70 75 80<br />
Trp Ala Arg Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Ile Thr Ser Pro Thr Ser Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Gly Ser Thr Tyr Phe Thr Asp Gly Gly His Arg Leu Asp Leu<br />
556<br />
11<br />
PRT<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
556<br />
Gln Ala Thr Glu Ser Ile Gly Asn Glu Leu Ser<br />
1 5 10<br />
557<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
557<br />
Ser Ala Ser Thr Leu Ala Ser<br />
1 5<br />
558<br />
<strong>12</strong><br />
PRT<br />
- 410 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
558<br />
Gln Gln Gly Tyr Ser Ser Ala Asn Ile Asp Asn Ala<br />
1 5 10<br />
559<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
559<br />
Lys Tyr Tyr Met Ser<br />
1 5<br />
560<br />
17<br />
PRT<br />
Oryctolagus cuniculus<br />
560<br />
Tyr Ile Asp Ser Thr Thr Val Asn Thr Tyr Tyr Ala Thr Trp Ala Arg<br />
1 5 10 15<br />
Gly<br />
561<br />
14<br />
PRT<br />
Oryctolagus cuniculus<br />
561<br />
Gly Ser Thr Tyr Phe Thr Asp Gly Gly His Arg Leu Asp Leu<br />
1 5 10<br />
562<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
562<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctctgtgg aggtagctgt gggaggcaca <strong>12</strong>0<br />
- 411 -<br />
공개특허 10-2011-01<strong>12</strong>308
gtcaccatca agtgccaggc cactgagagc attggcaatg agttatcctg gtatcagcag 180<br />
aaaccagggc aggctcccaa gctcctgatc tattctgcat ccactctggc atctggggtc 240<br />
ccatcgcggt tcaaaggcag tggatctggg acacagttca ctctcaccat caccggcgtg 300<br />
gagtgtgatg atgctgccac ttactactgt caacagggtt atagtagtgc taatattgat 360<br />
aatgct 366<br />
563<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
563<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
accgtctctg gattctccct cagtaagtac tacatgagct gggtccgcca ggctccagag 180<br />
aaggggctga aatacatcgg atacattgat agtactactg ttaatacata ctacgcgacc 240<br />
tgggcgagag gccgattcac catctccaaa acctcgacca cggtggatct gaagatcacc 300<br />
agtccgacaa gtgaggacac ggccacctat ttctgtgcca gaggaagtac ttattttact 360<br />
gatggaggcc atcggttgga tctc 384<br />
564<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
564<br />
caggccactg agagcattgg caatgagtta tcc 33<br />
565<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
565<br />
tctgcatcca ctctggcatc t 21<br />
566<br />
36<br />
DNA<br />
- 4<strong>12</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
566<br />
caacagggtt atagtagtgc taatattgat aatgct 36<br />
567<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
567<br />
aagtactaca tgagc 15<br />
568<br />
51<br />
DNA<br />
Oryctolagus cuniculus<br />
568<br />
tacattgata gtactactgt taatacatac tacgcgacct gggcgagagg c 51<br />
569<br />
42<br />
DNA<br />
Oryctolagus cuniculus<br />
569<br />
ggaagtactt attttactga tggaggccat cggttggatc tc 42<br />
570<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
570<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Val Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Thr<br />
35 40 45<br />
Glu Ser Ile Gly Asn Glu Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln<br />
- 413 -<br />
공개특허 10-2011-01<strong>12</strong>308
50 55 60<br />
Ala Pro Lys Leu Leu Ile Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr<br />
85 90 95<br />
Ile Thr Gly Val Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Ser Ser Ala Asn Ile Asp Asn Ala<br />
571<br />
<strong>12</strong>4<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
571<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Thr Tyr Asn Met Gly Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ser Ile Thr Ile Asp Gly Arg Thr Tyr Tyr Ala Ser Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Val Ser Lys Ser Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Leu Thr Thr Gly Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Ile Leu Ile Val Ser Tyr Gly Ala Phe Thr Ile<br />
572<br />
11<br />
115 <strong>12</strong>0<br />
- 414 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
572<br />
Gln Ala Thr Glu Ser Ile Gly Asn Glu Leu Ser<br />
1 5 10<br />
573<br />
7<br />
PRT<br />
Oryctolagus cuniculus<br />
573<br />
Ser Ala Ser Thr Leu Ala Ser<br />
1 5<br />
574<br />
<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
574<br />
Gln Gln Gly Tyr Ser Ser Ala Asn Ile Asp Asn Ala<br />
1 5 10<br />
575<br />
5<br />
PRT<br />
Oryctolagus cuniculus<br />
575<br />
Thr Tyr Asn Met Gly<br />
1 5<br />
576<br />
16<br />
PRT<br />
Oryctolagus cuniculus<br />
576<br />
Ser Ile Thr Ile Asp Gly Arg Thr Tyr Tyr Ala Ser Trp Ala Lys Gly<br />
1 5 10 15<br />
- 415 -<br />
공개특허 10-2011-01<strong>12</strong>308
577<br />
11<br />
PRT<br />
Oryctolagus cuniculus<br />
577<br />
Ile Leu Ile Val Ser Tyr Gly Ala Phe Thr Ile<br />
1 5 10<br />
578<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
578<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctctgtgg aggtagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cactgagagc attggcaatg agttatcctg gtatcagcag 180<br />
aaaccagggc aggctcccaa gctcctgatc tattctgcat ccactctggc atctggggtc 240<br />
ccatcgcggt tcaaaggcag tggatctggg acacagttca ctctcaccat caccggcgtg 300<br />
gagtgtgatg atgctgccac ttactactgt caacagggtt atagtagtgc taatattgat 360<br />
aatgct 366<br />
579<br />
372<br />
DNA<br />
Oryctolagus cuniculus<br />
579<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggta acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gattctccct cagtacctac aacatgggct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aagtattact attgatggtc gcacatacta cgcgagctgg 240<br />
gcgaaaggcc gattcaccgt ctccaaaagc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ctgacaaccg gggacacggc cacctatttc tgtgccagga ttcttattgt ttcttatggg 360<br />
gcctttacca tc 372<br />
580<br />
33<br />
- 416 -<br />
공개특허 10-2011-01<strong>12</strong>308
DNA<br />
Oryctolagus cuniculus<br />
580<br />
caggccactg agagcattgg caatgagtta tcc 33<br />
581<br />
21<br />
DNA<br />
Oryctolagus cuniculus<br />
581<br />
tctgcatcca ctctggcatc t 21<br />
582<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
582<br />
caacagggtt atagtagtgc taatattgat aatgct 36<br />
583<br />
15<br />
DNA<br />
Oryctolagus cuniculus<br />
583<br />
acctacaaca tgggc 15<br />
584<br />
48<br />
DNA<br />
Oryctolagus cuniculus<br />
584<br />
agtattacta ttgatggtcg cacatactac gcgagctggg cgaaaggc 48<br />
585<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
585<br />
- 417 -<br />
공개특허 10-2011-01<strong>12</strong>308
attcttattg tttcttatgg ggcctttacc atc 33<br />
586<br />
105<br />
PRT<br />
Artificial Sequence<br />
Kappa constant domain<br />
586<br />
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu<br />
1 5 10 15<br />
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro<br />
20 25 30<br />
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly<br />
35 40 45<br />
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr<br />
50 55 60<br />
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His<br />
65 70 75 80<br />
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val<br />
85 90 95<br />
Thr Lys Ser Phe Asn Arg Gly Glu Cys<br />
587<br />
315<br />
DNA<br />
100 105<br />
Artificial Sequence<br />
Kappa constant domain<br />
587<br />
gtggctgcac catctgtctt catcttcccg ccatctgatg agcagttgaa atctggaact 60<br />
gcctctgttg tgtgcctgct gaataacttc tatcccagag aggccaaagt acagtggaag <strong>12</strong>0<br />
gtggataacg ccctccaatc gggtaactcc caggagagtg tcacagagca ggacagcaag 180<br />
gacagcacct acagcctcag cagcaccctg acgctgagca aagcagacta cgagaaacac 240<br />
aaagtctacg cctgcgaagt cacccatcag ggcctgagct cgcccgtcac aaagagcttc 300<br />
- 418 -<br />
공개특허 10-2011-01<strong>12</strong>308
aacaggggag agtgt 315<br />
588<br />
330<br />
PRT<br />
Artificial Sequence<br />
Gamma-1 constant domain<br />
588<br />
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys<br />
1 5 10 15<br />
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr<br />
20 25 30<br />
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser<br />
35 40 45<br />
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser<br />
50 55 60<br />
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr<br />
65 70 75 80<br />
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys<br />
85 90 95<br />
Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys<br />
100 105 110<br />
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys<br />
130 135 140<br />
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp<br />
145 150 155 160<br />
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu<br />
165 170 175<br />
Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu<br />
180 185 <strong>19</strong>0<br />
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn<br />
- 4<strong>19</strong> -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>19</strong>5 200 205<br />
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly<br />
210 215 220<br />
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu<br />
225 230 235 240<br />
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr<br />
245 250 255<br />
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn<br />
260 265 270<br />
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe<br />
275 280 285<br />
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn<br />
290 295 300<br />
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr<br />
305 310 315 320<br />
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys<br />
589<br />
990<br />
DNA<br />
Artificial Sequence<br />
325 330<br />
Gamma-1 constant domain<br />
589<br />
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60<br />
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg <strong>12</strong>0<br />
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180<br />
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240<br />
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagag agttgagccc 300<br />
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 360<br />
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420<br />
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480<br />
- 420 -<br />
공개특허 10-2011-01<strong>12</strong>308
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacgcc 540<br />
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600<br />
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660<br />
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggaggag 720<br />
atgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780<br />
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840<br />
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900<br />
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960<br />
cagaagagcc tctccctgtc tccgggtaaa 990<br />
590<br />
15<br />
PRT<br />
Homo sapiens<br />
590<br />
Val Pro Pro Gly Glu Asp Ser Lys Asp Val Ala Ala Pro His Arg<br />
1 5 10 15<br />
591<br />
15<br />
PRT<br />
Homo sapiens<br />
591<br />
Gly Glu Asp Ser Lys Asp Val Ala Ala Pro His Arg Gln Pro Leu<br />
1 5 10 15<br />
592<br />
15<br />
PRT<br />
Homo sapiens<br />
592<br />
Ser Lys Asp Val Ala Ala Pro His Arg Gln Pro Leu Thr Ser Ser<br />
1 5 10 15<br />
593<br />
15<br />
PRT<br />
- 421 -<br />
공개특허 10-2011-01<strong>12</strong>308
Homo sapiens<br />
593<br />
Val Ala Ala Pro His Arg Gln Pro Leu Thr Ser Ser Glu Arg Ile<br />
1 5 10 15<br />
594<br />
15<br />
PRT<br />
Homo sapiens<br />
594<br />
Pro His Arg Gln Pro Leu Thr Ser Ser Glu Arg Ile Asp Lys Gln<br />
1 5 10 15<br />
595<br />
15<br />
PRT<br />
Homo sapiens<br />
595<br />
Gln Pro Leu Thr Ser Ser Glu Arg Ile Asp Lys Gln Ile Arg Tyr<br />
1 5 10 15<br />
596<br />
15<br />
PRT<br />
Homo sapiens<br />
596<br />
Thr Ser Ser Glu Arg Ile Asp Lys Gln Ile Arg Tyr Ile Leu Asp<br />
1 5 10 15<br />
597<br />
15<br />
PRT<br />
Homo sapiens<br />
597<br />
Glu Arg Ile Asp Lys Gln Ile Arg Tyr Ile Leu Asp Gly Ile Ser<br />
1 5 10 15<br />
598<br />
- 422 -<br />
공개특허 10-2011-01<strong>12</strong>308
15<br />
PRT<br />
Homo sapiens<br />
598<br />
Asp Lys Gln Ile Arg Tyr Ile Leu Asp Gly Ile Ser Ala Leu Arg<br />
1 5 10 15<br />
599<br />
15<br />
PRT<br />
Homo sapiens<br />
599<br />
Ile Arg Tyr Ile Leu Asp Gly Ile Ser Ala Leu Arg Lys Glu Thr<br />
1 5 10 15<br />
600<br />
15<br />
PRT<br />
Homo sapiens<br />
600<br />
Ile Leu Asp Gly Ile Ser Ala Leu Arg Lys Glu Thr Cys Asn Lys<br />
1 5 10 15<br />
601<br />
15<br />
PRT<br />
Homo sapiens<br />
601<br />
Gly Ile Ser Ala Leu Arg Lys Glu Thr Cys Asn Lys Ser Asn Met<br />
1 5 10 15<br />
602<br />
15<br />
PRT<br />
Homo sapiens<br />
602<br />
Ala Leu Arg Lys Glu Thr Cys Asn Lys Ser Asn Met Cys Glu Ser<br />
- 423 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10 15<br />
603<br />
15<br />
PRT<br />
Homo sapiens<br />
603<br />
Lys Glu Thr Cys Asn Lys Ser Asn Met Cys Glu Ser Ser Lys Glu<br />
1 5 10 15<br />
604<br />
15<br />
PRT<br />
Homo sapiens<br />
604<br />
Cys Asn Lys Ser Asn Met Cys Glu Ser Ser Lys Glu Ala Leu Ala<br />
1 5 10 15<br />
605<br />
15<br />
PRT<br />
Homo sapiens<br />
605<br />
Ser Asn Met Cys Glu Ser Ser Lys Glu Ala Leu Ala Glu Asn Asn<br />
1 5 10 15<br />
606<br />
15<br />
PRT<br />
Homo sapiens<br />
606<br />
Cys Glu Ser Ser Lys Glu Ala Leu Ala Glu Asn Asn Leu Asn Leu<br />
1 5 10 15<br />
607<br />
15<br />
PRT<br />
Homo sapiens<br />
607<br />
- 424 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ser Lys Glu Ala Leu Ala Glu Asn Asn Leu Asn Leu Pro Lys Met<br />
1 5 10 15<br />
608<br />
15<br />
PRT<br />
Homo sapiens<br />
608<br />
Ala Leu Ala Glu Asn Asn Leu Asn Leu Pro Lys Met Ala Glu Lys<br />
1 5 10 15<br />
609<br />
15<br />
PRT<br />
Homo sapiens<br />
609<br />
Glu Asn Asn Leu Asn Leu Pro Lys Met Ala Glu Lys Asp Gly Cys<br />
1 5 10 15<br />
610<br />
15<br />
PRT<br />
Homo sapiens<br />
610<br />
Leu Asn Leu Pro Lys Met Ala Glu Lys Asp Gly Cys Phe Gln Ser<br />
1 5 10 15<br />
611<br />
15<br />
PRT<br />
Homo sapiens<br />
611<br />
Pro Lys Met Ala Glu Lys Asp Gly Cys Phe Gln Ser Gly Phe Asn<br />
1 5 10 15<br />
6<strong>12</strong><br />
15<br />
PRT<br />
- 425 -<br />
공개특허 10-2011-01<strong>12</strong>308
Homo sapiens<br />
6<strong>12</strong><br />
Ala Glu Lys Asp Gly Cys Phe Gln Ser Gly Phe Asn Glu Glu Thr<br />
1 5 10 15<br />
613<br />
15<br />
PRT<br />
Homo sapiens<br />
613<br />
Asp Gly Cys Phe Gln Ser Gly Phe Asn Glu Glu Thr Cys Leu Val<br />
1 5 10 15<br />
614<br />
15<br />
PRT<br />
Homo sapiens<br />
614<br />
Phe Gln Ser Gly Phe Asn Glu Glu Thr Cys Leu Val Lys Ile Ile<br />
1 5 10 15<br />
615<br />
15<br />
PRT<br />
Homo sapiens<br />
615<br />
Gly Phe Asn Glu Glu Thr Cys Leu Val Lys Ile Ile Thr Gly Leu<br />
1 5 10 15<br />
616<br />
15<br />
PRT<br />
Homo sapiens<br />
616<br />
Glu Glu Thr Cys Leu Val Lys Ile Ile Thr Gly Leu Leu Glu Phe<br />
1 5 10 15<br />
617<br />
- 426 -<br />
공개특허 10-2011-01<strong>12</strong>308
15<br />
PRT<br />
Homo sapiens<br />
617<br />
Cys Leu Val Lys Ile Ile Thr Gly Leu Leu Glu Phe Glu Val Tyr<br />
1 5 10 15<br />
618<br />
15<br />
PRT<br />
Homo sapiens<br />
618<br />
Lys Ile Ile Thr Gly Leu Leu Glu Phe Glu Val Tyr Leu Glu Tyr<br />
1 5 10 15<br />
6<strong>19</strong><br />
15<br />
PRT<br />
Homo sapiens<br />
6<strong>19</strong><br />
Thr Gly Leu Leu Glu Phe Glu Val Tyr Leu Glu Tyr Leu Gln Asn<br />
1 5 10 15<br />
620<br />
15<br />
PRT<br />
Homo sapiens<br />
620<br />
Leu Glu Phe Glu Val Tyr Leu Glu Tyr Leu Gln Asn Arg Phe Glu<br />
1 5 10 15<br />
621<br />
15<br />
PRT<br />
Homo sapiens<br />
621<br />
Glu Val Tyr Leu Glu Tyr Leu Gln Asn Arg Phe Glu Ser Ser Glu<br />
- 427 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10 15<br />
622<br />
15<br />
PRT<br />
Homo sapiens<br />
622<br />
Leu Glu Tyr Leu Gln Asn Arg Phe Glu Ser Ser Glu Glu Gln Ala<br />
1 5 10 15<br />
623<br />
15<br />
PRT<br />
Homo sapiens<br />
623<br />
Leu Gln Asn Arg Phe Glu Ser Ser Glu Glu Gln Ala Arg Ala Val<br />
1 5 10 15<br />
624<br />
15<br />
PRT<br />
Homo sapiens<br />
624<br />
Arg Phe Glu Ser Ser Glu Glu Gln Ala Arg Ala Val Gln Met Ser<br />
1 5 10 15<br />
625<br />
15<br />
PRT<br />
Homo sapiens<br />
625<br />
Ser Ser Glu Glu Gln Ala Arg Ala Val Gln Met Ser Thr Lys Val<br />
1 5 10 15<br />
626<br />
15<br />
PRT<br />
Homo sapiens<br />
- 428 -<br />
공개특허 10-2011-01<strong>12</strong>308
626<br />
Glu Gln Ala Arg Ala Val Gln Met Ser Thr Lys Val Leu Ile Gln<br />
1 5 10 15<br />
627<br />
15<br />
PRT<br />
Homo sapiens<br />
627<br />
Arg Ala Val Gln Met Ser Thr Lys Val Leu Ile Gln Phe Leu Gln<br />
1 5 10 15<br />
628<br />
15<br />
PRT<br />
Homo sapiens<br />
628<br />
Gln Met Ser Thr Lys Val Leu Ile Gln Phe Leu Gln Lys Lys Ala<br />
1 5 10 15<br />
629<br />
15<br />
PRT<br />
Homo sapiens<br />
629<br />
Thr Lys Val Leu Ile Gln Phe Leu Gln Lys Lys Ala Lys Asn Leu<br />
1 5 10 15<br />
630<br />
15<br />
PRT<br />
Homo sapiens<br />
630<br />
Leu Ile Gln Phe Leu Gln Lys Lys Ala Lys Asn Leu Asp Ala Ile<br />
1 5 10 15<br />
631<br />
15<br />
PRT<br />
- 429 -<br />
공개특허 10-2011-01<strong>12</strong>308
Homo sapiens<br />
631<br />
Phe Leu Gln Lys Lys Ala Lys Asn Leu Asp Ala Ile Thr Thr Pro<br />
1 5 10 15<br />
632<br />
15<br />
PRT<br />
Homo sapiens<br />
632<br />
Lys Lys Ala Lys Asn Leu Asp Ala Ile Thr Thr Pro Asp Pro Thr<br />
1 5 10 15<br />
633<br />
15<br />
PRT<br />
Homo sapiens<br />
633<br />
Lys Asn Leu Asp Ala Ile Thr Thr Pro Asp Pro Thr Thr Asn Ala<br />
1 5 10 15<br />
634<br />
15<br />
PRT<br />
Homo sapiens<br />
634<br />
Asp Ala Ile Thr Thr Pro Asp Pro Thr Thr Asn Ala Ser Leu Leu<br />
1 5 10 15<br />
635<br />
15<br />
PRT<br />
Homo sapiens<br />
635<br />
Thr Thr Pro Asp Pro Thr Thr Asn Ala Ser Leu Leu Thr Lys Leu<br />
1 5 10 15<br />
636<br />
- 430 -<br />
공개특허 10-2011-01<strong>12</strong>308
15<br />
PRT<br />
Homo sapiens<br />
636<br />
Asp Pro Thr Thr Asn Ala Ser Leu Leu Thr Lys Leu Gln Ala Gln<br />
1 5 10 15<br />
637<br />
15<br />
PRT<br />
Homo sapiens<br />
637<br />
Thr Asn Ala Ser Leu Leu Thr Lys Leu Gln Ala Gln Asn Gln Trp<br />
1 5 10 15<br />
638<br />
15<br />
PRT<br />
Homo sapiens<br />
638<br />
Ser Leu Leu Thr Lys Leu Gln Ala Gln Asn Gln Trp Leu Gln Asp<br />
1 5 10 15<br />
639<br />
15<br />
PRT<br />
Homo sapiens<br />
639<br />
Thr Lys Leu Gln Ala Gln Asn Gln Trp Leu Gln Asp Met Thr Thr<br />
1 5 10 15<br />
640<br />
15<br />
PRT<br />
Homo sapiens<br />
640<br />
Gln Ala Gln Asn Gln Trp Leu Gln Asp Met Thr Thr His Leu Ile<br />
- 431 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10 15<br />
641<br />
15<br />
PRT<br />
Homo sapiens<br />
641<br />
Asn Gln Trp Leu Gln Asp Met Thr Thr His Leu Ile Leu Arg Ser<br />
1 5 10 15<br />
642<br />
15<br />
PRT<br />
Homo sapiens<br />
642<br />
Leu Gln Asp Met Thr Thr His Leu Ile Leu Arg Ser Phe Lys Glu<br />
1 5 10 15<br />
643<br />
15<br />
PRT<br />
Homo sapiens<br />
643<br />
Met Thr Thr His Leu Ile Leu Arg Ser Phe Lys Glu Phe Leu Gln<br />
1 5 10 15<br />
644<br />
15<br />
PRT<br />
Homo sapiens<br />
644<br />
His Leu Ile Leu Arg Ser Phe Lys Glu Phe Leu Gln Ser Ser Leu<br />
1 5 10 15<br />
645<br />
15<br />
PRT<br />
Homo sapiens<br />
- 432 -<br />
공개특허 10-2011-01<strong>12</strong>308
645<br />
Leu Arg Ser Phe Lys Glu Phe Leu Gln Ser Ser Leu Arg Ala Leu<br />
1 5 10 15<br />
646<br />
15<br />
PRT<br />
Homo sapiens<br />
646<br />
Phe Lys Glu Phe Leu Gln Ser Ser Leu Arg Ala Leu Arg Gln Met<br />
1 5 10 15<br />
647<br />
111<br />
PRT<br />
Oryctolagus cuniculus<br />
647<br />
Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser Val Ser Ala Ala Val Gly<br />
1 5 10 15<br />
Gly Thr Val Thr Ile Lys Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu<br />
20 25 30<br />
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln Arg Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Ser Ser Arg Phe Lys Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Asp Leu Glu Cys<br />
65 70 75 80<br />
Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn<br />
85 90 95<br />
Ile Asp Asn Ala Phe Gly Gly Gly Thr Glu Val Val Val Lys Arg<br />
648<br />
88<br />
PRT<br />
Homo sapiens<br />
100 105 110<br />
- 433 -<br />
공개특허 10-2011-01<strong>12</strong>308
648<br />
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp<br />
20 25 30<br />
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Glu Asp Phe Ala Thr Tyr Tyr Cys<br />
649<br />
88<br />
PRT<br />
85<br />
Homo sapiens<br />
649<br />
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr<br />
20 25 30<br />
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Glu Asp Val Ala Thr Tyr Tyr Cys<br />
650<br />
88<br />
85<br />
- 434 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Homo sapiens<br />
650<br />
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp<br />
20 25 30<br />
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Asp Asp Phe Ala Thr Tyr Tyr Cys<br />
651<br />
111<br />
PRT<br />
85<br />
Artificial Sequence<br />
Humanized antibody<br />
651<br />
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu<br />
20 25 30<br />
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn<br />
- 435 -<br />
공개특허 10-2011-01<strong>12</strong>308
85 90 95<br />
Ile Asp Asn Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg<br />
652<br />
117<br />
PRT<br />
100 105 110<br />
Oryctolagus cuniculus<br />
652<br />
Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro Gly Thr Pro<br />
1 5 10 15<br />
Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser Asn Tyr Tyr<br />
20 25 30<br />
Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile Gly<br />
35 40 45<br />
Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Trp Ala Ile Gly<br />
50 55 60<br />
Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu Lys Met Thr<br />
65 70 75 80<br />
Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr Phe Cys Ala Arg Asp Asp<br />
85 90 95<br />
Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln Gly Thr Leu<br />
Val Thr Val Ser Ser<br />
115<br />
653<br />
97<br />
PRT<br />
Homo sapiens<br />
653<br />
100 105 110<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Asn<br />
- 436 -<br />
공개특허 10-2011-01<strong>12</strong>308
20 25 30<br />
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Ser Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
Arg<br />
654<br />
97<br />
PRT<br />
Homo sapiens<br />
654<br />
85 90 95<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Ile Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Asn<br />
20 25 30<br />
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Ser Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
Arg<br />
655<br />
98<br />
85 90 95<br />
- 437 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Homo sapiens<br />
655<br />
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr<br />
20 25 30<br />
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Ser Val Ile Tyr Ser Gly Gly Ser Ser Thr Tyr Tyr Ala Asp Ser Val<br />
50 55 60<br />
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr<br />
65 70 75 80<br />
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys<br />
Ala Lys<br />
656<br />
<strong>12</strong>0<br />
PRT<br />
Artificial sequence<br />
Humanized antibody<br />
656<br />
85 90 95<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Trp Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
- 438 -<br />
공개특허 10-2011-01<strong>12</strong>308
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
100 105 110<br />
Gly Thr Leu Val Thr Val Ser Ser<br />
657<br />
<strong>12</strong>0<br />
PRT<br />
115 <strong>12</strong>0<br />
Artificial sequence<br />
Humanized antibody<br />
657<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
100 105 110<br />
Gly Thr Leu Val Thr Val Ser Ser<br />
658<br />
166<br />
PRT<br />
115 <strong>12</strong>0<br />
- 439 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
658<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Asn Tyr Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser<br />
65 70 75 80<br />
Ala Ile Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
130 135 140<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
145 150 155 160<br />
Leu Gly Cys Leu Val Lys<br />
659<br />
16<br />
PRT<br />
165<br />
Oryctolagus cuniculus<br />
659<br />
Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser Ala Ile Gly<br />
1 5 10 15<br />
660<br />
- 440 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
660<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Ile Asn Asn Glu Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Arg Pro Lys Leu Leu Ile Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Ser Leu Arg Asn Ile Asp Asn Ala<br />
661<br />
<strong>12</strong>5<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
661<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Asn Tyr Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
- 441 -<br />
공개특허 10-2011-01<strong>12</strong>308
50 55 60<br />
Trp Ile Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Ile Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
662<br />
366<br />
DNA<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
662<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctcggtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccaggc cagtcagagc attaacaatg aattatcctg gtatcagcag 180<br />
aaaccagggc agcgtcccaa gctcctgatc tatagggcat ccactctggc atctggggtc 240<br />
tcatcgcggt tcaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caacagggtt atagtctgag gaatattgat 360<br />
aatgct 366<br />
663<br />
375<br />
DNA<br />
Oryctolagus cuniculus<br />
663<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtaactac tacgtgacct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatcatttat ggtagtgatg aaacggccta cgcgacctgg 240<br />
gcgataggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ctgacagccg cggacacggc cacctatttc tgtgccagag atgatagtag tgactgggat 360<br />
- 442 -<br />
공개특허 10-2011-01<strong>12</strong>308
gcaaaattta acttg 375<br />
664<br />
450<br />
PRT<br />
Oryctolagus cuniculus<br />
664<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Trp Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
100 105 110<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
130 135 140<br />
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser<br />
145 150 155 160<br />
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val<br />
165 170 175<br />
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro<br />
180 185 <strong>19</strong>0<br />
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys<br />
- 443 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>19</strong>5 200 205<br />
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp<br />
210 215 220<br />
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly<br />
225 230 235 240<br />
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile<br />
245 250 255<br />
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu<br />
260 265 270<br />
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His<br />
275 280 285<br />
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg<br />
290 295 300<br />
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys<br />
305 310 315 320<br />
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu<br />
325 330 335<br />
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr<br />
340 345 350<br />
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu<br />
355 360 365<br />
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp<br />
370 375 380<br />
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val<br />
385 390 395 400<br />
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp<br />
405 410 415<br />
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His<br />
420 425 430<br />
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro<br />
Gly Lys<br />
435 440 445<br />
- 444 -<br />
공개특허 10-2011-01<strong>12</strong>308
450<br />
665<br />
450<br />
PRT<br />
Oryctolagus cuniculus<br />
665<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
100 105 110<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
130 135 140<br />
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser<br />
145 150 155 160<br />
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val<br />
165 170 175<br />
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro<br />
180 185 <strong>19</strong>0<br />
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys<br />
- 445 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>19</strong>5 200 205<br />
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp<br />
210 215 220<br />
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly<br />
225 230 235 240<br />
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile<br />
245 250 255<br />
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu<br />
260 265 270<br />
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His<br />
275 280 285<br />
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg<br />
290 295 300<br />
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys<br />
305 310 315 320<br />
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu<br />
325 330 335<br />
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr<br />
340 345 350<br />
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu<br />
355 360 365<br />
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp<br />
370 375 380<br />
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val<br />
385 390 395 400<br />
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp<br />
405 410 415<br />
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His<br />
420 425 430<br />
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro<br />
435 440 445<br />
- 446 -<br />
공개특허 10-2011-01<strong>12</strong>308
Gly Lys<br />
450<br />
666<br />
216<br />
PRT<br />
Oryctolagus cuniculus<br />
666<br />
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp<br />
1 5 10 15<br />
Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu Leu<br />
20 25 30<br />
Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr<br />
35 40 45<br />
Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser<br />
50 55 60<br />
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp<br />
65 70 75 80<br />
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn Ile<br />
85 90 95<br />
Asp Asn Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val<br />
100 105 110<br />
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg<br />
130 135 140<br />
Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn<br />
145 150 155 160<br />
Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser<br />
165 170 175<br />
Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys<br />
180 185 <strong>19</strong>0<br />
Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr<br />
- 447 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>19</strong>5 200 205<br />
Lys Ser Phe Asn Arg Gly Glu Cys<br />
210 215<br />
667<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
667<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Glu Val Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Glu Thr Ile Tyr Ser Trp Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln<br />
50 55 60<br />
Pro Pro Lys Leu Leu Ile Tyr Gln Ala Ser Asp Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Pro Ser Arg Phe Ser Gly Ser Gly Ala Gly Thr Glu Tyr Thr Leu Thr<br />
85 90 95<br />
Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
100 105 110<br />
Gly Tyr Ser Gly Ser Asn Val Asp Asn Val<br />
668<br />
<strong>12</strong>6<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
668<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Glu Gln Leu Lys Glu Ser Gly Gly Arg Leu Val Thr<br />
- 448 -<br />
공개특허 10-2011-01<strong>12</strong>308
20 25 30<br />
Pro Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu<br />
35 40 45<br />
Asn Asp His Ala Met Gly Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Tyr Ile Gly Phe Ile Asn Ser Gly Gly Ser Ala Arg Tyr Ala Ser<br />
65 70 75 80<br />
Trp Ala Glu Gly Arg Phe Thr Ile Ser Arg Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Met Thr Ser Leu Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Val Arg Gly Gly Ala Val Trp Ser Ile His Ser Phe Asp Pro<br />
669<br />
366<br />
DNA<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
669<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctctgtgg aggtagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca attgccaggc cagtgagacc atttacagtt ggttatcctg gtatcagcag 180<br />
aagccagggc agcctcccaa gctcctgatc taccaggcat ccgatctggc atctggggtc 240<br />
ccatcgcgat tcagcggcag tggggctggg acagagtaca ctctcaccat cagcggcgtg 300<br />
cagtgtgacg atgctgccac ttactactgt caacagggtt atagtggtag taatgttgat 360<br />
aatgtt 366<br />
670<br />
378<br />
DNA<br />
Oryctolagus cuniculus<br />
670<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
gagcagctga aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacacttacc <strong>12</strong>0<br />
- 449 -<br />
공개특허 10-2011-01<strong>12</strong>308
tgcacagcct ctggattctc cctcaatgac catgcaatgg gctgggtccg ccaggctcca 180<br />
gggaaggggc tggaatacat cggattcatt aatagtggtg gtagcgcacg ctacgcgagc 240<br />
tgggcagaag gccgattcac catctccaga acctcgacca cggtggatct gaaaatgacc 300<br />
agtctgacaa ccgaggacac ggccacctat ttctgtgtca gagggggtgc tgtttggagt 360<br />
attcatagtt ttgatccc 378<br />
671<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
671<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asp Asn Asn Tyr Leu Ser Trp Phe Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Val Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Thr Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Val Tyr Asp Asp Asp Ser Asp Asn Ala<br />
672<br />
<strong>12</strong>5<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
672<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
- 450 -<br />
공개특허 10-2011-01<strong>12</strong>308
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Val Tyr Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Phe Ile Thr Met Ser Asp Asn Ile Asn Tyr Ala Ser Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Ser Arg Gly Trp Gly Thr Met Gly Arg Leu Asp Leu<br />
673<br />
369<br />
DNA<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
673<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccg ccgtgctgac ccagactcca tctcccgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccaggc cagtcagagt gtttatgaca acaactactt atcctggttt 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctatg gtgcatccac tctggcatct 240<br />
ggggtcccat cgcggttcgt gggcagtgga tctgggacac agttcactct caccatcaca 300<br />
gacgtgcagt gtgacgatgc tgccacttac tattgtgcag gcgtttatga tgatgatagt 360<br />
gataatgcc 369<br />
674<br />
375<br />
DNA<br />
Oryctolagus cuniculus<br />
674<br />
- 451 -<br />
공개특허 10-2011-01<strong>12</strong>308
atggagactg ggctgcgctg gcttctcctg gtggctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acccctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtgtctac tacatgaact gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg attcattaca atgagtgata atataaatta cgcgagctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagga gtcgtggctg gggtacaatg 360<br />
ggtcggttgg atctc 375<br />
675<br />
<strong>12</strong>3<br />
PRT<br />
Oryctolagus cuniculus<br />
675<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Ile Cys Asp Pro Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Pro Val Gly Gly Thr Val Ser Ile Ser Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Tyr Glu Asn Asn Tyr Leu Ser Trp Phe Gln Gln Lys Pro<br />
50 55 60<br />
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly Ala Ser Thr Leu Asp Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Thr Asp Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Val Tyr Asp Asp Asp Ser Asp Asp Ala<br />
676<br />
<strong>12</strong>6<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
- 452 -<br />
공개특허 10-2011-01<strong>12</strong>308
676<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Glu Gln Leu Lys Glu Ser Gly Gly Gly Leu Val Thr<br />
20 25 30<br />
Pro Gly Gly Thr Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu<br />
35 40 45<br />
Asn Ala Tyr Tyr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu<br />
50 55 60<br />
Glu Trp Ile Gly Phe Ile Thr Leu Asn Asn Asn Val Ala Tyr Ala Asn<br />
65 70 75 80<br />
Trp Ala Lys Gly Arg Phe Thr Phe Ser Lys Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Met Thr Ser Pro Thr Pro Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Ser Arg Gly Trp Gly Ala Met Gly Arg Leu Asp Leu<br />
677<br />
369<br />
DNA<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
677<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
atatgtgacc ctgtgctgac ccagactcca tctcccgtat ctgcacctgt gggaggcaca <strong>12</strong>0<br />
gtcagcatca gttgccaggc cagtcagagt gtttatgaga acaactattt atcctggttt 180<br />
cagcagaaac cagggcagcc tcccaagctc ctgatctatg gtgcatccac tctggattct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccattaca 300<br />
gacgtgcagt gtgacgatgc tgccacttac tattgtgcag gcgtttatga tgatgatagt 360<br />
gatgatgcc 369<br />
678<br />
378<br />
DNA<br />
- 453 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
678<br />
atggagactg ggctgcgctg gcttctcctg gtggctgtgc tcaaaggtgt ccagtgtcag 60<br />
gagcagctga aggagtccgg aggaggcctg gtaacgcctg gaggaaccct gacactcacc <strong>12</strong>0<br />
tgcacagcct ctggattctc cctcaatgcc tactacatga actgggtccg ccaggctcca 180<br />
gggaaggggc tggaatggat cggattcatt actctgaata ataatgtagc ttacgcgaac 240<br />
tgggcgaaag gccgattcac cttctccaaa acctcgacca cggtggatct gaaaatgacc 300<br />
agtccgacac ccgaggacac ggccacctat ttctgtgcca ggagtcgtgg ctggggtgca 360<br />
atgggtcggt tggatctc 378<br />
679<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
679<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Gln Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Asn Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Val Asp Asp Asn Asn Trp Leu Gly Trp Tyr Gln Gln Lys Arg<br />
50 55 60<br />
Gly Gln Pro Pro Lys Tyr Leu Ile Tyr Ser Ala Ser Thr Leu Ala Ser<br />
65 70 75 80<br />
Gly Val Pro Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Gln Phe Thr<br />
85 90 95<br />
Leu Thr Ile Ser Asp Leu Glu Cys Asp Asp Ala Ala Thr Tyr Tyr Cys<br />
100 105 110<br />
Ala Gly Gly Phe Ser Gly Asn Ile Phe Ala<br />
680<br />
<strong>12</strong>2<br />
115 <strong>12</strong>0<br />
- 454 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Oryctolagus cuniculus<br />
680<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Gly Gly Phe Gly Thr Thr Tyr Tyr Ala Thr Trp<br />
65 70 75 80<br />
Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Arg Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Gly Gly Pro Gly Asn Gly Gly Asp Ile<br />
681<br />
366<br />
DNA<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
681<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgccc aagtgctgac ccagactcca tcgcctgtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca actgccaggc cagtcagagt gttgatgata acaactggtt aggctggtat 180<br />
cagcagaaac gagggcagcc tcccaagtac ctgatctatt ctgcatccac tctggcatct 240<br />
ggggtcccat cgcggttcaa aggcagtgga tctgggacac agttcactct caccatcagc 300<br />
gacctggagt gtgacgatgc tgccacttac tactgtgcag gcggttttag tggtaatatc 360<br />
tttgct 366<br />
- 455 -<br />
공개특허 10-2011-01<strong>12</strong>308
682<br />
366<br />
DNA<br />
Oryctolagus cuniculus<br />
682<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagtctctg gcttctccct cagtagctat gcaatgagct gggtccgcca ggctccagga 180<br />
aaggggctgg agtggatcgg aatcattggt ggttttggta ccacatacta cgcgacctgg 240<br />
gcgaaaggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgag aatcaccagt 300<br />
ccgacaaccg aggacacggc cacctatttc tgtgccagag gtggtcctgg taatggtggt 360<br />
gacatc 366<br />
683<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
683<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Thr Phe Ala Ala Val Leu Thr Gln Thr Pro Ser Pro<br />
20 25 30<br />
Val Ser Val Pro Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ser Ser<br />
35 40 45<br />
Gln Ser Val Tyr Asn Asn Phe Leu Ser Trp Tyr Gln Gln Lys Pro Gly<br />
50 55 60<br />
Gln Pro Pro Lys Leu Leu Ile Tyr Gln Ala Ser Lys Leu Ala Ser Gly<br />
65 70 75 80<br />
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu<br />
85 90 95<br />
Thr Ile Ser Gly Val Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Leu<br />
100 105 110<br />
Gly Gly Tyr Asp Asp Asp Ala Asp Asn Ala<br />
- 456 -<br />
공개특허 10-2011-01<strong>12</strong>308
684<br />
<strong>12</strong>8<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
684<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Lys Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser<br />
35 40 45<br />
Asp Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Ile Ile Tyr Ala Gly Ser Gly Ser Thr Trp Tyr Ala Ser<br />
65 70 75 80<br />
Trp Ala Lys Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp<br />
85 90 95<br />
Leu Lys Ile Thr Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys<br />
100 105 110<br />
Ala Arg Asp Gly Tyr Asp Asp Tyr Gly Asp Phe Asp Arg Leu Asp Leu<br />
685<br />
366<br />
DNA<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
685<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
acatttgcag ccgtgctgac ccagacacca tcgcccgtgt ctgtacctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca agtgccagtc cagtcagagt gtttataata atttcttatc gtggtatcag 180<br />
cagaaaccag ggcagcctcc caagctcctg atctaccagg catccaaact ggcatctggg 240<br />
gtcccagata ggttcagcgg cagtggatct gggacacagt tcactctcac catcagcggc 300<br />
- 457 -<br />
공개특허 10-2011-01<strong>12</strong>308
gtgcagtgtg acgatgctgc cacttactac tgtctaggcg gttatgatga tgatgctgat 360<br />
aatgct 366<br />
686<br />
384<br />
DNA<br />
Oryctolagus cuniculus<br />
686<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tcaaaggtgt ccagtgtcag 60<br />
tcggtggagg agtccggggg tcgcctggtc acgcctggga cacccctgac gctcacctgc <strong>12</strong>0<br />
acagtctctg gaatcgacct cagtgactat gcaatgagct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatcatttat gctggtagtg gtagcacatg gtacgcgagc 240<br />
tgggcgaaag gccgattcac catctccaaa acctcgacca cggtggatct gaaaatcacc 300<br />
agtccgacaa ccgaggacac ggccacctat ttctgtgcca gagatggata cgatgactat 360<br />
ggtgatttcg atcgattgga tctc 384<br />
687<br />
<strong>12</strong>2<br />
PRT<br />
Oryctolagus cuniculus<br />
687<br />
Met Asp Thr Arg Ala Pro Thr Gln Leu Leu Gly Leu Leu Leu Leu Trp<br />
1 5 10 15<br />
Leu Pro Gly Ala Arg Cys Ala Tyr Asp Met Thr Gln Thr Pro Ala Ser<br />
20 25 30<br />
Val Ser Ala Ala Val Gly Gly Thr Val Thr Ile Lys Cys Gln Ala Ser<br />
35 40 45<br />
Gln Ser Ile Asn Asn Glu Leu Ser Trp Tyr Gln Gln Lys Ser Gly Gln<br />
50 55 60<br />
Arg Pro Lys Leu Leu Ile Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val<br />
65 70 75 80<br />
Ser Ser Arg Phe Lys Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr<br />
85 90 95<br />
Ile Ser Asp Leu Glu Cys Ala Asp Ala Ala Thr Tyr Tyr Cys Gln Gln<br />
- 458 -<br />
공개특허 10-2011-01<strong>12</strong>308
100 105 110<br />
Gly Tyr Ser Leu Arg Asn Ile Asp Asn Ala<br />
688<br />
<strong>12</strong>5<br />
PRT<br />
115 <strong>12</strong>0<br />
Oryctolagus cuniculus<br />
688<br />
Met Glu Thr Gly Leu Arg Trp Leu Leu Leu Val Ala Val Leu Ser Gly<br />
1 5 10 15<br />
Val Gln Cys Gln Ser Leu Glu Glu Ser Gly Gly Arg Leu Val Thr Pro<br />
20 25 30<br />
Gly Thr Pro Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Asn Tyr Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
50 55 60<br />
Trp Ile Gly Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Trp<br />
65 70 75 80<br />
Ala Ile Gly Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu<br />
85 90 95<br />
Lys Met Thr Ser Leu Thr Ala Ala Asp Thr Ala Thr Tyr Phe Cys Ala<br />
100 105 110<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu<br />
689<br />
366<br />
DNA<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Oryctolagus cuniculus<br />
689<br />
atggacacga gggcccccac tcagctgctg gggctcctgc tgctctggct cccaggtgcc 60<br />
agatgtgcct atgatatgac ccagactcca gcctcggtgt ctgcagctgt gggaggcaca <strong>12</strong>0<br />
gtcaccatca aatgccaggc cagtcagagc attaacaatg aattatcctg gtatcagcag 180<br />
- 459 -<br />
공개특허 10-2011-01<strong>12</strong>308
aaatcagggc agcgtcccaa gctcctgatc tatagggcat ccactctggc atctggggtc 240<br />
tcatcgcggt tcaaaggcag tggatctggg acagagttca ctctcaccat cagcgacctg 300<br />
gagtgtgccg atgctgccac ttactactgt caacagggtt atagtctgag gaatattgat 360<br />
aatgct 366<br />
690<br />
375<br />
DNA<br />
Oryctolagus cuniculus<br />
690<br />
atggagactg ggctgcgctg gcttctcctg gtcgctgtgc tctcaggtgt ccagtgtcag 60<br />
tcgctggagg agtccggggg tcgcctggtc acgcctggga cacccctgac actcacctgc <strong>12</strong>0<br />
acagcctctg gattctccct cagtaactac tacatgacct gggtccgcca ggctccaggg 180<br />
aaggggctgg aatggatcgg aatgatttat ggtagtgatg aaacagccta cgcgaactgg 240<br />
gcgataggcc gattcaccat ctccaaaacc tcgaccacgg tggatctgaa aatgaccagt 300<br />
ctgacagccg cggacacggc cacctatttc tgtgccagag atgatagtag tgactgggat 360<br />
gcaaaattta acttg 375<br />
691<br />
450<br />
PRT<br />
Oryctolagus cuniculus<br />
691<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Trp Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
- 460 -<br />
공개특허 10-2011-01<strong>12</strong>308
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
100 105 110<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
130 135 140<br />
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser<br />
145 150 155 160<br />
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val<br />
165 170 175<br />
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro<br />
180 185 <strong>19</strong>0<br />
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys<br />
<strong>19</strong>5 200 205<br />
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp<br />
210 215 220<br />
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly<br />
225 230 235 240<br />
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile<br />
245 250 255<br />
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu<br />
260 265 270<br />
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His<br />
275 280 285<br />
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg<br />
290 295 300<br />
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys<br />
305 310 315 320<br />
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu<br />
325 330 335<br />
- 461 -<br />
공개특허 10-2011-01<strong>12</strong>308
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr<br />
340 345 350<br />
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu<br />
355 360 365<br />
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp<br />
370 375 380<br />
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val<br />
385 390 395 400<br />
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp<br />
405 410 415<br />
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His<br />
420 425 430<br />
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro<br />
Gly Lys<br />
450<br />
692<br />
450<br />
PRT<br />
435 440 445<br />
Oryctolagus cuniculus<br />
692<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Met Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Asn Ser Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
- 462 -<br />
공개특허 10-2011-01<strong>12</strong>308
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
100 105 110<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
130 135 140<br />
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser<br />
145 150 155 160<br />
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val<br />
165 170 175<br />
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro<br />
180 185 <strong>19</strong>0<br />
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys<br />
<strong>19</strong>5 200 205<br />
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp<br />
210 215 220<br />
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly<br />
225 230 235 240<br />
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile<br />
245 250 255<br />
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu<br />
260 265 270<br />
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His<br />
275 280 285<br />
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg<br />
290 295 300<br />
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys<br />
305 310 315 320<br />
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu<br />
325 330 335<br />
- 463 -<br />
공개특허 10-2011-01<strong>12</strong>308
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr<br />
340 345 350<br />
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu<br />
355 360 365<br />
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp<br />
370 375 380<br />
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val<br />
385 390 395 400<br />
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp<br />
405 410 415<br />
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His<br />
420 425 430<br />
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro<br />
Gly Lys<br />
450<br />
693<br />
217<br />
PRT<br />
435 440 445<br />
Oryctolagus cuniculus<br />
693<br />
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu<br />
20 25 30<br />
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn<br />
- 464 -<br />
공개특허 10-2011-01<strong>12</strong>308
85 90 95<br />
Ile Asp Asn Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr<br />
100 105 110<br />
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro<br />
130 135 140<br />
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly<br />
145 150 155 160<br />
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr<br />
165 170 175<br />
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His<br />
180 185 <strong>19</strong>0<br />
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val<br />
<strong>19</strong>5 200 205<br />
Thr Lys Ser Phe Asn Arg Gly Glu Cys<br />
210 215<br />
694<br />
33<br />
DNA<br />
Oryctolagus cuniculus<br />
694<br />
caggccagtc agagcattaa caatgagtta tcc 33<br />
695<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
695<br />
caacagggtt atagtctgag gaacattgat aatgct 36<br />
696<br />
48<br />
DNA<br />
- 465 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
696<br />
atcatctatg gtagtgatga aaccgcctac gctacctccg ctataggc 48<br />
697<br />
36<br />
DNA<br />
Oryctolagus cuniculus<br />
<br />
697<br />
gatgatagta gtgactggga tgcaaagttc aacttg 36<br />
698<br />
336<br />
DNA<br />
Oryctolagus cuniculus<br />
698<br />
gctatccaga tgacccagtc tccttcctcc ctgtctgcat ctgtaggaga cagagtcacc 60<br />
atcacttgcc aggccagtca gagcattaac aatgagttat cctggtatca gcagaaacca <strong>12</strong>0<br />
gggaaagccc ctaagctcct gatctatagg gcatccactc tggcatctgg ggtcccatca 180<br />
aggttcagcg gcagtggatc tgggacagac ttcactctca ccatcagcag cctgcagcct 240<br />
gatgattttg caacttatta ctgccaacag ggttatagtc tgaggaacat tgataatgct 300<br />
ttcggcggag ggaccaaggt ggaaatcaaa cgtacg 336<br />
699<br />
1<strong>12</strong><br />
PRT<br />
Oryctolagus cuniculus<br />
699<br />
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu<br />
20 25 30<br />
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
- 466 -<br />
공개특허 10-2011-01<strong>12</strong>308
50 55 60<br />
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn<br />
85 90 95<br />
Ile Asp Asn Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr<br />
700<br />
360<br />
DNA<br />
100 105 110<br />
Oryctolagus cuniculus<br />
700<br />
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60<br />
tcctgtgcag cctctggatt ctccctcagt aactactacg tgacctgggt ccgtcaggct <strong>12</strong>0<br />
ccagggaagg ggctggagtg ggtcggcatc atctatggta gtgatgaaac cgcctacgct 180<br />
acctccgcta taggccgatt caccatctcc agagacaatt ccaagaacac cctgtatctt 240<br />
caaatgaaca gcctgagagc tgaggacact gctgtgtatt actgtgctag agatgatagt 300<br />
agtgactggg atgcaaagtt caacttgtgg ggccaaggga ccctcgtcac cgtctcgagc 360<br />
701<br />
651<br />
DNA<br />
Oryctolagus cuniculus<br />
701<br />
gctatccaga tgacccagtc tccttcctcc ctgtctgcat ctgtaggaga cagagtcacc 60<br />
atcacttgcc aggccagtca gagcattaac aatgagttat cctggtatca gcagaaacca <strong>12</strong>0<br />
gggaaagccc ctaagctcct gatctatagg gcatccactc tggcatctgg ggtcccatca 180<br />
aggttcagcg gcagtggatc tgggacagac ttcactctca ccatcagcag cctgcagcct 240<br />
gatgattttg caacttatta ctgccaacag ggttatagtc tgaggaacat tgataatgct 300<br />
ttcggcggag ggaccaaggt ggaaatcaaa cgtacggtgg ctgcaccatc tgtcttcatc 360<br />
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420<br />
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480<br />
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540<br />
- 467 -<br />
공개특허 10-2011-01<strong>12</strong>308
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600<br />
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg t 651<br />
702<br />
217<br />
PRT<br />
Oryctolagus cuniculus<br />
702<br />
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu<br />
20 25 30<br />
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
35 40 45<br />
Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn<br />
85 90 95<br />
Ile Asp Asn Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr<br />
100 105 110<br />
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro<br />
130 135 140<br />
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly<br />
145 150 155 160<br />
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr<br />
165 170 175<br />
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His<br />
180 185 <strong>19</strong>0<br />
- 468 -<br />
공개특허 10-2011-01<strong>12</strong>308
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val<br />
<strong>19</strong>5 200 205<br />
Thr Lys Ser Phe Asn Arg Gly Glu Cys<br />
210 215<br />
703<br />
1350<br />
DNA<br />
Oryctolagus cuniculus<br />
703<br />
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60<br />
tcctgtgcag cctctggatt ctccctcagt aactactacg tgacctgggt ccgtcaggct <strong>12</strong>0<br />
ccagggaagg ggctggagtg ggtcggcatc atctatggta gtgatgaaac cgcctacgct 180<br />
acctccgcta taggccgatt caccatctcc agagacaatt ccaagaacac cctgtatctt 240<br />
caaatgaaca gcctgagagc tgaggacact gctgtgtatt actgtgctag agatgatagt 300<br />
agtgactggg atgcaaagtt caacttgtgg ggccaaggga ccctcgtcac cgtctcgagc 360<br />
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 420<br />
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 480<br />
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 540<br />
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 600<br />
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagag agttgagccc 660<br />
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cctgggggga 720<br />
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 780<br />
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 840<br />
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacgcc 900<br />
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 960<br />
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 1020<br />
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggaggag 1080<br />
atgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 1140<br />
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg <strong>12</strong>00<br />
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg <strong>12</strong>60<br />
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 1320<br />
- 469 -<br />
공개특허 10-2011-01<strong>12</strong>308
cagaagagcc tctccctgtc tccgggtaaa 1350<br />
704<br />
450<br />
PRT<br />
Oryctolagus cuniculus<br />
704<br />
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly<br />
1 5 10 15<br />
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Asn Tyr<br />
20 25 30<br />
Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val<br />
35 40 45<br />
Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser Ala Ile<br />
50 55 60<br />
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu<br />
65 70 75 80<br />
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala<br />
85 90 95<br />
Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp Gly Gln<br />
100 105 110<br />
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala<br />
130 135 140<br />
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser<br />
145 150 155 160<br />
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val<br />
165 170 175<br />
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro<br />
180 185 <strong>19</strong>0<br />
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys<br />
- 470 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>19</strong>5 200 205<br />
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp<br />
210 215 220<br />
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly<br />
225 230 235 240<br />
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile<br />
245 250 255<br />
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu<br />
260 265 270<br />
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His<br />
275 280 285<br />
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg<br />
290 295 300<br />
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys<br />
305 310 315 320<br />
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu<br />
325 330 335<br />
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr<br />
340 345 350<br />
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu<br />
355 360 365<br />
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp<br />
370 375 380<br />
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val<br />
385 390 395 400<br />
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp<br />
405 410 415<br />
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His<br />
420 425 430<br />
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro<br />
Gly Lys<br />
435 440 445<br />
- 471 -<br />
공개특허 10-2011-01<strong>12</strong>308
450<br />
705<br />
705<br />
DNA<br />
Oryctolagus cuniculus<br />
705<br />
atgaagtggg taacctttat ttcccttctg tttctcttta gcagcgctta ttccgctatc 60<br />
cagatgaccc agtctccttc ctccctgtct gcatctgtag gagacagagt caccatcact <strong>12</strong>0<br />
tgccaggcca gtcagagcat taacaatgag ttatcctggt atcagcagaa accagggaaa 180<br />
gcccctaagc tcctgatcta tagggcatcc actctggcat ctggggtccc atcaaggttc 240<br />
agcggcagtg gatctgggac agacttcact ctcaccatca gcagcctgca gcctgatgat 300<br />
tttgcaactt attactgcca acagggttat agtctgagga acattgataa tgctttcggc 360<br />
ggagggacca aggtggaaat caaacgtacg gtggctgcac catctgtctt catcttcccg 420<br />
ccatctgatg agcagttgaa atctggaact gcctctgttg tgtgcctgct gaataacttc 480<br />
tatcccagag aggccaaagt acagtggaag gtggataacg ccctccaatc gggtaactcc 540<br />
caggagagtg tcacagagca ggacagcaag gacagcacct acagcctcag cagcaccctg 600<br />
acgctgagca aagcagacta cgagaaacac aaagtctacg cctgcgaagt cacccatcag 660<br />
ggcctgagct cgcccgtcac aaagagcttc aacaggggag agtgt 705<br />
706<br />
235<br />
PRT<br />
Oryctolagus cuniculus<br />
706<br />
Met Lys Trp Val Thr Phe Ile Ser Leu Leu Phe Leu Phe Ser Ser Ala<br />
1 5 10 15<br />
Tyr Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser<br />
20 25 30<br />
Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn<br />
35 40 45<br />
Asn Glu Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu<br />
50 55 60<br />
- 472 -<br />
공개특허 10-2011-01<strong>12</strong>308
Leu Ile Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe<br />
65 70 75 80<br />
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu<br />
85 90 95<br />
Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu<br />
100 105 110<br />
Arg Asn Ile Asp Asn Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu<br />
130 135 140<br />
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe<br />
145 150 155 160<br />
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln<br />
165 170 175<br />
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser<br />
180 185 <strong>19</strong>0<br />
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu<br />
<strong>19</strong>5 200 205<br />
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser<br />
210 215 220<br />
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys<br />
225 230 235<br />
707<br />
1404<br />
DNA<br />
Oryctolagus cuniculus<br />
707<br />
atgaagtggg taacctttat ttcccttctg tttctcttta gcagcgctta ttccgaggtg 60<br />
cagctggtgg agtctggggg aggcttggtc cagcctgggg ggtccctgag actctcctgt <strong>12</strong>0<br />
gcagcctctg gattctccct cagtaactac tacgtgacct gggtccgtca ggctccaggg 180<br />
aaggggctgg agtgggtcgg catcatctat ggtagtgatg aaaccgccta cgctacctcc 240<br />
gctataggcc gattcaccat ctccagagac aattccaaga acaccctgta tcttcaaatg 300<br />
- 473 -<br />
공개특허 10-2011-01<strong>12</strong>308
aacagcctga gagctgagga cactgctgtg tattactgtg ctagagatga tagtagtgac 360<br />
tgggatgcaa agttcaactt gtggggccaa gggaccctcg tcaccgtctc gagcgcctcc 420<br />
accaagggcc catcggtctt ccccctggca ccctcctcca agagcacctc tgggggcaca 480<br />
gcggccctgg gctgcctggt caaggactac ttccccgaac cggtgacggt gtcgtggaac 540<br />
tcaggcgccc tgaccagcgg cgtgcacacc ttcccggctg tcctacagtc ctcaggactc 600<br />
tactccctca gcagcgtggt gaccgtgccc tccagcagct tgggcaccca gacctacatc 660<br />
tgcaacgtga atcacaagcc cagcaacacc aaggtggaca agagagttga gcccaaatct 720<br />
tgtgacaaaa ctcacacatg cccaccgtgc ccagcacctg aactcctggg gggaccgtca 780<br />
gtcttcctct tccccccaaa acccaaggac accctcatga tctcccggac ccctgaggtc 840<br />
acatgcgtgg tggtggacgt gagccacgaa gaccctgagg tcaagttcaa ctggtacgtg 900<br />
gacggcgtgg aggtgcataa tgccaagaca aagccgcggg aggagcagta cgccagcacg 960<br />
taccgtgtgg tcagcgtcct caccgtcctg caccaggact ggctgaatgg caaggagtac 1020<br />
aagtgcaagg tctccaacaa agccctccca gcccccatcg agaaaaccat ctccaaagcc 1080<br />
aaagggcagc cccgagaacc acaggtgtac accctgcccc catcccggga ggagatgacc 1140<br />
aagaaccagg tcagcctgac ctgcctggtc aaaggcttct atcccagcga catcgccgtg <strong>12</strong>00<br />
gagtgggaga gcaatgggca gccggagaac aactacaaga ccacgcctcc cgtgctggac <strong>12</strong>60<br />
tccgacggct ccttcttcct ctacagcaag ctcaccgtgg acaagagcag gtggcagcag 1320<br />
gggaacgtct tctcatgctc cgtgatgcat gaggctctgc acaaccacta cacgcagaag 1380<br />
agcctctccc tgtctccggg taaa 1404<br />
708<br />
468<br />
PRT<br />
Oryctolagus cuniculus<br />
708<br />
Met Lys Trp Val Thr Phe Ile Ser Leu Leu Phe Leu Phe Ser Ser Ala<br />
1 5 10 15<br />
Tyr Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro<br />
20 25 30<br />
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser<br />
35 40 45<br />
Asn Tyr Tyr Val Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu<br />
- 474 -<br />
공개특허 10-2011-01<strong>12</strong>308
50 55 60<br />
Trp Val Gly Ile Ile Tyr Gly Ser Asp Glu Thr Ala Tyr Ala Thr Ser<br />
65 70 75 80<br />
Ala Ile Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu<br />
85 90 95<br />
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr<br />
100 105 110<br />
Cys Ala Arg Asp Asp Ser Ser Asp Trp Asp Ala Lys Phe Asn Leu Trp<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro<br />
130 135 140<br />
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr<br />
145 150 155 160<br />
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr<br />
165 170 175<br />
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro<br />
180 185 <strong>19</strong>0<br />
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr<br />
<strong>19</strong>5 200 205<br />
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn<br />
210 215 220<br />
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser<br />
225 230 235 240<br />
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu<br />
245 250 255<br />
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu<br />
260 265 270<br />
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser<br />
275 280 285<br />
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu<br />
290 295 300<br />
- 475 -<br />
공개특허 10-2011-01<strong>12</strong>308
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr<br />
305 310 315 320<br />
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn<br />
325 330 335<br />
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro<br />
340 345 350<br />
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln<br />
355 360 365<br />
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val<br />
370 375 380<br />
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val<br />
385 390 395 400<br />
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro<br />
405 410 415<br />
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr<br />
420 425 430<br />
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val<br />
435 440 445<br />
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu<br />
450 455 460<br />
Ser Pro Gly Lys<br />
465<br />
709<br />
111<br />
PRT<br />
Oryctolagus cuniculus<br />
709<br />
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly<br />
1 5 10 15<br />
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Asn Asn Glu<br />
20 25 30<br />
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile<br />
- 476 -<br />
공개특허 10-2011-01<strong>12</strong>308
35 40 45<br />
Tyr Arg Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly<br />
50 55 60<br />
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro<br />
65 70 75 80<br />
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Ser Leu Arg Asn<br />
85 90 95<br />
Ile Asp Asn Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg<br />
710<br />
11<br />
PRT<br />
Homo sapiens<br />
710<br />
100 105 110<br />
Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly<br />
1 5 10<br />
711<br />
11<br />
PRT<br />
Homo sapiens<br />
711<br />
Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala<br />
1 5 10<br />
7<strong>12</strong><br />
11<br />
PRT<br />
Homo sapiens<br />
7<strong>12</strong><br />
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala<br />
1 5 10<br />
713<br />
7<br />
PRT<br />
- 477 -<br />
공개특허 10-2011-01<strong>12</strong>308
Homo sapiens<br />
713<br />
Ala Ala Ser Ser Leu Gln Ser<br />
1 5<br />
714<br />
7<br />
PRT<br />
Homo sapiens<br />
714<br />
Ala Ala Ser Thr Leu Gln Ser<br />
1 5<br />
715<br />
7<br />
PRT<br />
Homo sapiens<br />
715<br />
Lys Ala Ser Ser Leu Glu Ser<br />
1 5<br />
716<br />
5<br />
PRT<br />
Homo sapiens<br />
716<br />
Ser Asn Tyr Met Ser<br />
1 5<br />
717<br />
16<br />
PRT<br />
Homo sapiens<br />
717<br />
Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly<br />
1 5 10 15<br />
718<br />
17<br />
- 478 -<br />
공개특허 10-2011-01<strong>12</strong>308
2<strong>12</strong>> PRT<br />
Homo sapiens<br />
718<br />
Val Ile Tyr Ser Gly Gly Ser Ser Thr Tyr Tyr Ala Asp Ser Val Lys<br />
1 5 10 15<br />
Gly<br />
7<strong>19</strong><br />
330<br />
PRT<br />
Artificial Sequence<br />
Gamma-1 constant domain<br />
7<strong>19</strong><br />
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys<br />
1 5 10 15<br />
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr<br />
20 25 30<br />
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser<br />
35 40 45<br />
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser<br />
50 55 60<br />
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr<br />
65 70 75 80<br />
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys<br />
85 90 95<br />
Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys<br />
100 105 110<br />
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys<br />
130 135 140<br />
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp<br />
- 479 -<br />
공개특허 10-2011-01<strong>12</strong>308
145 150 155 160<br />
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu<br />
165 170 175<br />
Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu<br />
180 185 <strong>19</strong>0<br />
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn<br />
<strong>19</strong>5 200 205<br />
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly<br />
210 215 220<br />
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu<br />
225 230 235 240<br />
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr<br />
245 250 255<br />
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn<br />
260 265 270<br />
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe<br />
275 280 285<br />
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn<br />
290 295 300<br />
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr<br />
305 310 315 320<br />
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys<br />
720<br />
297<br />
DNA<br />
325 330<br />
Oryctolagus cuniculus<br />
720<br />
atccagatga cccagtctcc ttcctccctg tctgcatctg taggagacag agtcaccatc 60<br />
acttgccagg ccagtcagag cattaacaat gagttatcct ggtatcagca gaaaccaggg <strong>12</strong>0<br />
aaagccccta agctcctgat ctatagggca tccactctgg catctggggt cccatcaagg 180<br />
- 480 -<br />
공개특허 10-2011-01<strong>12</strong>308
ttcagcggca gtggatctgg gacagacttc actctcacca tcagcagcct gcagcctgat 240<br />
gattttgcaa cttattactg ccaacagggt tatagtctga ggaacattga taatgct 297<br />
721<br />
333<br />
DNA<br />
Oryctolagus cuniculus<br />
721<br />
gcctatgata tgacccagac tccagcctcg gtgtctgcag ctgtgggagg cacagtcacc 60<br />
atcaagtgcc aggccagtca gagcattaac aatgaattat cctggtatca gcagaaacca <strong>12</strong>0<br />
gggcagcgtc ccaagctcct gatctatagg gcatccactc tggcatctgg ggtctcatcg 180<br />
cggttcaaag gcagtggatc tgggacagag ttcactctca ccatcagcga cctggagtgt 240<br />
gccgatgctg ccacttacta ctgtcaacag ggttatagtc tgaggaatat tgataatgct 300<br />
ttcggcggag ggaccgaggt ggtggtcaaa cgt 333<br />
722<br />
648<br />
DNA<br />
Oryctolagus cuniculus<br />
722<br />
atccagatga cccagtctcc ttcctccctg tctgcatctg taggagacag agtcaccatc 60<br />
acttgccagg ccagtcagag cattaacaat gagttatcct ggtatcagca gaaaccaggg <strong>12</strong>0<br />
aaagccccta agctcctgat ctatagggca tccactctgg catctggggt cccatcaagg 180<br />
ttcagcggca gtggatctgg gacagacttc actctcacca tcagcagcct gcagcctgat 240<br />
gattttgcaa cttattactg ccaacagggt tatagtctga ggaacattga taatgctttc 300<br />
ggcggaggga ccaaggtgga aatcaaacgt acggtggctg caccatctgt cttcatcttc 360<br />
ccgccatctg atgagcagtt gaaatctgga actgcctctg ttgtgtgcct gctgaataac 420<br />
ttctatccca gagaggccaa agtacagtgg aaggtggata acgccctcca atcgggtaac 480<br />
tcccaggaga gtgtcacaga gcaggacagc aaggacagca cctacagcct cagcagcacc 540<br />
ctgacgctga gcaaagcaga ctacgagaaa cacaaagtct acgcctgcga agtcacccat 600<br />
cagggcctga gctcgcccgt cacaaagagc ttcaacaggg gagagtgt 648<br />
723<br />
333<br />
DNA<br />
- 481 -<br />
공개특허 10-2011-01<strong>12</strong>308
Oryctolagus cuniculus<br />
723<br />
gctatccaga tgacccagtc tccttcctcc ctgtctgcat ctgtaggaga cagagtcacc 60<br />
atcacttgcc aggccagtca gagcattaac aatgagttat cctggtatca gcagaaacca <strong>12</strong>0<br />
gggaaagccc ctaagctcct gatctatagg gcatccactc tggcatctgg ggtcccatca 180<br />
aggttcagcg gcagtggatc tgggacagac ttcactctca ccatcagcag cctgcagcct 240<br />
gatgattttg caacttatta ctgccaacag ggttatagtc tgaggaacat tgataatgct 300<br />
ttcggcggag ggaccaaggt ggaaatcaaa cgt 333<br />
724<br />
327<br />
DNA<br />
Oryctolagus cuniculus<br />
724<br />
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc 60<br />
tcctgtgcag cctctggatt ctccctcagt aactactacg tgacctgggt ccgtcaggct <strong>12</strong>0<br />
ccagggaagg ggctggagtg ggtcggcatc atctatggta gtgatgaaac cgcctacgct 180<br />
acctccgcta taggccgatt caccatctcc agagacaatt ccaagaacac cctgtatctt 240<br />
caaatgaaca gcctgagagc tgaggacact gctgtgtatt actgtgctag agatgatagt 300<br />
agtgactggg atgcaaagtt caacttg 327<br />
725<br />
351<br />
DNA<br />
Oryctolagus cuniculus<br />
725<br />
cagtcgctgg aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc 60<br />
tgcacagcct ctggattctc cctcagtaac tactacgtga cctgggtccg ccaggctcca <strong>12</strong>0<br />
gggaaggggc tggaatggat cggaatcatt tatggtagtg atgaaacggc ctacgcgacc 180<br />
tgggcgatag gccgattcac catctccaaa acctcgacca cggtggatct gaaaatgacc 240<br />
agtctgacag ccgcggacac ggccacctat ttctgtgcca gagatgatag tagtgactgg 300<br />
gatgcaaaat ttaacttgtg gggccaaggc accctggtca ccgtctcgag c 351<br />
726<br />
224<br />
- 482 -<br />
공개특허 10-2011-01<strong>12</strong>308
PRT<br />
Homo sapiens<br />
726<br />
Met Glu Lys Leu Leu Cys Phe Leu Val Leu Thr Ser Leu Ser His Ala<br />
1 5 10 15<br />
Phe Gly Gln Thr Asp Met Ser Arg Lys Ala Phe Val Phe Pro Lys Glu<br />
20 25 30<br />
Ser Asp Thr Ser Tyr Val Ser Leu Lys Ala Pro Leu Thr Lys Pro Leu<br />
35 40 45<br />
Lys Ala Phe Thr Val Cys Leu His Phe Tyr Thr Glu Leu Ser Ser Thr<br />
50 55 60<br />
Arg Gly Tyr Ser Ile Phe Ser Tyr Ala Thr Lys Arg Gln Asp Asn Glu<br />
65 70 75 80<br />
Ile Leu Ile Phe Trp Ser Lys Asp Ile Gly Tyr Ser Phe Thr Val Gly<br />
85 90 95<br />
Gly Ser Glu Ile Leu Phe Glu Val Pro Glu Val Thr Val Ala Pro Val<br />
100 105 110<br />
His Ile Cys Thr Ser Trp Glu Ser Ala Ser Gly Ile Val Glu Phe Trp<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Val Asp Gly Lys Pro Arg Val Arg Lys Ser Leu Lys Lys Gly Tyr Thr<br />
130 135 140<br />
Val Gly Ala Glu Ala Ser Ile Ile Leu Gly Gln Glu Gln Asp Ser Phe<br />
145 150 155 160<br />
Gly Gly Asn Phe Glu Gly Ser Gln Ser Leu Val Gly Asp Ile Gly Asn<br />
165 170 175<br />
Val Asn Met Trp Asp Phe Val Leu Ser Pro Asp Glu Ile Asn Thr Ile<br />
180 185 <strong>19</strong>0<br />
Tyr Leu Gly Gly Pro Phe Ser Pro Asn Val Leu Asn Trp Arg Ala Leu<br />
<strong>19</strong>5 200 205<br />
Lys Tyr Glu Val Gln Gly Glu Val Phe Thr Lys Pro Gln Leu Trp Pro<br />
210 215 220<br />
727<br />
- 483 -<br />
공개특허 10-2011-01<strong>12</strong>308
468<br />
PRT<br />
Homo sapiens<br />
727<br />
Met Leu Ala Val Gly Cys Ala Leu Leu Ala Ala Leu Leu Ala Ala Pro<br />
1 5 10 15<br />
Gly Ala Ala Leu Ala Pro Arg Arg Cys Pro Ala Gln Glu Val Ala Arg<br />
20 25 30<br />
Gly Val Leu Thr Ser Leu Pro Gly Asp Ser Val Thr Leu Thr Cys Pro<br />
35 40 45<br />
Gly Val Glu Pro Glu Asp Asn Ala Thr Val His Trp Val Leu Arg Lys<br />
50 55 60<br />
Pro Ala Ala Gly Ser His Pro Ser Arg Trp Ala Gly Met Gly Arg Arg<br />
65 70 75 80<br />
Leu Leu Leu Arg Ser Val Gln Leu His Asp Ser Gly Asn Tyr Ser Cys<br />
85 90 95<br />
Tyr Arg Ala Gly Arg Pro Ala Gly Thr Val His Leu Leu Val Asp Val<br />
100 105 110<br />
Pro Pro Glu Glu Pro Gln Leu Ser Cys Phe Arg Lys Ser Pro Leu Ser<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Asn Val Val Cys Glu Trp Gly Pro Arg Ser Thr Pro Ser Leu Thr Thr<br />
130 135 140<br />
Lys Ala Val Leu Leu Val Arg Lys Phe Gln Asn Ser Pro Ala Glu Asp<br />
145 150 155 160<br />
Phe Gln Glu Pro Cys Gln Tyr Ser Gln Glu Ser Gln Lys Phe Ser Cys<br />
165 170 175<br />
Gln Leu Ala Val Pro Glu Gly Asp Ser Ser Phe Tyr Ile Val Ser Met<br />
180 185 <strong>19</strong>0<br />
Cys Val Ala Ser Ser Val Gly Ser Lys Phe Ser Lys Thr Gln Thr Phe<br />
<strong>19</strong>5 200 205<br />
Gln Gly Cys Gly Ile Leu Gln Pro Asp Pro Pro Ala Asn Ile Thr Val<br />
- 484 -<br />
공개특허 10-2011-01<strong>12</strong>308
210 215 220<br />
Thr Ala Val Ala Arg Asn Pro Arg Trp Leu Ser Val Thr Trp Gln Asp<br />
225 230 235 240<br />
Pro His Ser Trp Asn Ser Ser Phe Tyr Arg Leu Arg Phe Glu Leu Arg<br />
245 250 255<br />
Tyr Arg Ala Glu Arg Ser Lys Thr Phe Thr Thr Trp Met Val Lys Asp<br />
260 265 270<br />
Leu Gln His His Cys Val Ile His Asp Ala Trp Ser Gly Leu Arg His<br />
275 280 285<br />
Val Val Gln Leu Arg Ala Gln Glu Glu Phe Gly Gln Gly Glu Trp Ser<br />
290 295 300<br />
Glu Trp Ser Pro Glu Ala Met Gly Thr Pro Trp Thr Glu Ser Arg Ser<br />
305 310 315 320<br />
Pro Pro Ala Glu Asn Glu Val Ser Thr Pro Met Gln Ala Leu Thr Thr<br />
325 330 335<br />
Asn Lys Asp Asp Asp Asn Ile Leu Phe Arg Asp Ser Ala Asn Ala Thr<br />
340 345 350<br />
Ser Leu Pro Val Gln Asp Ser Ser Ser Val Pro Leu Pro Thr Phe Leu<br />
355 360 365<br />
Val Ala Gly Gly Ser Leu Ala Phe Gly Thr Leu Leu Cys Ile Ala Ile<br />
370 375 380<br />
Val Leu Arg Phe Lys Lys Thr Trp Lys Leu Arg Ala Leu Lys Glu Gly<br />
385 390 395 400<br />
Lys Thr Ser Met His Pro Pro Tyr Ser Leu Gly Gln Leu Val Pro Glu<br />
405 410 415<br />
Arg Pro Arg Pro Thr Pro Val Leu Val Pro Leu Ile Ser Pro Pro Val<br />
420 425 430<br />
Ser Pro Ser Ser Leu Gly Ser Asp Asn Thr Ser Ser His Asn Arg Pro<br />
435 440 445<br />
Asp Ala Arg Asp Pro Arg Ser Pro Tyr Asp Ile Ser Asn Thr Asp Tyr<br />
450 455 460<br />
- 485 -<br />
공개특허 10-2011-01<strong>12</strong>308
Phe Phe Pro Arg<br />
465<br />
728<br />
918<br />
PRT<br />
Homo sapiens<br />
728<br />
Met Leu Thr Leu Gln Thr Trp Val Val Gln Ala Leu Phe Ile Phe Leu<br />
1 5 10 15<br />
Thr Thr Glu Ser Thr Gly Glu Leu Leu Asp Pro Cys Gly Tyr Ile Ser<br />
20 25 30<br />
Pro Glu Ser Pro Val Val Gln Leu His Ser Asn Phe Thr Ala Val Cys<br />
35 40 45<br />
Val Leu Lys Glu Lys Cys Met Asp Tyr Phe His Val Asn Ala Asn Tyr<br />
50 55 60<br />
Ile Val Trp Lys Thr Asn His Phe Thr Ile Pro Lys Glu Gln Tyr Thr<br />
65 70 75 80<br />
Ile Ile Asn Arg Thr Ala Ser Ser Val Thr Phe Thr Asp Ile Ala Ser<br />
85 90 95<br />
Leu Asn Ile Gln Leu Thr Cys Asn Ile Leu Thr Phe Gly Gln Leu Glu<br />
100 105 110<br />
Gln Asn Val Tyr Gly Ile Thr Ile Ile Ser Gly Leu Pro Pro Glu Lys<br />
115 <strong>12</strong>0 <strong>12</strong>5<br />
Pro Lys Asn Leu Ser Cys Ile Val Asn Glu Gly Lys Lys Met Arg Cys<br />
130 135 140<br />
Glu Trp Asp Gly Gly Arg Glu Thr His Leu Glu Thr Asn Phe Thr Leu<br />
145 150 155 160<br />
Lys Ser Glu Trp Ala Thr His Lys Phe Ala Asp Cys Lys Ala Lys Arg<br />
165 170 175<br />
Asp Thr Pro Thr Ser Cys Thr Val Asp Tyr Ser Thr Val Tyr Phe Val<br />
180 185 <strong>19</strong>0<br />
Asn Ile Glu Val Trp Val Glu Ala Glu Asn Ala Leu Gly Lys Val Thr<br />
- 486 -<br />
공개특허 10-2011-01<strong>12</strong>308
<strong>19</strong>5 200 205<br />
Ser Asp His Ile Asn Phe Asp Pro Val Tyr Lys Val Lys Pro Asn Pro<br />
210 215 220<br />
Pro His Asn Leu Ser Val Ile Asn Ser Glu Glu Leu Ser Ser Ile Leu<br />
225 230 235 240<br />
Lys Leu Thr Trp Thr Asn Pro Ser Ile Lys Ser Val Ile Ile Leu Lys<br />
245 250 255<br />
Tyr Asn Ile Gln Tyr Arg Thr Lys Asp Ala Ser Thr Trp Ser Gln Ile<br />
260 265 270<br />
Pro Pro Glu Asp Thr Ala Ser Thr Arg Ser Ser Phe Thr Val Gln Asp<br />
275 280 285<br />
Leu Lys Pro Phe Thr Glu Tyr Val Phe Arg Ile Arg Cys Met Lys Glu<br />
290 295 300<br />
Asp Gly Lys Gly Tyr Trp Ser Asp Trp Ser Glu Glu Ala Ser Gly Ile<br />
305 310 315 320<br />
Thr Tyr Glu Asp Arg Pro Ser Lys Ala Pro Ser Phe Trp Tyr Lys Ile<br />
325 330 335<br />
Asp Pro Ser His Thr Gln Gly Tyr Arg Thr Val Gln Leu Val Trp Lys<br />
340 345 350<br />
Thr Leu Pro Pro Phe Glu Ala Asn Gly Lys Ile Leu Asp Tyr Glu Val<br />
355 360 365<br />
Thr Leu Thr Arg Trp Lys Ser His Leu Gln Asn Tyr Thr Val Asn Ala<br />
370 375 380<br />
Thr Lys Leu Thr Val Asn Leu Thr Asn Asp Arg Tyr Leu Ala Thr Leu<br />
385 390 395 400<br />
Thr Val Arg Asn Leu Val Gly Lys Ser Asp Ala Ala Val Leu Thr Ile<br />
405 410 415<br />
Pro Ala Cys Asp Phe Gln Ala Thr His Pro Val Met Asp Leu Lys Ala<br />
420 425 430<br />
Phe Pro Lys Asp Asn Met Leu Trp Val Glu Trp Thr Thr Pro Arg Glu<br />
435 440 445<br />
- 487 -<br />
공개특허 10-2011-01<strong>12</strong>308
Ser Val Lys Lys Tyr Ile Leu Glu Trp Cys Val Leu Ser Asp Lys Ala<br />
450 455 460<br />
Pro Cys Ile Thr Asp Trp Gln Gln Glu Asp Gly Thr Val His Arg Thr<br />
465 470 475 480<br />
Tyr Leu Arg Gly Asn Leu Ala Glu Ser Lys Cys Tyr Leu Ile Thr Val<br />
485 490 495<br />
Thr Pro Val Tyr Ala Asp Gly Pro Gly Ser Pro Glu Ser Ile Lys Ala<br />
500 505 510<br />
Tyr Leu Lys Gln Ala Pro Pro Ser Lys Gly Pro Thr Val Arg Thr Lys<br />
515 520 525<br />
Lys Val Gly Lys Asn Glu Ala Val Leu Glu Trp Asp Gln Leu Pro Val<br />
530 535 540<br />
Asp Val Gln Asn Gly Phe Ile Arg Asn Tyr Thr Ile Phe Tyr Arg Thr<br />
545 550 555 560<br />
Ile Ile Gly Asn Glu Thr Ala Val Asn Val Asp Ser Ser His Thr Glu<br />
565 570 575<br />
Tyr Thr Leu Ser Ser Leu Thr Ser Asp Thr Leu Tyr Met Val Arg Met<br />
580 585 590<br />
Ala Ala Tyr Thr Asp Glu Gly Gly Lys Asp Gly Pro Glu Phe Thr Phe<br />
595 600 605<br />
Thr Thr Pro Lys Phe Ala Gln Gly Glu Ile Glu Ala Ile Val Val Pro<br />
610 615 620<br />
Val Cys Leu Ala Phe Leu Leu Thr Thr Leu Leu Gly Val Leu Phe Cys<br />
625 630 635 640<br />
Phe Asn Lys Arg Asp Leu Ile Lys Lys His Ile Trp Pro Asn Val Pro<br />
645 650 655<br />
Asp Pro Ser Lys Ser His Ile Ala Gln Trp Ser Pro His Thr Pro Pro<br />
660 665 670<br />
Arg His Asn Phe Asn Ser Lys Asp Gln Met Tyr Ser Asp Gly Asn Phe<br />
675 680 685<br />
Thr Asp Val Ser Val Val Glu Ile Glu Ala Asn Asp Lys Lys Pro Phe<br />
- 488 -<br />
공개특허 10-2011-01<strong>12</strong>308
690 695 700<br />
Pro Glu Asp Leu Lys Ser Leu Asp Leu Phe Lys Lys Glu Lys Ile Asn<br />
705 710 715 720<br />
Thr Glu Gly His Ser Ser Gly Ile Gly Gly Ser Ser Cys Met Ser Ser<br />
725 730 735<br />
Ser Arg Pro Ser Ile Ser Ser Ser Asp Glu Asn Glu Ser Ser Gln Asn<br />
740 745 750<br />
Thr Ser Ser Thr Val Gln Tyr Ser Thr Val Val His Ser Gly Tyr Arg<br />
755 760 765<br />
His Gln Val Pro Ser Val Gln Val Phe Ser Arg Ser Glu Ser Thr Gln<br />
770 775 780<br />
Pro Leu Leu Asp Ser Glu Glu Arg Pro Glu Asp Leu Gln Leu Val Asp<br />
785 790 795 800<br />
His Val Asp Gly Gly Asp Gly Ile Leu Pro Arg Gln Gln Tyr Phe Lys<br />
805 810 815<br />
Gln Asn Cys Ser Gln His Glu Ser Ser Pro Asp Ile Ser His Phe Glu<br />
820 825 830<br />
Arg Ser Lys Gln Val Ser Ser Val Asn Glu Glu Asp Phe Val Arg Leu<br />
835 840 845<br />
Lys Gln Gln Ile Ser Asp His Ile Ser Gln Ser Cys Gly Ser Gly Gln<br />
850 855 860<br />
Met Lys Met Phe Gln Glu Val Ser Ala Ala Asp Ala Phe Gly Pro Gly<br />
865 870 875 880<br />
Thr Glu Gly Gln Val Glu Arg Phe Glu Thr Val Gly Met Glu Ala Ala<br />
885 890 895<br />
Thr Asp Glu Gly Met Pro Lys Ser Tyr Leu Pro Gln Thr Val Arg Gln<br />
Gly Gly Tyr Met Pro Gln<br />
915<br />
900 905 910<br />
- 489 -<br />
공개특허 10-2011-01<strong>12</strong>308