full text
full text
full text
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
148 •˜ 20 Farbe, chemische Konstitution und Mesomerie S 20 Farbe, chemische Konstitution und Mesomerie 149<br />
bzw. N + B-(2p + o*) Ubergange genannt. Die Berechtigung einer<br />
solchen Zuordnung liefert die experimentelle Feststellung1, das<br />
das erste Ionisationspotential dieser Verbindung zahlenmasig mit<br />
diesen Ubergangen ubereinstimmt.<br />
Sterische Faktoren konnen nicht nur die Lage der Absorptionsmaxima,<br />
sondern auch deren Hohe stark beeinflussen. Einige interessante<br />
Falle, uber die PICKETT und RODEBUSCH (1940) berichtet<br />
haben, sollen hier besprochen werden. Die genannten Autoren<br />
stellten folgende Reihenfolge der Absorptionshohe und Lage der<br />
substituierten Benzaldehyde bzw. Benzophenone fest.<br />
Sowohl in der Benzaldehyd- als auch in der Benzophenonreihe<br />
andert sich die Lage des Absorptionsmaximums kaum mit der<br />
Stellung der eingefuhrten CH3-Gruppen. Die Absorptionsintensitat<br />
jedoch fallt standig ab, je naher die CH,- Gruppe der Aldehydbzw.<br />
Ketogruppe ruckt. Fur die o-disubstituierten Methylderivate<br />
ist der Abfall am starksten. Die Absorptionshohe betragt bei den<br />
Aldehyden nur bei den Ketonen Ca. I/, der Absorption der Verbindungen<br />
mit p-standigen CH3-Gruppen. Es handelt sich hier um<br />
einen sterischen Effekt der ortho-standigen CH,-Gruppen, der sich<br />
in einer etwas komplizierten Weise auf die Intensitat der Absorption<br />
auswirkt.<br />
Die dafur von BRAUDE~ gegebene Erklarung bewegt sich auf<br />
folgenden Linien: Die Abnahme der Intensitat ist auf einen<br />
1 R. S. MULLIEEN, J. chem. Phys. 3, 504 (1935).<br />
E. A. BRAUDE U. a., J. chem. Soc. 1890 (1949), 3754 (1955). L. H.<br />
SCHWARTZMANN U. B. B. CORSON, J. Amer. chem. Soc. 76,781 (1954). G. D.<br />
HEDDEN U. W. G. BROWN, ibid. 76, 3744 (1953). Vgl. jedoch die Darstellung<br />
von R. B. TURNER U. D. W. VOITLE, J. Am. Chem. Soc. 73, 1403 (1951).<br />
verhinderten Elektronenubergang zwischen einer nicht ebenen Anordnung<br />
der Phenyl- und Carboxylgruppe im Grundzustand und<br />
einer ebenen Anordnung im angeregten Zustand zuruckzufuhren.<br />
Die Phenylebene und die C=O-Ebene sind bestrebt, auf Grund der<br />
Mesomerie sich konplanar einzustellen, andererseits fuhren sie im<br />
Grundzustand wegen der freien Drehbarkeit der a-Bindung Torsionsschwingungen<br />
um diese Achse aus. Im angeregten Zustand ist<br />
die freie Drehbarkeit weitgehend behindert, weil ein Elektronen-<br />
Ubergang wahrscheinlich von der Phenyl- zur Carboxylgruppe<br />
stattgefunden hat, der eine quasi-doppelte Bindung zwischen diesen<br />
Gruppen herstellt. Diese verkleinert indes die Amplitude der Torsionsschwingung.<br />
Noch wesentlich geringer ist die Ausschwingung<br />
um die Verbindungsachse wegen raumlicher Hinderung, wenn in<br />
o-Stellung zwei CH,-Gruppen stehen. Diese Verhaltnisse ubersieht<br />
man am besten an der graphischen Darstellung des Potentialverlaufes<br />
des Molekuls wahrend der Torsionsschwingung im Elektronen-Grundzustand<br />
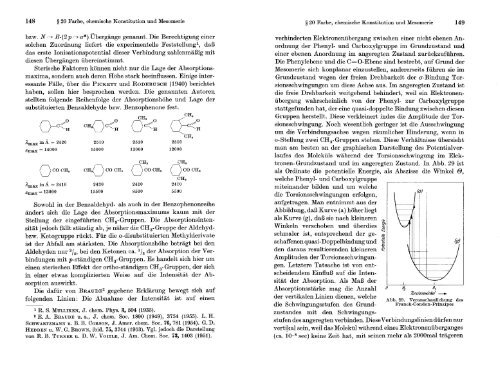
und im angeregten Zustand. In Abb. 29 ist<br />
als Ordinate die potentielle Energie, als Abszisse die Winkel O,<br />
welche Phenyl- und Carboxylgruppe<br />
miteinander bilden und um welche<br />
die Torsionsschwingungen erfolgen,<br />
aufgetragen. Man entnimmt aus der<br />
Abbildung, das Kurve (a) hoher liegt<br />
als Kurve (g), das sie nach kleineren<br />
Winkeln verschoben und uberdies<br />
schmaler ist, entsprechend der geschaffenen<br />
quasi-Doppelbindung und<br />
den daraus resultierenden kleineren<br />
Amplituden der Torsionsschwingungen.<br />
Letztere Tatsache ist von entscheidendem<br />
Einflus auf die Intensitat<br />
der Absomtion. Als Mas der<br />
Absorptionsstarke mag die Anzahl 0 82 - . . ,ff?<br />
-<br />
/ors~onsw/nXe/-<br />
der vertikalen Linien dienen, welche<br />
Abb. 29. Veranschaulichung des<br />
die Schwingungsstufen des Grund- ~ranck-~ondon-~rinzipes<br />
zustandes mit den Schwingungsstufen<br />
des angeregten verbinden. DieseVerbindungslinien durfen nur<br />
vertikal sein, weil das Molekul wahrend eines Elektronenuberganges<br />
(Ca. 10-* sec) keine Zeit hat, mit seinen mehr als 2000mal trageren