liiiMIIIfl~UDliiiMIII~U - Biblioteca de la Universidad Complutense ...
liiiMIIIfl~UDliiiMIII~U - Biblioteca de la Universidad Complutense ...
liiiMIIIfl~UDliiiMIII~U - Biblioteca de la Universidad Complutense ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Capítulo 3<br />
Cítoesqueleto<br />
Estados cetóticos<br />
(l~1ipogluce,raia, 4lnsulina?Olucagón, ¿7)<br />
—st<br />
OA<br />
X~PK<br />
AMP<br />
---.9<br />
A<br />
9<br />
AG<br />
Mitocondria<br />
Discusión General y Conclusiones<br />
Esquema 3<br />
¡ GG<br />
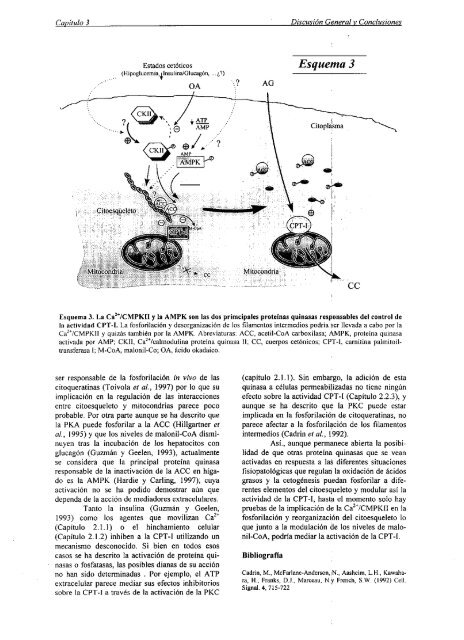
2~/CMPKII y <strong>la</strong> AMPK son <strong>la</strong>s dos primeipales proteínas quinasas responsables <strong>de</strong>l control <strong>de</strong><br />
Esquema <strong>la</strong> actividad 3. La CPT-1. Ca La fosfori<strong>la</strong>ción y <strong>de</strong>sorganización <strong>de</strong> los fi<strong>la</strong>mentos intermedios podría ser llevada a cabo por <strong>la</strong><br />
Ca2t’CMPKII y quizás también por <strong>la</strong> AMPK. Abreviaturas: ACC, acetil-CoA carboxi<strong>la</strong>sa; AMPK, proteína quinasa<br />
activada por AMP; CKJI, Ca2~/calmodulina proteína quinasa II; CC, cuerpos cetónicos; CPT-l, carnitina palmitoilrransferasa<br />
1; M-CoA, malonil-Co; (JA, ácido okadaico.<br />
ser responsable <strong>de</strong> <strong>la</strong> fosfori<strong>la</strong>ción in viyo <strong>de</strong> <strong>la</strong>s<br />
citoqueratinas (Toivo<strong>la</strong> el aL, 1997) por lo que su<br />
implicación en <strong>la</strong> regu<strong>la</strong>ción <strong>de</strong> <strong>la</strong>s interacciones<br />
entre citoesqueleto y mitocondrias parece poco<br />
probable. Por otra parte aunque se ha <strong>de</strong>scrito que<br />
<strong>la</strong> PKA pue<strong>de</strong> fosfori<strong>la</strong>r a <strong>la</strong> ACG (Hillgartner el<br />
aL, 1995) y que los niveles <strong>de</strong> malonil-GoA disminuyen<br />
tras <strong>la</strong> incubación <strong>de</strong> los hepatocitos con<br />
glucagón (Guzmán y Geelen, 1993), actualmente<br />
se consi<strong>de</strong>ra que <strong>la</strong> principal proteína quinasa<br />
responsable <strong>de</strong> <strong>la</strong> inactivacióra <strong>de</strong> <strong>la</strong> ACO era hígado<br />
es <strong>la</strong> AMPK (Hardie y Carling, 1997); cuya<br />
activación no se ha podido <strong>de</strong>mostrar aún que<br />
<strong>de</strong>penda <strong>de</strong> <strong>la</strong> acción <strong>de</strong> mediadores extracelu<strong>la</strong>res.<br />
Tanto <strong>la</strong> insulina (Guzmán y Geelen,<br />
1993) como los agentes que movilizan Ca2~<br />
(Capítulo 2.1.1) o el hinchamiento celu<strong>la</strong>r<br />
(Capítulo 2.1.2) inhiben a <strong>la</strong> CPT-l utilizando un<br />
mecanismo <strong>de</strong>sconocido. Si bien en todos esos<br />
casos se ha <strong>de</strong>scrito <strong>la</strong> activación <strong>de</strong> proteína qui-<br />
- nasas o fosfatasas, <strong>la</strong>s posibles dianas <strong>de</strong> su acción<br />
no han sido <strong>de</strong>terminadas . Por ejemplo, el ATP<br />
extracelu<strong>la</strong>r parece mediar sus efectos inhibitorios<br />
sobre <strong>la</strong> CPT-l a través <strong>de</strong> <strong>la</strong> activación <strong>de</strong> <strong>la</strong> PKC<br />
(capItulo 2.1.1). Sin embargo, <strong>la</strong> adición <strong>de</strong> esta<br />
quinasa a célu<strong>la</strong>s permeabitizadas no tiene ningún<br />
efecto sobre <strong>la</strong> actividad GPT-l (Capitulo 2.2.3), y<br />
aunque se ha <strong>de</strong>scrito que <strong>la</strong> PKC pue<strong>de</strong> estar<br />
implicada en <strong>la</strong> fosfori<strong>la</strong>ción <strong>de</strong> citoqueratinas, no<br />
parece afectar a <strong>la</strong> fosfori<strong>la</strong>ción <strong>de</strong> los fi<strong>la</strong>mentos<br />
intermedios (Gadrin el aL, 1992).<br />
Así., aunque permanece abierta <strong>la</strong> posibilidad<br />
<strong>de</strong> que otras proteína quinasas que se vean<br />
activadas en respuesta a <strong>la</strong>s diferentes situaciones<br />
fisiopatológicas que regu<strong>la</strong>n <strong>la</strong> oxidación <strong>de</strong> ácidos<br />
grasos y <strong>la</strong> cetogénesis puedan fosfori<strong>la</strong>r a diferentes<br />
elementos <strong>de</strong>l citoesqueleto y modu<strong>la</strong>r así <strong>la</strong><br />
actividad <strong>de</strong> <strong>la</strong> GPT-l, hasta el momento solo hay<br />
pruebas <strong>de</strong> <strong>la</strong> implicación <strong>de</strong> <strong>la</strong> Ca2~/CMPK11 en <strong>la</strong><br />
fosfori<strong>la</strong>ción y reorganización <strong>de</strong>l citoesqueleto lo<br />
que junto a <strong>la</strong> modu<strong>la</strong>ción ¿le los niveles <strong>de</strong> malonil-CoA,<br />
podría mediar <strong>la</strong> activación <strong>de</strong> <strong>la</strong> CPT-l.<br />
Bibliografía<br />
Citop<strong>la</strong>sma<br />
Cadrin, M., McFar<strong>la</strong>ne-An<strong>de</strong>rson, N., Aashein,, L.i-1., Kawahara,<br />
H., Franks, Di., Marceau, NS’ French, SM. (1992) Cdl.<br />
Signal. 4, 715-722