Biochemiepraktikum
Biochemiepraktikum
Biochemiepraktikum
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
4<br />
Biochemie Praktikum: Proteinchemie<br />
I. Erstellen einer Eichgerade für eine Proteinbestimmung nach<br />
Bradford:<br />
Um die ermittelten Extinktionswerte einer Proteinkonzentration c zuweisen zu können, muß<br />
eine Eichgerade erstellt werden. Dazu nimmt man eine Rinderserumalbuminlösung (BSA-<br />
Lsg.) bekannter Konzentration (1 mg / ml) und mißt die Extinktionswerte verschiedener<br />
Verdünnungen dieser Lösung. Durch Auftragen der Proteinkonzentrationen gegen die<br />
zugehörigen Extinktionswerte erhält man die Eichgerade.<br />
Die Verdünnungsreihen werden in 1,5ml Eppendorf-Gefäßen („Eppis“) vorbereitet.<br />
Gemessen wird bei 595 nm. Vor Beginn der Messung wird das Spektrometer mit 1 ml<br />
Bradford-Stammlösung + 100 µl H 2 O auf 0 gestellt.<br />
Von den Verdünnungen werden nun jeweils 100µl zu 1ml Bradford-Stammlösung (vorgelegt<br />
in Küvetten) gegeben. Die Küvetten mit Parafilm abdichten, gut vermischen, 10 min<br />
inkubieren und anschließend messen.<br />
Proteinverdünnungen zur Ermittlung der Eichgerade (2 mal unabhängig voneinander ansetzen<br />
und messen):<br />
Konz. c<br />
[µg/ml]<br />
0 10 20 30 40 50 60 70 80 90 100<br />
µl H 2 O 1000 990 980 970 960 950 940 930 920 910 900<br />
µl BSA<br />
(1 mg/ml)<br />
Extinktion<br />
1. Messung<br />
Extinktion<br />
2. Messung<br />
0 10 20 30 40 50 60 70 80 90 100<br />
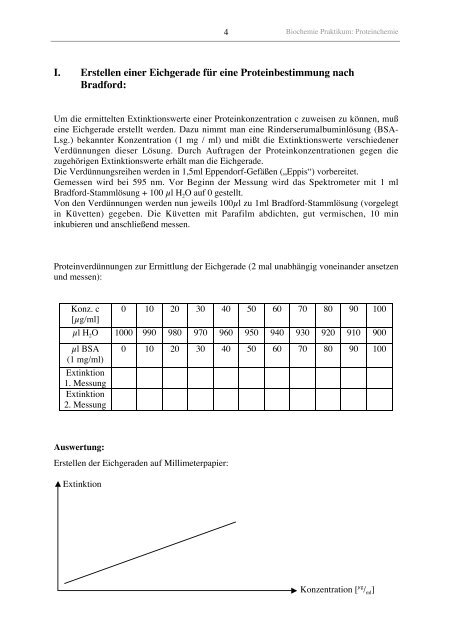
Auswertung:<br />
Erstellen der Eichgeraden auf Millimeterpapier:<br />
Extinktion<br />
Konzentration [ µg / ml ]