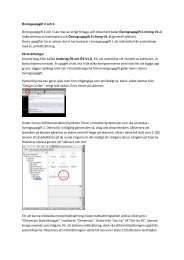
<strong>Kontaktledningsstolpen</strong> <strong>ur</strong> <strong>ett</strong> beständighetsperspektivsom syrediffusionen fortfarande är förhållandevis hög, d<strong>ett</strong>a är fallet då RF är 90-95%. Dessa RF-nivåer är mycket vanliga i svenska utomhuskonstruktioner, d<strong>ett</strong>aoavs<strong>ett</strong> om konstruktionen är direkt exponerad för väta eller ej (Fagerlund 1992,s.55).Rent generellt kan sägas att korrosion är en långsam process vilket normalt innebär attnedbrytningen av stålet upptäcks innan mer allvarliga incidenter, såsom personskadorsamt dödsfall, inträffar. Korrosion medför m.a.o. framförallt negativa ekonomiskakonsekvenser (Broomsfield 1997, s.2).Elektrokemisk korrosionDå <strong>ett</strong> materialprov av järn placeras i vatten, kommer delar av materialet att lösasupp, en oxidation sker vid anodytan (Camitz 1994, s.18). Järnatomerna på ytan går ilösning, under bildning av järnjoner, d<strong>ett</strong>a enligt följande:Fe → Fe2 + +2e−(Brennert 1980, s.67, Broomfield 1997, s.6)För att upprätthålla elektrisk neutralitet måste de två elektronerna konsumeras vilketgörs i reaktion tillsammans med vatten och syre vid katodytan, d<strong>ett</strong>a enligt följande:−2e + H 2 O + 1/2O2→ 2OH−Denna reaktion förstärker betongens alkalinitet runt stålet lokalt och stärker på d<strong>ett</strong>asätt det passiva lagret vid katoden (Broomfield 1997, s.6).Hydroxiden reagerar tillsammans med järnjoner vid anoden enligt nedan:Fe2++ 2OH−→ Fe(OH)2(Broomfield 1997, s.7)Rost har bildats. D<strong>ett</strong>a är den enklaste formeln för järnets korrosion i luftat vattenFe(OH) 2 oxideras vidare av luftens syre till Fe(OH) 3 eller någon annan förening avjärn(ΙΙΙ). Föreningen brukar betecknas Fe 2 O 3 nH 2 O, där n markerar att föreningen haren varierande vattenhalt (Brennert 1980, s.71). För förtydligande av rostbildningsprocessensom beskrivits ovan se fig<strong>ur</strong> 3.1.Fig<strong>ur</strong> 3.1 Rostbildning på järn (Nilsson 2008)45
<strong>Kontaktledningsstolpen</strong> <strong>ur</strong> <strong>ett</strong> beständighetsperspektivReaktionerna som sker vid anoden respektive katoden ger upphov till en elektriskpotentialskillnad mellan ytorna vilken alstrar en elektrisk ström, korrosionsström. H<strong>ur</strong>hög korrosionshastighet som uppnås på anodytan bestäms bl.a. på h<strong>ur</strong> lätt dennakorrosionsström kan flyta i korrosionscellen. Delprocesserna bidrar samtliga tillkorrosionen vilket innebär att om en delprocess avstannar saktar hela korrosionsförloppetned (Camitz 1994, s.18-19).Rosten som blir slutprodukten av korrosionsprocessen upptar en volym som är 2-10gånger större än stålets <strong>ur</strong>sprungliga volym. Vid ingjutet stål ger volymökningenupphov till <strong>ett</strong> tryck mellan stål och betong vilket då det blir tillräckligt stort medförsprickor och avskalning. Många gånger är problemet med korroderat stål just att rostvolymenär högre och inte det faktum att stålet har förlorat i kapacitet (Poukhonto2003, s.110, Fagerlund 1992, s.40, Broomfield 1997, s.7, 25, 36).För att ovanstående reaktioner skall kunna åstadkommas krävs, som redan nämnts, enyta som fungerar som anod och en yta som fungerar som katod, d<strong>ett</strong>a för att åstadkommaen spänningsskillnad och därmed underhålla <strong>ett</strong> flöde. Anodiska ochkatodiska ytor kan förekomma på <strong>ett</strong> och samma metallstycke och där ge upphov tillkorrosionsceller. Det enda som krävs för att <strong>ett</strong> och samma metallstycke skall fungerabåde som anod och katod är att områden i eller intill metallytan på något sätt uppvisarinhomogenitet (Brennert 1980, s.72).Klorider, hög temperat<strong>ur</strong> och lågt pH-värde är samtliga parametrar som främjar järnochaluminiummetallernas korrosion (Brennert 1980, s.74).LuftningscellDå tillgång på syre är en förutsättning för att korrosion skall ske ligger det näratillhands att dra slutsatsen att korrosionen torde ske med högst hastighet där syrekoncentrationenär som störst. Normalt s<strong>ett</strong> är denna slutsats korrekt men undantagfinns (Brennert 1980, s.72).En renslipad järnbit placeras i luftat vatten och en del av materialets yta täcks med <strong>ett</strong>oledande föremål, (så att ingen galvanisk cell istället bildas mellan d<strong>ett</strong>a föremål ochmaterialytan), exempelvis en glasskiva. Innan järnet placeras i lösningen hinner enpassiviserande oxidhinna bildas då järnet är i kontakt med luften. D<strong>ett</strong>a passiverandelager skyddar till en början järnet men förstörs efterhand. På de ställen som skiktetskadas korroderar järnet med följd att syre förbrukas. I området under glasskivan blirsyrekoncentrationen låg då det förbrukade syret ersätts långsamt. Då syret är förbrukatäger framförallt den anodiska reaktionen, Fe = Fe+ + 2e, rum. Anod-2 −lösningen blir svagt s<strong>ur</strong> av korrosionsprodukterna, d.v.s pH-värdet sjunker. P.g.a.d<strong>ett</strong>a faktum kan inte en återbildning av oxidhinnan ske, istället bryts densamma nerförhållandevis hastigt (Brennert 1980, s.72).Utanför glasskivan äger den katodiska reaktionen,+2H+ 12 O2+ 2e = H 2O, rum.−46