PDF Download - Laborwelt
PDF Download - Laborwelt
PDF Download - Laborwelt
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
B L I T Z L I C H T<br />
Correlation G (τ)<br />
Correlation G (τ)<br />
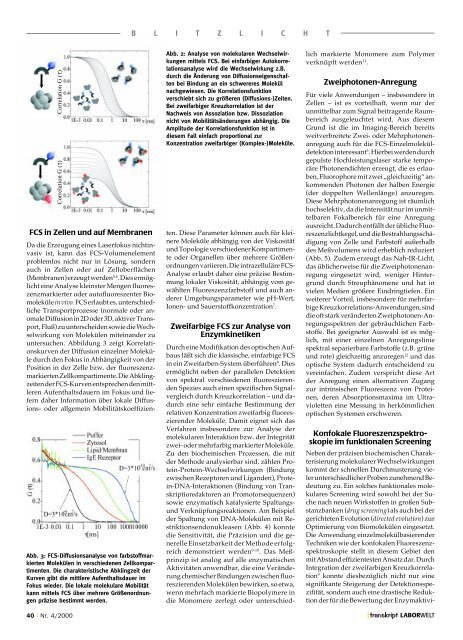
FCS in Zellen und auf Membranen<br />
Abb. 3: FCS-Diffusionsanalyse von farbstoffmarkierten<br />
Molekülen in verschiedenen Zellkompartimenten.<br />
Die charakteristische Abklingzeit der<br />
Kurven gibt die mittlere Aufenthaltsdauer im<br />
Fokus wieder. Die lokale molekulare Mobilität<br />
kann mittels FCS über mehrere Größenordnungen<br />
präzise bestimmt werden.<br />
Abb. 2: Analyse von molekularen Wechselwirkungen<br />
mittels FCS. Bei einfarbiger Autokorrelationsanalyse<br />
wird die Wechselwirkung z.B.<br />
durch die Änderung von Diffusionseigenschaften<br />
bei Bindung an ein schwereres Molekül<br />
nachgewiesen. Die Korrelationsfunktion<br />
verschiebt sich zu größeren (Diffusions-)Zeiten.<br />
Bei zweifarbiger Kreuzkorrelation ist der<br />
Nachweis von Assoziation bzw. Dissoziation<br />
nicht von Mobilitätsänderungen abhängig. Die<br />
Amplitude der Korrelationsfunktion ist in<br />
diesem Fall einfach proportional zur<br />
Konzentration zweifarbiger (Komplex-)Moleküle.<br />
Da die Erzeugung eines Laserfokus nichtinvasiv<br />
ist, kann das FCS-Volumenelement<br />
problemlos nicht nur in Lösung, sondern<br />
auch in Zellen oder auf Zelloberflächen<br />
(Membranen) erzeugt werden 5,6 . Dies ermöglicht<br />
eine Analyse kleinster Mengen fluoreszenzmarkierter<br />
oder autofluoreszenter Biomoleküle<br />
in vivo. FCS erlaubt es, unterschiedliche<br />
Transportprozesse (normale oder anomale<br />
Diffusion in 2D oder 3D, aktiver Transport,<br />
Fluß) zu unterscheiden sowie die Wechselwirkung<br />
von Molekülen miteinander zu<br />
untersuchen. Abbildung 3 zeigt Korrelationskurven<br />
der Diffusion einzelner Moleküle<br />
durch den Fokus in Abhängigkeit von der<br />
Position in der Zelle bzw. der fluoreszenzmarkierten<br />
Zellkompartimente. Die Abklingzeiten<br />
der FCS-Kurven entsprechen den mittleren<br />
Aufenthaltsdauern im Fokus und liefern<br />
daher Information über lokale Diffusions-<br />
oder allgemein Mobilitätskoeffizienten.<br />
Diese Parameter können auch für kleinere<br />
Moleküle abhängig von der Viskosität<br />
und Topologie verschiedener Kompartimente<br />
oder Organellen über mehrere Größenordnungen<br />
variieren. Die intrazelluläre FCS-<br />
Analyse erlaubt daher eine präzise Bestimmung<br />
lokaler Viskosität, abhängig vom gewählten<br />
Fluoreszenzfarbstoff und auch anderer<br />
Umgebungsparameter wie pH-Wert,<br />
Ionen- und Sauerstoffkonzentration 7 .<br />
Zweifarbige FCS zur Analyse von<br />
Enzymkinetiken<br />
Durch eine Modifikation des optischen Aufbaus<br />
läßt sich die klassische, einfarbige FCS<br />
in ein Zweifarben-System überführen 8 . Dies<br />
ermöglicht neben der parallelen Detektion<br />
von spektral verschiedenen fluoreszierenden<br />
Spezies auch einen spezifischen Signalvergleich<br />
durch Kreuzkorrelation – und dadurch<br />
eine sehr einfache Bestimmung der<br />
relativen Konzentration zweifarbig fluoreszierender<br />
Moleküle. Damit eignet sich das<br />
Verfahren insbesondere zur Analyse der<br />
molekularen Interaktion bzw. der Integrität<br />
zwei- oder mehrfarbig markierter Moleküle.<br />
Zu den biochemischen Prozessen, die mit<br />
der Methode analysierbar sind, zählen Protein-Protein-Wechselwirkungen<br />
(Bindung<br />
zwischen Rezeptoren und Liganden), Protein-DNA-Interaktionen<br />
(Bindung von Transkriptionsfaktoren<br />
an Promotorsequenzen)<br />
sowie enzymatisch katalysierte Spaltungsund<br />
Verknüpfungsreaktionen. Am Beispiel<br />
der Spaltung von DNA-Molekülen mit Restriktionsendonukleasen<br />
(Abb. 4) konnte<br />
die Sensitivität, die Präzision und die generelle<br />
Einsetzbarkeit der Methode erfolgreich<br />
demonstriert werden 9-10 . Das Meßprinzip<br />
ist analog auf alle enzymatischen<br />
Aktivitäten anwendbar, die eine Veränderung<br />
chemischer Bindungen zwischen fluoreszierenden<br />
Molekülen bewirken, so etwa,<br />
wenn mehrfach markierte Biopolymere in<br />
die Monomere zerlegt oder unterschiedlich<br />
markierte Monomere zum Polymer<br />
verknüpft werden 11 .<br />
Zweiphotonen-Anregung<br />
Für viele Anwendungen – insbesondere in<br />
Zellen – ist es vorteilhaft, wenn nur der<br />
unmittelbar zum Signal beitragende Raumbereich<br />
ausgeleuchtet wird. Aus diesem<br />
Grund ist die im Imaging-Bereich bereits<br />
weitverbreitete Zwei- oder Mehrphotonenanregung<br />
auch für die FCS-Einzelmoleküldetektion<br />
interessant 5 . Hierbei werden durch<br />
gepulste Hochleistungslaser starke temporäre<br />
Photonendichten erzeugt, die es erlauben,<br />
Fluorophore mit zwei „gleichzeitig“ ankommenden<br />
Photonen der halben Energie<br />
(der doppelten Wellenlänge) anzuregen.<br />
Diese Mehrphotonenanregung ist räumlich<br />
hochselektiv, da die Intensität nur im unmittelbaren<br />
Fokalbereich für eine Anregung<br />
ausreicht. Dadurch entfällt der übliche Fluoreszenzlichtkegel,<br />
und die Bestrahlungsschädigung<br />
von Zelle und Farbstoff außerhalb<br />
des Meßvolumens wird erheblich reduziert<br />
(Abb. 5). Zudem erzeugt das Nah-IR-Licht,<br />
das üblicherweise für die Zweiphotonenanregung<br />
eingesetzt wird, weniger Hintergrund<br />
durch Streuphänomene und hat in<br />
vielen Medien größere Eindringtiefen. Ein<br />
weiterer Vorteil, insbesondere für mehrfarbige<br />
Kreuzkorrelations-Anwendungen, sind<br />
die oft stark veränderten Zweiphotonen-Anregungsspektren<br />
der gebräuchlichen Farbstoffe.<br />
Bei geeigneter Auswahl ist es möglich,<br />
mit einer einzelnen Anregungslinie<br />
spektral separierbare Farbstoffe (z.B. grüne<br />
und rote) gleichzeitig anzuregen 12 und das<br />
optische System dadurch entscheidend zu<br />
vereinfachen. Zudem verspricht diese Art<br />
der Anregung einen alternativen Zugang<br />
zur intrinsischen Fluoreszenz von Proteinen,<br />
deren Absorptionsmaxima im Ultravioletten<br />
eine Messung in herkömmlichen<br />
optischen Systemen erschweren.<br />
Konfokale Fluoreszenzspektroskopie<br />
im funktionalen Screening<br />
Neben der präzisen biochemischen Charakterisierung<br />
molekularer Wechselwirkungen<br />
kommt der schnellen Durchmusterung vieler<br />
unterschiedlicher Proben zunehmend Bedeutung<br />
zu. Ein solches funktionales molekulares<br />
Screening wird sowohl bei der Suche<br />
nach neuen Wirkstoffen in großen Substanzbanken<br />
(drug screening) als auch bei der<br />
gerichteten Evolution (directed evolution) zur<br />
Optimierung von Biomolekülen eingesetzt.<br />
Die Anwendung einzelmolekülbasierender<br />
Techniken wie der konfokalen Fluoreszenzspektroskopie<br />
stellt in diesem Gebiet den<br />
mit Abstand effizientesten Ansatz dar. Durch<br />
Integration der zweifarbigen Kreuzkorrelation<br />
9 konnte diesbezüglich nicht nur eine<br />
signifikante Steigerung der Detektionsspezifität,<br />
sondern auch eine drastische Reduktion<br />
der für die Bewertung der Enzymaktivi-<br />
40 | Nr. 4/2000 |transkript LABORWELT