Das Liebig-Laboratorium Lehramt AC1 neu
Das Liebig-Laboratorium Lehramt AC1 neu
Das Liebig-Laboratorium Lehramt AC1 neu
- TAGS
- lehramt
- www.cup.lmu.de
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
64<br />
Versuch 6.12<br />
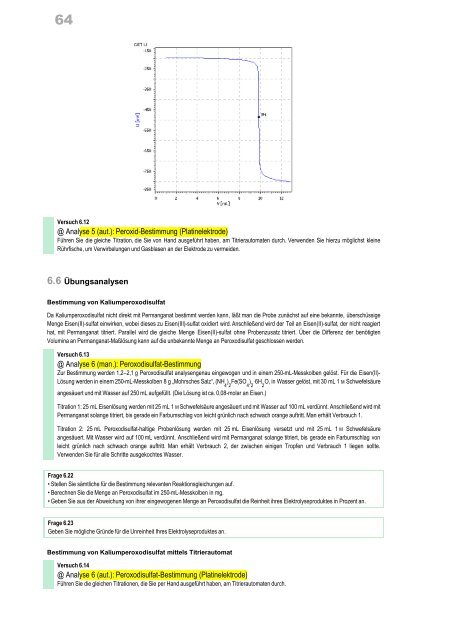
@ Analyse 5 (aut.): Peroxid-Bestimmung (Platinelektrode)<br />
Führen Sie die gleiche Titration, die Sie von Hand ausgeführt haben, am Titrierautomaten durch. Verwenden Sie hierzu möglichst kleine<br />
Rührfische, um Verwirbelungen und Gasblasen an der Elektrode zu vermeiden.<br />
6.6 Übungsanalysen<br />
Bestimmung von Kaliumperoxodisulfat<br />
Da Kaliumperoxodisulfat nicht direkt mit Permanganat bestimmt werden kann, läßt man die Probe zunächst auf eine bekannte, überschüssige<br />
Menge Eisen(II)-sulfat einwirken, wobei dieses zu Eisen(III)-sulfat oxidiert wird. Anschließend wird der Teil an Eisen(II)-sulfat, der nicht reagiert<br />
hat, mit Permanganat titriert. Parallel wird die gleiche Menge Eisen(II)-sulfat ohne Probenzusatz titriert. Über die Differenz der benötigten<br />
Volumina an Permanganat-Maßlösung kann auf die unbekannte Menge an Peroxodisulfat geschlossen werden.<br />
Versuch 6.13<br />
@ Analyse 6 (man.): Peroxodisulfat-Bestimmung<br />
Zur Bestimmung werden 1,2–2,1 g Peroxodisulfat analysengenau eingewogen und in einem 250-mL-Messkolben gelöst. Für die Eisen(II)-<br />
Lösung werden in einem 250-mL-Messkolben 8 g „Mohrsches Salz“, (NH 4 ) 2 Fe(SO 4 ) 2 ·6H 2 O, in Wasser gelöst, mit 30 mL 1 M Schwefelsäure<br />
angesäuert und mit Wasser auf 250 mL aufgefüllt. (Die Lösung ist ca. 0,08-molar an Eisen.)<br />
Titration 1: 25 mL Eisenlösung werden mit 25 mL 1 M Schwefelsäure angesäuert und mit Wasser auf 100 mL verdünnt. Anschließend wird mit<br />
Permanganat solange titriert, bis gerade ein Farbumschlag von leicht grünlich nach schwach orange auftritt. Man erhält Verbrauch 1.<br />
Titration 2: 25 mL Peroxodisulfat-haltige Probenlösung werden mit 25 mL Eisenlösung versetzt und mit 25 mL 1 M Schwefelsäure<br />
angesäuert. Mit Wasser wird auf 100 mL verdünnt. Anschließend wird mit Permanganat solange titriert, bis gerade ein Farbumschlag von<br />
leicht grünlich nach schwach orange auftritt. Man erhält Verbrauch 2, der zwischen einigen Tropfen und Verbrauch 1 liegen sollte.<br />
Verwenden Sie für alle Schritte ausgekochtes Wasser.<br />
Frage 6.22<br />
• Stellen Sie sämtliche für die Bestimmung relevanten Reaktionsgleichungen auf.<br />
• Berechnen Sie die Menge an Peroxodisulfat im 250-mL-Messkolben in mg.<br />
• Geben Sie aus der Abweichung von ihrer eingewogenen Menge an Peroxodisulfat die Reinheit ihres Elektrolyseproduktes in Prozent an.<br />
Frage 6.23<br />
Geben Sie mögliche Gründe für die Unreinheit Ihres Elektrolyseproduktes an.<br />
Bestimmung von Kaliumperoxodisulfat mittels Titrierautomat<br />
Versuch 6.14<br />
@ Analyse 6 (aut.): Peroxodisulfat-Bestimmung (Platinelektrode)<br />
Führen Sie die gleichen Titrationen, die Sie per Hand ausgeführt haben, am Titrierautomaten durch.