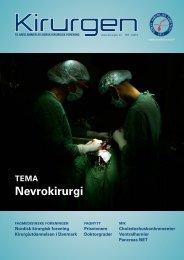
NTLF-Nytt Mikropreparat som viser koagulasjonsnekrose i ablasjonsområdet etter HIFU-behandling. bemerket "ubehag" i behandlingsområdet, 23 % hadde "hudtoksisitet" (smerte og hyperemi i huden over behandlingsområdet), 10 % hadde lokal hevelse av bløtvevet over behandlingsområdet og 10 % hadde forbigående feber. Det var ingen endringer i biokjemiske markører for lever- og nyrefunksjon. Forbigående økning i leverenzymer og bilirubin ble observert hos en liten del av pasientene. Alle pasientene ble utskrevet dagen etter inngrepet. Behandlingsresultater ble kontrollert av MR, kontrastforsterket ultralyd og histologi som bekreftet selektiv ablasjon av levertumorer i alle pasientene. F.Wu et al. analyserte prospektivt 55 pasienter med hepatocellulært karsi<strong>no</strong>m behandlet med HIFU.[31] Studien inkluderte 15 pasienter med stadium II, 16 pasienter stadium IIIA og 24 pasienter med stadium IIIC. Alle pasientene hadde ledsagende levercirrhose. 53 av 55 pasienter hadde tumorstørrelse over 5 cm. Bare fire pasienter ble vurdert til å være resektable, men takket nei til tilbudt leverreseksjon. Prosedyren hadde ingen betydelig bivirkning. Ved CT, MR, og ultralyd kontroll fant man avaskulær og skrumpet destruksjonssone. Man merket fall i nivå av α-fetoprotein hos 89 % av pasientene som hadde preprosedural økte verdier av markøren. I 34 % av pasientene falt α-fetoprotein til <strong>no</strong>rmal nivåer. 53 % av pasientene hadde lett og forbigående økning i leverenzymer etter HIFU. Bivirkninger av behandlingen ble observert hos 24 %. Det var moderat feber hos 2 pasienter, overfladiske brannskader hos 6 pasienter, brannskader av 3. grad hos 1 pasient og forbigående smerter hos 4 pasienter. 6, 12 og 18 må<strong>ned</strong>ers overlevelse var henholdsvis 86 %, 62 % og 35 %. G. Xu et al. behandlet 145 pasienter med hepatocellulært karsi<strong>no</strong>m.[32] Symptomene forbedret seg eller smertene ble mindre hos 85 % av de 145 pasientene og α-fetoprotein i serum falt hos 72 %. Tumorstørrelsen krympet i ulik grad. 2-års overlevelse var 80 % hos pasienter med stadium IB, 51 % i stadium IIA og 47 % i stadium IIIA. Økning av kroppstemperatur og forstyrrelser av hjerterytme var typiske komplikasjoner under prosedyren. Brannskader var mest vanlig komplikasjon i etterkant av prosedyren. K.K. Ng et al. rapporterte resultater ved behandling av 49 pasienter med hepatocellulært karsi<strong>no</strong>m.[33] Median størrelse av de behandlede tumorer var 2,2 cm (0,9-8). Flertallet av pasientene hadde single tumorer (84 %). Kunstig høyre hydrothorax under HIFU behandling ble etablert i 63 % for å redusere mulige skader på lungen og diafragma. Mortaliteten var 2 % og komplikasjoner oppstå i 8 % av tilfellene. HIFUs effektivitet ble oppgitt til 80 %. Den økte fra 67 % i den første serien til 90 % for de siste 28 pasientene. Tumorstørrelse (≥ 3,0 cm) var en signifikant risikofaktor som påvirket fullstendig ablasjonhyppighet. 1-års og 3-års overlevelse var 88 % og 62 %. Det ble konkludert med at HIFU er en effektiv behandlingsmodalitet ved i<strong>no</strong>perabel hepatocellulært karsi<strong>no</strong>m hvor man oppnådde høy effektivitetsrate og god overlevelse. M.Y. Park et al. rapporterte resultater etter behandling av 13 pasienter med metastaser i leveren, 10 fra kolorektal-kreft og 3 fra magekreft.[34] Gjen<strong>no</strong>msnittlig oppfølgingsperiode var 22 og 58 uker henholdsvis. Summen av totale lesjonsstørrelse var i gjen<strong>no</strong>msnitt 8.4 cm og 8.8 cm. Lokale tilbakefall oppstod hos 80 % av pasienter med kolorektale metastaser, mens ingen pasienter utviklet tilbakefall etter HIFU-ablasjon av metastaser fra magekreft. Studien konkluderte at HIFU-behandling av levermetastasene fra tykktarm- og magekreft ser ut å være en trygg prosedyre, men effekten av slik behandling er uklar og videre forskning i dette emnet er nødvendig. Hvis man tar i betraktning at HIFU ble brukt i ganske avanserte stadier av kreftsykdommen i leveren, kan man tolke resultatene fra rapporterte i kliniske studier som gode, de tilsvarer de beste resultatene som ble rapportert for radiofrekvensablasjon og cryoablation.[35;36] Framtid Det viktigste verktøyet for å forbedre metoden er å øke kraften i fokusert ultralyd, <strong>no</strong>e som vil redusere varigheten av prosedyren. Denne faktoren er spesielt viktig for store leversvulster.[28-30] Bruk av ekkokontrastmidler er en annen måte å forkorte prosedyretiden. Disse midlene øker vevets motstand mot ultralydbølger, og dermed øker absorpsjonen av ultralydenergi.[37;38] Dette vil øke arealet (eller redusere tiden) av elementær klasterablasjon. Kombinasjonen av selektiv regional kjemoterapi ved hjelp av thermosensitive lysosomer med HIFU er også et lovende verktøy for å øke effektiviteten av HIFU. En viktig oppgave er å forbedre prosedyreovervåkingen. I denne konteksten kan en ny generasjon av MR-systemer (≥3 Tesla) og temperaturfølsomme magnetiske kontrastmidler spille en viktig rolle.[39] Leveren beveger seg i forhold til respirasjonen, <strong>no</strong>e som gjør det vanskelig å gjen<strong>no</strong>mføre HIFU. Dette problemet kan få en løsning ved utvikling av MR-systemer med feedback.[40;41] Informasjon om endringen av koordinater for det planlagte behandlingspunktet vil bli overført til strålingsproben slik at man igjen kan justere fokuseringen av ultralydenergien. HIFU-ablasjon under kunstig respirasjonspauser er et annet alternativ.[42] Problemet med skjerming av behandlingsområder med ribbein kan også løses av feedback-systemet. Det kan korrigeres på softwarenivå ved å justere opp eller <strong>ned</strong> intensiteten av de enkelte utstrålende elementene for å redusere risikoen for forbrenninger på grunn av ribbeinsabsorpsjon av ultralydenergi og for å samtidig skaffe tilstrekkelig energikompensasjon for tap av energi på grunn av ribbeinsskjerming.[43;44] Det er lite kjent om HIFUs virkning i områder i umiddelbar nærhet til store blodkar (v. porta, <strong>ned</strong>re kaval-vene).[45] Siden det er nødvendig å ta i betraktning kjølingsrollen av de store blodkarene, er det spesielt vanskelig i dette tilfellet å beregne intensitet av fokusert ultralydenergi og å velge behandlingsregime av elementære klasterablasjoner.[46] Det er ingen tvil om at HIFU-teknikken vil finne sin plass i behandling av både primær og metastatiske leversvulster. Med mål av integrert vurdering og forbedring av HIFU trenger man samarbeid mellom kirurger, onkologer, patologer, histologer, radiologer, fysikere i tillegg til rent instrumentelle og tekniske forbedringer. De fleste eksperimentelle studier innen HIFU av leveren har nativ lever som behandlingsmodell. Det er også viktig å drive eksperimentell forskning med ablasjon av eksperimentelle leversvulster.[47;48] Ferdigstillelse av resultater for langtidsoverlevelse vil bidra til en mer nøyaktig vurdering av rollen til ekstrakorporal HIFU i behandling av leversvulster. Godt etablerte rutiner for postprosedural oppfølging er avgjørende i denne sammenhengen • Referanser 1. Padma, S., Martinie, J. B., and Iannitti, D. A. Liver tumor ablation: percutaneous and open approaches. J Surg Oncol. 100:619-634, 2009. 2. Wood, R. W., and Loomis, L. The physical and biological effects of high frequency sound waves of great intensity. Phil Mag. 4:417-436, 1927. 3. FRY, W. J., MOSBERG, W. H., Jr., BARNARD, J. W., and FRY, F. J. Production of focal destructive lesions in the central nervous system with ultrasound. J Neurosurg. 11:471-478, 1954. 4. ter Haar, G. R. High intensity focused ultrasound for the treatment of tumors. Echocardiography. 18:317-322, 2001. 5. Leslie, T. A., Ken<strong>ned</strong>y, J. E., Illing, R. O., ter Haar, G. R., Wu, F., Phillips, R. R., Friend, P. J., Roberts, I. S., Cranston, D. W., and Middleton, M. R. High-intensity 140 <strong>Kirurgen</strong> nr. 2, <strong>2012</strong>
focused ultrasound ablation of liver tumours: can radiological assessment predict the histological response? Br. J Radiol. 81:564-571, 2008. 6. Hill, C. R., Rivens, I., Vaughan, M. G., and ter Haar, G. R. Lesion development in focused ultrasound surgery: a general model. Ultrasound Med. Biol. 20:259-269, 1994. 7. Maris, H., and Balibar, S. Negative pressures and cavitation in liquid helium. Physics Today 53:29-32, 2000. 8. Mouge<strong>no</strong>t, C., Salomir, R., Palussiere, J., Grenier, N., and Moonen, C. T. Automatic spatial and temporal temperature control for MR-guided focused ultrasound using fast 3D MR thermometry and multispiral trajectory of the focal point. Magn Reson. Med. 52:1005-1015, 2004. 9. Souchon, R., Bouchoux, G., Maciejko, E., Lafon, C., Cathig<strong>no</strong>l, D., Bertrand, M., and Chapelon, J. Y. Monitoring the formation of thermal lesions with heat-induced echo-strain imaging: a feasibility study. Ultrasound Med. Biol. 31:251-259, 2005. 10. Hynynen, K., Pomeroy, O., Smith, D. N., Huber, P. E., McDan<strong>no</strong>ld, N. J., Kettenbach, J., Baum, J., Singer, S., and Jolesz, F. A. MR imaging-guided focused ultrasound surgery of fibroade<strong>no</strong>mas in the breast: a feasibility study. Radiology 219:176-185, 2001. 11. www.insightec.com. <strong>2012</strong>. 12. www.healthcare.philips.com/main/shared/assets/ multimedia/imaging20/pdfs/MR_Sonalleve_HIFU_ whitepaper.pdf. <strong>2012</strong>. 13. www.utlltd.co.uk/index.php?option=com_content&task =view&id=66&Itemid=106. <strong>2012</strong>. 14. Zderic, V., Keshavarzi, A., Andrew, M. A., Vaezy, S., and Martin, R. W. Attenuation of porcine tissues in vivo after high-intensity ultrasound treatment. Ultrasound Med. Biol. 30:61-66, 2004. 15. Gig<strong>no</strong>ux, B. M., Scoazec, J. Y., Curiel, L., Beziat, C., and Chapelon, J. Y. [High intensity focused ultrasonic destruction of hepatic parenchyma]. Ann. Chir 128:18- 25, 2003. 16. Oosterhof, G. O., Cornel, E. B., Smits, G. A., Debruyne, F. M., and Schalken, J. A. Influence of high-intensity focused ultrasound on the development of metastases. Eur. Urol. 32:91-95, 1997. 17. Stewart, E. A., Gedroyc, W. M., Tempany, C. M., Quade, B. J., Inbar, Y., Ehrenstein, T., Shushan, A., Hindley, J. T., Goldin, R. D., David, M., Sklair, M., and Rabi<strong>no</strong>vici, J. Focused ultrasound treatment of uterine fibroid tumors: safety and feasibility of a <strong>no</strong>ninvasive thermoablative technique. Am. J Obstet. Gynecol 189:48-54, 2003. 18. Wu, F., Wang, Z. B., Chen, W. Z., Zou, J. Z., Bai, J., Zhu, H., Li, K. Q., Xie, F. L., Jin, C. B., Su, H. B., and Gao, G. W. Extracorporeal focused ultrasound surgery for treatment of human solid carci<strong>no</strong>mas: early Chinese clinical experience. Ultrasound Med. Biol. 30:245-260, 2004. 19. Li, J. J., Xu, G. L., Gu, M. F., Luo, G. Y., Rong, Z., Wu, P. H., and Xia, J. C. Complications of high intensity focused ultrasound in patients with recurrent and metastatic abdominal tumors. World J Gastroenterol. 13:2747-2751, 2007. 20. Luo, W., Zhou, X., Gong, X., Zheng, M., Zhang, J., and Guo, X. Study of sequential histopathologic changes, apoptosis, and cell proliferation in rabbit livers after high-intensity focused ultrasound ablation. J Ultrasound Med. 26:477-485, 2007. 21. Auboiroux, V., Viallon, M., Roland, J., Hyacinthe, J. N., Petrusca, L., Morel, D. R., Goget, T., Terraz, S., Gross, P., Becker, C. D., and Salomir, R. ARFI-prepared MRgHIFU in liver: Simultaneous mapping of ARFI-displacement and temperature elevation, using a fast GRE-EPI sequence. Magn Reson. Med. <strong>2012</strong>. 22. Choi, M. J., Guntur, S. R., Lee, J. M., Paeng, D. G., Lee, K. I., and Coleman, A. Changes in ultrasonic properties of liver tissue in vitro during heating-cooling cycle concomitant with thermal coagulation. Ultrasound Med. Biol. 37:2000-<strong>2012</strong>, 2011. 23. Holbrook, A. B., Gha<strong>no</strong>uni, P., Santos, J. M., Medan, Y., and Butts, P. K. In vivo MR acoustic radiation force imaging in the porcine liver. Med. Phys. 38:5081-5089, 2011. 24. Quesson, B., Laurent, C., Maclair, G., de Senneville, B. D., Mouge<strong>no</strong>t, C., Ries, M., Carteret, T., Rullier, A., and Moonen, C. T. Real-time volumetric MRI thermometry of focused ultrasound ablation in vivo: a feasibility study in pig liver and kidney. NMR Biomed. 24:145-153, 2011. 25. Che<strong>no</strong>t, J., Melodelima, D., N'Djin, W. A., Souchon, R., Rivoire, M., and Chapelon, J. Y. Intra-operative ultrasound hand-held strain imaging for the visualization of ablations produced in the liver with a toroidal HIFU transducer: first in vivo results. Phys. Med. Biol. 55:3131-3144, 2010. 26. Parmentier, H., Melodelima, D., N'Djin, A., Chesnais, S., Chapelon, J. Y., and Rivoire, M. High-intensity focused ultrasound ablation for the treatment of colorectal liver metastases during an open procedure: study on the pig. Ann. Surg. 249:129-136, 2009. 27. Wu, F., Chen, W. Z., Bai, J., Zou, J. Z., Wang, Z. L., Zhu, H., and Wang, Z. B. Pathological changes in human malignant carci<strong>no</strong>ma treated with high-intensity focused ultrasound. Ultrasound Med. Biol. 27:1099- 1106, 2001. 28. Wu, F., Wang, Z. B., Chen, W. Z., Zou, J. Z., Bai, J., Zhu, H., Li, K. Q., Jin, C. B., Xie, F. L., and Su, H. B. Advanced hepatocellular carci<strong>no</strong>ma: treatment with highintensity focused ultrasound ablation combi<strong>ned</strong> with transcatheter arterial embolization. Radiology 235:659- 667, 2005. 29. Li, C. X., Xu, G. L., Jiang, Z. Y., Li, J. J., Luo, G. Y., Shan, H. B., Zhang, R., and Li, Y. Analysis of clinical effect of high-intensity focused ultrasound on liver cancer. World J Gastroenterol. 10:2201-2204, 2004. 30. Illing, R. O., Ken<strong>ned</strong>y, J. E., Wu, F., ter Haar, G. R., Protheroe, A. S., Friend, P. J., Gleeson, F. V., Cranston, D. W., Phillips, R. R., and Middleton, M. R. The safety and feasibility of extracorporeal high-intensity focused ultrasound (HIFU) for the treatment of liver and kidney tumours in a Western population. Br. J Cancer 93:890- 895, 2005. 31. Wu, F., Wang, Z. B., Chen, W. Z., Zhu, H., Bai, J., Zou, J. Z., Li, K. Q., Jin, C. B., Xie, F. L., and Su, H. B. Extracorporeal high intensity focused ultrasound ablation in the treatment of patients with large hepatocellular carci<strong>no</strong>ma. Ann. Surg Oncol. 11:1061- 1069, 2004. 32. Xu, G., Luo, G., He, L., Li, J., Shan, H., Zhang, R., Li, Y., Gao, X., Lin, S., and Wang, G. Follow-up of highintensity focused ultrasound treatment for patients with hepatocellular carci<strong>no</strong>ma. Ultrasound Med. Biol. 37:1993-1999, 2011. 33. Ng, K. K., Poon, R. T., Chan, S. C., Chok, K. S., Cheung, T. T., Tung, H., Chu, F., Tso, W. K., Yu, W. C., Lo, C. M., and Fan, S. T. High-intensity focused ultrasound for hepatocellular carci<strong>no</strong>ma: a single-center experience. Ann. Surg 253:981-987, 2011. 34. Park, M. Y., Jung, S. E., Cho, S. H., Piao, X. H., Hahn, S. T., Han, J. Y., and Woo, I. S. Preliminary experience using high intensity focused ultrasound for treating liver metastasis from colon and stomach cancer. Int. J. Hyperthermia 25:180-188, 2009. 35. Hansler, J., Frieser, M., Tietz, V., Uhlke, D., Wissniowski, T. T., Bernatik, T., Hahn, E. G., and Strobel, D. Percutaneous ultrasound-guided radiofrequency ablation (RFA) using saline-perfused (wet) needle electrodes for the treatment of hepatocellular carci<strong>no</strong>ma--long term experience. Ultraschall Med. 28:604-611, 2007. 36. Adam, R., Hagopian, E. J., Linhares, M., Krissat, J., Savier, E., Azoulay, D., Kunstlinger, F., Castaing, D., and Bismuth, H. A comparison of percutaneous cryosurgery and percutaneous radiofrequency for unresectable hepatic malignancies. Arch. Surg 137:1332-1339, 2002. 37. Luo, W., Zhou, X., Ren, X., Zheng, M., Zhang, J., and He, G. Enhancing effects of So<strong>no</strong>Vue, a microbubble so<strong>no</strong>graphic contrast agent, on high-intensity focused ultrasound ablation in rabbit livers in vivo. J Ultrasound Med. 26:469-476, 2007. 38. Chung, D. J., Cho, S. H., Lee, J. M., and Hahn, S. T. Effect of microbubble contrast agent during high intensity focused ultrasound ablation on rabbit liver in vivo. Eur. J. Radiol. 81:e519-e523, <strong>2012</strong>. 39. Mulder, W. J., Strijkers, G. J., van Tilborg, G. A., Griffioen, A. W., and Nicolay, K. Lipid-based na<strong>no</strong>particles for contrast-enhanced MRI and molecular imaging. NMR Biomed. 19:142-164, 2006. 40. Tanter, M., Per<strong>no</strong>t, M., Aubry, J. F., Montaldo, G., Marquet, F., and Fink, M. Compensating for bone interfaces and respiratory motion in high-intensity focused ultrasound. Int. J Hyperthermia 23:141-151, 2007. 41. Rijkhorst, E. J., Rivens, I., Haar, G., Hawkes, D., and Barratt, D. Effects of respiratory liver motion on heating for gated and model-based motion-compensated high-intensity focused ultrasound ablation. Med. Image Comput. Comput. Assist. Interv. 14:605-612, 2011. 42. Courivaud, F., Kazaryan, A. M., Lund, A., Halvorsen, P. S., Edwin, B., and Hol, P. K. In-Vivo MR Guided High Intensity Focused Ultrasound Ablation of Pig Liver Tissues: Preliminary Results of a Survival Study. Proceedings of the19th Annual Meeting of the International Society for Magnetic Resonance in Medicine, 7-13 May 2011, Montreal, Canada: 1740 2011. 43. Civale, J., Clarke, R., Rivens, I., and ter, H. G. The use of a segmented transducer for rib sparing in HIFU treatments. Ultrasound Med. Biol. 32:1753-1761, 2006. 44. Quesson, B., Merle, M., Kohler, M. O., Mouge<strong>no</strong>t, C., Roujol, S., de Senneville, B. D., and Moonen, C. T. A method for MRI guidance of intercostal high intensity focused ultrasound ablation in the liver. Med. Phys. 37:2533-2540, 2010. 45. Gao, Y., Gao, S., Zhao, B., Zhao, Y., Hua, X., Tan, K., and Liu, Z. Vascular effects of microbubble-enhanced, pulsed, focused ultrasound on liver blood perfusion. Ultrasound Med. Biol. 38:91-98, <strong>2012</strong>. 46. Frich, L., Hol, P. K., Roy, S., Mala, T., Edwin, B., Clausen, O. P., and Gladhaug, I. P. Experimental hepatic radiofrequency ablation using wet electrodes: electrode-to-vessel distance is a significant predictor for delayed portal vein thrombosis. Eur. Radiol. 16:1990-1999, 2006. 47. Sasaki, K., Medan, M. S., Azuma, T., Kawabata, K., Shimoda, M., and Umemura, S. Effect of echo-guided high-intensity focused ultrasound ablation on localized experimental tumors. J Vet. Med. Sci. 68:1069-1074, 2006. 48. Luo, W., Zhou, X., Yu, M., He, G., Zheng, X., Li, Q., Liu, Q., Han, Z., Zhang, J., and Qian, Y. Ablation of highintensity focused ultrasound assisted with So<strong>no</strong>Vue on Rabbit VX2 liver tumors: sequential findings with histopathology, immu<strong>no</strong>histochemistry, and enzyme histochemistry. Ann. Surg. Oncol. 16:2359-2368, 2009. Studie om simulatortrening ved single-port kirurgi i gang Single port kirurgi er en teknikk som de siste årene har blitt tatt i bruk ved flere kirurgiske inngrep [1, 2]. Single-port kirurgi, med kun et snitt i buken, stiller operatøren ovenfor nye utfordringer under inngrep. Til tross for spesielle instrumenter, som enten er krysset eller kurvede, er det lettere å oppnå kollisjoner mellom instrumentene. For å sikre en god innføring av nye teknikker er det viktig at operatøren er forberedt før han eller hun starter opp med slik kirurgi. Dette kan for eksempel gjøres ved å trene ved hjelp av virtual reality (VR) simulatorer. SimSurgery introduserte nylig en modul for å trene på single-port på sin SEP-simulator. For å studere effekten av trening på denne modulen ønsker vi å gjen<strong>no</strong>mføre en multisenter studie med deltakelse fra Oslo universitetssykehus, Akershus universitetssykehus og St. Olavs Hospital. Deltagerne i studien vil bli randomisert til enten en kontroll gruppe eller en gruppe som mottar simulatortrening. Treningen vil være distribuert [3], det vil si foregå over flere treningsøkter spredt ut over tid, og deltagerne vil trene til et gitt nivå (criterion-based) [4] basert på det kirurger med erfaring i single port kirurgi presterer. Studiegruppen består av Arne Rosseland (OUS), Anders Debes (AHUS), Ronald Mårvik (St. Olavs Hospital) og ledes av Cecilie Våpenstad (SINTEF). Referanser 1. Lirici MM (<strong>2012</strong>) Single site laparoscopic surgery: An intermediate step toward <strong>no</strong> (visible) scar surgery or the next gold standard in minimally invasive surgery? Minim Invasive Ther Allied Tech<strong>no</strong>l 21: 1-7 2. Ahmed K, Wang TT, Patel VM, Nagpal K, Clark J, Ali M, Deeba S, Ashrafian H, Darzi A, Athanasiou T, Paraskeva P (2011) The role of single-incision laparoscopic surgery in abdominal and pelvic surgery: a systematic review. Surgical endoscopy 25: 378-396 3. Verdaasdonk EG, Stassen LP, van Wijk RP, Dankelman J (2007) The influence of different training schedules on the learning of psychomotor skills for endoscopic surgery. Surg Endosc 21: 214-219 4. Brinkman WM, Buzink SN, Alevizos L, de Hingh IH, Jakimowicz JJ (<strong>2012</strong>) Criterion-based laparoscopic training reduces total training time. Surgical endoscopy 26: 1095-1101 NTLF-Nytt <strong>Kirurgen</strong> nr. 2, <strong>2012</strong> 141