CAPÍTULO 5. Termodinámica - Biblioteca
CAPÍTULO 5. Termodinámica - Biblioteca
CAPÍTULO 5. Termodinámica - Biblioteca
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Calor y <strong>Termodinámica</strong> Hugo Medina Guzmán<br />
5<br />
−6<br />
p1V<br />
1 1,<br />
013×<br />
10 × 113×<br />
10<br />
T 1 = =<br />
= 689 K<br />
. 3<br />
nR 2,<br />
00 × 10 × 8,<br />
31<br />
20,<br />
9<br />
C p<br />
C p<br />
c)<br />
−3<br />
= 2,<br />
00 × 10 C ( 689 − 384)<br />
20,<br />
9×<br />
10<br />
=<br />
2×<br />
305<br />
20.<br />
9×<br />
10<br />
=<br />
2×<br />
305<br />
CV p<br />
C V<br />
3<br />
3<br />
= C − R ⇒<br />
= 34 , 3 − 8,<br />
31 =<br />
p<br />
J<br />
= 34,<br />
3<br />
mol K<br />
J<br />
= 34,<br />
3<br />
mol K<br />
J<br />
26<br />
mol<br />
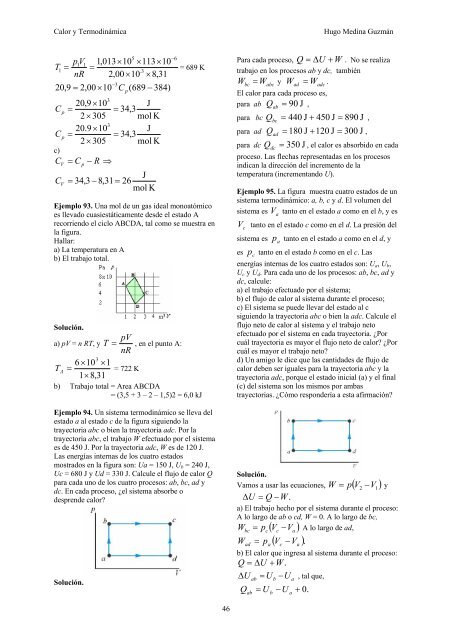
Ejemplo 93. Una mol de un gas ideal monoatómico<br />
es llevado cuasiestáticamente desde el estado A<br />
recorriendo el ciclo ABCDA, tal como se muestra en<br />
la figura.<br />
Hallar:<br />
a) La temperatura en A<br />
b) El trabajo total.<br />
Solución.<br />
pV<br />
a) pV = n RT, y T = , en el punto A:<br />
nR<br />
3<br />
6 × 10 × 1<br />
T A =<br />
= 722 K<br />
1×<br />
8,<br />
31<br />
b) Trabajo total = Area ABCDA<br />
= (3,5 + 3 – 2 – 1,5)2 = 6,0 kJ<br />
Ejemplo 94. Un sistema termodinámico se lleva del<br />
estado a al estado c de la figura siguiendo la<br />
trayectoria abc o bien la trayectoria adc. Por la<br />
trayectoria abc, el trabajo W efectuado por el sistema<br />
es de 450 J. Por la trayectoria adc, W es de 120 J.<br />
Las energías internas de los cuatro estados<br />
mostrados en la figura son: Ua = 150 J, Ub = 240 J,<br />
Uc = 680 J y Ud = 330 J. Calcule el flujo de calor Q<br />
para cada uno de los cuatro procesos: ab, bc, ad y<br />
dc. En cada proceso, ¿el sistema absorbe o<br />
desprende calor?<br />
Solución.<br />
K<br />
46<br />
Para cada proceso, Q = ΔU<br />
+ W . No se realiza<br />
trabajo en los procesos ab y dc, también<br />
W bc = Wabc<br />
y W ad = Wadc<br />
.<br />
El calor para cada proceso es,<br />
para ab Q ab = 90 J ,<br />
para bc Q bc = 440 J + 450 J = 890 J ,<br />
para ad Q ad = 180 J + 120 J = 300 J ,<br />
para dc Q dc = 350 J , el calor es absorbido en cada<br />
proceso. Las flechas representadas en los procesos<br />
indican la dirección del incremento de la<br />
temperatura (incrementando U).<br />
Ejemplo 9<strong>5.</strong> La figura muestra cuatro estados de un<br />
sistema termodinámico: a, b, c y d. El volumen del<br />
sistema es V a tanto en el estado a como en el b, y es<br />
V c tanto en el estado c como en el d. La presión del<br />
sistema es p a tanto en el estado a como en el d, y<br />
es p c tanto en el estado b como en el c. Las<br />
energías internas de los cuatro estados son: Ua, Ub,<br />
Uc y Ud. Para cada uno de los procesos: ab, bc, ad y<br />
dc, calcule:<br />
a) el trabajo efectuado por el sistema;<br />
b) el flujo de calor al sistema durante el proceso;<br />
c) El sistema se puede llevar del estado al c<br />
siguiendo la trayectoria abc o bien la adc. Calcule el<br />
flujo neto de calor al sistema y el trabajo neto<br />
efectuado por el sistema en cada trayectoria. ¿Por<br />
cuál trayectoria es mayor el flujo neto de calor? ¿Por<br />
cuál es mayor el trabajo neto?<br />
d) Un amigo le dice que las cantidades de flujo de<br />
calor deben ser iguales para la trayectoria abc y la<br />
trayectoria adc, porque el estado inicial (a) y el final<br />
(c) del sistema son los mismos por ambas<br />
trayectorias. ¿Cómo respondería a esta afirmación?<br />
Solución.<br />
Vamos a usar las ecuaciones, ( 2 1)<br />
V V p W = − y<br />
Δ U = Q −W<br />
.<br />
a) El trabajo hecho por el sistema durante el proceso:<br />
A lo largo de ab o cd, W = 0. A lo largo de bc,<br />
Wbc = pc<br />
( Vc<br />
−Va<br />
) A lo largo de ad,<br />
Wad = pa<br />
( Vc<br />
−Va<br />
).<br />
b) El calor que ingresa al sistema durante el proceso:<br />
Q = ΔU<br />
+ W.<br />
Δ U = U −U<br />
, tal que,<br />
Q<br />
ab b a<br />
ab = U b −U<br />
a<br />
+<br />
0.