Modalităţi de optimizare a formelor farmaceutice cu antiinflamatoare
Modalităţi de optimizare a formelor farmaceutice cu antiinflamatoare
Modalităţi de optimizare a formelor farmaceutice cu antiinflamatoare
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Permeabilitatea medicamentului din sistemele preparate în compartimentul donator prin intermediul<br />
unei membrane semipermeabile, implică trei procese conse<strong>cu</strong>tive mai întâi dizolvarea parti<strong>cu</strong>lelor soli<strong>de</strong><br />
dispersate, apoi difuzia medicamentului <strong>de</strong>-a lungul mediului <strong>de</strong> dizolvare sau umflarea matriţei polimerice<br />
şi, în final permeabilitatea sa prin membrană. Toate cele trei procese contribuie la viteza <strong>de</strong> difuziune.<br />
Rezultatele arată că, complexarea creşte difuzia piroxicamului prin creşterea cantităţii <strong>de</strong> specii difuzabile în<br />
faza donatoare, prin mărirea solubilităţii medicamentului. Totuşi complexul nu a putut penetra (piroxicamul<br />
în complex a fost în echilibru dinamic rapid <strong>cu</strong> piroxicamul liber), formând continuu mole<strong>cu</strong>lele <strong>de</strong> piroxicam<br />
în formă difuzabilă către membrană. De aceea, complexarea <strong>cu</strong> ciclo<strong>de</strong>xtrină creşte gradul concentraţiei<br />
piroxicamului peste membrană, ceea ce duce la o creştere a coeficientului <strong>de</strong> difuziune pentru piroxicam<br />
(tabel XVI). Prezenţa unei faze soli<strong>de</strong> în sistem (dispersia medicamentului/complex în apă sau gel), asigură o<br />
activitate termodinamică mare, constantă, a piroxicamului la suprafaţa membranei, înlo<strong>cu</strong>ind mole<strong>cu</strong>lele <strong>de</strong><br />
piroxicam pierdute datorită difuziei <strong>de</strong>-a lungul membranei semipermeabile, <strong>cu</strong> dizolvarea fazei soli<strong>de</strong>.<br />
Ciclo<strong>de</strong>xtrina solubilizează medicamentele lipofile în vehi<strong>cu</strong>lul apos şi conduce mole<strong>cu</strong>lele <strong>de</strong> medicament la<br />
suprafaţa <strong>de</strong> barieră un<strong>de</strong> apar disocieri ale complecşilor şi permeabilitatea medicamentului <strong>de</strong>-a lungul<br />
membranei semipermeabile.<br />
Prezenţa HPMC în geluri întârzie cedarea <strong>de</strong> piroxicam comparativ <strong>cu</strong> datele permeabilităţii piroxicamului<br />
din suspensiile apoase. Acest efect <strong>de</strong> întârziere poate fi explicat prin difuzia lentă a piroxicamului<br />
<strong>de</strong>-a lungul stratului matriţei <strong>de</strong> HPMC. HPMC umflată, controlează difuzia piroxicamului şi, în cosecinţă,<br />
cedarea sa. O difuziune mai mică a piroxicamului <strong>de</strong>-a lungul matriţei HPMC, a fost etapa limitantă a vitezei<br />
în procesul general <strong>de</strong> difuziune.<br />
Valorile constante ale stabilităţii pentru β-CD şi complecşi PX-RAMEB au fost diferite. RAMEB<br />
s-a dovedit a avea proprietăţi mai bune <strong>de</strong> solubilizare şi <strong>de</strong> complexare pentru piroxicam <strong>de</strong>cât β-CD, aşa<br />
<strong>cu</strong>m s-a putut <strong>de</strong>duce din valorile constantei <strong>de</strong> stabilitate mari, obţinute pentru complecşi. Proprietăţile mai<br />
bune <strong>de</strong> complexare ale RAMEB nu au afectat semnificativ difuzabilitatea piroxicamului din apă. Valorile<br />
coeficientului <strong>de</strong> difuziune pentru ambele ciclo<strong>de</strong>xtrine au fost aproape la fel. Ele au diferit doar în cazul<br />
permeabilităţii medicamentului din gelurile <strong>de</strong> HPMC.<br />
Un număr <strong>de</strong> lucrări [201, 205] au dis<strong>cu</strong>tat <strong>de</strong>spre influenţa vâscozităţii formulărilor asupra cedării<br />
medicamentului din formulări locale, <strong>de</strong>monstrând că o creştere a vâscozităţii va scă<strong>de</strong>a rata <strong>de</strong> cedare a<br />
medicamentului. Vâscozitatea e o proprietate fizică, care, la nivel mole<strong>cu</strong>lar, poate fi redusă la termenul unei<br />
viteze cres<strong>cu</strong>te a difuziei prin gel, ca o consecinţă a conţinutului redus <strong>de</strong> solvent.<br />
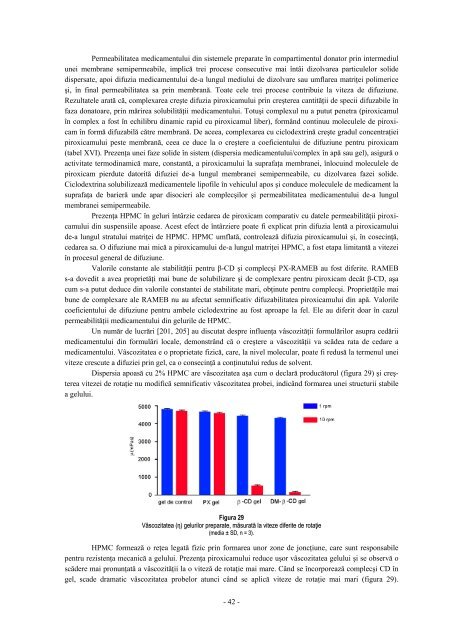
Dispersia apoasă <strong>cu</strong> 2% HPMC are vâscozitatea aşa <strong>cu</strong>m o <strong>de</strong>clară producătorul (figura 29) şi creşterea<br />
vitezei <strong>de</strong> rotaţie nu modifică semnificativ vâscozitatea probei, indicând formarea unei structurii stabile<br />
a gelului.<br />
Figura 29<br />
Vâscozitatea (η) gelurilor preparate, măsurată la viteze diferite <strong>de</strong> rotaţie<br />
(media ± SD, n = 3).<br />
HPMC formează o reţea legată fizic prin formarea unor zone <strong>de</strong> joncţiune, care sunt responsabile<br />
pentru rezistenţa mecanică a gelului. Prezenţa piroxicamului reduce uşor vâscozitatea gelului şi se observă o<br />
scă<strong>de</strong>re mai pronunţată a vâscozităţii la o viteză <strong>de</strong> rotaţie mai mare. Când se încorporează complecşi CD în<br />
gel, sca<strong>de</strong> dramatic vâscozitatea probelor atunci când se aplică viteze <strong>de</strong> rotaţie mai mari (figura 29).<br />
- 42 -