1208 FARMACIA HOSPITALARIAciente para justificar su utilización en pacientes confactores <strong>de</strong> riesgo cardiacos o enfermedad cardiacasubyacente. Los pacientes que reciben <strong>de</strong>xrazoxano<strong>de</strong>ben seguir siendo monitorizados para prevenir la toxicidadcardiaca.La amifostina es un profármaco que forma complejoscon los <strong>de</strong>rivados reactivos <strong>de</strong> cisplatino y <strong>de</strong>agentes alquilantes. Las fosfatasas alcalinas <strong>de</strong> la membranacitoplásmica facilitan su conversión a la formaactiva (143) . Según los ensayos <strong>de</strong> fase I su dosis óptima sesitúa entre 740 y 910 mg/m 2 , pero esta última producehipotensión y vómitos, por lo que se requiere un a<strong>de</strong>cuadahidratación y el uso <strong>de</strong> antieméticos (144,145) .Suefecto hipotensor pue<strong>de</strong> ser combatido por la adición<strong>de</strong> efedrina (146) o suspendiendo los fármacos hipotensores24 h antes <strong>de</strong> su administración. La amifostinaestá indicada para la reducción <strong>de</strong> la nefrotoxicidad enpacientes que reciben quimioterapia basada en el cisplatino.A pesar <strong>de</strong> su indicación en la reducción <strong>de</strong> laneutropenia en pacientes tratados con agentes alquilantes,<strong>de</strong>be seguir consi<strong>de</strong>rándose la reducción <strong>de</strong> dosiso el empleo <strong>de</strong> factores <strong>de</strong> crecimiento hemopoyéticocomo tratamientos alternativos a la amifostina. Lainformación actual es insuficiente para recomendar eluso <strong>de</strong> la amifostina para evitar la trombocitopenia o laneurotoxicidad y ototoxicidad <strong>de</strong>l cisplatino. Del mismomodo, también hay información insuficiente <strong>de</strong> suuso en la prevención <strong>de</strong> la neurotoxicidad asociada apaclitaxel. En cambio, la amifostina sí ha sido aprobadapara reducir la inci<strong>de</strong>ncia <strong>de</strong> xerostomía aguda y retardadaen pacientes con tumores <strong>de</strong> cabeza y cuellosometidos a irradiación fraccionada, pero disponemos<strong>de</strong> datos insuficientes para justificar su utilización en lamucositis inducida por radioterapia. También hay quetener en cuenta el riesgo <strong>de</strong> hipotensión tras su administracióncomo factor limitante <strong>de</strong> su empleo en algunospacientes.7CONTROL SINTOMÁTICO7.1. Dolor7.1.1. Características e inci<strong>de</strong>nciaSegún la <strong>de</strong>finición <strong>de</strong> la Asociación Internacionalpara el Estudio <strong>de</strong>l Dolor (IASP) el dolor “es unaexperiencia sensorial y emocional <strong>de</strong>sagradable, asociadacon una lesión real o potencial <strong>de</strong> los tejidos, o quese <strong>de</strong>scribe como producida por dicha lesión” (147) .Setrata, por tanto, <strong>de</strong> una experiencia subjetiva mixta, somáticay psíquica, única para cada individuo y queexiste siempre que un paciente diga que algo le duele.El dolor constituye uno <strong>de</strong> los síntomas más frecuentes<strong>de</strong> los pacientes con cáncer (148,149) (Tabla 18).Estudios realizados en distintos países indican que la inci<strong>de</strong>ncia<strong>de</strong> dolor aumenta con la progresión <strong>de</strong> la enfermedadsituándose entre el 30 y 40% en los pacientesque reciben tratamiento activo llegando al 70-90%en los que presentan enfermedad avanzada (150) .La prevalencia <strong>de</strong> este síntoma <strong>de</strong>pen<strong>de</strong> fundamentalmente<strong>de</strong> dos variables: el estadio <strong>de</strong> la enfermedady la localización tumoral. Consi<strong>de</strong>rando esteúltimo factor los valores oscilan <strong>de</strong>s<strong>de</strong> casi un 100 % <strong>de</strong>los tumores óseos, a un 70 a 80% <strong>de</strong> los genitourinarios,orales y digestivos, un 40-50% en mama y pulmón,hasta solamente 5 % en la leucemia (151)(152) . Aproximadamenteen el 75% <strong>de</strong> los casos, el dolor <strong>de</strong>l pacientecanceroso es <strong>de</strong>bido a la propia enfermedad, en el20% suele ser secundario al tratamiento, y hasta un5% <strong>de</strong> los dolores no está relacionado ni con la enfermedadni con el tratamiento aplicado (153) . Solamenteun 30% <strong>de</strong> los pacientes refieren una única localizaciónpara su dolor, mientras que un 39% presentandolor en 2 localizaciones y el 31% restante en 3 ómás (154) .En el 90% <strong>de</strong> los casos, el dolor oncológico es <strong>de</strong>tipo crónico. En contraste con el dolor agudo, el dolorcrónico suele tener un comienzo mal <strong>de</strong>finido y seacompaña raramente <strong>de</strong> signos objetivos e hiperactividad<strong>de</strong>l sistema nervioso autónomo que lleva al clínicoa pensar que: "no parece tener tanto dolor comodice". Por otra parte, el dolor crónico suele ir acompañado<strong>de</strong> signos <strong>de</strong> <strong>de</strong>presión, ansiedad, insomnio,etc. La compleja interrelación <strong>de</strong> todos estos factoresdan lugar al término “dolor total” (155) . Frecuentementese acompaña <strong>de</strong> episodios <strong>de</strong> dolor agudo <strong>de</strong>scritosen la literatura como dolor irruptivo, inci<strong>de</strong>nte,episódico, esporádico o breakthrough pain.Atendiendo al mecanismo fisiopatológico el dolorse pue<strong>de</strong> clasificar en nociceptivo y neuropático(Tabla 19). Esta diferenciación tiene importantes repercusionesterapéuticas7.1.2. Principios generales <strong>de</strong>l tratamiento farmacológicoEs importante señalar que las medidas <strong>de</strong> alivio<strong>de</strong>l dolor <strong>de</strong>ben abordarse como parte <strong>de</strong> una atenciónoncológica integral y pluridisciplinar. En primerlugar es necesario efectuar una valoración <strong>de</strong>tallada<strong>de</strong> los distintos tipos <strong>de</strong> dolor concurrentes así
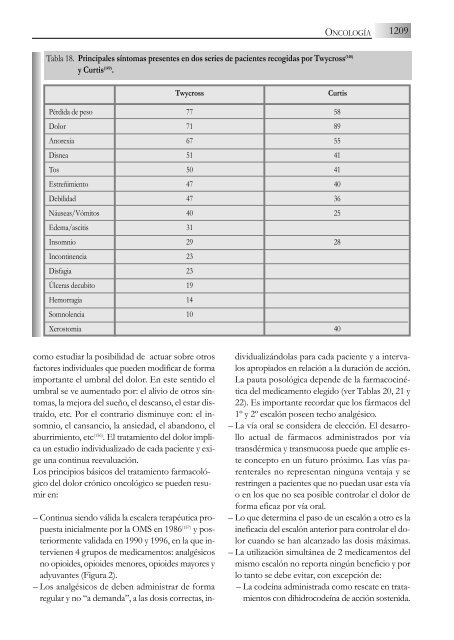
ONCOLOGÍA1209Tabla 18. Principales síntomas presentes en dos series <strong>de</strong> pacientes recogidas por Twycross (148)y Curtis (149) .TwycrossCurtisPérdida <strong>de</strong> peso 7758Dolor 7189Anorexia 6755Disnea 5141Tos 5041Estreñimiento 4740Debilidad 4736Náuseas/Vómitos 4025E<strong>de</strong>ma/ascitis 31Insomnio 2928Incontinencia 23Disfagia 23Úlceras <strong>de</strong>cubito 19Hemorragia 14Somnolencia 10Xerostomia 40como estudiar la posibilidad <strong>de</strong> actuar sobre otrosfactores individuales que pue<strong>de</strong>n modificar <strong>de</strong> formaimportante el umbral <strong>de</strong>l dolor. En este sentido elumbral se ve aumentado por: el alivio <strong>de</strong> otros síntomas,la mejora <strong>de</strong>l sueño, el <strong>de</strong>scanso, el estar distraído,etc. Por el contrario disminuye con: el insomnio,el cansancio, la ansiedad, el abandono, elaburrimiento, etc (156) . El tratamiento <strong>de</strong>l dolor implicaun estudio individualizado <strong>de</strong> cada paciente y exigeuna continua reevaluación.Los principios básicos <strong>de</strong>l tratamiento farmacológico<strong>de</strong>l dolor crónico oncológico se pue<strong>de</strong>n resumiren:– Continua siendo válida la escalera terapéutica propuestainicialmente por la OMS en 1986 (157) y posteriormentevalidada en 1990 y 1996, en la que intervienen4 grupos <strong>de</strong> medicamentos: analgésicosno opioi<strong>de</strong>s, opioi<strong>de</strong>s menores, opioi<strong>de</strong>s mayores yadyuvantes (Figura 2).– Los analgésicos <strong>de</strong> <strong>de</strong>ben administrar <strong>de</strong> formaregular y no “a <strong>de</strong>manda”, a las dosis correctas, individualizándolaspara cada paciente y a intervalosapropiados en relación a la duración <strong>de</strong> acción.La pauta posológica <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la farmacocinética<strong>de</strong>l medicamento elegido (ver Tablas 20, 21 y22). Es importante recordar que los fármacos <strong>de</strong>l1º y 2º escalón poseen techo analgésico.– La vía oral se consi<strong>de</strong>ra <strong>de</strong> elección. El <strong>de</strong>sarrolloactual <strong>de</strong> fármacos administrados por víatransdérmica y transmucosa pue<strong>de</strong> que amplíe esteconcepto en un futuro próximo. Las vías parenteralesno representan ninguna ventaja y serestringen a pacientes que no puedan usar esta víao en los que no sea posible controlar el dolor <strong>de</strong>forma eficaz por vía oral.– Lo que <strong>de</strong>termina el paso <strong>de</strong> un escalón a otro es laineficacia <strong>de</strong>l escalón anterior para controlar el dolorcuando se han alcanzado las dosis máximas.– La utilización simultánea <strong>de</strong> 2 medicamentos <strong>de</strong>lmismo escalón no reporta ningún beneficio y porlo tanto se <strong>de</strong>be evitar, con excepción <strong>de</strong>:– La co<strong>de</strong>ína administrada como rescate en tratamientoscon dihidroco<strong>de</strong>ína <strong>de</strong> acción sostenida.