PDF Download - Laborwelt
PDF Download - Laborwelt
PDF Download - Laborwelt
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Microarrays<br />
�<br />
ASK-Chip: Gezielte Analyse<br />
des menschlichen Kinoms<br />
Dr. Achim Knappik, MorphoSys - Antibodies by Design, Martinsried;<br />
Dr. Michael Kubbutat, ProQinase, Freiburg; Dr. Hans-Jürgen Volkmer, NMI, Reutlingen<br />
Derzeit sind mehr als 500 Proteinkinasen des Menschen bekannt, die durch Phosphorylierungen<br />
die Aktivität von Proteinen modulieren, Zellsignale weiterleiten und damit nahezu<br />
alle biologischen Prozesse beeinflussen. Proteinkinasen funktionieren als komplexes Netzwerk,<br />
das bei vielen Erkrankungen gestört ist. Medikamente, die einzelne Proteinkinasen<br />
hemmen, können diese Störungen eventuell beheben.<br />
Das gezielte Zusammenwirken komplexer<br />
Protein-Netzwerke im menschlichen<br />
Körper ist eine Grundvoraussetzung für<br />
das korrekte Ablaufen vieler molekularer<br />
Prozesse. Eines der vielleicht bedeutendsten<br />
Netzwerke hierbei ist das der Proteinkinasen<br />
(PK), die die zweitgrößte Proteinfamilie im<br />
menschlichen Genom überhaupt darstellen<br />
– fast 2% aller menschlichen Gene kodieren<br />
für Proteinkinasen. Die Enzyme fungieren<br />
als Schaltelemente und beeinflussen die<br />
meisten Funktionen im Stoffwechsel sowie<br />
das Wachstum und die Differenzierung<br />
der verschiedenen Zelltypen. Eine Reihe<br />
von Kinasen steht folglich im Verdacht,<br />
T E C H - T R A N S F E R<br />
bei verschiedenen Krankheiten, wie Krebs,<br />
Entzündungen oder Herz-Kreislauf-Erkrankungen,<br />
eine zentrale Rolle zu spielen. Der<br />
gezielte Einsatz von Medikamenten könnte<br />
theoretisch individuelle Fehlfunktionen einzelner<br />
Proteinkinasen und damit ausgelöste<br />
Kettenreaktionen innerhalb des gesamten<br />
Netzwerkes entgegenwirken. Bislang fehlen<br />
jedoch ein umfangreiches Gesamtbild und<br />
Verständnis dieses Netzwerkes, um die<br />
Auswirkungen von Medikamenten auf das<br />
Zusammenspiel aller Vertreter realistisch<br />
abschätzen zu können. Die Medikamentenforschung<br />
in diesem Bereich benötigt<br />
deshalb neue, optimierte Werkzeuge.<br />
In einem solchen Projekt wollen derzeit die<br />
Freiburger ProQinase als Geschäftseinheit<br />
der KTB Tumorforschungs GmbH, das<br />
Naturwissenschaftliche und Medizinische<br />
Institut (NMI), Reutlingen, und die Morpho-<br />
Sys-Geschäftseinheit Antibodies by Design<br />
ein neues Analyse-System etablieren. Das<br />
vom Bundesministerium für Bildung und<br />
Forschung (BMBF) geförderte Projekt hat sich<br />
die Bereitstellung von Werkzeugen für die<br />
Analyse aller menschlichen Proteinkinasen<br />
– des menschlichen „Kinoms“ – zum Ziel<br />
gesetzt. Hierbei werden sowohl die Proteinkinase-Plattform<br />
von ProQinase, spezifische<br />
Antikörper aus der HuCAL ® -Bibliothek von<br />
Antibodies by Design als auch siRNA- und<br />
BioChip-Technologien des NMI miteinander<br />
kombiniert. Aus der Zusammenarbeit wird<br />
ein adenoviraler siRNA-Kinom-Chip (ASK)<br />
hervorgehen, der als Komplettsystem die<br />
gleichzeitige Inhibition aller menschlichen<br />
Proteinkinasen, und damit deren Funktionsanalyse<br />
ermöglichen wird.<br />
Interdisziplinärer Ansatz<br />
Ein solch interdisziplinärer Ansatz ist natürlich<br />
vor etliche Herausforderungen gestellt.<br />
Von zentraler Bedeutung sind insbesondere<br />
hinreichende Mengen gereinigter Proteinkinasen<br />
für die Antikörperentwicklung, die<br />
Etablierung von Methoden zur gezielten<br />
Abschaltung von Proteinkinasen in Primärzellinien<br />
und zugleich die Herstellung hochspezifischer<br />
Antikörper zur Validierung der<br />
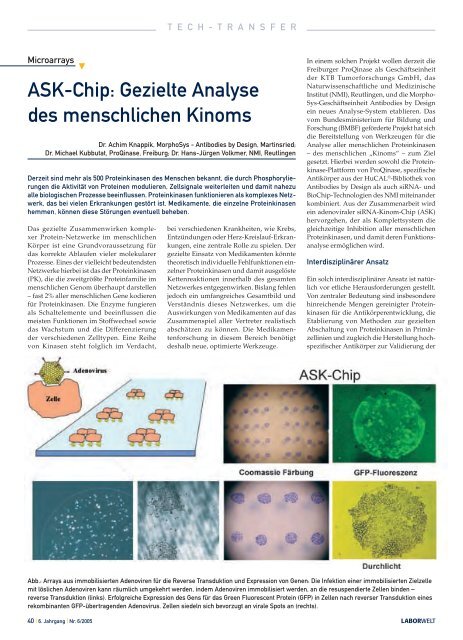
Abb.: Arrays aus immobilisierten Adenoviren für die Reverse Transduktion und Expression von Genen: Die Infektion einer immobilisierten Zielzelle<br />
mit löslichen Adenoviren kann räumlich umgekehrt werden, indem Adenoviren immobilisiert werden, an die resuspendierte Zellen binden –<br />
reverse Transduktion (links). Erfolgreiche Expression des Gens für das Green Fluorescent Protein (GFP) in Zellen nach reverser Transduktion eines<br />
rekombinanten GFP-übertragenden Adenovirus. Zellen siedeln sich bevorzugt an virale Spots an (rechts).<br />
40 | 6. Jahrgang | Nr. 6/2005 LABORWELT