Lílian dos Santos Brandão SÍNTESE E CARACTERIZAÇÃO DE ...
Lílian dos Santos Brandão SÍNTESE E CARACTERIZAÇÃO DE ...
Lílian dos Santos Brandão SÍNTESE E CARACTERIZAÇÃO DE ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Perda de massa (%)<br />
100<br />
95<br />
90<br />
0 100 200 300 400 500 600 700<br />
Temperatura (°C)<br />
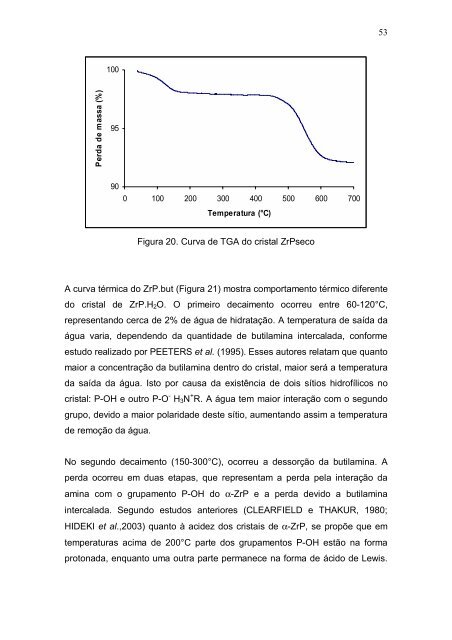
Figura 20. Curva de TGA do cristal ZrPseco<br />
A curva térmica do ZrP.but (Figura 21) mostra comportamento térmico diferente<br />
do cristal de ZrP.H2O. O primeiro decaimento ocorreu entre 60-120°C,<br />
representando cerca de 2% de água de hidratação. A temperatura de saída da<br />
água varia, dependendo da quantidade de butilamina intercalada, conforme<br />
estudo realizado por PEETERS et al. (1995). Esses autores relatam que quanto<br />
maior a concentração da butilamina dentro do cristal, maior será a temperatura<br />
da saída da água. Isto por causa da existência de dois sítios hidrofílicos no<br />
cristal: P-OH e outro P-O - H3N + R. A água tem maior interação com o segundo<br />
grupo, devido a maior polaridade deste sítio, aumentando assim a temperatura<br />
de remoção da água.<br />
No segundo decaimento (150-300°C), ocorreu a dessorção da butilamina. A<br />
perda ocorreu em duas etapas, que representam a perda pela interação da<br />
amina com o grupamento P-OH do α-ZrP e a perda devido a butilamina<br />
intercalada. Segundo estu<strong>dos</strong> anteriores (CLEARFIELD e THAKUR, 1980;<br />
HI<strong>DE</strong>KI et al.,2003) quanto à acidez <strong>dos</strong> cristais de α-ZrP, se propõe que em<br />
temperaturas acima de 200°C parte <strong>dos</strong> grupamentos P-OH estão na forma<br />
protonada, enquanto uma outra parte permanece na forma de ácido de Lewis.<br />
53