View/Open - JUWEL - Forschungszentrum Jülich
View/Open - JUWEL - Forschungszentrum Jülich
View/Open - JUWEL - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
9. Biotransformationen im Zweiphasensystem<br />
cematspaltung von Benzoin ein interessantes Reaktionssystem für die Anwendung des<br />
organisch-wässrigen Zweiphasensystems dar.<br />
9.4.1. Charakterisierung der Racematspaltung<br />
Da über die BAL-katalysierte Racematspaltung bislang nur sehr wenig bekannt ist,<br />
soll diese Reaktion zunächst für das homogene Reaktionssystem charakterisiert werden.<br />
Dazu werden die in Kapitel 3 entwickelten Reaktionsbedingungen eingestellt.<br />
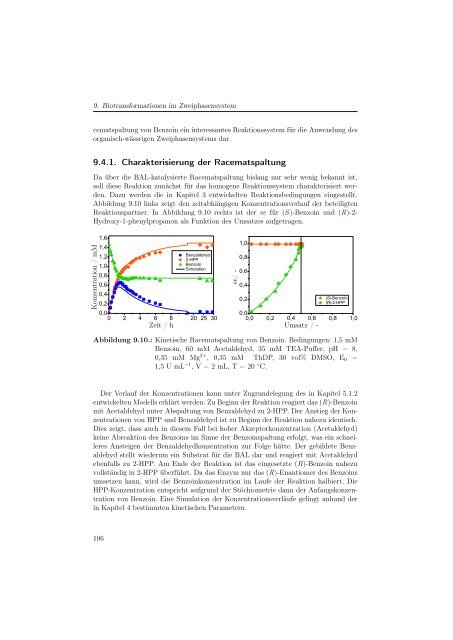
Abbildung 9.10 links zeigt den zeitabhängigen Konzentrationsverlauf der beteiligten<br />
Reaktionspartner. In Abbildung 9.10 rechts ist der ee für (S)-Benzoin und (R)-2-<br />
Hydroxy-1-phenylpropanon als Funktion des Umsatzes aufgetragen.<br />
Konzentration / mM<br />
1,6<br />
1,4<br />
1,2<br />
Benzaldehyd<br />
2-HPP<br />
1,0<br />
0,8<br />
0,6<br />
0,4<br />
0,2<br />
Benzoin<br />
Simulation<br />
0,0<br />
0 2 4 6 8 20 25 30<br />
Zeit / h<br />
ee/ -<br />
1,0<br />
0,8<br />
0,6<br />
0,4<br />
0,2<br />
(S)-Benzoin<br />
(R)-2-HPP<br />
0,0<br />
0,0 0,2 0,4 0,6 0,8 1,0<br />
Umsatz / -<br />
Abbildung 9.10.: Kinetische Racematspaltung von Benzoin. Bedingungen: 1,5 mM<br />
Benzoin, 60 mM Acetaldehyd, 35 mM TEA-Puffer, pH = 8,<br />
0,35 mM Mg 2+ , 0,35 mM ThDP, 30 vol% DMSO, E0 =<br />
1,5 U mL −1 ,V=2mL,T=20 ◦ C.<br />
Der Verlauf der Konzentrationen kann unter Zugrundelegung des in Kapitel 5.1.2<br />
entwickelten Modells erklärt werden. Zu Beginn der Reaktion reagiert das (R)-Benzoin<br />
mit Acetaldehyd unter Abspaltung von Benzaldehyd zu 2-HPP. Der Anstieg der Konzentrationen<br />
von HPP und Benzaldehyd ist zu Beginn der Reaktion nahezu identisch.<br />
Dies zeigt, dass auch in diesem Fall bei hoher Akzeptorkonzentration (Acetaldehyd)<br />
keine Abreaktion des Benzoins im Sinne der Benzoinspaltung erfolgt, was ein schnelleres<br />
Ansteigen der Benzaldehydkonzentration zur Folge hätte. Der gebildete Benzaldehyd<br />
stellt wiederum ein Substrat für die BAL dar und reagiert mit Acetaldehyd<br />
ebenfalls zu 2-HPP. Am Ende der Reaktion ist das eingesetzte (R)-Benzoin nahezu<br />
vollständig in 2-HPP überführt. Da das Enzym nur das (R)-Enantiomer des Benzoins<br />
umsetzen kann, wird die Benzoinkonzentration im Laufe der Reaktion halbiert. Die<br />
HPP-Konzentration entspricht aufgrund der Stöchiometrie dann der Anfangskonzentration<br />
von Benzoin. Eine Simulation der Konzentrationsverläufe gelingt anhand der<br />
in Kapitel 4 bestimmten kinetischen Parametern.<br />
106