View/Open - JUWEL - Forschungszentrum Jülich
View/Open - JUWEL - Forschungszentrum Jülich
View/Open - JUWEL - Forschungszentrum Jülich
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
4. Kinetik<br />
Bei Vergleich der für die Benzoinbildung bestimmten Daten (Kapitel 4.2.2) fällt auf,<br />
dass die KM-Werte, die für Benzaldehyd bestimmt wurden, sich auch unter Berücksichtigung<br />
der Fehlergrenzen deutlich unterscheiden. Dies scheint jedoch nur auf den<br />
ersten Blick widersprüchlich, denn bei der Benzoinbildung (Reaktion 01) reagiert der<br />
Benzaldehyd sowohl als Donor- als auch als Akzeptoraldehyd. Bei der HPP-Bildung<br />
(Reaktion 04) dagegen fungiert der Benzaldehyd nur als Donor. Wenn man davon<br />
ausgeht, dass Donor und Akzeptor an verschiedene Stellen im aktiven Zentrum des<br />
Enzyms binden (mit verschiedener Affinität zur jeweiligen Bindungsstelle), so erscheinen<br />
die daraus resultierenden unterschiedlichen KM-Werte für Donor und Akzeptor<br />
durchaus plausibel, obwohl es sich um ein und dasselbe Molekül handelt. Im Vergleich<br />
zu Kapitel 4.2.4 ist der in dieser Versuchsreihe bestimmte KM-Wert für Acetaldehyd<br />
etwas kleiner. Jedoch ist unter Berücksichtigung der Fehlergrenzen der Unterschied<br />
nicht signifikant.<br />
Bei den kinetischen Untersuchungen zur HPP-Bildung (Reaktion 04) konnten Hinweise<br />
auf eine Produktinhibierung durch HPP gefunden werden. Eine Quantifizierung<br />
der Inhibierung scheiterte jedoch an experimetellen Schwierigkeiten. Da bei den Experimenten<br />
zur Inhibierung schon von Beginn an hohe HPP-Konzentrationen eingestellt<br />
werden, ist eine starke Verdünnung der Proben für die HPLC-Analytik nötig, was die<br />
Messgenauigkeit stark herabsetzt.<br />
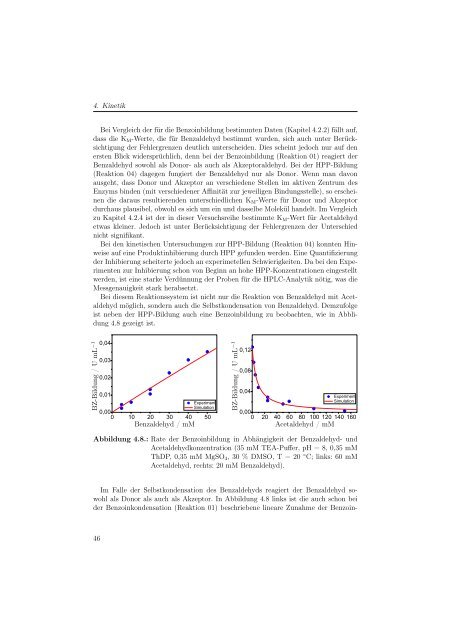
Bei diesem Reaktionssystem ist nicht nur die Reaktion von Benzaldehyd mit Acetaldehyd<br />
möglich, sondern auch die Selbstkondensation von Benzaldehyd. Demzufolge<br />
ist neben der HPP-Bildung auch eine Benzoinbildung zu beobachten, wie in Abblidung<br />
4.8 gezeigt ist.<br />
BZ-Bildung / U mL −1<br />
0,04<br />
0,03<br />
0,02<br />
0,01<br />
Experiment<br />
Simulation<br />
0,00<br />
0 10 20 30 40 50<br />
Benzaldehyd / mM<br />
BZ-Bildung / U mL −1<br />
0,12<br />
0,08<br />
0,04<br />
Experiment<br />
Simulation<br />
0,00<br />
0 20 40 60 80 100 120 140 160<br />
Acetaldehyd / mM<br />
Abbildung 4.8.: Rate der Benzoinbildung in Abhängigkeit der Benzaldehyd- und<br />
Acetaldehydkonzentration (35 mM TEA-Puffer, pH = 8, 0,35 mM<br />
ThDP,0,35mMMgSO4, 30 % DMSO, T = 20 ◦ C; links: 60 mM<br />
Acetaldehyd, rechts: 20 mM Benzaldehyd).<br />
Im Falle der Selbstkondensation des Benzaldehyds reagiert der Benzaldehyd sowohl<br />
als Donor als auch als Akzeptor. In Abbildung 4.8 links ist die auch schon bei<br />
der Benzoinkondensation (Reaktion 01) beschriebene lineare Zunahme der Benzoin-<br />
46