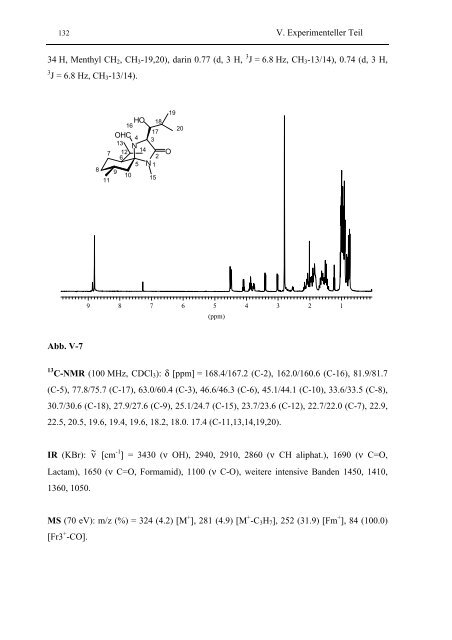
132 V. Experimenteller Teil34 H, Menthyl CH 2 , CH 3 -19,20), darin 0.77 (d, 3 H, 3 J = 6.8 Hz, CH 3 -13/14), 0.74 (d, 3 H,3 J = 6.8 Hz, CH 3 -13/14).819HO 18162017OHC 4 313 N147 12 O625 N 1910111598765(ppm)4321Abb. V-713 C-NMR (100 MHz, CDCl 3 ): δ [ppm] = 168.4/167.2 (C-2), 162.0/160.6 (C-16), 81.9/81.7(C-5), 77.8/75.7 (C-17), 63.0/60.4 (C-3), 46.6/46.3 (C-6), 45.1/44.1 (C-10), 33.6/33.5 (C-8),30.7/30.6 (C-18), 27.9/27.6 (C-9), 25.1/24.7 (C-15), 23.7/23.6 (C-12), 22.7/22.0 (C-7), 22.9,22.5, 20.5, 19.6, 19.4, 19.6, 18.2, 18.0. 17.4 (C-11,13,14,19,20).IR (KBr): ~ ν [cm -1 ] = 3430 (ν OH), 2940, 2910, 2860 (ν CH aliphat.), 1690 (ν C=O,Lactam), 1650 (ν C=O, Formamid), 1100 (ν C-O), weitere intensive Banden 1450, 1410,1360, 1050.MS (70 eV): m/z (%) = 324 (4.2) [M + ], 281 (4.9) [M + -C 3 H 7 ], 252 (31.9) [Fm + ], 84 (100.0)[Fr3 + -CO].
V. Experimenteller Teil 133(1’S,3S,5R,6S,9R)-4-Formyl-3-(1’-hydroxy-2’,2’-dimethyl-propyl)-6-isopropyl-1,9-dimethyl-1,4-diazaspiro[4.5]decan-2-on (21d)1.00 g (3.98 mmol) Formyl-MMI 2 werden gemäß AAV 1 mit 1.32 ml (12 mmol)Pivalaldehyd umgesetzt. In einer Ausbeute von 95 % wird das Rohprodukt in Form einesgelblichen Öls erhalten. Das Verhältnis von regulärem Aldoladdukt <strong>und</strong> dem aus derWanderung der Formylgruppe resultierenden Produkt liegt bei 5:1. Die Trennung gelingtdurch Säulenchromatographie an Kieselgel mit EE/Cyclohexan = 2:1 problemlos. Die beidenProdukte werden in einer Ausbeute von 770 g (57 %) (21d) als farbloser Feststoff, der ausDiethylether kristallisiert werden kann, bzw. 108 mg (8 %) (22)als farbloses Öl isoliert.Schmp.: 143 °CDC: R f = 0.32 (Ethylacetat/Cyclohexan = 2:1), IodDrehwert: [α] 20D = +102.7 (c = 1 in CHCl 3)198711HO 181617OHC 4 313 N12 14625 N 1910 15O202198765(ppm)4321Abb. V-81 H-NMR (400 MHz, CDCl 3 ): δ [ppm] = 8.72 (s, 1 H, CHO), 4.55 (s, 1 H, CH-3), 3.75 (d,1 H, 3 J = 10.4 Hz, CH-17), 2.75 (s, 3 H, NCH 3 ), 2.71 (s br, 1 H, OH), 2.08 (ddd, 1 H,2 J = 13.7 Hz, 3 J = 3.6 Hz, 4 J = 2.0 Hz, CH 2 -10 eq ), 1.92 (dm, 1 H, 2,3 J = 13.2 Hz, CH 2 -8 eq ),
- Seite 1:
Synthese und Transformationen chira
- Seite 4:
Die vorliegende Arbeit wurde in der
- Seite 7 und 8:
konz.LDAmmCPBAMeMSνNMRNOENOESYoopP
- Seite 9:
Inhaltsverzeichnis3.4. Epoxidation.
- Seite 12 und 13:
2 I. Einleitungwerden. [3] Es trete
- Seite 14 und 15:
4 I. Einleitungwirtsspezifisches Ph
- Seite 17 und 18:
I. Einleitung 7Zur Darstellung von
- Seite 19 und 20:
I. Einleitung 9Anwendungsbreite von
- Seite 21 und 22:
II. Aufgabenstellung 11II. Aufgaben
- Seite 23 und 24:
II. Aufgabenstellung 13aminosäures
- Seite 25:
III. Diskussion und Ergebnisse 15II
- Seite 28 und 29:
18 III. Diskussion und ErgebnisseEi
- Seite 30 und 31:
20 III. Diskussion und ErgebnisseOO
- Seite 32 und 33:
22 III. Diskussion und ErgebnisseOH
- Seite 34 und 35:
24 III. Diskussion und Ergebnisse2.
- Seite 36 und 37:
26 III. Diskussion und ErgebnisseON
- Seite 38 und 39:
28 III. Diskussion und Ergebnissegr
- Seite 40 und 41:
30 III. Diskussion und Ergebnisse21
- Seite 42 und 43:
32 III. Diskussion und Ergebnissebe
- Seite 44 und 45:
34 III. Diskussion und ErgebnisseKo
- Seite 46 und 47:
36 III. Diskussion und ErgebnisseDa
- Seite 48 und 49:
38 III. Diskussion und ErgebnisseEi
- Seite 50:
40 III. Diskussion und ErgebnisseDi
- Seite 53 und 54:
III. Diskussion und Ergebnisse 43Um
- Seite 55 und 56:
III. Diskussion und Ergebnisse 45mi
- Seite 57 und 58:
III. Diskussion und Ergebnisse 47OH
- Seite 59 und 60:
III. Diskussion und Ergebnisse 49zu
- Seite 61 und 62:
III. Diskussion und Ergebnisse 51Me
- Seite 63 und 64:
III. Diskussion und Ergebnisse 53Ab
- Seite 65 und 66:
III. Diskussion und Ergebnisse 55Th
- Seite 67 und 68:
III. Diskussion und Ergebnisse 57De
- Seite 69 und 70:
III. Diskussion und Ergebnisse 59HO
- Seite 71 und 72:
III. Diskussion und Ergebnisse 61ko
- Seite 73 und 74:
III. Diskussion und Ergebnisse 63Be
- Seite 75 und 76:
III. Diskussion und Ergebnisse 65pr
- Seite 77 und 78:
III. Diskussion und Ergebnisse 67OH
- Seite 79 und 80:
III. Diskussion und Ergebnisse 69Re
- Seite 81 und 82:
III. Diskussion und Ergebnisse 71De
- Seite 83 und 84:
III. Diskussion und Ergebnisse 73ra
- Seite 85 und 86:
III. Diskussion und Ergebnisse 75RX
- Seite 87 und 88:
III. Diskussion und Ergebnisse 77Ko
- Seite 89 und 90:
III. Diskussion und Ergebnisse 793.
- Seite 91 und 92: III. Diskussion und Ergebnisse 81OH
- Seite 93 und 94: III. Diskussion und Ergebnisse 83Ak
- Seite 95 und 96: III. Diskussion und Ergebnisse 85Hy
- Seite 97 und 98: III. Diskussion und Ergebnisse 87OS
- Seite 99 und 100: III. Diskussion und Ergebnisse 89Ak
- Seite 101 und 102: III. Diskussion und Ergebnisse 91Er
- Seite 103 und 104: III. Diskussion und Ergebnisse 93ac
- Seite 105 und 106: III. Diskussion und Ergebnisse 95OO
- Seite 107 und 108: III. Diskussion und Ergebnisse 97Ei
- Seite 109 und 110: III. Diskussion und Ergebnisse 9944
- Seite 111 und 112: IV. Zusammenfassung 101IV. Zusammen
- Seite 113 und 114: IV. Zusammenfassung 103dieHydroxylf
- Seite 115 und 116: IV. Zusammenfassung 105OR 1ONNR 2OR
- Seite 117 und 118: V. Experimenteller Teil 107HPLC wur
- Seite 119 und 120: V. Experimenteller Teil 1090.66 %ig
- Seite 121 und 122: V. Experimenteller Teil 111organisc
- Seite 123 und 124: V. Experimenteller Teil 113aufgekoc
- Seite 125 und 126: V. Experimenteller Teil 1153.6 ml (
- Seite 127 und 128: V. Experimenteller Teil 117871116 1
- Seite 129 und 130: V. Experimenteller Teil 11924 h am
- Seite 131 und 132: V. Experimenteller Teil 1214. Verbi
- Seite 133 und 134: V. Experimenteller Teil 123(3RS,5R,
- Seite 135 und 136: V. Experimenteller Teil 1254.1. Ald
- Seite 137 und 138: V. Experimenteller Teil 12787112019
- Seite 139 und 140: V. Experimenteller Teil 12987112019
- Seite 141: V. Experimenteller Teil 13113 C-NMR
- Seite 145 und 146: V. Experimenteller Teil 135198OHCO
- Seite 147 und 148: V. Experimenteller Teil 1373 J = 6.
- Seite 149 und 150: V. Experimenteller Teil 139weitere
- Seite 151 und 152: V. Experimenteller Teil 141dimethyl
- Seite 153 und 154: V. Experimenteller Teil 14320218192
- Seite 155 und 156: V. Experimenteller Teil 145871119HO
- Seite 157 und 158: V. Experimenteller Teil 147O198711S
- Seite 159 und 160: V. Experimenteller Teil 1492.99 (s,
- Seite 161 und 162: V. Experimenteller Teil 151IR (Film
- Seite 163 und 164: V. Experimenteller Teil 153Alkohols
- Seite 165 und 166: V. Experimenteller Teil 155434 mg (
- Seite 167 und 168: V. Experimenteller Teil 157aromat.)
- Seite 169 und 170: V. Experimenteller Teil 159(12.7) [
- Seite 171 und 172: V. Experimenteller Teil 16187111920
- Seite 173 und 174: V. Experimenteller Teil 1633 J = 7.
- Seite 175 und 176: V. Experimenteller Teil 1654.5. Met
- Seite 177 und 178: V. Experimenteller Teil 167IR (Film
- Seite 179 und 180: V. Experimenteller Teil 169MS (70 e
- Seite 181 und 182: V. Experimenteller Teil 171(2S,3R)-
- Seite 183 und 184: V. Experimenteller Teil 173(3RS,5R,
- Seite 185 und 186: V. Experimenteller Teil 1758711O201
- Seite 187 und 188: V. Experimenteller Teil 1771 H-NMR
- Seite 189 und 190: V. Experimenteller Teil 179EA: C 18
- Seite 191 und 192: V. Experimenteller Teil 181Anschlie
- Seite 193 und 194:
V. Experimenteller Teil 183anschlie
- Seite 195 und 196:
V. Experimenteller Teil 1858711OS 1
- Seite 197 und 198:
V. Experimenteller Teil 18719,20,21
- Seite 199 und 200:
V. Experimenteller Teil 18913 C-NMR
- Seite 201 und 202:
V. Experimenteller Teil 191(5R,6S,9
- Seite 203 und 204:
V. Experimenteller Teil 1931871117
- Seite 205 und 206:
V. Experimenteller Teil 1951 H-NMR
- Seite 207 und 208:
V. Experimenteller Teil 1971 H-NMR
- Seite 209 und 210:
V. Experimenteller Teil 199EA: C 21
- Seite 211 und 212:
V. Experimenteller Teil 201DC: R f
- Seite 213 und 214:
VI. Literatur 203VI. Literatur[1] a
- Seite 215 und 216:
VI. Literatur 205b) A. G. Myers, J.
- Seite 217 und 218:
VI. Literatur 207[62] E. J. Iwanowi
- Seite 219 und 220:
VI. Literatur 209[102] a) [70]; b)
- Seite 221 und 222:
VI. Literatur 211[132] L. A. Marcau
- Seite 223:
VI. Literatur 213[163] a) C. H. Cum