You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
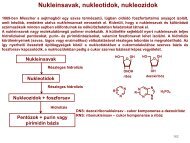
77hidrogén<strong>kötés</strong>eket képeznek. Ezek – a szénhidrogénekre nem jellemző – intermolekuláriskölcsönhatások okozzák a szénhidrogénektől jelentősen eltérő fizikai tulajdonságokat. Azintermolekuláris hidrogénhíd kötődések az aminokban gyengébbek, mint az alkoholokban.(nitrogén kisebb méretű, a vegyérték elektronok és a nemkötő pár nagyobb magvonzás alattállnak).R 1R 2NHR 1NO H OH R 2 RRHamin alkoholAz alacsonyabb szénatomszámú aminok vízben jól oldódnak (jobban, mint azalkoholok és az éterek, mert a nitrogénatom jobb protonakceptor, mint az oxigén), a nagyobbszénatomszámúak (pl. az aromás aminok) esetében a szénhidrogén-maradékok hidrofóbjellege kerül túlsúlyba és ezért az oldhatósága romlik. Az aminok szerves oldószerekben jóloldódnak. A kvaterner ammónium vegyületek és a különböző rendű aminok ammóniumsóiionos szerkezetük révén vízben általában jól, szerves oldószerekben kevésbé vagy egyáltalánnem oldódnak.Az aminok kellemetlen szagú vegyületek (pl. a bomló hal szaga származikaminokból). A szagra való utalás sok esetben az amin nevében is tükröződik A bután-1,4-diamin triviális neve: putreszcin (putresco: megrothad), a bután-1,5-diamin triviális neve:kadaverin (cadaver: hulla).Az aminok bázicitásaGázfázisban szolvatáció hiányában a bázicitást a szubsztituensek elektronos hatása határozzameg. Elektronküldő csoportok növelik a nitrogénatom elektronsűrűségét és így a bázicitást is.Bázicitás növekvő sorrendje gázfázisban:R>R > NR>> NH>R > NH 2 > NH 3>RROldat fázisban – így vízben is – mindezen túl a dipol–dipol kölcsönhatás és hidrogén<strong>kötés</strong>hatása is érvényesül.HHH 3 CNHXH 3 CNHXdipól-dipólkölcsönhatásHHOHHHOHhidrogén<strong>kötés</strong>Vizes közegben az alkilcsoportnak kettős hatása van az ammóniumionra. Egyrésztelektronküldő sajátsága révén elősegíti a töltésdiszpergálódást, s így az iont stabilizálja,