Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
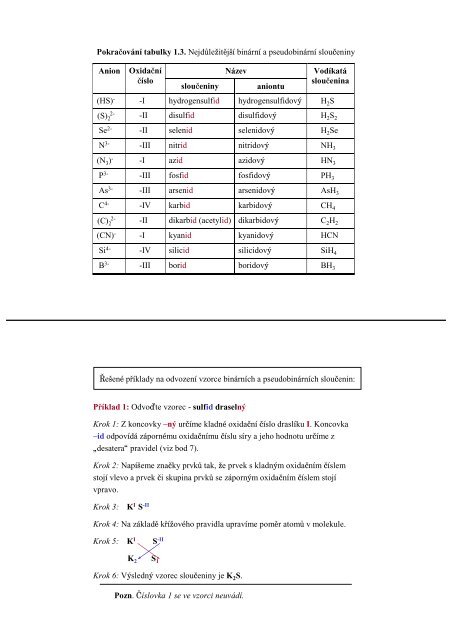
Pokračování tabulky 1.3. Nejdůležitější binární a pseudobinární sloučeniny<br />
Anion<br />
Oxidační<br />
číslo<br />
sloučeniny<br />
Název<br />
aniontu<br />
Vodíkatá<br />
sloučenina<br />
(HS) - -I hydrogensulfid hydrogensulfidový H 2 S<br />
2-<br />
(S) 2<br />
-II disulfid disulfidový H 2 S 2<br />
Se 2- -II selenid selenidový H 2 Se<br />
N 3- -III nitrid nitridový NH 3<br />
(N 3 ) - -I azid azidový HN 3<br />
P 3- -III fosfid fosfidový PH 3<br />
As 3- -III arsenid arsenidový AsH 3<br />
C 4- -IV karbid karbidový CH 4<br />
2-<br />
(C) 2<br />
-II dikarbid (acetylid) dikarbidový C 2 H 2<br />
(CN) - -I kyanid kyanidový HCN<br />
Si 4- -IV silicid silicidový SiH 4<br />
B 3- -III borid boridový BH 3<br />
Řešené příklady na odvození vzorce binárních a pseudobinárních sloučenin:<br />
Příklad 1: Odvoďte vzorec - sulfid draselný<br />
Krok 1: Z koncovky –ný určíme kladné oxidační číslo draslíku I. Koncovka<br />
–id odpovídá zápornému oxidačnímu číslu síry a jeho hodnotu určíme z<br />
„desatera“ pravidel (viz bod 7).<br />
Krok 2: Napíšeme značky prvků tak, že prvek s kladným oxidačním číslem<br />
stojí vlevo a prvek či skupina prvků se záporným oxidačním číslem stojí<br />
vpravo.<br />
Krok 3:<br />
K I S -II<br />
Krok 4: Na základě křížového pravidla upravíme poměr atomů v molekule.<br />
Krok 5: K I S -II<br />
K 2 S 1<br />
Krok 6: Výsledný vzorec sloučeniny je K 2 S.<br />
Pozn. Číslovka 1 se ve vzorci neuvádí.