ГЛАВА 2 СТРОЕНИЕ МОЛЕКУЛ И ХИМИЧЕСКАЯ СВЯЗЬ 2.1 ...
ГЛАВА 2 СТРОЕНИЕ МОЛЕКУЛ И ХИМИЧЕСКАЯ СВЯЗЬ 2.1 ...
ГЛАВА 2 СТРОЕНИЕ МОЛЕКУЛ И ХИМИЧЕСКАЯ СВЯЗЬ 2.1 ...
- No tags were found...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
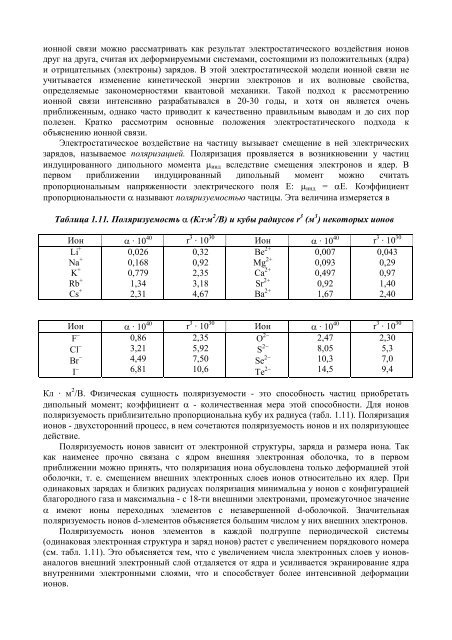
ионной связи можно рассматривать как результат электростатического воздействия ионовдруг на друга, считая их деформируемыми системами, состоящими из положительных (ядра)и отрицательных (электроны) зарядов. В этой электростатической модели ионной связи неучитывается изменение кинетической энергии электронов и их волновые свойства,определяемые закономерностями квантовой механики. Такой подход к рассмотрениюионной связи интенсивно разрабатывался в 20-30 годы, и хотя он является оченьприближенным, однако часто приводит к качественно правильным выводам и до сих порполезен. Кратко рассмотрим основные положения электростатического подхода кобъяснению ионной связи.Электростатическое воздействие на частицу вызывает смещение в ней электрическихзарядов, называемое поляризацией. Поляризация проявляется в возникновении у частициндуцированного дипольного момента µ инд вследствие смещения электронов и ядер. Впервом приближении индуцированный дипольный момент можно считатьпропорциональным напряженности электрического поля Е: µ инд = αЕ. Коэффициентпропорциональности α называют поляризуемостью частицы. Эта величина измеряется вТаблица 1.11. Поляризуемость α (Кл·м 2 /В) и кубы радиусов r 3 (м 3 ) некоторых ионов<strong>И</strong>он α · 10 40 r 3 · 10 30 <strong>И</strong>он α · 10 40 r 3 · 10 30Li +Na +K +Rb +Cs + 0,0260,1680,7791,342,310,320,922,353,184,67Be 2+Mg 2+Ca 2+Sr 2+Ba 2+ 0,0070,0930,4970,921,670,0430,290,971,402,40<strong>И</strong>он α · 10 40 r 3 · 10 30 <strong>И</strong>он α · 10 40 r 3 · 10 30F −0,862,35O 2−2,472,30Br −4,497,50Se 2−10,37,0I − 6,8110,6Te 2− 14,59,4Cl −3,215,92S 2−8,055,3Кл · м 2 /В. Физическая сущность поляризуемости - это способность частиц приобретатьдипольный момент; коэффициент α - количественная мера этой способности. Для ионовполяризуемость приблизительно пропорциональна кубу их радиуса (табл. 1.11). Поляризацияионов - двухсторонний процесс, в нем сочетаются поляризуемость ионов и их поляризующеедействие.Поляризуемость ионов зависит от электронной структуры, заряда и размера иона. Таккак наименее прочно связана с ядром внешняя электронная оболочка, то в первомприближении можно принять, что поляризация иона обусловлена только деформацией этойоболочки, т. е. смещением внешних электронных слоев ионов относительно их ядер. Приодинаковых зарядах и близких радиусах поляризация минимальна у ионов с конфигурациейблагородного газа и максимальна - с 18-ти внешними электронами, промежуточное значениеα имеют ионы переходных элементов с незавершенной d-оболочкой. Значительнаяполяризуемость ионов d-элементов объясняется большим числом у них внешних электронов.Поляризуемость ионов элементов в каждой подгруппе периодической системы(одинаковая электронная структура и заряд ионов) растет с увеличением порядкового номера(см. табл. 1.11). Это объясняется тем, что с увеличением числа электронных слоев у ионованалоговвнешний электронный слой отдаляется от ядра и усиливается экранирование ядравнутренними электронными слоями, что и способствует более интенсивной деформацииионов.