You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
4.2. Découverte du noyau atomique : l’expérience <strong>de</strong> Rutherford<br />
Malgré son nom, l’atome ne pouvait plus être considéré comme indivisible <strong>de</strong>puis la découverte <strong>de</strong> l’électron par Thomson en 1897. Ce<br />
<strong>de</strong>rnier décrivait l’atome comme une sorte <strong>de</strong> pastèque miniature.<br />
Au contraire, Rutherford pensait que la charge positive <strong>de</strong> l’atome <strong>de</strong>vait être concentrée dans un très petit volume. Il en eut la certitu<strong>de</strong><br />
en réalisant une série d’expériences sur <strong>de</strong>s éléments radioactifs découverts par Becquerel quelques années plus tôt. Le radi um est un<br />
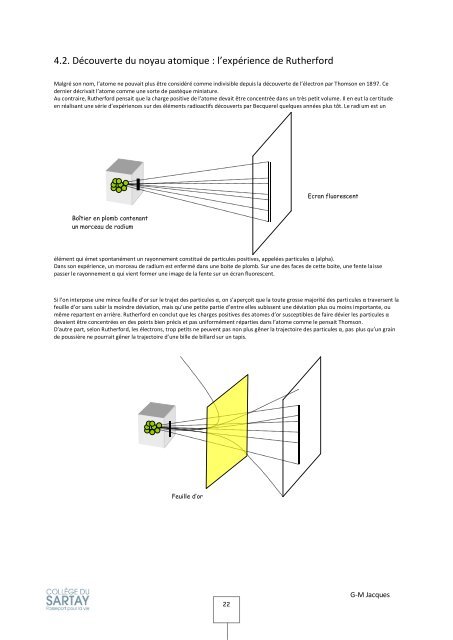
Boîtier en plomb contenant<br />
un morceau <strong>de</strong> radium<br />
élément qui émet spontanément un rayonnement constitué <strong>de</strong> particules positives, appelées particules α (alpha).<br />
Dans son expérience, un morceau <strong>de</strong> radium est enfermé dans une boite <strong>de</strong> plomb. Sur une <strong>de</strong>s faces <strong>de</strong> cette boite, une fente laisse<br />
passer le rayonnement α qui vient former une image <strong>de</strong> la fente sur un écran fluorescent.<br />
Si l’on interpose une mince feuille d’or sur le trajet <strong>de</strong>s particules α, on s’aperçoit que la toute grosse majorité <strong>de</strong>s particules α traversent la<br />
feuille d’or sans subir la moindre déviation, mais qu’une petite partie d’entre elles subissent une déviation plus ou moins importante, ou<br />
même repartent en arrière. Rutherford en conclut que les charges positives <strong>de</strong>s atomes d’or susceptibles <strong>de</strong> faire dévier les particules α<br />
<strong>de</strong>vaient être concentrées en <strong>de</strong>s points bien précis et pas uniformément réparties dans l’atome comme le pensait Thomson.<br />
D’autre part, selon Rutherford, les électrons, trop petits ne peuvent pas non plus gêner la trajectoire <strong>de</strong>s particules α, pas plus qu’un grain<br />
<strong>de</strong> poussière ne pourrait gêner la trajectoire d’une bille <strong>de</strong> billard sur un tapis.<br />
Feuille d’or<br />
22<br />
Ecran fluorescent<br />
G-M <strong>Jacques</strong>








![[Document d'intentions pédagogiques] - Collège du Sartay](https://img.yumpu.com/49774314/1/184x260/document-dintentions-pacdagogiques-collage-du-sartay.jpg?quality=85)