Jahresbericht 2007 - Leibniz-Institut für Katalyse
Jahresbericht 2007 - Leibniz-Institut für Katalyse
Jahresbericht 2007 - Leibniz-Institut für Katalyse
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Oxidationen Aromatenveredelung<br />
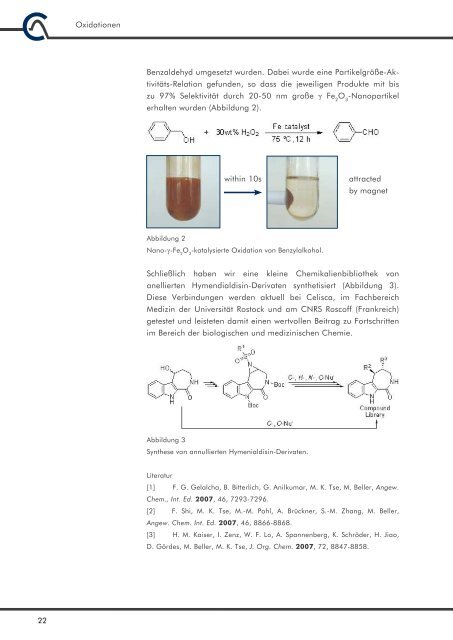
Benzaldehyd umgesetzt wurden. Dabei wurde eine Partikelgröße-Aktivitäts-Relation<br />
gefunden, so dass die jeweiligen Produkte mit bis<br />
zu 97% Selektivität durch 20-50 nm große γ Fe O -Nanopartikel<br />
2 3<br />
erhalten wurden (Abbildung 2).<br />
within 10s attracted<br />
by magnet<br />
Abbildung 2<br />
Nano-γ-Fe O -katalysierte Oxidation von Benzylalkohol.<br />
2 3<br />
Schließlich haben wir eine kleine Chemikalienbibliothek von<br />
anellierten Hymendialdisin-Derivaten synthetisiert (Abbildung 3).<br />
Diese Verbindungen werden aktuell bei Celisca, im Fachbereich<br />
Medizin der Universität Rostock und am CNRS Roscoff (Frankreich)<br />
getestet und leisteten damit einen wertvollen Beitrag zu Fortschritten<br />
im Bereich der biologischen und medizinischen Chemie.<br />
Abbildung 3<br />
Synthese von annullierten Hymenialdisin-Derivaten.<br />
Literatur<br />
[1] F. G. Gelalcha, B. Bitterlich, G. Anilkumar, M. K. Tse, M. Beller, Angew.<br />
Chem., Int. Ed. <strong>2007</strong>, 46, 7293-7296.<br />
[2] F. Shi, M. K. Tse, M.-M. Pohl, A. Brückner, S.-M. Zhang, M. Beller,<br />
Angew. Chem. Int. Ed. <strong>2007</strong>, 46, 8866-8868.<br />
[3] H. M. Kaiser, I. Zenz, W. F. Lo, A. Spannenberg, K. Schröder, H. Jiao,<br />
D. Gördes, M. Beller, M. K. Tse, J. Org. Chem. <strong>2007</strong>, 72, 8847-8858.<br />
Aromatenveredelung<br />
Zielsetzung<br />
Die katalytische Funktionalisierung von Arylhalogeniden und<br />
ähnlichen Verbindungen bietet einen direkten Zugang zu<br />
aromatischen Aminen und Ethern, arylierten Olefinen, Biarylen,<br />
Benzaldehyden, Benzonitrilen usw. Derartige substituierte Aromaten<br />
sind als Pharmazeutika, Agrochemikalien und Feinchemikalien von<br />
enormer Bedeutung.<br />
In unserer Gruppe werden neue Katalysatorsysteme <strong>für</strong> die Veredelung<br />
von Ar–X-Verbindungen, insbesondere von industriell besonders<br />
interessanten Arylchloriden, entwickelt [1]. Die Anwendung dieser<br />
Modellsysteme auf „reale“ Strukturen, insbesondere zur Synthese von<br />
Pharma-Intermediaten, ist ein weiteres Ziel unserer Arbeiten.<br />
22 23<br />
Ergebnisse<br />
Auf den Gebieten Cyanierung von Arylhalogeniden und Synthese von<br />
Diaryl- sowie Alkylarylethern wurden in industriellen Kooperationen<br />
v.a. Intermediate <strong>für</strong> die Feinchemie und die pharmazeutische<br />
Industrie (z.B. Diafenthiuron [2]) bearbeitet.<br />
Für die Sonogashira-Reaktion von<br />
Arylbromiden und –chloriden wurden<br />
neue Katalysatorsysteme entwickelt, die<br />
auf den beiden Ligandklassen cataCXium<br />
A (BuPAd ) und cataCXium P beruhen.<br />
2<br />
Liganden des nebenstehenden Typs<br />
(cataCXium P) konnten auch <strong>für</strong> die<br />
Synthese von Phenolen und Anilinen aus<br />
den entsprechenden Halogenaromaten<br />
und Wasser bzw. Ammoniak erfolgreich<br />
eingesetzt werden. Hier<strong>für</strong> ist der<br />
richtige sterische Anspruch am P-Donor<br />
von entscheidender Bedeutung. In der<br />
Literatur gibt es deshalb bisher auch fast<br />
keine anderen Katalysatorsysteme <strong>für</strong> diese Reaktionen. Die einfache<br />
Synthese von Phenolen und Anilinen ist v.a. technisch von erheblicher<br />
Bedeutung.<br />
Themenleiter:<br />
Dr. Alexander Zapf<br />
Tel.: (0381) 1281 - 122<br />
Fax: (0381) 128151 - 122<br />
alexander.zapf@ catalysis.de<br />
Kooperationspartner:<br />
TU München<br />
Prof. Dr. Kalinin, Moskau