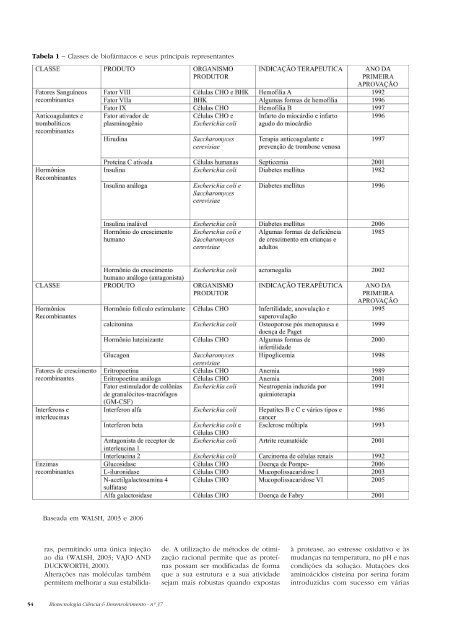
Tabela 1 – Classes de biofármacos e seus principais representantesBaseada em WALSH, 2003 e 2006ras, permitindo uma única injeçãoao dia (WALSH, 2003; VAJO ANDDUCKWORTH, 2000).Alterações nas moléculas tambémpermitem melhorar a sua estabilidade.A utilização de métodos de otimizaçãoracional permite que as proteínaspossam ser modificadas de formaque a sua estrutura e a sua atividadesejam mais robustas quando expostasà protease, ao estresse oxidativo e àsmudanças na temperatura, no pH e nascondições da solução. Mutações dosaminoácidos cisteína por serina foramintroduzidas com sucesso em várias54 <strong>Biotecnologia</strong> Ciência & <strong>Desenvolvimento</strong> - nº <strong>37</strong>
proteínas terapêuticas como, por exemplo,com o interferon beta 1b (MARK etal., 1984; MARSHALL et al., 2003).Uma ferramenta que tem sido utilizadapara alterar a farmacocinética de algunsbiofármacos é a peguilação, um processoem que cadeias de polietilenoglicolsão ligadas aos peptídeos e proteínas.Em geral, a peguilação reduz avelocidade de clearance plasmático porreduzir a degradação metabólica e acaptação mediada pelo receptor da proteínada circulação sistêmica. Esta técnicatambém melhora o perfil de segurançadas proteínas por conferir umaproteção antigênica e imunogênica aosseus epitopos. Vários biofármacos estãono mercado na forma peguiladacomo o interferon alfa (PEGasys ® ePEG-Intron ® ), o hormônio do crescimento(Somavert ® ) e a asparaginase (Oncaspar® ) (MARSHALL et al., 2003;FROKJAER AND OTZEN, 2005; HARRISAND CHESS, 2003).2. DIFICULDADES NAADMINISTRAÇÃODE BIOFÁRMACOSAs proteínas e peptídeos têm proporcionadoum crescente interesse devidoao seu papel na fisiopatologia e ao seuprogresso nas áreas de biotecnologia ebioquímica. O uso dessas moléculas emmedicina, no entanto, tem sido limitadodevido a sua baixa biodisponibilidade,a qual resulta da sua baixa estabilidadefrente às enzimas proteolíticase à degradação hidrolítica, da baixa permeabilidade,e da curta meia-vida nacirculação sistêmica (REIS et al., 2006).Desde 1987, Carey já enfatizava queuma das principais limitações na utilizaçãodas proteínas recombinantes naclínica era a questão da impossibilidadede administração por via oral. Vinteanos depois, esse continua a ser, semdúvida, um ponto a ser totalmente solucionado.A via oral é a rota de administração demedicamentos preferida e mais amplamenteutilizada. No entanto, ela geralmentenão está disponível para a liberaçãode macromoléculas tais como proteínas.A instabilidade inerente das proteínasao trato gastrintestinal, assimcomo a baixa permeabilidade atravésdas membranas biológicas devido à altamassa molecular e à superfície polar características,implicam no tratamentopela via parenteral (FROKJAER ANDOTZEN, 2005; JORGENSEN et al., 2006).No entanto, essa via apresenta algunsinconvenientes ao paciente, especialmentenos casos crônicos, o que diminuia adesão ao tratamento, comprometendo,assim, o resultado esperado.Muitos esforços de pesquisa estão sendofeitos para melhorar a adesão dopaciente, seja através do emprego devias alternativas de administração oupor redução da freqüência de injeções.A maioria dos medicamentos a base deproteínas é formulada como suspensõesou soluções aquosas prontas para o usoou como pó liofilizado para reconstituiçãodo produto. A formulação de proteínasdepende do conhecimento dassuas características físico-quimicas e biológicas,incluindo estabilidade químicae física, imunogenicidade e propriedadesfarmacocinéticas. A atividade terapêuticade proteínas é altamente dependenteda sua estrutura conformacional.No entanto, a estrutura da proteínaé flexível e sensível a condições externas,o que significa que a sua produção,formulação e manipulação necessitemde atenção especial na otimizaçãoda eficácia e da segurança, incluindoa minimização da resposta imune(FROKJAER AND OTZEN, 2005).De uma perspectiva de formulação, asproteínas são moléculas complexas edesafiadoras para o desenvolvimento desistemas de liberação de fármacos. Osucesso de uma formulação dependeda capacidade da proteína em mantersua estrutura nativa e atividade durantea preparação e a liberação no organismo,assim como durante o período deestocagem. Algumas proteínas precisamde liberação sustentada, enquanto outrasrequerem uma liberação controlada,imediata ou pulsada. A liberaçãopode ser alcançada utilizando diferentessistemas particulados de liberaçãode fármacos, tais como as micro e nanopartículaspoliméricas, os hidrogéis,os lipossomas e as emulsões (JORGEN-SEN et al., 2006 ).A demanda por melhores formas paraa administração de proteínas tem resultadona pesquisa pelo desenvolvimentode tecnologias farmacêuticas,e empresasfocadas nos métodos de liberaçãode fármacos têm crescido a cadaano. A maioria das proteínas que estãono mercado podem ser consideradascomo candidatas para os novos métodosde liberação, uma vez que são facilmenteliberadas pelas vias tradicionaiscomo na forma de injeções subcutâneas(SC), intramusculares (IM) ouintravenosas (IV) e têm a sua farmacologiabem caracterizada. Devem ser consideradosfatores como a competiçãode mercado, a conveniência, a adesãodo paciente, a necessidade de liberaçãotópica ou local, a toxicidade sistêmica eas questões de segurança. Alguns métodosestão sendo desenvolvidos e estãodirecionados para a competição de mercadopara os biofármacos aprovados,como a insulina, o hormônio do crescimentohumano, os interferons e a eritropoietina.Esses sistemas objetivam umamelhoria na adesão do paciente ao tratamento.Em muitos casos, a administraçãotópica de proteínas constitui uma viapreferencial à sistêmica, pois esta últimanão promove níveis significativos no localda doença. Em determinadas situaçõessão necessários elevados níveis sistêmicospara alcançar efeito local nos tecidosalvo, o que muitas vezes causa efeitostóxicos indesejáveis. Devem ser aindaconsideradas questões como o impactodos processos de produção do sistemade liberação na integridade da proteína,e também a integridade da proteínaapós sua liberação no local de administração.A administração de proteínas degradadaspode representar além dos efeitoscolaterais, a perda da potência. Paraa administração sistêmica de proteínas, aquantidade liberada na circulação é dependenteda eficiência do sistema de liberaçãoe da biologia intrínseca da viade administração (CLELAND et al., 2001).Quando são consideradas as novas opçõespara administração de proteínas, avia mais comumente abordada é a parenteral,devido ao maior número de estudosem animais e aos testes clínicos quegarantem uma maior segurança e eficácia.Os pulmões têm sido extensivamenteestudados como uma via de administraçãode proteínas pela a sua grande áreade superfície e por permitir uma rápidaabsorção devido ao contato próximo entreos alvéolos e a circulação (GONDA,2000; CLELAND et al., 2001). A insulinaé, sem dúvida, o protótipo biofarmacêutico,tendo sido o Exubera ® (Pfizer) a primeiraformulação inalatória aprovadapelo FDA (Food and Drug Administration),e que permite administrar uma formade insulina em pó seco. Cerca de 40%da proteína chega ao pulmão profundoe 10% é biodisponível. O início de açãoda insulina inalada é mais rápido do quea injetável de ação rápida, o que permitea sua utilização pré-prandial (MCMAHONAND ARKY, 2007). Estudos clínicos demonstraramuma equivalência significativacomparativamente a várias formas deinsulina convencional. A insulina inaladaapresentou-se efetiva, bem tolerada emelhor aceita em pacientes com diabetestipo 1 e tipo 2 (HOLLANDER et al., 2004;WANNMACHER, 2005).<strong>Biotecnologia</strong> Ciência & <strong>Desenvolvimento</strong> - nº <strong>37</strong> 55
- Page 1 and 2:
Biotecnologia Ciência & Desenvolvi
- Page 3 and 4: BC&D - Como o senhor avalia aposiç
- Page 5 and 6: dicamentos.Os anticorpos monoclonai
- Page 8 and 9: PesquisaLUCIFERASES DE VAGALUMESPes
- Page 10 and 11: ger & McElroy, 1965; Hastings,1995)
- Page 12 and 13: ciferases de elaterídeos e fengod
- Page 14 and 15: utilizados como marcadores sensíve
- Page 16: 5,5-dimethyloxyluciferin. JACS 124:
- Page 19 and 20: Rev. Bras. Entom. 33: 359-366..Vivi
- Page 21 and 22: vimento de pesquisas científicas (
- Page 23 and 24: ubíquos) é inferior a 100, envolv
- Page 25 and 26: (tais como genes, operons, grupos[c
- Page 27 and 28: evolution of mycobacterialpathogeni
- Page 29 and 30: GLOSSÁRIOAlgoritmo. Procedimento o
- Page 31 and 32: oócito e melhora o posterior desen
- Page 33 and 34: Figura 7: Ilustração de resultado
- Page 35 and 36: 10. COELHO, L. A.; ESPER, C. R.;GAR
- Page 37 and 38: - permitir a rápida liberação do
- Page 39 and 40: de crescimento, quatro grupos de mi
- Page 41 and 42: skovia xanthineolytica LL-G109 (And
- Page 43 and 44: Tabela 1. Purificação da β-1,3 g
- Page 45 and 46: depende em parte, da venda dos subp
- Page 47 and 48: tipo poro-canal-G1pF atua por sensi
- Page 49 and 50: eutilização de células imobiliza
- Page 51 and 52: ANP - AGENCIA NACIONAL DE PETROLEO
- Page 53: inantes, incluindo eritropoetinas,
- Page 57 and 58: capsuladas, a redução de efeitos
- Page 59 and 60: Zhang W, Rong Z, Chen H, Jiang X.Br
- Page 61 and 62: FIGURA 1. Estrutura “Markush”Ma
- Page 63 and 64: Figura 2, todos os compostos origin
- Page 65 and 66: Figura 2. O filo Porifera é dividi
- Page 67 and 68: Figura 4. Microscopia eletrônica d
- Page 69 and 70: plication of genomics to uncultured
- Page 71 and 72: viabilidade celular (1) a técnica
- Page 73 and 74: Gráfico 02: Média das viabilidade
- Page 75 and 76: Tabela 04: Análise das médias de
- Page 77 and 78: icus blazei. Atualmente é também
- Page 79: 5. Agaricus sylvaticus é sinônimo