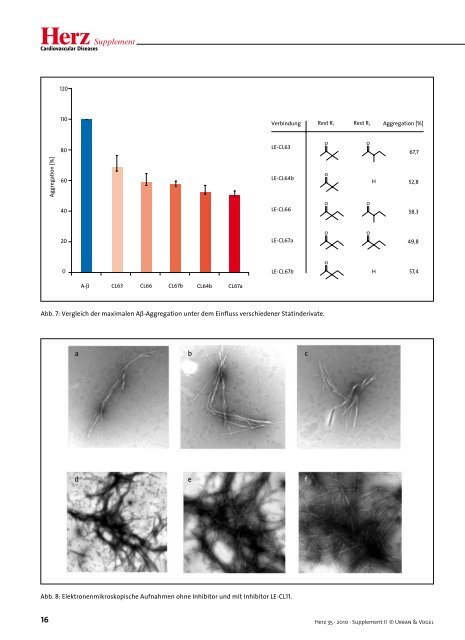
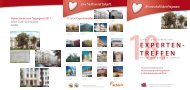
Herz Supplement Cardiovascular Diseases Aggregation [%] 120 110 80 60 40 20 0 A-β CL63 CL66 CL67b CL64b CL67a Verbindung Rest R1 Rest R2 Aggregation [%] 16 Herz 35 · 2010 · Supplement II © Urban & Vogel LE-CL63 LE-CL64b LE-CL66 LE-CL67a LE-CL67b Abb. 7: Vergleich der maximalen Aβ-Aggregation unter dem Einfluss verschiedener Statinderivate. a b c d e f Abb. 8: Elektronenmikroskopische Aufnahmen ohne Inhibitor und mit Inhibitor LE-CL11. 0 0 0 0 0 0 0 0 H H 67,7 52,8 58,3 49,8 57,4
Der durch Fluoreszenzmessungen erkannte Einfluss der Substanzen auf die Amyloidaggregation wurde schließlich auch durch elektronenmikroskopische Aufnahmen mit Negativkontrastierung bestätigt, welche es ermöglichten, die Struktur und Form der gebildeten βAmyloid Fibrillen zu sehen. Hierbei wurde den Proben kein Fluoreszenzindikator zugesetzt. Auch hier wiesen Proben, die 90 Stunden mit dem Inhibitor LE-CL11 (Abb. 8 a, b, c) behandelt waren, eine im Vergleich zu unbehandelten Kontrollproben (Abb. 8 d, e, f) veränderte und stark reduzierte Aβ40 Aggregation auf, was wiederum eine verminderte Plaquebildung in Aussicht stellt. Resümee Es ist gelungen, Statine chemisch so zu verändern, dass diese neuen Substanzen die Aggregation <strong>von</strong> amyloidogenem AßPolypeptid signifikant inhibieren. Vor allem resultierte aus der Nitratoacylierung zu einem SimvastatinNitratHybrid ein besonders potenter Inhibitor. Der Vergleich aller getesteten Substanzen lässt bisher keine deutliche StrukturWirkungsBeziehung erkennen. Auch bleibt bislang ungeklärt, ob und gegebenenfalls welchen Einfluss das organische Nitrat auf die Inhibition der direkten AßAggregation ausübt. Eine erste Antwort auf die Frage, ob die neuen Statinderivate auch klinisch erfolgreiche, neuartige AlzheimerTherapeutika sein können, soll nun durch InvivoUntersuchungen an transgenen Tieren gegeben werden. n Summary Statins are classically used in the treatment and prevention of hypercholesterolaemia due to their ability to reduce cholesterol synthesis. They act by blocking the HMG CoA reductase, which is the rate limiting enzyme in cholesterol synthesis. However, some studies have suggested the possible use of statins as potential therapeutics in the treatment of Alzheimer’s disease. Different pathways apart from their inhibitory activity on HMGCoA reductase have been explored. It has been shown that statins in Herz 35 · 2010 · Supplement II © Urban & Vogel fluence the release of βamyloid, which aggregates to senile plaques, a pathological hallmark of AD. Although the exact mechanism still remains unknown, this has been attributed to decreased cholesterol levels, as well as decreased isoprenoid biosynthesis, which directly influences APP processing. We have tested statin derivatives direct effect on amyloidaggregation as another possible pathway of their mode of action. Moreover we explored the possibility that modifying chemically the statins at their free lactonichydroxygroup could lead to compounds with inhibitory potency on direct Aβaggregation and hence prevent plaque formation. Surprisingly, results showed that a nitratoacylatedstatin derivative (LECL11) potently reduces amyloid aggregation down to 35% of untreated control. Keywords: statins – organic nitrates – statin nitrate hybride molecule – Alzheimer’s disease Literatur 1. Jick H, Zornberg GL, Seshadri S, Drachman DA. Statins and the risk of dementia. The Lancet 2000;356: 1627–31 2. Parson RB, Farrant JK, Price GC, Subramaniam D, Austen BM. Regulation of the lipodation of β-secretase by statins. Biochem Soc Trans 2007;35(3):577–582 3. Ostrowski SM, Wilkinson BJ, Golde TE, Landreth G. Statins reduce Amyloid-β production through inhibition of protein isoprenylation. J Biol Chem 2007; 282(37):26832–44 4. Gellermann G, Ullrich K, Tannert A, Unger C, Habicht G, Sauter S, Hortschansky P, Horn U, Möllmann U, Decker M, Lehmann J, Fändrich M. Alzheimer-like plaque formation by human macrophages is reduced by fibrillation inhibitors and lovastatin. J Mol Biol 2006;360:251–257 Für die Verfasser: Jochen Lehmann Pharmazeutisches Institut der Friedrich-Schiller- Universität Jena Lehrstuhl für Pharmazeutische/Medizinische Chemie Philosophenweg 12 07747 Jena, Germany Tel.: +49 (0) 3641 949825 Fax: +49 (0) 3641 949802 E-Mail: j.lehmann@uni-jena.de Organische Nitrate 17