You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
5-6 liter vér esetén kb. 700-960 g Hb áll a test<br />
rendelkezésére. Mivel a Hb 0,334% vasat tartalmaz,<br />
3 gramm vas (a test teljes vastartalmának 70%-a)<br />
van benne lekötve.<br />
A Hb-molekulák mindegyike egy-egy összetett<br />
fehérjetest. Egy fehérjekomponens, a globin (lat.<br />
globus = gömb) alkotja, amely négy darab, egy-<br />
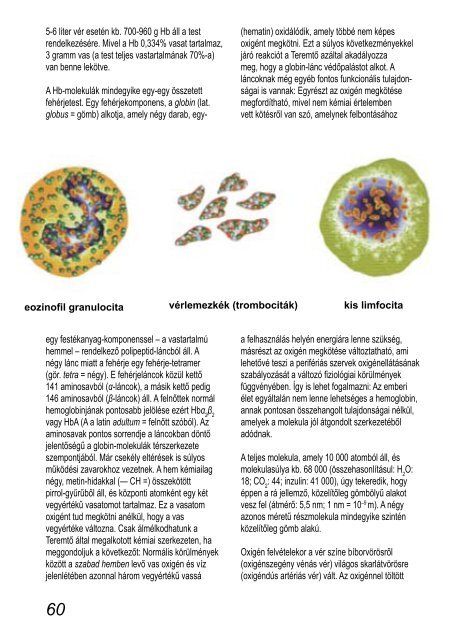
eozinofil granulocita vérlemezkék (trombociták) kis limfocita<br />
egy festékanyag-komponenssel – a vastartalmú<br />
hemmel – rendelkező polipeptid-láncból áll. A<br />
négy lánc miatt a fehérje egy fehérje-tetramer<br />
(gör. tetra = négy). E fehérjeláncok közül kettő<br />
141 aminosavból (α-láncok), a másik kettő pedig<br />
146 aminosavból (β-láncok) áll. A felnőttek normál<br />
hemoglobinjának pontosabb jelölése ezért Hbα 2 β 2<br />
vagy HbA (A a latin adultum = felnőtt szóból). Az<br />
aminosavak pontos sorrendje a láncokban döntő<br />
jelentőségű a globin-molekulák térszerkezete<br />
szempontjából. Már csekély eltérések is súlyos<br />
működési zavarokhoz vezetnek. A hem kémiailag<br />
négy, metin-hidakkal (— CH =) összekötött<br />
pirrol-gyűrűből áll, és központi atomként egy két<br />
vegyértékű vasatomot tartalmaz. Ez a vasatom<br />
oxigént tud megkötni anélkül, hogy a vas<br />
vegyértéke változna. Csak álmélkodhatunk a<br />
Teremtő által megalkotott kémiai szerkezeten, ha<br />
meggondoljuk a következőt: Normális körülmények<br />
között a szabad hemben levő vas oxigén és víz<br />
jelenlétében azonnal három vegyértékű vassá<br />
60<br />
(hematin) oxidálódik, amely többé nem képes<br />
oxigént megkötni. Ezt a súlyos következményekkel<br />
járó reakciót a Teremtő azáltal akadályozza<br />
meg, hogy a globin-lánc védőpalástot alkot. A<br />
láncoknak még egyéb fontos funkcionális tulajdonságai<br />
is vannak: Egyrészt az oxigén megkötése<br />
megfordítható, mivel nem kémiai értelemben<br />
vett kötésről van szó, amelynek felbontásához<br />
a felhasználás helyén energiára lenne szükség,<br />
másrészt az oxigén megkötése változtatható, ami<br />
lehetővé teszi a perifériás szervek oxigénellátásának<br />
szabályozását a változó fiziológiai körülmények<br />
függvényében. Így is lehet fogalmazni: Az emberi<br />
élet egyáltalán nem lenne lehetséges a hemoglobin,<br />
annak pontosan összehangolt tulajdonságai nélkül,<br />
amelyek a molekula jól átgondolt szerkezetéből<br />
adódnak.<br />
A teljes molekula, amely 10 000 atomból áll, és<br />
molekulasúlya kb. 68 000 (összehasonlításul: H 2 O:<br />
18; CO 2 : 44; inzulin: 41 000), úgy tekeredik, hogy<br />
éppen a rá jellemző, közelítőleg gömbölyű alakot<br />
vesz fel (átmérő: 5,5 nm; 1 nm = 10 –9 m). A négy<br />
azonos méretű részmolekula mindegyike szintén<br />
közelítőleg gömb alakú.<br />
Oxigén felvételekor a vér színe bíborvörösről<br />
(oxigénszegény vénás vér) világos skarlátvörösre<br />
(oxigéndús artériás vér) vált. Az oxigénnel töltött