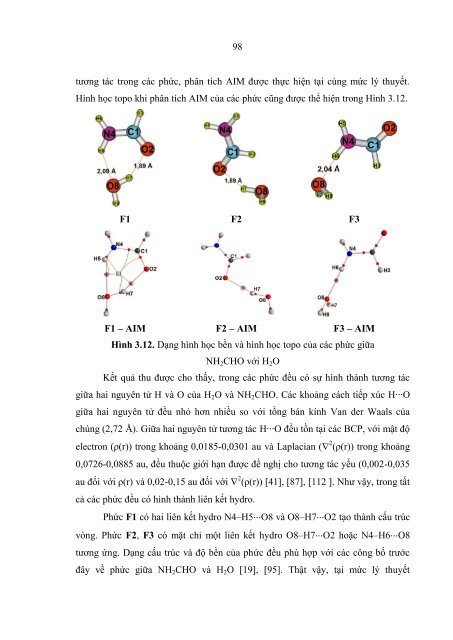
98 tương tác trong các phức, phân tích AIM được thực hiện tại cùng mức lý thuyết. Hình học topo khi phân tích AIM của các phức cũng được thể hiện trong Hình 3.12. F1 F2 F3 F1 – AIM F2 – AIM F3 – AIM Hình 3.12. Dạng hình học bền và hình học topo của các phức giữa NH 2 CHO với H 2 O Kết quả thu được cho thấy, trong các phức đều có sự hình thành tương tác giữa hai nguyên tử H và O của H 2 O và NH 2 CHO. Các khoảng cách tiếp xúc H∙∙∙O giữa hai nguyên tử đều nhỏ hơn nhiều so với tổng bán kính Van der Waals của chúng (2,72 Å). Giữa hai nguyên tử tương tác H∙∙∙O đều tồn tại các BCP, với mật độ electron (ρ(r)) trong khoảng 0,0185-0,0301 au và Laplacian ( 2 (ρ(r)) trong khoảng 0,0726-0,0885 au, đều thuộc giới hạn được đề nghị cho tương tác yếu (0,002-0,035 au đối với ρ(r) và 0,02-0,15 au đối với 2 (ρ(r)) [41], [87], [112 ]. Như vậy, trong tất cả các phức đều có hình thành liên kết hydro. Phức F1 có hai liên kết hydro N4–H5O8 và O8–H7O2 tạo thành cấu trúc vòng. Phức F2, F3 có mặt chỉ một liên kết hydro O8–H7O2 hoặc N4–H6O8 tương ứng. Dạng cấu trúc và độ bền của phức đều phù hợp với các công bố trước đây về phức giữa NH 2 CHO và H 2 O [19], [95]. Thật vậy, tại mức lý thuyết
99 B3LYP/aug-cc-pVTZ, năng lượng tương tác khi hiệu chỉnh BSSE của F1, F2 lần lượt là -35,17, -24,49 kJ.mol -1 , (theo [19]: tại MP2/6-311++G(d,p), giá trị này là - 32,84; -24,09 kJ.mol -1 ). Năng lượng tương tác hiệu chỉnh cả ZPE và BSSE của F2, F3 là -16,61 và -13,41 kJ.mol -1 (theo [95]: tại MP2/aug-cc-pVTZ là -15,73 và - 13,81 kJ.mol -1 ). Bảng 3.24. Năng lượng tương tác (ΔE, ΔE * , kJ.mol -1 ), năng lượng của một liên kết hydro (E H∙∙∙O , kJ.mol -1 ), sự thay đổi độ dài (r, Å) và tần số dao động hóa trị (,cm - 1 ) của liên kết tham gia liên kết hydro so với trong monome ban đầu, và phân tích NBO của các phức giữa NH 2 CHO và H 2 O E inter (n(O) %s Phức ΔE ΔE * E H∙∙∙O ∆r * →*(N(O) (O/N) –H) -17,1 0,0073 -119,2 0,0077 1,41 3,85 F1 -25,0 -24,6 -32,4 a 0,0152 a -298,5 a 0,0223 a 4,98 a 10,32 a F2 -16,9 -16,6 -32,5 0,0117 -236,3 0,0182 4,68 9,77 F3 -13,7 -13,4 -19,4 0,0058 -98,9 0,0089 1,72 5,42 a cho liên kết O8–H7 trong F1 Bảng 3.24 cho thấy, các phức thu được khá bền, F1 bền nhất, đến F2, và kém bền nhất là F3. Năng lượng của liên kết hydro O–HO trong hai phức F1 và F2 xấp xỉ nhau, còn năng lượng liên kết hydro N–HO trong F3 âm hơn một ít so với trong F1. Sự đóng góp của hai loại liên kết hydro này làm cho năng lượng tương tác của F1 âm hơn rất nhiều so với hai phức còn lại. Như vậy, liên kết hydro kiểu O– HO bền hơn, đóng góp lớn hơn đến độ bền phức F1 so với liên kết hydro N– HO. Năng lượng tương tác siêu liên hợp ngoại phân tử trong F1 E inter (n(O2)→*(O8–H7) lớn vượt hẳn E inter (n(O8)→*(N4–H5) cũng minh chứng cho nhận định này (bảng 3.24). Xem xét sự thay đổi độ dài liên kết, tần số dao động hóa trị của liên kết N4– H5(6) và O8–H7 so với monome ban đầu cho thấy, tất cả các liên kết đều có r > 0,
- Page 1 and 2:
BỘ GIÁO DỤC VÀ ĐÀO TẠO TR
- Page 3 and 4:
LỜI CAM ĐOAN Tôi xin cam đoan
- Page 5 and 6:
MỤC LỤC LỜI CAM ĐOAN LỜI C
- Page 7 and 8:
2.3.3. Liên kết hydro chuyển d
- Page 9 and 10:
3.8. Nghiên cứu cấu trúc, đ
- Page 11 and 12:
PA (Proton Affinity) Ái lực prot
- Page 13 and 14:
vào liên kết hydro trong các m
- Page 15 and 16:
DANH MỤC CÁC HÌNH ẢNH, ĐỒ
- Page 17 and 18:
1 MỞ ĐẦU 1. Lý do chọn đ
- Page 19 and 20:
3 Hai nhóm nghiên cứu chính v
- Page 21 and 22:
5 siêu liên hợp nội, ngoại
- Page 23 and 24:
7 ứng dụng trong tách, chiết
- Page 25 and 26:
9 r iA : khoảng cách giữa elec
- Page 27 and 28:
11 cực trị của hàm sóng kh
- Page 29 and 30:
13 năng lượng tương quan. Có
- Page 31 and 32:
15 Theo công thức Slater, năng
- Page 33 and 34:
17 E (1.25) 0 0 0 Ĥ 0 n n n +
- Page 35 and 36:
19 đơn là zero. Toán tử Tˆ 2
- Page 37 and 38:
21 1 (r ) (r ) 1 2 drdr 1 2
- Page 39 and 40:
23 Sự gần đúng LSDA đánh gi
- Page 41 and 42:
25 Nếu một phân tử có thể
- Page 43 and 44:
27 laplacian và 2 (ρ(r)) < 0. Ng
- Page 45 and 46:
29 cực đại đến khối nguy
- Page 47 and 48:
31 Năng lượng tương tác Hart
- Page 49 and 50:
33 Waals được đặc trưng r
- Page 51 and 52:
35 Hình 2.2. Tương tác lưỡng
- Page 53 and 54:
37 và ảnh hưởng tương đố
- Page 55 and 56:
39 thơm thiếu electron (vì vòn
- Page 57 and 58:
41 trị, khó bị biến dạng v
- Page 59 and 60:
43 nguyên tử có độ âm đi
- Page 61 and 62:
45 Liên kết hydro chuyển dời
- Page 63 and 64: 47 được từ thực nghiệm. T
- Page 65 and 66: 49 - Xem xét sự phụ thuộc c
- Page 67 and 68: 51 động hoá trị được tín
- Page 69 and 70: 53 hiệu chỉnh ZPE và BSSE, và
- Page 71 and 72: 55 Đối với phức P6, tương
- Page 73 and 74: 57 CO 2 ∙∙∙C 2 H 3 X không x
- Page 75 and 76: 59 3.1.2.2. Sự thay đổi độ
- Page 77 and 78: 61 trong các phức trên. Đáng
- Page 79 and 80: 63 a) Các phức cis-XCH=CHX∙∙
- Page 81 and 82: 65 Bảng 3.7. Phân tích AIM củ
- Page 83 and 84: 67 lượng hình thành phức l
- Page 85 and 86: 69 trong CH 2 =CH 2 ∙∙∙CO 2 n
- Page 87 and 88: 71 Sự tồn tại của tương t
- Page 89 and 90: 73 các phần tử cho và nhận
- Page 91 and 92: 75 M1F M1Cl M1Br M1F-AIM M1Cl-AIM M
- Page 93 and 94: 77 Kết quả bảng 3.12 cho th
- Page 95 and 96: 79 pVTZ//MP2/6-311++G(2d,2p) và CC
- Page 97 and 98: 81 là -14,4 kJ.mol -1 tại MP2/au
- Page 99 and 100: 83 kết C-H giảm theo thứ tự
- Page 101 and 102: 85 trong việc làm bền phức.
- Page 103 and 104: 87 H1 H2 H3 H4 H1 - AIM H2 - AIM H3
- Page 105 and 106: 89 Bảng 3.19. Năng lượng tư
- Page 107 and 108: 91 Bảng 3.21. Phân tích NBO cho
- Page 109 and 110: 93 Bảng 3.22. Khoảng cách tư
- Page 111 and 112: 95 NBO cho monome và các phức c
- Page 113: 97 obitan n(N) và (CN) của XCN t
- Page 117 and 118: 101 F1X F2X F3X F3CH 3 F1X-AIM F2X-
- Page 119 and 120: 103 Bảng 3.26. PA(O), DPE(N-H) v
- Page 121 and 122: 105 Bảng 3.27. Sự thay đổi
- Page 123 and 124: 107 Năng lượng tương tác c
- Page 125 and 126: 109 Bảng 3.29. Các thông số t
- Page 127 and 128: 111 3.6.2. Sự thay đổi độ d
- Page 129 and 130: 113 tự, trong hình học V2, khi
- Page 131 and 132: 115 C1(H-H) C1(F-H) C1(Cl-H) C1(Br-
- Page 133 and 134: 117 F) tương ứng là -14,6 và
- Page 135 and 136: 119 (độ bazơ tại N trong FCN
- Page 137 and 138: 121 kết C-H trong phần tử cho
- Page 139 and 140: 123 Hình 3.18. Mối quan hệ c
- Page 141 and 142: 125 Mối quan hệ giữa năng l
- Page 143 and 144: 127 Bảng 3.37 cho thấy, năng l
- Page 145 and 146: 129 Khi phức hình thành, có s
- Page 147 and 148: 131 Hình 3.20. Cấu trúc bền c
- Page 149 and 150: 133 Bảng 3.40. Kết quả phân
- Page 151 and 152: 135 khi hình thành phức làm t
- Page 153 and 154: 137 Hình 3.21. Hình học topo c
- Page 155 and 156: 139 - Tất cả liên kết hydro
- Page 157 and 158: 141 Cl, Br), độ bền các phứ
- Page 159 and 160: DANH MỤC CÁC CÔNG TRÌNH CÔNG
- Page 161 and 162: TÀI LIỆU THAM KHẢO Tiếng Vi
- Page 163 and 164: 20. Bader R. F. W. (1990), Atoms in
- Page 165 and 166:
41. Dethlefs K. M., Hobza P. (2000)
- Page 167 and 168:
64. Hibbert F., Emsley J. (1990),
- Page 169 and 170:
86. Khanh P. N., Ngan V. T., Man N.
- Page 171 and 172:
106. Nishio M. (2011), “The CH/π
- Page 173 and 174:
126. Scheiner S. (2011), “Weak H-
- Page 175 and 176:
144. Vieceli J., Benjamin I. (2003)
- Page 177 and 178:
O, -3.5895701677, 0., -1.7532670765
- Page 179 and 180:
P4Cl C, -0.9185542917,-1.7582154418
- Page 181 and 182:
C, 0.0523383018, 0., 0.0579259512 H
- Page 183 and 184:
O, -2.3684545309, 0.8322611091, -0.
- Page 185 and 186:
H, 1.544488533, 1.0058527159, 1.760
- Page 187 and 188:
H, -1.9480373789, 1.6326156722, 1.4
- Page 189 and 190:
O, 3.5006214441, 0.6241457119, 0. O
- Page 191 and 192:
R = CH 3 , X = Cl C, 1.8252650463,
- Page 193 and 194:
H, -2.8665918784, 2.1713712054, -0.
- Page 195 and 196:
H, -3.4277792465,-1.8340412235,-0.3
- Page 197 and 198:
H, -2.0077062366,-0.449061949, 0. H
- Page 199 and 200:
H, 0.285936, -1.893647, 0. C1(F-H)
- Page 201 and 202:
O, 0.3708504274, 0.9757767063, 0. C
- Page 203 and 204:
N, -6.314802309, 0.4091180392, 0.05
- Page 205 and 206:
N, 0.6331385608, -1.7391609289,-0.0