NGHIÊN CỨU LÝ THUYẾT LIÊN KẾT HYDRO X–H∙∙∙O/N (X = C, N) BẰNG PHƯƠNG PHÁP HÓA HỌC LƯỢNG TỬ
https://drive.google.com/file/d/1JEB8TAlT8w0QlQh1855S4PkaNbgdN-Ap/view?usp=sharing
https://drive.google.com/file/d/1JEB8TAlT8w0QlQh1855S4PkaNbgdN-Ap/view?usp=sharing
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
123<br />
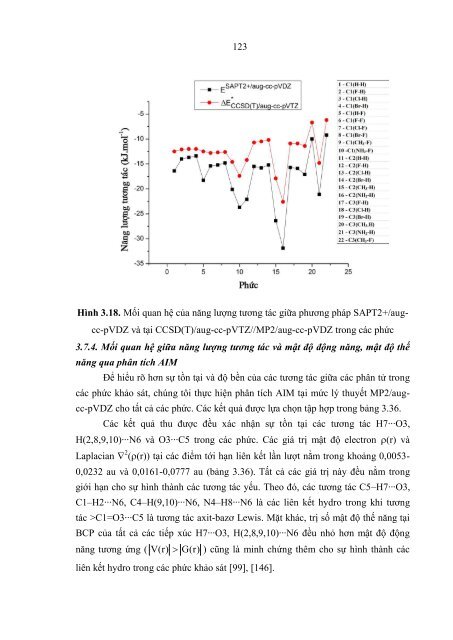
Hình 3.18. Mối quan hệ của năng lượng tương tác giữa phương pháp SAPT2+/augcc-pVDZ<br />
và tại CCSD(T)/aug-cc-pVTZ//MP2/aug-cc-pVDZ trong các phức<br />
3.7.4. Mối quan hệ giữa năng lượng tương tác và mật độ động năng, mật độ thế<br />
năng qua phân tích AIM<br />
Để hiểu rõ hơn sự tồn tại và độ bền của các tương tác giữa các phân tử trong<br />
các phức khảo sát, chúng tôi thực hiện phân tích AIM tại mức lý thuyết MP2/augcc-pVDZ<br />
cho tất cả các phức. Các kết quả được lựa chọn tập hợp trong bảng 3.36.<br />
Các kết quả thu được đều xác nhận sự tồn tại các tương tác H7∙∙∙O3,<br />
H(2,8,9,10)∙∙∙N6 và O3∙∙∙C5 trong các phức. Các giá trị mật độ electron (r) và<br />
Laplacian 2 ((r)) tại các điểm tới hạn liên kết lần lượt nằm trong khoảng 0,0053-<br />
0,0232 au và 0,0161-0,0777 au (bảng 3.36). Tất cả các giá trị này đều nằm trong<br />
giới hạn cho sự hình thành các tương tác yếu. Theo đó, các tương tác C5–H7∙∙∙O3,<br />
C1–H2∙∙∙N6, C4–H(9,10)∙∙∙N6, N4–H8∙∙∙N6 là các liên kết hydro trong khi tương<br />
tác >C1=O3∙∙∙C5 là tương tác axit-bazơ Lewis. Mặt khác, trị số mật độ thế năng tại<br />
BCP của tất cả các tiếp xúc H7∙∙∙O3, H(2,8,9,10)∙∙∙N6 đều nhỏ hơn mật độ động<br />
năng tương ứng ( V(r) G(r) ) cũng là minh chứng thêm cho sự hình thành các<br />
liên kết hydro trong các phức khảo sát [99], [146].