Download (4Mb) - tuprints
Download (4Mb) - tuprints
Download (4Mb) - tuprints
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
7.1. Ethanolamin<br />
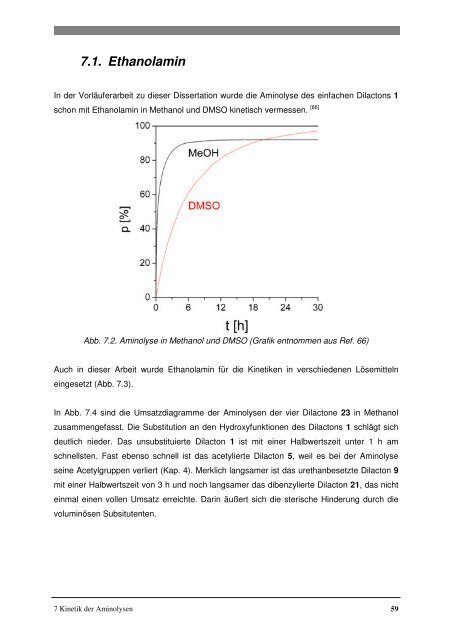
In der Vorläuferarbeit zu dieser Dissertation wurde die Aminolyse des einfachen Dilactons 1<br />
schon mit Ethanolamin in Methanol und DMSO kinetisch vermessen. [66]<br />
Abb. 7.2. Aminolyse in Methanol und DMSO (Grafik entnommen aus Ref. 66)<br />
Auch in dieser Arbeit wurde Ethanolamin für die Kinetiken in verschiedenen Lösemitteln<br />
eingesetzt (Abb. 7.3).<br />
In Abb. 7.4 sind die Umsatzdiagramme der Aminolysen der vier Dilactone 23 in Methanol<br />
zusammengefasst. Die Substitution an den Hydroxyfunktionen des Dilactons 1 schlägt sich<br />
deutlich nieder. Das unsubstituierte Dilacton 1 ist mit einer Halbwertszeit unter 1 h am<br />
schnellsten. Fast ebenso schnell ist das acetylierte Dilacton 5, weil es bei der Aminolyse<br />
seine Acetylgruppen verliert (Kap. 4). Merklich langsamer ist das urethanbesetzte Dilacton 9<br />
mit einer Halbwertszeit von 3 h und noch langsamer das dibenzylierte Dilacton 21, das nicht<br />
einmal einen vollen Umsatz erreichte. Darin äußert sich die sterische Hinderung durch die<br />
voluminösen Subsitutenten.<br />
7 Kinetik der Aminolysen 59