Degradação de Substâncias de Relevância Ambiental por ...
Degradação de Substâncias de Relevância Ambiental por ...
Degradação de Substâncias de Relevância Ambiental por ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
- O3S<br />
- O3S<br />
m/z 206<br />
N N<br />
HO<br />
.<br />
não <strong>de</strong>tectado<br />
- O3S<br />
[2 - H] -<br />
+<br />
- O3S<br />
.<br />
HO<br />
SO 3 -<br />
m/z 150.5<br />
SO3 -<br />
não <strong>de</strong>tectado<br />
O3<br />
[O]<br />
H2O<br />
- O3S<br />
O O -<br />
O3S<br />
- N2O; - O2 N N<br />
O<br />
HO<br />
intermediário ozoní<strong>de</strong>o<br />
não <strong>de</strong>tectado<br />
- O3S OH<br />
2a m/z 223<br />
não <strong>de</strong>tectado<br />
+<br />
SO 3 -<br />
- O3S<br />
HO<br />
HO<br />
2b m/z 159<br />
SO 3 -<br />
não <strong>de</strong>tectado<br />
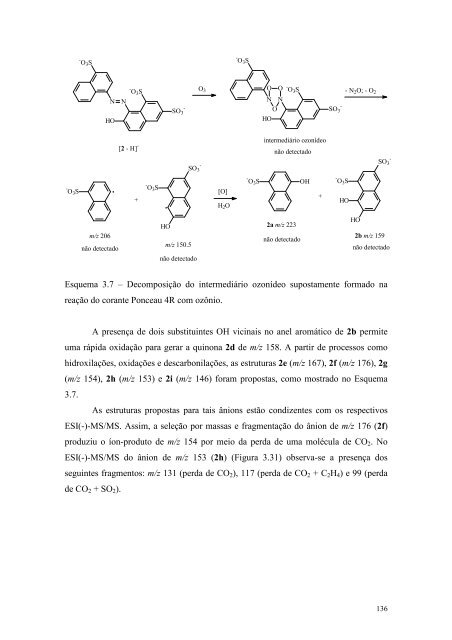
Esquema 3.7 – Decomposição do intermediário ozoní<strong>de</strong>o supostamente formado na<br />
reação do corante Ponceau 4R com ozônio.<br />
A presença <strong>de</strong> dois substituintes OH vicinais no anel aromático <strong>de</strong> 2b permite<br />
uma rápida oxidação para gerar a quinona 2d <strong>de</strong> m/z 158. A partir <strong>de</strong> processos como<br />
hidroxilações, oxidações e <strong>de</strong>scarbonilações, as estruturas 2e (m/z 167), 2f (m/z 176), 2g<br />
(m/z 154), 2h (m/z 153) e 2i (m/z 146) foram propostas, como mostrado no Esquema<br />
3.7.<br />
As estruturas propostas para tais ânions estão condizentes com os respectivos<br />
ESI(-)-MS/MS. Assim, a seleção <strong>por</strong> massas e fragmentação do ânion <strong>de</strong> m/z 176 (2f)<br />
produziu o íon-produto <strong>de</strong> m/z 154 <strong>por</strong> meio da perda <strong>de</strong> uma molécula <strong>de</strong> CO2. No<br />
ESI(-)-MS/MS do ânion <strong>de</strong> m/z 153 (2h) (Figura 3.31) observa-se a presença dos<br />
seguintes fragmentos: m/z 131 (perda <strong>de</strong> CO2), 117 (perda <strong>de</strong> CO2 + C2H4) e 99 (perda<br />
<strong>de</strong> CO2 + SO2).<br />
136