4 1.1. Las vitaminas<strong>de</strong>nominaron“vitamina A liposoluble” [7,8] , que finalmente resultaría ser unacombinación <strong>de</strong> <strong>la</strong>s vitaminas A y D. En los años subsiguientes se i<strong>de</strong>ntificaron<strong>la</strong> tiamina (vitamina B 1 ), <strong>la</strong> ribof<strong>la</strong>vina (vitamina B 2 ) y el ácido nicotínico.Poco <strong>de</strong>spués se <strong>de</strong>scubrió que estas vitaminas actúan como componentes fundamentales<strong>de</strong> algunos coenzimas. Por ejemplo, el enzima que ahora recibe elnombre <strong>de</strong> piruvato<strong>de</strong>scarboxi<strong>la</strong>sa, que cataliza <strong>la</strong> <strong>de</strong>scarboxi<strong>la</strong>ción <strong><strong>de</strong>l</strong> ácidopirúvico o acetal<strong>de</strong>hido y CO 2 en <strong>la</strong> fermentación alcohólica <strong><strong>de</strong>l</strong> azúcar por <strong>la</strong>levadura, precisa <strong>de</strong> un cofactor orgánico termoestable l<strong>la</strong>mado cocarboxi<strong>la</strong>sa,cuyo ais<strong>la</strong>miento consiguieron Kyger C. Lohmann y P. Schuster en 1936. Posteriormente,estos investigadores <strong>de</strong>scubrieron que <strong>la</strong> carboxi<strong>la</strong>sa contiene unamolécu<strong>la</strong> <strong>de</strong> tiamina, o vitamina B 1 . Muy pronto i<strong>de</strong>ntificaron a <strong>la</strong> ribof<strong>la</strong>vinay al ácido nicotínico como componentes importantes <strong>de</strong> otros coenzimas ynecesarios para <strong>la</strong> oxidación enzimática <strong>de</strong> los glúcidos. Estos <strong>de</strong>scubrimientos<strong>de</strong>mostraron, no so<strong>la</strong>mente el papel biológico <strong>de</strong> muchas vitaminas y el porqué actúan en cantida<strong>de</strong>s mínimas, sino que iluminaron el camino que conducea una mejor compresión molecu<strong>la</strong>r <strong><strong>de</strong>l</strong> mecanismo mediante el cual loscoenzimas y los enzimas aceleran <strong>la</strong> velocidad <strong>de</strong> <strong>la</strong>s reacciones químicas.Actualmente se sabe que <strong>la</strong>s vitaminas son molécu<strong>la</strong>s orgánicas, <strong>de</strong> naturalezay composición variada, imprescindibles en los procesos metabólicosque tienen lugar en los seres vivos. No aportan energía, ya que no se utilizancomo combustible, pero sin el<strong>la</strong>s el organismo no es capaz <strong>de</strong> aprovechar loselementos constructivos y energéticos suministrados por <strong>la</strong> alimentación, puesayudan a convertir los alimentos en energía. Normalmente se utilizan en elinterior <strong>de</strong> <strong>la</strong>s célu<strong>la</strong>s como antecesoras <strong>de</strong> los coenzimas, a partir <strong>de</strong> los cualesse e<strong>la</strong>boran los miles <strong>de</strong> enzimas que regu<strong>la</strong>n <strong>la</strong>s reacciones químicas <strong>de</strong> <strong>la</strong>s queviven <strong>la</strong>s célu<strong>la</strong>s. De hecho casi todos los transportadores activados que actúancomo coenzimas son <strong>de</strong>rivados <strong>de</strong> vitaminas, y por tanto estás últimas son necesariasen pequeñas cantida<strong>de</strong>s en <strong>la</strong> dieta <strong>de</strong> algunos animales superiores.La Tab<strong>la</strong> 1.1 presenta <strong>la</strong>s vitaminas que actúan como coenzimas. Esta serie <strong>de</strong>vitaminas se conoce como grupo <strong>de</strong> <strong>la</strong>s vitaminas B, o complejo B. Se ha <strong>de</strong>seña<strong>la</strong>r que, en todos los casos, <strong>la</strong> vitamina <strong>de</strong>be modificarse antes <strong>de</strong> realizarsu función.Las vitaminas ejercen <strong>la</strong>s mismas funciones en casi todos los seres vivos,pero los animales superiores, a lo <strong>la</strong>rgo <strong>de</strong> <strong>la</strong> evolución, han perdido <strong>la</strong> capacidad<strong>de</strong> sintetizar<strong>la</strong>s. Así, por ejemplo, mientras <strong>la</strong> Escherichia coli pue<strong>de</strong> crecercon glucosa y sales orgánicas, el ser humano requiere al menos 12 vitaminasen su dieta.[7] E. V. McCollum and M. Davis, “The necessity of certain lipins in the diet duringgrowth,” Journal of Biological Chemistry, vol. 15, no. 1, pp. 167–175, 1913.[8] T. B. Osborne and L. B. Men<strong><strong>de</strong>l</strong>, “The re<strong>la</strong>tion of growth to the chemical constituentsof the diet,” Journal of Biological Chemistry, vol. 15, no. 2, pp. 311–326, 1913.
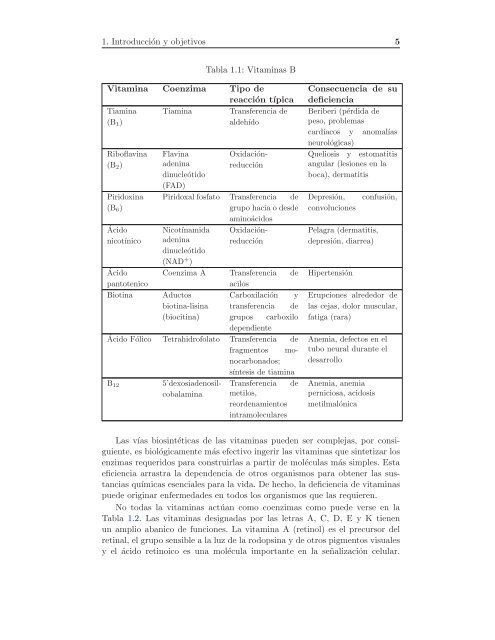
1. Introducción y objetivos 5Tab<strong>la</strong> 1.1: Vitaminas BVitamina Coenzima Tipo <strong>de</strong>reacción típicaTiamina Tiamina Transferencia <strong>de</strong>(B 1 )al<strong>de</strong>hídoRibof<strong>la</strong>vina(B 2 )Piridoxina(B 6 )ÁcidonicotínicoÁcidopantotenicoBiotinaF<strong>la</strong>vinaa<strong>de</strong>ninadinucleótido(FAD)Piridoxal fosfato Transferencia <strong>de</strong>grupo hacia o <strong>de</strong>s<strong>de</strong>aminoácidosNicotínamidaa<strong>de</strong>ninadinucleótido(NAD + )Coenzima A Transferencia <strong>de</strong>acilosAductos Carboxi<strong>la</strong>ción ybiotina-lisina transferencia <strong>de</strong>(biocitina) grupos carboxilo<strong>de</strong>pendienteOxidaciónreducciónOxidaciónreducciónÁcido Fólico Tetrahidrofo<strong>la</strong>to Transferencia <strong>de</strong>fragmentos monocarbonados;síntesis <strong>de</strong> tiaminaB 12 5’<strong>de</strong>xosia<strong>de</strong>nosilcoba<strong>la</strong>minaTransferencia <strong>de</strong>metilos,reor<strong>de</strong>namientosintramolecu<strong>la</strong>resConsecuencia <strong>de</strong> su<strong>de</strong>ficienciaBeriberi (pérdida <strong>de</strong>peso, problemascardíacos y anomalíasneurológicas)Queliosis y estomatitisangu<strong>la</strong>r (lesiones en <strong>la</strong>boca), <strong>de</strong>rmatitisDepresión,convolucionesPe<strong>la</strong>gra (<strong>de</strong>rmatitis,<strong>de</strong>presión, diarrea)Hipertensiónconfusión,Erupciones alre<strong>de</strong>dor <strong><strong>de</strong>l</strong>as cejas, dolor muscu<strong>la</strong>r,fatiga (rara)Anemia, <strong>de</strong>fectos en eltubo neural durante el<strong>de</strong>sarrolloAnemia, anemiaperniciosa, acidosismetilmalónicaLas vías biosintéticas <strong>de</strong> <strong>la</strong>s vitaminas pue<strong>de</strong>n ser complejas, por consiguiente,es biológicamente más efectivo ingerir <strong>la</strong>s vitaminas que sintetizar losenzimas requeridos para construir<strong>la</strong>s a partir <strong>de</strong> molécu<strong>la</strong>s más simples. Estaeficiencia arrastra <strong>la</strong> <strong>de</strong>pen<strong>de</strong>ncia <strong>de</strong> otros organismos para obtener <strong>la</strong>s sustanciasquímicas esenciales para <strong>la</strong> vida. De hecho, <strong>la</strong> <strong>de</strong>ficiencia <strong>de</strong> vitaminaspue<strong>de</strong> originar enfermeda<strong>de</strong>s en todos los organismos que <strong>la</strong>s requieren.No todas <strong>la</strong> vitaminas actúan como coenzimas como pue<strong>de</strong> verse en <strong>la</strong>Tab<strong>la</strong> 1.2. Las vitaminas <strong>de</strong>signadas por <strong>la</strong>s letras A, C, D, E y K tienenun amplio abanico <strong>de</strong> funciones. La vitamina A (retinol) es el precursor <strong><strong>de</strong>l</strong>retinal, el grupo sensible a <strong>la</strong> luz <strong>de</strong> <strong>la</strong> rodopsina y <strong>de</strong> otros pigmentos visualesy el ácido retinoico es una molécu<strong>la</strong> importante en <strong>la</strong> señalización celu<strong>la</strong>r.
- Page 5: VANTONIO FEZNÁNDEZ RAMOS Y SAULO A
- Page 9 and 10: Índice general1. Introducción y o
- Page 12 and 13: XIIÍNDICE DE FIGURAS3.4. Confórme
- Page 15 and 16: Capítulo 1Introducción y objetivo
- Page 17: 1. Introducción y objetivos 3su ef
- Page 21 and 22: 1. Introducción y objetivos 7algun
- Page 23 and 24: 1. Introducción y objetivos 91.3.
- Page 25 and 26: 1. Introducción y objetivos 11Tabl
- Page 27 and 28: 1. Introducción y objetivos 13la p
- Page 29 and 30: 1. Introducción y objetivos 15C 8
- Page 31 and 32: 1. Introducción y objetivos 17Tabl
- Page 33 and 34: 1. Introducción y objetivos 19C 8
- Page 35 and 36: 1. Introducción y objetivos 21Figu
- Page 37 and 38: 1. Introducción y objetivos 23medi
- Page 39 and 40: Capítulo 2Métodos teóricosPara a
- Page 41 and 42: 2. Métodos teóricos 27Sin embargo
- Page 43 and 44: 2. Métodos teóricos 29mínimo. Mi
- Page 45 and 46: 2. Métodos teóricos 31podrán omi
- Page 47 and 48: 2. Métodos teóricos 33Para poder
- Page 49 and 50: 2. Métodos teóricos 35esférica d
- Page 51 and 52: 2. Métodos teóricos 37recibe el n
- Page 53 and 54: 2. Métodos teóricos 39Las integra
- Page 55 and 56: 2. Métodos teóricos 41electrón l
- Page 57 and 58: 2. Métodos teóricos 43son de áto
- Page 59 and 60: 2. Métodos teóricos 45e INDO. Sin
- Page 61 and 62: 2. Métodos teóricos 47centros y c
- Page 63 and 64: 2. Métodos teóricos 492.3.3. Mét
- Page 65 and 66: 2. Métodos teóricos 51cierto tama
- Page 67 and 68: 2. Métodos teóricos 53Teorema var
- Page 69 and 70:
2. Métodos teóricos 55el funciona
- Page 71 and 72:
2. Métodos teóricos 57• Por úl
- Page 73 and 74:
2. Métodos teóricos 59este nivel
- Page 75 and 76:
2. Métodos teóricos 61transición
- Page 77 and 78:
2. Métodos teóricos 63generalizad
- Page 79 and 80:
2. Métodos teóricos 65expresión
- Page 81 and 82:
2. Métodos teóricos 67(o 2) rotac
- Page 83 and 84:
2. Métodos teóricos 69partición
- Page 85 and 86:
2. Métodos teóricos 71en un incre
- Page 87:
2. Métodos teóricos 73La segunda
- Page 90 and 91:
76 3.1. Superficie de energía pote
- Page 92 and 93:
78 3.1. Superficie de energía pote
- Page 94 and 95:
80 3.1. Superficie de energía pote
- Page 96 and 97:
82 3.1. Superficie de energía pote
- Page 98 and 99:
Tabla 3.2: Energías en kcal/mol y
- Page 100 and 101:
86 3.1. Superficie de energía pote
- Page 102 and 103:
88 3.1. Superficie de energía pote
- Page 104 and 105:
Figura 3.9: Estructuras conformacio
- Page 106 and 107:
Tabla 3.3: Energías y principales
- Page 108 and 109:
94 3.2. Cálculos de dinámica dire
- Page 110 and 111:
96 3.2. Cálculos de dinámica dire
- Page 112 and 113:
98 3.2. Cálculos de dinámica dire
- Page 114 and 115:
100 3.2. Cálculos de dinámica dir
- Page 117 and 118:
Apéndice AMétodo simplex descende
- Page 119:
A. Método simplex descendente mult
- Page 122 and 123:
108el que se encuentra en favor de
- Page 124 and 125:
110 C.1. MORATE2end programCsubrout
- Page 126 and 127:
112 C.1. MORATE2if (i.eq.icurt.or.i
- Page 128 and 129:
114 C.2. CONFORATE& ,wts(nconfs,nfr
- Page 130 and 131:
116 C.2. CONFORATEC TSif (nat_ts.gt
- Page 132 and 133:
118 C.2. CONFORATECCCCif (iop6.eq.1
- Page 134 and 135:
120 C.2. CONFORATEakp_vtst(n,i)=ct(
- Page 136 and 137:
122 C.2. CONFORATECCwrite(6,30) tem
- Page 138 and 139:
124 C.2. CONFORATEC Compute traslat
- Page 140 and 141:
126 C.2. CONFORATEC Read input data
- Page 142 and 143:
128 C.2. CONFORATECCCCenddoelsewrit
- Page 144 and 145:
130 C.2. CONFORATEstop1011 write(6,
- Page 146 and 147:
132 C.2. CONFORATElin=0C write(6,*)
- Page 148 and 149:
134 C.2. CONFORATE& ,numsta,numstb,
- Page 150 and 151:
136 C.2. CONFORATEwrite(6,33) (dmir
- Page 152 and 153:
138 C.2. CONFORATEendC Compute the
- Page 154 and 155:
140 C.2. CONFORATEC Full F matrixdo
- Page 156 and 157:
142 C.2. CONFORATE* NAGOYA UNIVERSI
- Page 158 and 159:
144 C.2. CONFORATE* * * * * * * * *
- Page 160 and 161:
146 C.2. CONFORATEDO 400 J=1,N400 V
- Page 162 and 163:
148 C.2. CONFORATE298. 63.0843 # Co
- Page 165 and 166:
Bibliografía[1] C. Funk, “On the
- Page 167 and 168:
BIBLIOGRAFÍA 153[24] A. Verloop, A
- Page 169 and 170:
BIBLIOGRAFÍA 155[47] D. Hartree,
- Page 171:
BIBLIOGRAFÍA 157G. Liu, A. Liashen