Comunicazioni orali e Poster sul Monitoraggio biologico - Giornale ...
Comunicazioni orali e Poster sul Monitoraggio biologico - Giornale ...
Comunicazioni orali e Poster sul Monitoraggio biologico - Giornale ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
COMUNICAZIONI ORALI E POSTER SUL MONITORAGGIO BIOLOGICO G Ital Med Lav Erg 2004; 26:4, Suppl<br />
94 www.gimle.fsm.it<br />
Ulteriore modifica apportata alla metodica di Lucas et al. è<br />
stata la sostituzione della colonna nuclosil ODS 5 µm Interchim<br />
con la colonna C 18 ODS 5 µm Beckman. Questo ci ha permesso<br />
di ottenere un cromatogramma più pulito e più veloce (circa 7<br />
minuti in meno per ogni campione) di quello ottenuto da Lucas<br />
et al. (Figura 3), peraltro da campioni incubati overnight e quindi<br />
qualitativamente diversi dai nostri.<br />
Infine, l’evaporazione sotto flusso di azoto è stata sostituita<br />
con quella a sistema chiuso sottovuoto: l’uso di tale apparato ha<br />
permesso di portare a secco un numero maggiore di campioni in<br />
minor tempo e, fattore non trascurabile, ha ridotto il possibile rischio<br />
di esposizione dell’analista. Inoltre, trattandosi di una centrifuga,<br />
il campione viene concentrato <strong>sul</strong> fondo della provetta<br />
evitandone la dispersione <strong>sul</strong>le pareti.<br />
Le prestazioni del metodo da noi messo a punto sono:<br />
– Separazione cromatografica: 6-OH-CHZ, CHZ e fenacetina<br />
(IS) sono state completamente separate e non sono state osservate<br />
interferenze con altri composti endogeni (Figura 4).<br />
– Precisione: è stata determinata sia in termini di ripetibilità<br />
che di riproducibilità ed espressa come coefficiente di varia-<br />
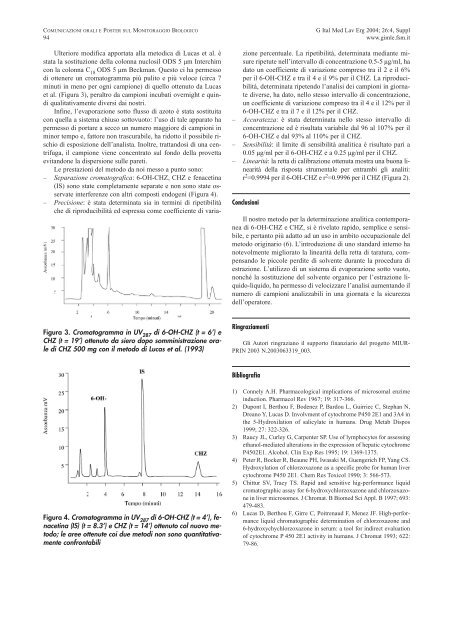
Figura 3. Cromatogramma in UV 287 di 6-OH-CHZ (t = 6’) e<br />
CHZ (t = 19’) ottenuto da siero dopo somministrazione orale<br />
di CHZ 500 mg con il metodo di Lucas et al. (1993)<br />
Figura 4. Cromatogramma in UV 287 di 6-OH-CHZ (t = 4’), fenacetina<br />
(IS) (t = 8.3’) e CHZ (t = 14’) ottenuto col nuovo metodo;<br />
le aree ottenute coi due metodi non sono quantitativamente<br />
confrontabili<br />
zione percentuale. La ripetibilità, determinata mediante misure<br />
ripetute nell’intervallo di concentrazione 0.5-5 µg/ml, ha<br />
dato un coefficiente di variazione compreso tra il 2 e il 6%<br />
per il 6-OH-CHZ e tra il 4 e il 9% per il CHZ. La riproducibilità,<br />
determinata ripetendo l’analisi dei campioni in giornate<br />
diverse, ha dato, nello stesso intervallo di concentrazione,<br />
un coefficiente di variazione compreso tra il 4 e il 12% per il<br />
6-OH-CHZ e tra il 7 e il 12% per il CHZ.<br />
– Accuratezza: è stata determinata nello stesso intervallo di<br />
concentrazione ed è ri<strong>sul</strong>tata variabile dal 96 al 107% per il<br />
6-OH-CHZ e dal 93% al 110% per il CHZ.<br />
– Sensibilità: il limite di sensibilità analitica è ri<strong>sul</strong>tato pari a<br />
0.05 µg/ml per il 6-OH-CHZ e a 0.25 µg/ml per il CHZ.<br />
– Linearità: la retta di calibrazione ottenuta mostra una buona linearità<br />
della risposta strumentale per entrambi gli analiti:<br />
r 2 =0.9994 per il 6-OH-CHZ e r 2 =0.9996 per il CHZ (Figura 2).<br />
Conclusioni<br />
Il nostro metodo per la determinazione analitica contemporanea<br />
di 6-OH-CHZ e CHZ, si è rivelato rapido, semplice e sensibile,<br />
e pertanto più adatto ad un uso in ambito occupazionale del<br />
metodo originario (6). L’introduzione di uno standard interno ha<br />
notevolmente migliorato la linearità della retta di taratura, compensando<br />
le piccole perdite di solvente durante la procedura di<br />
estrazione. L’utilizzo di un sistema di evaporazione sotto vuoto,<br />
nonché la sostituzione del solvente organico per l’estrazione liquido-liquido,<br />
ha permesso di velocizzare l’analisi aumentando il<br />
numero di campioni analizzabili in una giornata e la sicurezza<br />
dell’operatore.<br />
Ringraziamenti<br />
Gli Autori ringraziano il supporto finanziario del progetto MIUR-<br />
PRIN 2003 N.2003063319_003.<br />
Bibliografia<br />
1) Connely A.H. Pharmacological implications of microsomal enzime<br />
induction. Pharmacol Rev 1967; 19: 317-366.<br />
2) Dupont I, Berthou F, Bodenez P, Bardou L, Guirriec C, Stephan N,<br />
Dreano Y, Lucas D. Involvment of cytochrome P450 2E1 and 3A4 in<br />
the 5-Hydroxilation of salicylate in humans. Drug Metab Dispos<br />
1999; 27: 322-326.<br />
3) Raucy JL, Curley G, Carpenter SP. Use of lymphocytes for assessing<br />
ethanol-mediated alterations in the expression of hepatic cytochrome<br />
P4502E1. Alcohol. Clin Exp Res 1995; 19: 1369-1375.<br />
4) Peter R, Bocker R, Beaune PH, Iwasaki M, Guengerich FP, Yang CS.<br />
Hydroxylation of chlorzoxazone as a specific probe for human liver<br />
cytochrome P450 2E1. Chem Res Toxicol 1990; 3: 566-573.<br />
5) Chittur SV, Tracy TS. Rapid and sensitive hig-performance liquid<br />
cromatographic assay for 6-hydroxychlorzoxazone and chlorzoxazone<br />
in liver microsomes. J Chromat. B Biomed Sci Appl. B 1997; 693:<br />
479-483.<br />
6) Lucas D, Berthou F, Girre C, Poitrenaud F, Menez JF. High-performance<br />
liquid chromatographic determination of chlorzoxazone and<br />
6-hydroxychychlorzoxazone in serum: a tool for indirect evaluation<br />
of cytochrome P 450 2E1 activity in humans. J Chromat 1993; 622:<br />
79-86.