View - JUWEL - Forschungszentrum Jülich
View - JUWEL - Forschungszentrum Jülich
View - JUWEL - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
4.6. Enzymkinetiken<br />
______________________________________________________________________<br />
Aktivität / U * mg -1<br />
10<br />
9<br />
8<br />
7<br />
6<br />
5<br />
4<br />
3<br />
2<br />
1<br />
0<br />
0 2 4 6 8 10<br />
Konzentration NAD / mM<br />
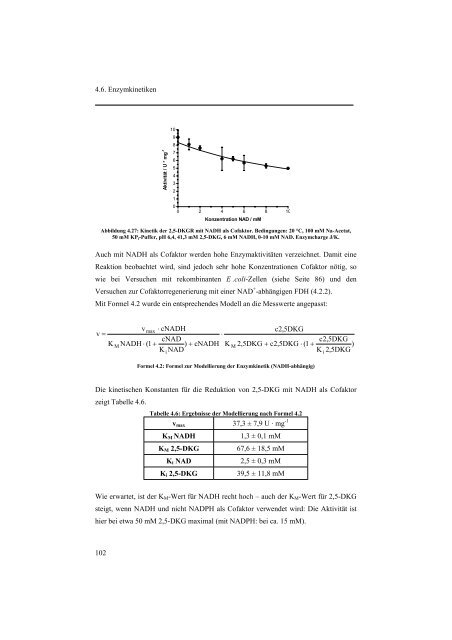
Abbildung 4.27: Kinetik der 2,5-DKGR mit NADH als Cofaktor. Bedingungen: 20 °C, 100 mM Na-Acetat,<br />
50 mM KP i -Puffer, pH 6,4, 41,3 mM 2,5-DKG, 6 mM NADH, 0-10 mM NAD. Enzymcharge J/K.<br />
Auch mit NADH als Cofaktor werden hohe Enzymaktivitäten verzeichnet. Damit eine<br />
Reaktion beobachtet wird, sind jedoch sehr hohe Konzentrationen Cofaktor nötig, so<br />
wie bei Versuchen mit rekombinanten E .coli-Zellen (siehe Seite 86) und den<br />
Versuchen zur Cofaktorregenerierung mit einer NAD + -abhängigen FDH (4.2.2).<br />
Mit Formel 4.2 wurde ein entsprechendes Modell an die Messwerte angepasst:<br />
v <br />
K<br />
M<br />
v max cNADH<br />
<br />
cNAD<br />
NADH (1 ) cNADH K<br />
K NAD<br />
i<br />
M<br />
c2,5DKG<br />
c2,5DKG<br />
2,5DKG c2,5DKG (1 <br />
)<br />
K 2,5DKG<br />
Formel 4.2: Formel zur Modellierung der Enzymkinetik (NADH-abhängig)<br />
i<br />
Die kinetischen Konstanten für die Reduktion von 2,5-DKG mit NADH als Cofaktor<br />
zeigt Tabelle 4.6.<br />
Tabelle 4.6: Ergebnisse der Modellierung nach Formel 4.2<br />
v max 37,3 ± 7,9 U · mg -1<br />
K M NADH<br />
K M 2,5-DKG<br />
K i NAD<br />
K i 2,5-DKG<br />
1,3 ± 0,1 mM<br />
67,6 ± 18,5 mM<br />
2,5 ± 0,3 mM<br />
39,5 ± 11,8 mM<br />
Wie erwartet, ist der K M -Wert für NADH recht hoch – auch der K M -Wert für 2,5-DKG<br />
steigt, wenn NADH und nicht NADPH als Cofaktor verwendet wird: Die Aktivität ist<br />
hier bei etwa 50 mM 2,5-DKG maximal (mit NADPH: bei ca. 15 mM).<br />
102