View - JUWEL - Forschungszentrum Jülich
View - JUWEL - Forschungszentrum Jülich
View - JUWEL - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Kapitel 3: Produktion von 2,5-Diketo-D-Gluconat mit Gluconobacter oxydans<br />
______________________________________________________________________<br />
3.3.4.4 Bestimmung der kinetischen Konstanten 4<br />
Um Rückschlüsse auf einen optimalen Reaktorbetrieb zu ziehen, reicht es aus, die<br />
reaktionskinetischen Parameter der Gesamtreaktion zu kennen. Immerhin ist es das Ziel,<br />
im ersten Reaktor möglichst viel 2,5-DKG zu produzieren. Die Zwischenschritte<br />
werden daher im Folgenden vernachlässigt, die Reaktion wie eine einstufige Reaktion<br />
betrachtet. So soll die optimale Ausgangsglucosekonzentration für den Reaktorbetrieb<br />
ermittelt werden.<br />
Es wurden mögliche Substrat- und Produktinhibierungen untersucht: Die Aktivität der<br />
Zellen wurde bei unterschiedlichen anfänglichen Glucosekonzentrationen bestimmt<br />
(Abbildung 3.23) sowie bei verschiedenen 2,5-DKG-Konzentrationen (Abbildung 3.24).<br />
Untersucht wurden lediglich die Zellen aus der 20-L-Fermentation. Problematisch ist<br />
dabei, dass die Reaktion über eine Dauer von mindestens 90 Minuten beobachtet<br />
werden muss, um die Aktivität der Zellen zu ermitteln. Innerhalb dieser Zeit werden<br />
jedoch schon erhebliche Mengen Substrat verbraucht sowie Intermediate und Produkt<br />
gebildet – das kann die Reaktionsgeschwindigkeit natürlich beeinflussen. Da jedoch<br />
nicht der Verbrauch an Glucose, sondern die Bildung von 2,5-DKG für den späteren<br />
Reaktorbetrieb interessant ist, war keine andere Vorgehensweise möglich.<br />
80<br />
70<br />
Aktivität / U * g -1<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
Aktivität, gemessen<br />
Aktivität, berechnet<br />
0<br />
0 50 100 150 200 250<br />
Glucosekonzentration / mM<br />
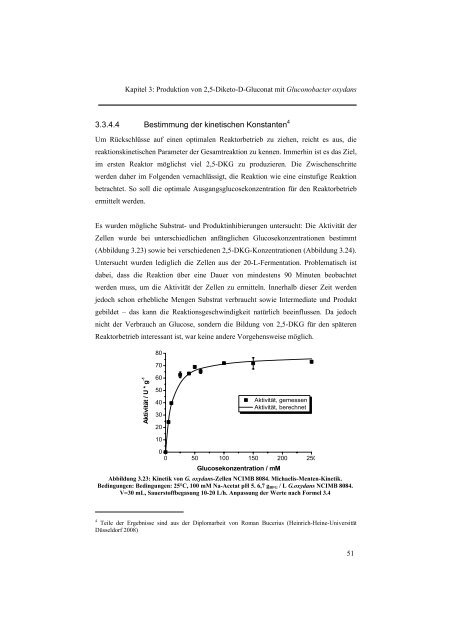
Abbildung 3.23: Kinetik von G. oxydans-Zellen NCIMB 8084. Michaelis-Menten-Kinetik.<br />
Bedingungen: Bedingungen: 25°C, 100 mM Na-Acetat pH 5. 6,7 g BFG / L G.oxydans NCIMB 8084.<br />
V=30 mL, Sauerstoffbegasung 10-20 L/h. Anpassung der Werte nach Formel 3.4<br />
4 Teile der Ergebnisse sind aus der Diplomarbeit von Roman Bucerius (Heinrich-Heine-Universität<br />
Düsseldorf 2008)<br />
51