Mechanische Anisotropie von Proteinen in ...
Mechanische Anisotropie von Proteinen in ...
Mechanische Anisotropie von Proteinen in ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
74 A. Fluoreszenzeigenschaften <strong>von</strong> GFP Polyprote<strong>in</strong>en<br />
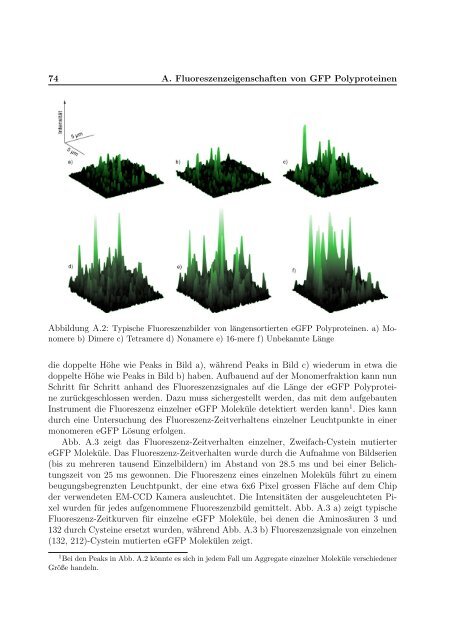
Abbildung A.2: Typische Fluoreszenzbilder <strong>von</strong> längensortierten eGFP Polyprote<strong>in</strong>en. a) Monomere<br />
b) Dimere c) Tetramere d) Nonamere e) 16-mere f) Unbekannte Länge<br />
die doppelte Höhe wie Peaks <strong>in</strong> Bild a), während Peaks <strong>in</strong> Bild c) wiederum <strong>in</strong> etwa die<br />
doppelte Höhe wie Peaks <strong>in</strong> Bild b) haben. Aufbauend auf der Monomerfraktion kann nun<br />
Schritt für Schritt anhand des Fluoreszenzsignales auf die Länge der eGFP Polyprote<strong>in</strong>e<br />
zurückgeschlossen werden. Dazu muss sichergestellt werden, das mit dem aufgebauten<br />
Instrument die Fluoreszenz e<strong>in</strong>zelner eGFP Moleküle detektiert werden kann 1 . Dies kann<br />
durch e<strong>in</strong>e Untersuchung des Fluoreszenz-Zeitverhaltens e<strong>in</strong>zelner Leuchtpunkte <strong>in</strong> e<strong>in</strong>er<br />
monomeren eGFP Lösung erfolgen.<br />
Abb. A.3 zeigt das Fluoreszenz-Zeitverhalten e<strong>in</strong>zelner, Zweifach-Cyste<strong>in</strong> mutierter<br />
eGFP Moleküle. Das Fluoreszenz-Zeitverhalten wurde durch die Aufnahme <strong>von</strong> Bildserien<br />
(bis zu mehreren tausend E<strong>in</strong>zelbildern) im Abstand <strong>von</strong> 28.5 ms und bei e<strong>in</strong>er Belichtungszeit<br />
<strong>von</strong> 25 ms gewonnen. Die Fluoreszenz e<strong>in</strong>es e<strong>in</strong>zelnen Moleküls führt zu e<strong>in</strong>em<br />
beugungsbegrenzten Leuchtpunkt, der e<strong>in</strong>e etwa 6x6 Pixel grossen Fläche auf dem Chip<br />
der verwendeten EM-CCD Kamera ausleuchtet. Die Intensitäten der ausgeleuchteten Pixel<br />
wurden für jedes aufgenommene Fluoreszenzbild gemittelt. Abb. A.3 a) zeigt typische<br />
Fluoreszenz-Zeitkurven für e<strong>in</strong>zelne eGFP Moleküle, bei denen die Am<strong>in</strong>osäuren 3 und<br />
132 durch Cyste<strong>in</strong>e ersetzt wurden, während Abb. A.3 b) Fluoreszenzsignale <strong>von</strong> e<strong>in</strong>zelnen<br />
(132, 212)-Cyste<strong>in</strong> mutierten eGFP Molekülen zeigt.<br />
1 Bei den Peaks <strong>in</strong> Abb. A.2 könnte es sich <strong>in</strong> jedem Fall um Aggregate e<strong>in</strong>zelner Moleküle verschiedener<br />
Größe handeln.