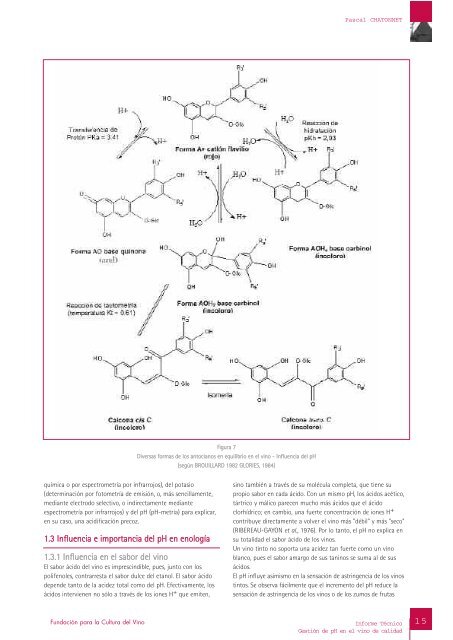
Pascal CHATONNETFigura 7Diversas formas <strong>de</strong> los antocianos <strong>en</strong> equilibrio <strong>en</strong> <strong>el</strong> <strong>vino</strong> - Influ<strong>en</strong>cia <strong>de</strong>l <strong>pH</strong>(según BROUILLARD 1982 GLORIES, 1984)química o por espectrometría por infrarrojos), <strong>de</strong>l potasio(<strong>de</strong>terminación por fotometría <strong>de</strong> emisión, o, más s<strong>en</strong>cillam<strong>en</strong>te,mediante <strong>el</strong>ectrodo s<strong>el</strong>ectivo, o indirectam<strong>en</strong>te medianteespectrometría por infrarrojos) y <strong>de</strong>l <strong>pH</strong> (<strong>pH</strong>-metría) para explicar,<strong>en</strong> su caso, una acidificación precoz.1.3 Influ<strong>en</strong>cia e importancia <strong>de</strong>l <strong>pH</strong> <strong>en</strong> <strong>en</strong>ología1.3.1 Influ<strong>en</strong>cia <strong>en</strong> <strong>el</strong> sabor <strong>de</strong>l <strong>vino</strong>El sabor ácido <strong>de</strong>l <strong>vino</strong> es imprescindible, pues, junto con lospolif<strong>en</strong>oles, contrarresta <strong>el</strong> sabor dulce <strong>de</strong>l etanol. El sabor ácido<strong>de</strong>p<strong>en</strong><strong>de</strong> tanto <strong>de</strong> la aci<strong>de</strong>z total como <strong>de</strong>l <strong>pH</strong>. Efectivam<strong>en</strong>te, losácidos intervi<strong>en</strong><strong>en</strong> no sólo a través <strong>de</strong> los iones H + que emit<strong>en</strong>,sino también a través <strong>de</strong> su molécula completa, que ti<strong>en</strong>e supropio sabor <strong>en</strong> cada ácido. Con un mismo <strong>pH</strong>, los ácidos acético,tártrico y málico parec<strong>en</strong> mucho más ácidos que <strong>el</strong> ácidoclorhídrico; <strong>en</strong> cambio, una fuerte conc<strong>en</strong>tración <strong>de</strong> iones H +contribuye directam<strong>en</strong>te a volver <strong>el</strong> <strong>vino</strong> más "débil" y más "seco"(RIBEREAU-GAYON et al., 1976). Por lo tanto, <strong>el</strong> <strong>pH</strong> no explica <strong>en</strong>su totalidad <strong>el</strong> sabor ácido <strong>de</strong> los <strong>vino</strong>s.Un <strong>vino</strong> tinto no soporta una aci<strong>de</strong>z tan fuerte como un <strong>vino</strong>blanco, pues <strong>el</strong> sabor amargo <strong>de</strong> sus taninos se suma al <strong>de</strong> susácidos.El <strong>pH</strong> influye asimismo <strong>en</strong> la s<strong>en</strong>sación <strong>de</strong> astring<strong>en</strong>cia <strong>de</strong> los <strong>vino</strong>stintos. Se observa fácilm<strong>en</strong>te que <strong>el</strong> increm<strong>en</strong>to <strong>de</strong>l <strong>pH</strong> reduce las<strong>en</strong>sación <strong>de</strong> astring<strong>en</strong>cia <strong>de</strong> los <strong>vino</strong>s o <strong>de</strong> los zumos <strong>de</strong> frutas15Fundación para la Cultura <strong>de</strong>l Vino<strong>Informe</strong> TécnicoGestión <strong>de</strong> <strong>pH</strong> <strong>en</strong> <strong>el</strong> <strong>vino</strong> <strong>de</strong> <strong>calidad</strong>15
1. Orig<strong>en</strong>, importancia y factores <strong>de</strong> variación <strong>de</strong> la aci<strong>de</strong>z y <strong>de</strong>l <strong>pH</strong>:visión g<strong>en</strong>eral <strong>de</strong> la problemática <strong>de</strong> la disminución <strong>de</strong> la aci<strong>de</strong>z <strong>de</strong> los <strong>vino</strong>stánicas (PELEG y NOBLE, 1999). Este f<strong>en</strong>óm<strong>en</strong>o se explica, al m<strong>en</strong>osparcialm<strong>en</strong>te, por la interacción <strong>de</strong> la aci<strong>de</strong>z con la precipitación o la<strong>de</strong>snaturalización <strong>de</strong> las proteínas <strong>en</strong>cargadas <strong>de</strong> la lubricación <strong>de</strong> lacavidad bucal <strong>en</strong> pres<strong>en</strong>cia <strong>de</strong> polif<strong>en</strong>oles. En efecto, la coagulación<strong>de</strong> las proteínas salivales es máxima a <strong>pH</strong> 4,4, haya o no polif<strong>en</strong>olespres<strong>en</strong>tes. En cambio, la s<strong>en</strong>sación <strong>de</strong> astring<strong>en</strong>cia <strong>de</strong> los polif<strong>en</strong>olesaum<strong>en</strong>ta significativam<strong>en</strong>te <strong>en</strong> pres<strong>en</strong>cia <strong>de</strong> ácidos, pues éstafacilita la interacción <strong>en</strong>tre las proteínas salivales y los polif<strong>en</strong>olesadsorbidos sobre las proteínas salivales (SEBERT et al., 2004).Un <strong>vino</strong> tinto soporta mejor la aci<strong>de</strong>z si ti<strong>en</strong>e un alto cont<strong>en</strong>ido <strong>de</strong>alcohol. Los <strong>vino</strong>s más duros son los ricos tanto <strong>en</strong> aci<strong>de</strong>z como <strong>en</strong>taninos. Un gran cont<strong>en</strong>ido <strong>de</strong> taninos sólo es aceptable si la aci<strong>de</strong>zes muy débil. De <strong>el</strong>lo se <strong>de</strong>spr<strong>en</strong><strong>de</strong> que los <strong>vino</strong>s con un altocont<strong>en</strong>ido <strong>de</strong> alcohol, ricos <strong>en</strong> taninos y <strong>de</strong> aci<strong>de</strong>z muy débil pue<strong>de</strong>nresultar "pesados", "pastosos" y sobre todo fatigosos <strong>en</strong> la cata. Hacetiempo, no era raro que <strong>el</strong> <strong>pH</strong> <strong>de</strong> los <strong>vino</strong>s tintos embot<strong>el</strong>ladosrondara con frecu<strong>en</strong>cia <strong>de</strong> 3,45 a 3,55. En la actualidad, <strong>de</strong>bido als<strong>en</strong>sible increm<strong>en</strong>to <strong>de</strong>l cont<strong>en</strong>ido medio <strong>de</strong> polif<strong>en</strong>oles y <strong>en</strong>especial <strong>de</strong> taninos, se ha vu<strong>el</strong>to difícil catar un <strong>vino</strong> tinto"mo<strong>de</strong>rno" que pres<strong>en</strong>te semejante niv<strong>el</strong> <strong>de</strong> <strong>pH</strong>: <strong>de</strong>bido a laastring<strong>en</strong>cia y la sequedad que éste confiere, esos <strong>vino</strong>s resultandifícilm<strong>en</strong>te bebibles por <strong>de</strong>bajo <strong>de</strong> <strong>pH</strong> 3,60-3,65.En <strong>el</strong> caso <strong>de</strong> los <strong>vino</strong>s blancos, la aus<strong>en</strong>cia <strong>de</strong> polif<strong>en</strong>oles hace qu<strong>el</strong>a cata no sea tan s<strong>en</strong>sible a la aci<strong>de</strong>z <strong>en</strong> g<strong>en</strong>eral y al <strong>pH</strong> <strong>en</strong>particular. A<strong>de</strong>más, las propieda<strong>de</strong>s "refrescantes" <strong>de</strong> los <strong>vino</strong>sblancos <strong>de</strong> marcada aci<strong>de</strong>z pue<strong>de</strong>n favorecer su apreciación cuando<strong>el</strong> equilibrio "dulce" <strong>en</strong> boca es sufici<strong>en</strong>te. Un <strong>vino</strong> g<strong>en</strong>eroso o suavesoporta mejor una mayor aci<strong>de</strong>z, pues <strong>el</strong> alcohol exacerba <strong>el</strong> sabordulce <strong>de</strong>l azúcar.La complejidad <strong>de</strong> las r<strong>el</strong>aciones exist<strong>en</strong>tes <strong>en</strong>tre <strong>el</strong> <strong>pH</strong> y la cataimpi<strong>de</strong> <strong>de</strong>finir un <strong>pH</strong> i<strong>de</strong>al a priori. En los <strong>vino</strong>s tintos, <strong>en</strong> especial losricos <strong>en</strong> polif<strong>en</strong>oles, sólo la cata permite evaluar <strong>el</strong> equilibrio óptimo<strong>de</strong> un <strong>vino</strong> <strong>de</strong>terminado.1.3.2 Influ<strong>en</strong>cia <strong>en</strong> <strong>el</strong> color <strong>de</strong> los <strong>vino</strong>s tintos y <strong>en</strong>los f<strong>en</strong>óm<strong>en</strong>os oxidativos corr<strong>el</strong>acionados con <strong>el</strong>mismoEl color <strong>de</strong> los <strong>vino</strong>s tintos <strong>de</strong>p<strong>en</strong><strong>de</strong> <strong>de</strong> su conc<strong>en</strong>tración <strong>de</strong>antocianos y <strong>de</strong> combinaciones taninos-antocianos. Losantocianos se comportan como ácidos débiles, cuyo color varía<strong>de</strong>l incoloro al azul o al rojo <strong>en</strong> función <strong>de</strong> la aci<strong>de</strong>z <strong>de</strong>l medio(figura 7). SOMERS (1977) ha señalado las r<strong>el</strong>aciones exist<strong>en</strong>tes<strong>en</strong>tre <strong>el</strong> cont<strong>en</strong>ido <strong>de</strong> potasio <strong>de</strong> los <strong>vino</strong>s, y <strong>el</strong> color apagado ycon t<strong>en</strong><strong>de</strong>ncia evolucionada (anaranjada) <strong>de</strong> los <strong>vino</strong>saustralianos con un alto niv<strong>el</strong> <strong>de</strong> <strong>pH</strong>. Sólo <strong>el</strong> catión flavilio A +(tinto), directam<strong>en</strong>te influ<strong>en</strong>ciado por una reacción <strong>de</strong> equilibrioque <strong>de</strong>p<strong>en</strong><strong>de</strong> <strong>de</strong>l <strong>pH</strong>, y la base quinona A0 (azul), que no hanreaccionado con <strong>el</strong> dióxido <strong>de</strong> azufre <strong>de</strong>l <strong>vino</strong> (mayoritariam<strong>en</strong>te<strong>en</strong> forma <strong>de</strong> HSO 3 <strong>en</strong> <strong>el</strong> <strong>pH</strong> <strong>de</strong>l <strong>vino</strong>), es <strong>de</strong>cir, <strong>en</strong> torno al 5 a 10% <strong>de</strong> los antocianos totales, exist<strong>en</strong> <strong>en</strong> formas coloreadas <strong>en</strong> losniv<strong>el</strong>es <strong>de</strong> <strong>pH</strong> <strong>de</strong> los <strong>vino</strong>s (figura 8).El experim<strong>en</strong>to <strong>de</strong> graduación <strong>de</strong> la catequina, núcleo f<strong>en</strong>ólico<strong>el</strong>em<strong>en</strong>tal <strong>de</strong> los taninos con<strong>de</strong>nsados <strong>de</strong>l <strong>vino</strong> tinto, mediante unasolución oxidante, permite explicar este f<strong>en</strong>óm<strong>en</strong>o (figura 10). Seobserva que <strong>el</strong> <strong>pH</strong> <strong>el</strong>evado reduce <strong>el</strong> volum<strong>en</strong> <strong>de</strong> solución oxidant<strong>en</strong>ecesaria para hacer pasar la totalidad <strong>de</strong> la (+) catequina <strong>de</strong> laFigura 8Evolución <strong>de</strong> las formas coloreadas (A + + A0) e incoloras (AOH + C) <strong>de</strong> los antocianos <strong>en</strong> los niv<strong>el</strong>es <strong>de</strong> <strong>pH</strong> <strong>de</strong> los <strong>vino</strong>sNota: A los niv<strong>el</strong>es <strong>de</strong> <strong>pH</strong> <strong>de</strong> los <strong>vino</strong>s (3,5-4,0), pue<strong>de</strong> haber <strong>en</strong>tre un 10,6% y un 18 % como máximo <strong>de</strong> antocianos libres <strong>en</strong> formacoloreada, pero <strong>en</strong> torno a un 6 a 12 % <strong>de</strong> dichos antocianos pue<strong>de</strong>n ser <strong>de</strong>colorados por <strong>el</strong> SO 2 libre <strong>en</strong> función <strong>de</strong> su conc<strong>en</strong>tración:A + + HSO 3- AHSO 3con una constante <strong>de</strong> equilibrio Ks = 10 5 M -1 y Ks = [AHSO 3 ]/[A + ] [HSO 3- ] (GLORIES, 1984).16Fundación para la Cultura <strong>de</strong>l Vino<strong>Informe</strong> TécnicoGestión <strong>de</strong> <strong>pH</strong> <strong>en</strong> <strong>el</strong> <strong>vino</strong> <strong>de</strong> <strong>calidad</strong>16