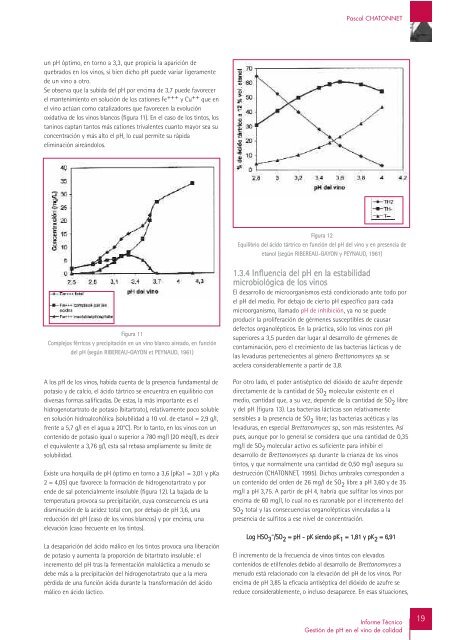
Pascal CHATONNETun <strong>pH</strong> óptimo, <strong>en</strong> torno a 3,3, que propicia la aparición <strong>de</strong>quebrados <strong>en</strong> los <strong>vino</strong>s, si bi<strong>en</strong> dicho <strong>pH</strong> pue<strong>de</strong> variar ligeram<strong>en</strong>te<strong>de</strong> un <strong>vino</strong> a otro.Se observa que la subida <strong>de</strong>l <strong>pH</strong> por <strong>en</strong>cima <strong>de</strong> 3,7 pue<strong>de</strong> favorecer<strong>el</strong> mant<strong>en</strong>imi<strong>en</strong>to <strong>en</strong> solución <strong>de</strong> los cationes Fe +++ y Cu ++ que <strong>en</strong><strong>el</strong> <strong>vino</strong> actúan como catalizadores que favorec<strong>en</strong> la evoluciónoxidativa <strong>de</strong> los <strong>vino</strong>s blancos (figura 11). En <strong>el</strong> caso <strong>de</strong> los tintos, lostaninos captan tantos más cationes trival<strong>en</strong>tes cuanto mayor sea suconc<strong>en</strong>tración y más alto <strong>el</strong> <strong>pH</strong>, lo cual permite su rápida<strong>el</strong>iminación aireándolos.Figura 12Equilibrio <strong>de</strong>l ácido tártrico <strong>en</strong> función <strong>de</strong>l <strong>pH</strong> <strong>de</strong>l <strong>vino</strong> y <strong>en</strong> pres<strong>en</strong>cia <strong>de</strong>etanol (según RIBEREAU-GAYON y PEYNAUD, 1961)Figura 11Complejos férricos y precipitación <strong>en</strong> un <strong>vino</strong> blanco aireado, <strong>en</strong> función<strong>de</strong>l <strong>pH</strong> (según RIBEREAU-GAYON et PEYNAUD, 1961)A los <strong>pH</strong> <strong>de</strong> los <strong>vino</strong>s, habida cu<strong>en</strong>ta <strong>de</strong> la pres<strong>en</strong>cia fundam<strong>en</strong>tal <strong>de</strong>potasio y <strong>de</strong> calcio, <strong>el</strong> ácido tártrico se <strong>en</strong>cu<strong>en</strong>tra <strong>en</strong> equilibrio condiversas formas salificadas. De estas, la más importante es <strong>el</strong>hidrog<strong>en</strong>otartrato <strong>de</strong> potasio (bitartrato), r<strong>el</strong>ativam<strong>en</strong>te poco soluble<strong>en</strong> solución hidroalcohólica (solubilidad a 10 vol. <strong>de</strong> etanol = 2,9 g/l,fr<strong>en</strong>te a 5,7 g/l <strong>en</strong> <strong>el</strong> agua a 20°C). Por lo tanto, <strong>en</strong> los <strong>vino</strong>s con uncont<strong>en</strong>ido <strong>de</strong> potasio igual o superior a 780 mg/l (20 mèq/l), es <strong>de</strong>cir<strong>el</strong> equival<strong>en</strong>te a 3,76 g/l, esta sal rebasa ampliam<strong>en</strong>te su límite <strong>de</strong>solubilidad.Existe una horquilla <strong>de</strong> <strong>pH</strong> óptimo <strong>en</strong> torno a 3,6 (pKa1 = 3,01 y pKa2 = 4,05) que favorece la formación <strong>de</strong> hidrog<strong>en</strong>otartrato y por<strong>en</strong><strong>de</strong> <strong>de</strong> sal pot<strong>en</strong>cialm<strong>en</strong>te insoluble (figura 12). La bajada <strong>de</strong> latemperatura provoca su precipitación, cuya consecu<strong>en</strong>cia es unadisminución <strong>de</strong> la aci<strong>de</strong>z total con, por <strong>de</strong>bajo <strong>de</strong> <strong>pH</strong> 3,6, unareducción <strong>de</strong>l <strong>pH</strong> (caso <strong>de</strong> los <strong>vino</strong>s blancos) y por <strong>en</strong>cima, una<strong>el</strong>evación (caso frecu<strong>en</strong>te <strong>en</strong> los tintos).La <strong>de</strong>saparición <strong>de</strong>l ácido málico <strong>en</strong> los tintos provoca una liberación<strong>de</strong> potasio y aum<strong>en</strong>ta la proporción <strong>de</strong> bitartrato insoluble: <strong>el</strong>increm<strong>en</strong>to <strong>de</strong>l <strong>pH</strong> tras la ferm<strong>en</strong>tación maloláctica a m<strong>en</strong>udo se<strong>de</strong>be más a la precipitación <strong>de</strong>l hidrog<strong>en</strong>otartrato que a la merapérdida <strong>de</strong> una función ácida durante la transformación <strong>de</strong>l ácidomálico <strong>en</strong> ácido láctico.1.3.4 Influ<strong>en</strong>cia <strong>de</strong>l <strong>pH</strong> <strong>en</strong> la estabilidadmicrobiológica <strong>de</strong> los <strong>vino</strong>sEl <strong>de</strong>sarrollo <strong>de</strong> microorganismos está condicionado ante todo por<strong>el</strong> <strong>pH</strong> <strong>de</strong>l medio. Por <strong>de</strong>bajo <strong>de</strong> cierto <strong>pH</strong> específico para cadamicroorganismo, llamado <strong>pH</strong> <strong>de</strong> inhibición, ya no se pue<strong>de</strong>producir la proliferación <strong>de</strong> gérm<strong>en</strong>es susceptibles <strong>de</strong> causar<strong>de</strong>fectos organolépticos. En la práctica, sólo los <strong>vino</strong>s con <strong>pH</strong>superiores a 3,5 pue<strong>de</strong>n dar lugar al <strong>de</strong>sarrollo <strong>de</strong> gérm<strong>en</strong>es <strong>de</strong>contaminación, pero <strong>el</strong> crecimi<strong>en</strong>to <strong>de</strong> las bacterias lácticas y <strong>de</strong>las levaduras pert<strong>en</strong>eci<strong>en</strong>tes al género Brettanomyces sp. seac<strong>el</strong>era consi<strong>de</strong>rablem<strong>en</strong>te a partir <strong>de</strong> 3,8.Por otro lado, <strong>el</strong> po<strong>de</strong>r antiséptico <strong>de</strong>l dióxido <strong>de</strong> azufre <strong>de</strong>p<strong>en</strong><strong>de</strong>directam<strong>en</strong>te <strong>de</strong> la cantidad <strong>de</strong> SO 2 molecular exist<strong>en</strong>te <strong>en</strong> <strong>el</strong>medio, cantidad que, a su vez, <strong>de</strong>p<strong>en</strong><strong>de</strong> <strong>de</strong> la cantidad <strong>de</strong> SO 2 librey <strong>de</strong>l <strong>pH</strong> (figura 13). Las bacterias lácticas son r<strong>el</strong>ativam<strong>en</strong>tes<strong>en</strong>sibles a la pres<strong>en</strong>cia <strong>de</strong> SO 2 libre; las bacterias acéticas y laslevaduras, <strong>en</strong> especial Brettanomyces sp., son más resist<strong>en</strong>tes. Asípues, aunque por lo g<strong>en</strong>eral se consi<strong>de</strong>ra que una cantidad <strong>de</strong> 0,35mg/l <strong>de</strong> SO 2 molecular activo es sufici<strong>en</strong>te para inhibir <strong>el</strong><strong>de</strong>sarrollo <strong>de</strong> Brettanomyces sp. durante la crianza <strong>de</strong> los <strong>vino</strong>stintos, y que normalm<strong>en</strong>te una cantidad <strong>de</strong> 0,50 mg/l asegura su<strong>de</strong>strucción (CHATONNET, 1995). Dichos umbrales correspon<strong>de</strong>n aun cont<strong>en</strong>ido <strong>de</strong>l or<strong>de</strong>n <strong>de</strong> 26 mg/l <strong>de</strong> SO 2 libre a <strong>pH</strong> 3,60 y <strong>de</strong> 35mg/l a <strong>pH</strong> 3,75. A partir <strong>de</strong> <strong>pH</strong> 4, habría que sulfitar los <strong>vino</strong>s por<strong>en</strong>cima <strong>de</strong> 60 mg/l, lo cual no es razonable por <strong>el</strong> increm<strong>en</strong>to <strong>de</strong>lSO 2 total y las consecu<strong>en</strong>cias organolépticas vinculadas a lapres<strong>en</strong>cia <strong>de</strong> sulfitos a ese niv<strong>el</strong> <strong>de</strong> conc<strong>en</strong>tración.Log HSO 3- /SO2 = <strong>pH</strong> - pK si<strong>en</strong>do pK 1 = 1,81 y pK 2 = 6,91El increm<strong>en</strong>to <strong>de</strong> la frecu<strong>en</strong>cia <strong>de</strong> <strong>vino</strong>s tintos con <strong>el</strong>evadoscont<strong>en</strong>idos <strong>de</strong> etilf<strong>en</strong>oles <strong>de</strong>bido al <strong>de</strong>sarrollo <strong>de</strong> Brettanomyces am<strong>en</strong>udo está r<strong>el</strong>acionado con la <strong>el</strong>evación <strong>de</strong>l <strong>pH</strong> <strong>de</strong> los <strong>vino</strong>s. Por<strong>en</strong>cima <strong>de</strong> <strong>pH</strong> 3,85 la eficacia antiséptica <strong>de</strong>l dióxido <strong>de</strong> azufre sereduce consi<strong>de</strong>rablem<strong>en</strong>te, o incluso <strong>de</strong>saparece. En esas situaciones,<strong>Informe</strong> TécnicoGestión <strong>de</strong> <strong>pH</strong> <strong>en</strong> <strong>el</strong> <strong>vino</strong> <strong>de</strong> <strong>calidad</strong>19
1. Orig<strong>en</strong>, importancia y factores <strong>de</strong> variación <strong>de</strong> la aci<strong>de</strong>z y <strong>de</strong>l <strong>pH</strong>:visión g<strong>en</strong>eral <strong>de</strong> la problemática <strong>de</strong> la disminución <strong>de</strong> la aci<strong>de</strong>z <strong>de</strong> los <strong>vino</strong>samortiguación <strong>en</strong> función <strong>de</strong> la graduación <strong>de</strong>l <strong>vino</strong> (o <strong>de</strong>l mosto)mediante una solución (<strong>de</strong> ácido) o <strong>de</strong> base fuerte conseguimi<strong>en</strong>to simultáneo <strong>de</strong>l <strong>pH</strong>.La acidificación consi<strong>de</strong>rable <strong>de</strong> los mostos ricos <strong>en</strong> potasio pue<strong>de</strong>producir <strong>vino</strong>s con una aci<strong>de</strong>z total muy fuerte sin una mejorasufici<strong>en</strong>te <strong>de</strong>l <strong>pH</strong>. La cata <strong>de</strong> dichos <strong>vino</strong>s, frecu<strong>en</strong>tes <strong>en</strong> climascálidos, se caracteriza por una s<strong>en</strong>sación inicial <strong>de</strong> suavidad y almismo tiempo una sequedad típica <strong>en</strong> final <strong>de</strong> boca que reduce lapersist<strong>en</strong>cia y <strong>el</strong> placer <strong>en</strong> la boca.Figura 13Influ<strong>en</strong>cia <strong>de</strong>l <strong>pH</strong> <strong>en</strong> <strong>el</strong> equilibrio <strong>de</strong> disociación <strong>de</strong>l SO 2 <strong>en</strong> <strong>el</strong> <strong>vino</strong>hay que consi<strong>de</strong>rar otros medios <strong>de</strong> lucha prev<strong>en</strong>tiva (CHATONNETet al., 1999).1.4 Medios <strong>de</strong> corrección <strong>de</strong> la aci<strong>de</strong>z débil y <strong>de</strong>l<strong>pH</strong> <strong>el</strong>evado a disposición <strong>de</strong>l <strong>en</strong>ólogo1.4.1 Corrección química <strong>de</strong> la aci<strong>de</strong>zEn pres<strong>en</strong>cia <strong>de</strong> uvas v<strong>en</strong>dimiadas con alto r<strong>en</strong>dimi<strong>en</strong>to, muymaduras, o proce<strong>de</strong>ntes <strong>de</strong> su<strong>el</strong>os ricos <strong>en</strong> potasio, <strong>el</strong> <strong>en</strong>ólogo se<strong>en</strong>cu<strong>en</strong>tra <strong>en</strong> pres<strong>en</strong>cia <strong>de</strong> mostos <strong>de</strong> aci<strong>de</strong>z débil, que finalm<strong>en</strong>tepodrían producir <strong>vino</strong>s <strong>de</strong>masiado "planos", o s<strong>en</strong>sibles a lasalteraciones microbiológicas. La t<strong>en</strong>tación, o la lógica, consistepues <strong>en</strong> realizar una corrección precoz, cuyo razonami<strong>en</strong>to resultano obstante muy difícil <strong>de</strong>bido a las múltiples interacciones.Conoci<strong>en</strong>do <strong>el</strong> cont<strong>en</strong>ido <strong>de</strong> ácido tártrico <strong>de</strong>l mosto y <strong>el</strong>cont<strong>en</strong>ido <strong>de</strong> potasio <strong>de</strong>l mosto tras <strong>el</strong> <strong>en</strong>cubado, se pue<strong>de</strong> realizaruna estimación <strong>de</strong>l <strong>pH</strong> final <strong>de</strong>l <strong>vino</strong>, y por lo tanto <strong>de</strong>l niv<strong>el</strong> <strong>de</strong>corrección necesario (ver 1.2.2), aunque siempre subsist<strong>en</strong>numerosas incertidumbres respecto al niv<strong>el</strong> exacto <strong>de</strong> precipitación<strong>de</strong> las sales <strong>de</strong> tártaro <strong>en</strong> <strong>el</strong> <strong>vino</strong>. Por <strong>de</strong>bajo <strong>de</strong> 6 g/l <strong>de</strong> ácidotártrico y por <strong>en</strong>cima <strong>de</strong> 1500 mg/l <strong>de</strong> potasio <strong>en</strong> <strong>el</strong> mosto,muchas veces <strong>el</strong> riesgo <strong>de</strong> superar un <strong>pH</strong> 3,80 al final <strong>de</strong>l procesoes consi<strong>de</strong>rable.La acidificación <strong>de</strong> los mostos y <strong>de</strong> los <strong>vino</strong>s está sujeta a unanormativa precisa (1,5 g/L <strong>de</strong> ácido tártrico puro <strong>en</strong> los mostos y2,5 g/l <strong>en</strong> los <strong>vino</strong>s, según la normativa <strong>de</strong> la ComunidadEuropea). La mayor dificultad consiste <strong>en</strong> prever la disminuciónefectiva <strong>de</strong>l <strong>pH</strong> t<strong>en</strong>i<strong>en</strong>do <strong>en</strong> cu<strong>en</strong>ta <strong>el</strong> efecto tampón,característico <strong>de</strong> cada <strong>vino</strong> o mosto, que se opone naturalm<strong>en</strong>te alas variaciones. El po<strong>de</strong>r amortiguador o <strong>de</strong> tampón β se expresapor la r<strong>el</strong>ación:β = ∆ [Ácido] / ∆ <strong>pH</strong> = 2,303 [HA] [A - ]/[HA] + [A - ]si<strong>en</strong>do [HA] la aci<strong>de</strong>z total y [A - ] la alcalinidad <strong>de</strong> las c<strong>en</strong>izas.También se pue<strong>de</strong> <strong>de</strong>terminar experim<strong>en</strong>talm<strong>en</strong>te <strong>el</strong> po<strong>de</strong>r <strong>de</strong>Teóricam<strong>en</strong>te, como dispone la legislación <strong>en</strong> Estados Unidos, laacidificación se <strong>de</strong>bería realizar con ácido tártrico combinado conyeso (sulfato <strong>de</strong> calcio). En efecto, <strong>el</strong> aporte <strong>de</strong> ácido tártricoprovoca un increm<strong>en</strong>to <strong>de</strong>l po<strong>de</strong>r <strong>de</strong> amortiguación, pero <strong>el</strong> aporte<strong>de</strong> calcio provoca simultáneam<strong>en</strong>te la precipitación <strong>de</strong> tartrato <strong>de</strong>calcio muy poco soluble, lo cual permite mejorar <strong>el</strong> r<strong>en</strong>dimi<strong>en</strong>to <strong>de</strong>la acidificación. En <strong>el</strong> caso <strong>de</strong> los <strong>vino</strong>s blancos que no efectúan suferm<strong>en</strong>tación maloláctica, también se podrá utilizar ácido málico sise obti<strong>en</strong><strong>en</strong> las pertin<strong>en</strong>tes autorizaciones legales tras <strong>el</strong> dictam<strong>en</strong>favorable <strong>de</strong> la Organización Internacional <strong>de</strong> la Viña y <strong>de</strong>l Vino(OIV).1.4.2 Corrección por medios físicos1.4.2.1 Intercambiadores <strong>de</strong> ionesLos primeros int<strong>en</strong>tos <strong>de</strong> aplicación <strong>en</strong>ológica <strong>de</strong> losintercambiadores <strong>de</strong> iones se remontan a los años 1950. Han sidorechazados globalm<strong>en</strong>te <strong>en</strong> Francia, y <strong>de</strong>spués <strong>en</strong> la CEE, sigui<strong>en</strong>dolas recom<strong>en</strong>daciones <strong>de</strong> la OIV. Sin embargo, Estados Unidos,Australia y Arg<strong>en</strong>tina han autorizado la utilización <strong>de</strong>intercambiadores <strong>de</strong> iones, y Europa importa sus <strong>vino</strong>s <strong>en</strong> gran<strong>de</strong>scantida<strong>de</strong>s.La utilización <strong>de</strong> intercambiadores <strong>de</strong> cationes permite <strong>el</strong>iminar <strong>el</strong>potasio, <strong>el</strong> calcio y, accesoriam<strong>en</strong>te, <strong>el</strong> hierro y <strong>el</strong> magnesio,sustituy<strong>en</strong>do estos iones por sodio o por iones H + . Con estetratami<strong>en</strong>to, se pue<strong>de</strong> conseguir una estabilización <strong>de</strong>l <strong>vino</strong> conrespecto a las precipitaciones tártricas y/o una acidificación. Lasprincipales resinas catiónicas utilizables son la Amberlita IR120 yIRC50, Dowex 50, Duolite C3, Rohm Hass IMAC HR y Rohm HassSAC. Las resinas se utilizan <strong>en</strong> inmersión, o, mejor aún, mediantepercolación <strong>de</strong>l <strong>vino</strong> (o <strong>de</strong>l mosto) a través <strong>de</strong> las columnas.Las resinas se pue<strong>de</strong>n utilizar <strong>en</strong> forma H + , Mg ++ o Na + . Seobti<strong>en</strong><strong>en</strong> <strong>en</strong> la forma a<strong>de</strong>cuada mediante un ciclo <strong>de</strong> reg<strong>en</strong>eración,percolando previam<strong>en</strong>te sobre <strong>el</strong> intercambiador una solución <strong>de</strong>cloruro <strong>de</strong> sodio, cloruro <strong>de</strong> magnesio o ácido clorhídrico parasaturar las agrupaciones sulfonadas (-SO 3 H) <strong>de</strong> la resina. En formahidróg<strong>en</strong>a, la sustitución <strong>de</strong> prácticam<strong>en</strong>te la totalidad <strong>de</strong> losdiversos cationes <strong>de</strong>l <strong>vino</strong> por iones H + pue<strong>de</strong> provocar unadisminución importante <strong>de</strong>l <strong>pH</strong>. Para evitar variaciones excesivas,sólo se pue<strong>de</strong> someter al tratami<strong>en</strong>to una parte <strong>de</strong>l <strong>vino</strong>,<strong>en</strong>samblándolo <strong>de</strong>spués.Al marg<strong>en</strong> <strong>de</strong> los problemas legislativos, <strong>el</strong> tratami<strong>en</strong>to medianteintercambiadores <strong>de</strong> iones plantea la necesidad <strong>de</strong>l reciclaje y la<strong>de</strong>puración <strong>de</strong> las aguas <strong>de</strong> lavado, ricas <strong>en</strong> sales minerales.20Fundación para la Cultura <strong>de</strong>l Vino