Quantitative Analyse von Arzneistoff-Membran-Wechselwirkungen ...
Quantitative Analyse von Arzneistoff-Membran-Wechselwirkungen ...
Quantitative Analyse von Arzneistoff-Membran-Wechselwirkungen ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Modellierung der Verteilungsvorgänge<br />
Die Aufsplittung der Objekte und die Elimination der Ausreißer (Abb. 45a, A) führt zu einer starken<br />
Zunahme der Vorhersagekraft aller PLS-<strong>Analyse</strong>n mit dem logPion in n-Octanol/Wasser (Tab. 35).<br />
Die Verteilung der Ionen <strong>von</strong> einfachen Basen ist in den PLS-Modellen nur durch einen positiven<br />
Einfluss <strong>von</strong> lipophilen <strong>Wechselwirkungen</strong> zu interpretieren und bleibt unabhängig <strong>von</strong> der<br />
Sondenwahl (Tab. 36, o12e und oo4e). Ohne die Konformationen der beiden Phenazine ergibt sich<br />
eine hohe Vorhersage der Verteilung der Monokationen der zweifachen Basen (Tab. 36, o12d, oo4d).<br />
Hier spielen <strong>Wechselwirkungen</strong> mit hydrophilen sowie polaren und geladenen Teilchen eine positive<br />
Rolle. Die Lipophilie ist zur Modellierung des Verteilungsverhaltens in n-Octanol/Wasser in<br />
Gegenwart <strong>von</strong> Ladungen nicht notwendig.<br />
Der logKSIP-Wert <strong>von</strong> Lercanidipin (B) wurde vermutlich falsch gemessen (Herbette et al. 1997) und<br />
liegt weit <strong>von</strong> übrigen Wertebereich der SIP-Konstanten entfernt. Das andere 1,4-Dihydropyridin mit<br />
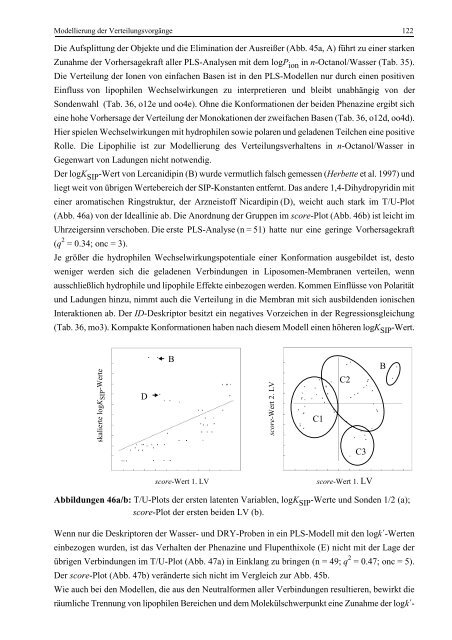
einer aromatischen Ringstruktur, der <strong>Arzneistoff</strong> Nicardipin (D), weicht auch stark im T/U-Plot<br />
(Abb. 46a) <strong>von</strong> der Ideallinie ab. Die Anordnung der Gruppen im score-Plot (Abb. 46b) ist leicht im<br />
Uhrzeigersinn verschoben. Die erste PLS-<strong>Analyse</strong> (n = 51) hatte nur eine geringe Vorhersagekraft<br />
(q 2 = 0.34; onc = 3).<br />
Je größer die hydrophilen Wechselwirkungspotentiale einer Konformation ausgebildet ist, desto<br />
weniger werden sich die geladenen Verbindungen in Liposomen-<strong>Membran</strong>en verteilen, wenn<br />
ausschließlich hydrophile und lipophile Effekte einbezogen werden. Kommen Einflüsse <strong>von</strong> Polarität<br />
und Ladungen hinzu, nimmt auch die Verteilung in die <strong>Membran</strong> mit sich ausbildenden ionischen<br />
Interaktionen ab. Der ID-Deskriptor besitzt ein negatives Vorzeichen in der Regressionsgleichung<br />
(Tab. 36, mo3). Kompakte Konformationen haben nach diesem Modell einen höheren logKSIP-Wert. skalierte logK SIP -Werte<br />
D<br />
B<br />
score-Wert 1. LV score-Wert 1. LV<br />
Abbildungen 46a/b: T/U-Plots der ersten latenten Variablen, logK SIP -Werte und Sonden 1/2 (a);<br />
score-Plot der ersten beiden LV (b).<br />
Wenn nur die Deskriptoren der Wasser- und DRY-Proben in ein PLS-Modell mit den logk´-Werten<br />
einbezogen wurden, ist das Verhalten der Phenazine und Flupenthixole (E) nicht mit der Lage der<br />
übrigen Verbindungen im T/U-Plot (Abb. 47a) in Einklang zu bringen (n = 49; q 2 = 0.47; onc = 5).<br />
Der score-Plot (Abb. 47b) veränderte sich nicht im Vergleich zur Abb. 45b.<br />
Wie auch bei den Modellen, die aus den Neutralformen aller Verbindungen resultieren, bewirkt die<br />
räumliche Trennung <strong>von</strong> lipophilen Bereichen und dem Molekülschwerpunkt eine Zunahme der logk´-<br />
score-Wert 2. LV<br />
C1<br />
C2<br />
C3<br />
B<br />
122