Quantitative Analyse von Arzneistoff-Membran-Wechselwirkungen ...
Quantitative Analyse von Arzneistoff-Membran-Wechselwirkungen ...
Quantitative Analyse von Arzneistoff-Membran-Wechselwirkungen ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Chromatografische Bestimmung des Verteilungsverhaltens<br />
Die Retention der nicht de/protonierbaren Verbindungen wird stärker vom Acetonitrilgehalt des<br />
Laufmittels beeinflusst als bei den strukturverwandten, positiv geladenen Verbindungen. Dabei<br />
besitzen die neutralen 1,4-Dihydropyridine die größten Abhängigkeit zwischen der Zunahme des<br />
logarithmierten Kapazitätsfaktors und der Zunahme des Acetonitrileinflusses. Allgemein weisen<br />
kleinere Werte des Acetonitrilkoeffizienten B darauf hin (basische Verbindungen; Abb. 23), dass die<br />
<strong>Wechselwirkungen</strong> zwischen den geladenen <strong>Arzneistoff</strong>molekülen und den Phosphatidylcholinen<br />
weniger durch die hydrophilen Eigenschaften der flüssigen Phase bestimmt werden.<br />
Der für die Effekte der Phosphationen charakteristische Koeffizient B ist nur bei Korrelation mit den<br />
logarithmierten Kapazitätsfaktoren <strong>von</strong> ionischen <strong>Arzneistoff</strong>molekülen signifikant (Tab. 10). Der<br />
extrapolierte logk´-Wert aller neutralen 1,4-Dihydropyridine und der Phenothiazine ohne basische<br />
Seitenkette wird statistisch gesehen nicht durch die Phosphationenkonzentration beeinflusst. Die<br />
Retentionszeiten der protonierten <strong>Arzneistoff</strong>e werden bei zunehmender Ionenstärke bzw. der<br />
Hydrophilie der Laufmittel exponentiell kleiner (Abb. 24).<br />
3-<br />
Koeffizient B [PO4 ]mM<br />
-0.3<br />
-0.4<br />
-0.5<br />
-0.6<br />
-0.7<br />
-0.8<br />
2.0 2.5 3.0 3.5 4.0 4.5<br />
extrapolierter logk´<br />
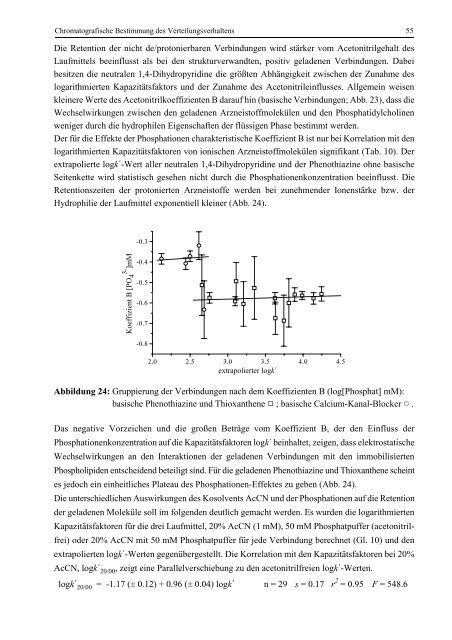
Abbildung 24: Gruppierung der Verbindungen nach dem Koeffizienten B (log[Phosphat] mM):<br />
basische Phenothiazine und Thioxanthene ; basische Calcium-Kanal-Blocker q .<br />
Das negative Vorzeichen und die großen Beträge vom Koeffizient B, der den Einfluss der<br />
Phosphationenkonzentration auf die Kapazitätsfaktoren logk´ beinhaltet, zeigen, dass elektrostatische<br />
<strong>Wechselwirkungen</strong> an den Interaktionen der geladenen Verbindungen mit den immobilisierten<br />
Phospholipiden entscheidend beteiligt sind. Für die geladenen Phenothiazine und Thioxanthene scheint<br />
es jedoch ein einheitliches Plateau des Phosphationen-Effektes zu geben (Abb. 24).<br />
Die unterschiedlichen Auswirkungen des Kosolvents AcCN und der Phosphationen auf die Retention<br />
der geladenen Moleküle soll im folgenden deutlich gemacht werden. Es wurden die logarithmierten<br />
Kapazitätsfaktoren für die drei Laufmittel, 20% AcCN (1 mM), 50 mM Phosphatpuffer (acetonitrilfrei)<br />
oder 20% AcCN mit 50 mM Phosphatpuffer für jede Verbindung berechnet (Gl. 10) und den<br />
extrapolierten logk´-Werten gegenübergestellt. Die Korrelation mit den Kapazitätsfaktoren bei 20%<br />
AcCN, logk´ 20/00 , zeigt eine Parallelverschiebung zu den acetonitrilfreien logk´-Werten.<br />
logk´ 20/00 = -1.17 (± 0.12) + 0.96 (± 0.04) logk´ n = 29 s = 0.17 r 2 = 0.95 F = 548.6<br />
55